-
Medical journals
- Career
NEARTERITICKÁ FORMA PŘEDNÍ ISCHEMICKÉ NEUROPATIE OPTIKU - LÉČBA A RIZIKOVÉ FAKTORY
Authors: S. Kalábová; K. Marešová; M. Karhanová
Authors‘ workplace: Oční klinika LF UP a FN Olomouc
Published in: Čes. a slov. Oftal., 76, 2020, No. 2, p. 78-87
Category: Original Article
doi: https://doi.org/10.31348/2020/15Overview
Cíl: Zjistit, zda různé léčebné postupy nearteriitické přední ischemické neuropatie optiku (NAION) mají vliv na výslednou zrakovou ostrost postiženého oka. Vyhodnotit výskyt rizikových faktorů, které dle literatury toto onemocnění provázejí.
Metodika: Do retrospektivní studie bylo zařazeno 55 očí 53 pacientů (41 mužů, 12 žen) ve věkovém rozmezí 46 až 85 let (průměr 64,9; medián 64,0), kteří byli v letech 2005 až 2016 hospitalizovaní na Oční klinice LF UP a FN Olomouc s diagnózou NAION, a kterým byla poskytnuta celková terapie intravenózně podanými vazodilatancii, a to buď samostatně, či v kombinaci s intravenózně aplikovanými kortikosteroidy. Hodnocena byla centrální zraková ostrost (CZO) před léčbou a bezprostředně po jejím ukončení. CZO byla vyšetřována na Snellenových optotypech a je uváděna v decimální hodnotě. Dle anamnestických údajů a zdravotní dokumentace jsme sledovali výskyt celkových onemocnění těchto pacientů, a to hypertenze, diabetu mellitu 2. typu a hypercholesterolemie a vyhodnotili možnou souvislost těchto onemocnění s NAION.
Výsledky: Ve skupině pacientů, kteří byli léčeni intravenózně podávanými vazodilatancii, se výsledná CZO zlepšila průměrně o 0,083. Ve skupině pacientů, kterým byla podána kromě vazodilatační terapie i terapie kortikosteroidní, se výsledná CZO zlepšila průměrně jen o 0,03. Přestože jsme zaznamenali výraznější zlepšení CZO ve skupině léčené pouze intravenózně podanými vazodilatancii, nebyl tento rozdíl statisticky signifikantní. Alespoň jeden rizikový faktor jsme zjistili u naprosté většiny pacientů (96 %). U 80 % pacientů se jednalo o hypertenzi, 43,6 % pacientů bylo léčeno pro diabetes mellitus a 72,7 % pacientů užívalo léky na hypercholesterolemii. Kombinací všech těchto onemocnění trpělo 36,4 % pacientů v souboru. Kuřáci a bývalí kuřáci nepřevyšovali zastoupením nekuřáky.
Závěr: Průměrné zlepšení výsledné CZO u pacientů po celkové léčbě pouze vazodilatancii bylo sice větší než u pacientů léčených kombinací vazodilatancií a kortikosteroidů, tento rozdíl však nebyl statisticky významný. U většiny pacientů v souboru jsme zaznamenali aspoň jeden celkový rizikový faktor, nejčastěji hypertenzi. Frekvence výskytu celkových rizikových faktorů byla srovnatelná s literaturou.
Klíčová slova:
nearteriitická forma přední ischemické neuropatie optiku – vazodilatancia – kortikosteroidy – rizikové faktory
ÚVOD
Nearteriitická forma přední ischemické neuropatie optického nervu (non-arteritic anterior ischemic optic neuropathy – NAION) je nejvíce rozšířená příčina akutního postižení optického nervu u pacientů v 6. a 7. dekádě. Onemocnění je způsobené okluzí zadních krátkých ciliárních arterií, které jsou větvemi arteria ophthalmica [14]. Nejedná se o onemocnění zánětlivé, nýbrž o důsledek vaskulární insuficience. Onemocnění lze tedy považovat za infarkt optického nervu, přesto jej nelze pro odlišný mechanismus vzniku srovnávat s infarktem mozku [4]. Projevuje se zpravidla náhlým bezbolestným poklesem zrakové ostrosti na jednom oku. Ztráta vidění se většinou objevuje ráno po probuzení, což ukazuje na možnou souvislost s noční hypotenzí [8]. Centrální zraková ostrost (CZO) se může pohybovat mezi 1,0 až pouhým vnímáním světla. Při vyšetření zorného pole bývá typicky nalezen dolní altitudinální skotom, ale může být i centrální, paracentrální, kvadrantový či arkuátní výpadek zorného pole. Při větším poklesu centrálního vizu často nacházíme relativní aferentní pupilární defekt (RAPD). Zhoršování vidění progreduje asi dva týdny a poté zůstává stabilní. Kromě snížené zrakové ostrosti může být různě vyjádřena i porucha vnímání barev – dyschromatopsie, která závisí na stupni postižení zrakové ostrosti.
Pro akutní fázi nearteriitické přední ischemické neuropatie optiku je typické bledé difúzní či sektorovité prosáknutí terče zrakového nervu, často spojené s několika peripapilárními třískovitými hemoragiemi, případně i vatovitými ischemickými ložisky přilehlé sítnice [16,20]. Klinické projevy tohoto onemocnění mohou být variabilní, v mnoha případech je obtížné stanovení definitivní diagnózy. Asi za 3 až 4 týdny od vzniku onemocnění nacházíme již atrofii a bledost terče, která může být difúzní, nebo též sektorovitá. V průběhu tohoto onemocnění dochází k úbytku nervových vláken jak peripapilárně, tak i v oblasti makuly [20]. Riziko vzniku téhož onemocnění na druhém oku je 10 % do dvou let a 15 až 25 % do pěti let [8,20]. Rekurence onemocnění na témže oku je 6 % [3]. V případě vzniku NAION na druhém oku můžeme pozorovat tzv. nepravý Foster-Kennedyho syndrom, což je atrofie terče zrakového nervu na jednom oku a bledý edém terče na oku druhém [16].
Predisponujícími morfologickými rizikovými faktory pro vznik onemocnění jsou malé terče s malou nebo téměř vymizelou exkavací a výrazně viditelnou vrstvou nervových vláken (tzv. crowded-disc či disc at risk) a drúzy terče zrakového nervu [9]. Tyto predispozice působí kompresivním mechanismem na zrakový nerv a mohou mít podíl na vzniku NAION. Z hlavních celkových rizikových faktorů jsou to zejména faktory vaskulární – hypertenze, diabetes mellitus, hypercholesterolemie, hyperkoagulační stavy (hyperhomocysteinemie), dále kolagenózy, noční hypotenze, syndrom obstrukční spánkové apnoe, léčba erektilní dysfunkce a kouření. Nebyla jednoznačně potvrzena predispozice pohlaví, ač častěji, i dle našich zkušeností, bývají postižení muži [18]. I některá jiná oční onemocnění mohou souviset se vznikem NAION, například věkem podmíněná makulární degenerace, či okluze retinální žíly [5]. Taktéž kataraktová chirurgie může být rizikovým faktorem pro vznik NAION (pooperačně zvýšený nitrooční tlak, nitrooční zánět, retrobulbárně podaná anestetika) [8].
Doposud bohužel neexistuje žádná prokazatelně účinná léčba NAION a ani prognóza stran zrakových funkcí není dobrá. Základem terapie je pečlivá úprava všech patologických stavů v těle, zejména již výše zmíněných vaskulárních onemocnění. V podpůrné terapii se používají antitrombotika a vazodilatancia [3,11]. Efekt celkově podávaných kortikosteroidů je udáván hlavně ve zmírnění otoku terče zrakového nervu [10,11,21,22]. Přesto žádná léčba nedokáže stav kauzálně vyléčit a ani nesnižuje riziko vzniku NAION na druhém oku či relapsu na tomtéž oku. Nově se zkouší intravitreální injekce steroidů (triamcinolonu) nebo inhibitorů vaskulárního endotelového růstového faktoru (vascular endothelial growth factor – VEGF), které by pomocí inhibice VEGF mohly redukovat vazogenní edém [3,8]. Použití neuroprotektiv v akutních stádiích NAION je dosud ve fázi studií [8]. U pacientů s progresivní formou NAION je možno zvážit provedení dekomprese obalů zrakového nervu, i když je tato metoda kontroverzní [15,16].
Cílem této práce je zjistit, zda různé léčebné postupy u pacientů s NAION, které používáme na našem pracovišti, měly vliv na výslednou CZO postiženého oka a vyhodnotit výskyt rizikových faktorů, které dle literatury toto onemocnění doprovázejí.
SOUBOR A METODIKA
Design studie
Do retrospektivní studie byli zařazeni všichni pacienti, kteří byli hospitalizovaní na Oční klinice LF UP a FN Olomouc v letech 2005 až 2016 s diagnózou NAION. Z databáze kliniky byl nejprve získán seznam pacientů (celkem 147 pacientů) s diagnózou NAION. Z toho se jich na cílené vyšetření za účelem této studie dostavilo 58. Do studie byli následně zařazeni všichni pacienti, kterým byla poskytnuta celková léčba intravenózně podávanými vazodilatancii, antitrombotiky a v indikovaných případech i kortikosteroidy intravenózně. Dle podané terapie byli pacienti následně rozděleni do dvou skupin. Do první skupiny byli zařazeni pacienti, kterým byla intravenózně podána pouze vazodilatační terapie a do druhé skupiny pacienti, kterým byla podána intravenózně vazodilatační i kortikosteroidní terapie. Ze studie bylo vyřazeno 5 pacientů, kteří nemohli být léčeni celkově vazodilatancii z interních důvodů, a byla jim podávána jiná terapie. Ve 3 případech se jednalo o monoterapii intravenózně aplikovanými kortikosteroidy, ve dvou případech byla na žádost pacienta léčba pouze ambulantní (perorálními vazodilatancii). Vzhledem k povaze studie byl odstup cíleného vyšetření od vzniku onemocnění různě dlouhý (3 měsíce až 11 let). Pro studii jsme vytvořili formulář, kam jsme zaznamenali všechny sledované i doplňující informace. Zaznamenali jsme typ terapie, délku potíží před zahájením léčby, pečlivě jsme odebrali osobní anamnézu, ve které jsme se zaměřili zejména na přítomnost hypertenze, diabetu mellitu 2. typu a hypercholesterolemie. Zaznamenali jsme také údaje o kouření. Podle zprávy z hospitalizace jsme zjistili CZO před léčbou a bezprostředně po ukončení léčby při propuštění pacienta. Zaznamenali jsme i aktuální CZO, kterou jsme však nezahrnuli do výsledného hodnocení pro možné ovlivnění jiným očním onemocněním, zejména kataraktou. CZO byla vyšetřena na Snellenových optotypech a zaznamenána v decimální hodnotě. Při slabé CZO v rozmezí počítání prstů před okem či pouze vnímání pohybu před okem jsme použili přepočtovou tabulku (Tabulka 1). Provedli jsme počítačový perimetr (Octopus, Haag Streit, Švýcarsko) na obou očích (celé zorné pole) a HRT (HRT 2, Heidelberg Retina Tomograph, Heidelberg engineering, Německo) vyšetření k zjištění průměrné velikosti terče zrakového nervu.
Table 1. Přepočet slabé centrální zrakové ostrosti do decimální hodnoty 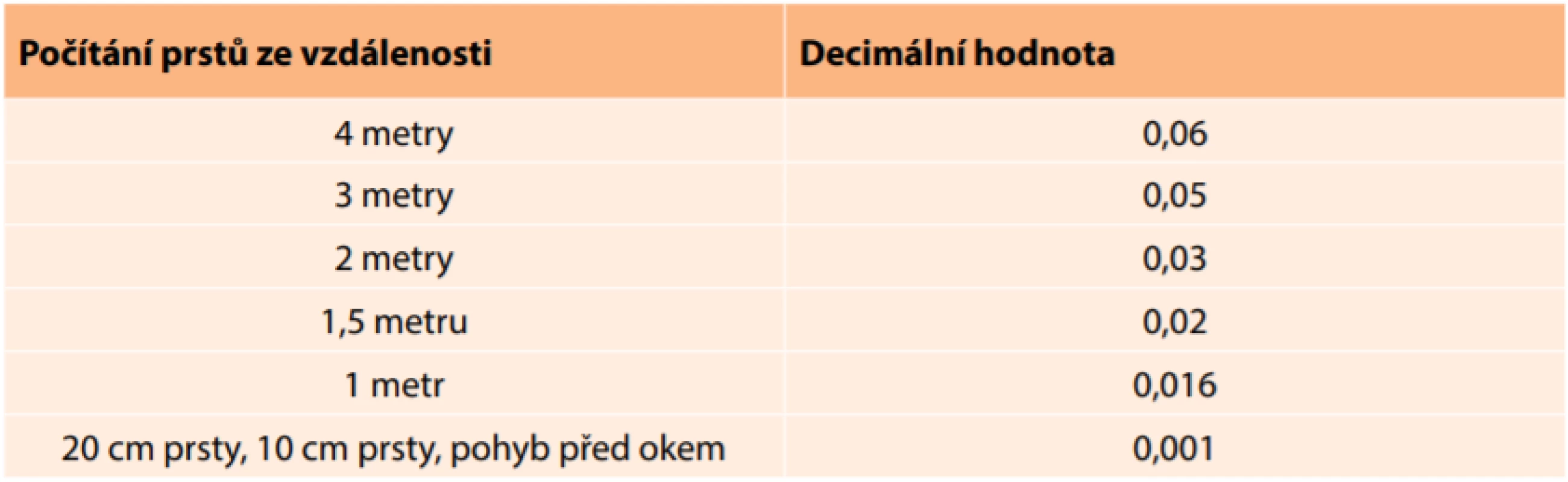
Podaná celková terapie
Na naší klinice pacienty s NAION standardně léčíme podáním infuze prokain hydrochloridu 0,2% (Prokain®) 500 ml na den v délce 5 dní, pokud jejich interní stav tuto léčbu nevylučuje. Při příznivém gradujícím se efektu bývá tato léčba prolongována až na 9 dní. Dále podáváme antitrombotika v terapeutické dávce (Fraxiparine® inj.), pokud již tato pacient neužívá (byť v perorální formě). V případě výrazného edému terče zrakového nervu, výrazném poklesu vidění či snížené zrakové ostrosti na druhém oku z různých důvodů k celkové terapii přidáváme intravenózně podávaný kortikosteroid metylprednisolon (SoluMedrol®) 500 mg na den v délce 3 dnů k urychlení resorpce edému.
Charakteristika souboru
Retrospektivně sledovanou skupinu tvořilo 55 očí 53 pacientů, kteří byli hospitalizovaní na Oční klinice LF UP a FN Olomouc v letech 2005 až 2016 s diagnózou NAION. Počet očí léčených intravenózně podávanými vazodilatancii (Prokain®) byl 37. Kombinovaná terapie Prokainem® a SoluMedrolem® byla indikovaná v 18 případech (Tabulka 2).
Table 2. Počet léčených očí v jednotlivých skupinách 
Mužů bylo celkem 41 (77,4 %), žen 12 (22,6 %). Zastoupení mužů a žen v jednotlivých skupinách je uvedeno v tabulce (Tabulka 3). Věkové rozmezí léčených pacientů bylo 46 až 85 let (průměr 64,9; medián 64,0). Věk mužů a žen v jednotlivých skupinách (věkové rozmezí, průměr, medián) je uveden v tabulce (Tabulka 4).
Table 3. Zastoupení pohlaví v jednotlivých skupinách 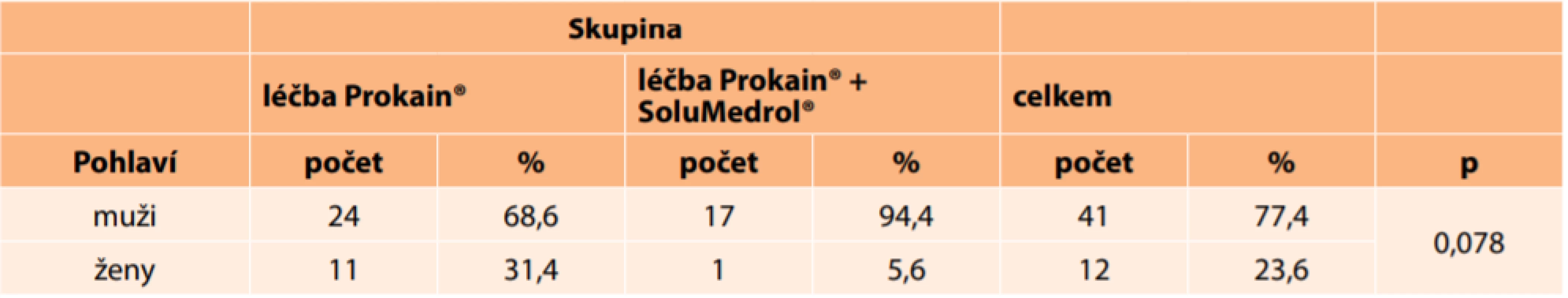
Table 4. Věk mužů a žen v jednotlivých skupinách 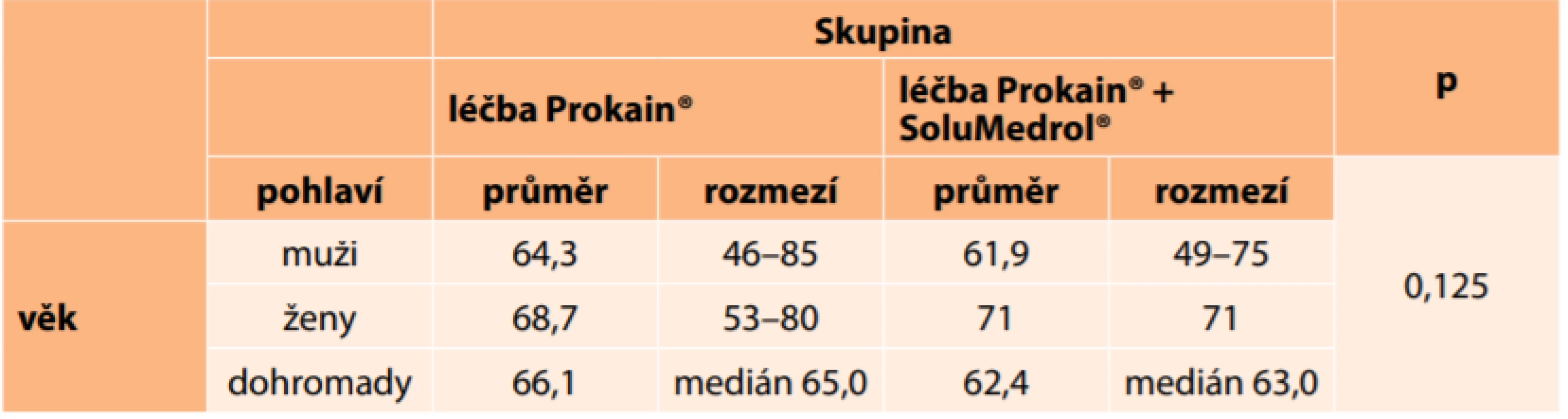
Analýza dat a statistické zhodnocení
Údaje každého pacienta byly zaznamenány do předchystaných formulářů. Data byla následně převedena do elektronické podoby, podrobena deskriptivní analýze a statisticky zpracována. Změna CZO byla posouzena pomocí Wilcoxonova párového testu. Závislost mezi změnou CZO a délkou obtíží byla analyzována pomocí Spearmanovy korelační analýzy. Obě skupiny podle léčby byly porovnány v kvantitativních parametrech pomocí Mann-Whitney U testu, v kategoriálních parametrech pomocí chí-kvadrát testu, resp. Fisherova testu v případě malých četností. Normalita dat byla testována pomocí Shapiro-Wilkova testu. Všechny testy byly dělány na hladině signifikance 0,05. K analýze dat byl použit statistický software IBM SPSS Statistics verze 22.
VÝSLEDKY
Při porovnání obou skupin podle pohlaví (Tabulka 3; p = 0,078) a věku (Tabulka 4; p = 0,125) nebyl nalezen signifikantní rozdíl.
U pacientů léčených pouze intravenózně podávanými vazodilatancii (Prokain®) byla průměrná CZO na začátku onemocnění 0,356 a bezprostředně po ukončení terapie 0,439. Výsledná CZO se zlepšila průměrně o 0,083. Ve skupině s kombinovanou terapii Prokainem® a SoluMedrolem® byla průměrná CZO před léčbou 0,398 a bezprostředně po ukončení léčby 0,429. Výsledná CZO se zlepšila průměrně o 0,031. Při statistickém porovnání se skupiny podle léčby signifikantně nelišily v CZO vstupní ani při propuštění. Nebyl zjištěn signifikantní rozdíl mezi skupinami ve změně zrakové ostrosti (Tabulka 5, p = 0,723).
Table 5. Průměrné hodnoty centrální zrakové ostrosti před léčbou a po léčbě 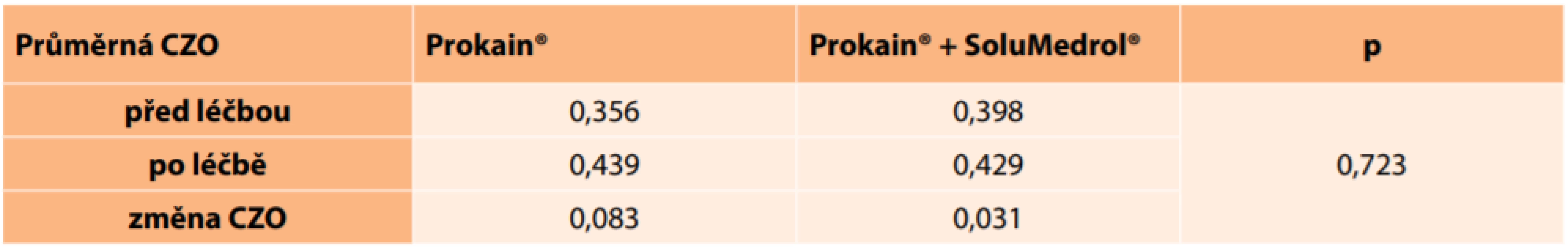
CZO – centrální zraková ostrost Ve skupině léčené Prokainem® se zlepšilo 15 očí. U stejného počtu očí nedošlo k žádné změně CZO a u 7 očí se CZO zhoršila (Tabulka 6, Graf 1). U pacientů léčených Prokainem® a SoluMedrolem® dosáhlo zlepšení 5 očí, u 11 očí se CZO nezměnila a ve 2 případech se zhoršila (Tabulka 6, Graf 2).
Table 6. Změna centrální zrakové ostrosti po léčbě v jednotlivých skupinách 
CZO – centrální zraková ostrost Graph 1. Změna centrální zrakové ostrosti po léčbě ve skupině léčené Prokainem® 
Graph 2. Změna centrální zrakové ostrosti po léčbě ve skupině léčené Prokainem® a SoluMedrolem® 
U zlepšených očí se ve skupině pacientů léčených pouze Prokainem® změnila CZO průměrně o 0,27 (Tabulka 7).
Table 7. Absolutní hodnoty centrální zrakové ostrosti u zlepšených pacientů ve skupině léčené Prokainem® 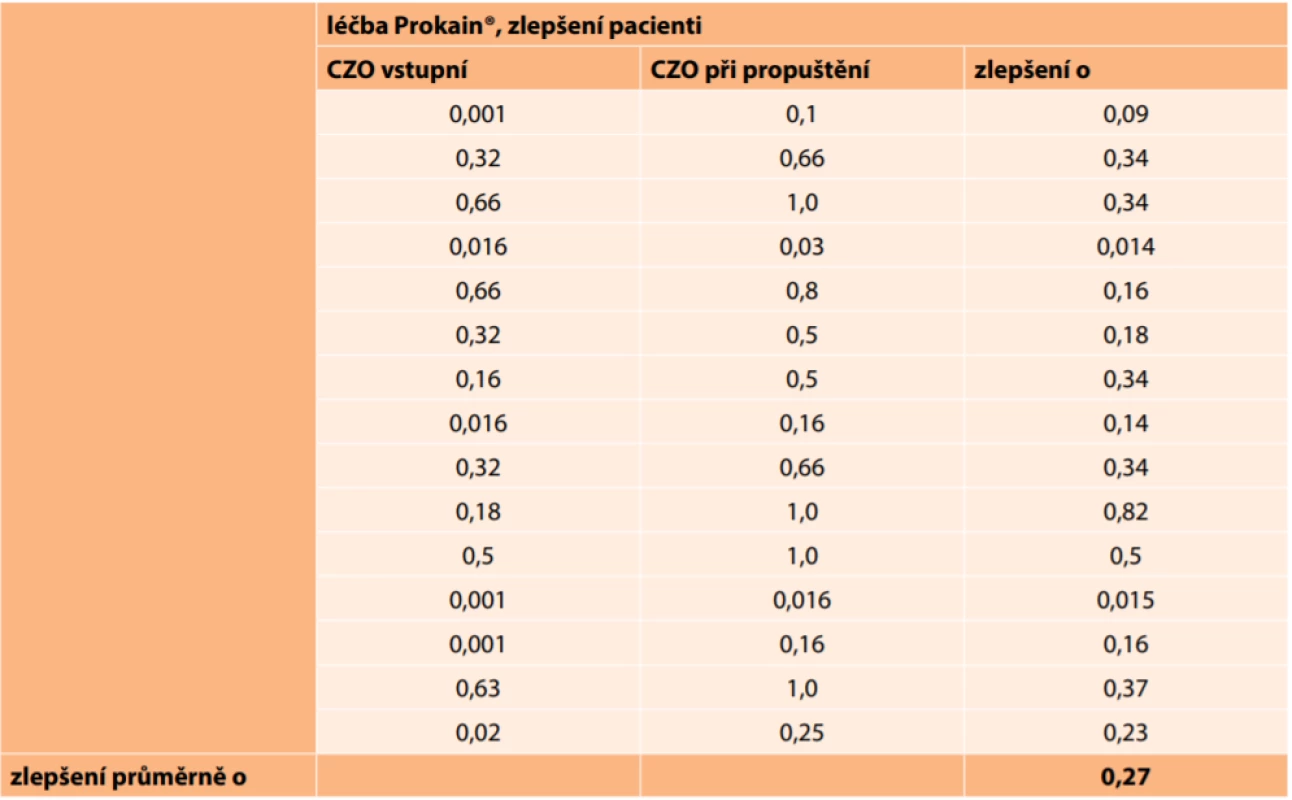
CZO – centrální zraková ostrost U zlepšených očí se ve skupině pacientů léčených Prokainem® a SoluMedrolem® změnila CZO průměrně o 0,17 (Tabulka 8).
Table 8. Absolutní hodnoty centrální zrakové ostrosti u zlepšených pacientů ve skupině léčené kombinovaně Prokainem® a SoluMedrolem® 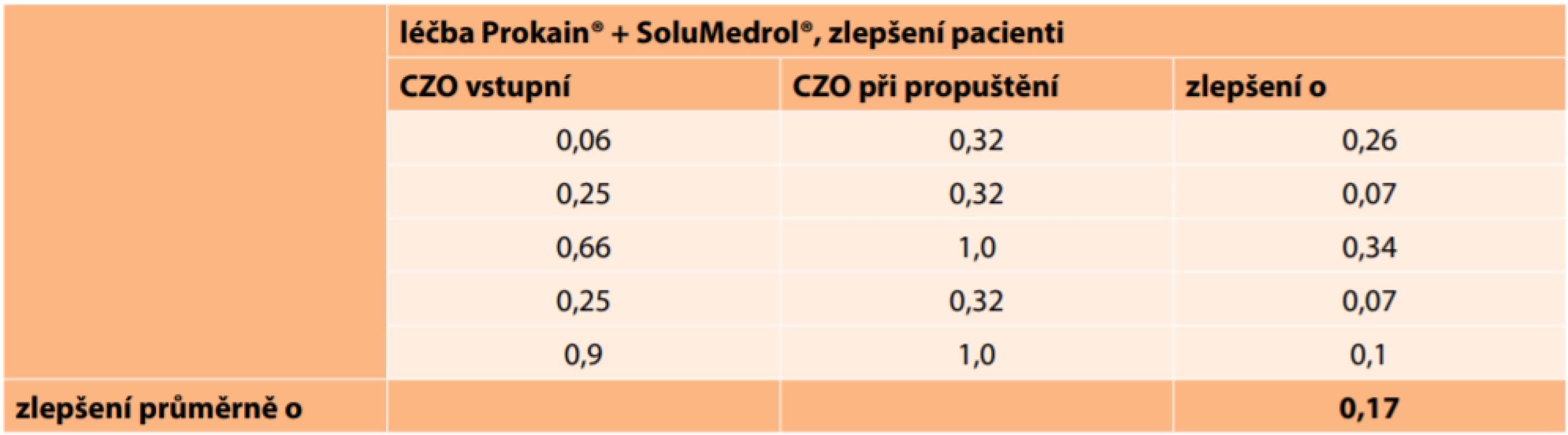
CZO – centrální zraková ostrost Průměrná délka obtíží před zahájením léčby byla ve skupině léčené Prokainem® 9,8 dní a ve skupině s kombinovanou léčbou 10,6 dne, přičemž časové rozmezí bylo mezi 1 dnem až 56 dny. Rozdíl délky obtíží mezi skupinami nebyl statisticky významný (Tabulka 9, p = 0,333). Mezi délkou trvání obtíží a změnou zrakové ostrosti nebyla prokázána signifikantní korelace (v celém souboru ani v jednotlivých skupinách).
Table 9. Průměrná délka obtíží před léčbou 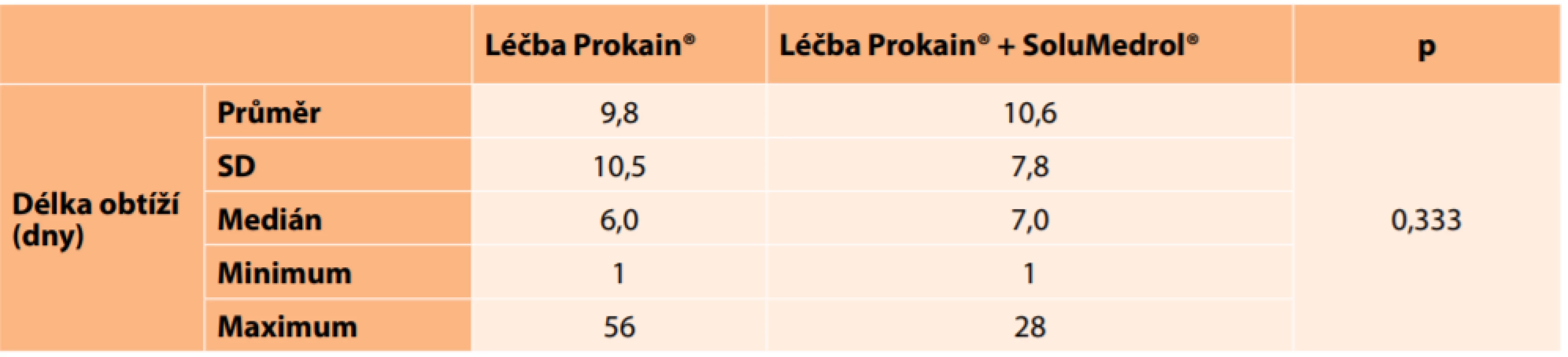
SD – směrodatná odchylka V celém sledovaném souboru mělo 80 % pacientů hypertenzi, 43,6 % pacientů byli diabetici 2. typu a 72,7 % pacientů se léčilo pro hypercholesterolemii. Všechny 3 sledované choroby mělo 36,4 % pacientů. Alespoň 1 rizikový faktor měla většina nemocných, tedy 96 %. Pouze ve 2 případech nebyl nalezen žádný rizikový faktor a tito pacienti se neléčili s žádnou jinou chorobou (Tabulka 10). Mezi oběma sledovanými skupinami nebyl zjištěn signifikantní rozdíl ve výskytu rizikových faktorů (Tabulka 11).
Table 10. Zastoupení celkových rizikových faktorů 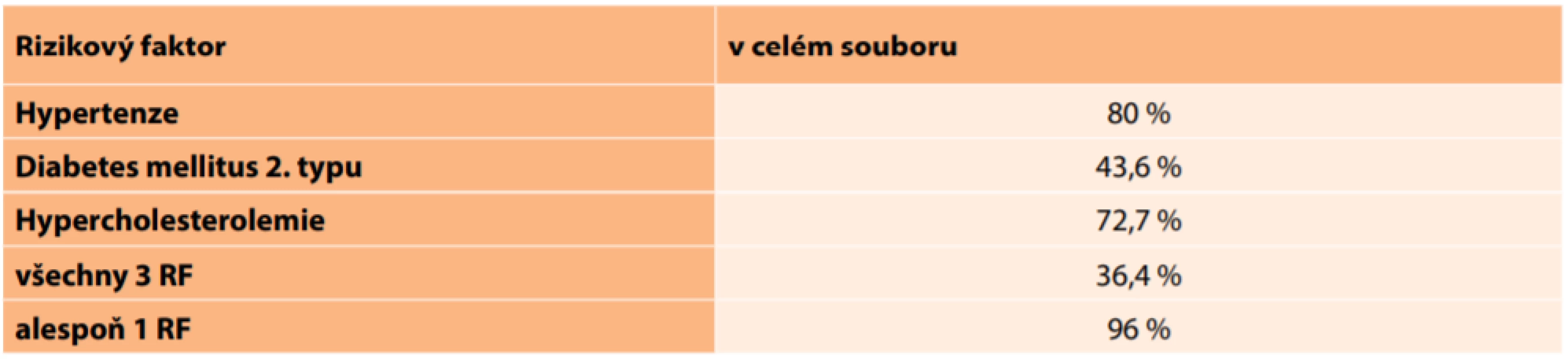
RF – rizikový faktor Table 11. Zastoupení rizikových faktorů v jednotlivých skupinách podle léčby 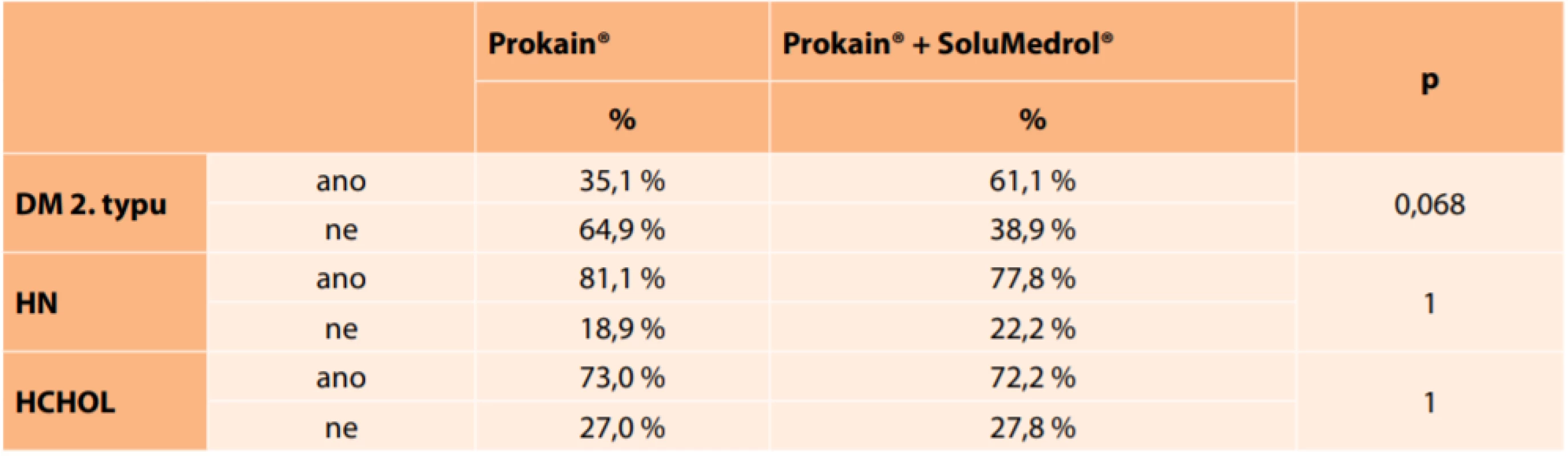
DM – diabetes mellitus; HN – hypertenze; HCHOL – hypercholesterolemie Z celého souboru kouřilo pouze 13,8 % pacientů, stopkuřáků bylo 20,7 % a zbylou část tvořili nekuřáci (60,3 %) (Tabulka 12, Graf 3). Při statistickém srovnání nebyl ve skupinách signifikantní rozdíl v kouření.
Table 12. Zastoupení kuřáků v celém souboru 
Graph 3. Zastoupení kuřáků v celém souboru 
Průměrná velikost terče zrakového nervu postiženého oka měřená pomocí HRT byla 1,85 mm2 a spadala do normálního rozmezí velikosti (1,63–2,43). Nejmenší terč měl 1,14 mm2 a největší měřil 3,37 mm2. V jednotlivých skupinách nebyl signifikantní rozdíl průměrných velikostí terčů. U 3 očí se nám toto vyšetření nepodařilo provést pro nedostatečnou fixaci okem při slabé CZO (Tabulka 13).
Table 13. Velikost terče zrakového nervu 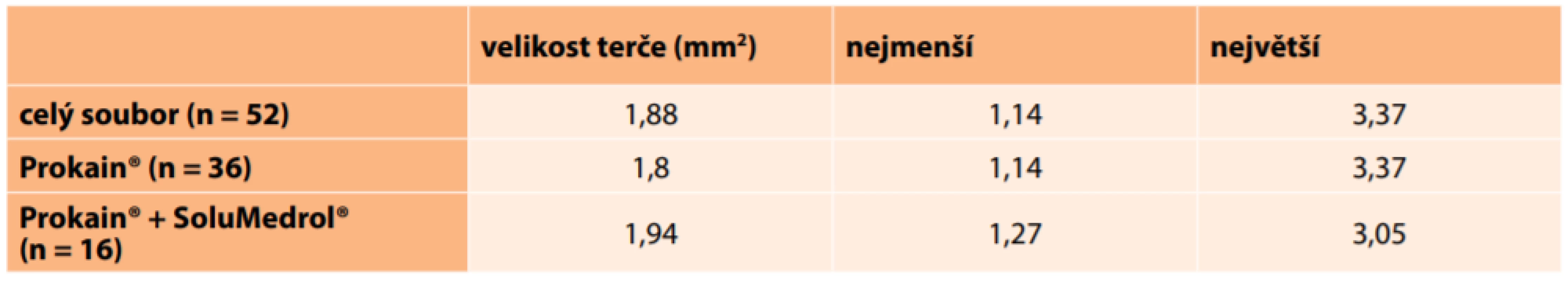
n – počet očí Z celého souboru mělo 25 % očí velikost papily pod normu (pod 1,63).
Drúzy zrakového terče jsme zjistili u jednoho pacienta (na nemocném oku).
U jednoho pacienta s bilaterálním postižením jsme zaznamenali všechny 3 celkové rizikové faktory (HN, DM 2. typu, hypercholesterolemie). Pacient byl kuřák. U dalšího pacienta s bilaterálním postižením jsme zaznamenali familiární hypercholesterolemii, hypertenzi a těžký syndrom spánkové apnoe.
DISKUSE
Ischemická neuropatie optiku (Ischemic Optic Neuropathy) je druhým nejčastěji se vyskytujícím onemocněním terče zrakového nervu u pacientů nad 50 let hned za glaukomem [14,16]. Terč zrakového nervu je rozdělen na povrchovou vrstvu nervových vláken, prelaminární oblast, oblast laminy cribrosy a oblast retrolaminární. Povrchová vrstva nervových vláken je zásobena hlavně z arteriol pocházejících z centrální retinální arterie. Prelaminární oblast dostává krevní zásobení z kruhu arteriol nazvaných circulus Halleri a circulus Zinni. Tento kruh je tvořen větvemi zadních krátkých ciliárních arterií, které jsou větvemi arteria ophthalmica. V menší míře je tato oblast zásobena z piálních cév odstupujících od retrobulbární části centrální sítnicové arterie. Autonomní nervový systém přispívá k regulaci retrobulbární a choroidální cirkulace, ale končí na lamina cribrosa, takže cévní systém zásobující přední část terče zrakového nervu nemá přímou inervaci [17].
Podle lokalizace ischemické příhody rozlišujeme přední ischemickou neuropatii optiku (AION), která je mnohem častější a je charakterizovaná typickou triádou – aferetním pupilárním defektem, poruchou zrakových funkcí, edémem terče zrakového nervu [14,16]. Vzácnou formou je zadní ischemická neuropatie optického nervu (posterior ischemic optic neuropathy – PION), která je relativně málo častá a jejíž příčinou je pravděpodobně okluze jedné či více piálních větví. V tomto případě oftalmoskopicky neprokazujeme edém terče zrakového nervu.
AION může souviset s mnoha celkovými onemocněními. V praxi však rozlišujeme dvě základní formy, a to arteriitickou (AAION) a nearteriitickou (NAION). Odlišení těchto dvou forem je zcela zásadní. Arteriitická forma přední ischemické neuropatie optiku (AAION) – tzv. Hortonova choroba (gigantocelulární arteriitida, temporální arteriitida) je granulomatózní nekrotizující arteriitida velkých a středně velkých povrchových tepen, zvláště povrchové temporální arterie, oftalmické arterie, zadní ciliární arterie a proximální vertebrální arterie. AAION může být jejím prvním klinickým příznakem. Taktéž se projevuje zhoršeným viděním, bolest hlavy je v temporální a okcipitální krajině, nacházíme palpační citlivost nad povrchovou temporální arterií, pacient udává klaudikační bolesti při žvýkání, což je způsobeno ischemií žvýkacího svalu (m. masseter), dále postižený ztrácí na váze, je malátný, má bolesti proximálních svalových skupin, má teploty a noční pocení. V laboratorních hodnotách bývá nalezena zejména vysoká hladina sedimentace erytrocytů (FW) až kolem 100 mm za hodinu, zvýšené CRP (C-reaktivní protein), anemie v krevním obraze a k diagnóze dále přispívá výsledek biopsie. Léčba AAION spočívá v systémovém podávání kortikosteroidů intravenózní cestou, a to co nejdříve, jak je to možné. Biopsie temporální arterie se provádí zejména z důvodu potvrzení diagnózy, přesto se při podezření na AAION nečeká na výsledek biopsie a léčba kortikosteroidy se zahajuje neprodleně. Včasná a správná diagnóza může rozhodnout nejen o zraku, ale někdy i o životě pacienta, proto diagnostika a léčba této choroby je vždy urgentní. U neléčených pacientů s již jednostranným postižením je velké riziko ztráty zrakové ostrosti i na druhém oku [18].
Léčba nearteriitické formy přední ischemické neuropatie optiku (NAION) již není tak jednoznačná, výsledky nejsou optimální a jsou stále hledány nové možnosti. Atkins et al. [3] hodnotí různé léčebné metody NAION jako postupy založené na empirii, které působí na předpokládaná agens související s tímto onemocněním – cévy, trombózu a samotný otok zrakového nervu. Ostatní léčba je zaměřená na neuroprotektivní efekt [8,10,11]. Možnou nedávno navrženou intervencí je intravitreální injekce steroidů a anti-VEGF preparátů. Prozatím však žádná studie neprokázala přínos medikamentózní či chirurgické terapie NAION. Podobně žádná studie neprokázala vliv léčby na vznik onemocnění na druhém oku.
V běžné klinické praxi se setkáváme se dvěma nejčastějšími léčebnými postupy, a to vazodilatační terapií a aplikací kortikosteroidů celkově. Tyto postupy jsou diskutovány i v literatuře a závěry nejsou jednoznačné. Podle Atkinse at al. [3] vychází léčba NAION celkovými kortikosteroidy ze studie z roku 1960 [7], kdy byl popsán vliv těchto léků na snížení permeability cévní stěny, a tedy na rychlejší vstřebávání edému terče. Tímto se snižuje komprese kapilár v papile zrakového nervu, zlepšuje se průtok krve a obnovuje se funkce „přeživších“ neuronů. Hayreh a Zimmerman [10] publikovali v roce 2008 prospektivní studii, ve které popisují vliv celkově podaných kortikosteroidů na rychlost vstřebání edému terče zrakového nervu. Při podávání prednisolonu perorálně do 2 týdnů od vzniku NAION se edém vstřebal za průměrně 6,8 týdne, u skupiny bez léčby prednisolonem to bylo za 8,2 týdne. Došli k závěru, že systémově podávané kortikoidy během akutní fáze NAION vedou k signifikantnímu zlepšení zrakové ostrosti a zorného pole. Na druhé straně Rebolleda et al. [21] ve své studii nezjistil žádný signifikantní rozdíl ve výsledné CZO mezi pacienty, kteří byli léčeni celkově kortikosteroidy a kontrolní skupinou. Al-Zubidi et al.[1] ve své přehledové práci došel k závěru, že i v současné době není kontroverze v užívání kortikosteroidů při NAION vyřešena. Užití celkové vazodilatační terapie při této diagnóze má dlouhou tradici, ať již samostatně či v kombinaci s kortikoidy. Steigerwald et al. [22] publikoval kazuistiky dvou pacientů, u kterých vedla systémová aplikace kortikosteroidů v kombinaci s intravenózně aplikovaným prostaglandinem E1 ke zlepšení zrakové ostrosti.
Při našem sledování se ukázalo, že monoterapie vazodilatačními preparáty měla ve výsledku lepší konečnou centrální zrakovou ostrost, než terapie posílená kortikosteroidy. Tento rozdíl však nebyl statisticky významný. Výsledky mohou být ovlivněny i tím, že kombinovaná terapie byla podána pacientům s horším nálezem na terči zrakového nervu.
Naše studie je retrospektivní. Do hodnocení jsme zařadili všechny pacienty, kteří splňovali daná kritéria. Slabinou studie je tedy zejména různá prodleva mezi vznikem NAION a podáním léčby a rozdílná doba od ukončení léčby s výstupním zhodnocením efektu terapie. U našich pacientů jsme ani jednou neindikovali dekompresi obalů zrakového nervu. Tato metoda může být indikována v případech progresivní formy NAION. Jirásková et al. [15] ve studii popisuje výsledky této chirurgické metody u konkrétních očních diagnóz, přičemž ve 25 případech byla dekomprese provedena u progresivní formy NAION. Autoři sledovali zrakovou ostrost a změny na perimetru. Prokázali statisticky významné zlepšení zrakové ostrosti i rozsahu zorného pole po operaci. Nejvýraznějšího zlepšení bylo dosaženo tam, kde byla operace provedena včasně. Hodnotili taktéž subjektivní spokojenost pacienta, která byla ve většině případů v kladném smyslu. V multicentrické randomizované klinické studii Ischemic Optic Neuropathy Decompression Trial (IONDT), která byla provedena v USA v letech 1992 až 1994, byla sledována bezpečnost a efekt dekomprese zrakového nervu u nemocných s NAION ve srovnání s kontrolní skupinou, která byla ponechána bez léčby. V této studii bylo vysoké procento peroperačních a pooperačních komplikací, jako je bolest a diplopie, a naopak vysoké procento spontánně zlepšených zrakových funkcí u kontrolní skupiny neléčených nemocných [13]. Výsledky této studie však byly zpochybněny právě pro vysoké procento komplikací souvisejících s operací, které mohly výsledky ovlivnit. Taktéž je sporný výběr nemocných vhodných k dekompresi [16]. Dickersin et al [6] dochází k podobnému závěru.
Výskyt rizikových faktorů kardiovaskulárních nemocí, které jsou zároveň rizikovými faktory vzniku nearteriitické přední ischemické neuropatie optiku, je v České republice v celé populaci vysoký. Hypertenze patří k nejčastějším kardiovaskulárním chorobám. Má u nás vysokou prevalenci, a to 60 % mužů a 62 % žen ve věku mezi 25-64 lety se zřetelným nárůstem výskytu ve vyšších věkových skupinách (v dekádě od 55 do 64 let má vysoký tlak 72 % mužů a 65 % žen) [24]. Prevalence diabetu mellitu 2. typu v České republice neustále narůstá. V současné době je v naší zemi registrováno něco pod 800 tisíc nemocných (8 %) s tímto chronickým metabolickým onemocněním. I celosvětově lze pozorovat zvyšující se výskyt diabetu 2. typu, a to nejen u dospělé populace, ale také u mladistvých. Jedná se o důsledek klesající fyzické aktivity a tomu nepřiměřeně velký energetický příjem [23]. Výskyt hypercholesterolemie udávají autoři ve 40 % [25], některé studie uvádí i vyšší zastoupení. Podle statistik Ministerstva zdravotnictví České republiky se jedná o 70 až 80 % populace. Jelikož se tyto nemoci neprojevují bolestí, řada lidí (až 25 %) o své chorobě vůbec neví a často se zjistí ať už při projevu na srdci, nebo právě na oku.
Atkins et al. [3] ve své práci uvádí, že ve sledovaném souboru pacientů s NAION mělo 60 % alespoň 1 vaskulární rizikový faktor, 47 % mělo hypertenzi a 24 % mělo diabetes. Kouření se v jejich studii nepotvrdilo být rizikovým faktorem vzniku onemocnění. Jako další potenciální rizikové faktory autoři uvádí spánkovou apnoe, celkovou hypoperfuzi, vazospazmy, chybnou autoregulaci, těžkou anemii a noční hypotenzi. Nepotvrdili souvislost s pohlavím. Gaier et al. [8] ve svém souhrnném článku popisuje jako vaskulární faktory vzniku NAION hypertenzi, diabetes, hyperlipidemii a kouření. Hypertenzi uvádí u 39–88 % nemocných s NAION, diabetes mellitus 2. typu v 15–49 % a hyperlipidemii u 48 % pacientů. Kouření uvádí u 49 % postižených. Obdobné výsledky uvádí i Newman et al. ve své rozsáhlé studii [12].
V našem souboru byl v 96 % přítomen alespoň jeden celkový rizikový faktor, nejčastěji se jednalo o vysoký krevní tlak. Všechny tři sledované choroby mělo 36,4 % pacientů. Zajímavým vedlejším výsledkem bylo zjištění, že pacienti s diabetes mellitus dostali častěji kombinovanou léčbu (61,1 %), tedy jejich vstupní nález byl horší.
Naše studie potvrdila, že většina lidí s přední ischemickou neuropatií optiku má některý z rizikových faktorů, a to buď samostatně, nebo v kombinaci. Rizikové faktory by tedy neměly být přehlíženy a mělo by se dbát na jejich důslednou kompenzaci, která vede ke snížení výskytu kardiovaskulárních onemocnění, a tedy i nearteriitické přední ischemie optiku. V naší studii jsme však nebyli schopni hodnotit stupeň kompenzace celkových onemocnění.
Většina zahraničních i domácích autorů uvádí podobné zastoupení těchto rizikových faktorů u nemocných s přední ischemickou neuropatií optiku [3,8,16,18], a to hypertenze (39–88 %), diabetu (15–48 %) a hypercholesterolemie 47 %. V našem souboru jsme zjistili podobný výskyt těchto onemocnění. Malé rozdíly mezi údaji v literatuře a naší studií mohou být vysvětleny odlišným životním stylem, zodpovědnějším přístupem cizinců ke svému zdraví, ale také třeba důslednější zdravotní péčí v České republice, která odhalí tyto nemoci již v preklinickém stádiu. Kuřáků byla v naší skupině menšina, aktivně kouřilo pouze 13,8 % pacientů a 20,7 % byli stopkuřáci s různě dlouhým obdobím od skončení kouření. Nejvíce bylo nekuřáků, nikdy nekouřilo 60,3 % pacientů.
Jako další možné rizikové faktory vzniku NAION je uváděna celá řada dalších patologických stavů – hyperkoagulační stavy (hyperhomocysteinemie), kolagenózy, noční hypotenze, syndrom obstrukční spánkové apnoe, léčba erektilní dysfunkce, polyarteritis nodosa a další. Např. Palombi et al. [19] se ve své studii zaměřil na obstrukční spánkovou apnoe jako rizikový faktor vzniku onemocnění. Zjistil, že 89 % pacientů s NAION splňovalo klinická kritéria pro spánkovou apnoe (sledována byla frekvence apnoe a hypopnoe za hodinu a jejich délka). Také Arda et al. [2] zjistil ve své studii podobný počet vysokého výskytu spánkové apnoe u nemocných s NAION, a to bez rozdílu pohlaví. Naopak Cestari et al. [5] ve své studii zjistil, že obstrukční spánková apnoe nemá spojitost se vznikem NAION. Obstrukční spánková apnoe je tedy častější u pacientů s přední ischemickou neuropatií optiku, ale není přímý rizikový faktor vzniku onemocnění, nýbrž se podílí na onemocnění spolu s dalšími rizikovými faktory. V naší studii jsme se těmto dalším možným rizikovým faktorům nevěnovali.
K predisponujícím morfologickým rizikovým faktorům pro vznik NAION patří výskyt drúz optického nervu a malý terč s malou nebo téměř vymizelou exkavací a výrazně viditelnou vrstvou nervových vláken (tzv. crowded-disc či disc at risk) [9]. V naší studii byla průměrná velikost terče zrakového nervu u pacientů s NAION sice v mezích normy, nicméně malý terč jsme verifikovali u 25 % očí a drúzy zrakového nervu u 1 nemocného. Tato morfologická predispozice v kombinaci s celkovými rizikovými faktory může hrát důležitou roli zejména pro riziko vzniku NAION na druhém oku.
U několika rizikových pacientů ze souboru se i přes vazodilatační intravenózní terapii a trvalou antitrombotickou medikaci objevilo onemocnění NAION i na druhém oku v odstupu několika let. Tento fakt potvrzuje údaje v literatuře, které hodnotí vazodilatační léčbu pouze jako podpůrnou, nikoliv však schopnou nemoc vyléčit a zabránit vzniku onemocnění na druhém oku.
ZÁVĚR
Přední ischemická neuropatie optiku je závažné zrak zhoršující onemocnění, které významně ovlivňuje život člověka. Je druhým nejčastěji se vyskytujícím onemocněním zrakového nervu u pacientů nad 50 let hned za glaukomem [16]. Dosud nelze eliminovat riziko vzniku téhož onemocnění na druhém oku, či rekurenci na oku tomtéž. Dobře známými rizikovými faktory vzniku NAION jsou hypertenze, diabetes mellitus a hypercholesterolemie, které se ukázaly ve vysokém zastoupení i v našem sledovaném souboru. Vzhledem k narůstající prevalenci všech těchto onemocnění, a to i v nižším věku, se můžeme domnívat, že poroste i výskyt NAION. Dosud neexistuje kauzální medikamentózní léčba, která by NAION vyléčila. Máme k dispozici pouze podpůrnou terapii, která působí systémově, přesto je její efekt diskutabilní. V léčbě se doporučuje přísná kompenzace přidružených interních onemocnění.
Čestné prohlášení:
Autoři práce prohlašují, že vznik i téma odborného sdělení a jeho zveřejnění není ve střetu zájmů a není podpořeno žádnou farmaceutickou firmou.
Dále autoři prohlašují, že práce nebyla zadána jinému časopisu ani jinde otištěna, s výjimkou kongresových abstrakt a doporučených postupů.
Do redakce doručeno dne: 26. 12. 2019
Do tisku přijato dne: 8. 3. 2020
MUDr. Silvie Kalábová
Oční klinika LF UP a FN Olomouc
I. P. Pavlova 6
779 00 Olomouc
Sources
1. Al-Zubidi, N. et al.: Systemic corticosteroids in nonarteritic ischemic optic neuropathy. Indian J Ophthalmol, 62(10);2014 : 1022–1024.
2. Arda, H., Birer, S., Aksu, M. et al.: Obstructive sleep apnoea prevalence in nonarteritic anterior ischaemic optic neuropathy. Br J Ophthalmol,97;2013 : 206-209.
3. Atkins, EA., Beau, BB., Newman, NJ., Biousse, V.: Treatment of Nonarteritic Anterior Ischemic Optic Neuropathy, Surv Ophthalmol,55(1);2010 : 47–63.
4. Biousse, V., Newman, NJ.: Ischemic optic neuropathies. N Engl J Med,372;2015 : 2428–2436.
5. Cestari, DM., Gaier, ED., Bouzika P. et al.: Demographic, systemic and ocular factors associated with non-arteritic anterior ischemic optic neuropathy. Ophthalmology,123(12);2016 : 2446–2455.
6. Dickersin, K., Li, T.: Surgery for nonarteritic anterior ischemic optic neuropathy. Cochrane Database Syst Rev,12(3);2015: CD001538.
7. Foulds, WS.: Visual disturbances in systemic disorders: optic neuropathy and systemic disease. Trans Ophthalmol Soc UK,89; 1970 : 125–46.
8. Gaier, ED., Turon, N.: The enigma of nonarteritic anterior ischemic optic neuropathy, Curr Opin Ophthalmol,27(6);2016 : 498–504.
9. Hauptvogelová, M., Šustykevičová, Z.: Non-arteritická predná ischemická optická neuropatia pri drúzách zrakového nervu. Cesk Slov Oftalmol,66 (4);2010 : 184–187.
10. Hayreh, SS., Zimmerman, MB.: Non-arteritic anterior ischemic optic neuropathy: role of systemic corticosteroid therapy. Graefes Arch Clin Exp Ophthalmol,246(7);2008 : 1029–46.
11. Hayreh, SS.: Anterior ischemic optic neuropathy. III. Treatment, prophylaxis and differential diagnosis. Br J Ophthalmol,58(12); 1974 : 981–9.
12. Newman, JN. et al.: (Research group):Characteristics of patients with nonarteritic anterior ischemic optic neuropathy eligible for the Ischemic Optic Neuropathy Decompression Trial. Arch Ophthalmol,114;1996 : 1366–1374.
13. Kaufman, D. et al. (Research group): Ischemic optic neuropathy decompression trial: twenty-four-month update. Arch Ophthalmol,118;2000 : 793–798.
14. Jirásková,N., Studnička, J., Rozsíval, P.: Papiledém a ischemický edém terče optiku, Čas Lék Čes,151;2012 : 527–530.
15. Jirásková, N., Rozsíval, P.: Výsledky 62 dekompresí obalů zrakového nervu,Cesk Slov Oftalmol,3;1999 : 136–144.
16. Jirásková, N.: Neurooftalmologie, minimum pro praxi, Triton, 2001,26–30 s.
17. Kuchynka, P. et al.: Oční lékařství, Grada, 2007,262 s.
18. Kuchynka, P. et al.: Oční lékařství, Grada, 2007,513–514 s.
19. Palombi, K.,Renard, E., Levy, P. et al.: Nonarteritic anterior ischaemic optic neuropathy is nearly systematicaly associated with obstructive sleep apnoea. Br J Ophthalmol,90;2006 : 879–882.
20. Pazderová, M., Novák, J.: Změny v tloušťce nervových vláken u non-arteritické formy AION na OCT,Cesk Slov Oftalmol,65(3); 2009 : 87–90.
21. Rebolleda, G., Pérez-López, M., Casas-LLera, P.: Visual and anatomical outcomes of non-arteritic anterior ischemic optic neuropathy with high-dose systemic corticosteroids. Graefes Arch Clin Exp Ophthalmol,251;2013 : 255–60.
22. Steigerwalt, RD., Cesarone, MR., Belcaro, G.: Arteritic anterior ischemic optic neuropathy treated with intravenous prostaglandin E1 and steroids.Int J Angiol, 19(3);2010 : 113–115.
23. Špinar, J., Lábrová, R.: Dapagliflozin a studie DECLARE – budoucnost léčby diabetes mellitus, Kardiol Rev Int Med,18(2);2016 : 119–124.
24. Štejfa, M.: Progresivní kontinuum – hypertenze, ischemická choroba srdeční, srdeční selhání a náhrada srdeční funkce, Kardiol Rev Int Med,13(1);2011 : 7–8.
25. Žák, A. a kolektiv: Ateroskleróza: Nové pohledy, Grada, 2011,96 s.
Labels
Ophthalmology
Article was published inCzech and Slovak Ophthalmology

2020 Issue 2-
All articles in this issue
- Zemřela prof. MUDr. Jarmila Boguszaková DrSc.
- Vzpomínka na doc. MUDr. Cigánka, CSc.
- EPIGENETICKÉ ZMENY V PATOGENÉZE MALÍGNEHO MELANÓMU UVEY A MOŽNOSTI ICH TERAPEUTICKÉHO OVPLYVNENIA. PRIEHLAĎ
- PRIMÁRNY INTRABULBÁRNY NEUROFIBRÓM
- ZVYŠUJE INTRAKAMERÁLNÍ APLIKACE TRIAMCINOLON ACETONIDU ÚČINNOST FAKOTRABEKULEKTOMIE? PŘÍPADOVÁ KONTROLNÍ STUDIE
- NEARTERITICKÁ FORMA PŘEDNÍ ISCHEMICKÉ NEUROPATIE OPTIKU - LÉČBA A RIZIKOVÉ FAKTORY
- AFLIBERCEPT V LÉČBĚ VASKULÁRNÍ SERÓZNÍ ABLACE PIGMENTOVÉHO LISTU SÍTNICE: ROČNÍ VÝSLEDKY ANATOMICKÝCH A FUNKČNÍCH ZMĚN
- BETAXOLOL, BRIMONIDIN A CARTEOLOL V LÉČBĚ NORMOTENZNÍCH GLAUKOMŮ.
- Czech and Slovak Ophthalmology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- NEARTERITICKÁ FORMA PŘEDNÍ ISCHEMICKÉ NEUROPATIE OPTIKU - LÉČBA A RIZIKOVÉ FAKTORY
- Vzpomínka na doc. MUDr. Cigánka, CSc.
- BETAXOLOL, BRIMONIDIN A CARTEOLOL V LÉČBĚ NORMOTENZNÍCH GLAUKOMŮ.
- AFLIBERCEPT V LÉČBĚ VASKULÁRNÍ SERÓZNÍ ABLACE PIGMENTOVÉHO LISTU SÍTNICE: ROČNÍ VÝSLEDKY ANATOMICKÝCH A FUNKČNÍCH ZMĚN
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

