-
Medical journals
- Career
AFLIBERCEPT V LÉČBĚ VASKULÁRNÍ SERÓZNÍ ABLACE PIGMENTOVÉHO LISTU SÍTNICE: ROČNÍ VÝSLEDKY ANATOMICKÝCH A FUNKČNÍCH ZMĚN
Authors: J. Románek 1; H. Palyzová 2; J. Grygar 2; J. Ernest 2
Authors‘ workplace: TANA oční klinika, s. r. o. 1; Oční klinika 1. Lékařské fakulty Univerzity Karlovy a Ústřední vojenské nemocnice v Praze 2
Published in: Čes. a slov. Oftal., 76, 2020, No. 2, p. 88-93
Category: Original Article
doi: https://doi.org/10.31348/2020/16Overview
Cíl: Zhodnotit výsledky roční terapie preparátem aflibercept u terapeuticky naivních pacientů s nálezem serózní ablace pigmentového listu sítnice (RPE) na podkladě okultní choroidální neovaskularizace (CNV).
Soubor a metodika: Retrospektivní analýza léčby 36 pacientů (38 očí) průměrného věku 77 let (SD ± 7) preparátem aflibercept 2,0 mg (Eylea, Bayer) na Oční klinice 1. Lékařské fakulty Univerzity Karlovy a Ústřední vojenské nemocnice v Praze. Všichni pacienti byli léčeni dle souhrnu údajů o přípravku (SPC) ve fixním režimu léčby, tj. třemi úvodními dávkami v měsíčních intervalech s následnou aplikací každé dva měsíce v celkové délce léčby 12 měsíců. Nejlépe korigovaná zraková ostrost (BCVA) byla hodnocena na ETDRS optotypech (Early Treatment Diabetic Retinopathy Study), parametry jako výška a šířka ablace RPE a centrální retinální tloušťka (CRT) byly měřeny pomocí spektrální optické koherenční tomografie (SD-OCT). Tyto hodnoty byly sledovány při vstupním vyšetření a dále při každé vizitě. Sledovali jsme také výskyt komplikací terapie.
Výsledky: Na konci sledovacího období jsme zaznamenali nárůst BCVA o 3,2 písmen (SD ± 11,6) ETDRS optotypu, tato změna byla na hranici signifikance (p = 0,05). Průměrná hodnota výšky ablace RPE po 12 měsících statisticky významně poklesla o 140 µm (SD ± 238, p < 0,01). Redukce výšky ablace silně korelovala se snížením CRT (R = 0,94, p < 0,001) a dále se zmenšením šířky ablace (R = 0,45, p < 0,01). Nebyla nalezena signifikantní korelace mezi poklesem výšky ablace a ziskem zrakové ostrosti. Ruptura RPE v průběhu léčby vznikla u 3 očí (8 %).
Závěr: Intravitreální léčba afliberceptem ve fixním režimu u pacientů se serózní ablací RPE na podkladě okultní CNV vykazuje vynikající anatomický efekt.
Nicméně korelace mezi ziskem písmen na ETDRS optotypech a zmenšením rozměrů ablace RPE nebyla zaznamenána.
Klíčová slova:
aflibercept – anti-VEGF – ablace pigmentového listu sítnice – okultní CNV
ÚVOD
Věkem podmíněná makulární degenerace (VPMD) je progresivní chronické onemocnění, které je nejčastější příčinou praktické slepoty ve vyspělých zemích u osob starších 50 let [1]. Za tento fakt je zodpovědná především její exsudativní forma se vznikem choroidální neovaskularizace [2]. V diagnostice exsudativní formy VPMD rozlišujeme několik jejich subtypů, z čehož kolem 10 % představuje vaskulární serózní ablace pigmentového listu sítnice [3]. Vaskulární serózní ablace RPE na podkladě okultní CNV nebo centrální retinální angiomatózní proliferace (RAP) je komplikovaným stavem s odlišným vývojem oproti ostatním neovaskulárním lézím. Horší prognóza je dána, kromě samotného procesu progrese CNV, přidruženou atrofizací RPE, rizikem jeho ruptury a v konečném důsledku tvorbou disciformní jizvy [4]. Nastavení ideálního léčebného plánu je považováno za složité nejen díky výše zmíněním komplikacím, ale také díky obecně nízké anatomické a funkční účinnosti léčby, což prokazují mnohé studie [5,6,7,8]. Jako jedinou, v současné době schválenou léčbou dle SPC, je intravitreální anti-VEGF terapie. Dle probíhajících studií se dále jeví jako účinná kombinace fotodynamické terapie a anti-VEGF [9].
Cílem této studie je retrospektivní zhodnocení roční léčby skupiny pacientů s nově diagnostikovanou serózní ablací RPE sekundární k okultní formě CNV a porovnání našich výsledků s výsledky klinických studií. V léčbě byl použit preparát aflibercept v režimu fixního dávkování.
SOUBOR, METODIKA
Do této retrospektivní studie prováděné na Oční klinice 1. Lékařské fakulty Univerzity Karlovy a Ústřední vojenské nemocnice v Praze bylo zařazeno 36 pacientů, 38 očí. Léčba probíhala v období od ledna 2017 do června 2019. Tabulka 1 shrnuje základní demografické a klinické údaje souboru pacientů.
Table 1. Vstupní demografické a klinické charakteristiky (počet pacientů n = 36) 
ETDRS = Early Treatment Diabetic Retinopathy Study, n = počet pacientů, RPE = retinální pigmentový epitel, SD = standardní odchylka Podmínkou zařazení do studie byl terapeuticky naivní pacient s nově diagnostikovanou vaskulární serózní ablací RPE, která byla po dobu nejméně 12 měsíců léčena přípravkem aflibercept ve fixním režimu. Léčba vycházela ze souhrnu údajů o přípravku, tedy zahájením třemi intravitreálními injekcemi 2 mg afliberceptu po jednom měsíci a dále čtyřmi injekcemi po dvou měsících. Vstupními kritérii, kromě výše uvedené diagnózy, byla nejlépe korigovaná zraková ostrost v rozmezí 35–70 ETDRS optotypu, rozsah léze do 8 DA (disc area, plocha papily zrakového nervu), rozsahu hemoragie maximálně do 25 % léze a průkaz aktivní CNV fluorescenční angiografií a spektrální optickou koherentní tomografií (SD-OCT). Přítomná vaskulární serózní ablace RPE musela mít subfoveolární lokalizaci (v rozmezí maximálně 500 µm od fovey) a vstupní výšku větší než 250 µm. Při každé vizitě bylo provedeno kompletní vyšetření zahrnující stanovení BCVA na ETDRS optotypech a SD-OCT (Heidelberg Spectralis; Heidelberg Industries, Heidelberg, Germany). Fluorescenční angiografie byla provedena při vstupní vizitě k potvrzení přítomnosti choroidální neovaskularizace asociované se serózní ablací RPE (Obrázek 1). Centrální retinální tloušťka byla definována jako vzdálenost mezi vnitřní limitující membránou (MLI) a Bruchovou membránou. Výška ablace RPE byla měřena softwarovým kaliperem jako maximální vertikální rozměr od RPE k Bruchově membráně (Obrázek 2). Šířka ablace RPE byla měřena identickou metodou jako maximální horizontální rozměr.
Image 1. Fluorescenční angiografie při vstupním vyšetření A. Časná fáze fluorescenční angiografie zachycující hyperfluorescenční ložisko choroidální neovaskularizace s průsakem v horním okraji léze, již okrajové plnění ablace retinálního pigmentového epitelu, při dolním okraji patrná hypofluorescence odpovídající hemoragii B. Střední fáze s postupným plněním ložiska ablace retinálního pigmentového epitelu fluoresceinem C. Pozdní fáze zachycující homogenní hyperfluorescenci s ostrými okraji 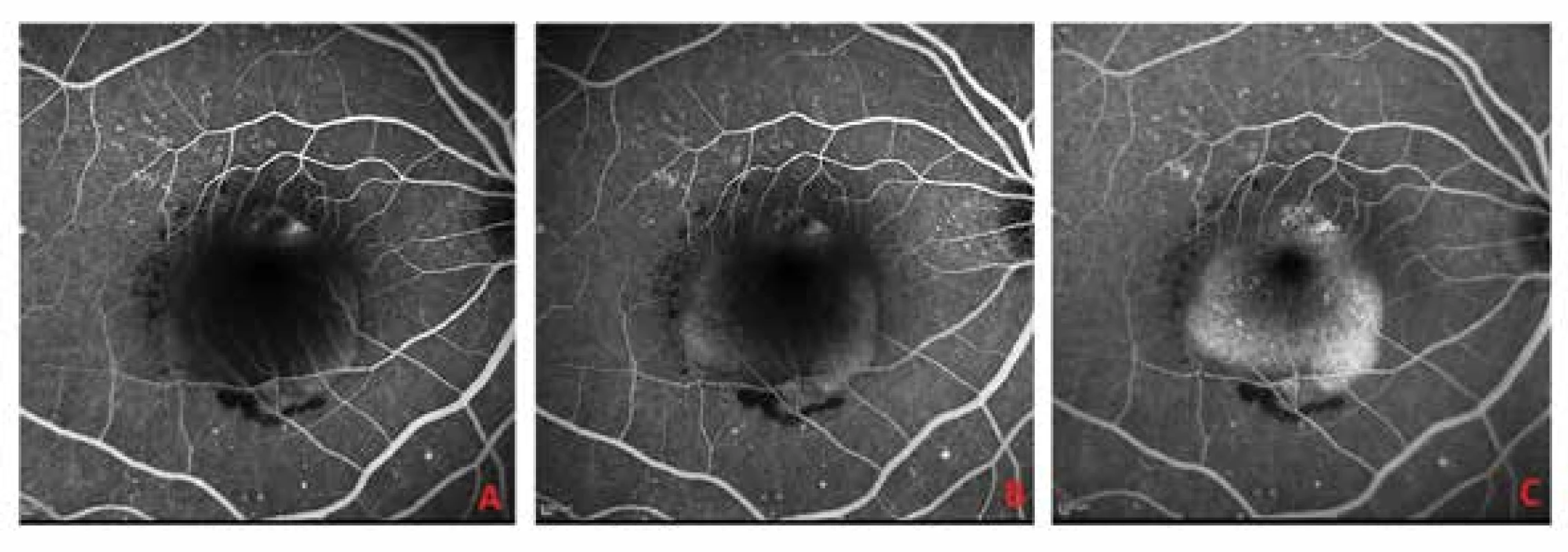
Image 2. SD-OCT snímek vaskulární serózní ablace retinálního pigmentového epitelu na podkladě okultní choroidální neovaskularizace A. Metodika měření výšky ablace retinálního pigmentového epitelu B. Metodika měření šířky ablace retinálního pigmentového epitelu 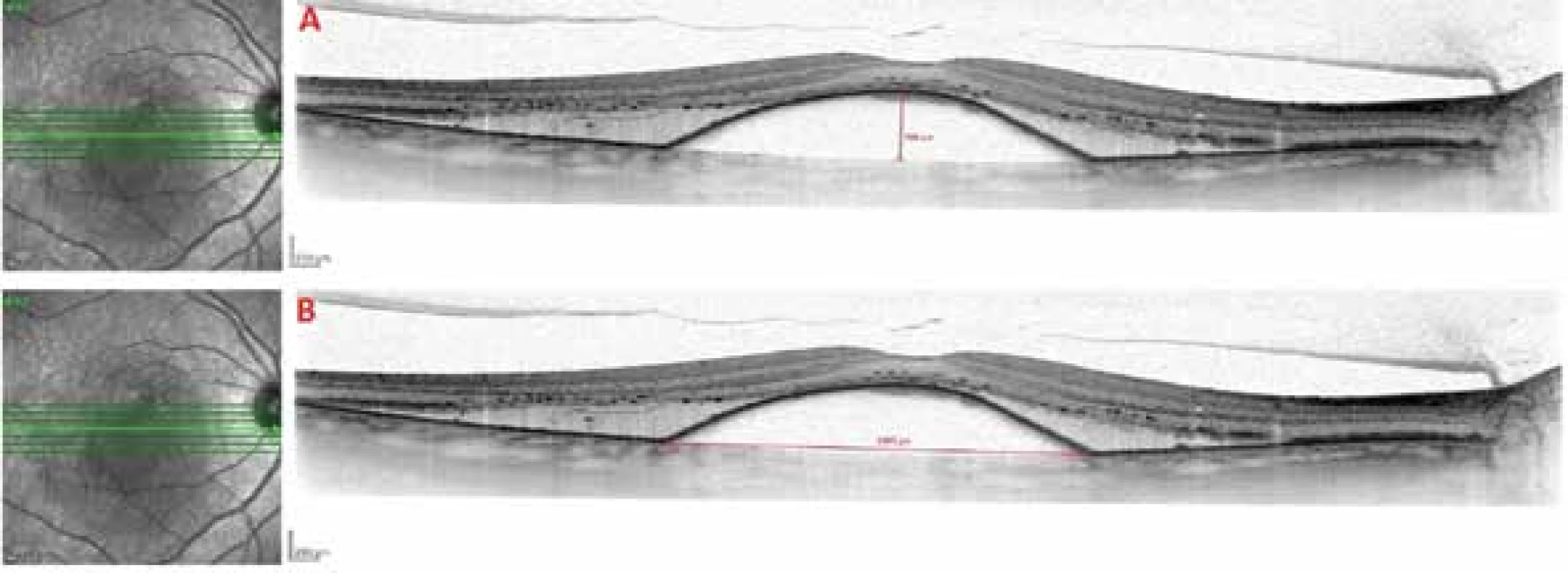
Statistická analýza
Kvantitativní hodnoty byly definovány průměrem a směrodatnou odchylkou. Následně byly analyzovány testem normality Kolmogorova-Smirnova. Jejich změny byly hodnoceny pomocí Studentova t-testu. Korelace mezi změnami výšky a šířky ablace RPE a CRT byla stanovena pomocí Pearsonova koeficientu korelace. Statistická významnost byla stanovena jako p < 0,05.
VÝSLEDKY
Ve vybraném souboru pacientů (38 očí), došlo po úvodních třech intravitreálních aplikacích afliberceptu ke zlepšení BCVA, oproti vstupním hodnotám, v průměru o 4,8 písmen (SD ± 9,0) ETDRS optotypu. Průměrná BCVA byla 61 písmen (SD ± 12). Tato změna byla hodnocena jako signifikantní o hladině významnosti p < 0,01. Ke zlepšení o více než 15 písmen došlo u 4 očí (11 %), 10 očí (26 %) se zlepšilo o 10 až 14 písmen, 9 očí (24 %) se zlepšilo v rozmezí 3 až 9 písmen.
Ke zhoršení o více než 15 písmen nedošlo u žádného ze studijních očí, zhoršení o 10 až 14 písmen bylo zaznamenáno u 2 očí (5 %) a zhoršení o 3 až 9 písmen bylo zjištěno u 6 očí (16 %). Sedm očí (18 %) bylo hodnoceno jak stabilních (rozmezí mezi ztrátou 2 písmen až zisku 2 písmen).
Při hodnocení BCVA po finální sedmé aplikaci, byla její průměrná hodnota 59 písmen (SD ± 13), průměrný zisk při porovnání se vstupní zrakovou ostrostí byl 3,2 písmen (SD ± 11,6). Tato změna, je ale dle statistické významnosti na hranici signifikance (p = 0,05). Zlepšení o > 15 písmen bylo zaznamenáno u 5 očí (13 %), zlepšení o 10–14 písmen také u 5 očí (13 %) a zlepšení o 3–9 písmen u 12 očí (32 %). Naopak 3 oči (8 %) se zhoršily o > 15 písmen, 2 oči (5 %) o 10–14 písmen a 6 očí (16 %) o 3–9 písmen. Stabilních (rozmezí mezi ztrátou 2 písmen až zisku 2 písmen) zůstalo 5 očí (13 %). Vývoj absolutních hodnot BCVA v průběhu aplikací zobrazuje Graf 1.
Graph 1. Změna nejlépe korigované zrakové ostrosti v průběhu ročního sledování 
Průměrná výška ablace RPE byla při vstupním vyšetření 479 µm (SD ± 202). V průběhu aplikací došlo k jejímu signifikantnímu snížení. Po 3. aplikaci došlo ke snížení výšky ablace o 132 µm (SD ± 205) při srovnání se vstupními hodnotami (p < 0,01). Ke kompletnímu vstřebání ablace v této fázi léčby nedošlo u žádného ze sledovaných očí. Pokud budeme hodnotit anatomickou regresi nálezu jako pokles výšky > 50 µm, tak k tomuto zlepšení došlo u 23 očí (61 %). Naopak zvětšení výšky ablace o > 50 µm bylo zaznamenáno u 4 očí (11 %).
Dále pak 11 očí (28 %) zůstalo stabilních. Průměrné snížení výšky ablace RPE po 7. aplikaci, v porovnání se vstupními měřeními, bylo 140 µm (SD ± 238, p < 0,01). K celkovému zlepšení nálezu (pokles výšky o > 50 µm) došlo u 23 očí (61 %). K celkovému zhoršení nálezu (vzestup výšky o > 50 µm) došlo u 5 očí (13 %). Stabilních zůstalo 10 očí (26 %). V jednom případě nastalo kompletní vstřebání ablace RPE.
Změny v hodnotách výšky ablace RPE korelovaly se změnami CRT (R = 0,94, p < 0,001). Tato korelace je dána subfoveolárním uložením ablace RPE. Redukce šířky ablace také korelovala s poklesem výšky ablace (R = 0,45, p < 0,01). To samé platilo při porovnání vývoje hodnot šířky ablace RPE a CRT (R = 0,46, p < 0,01). Vývoj absolutních hodnot výšky ablace RPE, šířky ablace RPE a CRT zobrazuje Graf 2.
Graph 2. Změny výšky a šířky ablace RPE a centrální retinální tloušťky v průběhu ročního sledování 
OCT nález při finální vizitě nevykazoval známky exsudativní aktivity (přítomnost intraretinální nebo subretinální tekutiny) u 15 očí (39 %). U dvou očí (5 %) byla zaznamenána přítomnost trhliny RPE při vstupní vizitě. V případě dalších 3 očí (8 %) došlo k ruptuře RPE, a to ve všech případech ihned po úvodní aplikaci. Ostatní komplikace spojené s intravitreální aplikací léčiv nebyly pozorovány.
DISKUSE
Okultní CNV asociovaná se serózní ablací RPE je považována za specifickou entitu exsudativní VPMD s obtížnou léčbou [10,11,12]. Dle Pauleikhoff a kol. [12] dochází bez léčby k signifikantní ztrátě BCVA o více než 3 řádky u 40 %–50 % očí v průběhu jednoho roku.
Khanani a kol. [13] analyzovali několik retrospektivních studií zkoumajících vliv anti-VEGF terapie, v různých intervalech dávkování, na vývoj ablace RPE sekundární k CNV. Pět ze zkoumaných retrospektivních studií zaznamenalo anatomické i funkční zlepšení, stejný počet studií popisuje zrakovou stabilitu a anatomické zlepšení a jedna studie popisuje pokles hodnot zrakové ostrosti i přes anatomické zlepšení nálezu. Závěrem této široké analýzy je náročná predikce anatomických a funkčních změn a absence jejich korelace.
Chen a kol. [14] hodnotil vliv léčby afliberceptem v průběhu jednoho roku u 28 očí s ablací RPE sekundární k okultní CNV. Studie prokázala zlepšení BCVA o 4,5 písmen (SD ± 23) ETDRS optotypu. Naše výsledky prokazují identický trend se zlepšením o 3,2 písmen (SD ± 11,6). Menší zisk přisuzujeme odlišnému léčebnému schématu, kdy na rozdíl od naší studie probíhala léčba intenzivněji, a to na úvod šesti měsíčními aplikacemi a až následně režimem dvouměsíčního dávkování. Právě délka tzv. loading fáze měla pravděpodobně podíl na lepším vývoji BCVA. V naší studii průměrná BCVA 61 písmen (SD ± 12) po 3. aplikaci poklesla na 59 písmen (SD ± 14) po 7. aplikaci. Je pravděpodobné, že k tomuto jevu přispěla změna z měsíčního intervalu loading fáze na interval dvouměsíčního dávkování. Tento závěr je ve shodě s dalšími klinickými studiemi zabývajícími se léčbou okultní CNV asociované se serózní ablací RPE v režimu dvouměsíčního aplikačního intervalu [15,16].
Broadhead a kol. [15] analyzovali anatomické změny v rámci roční léčby afliberceptem u 43 očí s ablací RPE sekundární k CNV. Šlo o skupinu pacientů s rezistentním nálezem ablace RPE po předchozí anti-VEGF terapii. Na konci sledovacího období zaznamenali anatomické zlepšení s poklesem výšky o > 50 µm u 42 % očí (v našem souboru 61 % očí), stabilní nález u 56 % očí (v našem souboru 26 %) a anatomické zhoršení u 2 % očí (v našem souboru 13 %). Odlišné proporcionální rozdělení u zmíněné studie, s převahou stabilních nálezů, je možné přisoudit předchozí anti-VEGF terapii. Přesto i v této studii, stejně jako naší, jsou změny poklesu výšky ablace RPE hodnoceny jako signifikantní.
Pokles výšky ablace RPE z průměrných 479 µm (SD ± 205) na 340 µm (SD ± 179) po ročním sledování v naší studii je ve srovnání s rozsáhlou studií publikovanou Cho a kol. [17] menší. Tato studie analyzuje soubor 202 očí s ablací RPE sekundární k CNV v rámci roční léčby ranibizumabem nebo afliberceptem s tří měsíční loading fází a následným režimem pro re nata (PRN). Udává pokles výšky ablace RPE z počátečních průměrných 453 µm (SD ± 261) na 230 µm (SD ± 142).
Méně výrazný pokles výšky ablace přisuzujeme menšímu počtu pacientů v našem souboru (38 očí oproti 202 očím v práci Cho a kol.). Přidruženým výsledkem zmíněné studie je signifikantně větší účinnost afliberceptu na pokles výšky ablace RPE v porovnání sranibizumabem (Lucentis, Novartis) [17].
Nález aktivity CNV potvrzené na OCT u 61 % očí v naší studii po 7. aplikaci, byl ve shodě s výsledky publikovanými Zinkernagel a kol. [16], kteří udávají při finálním hodnocení nálezu přítomnost intraretinální nebo subretinální tekutiny u 55 % očí.
Absence signifikantní korelace mezi poklesem výšky ablace a ziskem písmen v naší studii je konzistentní s výsledky jiných studií zabývajících se vlivem anti-VEGF terapie na rozměr ablace RPE [8,15,22]. Zlepšení BCVA u těchto pacientů je velmi suspektně dáno vlivem jiných faktorů, jako je přítomnost či absence intraretinální nebo subretinální tekutiny, než jen změna velikosti ablace RPE [8,15,22]. Naopak studie publikované Zinkernagel a kol. [16] a Chen a kol. [14] tvrdí, že úplné vstřebání ablace vede k vyššímu výskytu atrofie RPE, čili kompletní anatomická úprava není pro úspěšnost léčby stran zrakové ostrosti nutná nebo dokonce žádoucí.
Ruptura RPE může být, dle lokalizace, stavem komplikujícím terapii. Vzniká na podkladě kontrakce neovaskulární membrány po aplikovaném anti-VEGF preparátu. Zvýšené riziko je především u rozsáhlejších vaskulárních ablací RPE z důvodu většího intraluminálního tlaku [18]. Jako riziková je považována výška ablace větší než 400 µm [19]. Popisovaná incidence RPE ruptur je 17 %–26 % [18,20] s převažujícím výskytem v iniciálních fázích terapie [21]. V naší studii jsme zaznamenali výskyt ruptury u 8 % sledovaných (3 oči). Diskrepance v incidenci je opět dána menším souborem pacientů, ale ve všech zaznamenaných případech došlo k výskytu ruptury ihned po první aplikaci anti-VEGF preparátu, což je ve shodě s výsledky prezentovanými již zmíněnou studií [21].
Limitacemi naší studie je její retrospektivní design, menší soubor pacientů a absence kontrolní skupiny pacientů léčených jiným anti-VEGF preparátem.
ZÁVĚR
Závěrem lze konstatovat, že naše studie potvrdila vliv afliberceptu na anatomické zlepšení nálezu vaskulární serózní ablace RPE s její signifikantní redukcí. Absence spojitosti mezi poklesem ablace a ziskem písmen indikuje, že léčba tohoto subtypu CNV je při současné terapii nedostatečná a vyžaduje další studie zkoumající nové postupy či metody.
Čestné prohlášení: Autoři práce prohlašují, že vznik i téma odborného sdělení a jeho zveřejnění není ve střetu zájmů a není podpořeno žádnou farmaceutickou firmou. Zároveň čestně prohlašuji, že tato práce nebyla zadána jinému časopisu ani jinde otištěna.
Do redakce doručeno dne: 21. 2. 2020
Do tisku přijato dne: 5. 3. 2020
MUDr. Jaroslav Románek
TANA oční klinika, s.r.o.
Uhelná 8, 779 00 Olomouc
Sources
1. Klein, R., Klein, BE., Knudtson, MD., Meuer, SM., Swift, M., Gangnon, RE.: Fifteen-year cumulative incidence of age-related macular degeneration. Ophthalmology. 2007;114(2):253–262.
2. Bressler, NM.: Age-related macular degeneration is the leading cause of blindness. JAMA. 2004; 291(15):1900–1901.
3. Lommatzsch, APOD., Heimes, B., Gutfleisch, M. et al.: Serous pigment epithelial detachment in age-related macular degeneration: comparison of different treatments. Eye. 2009;23 : 2163–2168.
4. Poliner, LS., Olk, RJ., Burgess, D., Gordon, ME.: Natural history of retinal pigment epithelial detachments in age-related macular degeneration. Ophthalmology. 1986;93(5):543–551.
5. Suzuki, M., Nagai, N., Izumi-Nagai, K. et al.: Predictive factors for non-response to intravitreal ranibizumab treatment in agerelated macular degeneration. Br J Ophthalmol. 2014;98(9):1186–1191.
6. Ashraf, M., Souka, A., Adelman, RA.: Age‐related macular degeneration: using morphological predictors to modify current treatment protocols. Acta Ophthalmol. 2018;96 : 120-133.
7. Patel, KH., Chow, CC., Rathod, R. et al.: Rapid response of retinal pigment epithelial detachments to intravitreal aflibercept in neovascular age-related macular degeneration refractory to bevacizumab and ranibizumab. Eye (Lond). 2013;27 : 663–667.
8. Parodi, MB., Iacono, P., Papayannis, A. et al.: Intravitreal ranibizumab for pigment epithelial detachment with subfoveal occult neovascularization: a prospective 24-month case series. Am J Ophthalmol. 2013;155 : 103–108.
9. Gonzalez, A., Khurshid, G.: Treatment of retinal pigment epithelial detachment secondary to exudative age-related macular degeneration. Am J Ophthalmol Case Rep. 2017;9 : 18–22.
10. Gass, JD.: Serous retinal pigment epithelial detachment with a notch. A sign of occult choroidal neovascularization. Retina 1984;4(4):205–220.
11. Bird, AC., Marshall, J.: Retinal pigment epithelial detachments in the elderly. Trans Ophthalmol Soc. 1986;105 : 674–682.
12. Pauleikhoff, D., Loffert, D., Spital, G. et al.: Pigment epithelial detachment in the elderly. Clinical differentiation, natural course and pathogenetic implications. Graefes Arch Clin Exp Ophthalmol. 2002;240(7):533–538.
13. Khanani, AM., Eichenbaum, D., Schlottmann, PG., Tuomi, L., Sarraf, D.: Optimal management of pigment epithelial detachments in eyes with neovascular age-related macular degeneration. Retina. 2018;38(11):2103–2117.
14. Chen, X., Al-Sheikh, M., Chan, CK. et al.: Type 1 versus type 3 neovascularization in pigment epithelial detachments associated with age-related macular degeneration after anti-vascular endothelial growth factor therapy: a prospective study. Retina. 2016;36(S1):S50–S64.
15. Broadhead, GK., Hong, T., Zhu, M. et al.: Response of pigment epithelial detachments to intravitreal aflibercept among patients with treatment-resistant neovascular age-related macular degeneration. Retina. 2015;35 : 975–981.
16. Zinkernagel, MS., Wolf, S., Ebneter, A.: Fluctuations in pigment epithelial detachment and retinal fluid using a bimonthly treatment regimen with aflibercept for neovascular age-related macular degeneration. Ophthalmologica. 2016;235 : 42–48.
17. Cho, HJ., Kim, KM., Kim, HS. et al.: Response of pigment epithelial detachment to anti-vascular endothelial growth factor treatment in age-related macular degeneration. Am J Ophthalmol. 2016;166 : 112–119.
18. Introini, U., Torres Gimeno, A., Scotti, F. et al.: Vascularized retinal pigment epithelial detachment in age-related macular degeneration: treatment and RPE tear incidence. Graefes Arch Clin Exp Ophthalmol. 2012;250 : 1283–1292.
19. Chan, CK., Abraham, P., Meyer, CH. et al.: Optical coherence tomography-measured pigment epithelial detachment height as a predictor for retinal pigment epithelial tears associated with intravitreal bevacizumab injections. Retina. 2010;30 : 203–211.
20. Chang, LK., Sarraf, D.: Tears of the RPE: an old problem in a new era. Retina. 2007;27 : 523–527.
21. Cunningham, ET. Jr., Feiner, L., Chung, C. et al.: Incidence of retinal pigment epithelial tears after intravitreal ranibizumab injection for neovascular age-related macular degeneration. Ophthalmology. 2011;118 : 2447–2452.
22. Panos, GD., Gatzioufas, Z., Petropoulos, IK. et al.: Effect of ranibizumab on serous and vascular pigment epithelial detachments associated with exudative age-related macular degeneration. Drug Des Devel Ther. 2013;7 : 565–569.
Labels
Ophthalmology
Article was published inCzech and Slovak Ophthalmology

2020 Issue 2-
All articles in this issue
- Zemřela prof. MUDr. Jarmila Boguszaková DrSc.
- Vzpomínka na doc. MUDr. Cigánka, CSc.
- EPIGENETICKÉ ZMENY V PATOGENÉZE MALÍGNEHO MELANÓMU UVEY A MOŽNOSTI ICH TERAPEUTICKÉHO OVPLYVNENIA. PRIEHLAĎ
- PRIMÁRNY INTRABULBÁRNY NEUROFIBRÓM
- ZVYŠUJE INTRAKAMERÁLNÍ APLIKACE TRIAMCINOLON ACETONIDU ÚČINNOST FAKOTRABEKULEKTOMIE? PŘÍPADOVÁ KONTROLNÍ STUDIE
- NEARTERITICKÁ FORMA PŘEDNÍ ISCHEMICKÉ NEUROPATIE OPTIKU - LÉČBA A RIZIKOVÉ FAKTORY
- AFLIBERCEPT V LÉČBĚ VASKULÁRNÍ SERÓZNÍ ABLACE PIGMENTOVÉHO LISTU SÍTNICE: ROČNÍ VÝSLEDKY ANATOMICKÝCH A FUNKČNÍCH ZMĚN
- BETAXOLOL, BRIMONIDIN A CARTEOLOL V LÉČBĚ NORMOTENZNÍCH GLAUKOMŮ.
- Czech and Slovak Ophthalmology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- NEARTERITICKÁ FORMA PŘEDNÍ ISCHEMICKÉ NEUROPATIE OPTIKU - LÉČBA A RIZIKOVÉ FAKTORY
- Vzpomínka na doc. MUDr. Cigánka, CSc.
- BETAXOLOL, BRIMONIDIN A CARTEOLOL V LÉČBĚ NORMOTENZNÍCH GLAUKOMŮ.
- AFLIBERCEPT V LÉČBĚ VASKULÁRNÍ SERÓZNÍ ABLACE PIGMENTOVÉHO LISTU SÍTNICE: ROČNÍ VÝSLEDKY ANATOMICKÝCH A FUNKČNÍCH ZMĚN
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

