-
Medical journals
- Career
Intravenózní trombolytická terapie rekombinantním tkáňovým aktivátorem plazminogenu rt-PA (Actilyse®) – naše první zkušenosti z praxe
Authors: J. Pribula 1; P. Grajcar 2; A. Pribulová 3
Authors‘ workplace: neurologické oddělení, Městská nemocnice, Litoměřice 1; kardiovaskulární JIP, Městská nemocnice, Litoměřice 2; rehabilitační oddělení, Městská nemocnice, Litoměřice 3
Published in: Cesk Slov Neurol N 2007; 70/103(1): 57-61
Category: Short Communication
Motto: „ … nejvyšší prioritou je léčit všechny pacienty bezodkladně. To znamená, že týmy specializované na léčbu akutních ischemických iktů by měly zaměřit celé své úsilí na redukci času od příjezdu pacienta do nemocnice po zahájení léčby rt-PA za účelem zlepšit možnosti na příznivější uzdravení“ [1].
Profesor Werner Hacke, přednosta Neurologické kliniky, Univerzita v Heidelbergu, Německo, předseda vědecké komise studie ECASS IIOverview
Práce analyzuje první zkušenosti s intravenózní trombolytickou terapií rekombinantním aktivátorem plazminogenu (rt-PA) u pacientů postižených akutní ischemickou cévní mozkovou příhodou (aiCMP) v terapeutickém intervalu do 3 hodin od vzniku symptomatologie iktu. Retrospektivně hodnotí její průběh, výsledky a bezpečnost v lokálních podmínkách. Od ledna 2005 do června 2006 bylo na našem pracovišti léčeno 203 pacientů s aiCMP. Osm z nich (3,9 %) bylo léčených systémovou intravenózní trombolytickou terapií rt-PA. Indikační kritéria pro trombolytickou terapii byla identická s doporučením České lékařské komory (ČLK). Trombolytická léčba byla podána 5 mužům a 3 ženám s průměrným věkem 57 let. Průměrný čas mezi vznikem prvních příznaků aiCMP a i.v. podáním rt-PA představoval 107 minut a průměrný čas od příjmu pacienta na emergentní ambulanci po zahájení i.v. rt-PA byl 65 minut. Ve 2 případech se vstupní hypertenzí bylo pozorováno klinicky nezávažné drobné intracerebrální krvácení. V jednom případě došlo s odstupem 50 hodin po úspěšné trombolýze k recidivě aiCMP. Periprocedurálně nebyla pozorována žádná z fatálních komplikací. V retrospektivně hodnoceném mikrosouboru 8 pacientů jsme u všech zaznamenali časné zlepšení celkového stavu, hodnocené jako pokles klinického neurologického deficitu minimálně o 4 body dle škály NIHSS v prvních 24 hodinách po trombolýze. Efekt trombolytické terapie je evidentní i v obraze ADL (Activity of Daily Living) skórování po 90 dnech od vzniku iktu.
Klíčová slova:
rekombinantní tkáňový aktivátor plazminogenu, rt-PA, terapie akutního ischemického iktuÚvod
1. ledna 2006 uplynul právě rok, co v České republice vstoupilo do platnosti Závazné odborné stanovisko ČLK č. 4/2004 [2], podle kterého se v indikovaných případech v rámci kauzální terapie aiCMP u dospělých, v terapeutickém intervalu do 3 hodin od začátku symptomů, doporučuje použití intravenózní (i.v.) trombolytické léčby rekombinantním aktivátorem tkáňového plazminogenu (rt-PA). Efektivita této léčby byla prokázána podle principů medicíny založené na důkazech, randomizovanými placebem-kontrolovanými studiemi [3-5] a metaanalýzami [1,6]. Primárním cílem této práce bylo zjistit: a) jaké jsou časové parametry současného diagnostického postupu v lokálních podmínkách, b) zda-li existují časové rezervy pro redukci stávajícího diagnostického intervalu, c) retrospektivně zhodnotit průběh a eventuální rizika trombolytické terapie, kvantifikovat konečný klinický výsledek a s odstupem tak posoudit její efektivitu v mikrosouboru 8 pacientů.
Soubor a metodika
V období ledna 2005 až května 2006 bylo na neurologickém oddělení Městské nemocnice v Litoměřicích léčeno 203 pacientů s aiCMP. Jen 8 z nich (3,9 %) splňovalo indikační kritéria pro trombolytickou terapii rt-PA [2]. S cílem zkrátit čas od příjmu do podání rt-PA bylo sledováno několik parametrů. Především to byl čas mezi vznikem symptomů, dopravením pacienta do nemocnice a podáním rt-PA. V rámci hospitalizace se hodnotil tzv. investigační čas (doba nutná k provedení všech laboratorních a pomocných zobrazovacích vyšetření dle indikačního protokolu a eventuelně dalších vyšetření v rámci diferenciální diagnostiky). U všech pacientů byl při příjmu zhodnocen klinický neurostatus dle iktové škály NIHSS [7], s kontrolou NIHSS těsně před podáním rt-PA - (k posouzení eventuální regrese neurologického deficitu), které bylo opakováno s odstupem 1, 2, 3, 6 a 24 hodin a dále 7 dní po trombolýze (tab.1). Terapii rt-PA předcházelo CT vyšetření mozku, hodnocené lékařem-radiologem, které bylo podle klinického stavu opakované s odstupem 24 nebo 48 hodin. Od všech pacientů, nebo od jejich příbuzných, byl získán informovaný souhlas s trombolytickou léčbou. Intravenózně byla lege artis podána altepláza (Actylise®, Boehringer-Ingelheim International, Ingelheim nad Rýnem, Německo) v dávce 0,9 mg/kg hmotnosti pacienta. U všech pacientů byla tato terapie aplikována na kardiovaskulární jednotce intenzivní péče (KVJIP), kde byli následných 72 hodin kontinuálně monitorováni. Po dobu 24 hodin po ukončení trombolýzy nebyl podáván heparin, warfarin ani kyselina acetylsalicylová (ASA). U všech pacientů bylo provedeno transtorakální a transezofageální echokardiografické vyšetření. S odstupem bylo u pacientů, kteří souhlasili s genetickým vyšetřením, provedeno vyšetření vzorku krve na eventuální přítomnost některé z mutací koagulačních faktorů (faktor II, faktor V. - Leidenská mutace).
Table 1. Přehled jednotlivých časových parametrů a klinického stavu u pacientů léčených rt-PA. 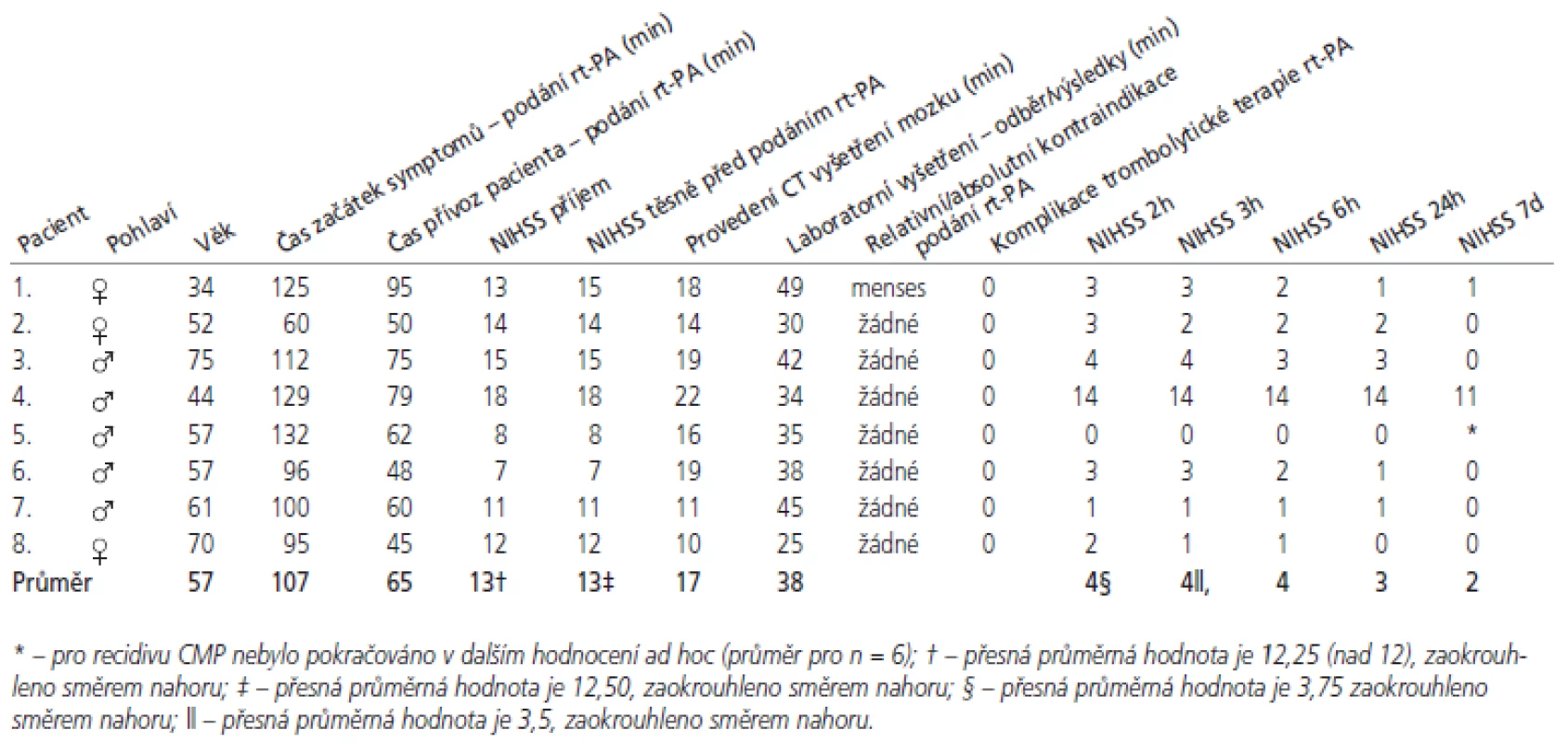
Výsledky
Celková i.v. rt-PA byla po splnění všech kritérií indikována u 5 mužů a 3 žen s průměrným věkem 57 let. Průměrný čas mezi vznikem prvních příznaků CMP a i.v. podáním rt-PA představoval 107 minut a mezi příjmem pacienta na emergentní ambulanci po zahájení i.v. rt-PA 65 minut. U všech 8 pacientů bylo pozorováno již časné zlepšení klinického stavu. Další benefit trombolytické léčby jsme pozorovali u 7 pacientů (tab. 2). V jednom případě byl pacient z dalšího hodnocení vyřazen pro recidivu aiCMP, která vznikla po 50 hodinách od ukončení trombolytické terapie, a to navzdory sekundární antiagregační (ASA v denní dávce 100 mg p.o) terapii, která byla zahájena s odstupem 24 hodin po ukončení trombolýzy. V celém mikrosouboru nebyla pozorována žádná z fatálních nebo kritických komplikací i.v. terapie rt-PA. U jedné z pacientek vznikla aiCMP 3. den menses – tento anamnestický údaj byl hodnocen jako relativní kontraindikace podání rt-PA [8] a samotná aplikace rt-PA i následné období proběhlo zcela bez komplikací. Průměrná hodnota NIHSS skóre v průběhu 3 hodin po podání představovala redukci ze 13 (v intervalu 7–18, n = 8) na 4 body (v intervalu 1–14, n = 8), a až na hodnotu 2 bodů po 90 dnech od iktální příhody (v intervalu 0–7, n = 7). Výsledný efekt trombolytické terapie je evidentní i v obraze ADL (Activity of Daily Living) skórování s odstupem 90 dnů od vzniku iktu (tab.2) [9-11].
Table 2. Efektivita systémové trombolytické terapie rt-PA vyjádřena formou N- a ADL-skóre. 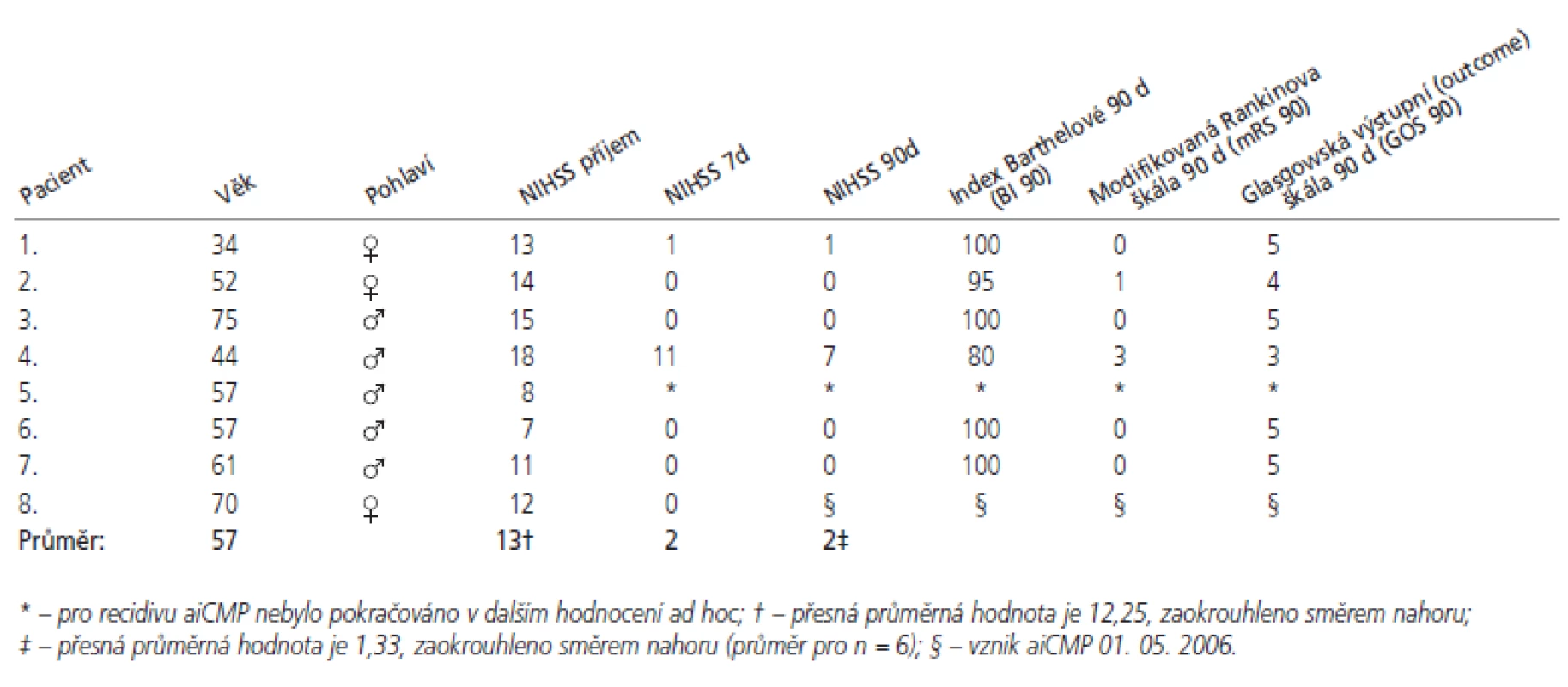
Diskuse
U 4, tedy poloviny referovaných pacientů, se délka investigačního času pohybovala na hranici nebo dokonce pod hodnotou 60 minut, ovšem průměrný interval 65 minut je stále příliš dlouhý (tab. 1). Proto byl lékaři KVJIP a neurologického oddělení vypracován vnitřní postup, který má pro pacienta s aiCMP do budoucna koordinovat činnost zdravotnického personálu. Optimální diagnostický management od příjmu pacienta po zahájení i.v. trombolýzy nesmí přesahovat dobu 60 minut, laboratorní výsledky musí být k dispozici do 45 minut od ordinace lékařem [12,13]. Ani u jednoho z našich pacientů se nevyskytlo symptomatické intrakraniální či systémové krvácení. V rámci diferenciální diagnózy dle anamnézy (akutní vznik s lancinující cefaleou parieto-okcipitálně vlevo, nikotinizmus a p.o. antikoncepce), ale i vzhledem k další progresi neurologického postižení (ze stadia centrální monoparézy s deficitem laterálního zorného pole na pravém oku do centrální hemiparézy s homonymní hemianopsií), bylo u mladé pacientky (I) nutné lumbální punkcí vyloučit možnost subarachnoidálního krvácení (SAK), a to i navzdory negativnímu CT vyšetření, které může být v prvních 24 hodinách pro 2-5 % SAK neprůkazné [14].Po vyšetření krevní skupiny pacientky byly pro možnost vzniku eventuálního krvácení zabezpečeny konzervy plné krve a náplav trombocytů.Kontrola eventuálních krvácivých komplikací byla v tomto případě zintenzivněna na 5minutové intervaly, s kontinuální kontrolou vitálních funkcí. Dle doporučení American Brain Attack Coalition (ABAC), pro případ hemoragické intracerebrální komplikace, musí být neurochirurgická léčba pro pacienty postižených aiCMP distančně i časově dostupná do dvou hodin [12,15]. V případě našich pacientů tato vzdálenost představuje 23 km a čas 17 minut vozidlem RZP a 8 minut vrtulníkem LZS. U 2 pacientů (VI,VII) se při kontrolním vyšetření mozku v CT obraze nenašly žádné postischemické známky proběhlé aiCMP. Ve 3 případech se při kontrole s odstupem 24-48 hodin po trombolytické terapii prezentovaly drobné infarzace - v případě mladé pacientky klinicky manifestovaná formou reziduální homonymní hemianopsie (I), u 2 starších pacientů bez neurologického deficitu (III,VIII). Ve 3 případech byly přítomny infarkty většího rozsahu (II,IV,V), z toho u 2 pacientů s nálezem drobného prokrvácení – v 1 případě bez jakéhokoliv neurologického deficitu (II), v druhém případě se jednalo o výše uvedenou recidivu CMP s progresí symptomatologie (V). Nutno zdůraznit, že u obou těchto pacientů byly před zahájením trombolýzy farmakologicky korigovány hodnoty TK. V souvislosti s pozdějším krvácením dominují určité radiodiagnostické či klinické nálezy, společné nebo častější právě u pacientů léčených i.v. rt-PA [15]. Některé z nich jsou považovány přímo za indikátory horšího klinického výsledku trombolytické terapie (obr.1) [15,16]. Již zmíněný nález drobných či větších ischemií v kontrolním CT obraze 5 pacientů je pravděpodobně výsledkem spolupůsobení několika faktorů – a to zejména podání rt-PA v průběhu 91.-180. minuty od vzniku symptomů, iniciální hypertenze (u 2 pacientů) a rozdílné vulnerability, nebo naopak rezistence jednotlivých oblastí mozkové tkáně ve vztahu k trvání hypoxie. V případě pacienta (IV), který byl postižen aiCMP záhy po probuzení (obr. 1, 2), nepřinesla trombolýza očekávaný efekt (obr.2). Ex post, pro tento případ spornou zůstává právě opodstatněnost časové indikace trombolytické terapie. Především proto, že dříve zcela jednoznačné časové údaje prezentované svědky aiCMP (navzdory velice exaktní příjmové anamnéze!), byly jimi samotnými s odstupem několika dnů postupně korigovány. Poučeni tímto případem, preferujeme názor, že k aiCMP, jejíž symptomatologie se objevila v horizontu několika minut po probuzení, je nutno přistupovat jako k iktální příhodě vzniklé ve spánku. A tudíž za validní časový údaj nutno považovat dobu před usnutím, kdy byl pacient naposled viděn svým okolím bez jakékoliv klinické symptomatologie. I u tohoto pacienta bylo pozorováno zlepšení klinického stavu i částečná regrese CT nálezu (obr.3), genetickým vyšetřením byla u něj prokázaná heterozygotní forma mutace MTHFR C667T.
Image 1. Obraz hyperdenzní a. cerebri media vpravo (šipka) – vstupní CT obraz u pacienta IV. 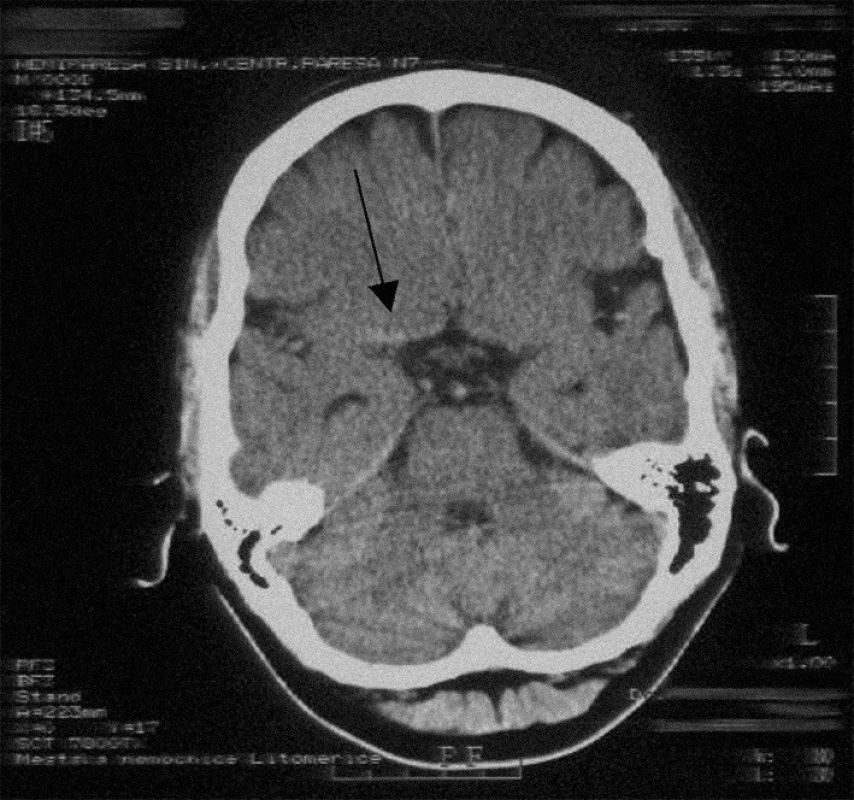
Image 2. Nález rozsáhlého hypodenzního ložiska v oblasti ACM l. dx. (provedeno s odstupem 24 hodin, pacient IV). 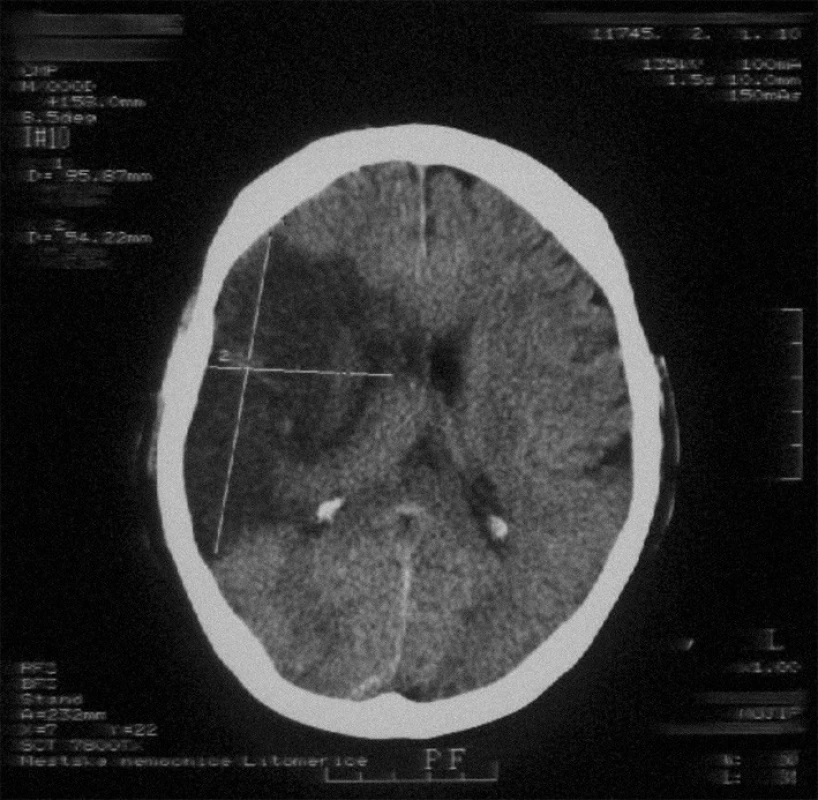
Image 3. Regrese původního rozsahu postižení v oblasti ACM vpravo (provedeno s odstupem 21 dnů, pacient IV). 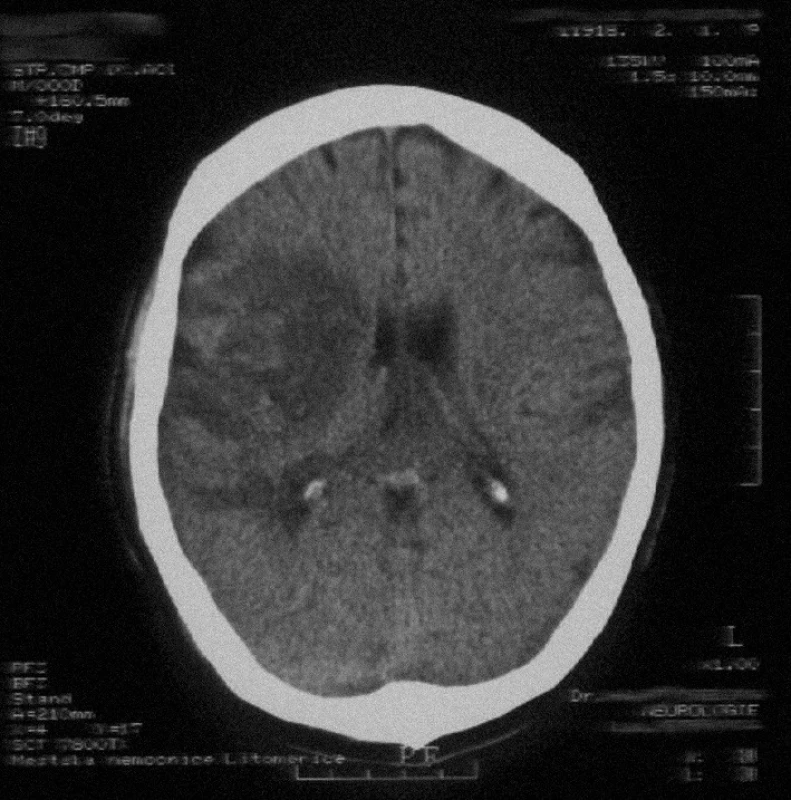
Závěr
I po schválení trombolytické terapie jako léčby první volby u ischemické CMP, většina indikovaných pacientů nemůže být takto léčena, a to především z důvodu časové prodlevy za interval terapeutického okna. Z našich dosavadních výsledků z praxe možno prezentovat, že podání trombolytické terapie na lůžku JIP, vybavené pro OD intenzivní péče 00055 [13] za předpokladu striktního splnění všech indikačních kritérií, je uskutečnitelné a bezpečné v podmínkách nemocnice se zkušenostmi v dosud standardní terapii aiCMP. Mnoho pacientů s časnými příznaky ischemického iktu vyhledá první dostupné nemocniční zařízení. Každé další převážení pacienta jenom zkracuje terapeutické časové okno, ve kterém je možno obnovit funkčnost postižené části mozku a zvrátit rozsah neurologického postižení. Některé klinické práce potvrzují, že nebylo pozorováno žádné zvýšené riziko krvácení ani ve skupině pacientů, u kterých byla trombolytická terapie zahájena, nebo zcela dokončena na oddělení emergentního příjmu, a to ještě před transferem pacienta na JIP - za předpokladu odborného lékařského dohledu a monitorace vitálních funkcí. A to i v případě, že dané nemocniční zařízení nedisponovalo přímo specializovanou jednotkou neuro-intenzivní péče [17]. Zdokonalení přednemocniční péče a koordinace nezbytného vyšetřovacího managementu mohou ještě více napomoci vylepšit definitivní výsledek této terapie.
MUDr. Jozef Pribula
Neurologické oddělení
Městská nemocnice
Žitenická 18
412 01 Litoměřice 1
e-mail: j.pribula@volny.cz
Přijato k recenzi: 10. 4. 2006
Přijato do tisku: 27. 6. 2006
Sources
1. Hacke W, Kaste M, Fieschi C et al. Randomised double-blind placebo controlled trial of trombolytic therapy with intravenous alteplase in acute ischemic stroke (ECAS II). Second European-Australasian Acute Stroke Study Investigators. Lancet 1998; 352 : 1245-51.
2. Česká lékařská komora. Závazné odborné stanovisko č.4/2004. Léčba akutní fáze mozkového infarktu. Tempus medicorum 2004; 12 : 4.
3. Hacke W, Kaste M, Fieschi C et al. Intravenous trombolysis with recombinant tissue plasminogen activator for acute hemispheric stroke (ECASS I). JAMA 1995; 274 : 1017-25.
4. Clark WM, Wissmann S, Albers GW et al. Recombinant tissue plasminogen activator (alteplase) for ischemic stroke 3-5 hours after symptom onset: the ATLANTIS Study: a randomised controlled trial: Alteplase Thrombolysis for Acute Noninterventional Therapy in Ischemic Stroke. JAMA 1999; 282 : 2019-26.
5. Alberts GW, Clark WM, Madden KP et al. ATLANTIS trial: results for patient treated within 3 hours of stroke onset. Alteplase Thrombolysis for Acute Noniterventional Therapy in Ischemic Stroke. Stroke 2002; 33 : 493-6.
6. Hacke W, Brott T, Caplan L et al. Thrombolysis in acute ischemic stroke. Controlled trials and clinical experience. Neurology 1999; 53(7, Suppl 4): S3-14.
7. Spitzer K, Smutzhard E. Documentation and Scores. In: Hacke W (ed). Neurocritical Care. Berlin: Springer-Verlag 1994 : 47-56.
8. Mikulík R, Dufek M. Trombolytická léčba mozkového infarktu – prospektivní sledování souboru pacientů. Čes a Slov Neurol Neurochir 2002; 65/98 : 328-33.
9. Sulter G, Steen Ch, De Keyser J. Use of the Barthel Index and Modifiesd Rankin Scale in Acute Stroke Trials. Stroke 1999; 30 : 1538-41.
10. van Swieten JC, Koudstaal PJ, Visser MCet al. Interobserver agreement for the Assesment of handicap in stroke patients. Stroke 1988; 19 : 604-7.
11. Collin C, Wade DT, Davies S et al. The Barthel ADL index: a reliability study. Int Disability Study 1988; 10 : 61-3.
12. Albert MJ, Hademenos G, Latchaw RF et al for the Brain Atack Coalition. Recommendations for the Establishment of Primary Stroke Centers. JAMA 2000; 283 : 3102-9.
13. Pracovní skupina Cerebrovaskulární sekce České neurologické společnosti ČLS JEP. Standard pro podání systémové trombolýzy pacientům s akutním mozkovým infarktem. Čes a Slov Neurol Neurochir 2006; 69/102 : 151-6.
14. Kalina M. Akutní neurologie. Praha: Triton 2000.
15. Cort MA, Kuo D. Ischemic Stroke Syndromes: The Challenges of Assessment, Prevention and Treatment. Part II: Physical Examination, Laboratory Investigation, Imaging, and Treatment. Emerg Med Rep 2004; 25/6 : 69-79.
16. Derex L, Hermier M, Adeleine P, Pialat JB, Wiart M, Berthezène Y et al. Clinical and imaging predictors of intracerebral haemorrhage in stroke patients treated with intravenous tissue plasminogen activator. J Neurol Neurosurg Psychiat 2005; 76 : 70-75.
17. Wiegand N, Lűthy R, Vogel B, Straumann E, Beynon Ch, Bertel O et al. Intravenous thrombolysis for ischaemic stroke is also safe and efficient without a specialised neuro-intensive care unit. Swiss Med Wkly 2004; 134 : 14-17.
Labels
Paediatric neurology Neurosurgery Neurology
Article was published inCzech and Slovak Neurology and Neurosurgery

2007 Issue 1-
All articles in this issue
- Diagnostika a léčba karcinózy mening u solidních nádorů
- Tau protein a beta amyloid v likvoru u Alzheimerovy choroby a normy odvozené od kognitivně zdravých kontrol
- Intravenózní trombolytická terapie rekombinantním tkáňovým aktivátorem plazminogenu rt-PA (Actilyse®) – naše první zkušenosti z praxe
- Využití stanovení klusterinu v séru a likvoru v diagnostice postižení CNS – pilotní studie
- Vliv oboustranného zúžení vnitřní krkavice na cerebrovaskulární rezervní kapacitu zadního mozkového povodí
- Huntingtonova nemoc: zkušenosti s genetickým testováním v letech 1994-2005
- Vyšetření vizuálních evokovaných potenciálů a sonografické vyhodnocení orbitální hemodynamiky u akutní unilaterální optické neuritidy
- Neuroendoskopie a matematický model dynamiky mozkových komor
- Syndrom kývavé panenky u supraselárních cyst: výsledky neuroendoskopické léčby u čtyř dětí
- Krvácení do glioblastomu při dopravní nehodě
- Panická porucha – Neuropsychiatrický profil
- Chirurgická léčba metastatického postižení krční páteře
- Kognitivní deficit po léčbě intrakraniálních aneuryzmat
- Využití transkraniálního doppleru k průkazu intrakraniální hypertenze u dětí se skafocefalií
- Prediktivní hodnota ultrasenzitivního C-reaktivního proteinu u cévní mozkové příhody a jeho vztah k ateroskleróze karotid
- Czech and Slovak Neurology and Neurosurgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Panická porucha – Neuropsychiatrický profil
- Tau protein a beta amyloid v likvoru u Alzheimerovy choroby a normy odvozené od kognitivně zdravých kontrol
- Diagnostika a léčba karcinózy mening u solidních nádorů
- Chirurgická léčba metastatického postižení krční páteře
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

