-
Medical journals
- Career
Skvamocelulárny karcinóm hrubého čreva – kazuistika
Authors: MUDr. Jurišová Silvia 1; MUDr. Angelis De Valentína 1; MUDr. Makovník Marek 2; MUDr. Hlavčák Peter 3; MUDr. Janega Pavol 4; MUDr. Macák Dušan 5; MUDr. Chovanec Michal 1; MUDr. Rejleková Katarína, PhD. 1; doc. MUDr. PhD. Ák Pin Daniel 6; doc. MUDr. Mardiak Jozef, CSc. 1; prof. MUDr. Mego Michal, PhD. 1
Authors‘ workplace: II. onkologická klinika LF UK a NOÚ, Bratislava, Slovenská republika 1; Rádiologické oddelenie, NOÚ, Bratislava, Slovenská republika 2; Histopatologia, a. s., Bratislava, Slovenská republika 3; Ústav patologickej anatómie, LF UK, Bratislava, Slovenská republika 4; Oddelenie patologickej anatómie, NOÚ, Bratislava, Slovenská republika 5; Klinika chirurgickej onkológie SZU a NOÚ, Bratislava, Slovenská republika 6
Published in: Klin Onkol 2020; 33(5): 380-384
Category: Case Report
doi: https://doi.org/10.14735/amko2020380Overview
Východiská: Primárne skvamocelulárne karcinómy (SCC) hrubého čreva sú extrémne zriedkavé a vyskytujú sa prevažne v piatej dekáde života, s miernou prevahou u mužov. Najčastejšími anatomickými miestami výskytu sú konečník a proximálne hrubé črevo. Klinické znaky a bežné diagnostické metódy nedokážu úplne jednoznačne odlíšiť SCC od adenokarcinómu.
Metódy: V tejto kazuistike prezentujeme prípad 68-ročného pacienta s SCC céka a colon ascendens, ktorý bol liečený resekciou a systémovou liečbou na báze gemcitabínu a cisplatiny.
Prípad: Pacient vo veku 68 rokov podstúpil pravostrannú hemikolektómiu pre karcinóm céka a colon ascendens, histologicky išlo o nízko diferencovaný epidermoidný karcinóm, grade 3 s iniciálnym štádiom pT4aN1aM0. Pre lokálnu recidívu v mieste resekcie so suspektnou infiltráciou priamych a šikmých brušných svalov bol liečený systémovou liečbou na báze gemcitabínu a cisplatiny s dosiahnutím parciálnej remisie. Následne bolo postchemoterapeutické reziduum radikálne odstránené, s dosiahnutím kompletnej remisie ochorenia, ktorá pretrváva 10 mesiacov od operačného výkonu.
Záver: Prípad zdôrazňuje potrebu multidisciplinárneho prístupu v liečbe tohto raritného ochorenia. Včasný chirurgický výkon zohráva kľúčovú úlohu. Aj keď štandardný chemoterapeutický režim nie je presne definovaný, použitie kombinácie cisplatiny a gemcitabínu viedlo u nášho pacienta k parciálnej remisii, ktorá následne umožnila radikálnu resekciu recidívy a následne dosiahnutie kompletnej remisie ochorenia.
Klíčová slova:
skvamocelulárny karcinóm – kolorektálny – systémová liečba
Úvod
Kolorektálny karcinóm (CRC) je treťou najčastejšou malignitou u mužov a druhou najčastejšou u žien. Ročne je celosvetovo diagnostikovaných 1,8 mil. nových prípadov. Podľa údajov Svetovej zdravotníckej organizácie v roku 2018 zomrelo na diagnózu CRC 861 000 pacientov [1].
Skvamocelulárny (SCC) karcinóm predstavuje minoritnú časť nádorov čreva. V literatúre je opísaných menej ako 100 prípadov [2]. Kvôli svojim klinicko-patologickým vlastnostiam je tento typ nádoru v porovnaní s adenokarcinómom agresívnejší, má horšiu prognózu a vyžaduje agresívnejší liečebný prístup. Použitím modifikovaných Dukesových kritérií pre štádium kolorektálneho karcinómu, aplikovateľných prevažne pre adenokarcinómy je 5-ročné prežívanie v štádiu B 56 %, v štádiu C 15 % a v štádiu D 5 % [6,7]. V dôsledku zriedkavého výskytu SCC hrubého čreva ostávajú klinické prejavy, liečba a prognóza zle definované.
V tejto kazuistike prezentujeme prípad 68-ročného pacienta s SCC céka a colon ascendens, ktorý bol liečený resekciou a systémovou liečbou na báze gemcitabínu a cisplatiny.
Prípad
Pacient vo veku 68 rokov podstúpil v auguste 2018 pravostrannú hemikolektómiu pre karcinóm céka a colon ascendens pT4aN1aM0; z 19 vyšetrených regionálnych lymfatických uzlín (LU) bola jedna postihnutá metastázou. Histologicky sa jednalo o extenzívny nízko diferencovaný epidermoidný karcinóm, grade 3 (obr. 1), so zachovanou reaktivitou tzv. mismatch repair (MMR) proteínov a neprítomnosťou expresie tyroidného transkripčného faktoru 1 (TTF-1), kinázou anaplastického lymfomu (ALK) a ROS proteínu, zatiaľ čo expresia ligandu membránového proteínu programovanej bunkovej smrti 1 (programmed-death ligand 1 – PD-L1) bola 50 %.
Image 1. Histologicky sa preukázal nízko diferencovaný epidermoidný karcinóm (A, B), grade 3. Nádor vykazoval imunoprofi l: antibody AE 1/3 + (C) , vimentín slabo + (D), cytokeratín CK 7 – (E) , CK 20 + (F), CDX2 – (G), proliferačný index Ki67 + 90 % (H), HE, IHC- -Px, 200x. 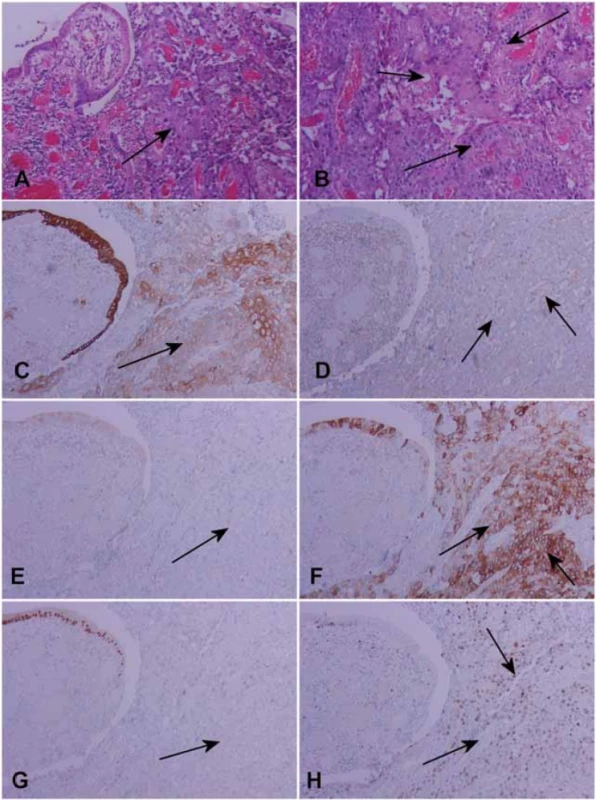
Pooperačné vyšetrenie počítačovou tomografiou (CT) v septembri 2018 zobrazilo v oblasti pravého hypogastria laterokaudálne pod oblasťou anastomózy laločnaté ložisko veľkosti 48 × 27 × 44 mm (obr. 2A). Ložisko v kraniálnej časti naliehalo na založený klip, stav bol hodnotený ako lokálna recidíva v mieste resekcie. Bola prítomná suspektná infiltrácia priamych a šikmých brušných svalov. Kaudálne od neho parailicky boli prítomné pruhovité štruktúry veľkosti do 22 × 5 mm, možné reaktívne LU, príp. ložiská karcinomatózy. Podobné štruktúry (do 15 × 8 mm) boli popísané aj ventrálne od a. iliaca communis. V septembri 2019 bola zahájená systémová liečba v schéme gemcitabín a cisplatina. Gemcitabín bol podávaný v dávke 1 000 mg/m² v deň 1 a deň 8, cisplatina v dávke 70 mg/m² v deň 1. V čase zahájenia systémovej liečby pacient nemal žiadne klinické ťažkosti, v laboratórnych parametroch bola zaznamenaná mierne zvýšená aktivita obštrukčných hepatálnych enzýmov, onkomarkery CEA a Ca 19.9 boli v norme. Pacient podstúpil 6 cyklov uvedenej liečby v 100% dávkach, bez nutnosti redukcie ako i príznakov závažnej toxicity. CT vyšetrenie po skončení liečby ukázalo efekt parciálnej remisie (obr. 2B). Pred plánovaným chirurgickým výkonom bolo realizované vyšetrenie pozitrónovou emisnou tomografiou (PET/CT) s nálezom hypermetabolického ložiska v pravom hypogastriu medzi kľučkou ilea a brušnou stenou. V apríli 2019 podstúpil laparotómiu, počas ktorej bolo kompletne resekované ložisko v oblasti ilea veľkosti do 3 cm. K ložisku bol fixovaný aj koniec slepej kľučky ilea, bola realizovaná ileotransverzoanastomóza „side-to-side“. Histologicky nález potvrdil recidívu nerohovatejúceho SCC s parciálnou exulceráciou sliznice tenkého čreva. V okolí, v mäkkom tkanive boli prítomné obrovskobunkové granulomatózne reparatívne zmeny. Resekčné okraje boli voľné. Následne bol pacient zaradený do sledovania, u pacienta pretrváva remisia 10 mesiacov od operačného výkonu.
Image 2. A. Laločnaté, postkontrastne sa sýtiace ložisko. 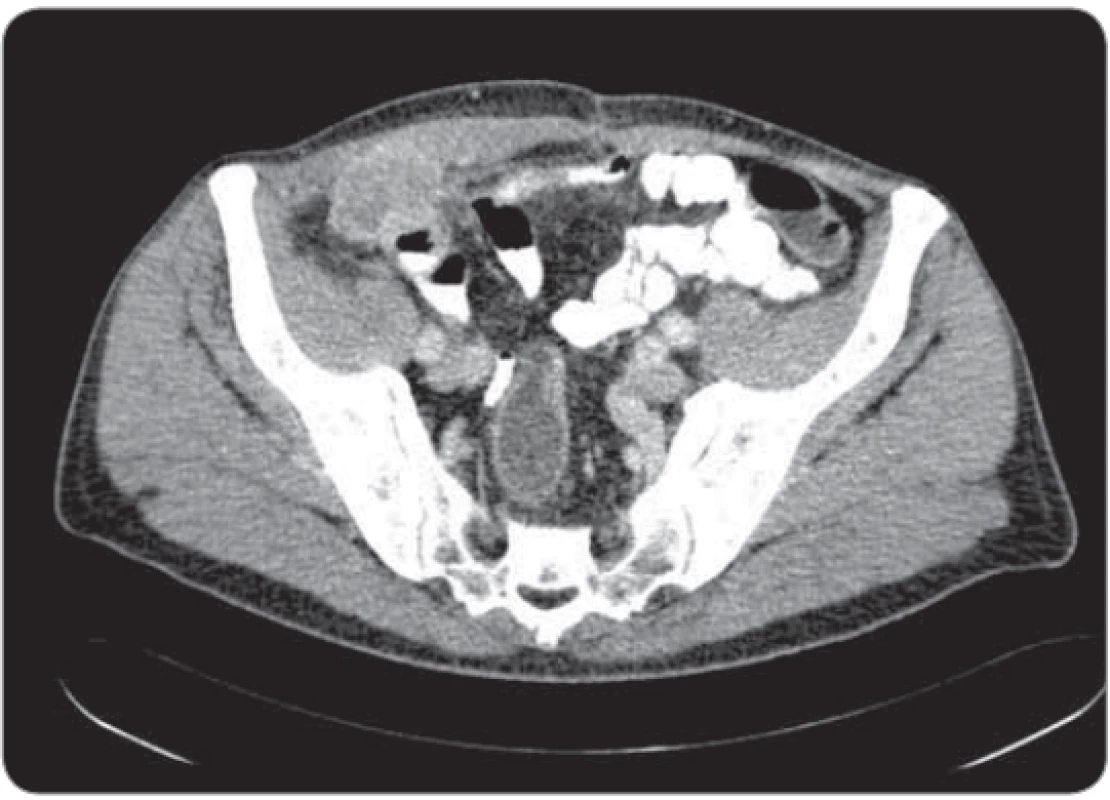
Obr. 2B. Efekt parciálnej remisie zobrazujúcej sa ako hypodenzné reziduum v blízkosti klipu. 
Diskusia
SCC sa môžu vyskytnúť v oblasti celého kolorekta, avšak najčastejším miestom výskytu je rektum (93,4 %), nasleduje pravé kolon (3,4 %) [2]. SCC čreva je extrémne nezvyčajný a na rozdiel od SCC pažeráka či análneho kanála sa vie iba málo o jeho etiológii, prognóze a optimálnej liečbe. Vyskytuje sa medzi 53.–60. rokom života, častejšieu mužov [4]. Rizikové faktory, ktoré súvisia so vznikom SCC kolorekta, nie sú presne identifikované. Najsilnejšie spojenie, ktoré sa v literatúre popisuje, je asociácia s proktitídou, zvyčajne sekundárne, po ulceróznej kolitíde [2,3,5]. Boli popísané aj prípady, kedy ochorenie vzniklo v teréne aktívnej Crohnovej choroby rekta a v prípade chronického prolapsu. V niektorých prípadoch bola aj predchádzajúca aplikácia rádioterapie na oblasť malej panvy. V dôsledku silnej asociácie medzi infekciou human papilloma vírusom (HPV) a vznikom SCC análneho kanála, sa niekoľko klinických štúdií zapodievalo úlohou HPV infekcie v rektálnom SCC [8–10]. Vzhľadom na obmedzené dôkazy nie je infekcia HPV jednoznačne potvrdená ako rizikový faktor pre vznik SCC [11,12]. Predpokladá sa, že je asociovaný s chronickým zápalom a infekciou. Občas môže byť ich vznik spojený s fistulou gastrointestinálneho traktu, lemovanou skvamóznou sliznicou.
Patogenéza SCC nie je dobre známa. Predpokladá sa, že pluripotentné kmeňové bunky s viacsmernou diferenciáciou sa vyvinú na SCC po poškodení slizníc. Ďalšia teória zdôrazňuje, že neutrálne bazálne bunky majú potenciál pre skvamóznu diferenciáciu po poškodení epitelu. Predpokladá sa, že infekcia HPV, ktorá sa spája s SCC pažeráka, môže súvisieť aj s patogenézou SCC hrubého čreva.
V dôsledku nízkej incidencie tohto ochorenia nie je optimálna liečba presne stanovená. Vo všeobecnosti môžeme povedať, že vychádza z liečby adenokarcinómov. Dominantné postavenie má chirurgický výkon s chemoterapiou a rádioterapiou. Optimálna kombinácia liečby a harmonogram chemorádioterapie pri lokálnom, ako aj metastatickom ochorení nie je známy. Účinnosť preukázali viaceré chemoterapeutiká ako 5 - fluorouracil (5-FU), mitomicín C, kapecitabín, cisplatina a oxalipaltina. Aj keď niekoľko prípadov naznačuje, že popri chirurgickom zákroku môže mať vo väčšine prípadov pozitívnu úlohu chemoterapia, v dôsledku zriedkavosti tohto ochorenia chýba dostatok údajov.
Najdôležitejším prognostickým faktorom je štádium ochorenia [13,14]. Copur et al preukázali priaznivú odpoveď na kombináciu paliatívnej chemoterapie s 5-FU, cisplatinou a etopozidem v pokročilom štádiu ochorenia [13]. Juturi et al použili kombináciu 5-FU, cisplatiny a kalcium leukovorínu ako kombinovanú liečbu v metastatickom štádiu SCC hrubého čreva [8]. V oboch prípadoch pacienti dostávali 6 cyklov kombinovanej liečby. V roku 2017 Abdelhai et al publikovali dva prípady SCC v oblasti colon ascendens. V prvom prípade sa jednalo o 27-ročnú pacientku s lokálnym ochorením. Tri a pol roka po chirurgickom výkone je v kompletnej remisii, bez aplikácie chemoterapie alebo rádioterapie. V druhom prípade 44-ročný muž, diagnostikovaný v IV. klinickom štádiu zomrel 6 mesiacov od stanovenia diagnózy. Okrem chirurgickej liečby podstúpil liečbu rádioterapiou a chemoterapiu na báze kapecitabínu a paklitaxelu, neskôr oxaliplatiny a 5-FU, všetko s efektom progresie ochorenia. Obidvaja títo pacienti boli mladší ako je uvádzaný priemerný vek 53–60 rokov [15]. Shufen et al v roku 2017 tiež publikovali kazuistiku 58-ročného muža s lokálne pokročilým SCC colon ascendens. V liečbe použili kombinovaný režim na báze gemcitabínu, oxaliplatiny a kapecitabínu. Pacient dosiahol 10-mesačného prežitia bez progresie [16]. V roku 1996 Petrelli et al popísali prípad 5 mužov a 2 žien s adenoskvamóznym kolorektálnym karcinómom. Chemoterapia bola použitá v adjuvantnej intencii alebo u pacientov s lokálnou alebo vzdialenou recidívou. Medián celkového prežívania bol 23 mesiacov. Medzi znaky, ktoré predpovedali zlú prognózu, patrili pravostranné lézie, ulcerované alebo prstencové karcinómy, pozitivita LU, grading 3–4 a metastatické štádium [17].
Záver
Prípad nášho pacienta zdôrazňuje potrebu multidisciplinárneho prístupu v liečbe tohto raritného ochorenia. Včasný chirurgický výkon zohráva kľúčovú úlohu. I keď štandardný chemoterapeutický režim nie je presne definovaný, použitie kombinácie cisplatiny a gemcitabínu viedlo u nášho pacienta k parciálnej remisii, ktorá následne umožnila radikálnu resekciu recidívy a následnú remisiu ochorenia.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
The authors declare they have no potential confl icts of interest concerning drugs, products, or services used in the study.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do bi omedicínských časopisů.
The Editorial Board declares that the manuscript met the ICMJE recommendation for biomedical papers.
prof. MUDr. Michal Mego, PhD.
II. onkologická klinika LF UK a NOÚ
Špitálska 24
813 72 Bratislava
Slovenská republika
e-mail: misomego@gmail.com
Obdŕžané/Submitted: 29. 3. 2020
Prijaté/Accepted: 20. 5. 2020
Sources
1. Bray F, Ferlay J, Soerjomataram I et al. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin 2018; 68 (6): 394–424. doi: 10.3322/caac.21492.
2. Michelassi F, Mishlove LA, Stipa F et al. Squamous-cell carcinoma of the colon. Dis Colon Rectum 1988; 31 (3): 228–235. doi: 10.1007/BF02552552.
3. Miyamoto H, Nishioka M, Kurita N et al. Squamous cell carcinoma of the descending colon: report of a case and literature review. Case Rep Gastroenterol 2007; 1 (1): 77–83. doi: 10.1159/000107470.
4. Copur S, Ledakis P, Novinski D et al. Squamous cell carcinoma of the colon with an elevated serum squamous cell carcinoma antigen responding to combination chemotherapy. Clinical Colorectal Cancer 2001; 1 (1): 55–58. doi: 10. 3816/CCC.2001.n.006.
5. Samo S, Sherid M, Liu K et al. Basaloid squamous cell carcinoma of the sigmoid colon. ACG Case Rep J 2015; 2 (3): 161. doi: 10.14309/crj.2015.41.
6. Machairas A, Tsapralis, Samaras VD et al. Basaloid squamous cell carcinoma of the rectum: a rare entity. J Med Cases 2013; 4 (8): 535–539. doi: 10.4021/jmc1386e.
7. Akkoca AN, Yanık S, ZT Ozdemir et al. TNM and Modified Dukes staging along with the demographic characteristics of patients with colorectal carcinoma. Int J Clin Exp Med 2014; 7 (9): 2828–2835.
8. Juturi JV, Francis B, Koontz PW et al. Squamous-cell carcinoma of the colon responsive to combination chemotherapy. Dis Colon Rectum 1999; 42 (1): 102–109. doi: 10.1007/BF0223519.
9. Frizelle FA, Hobday KS, Batts KP et al. Adenosquamous and squamous carcinoma of the colon and upper rectum. Dis Colon Rectum 2001; 44 (3): 341–346. 10.1007/BF02234730.
10. Dyson T, Draganov PV. Squamous cell cancer of the rectum. World J Gastroenterol 2009; 15 (35): 4380–4386. doi: 10. 3748/wjg.15.4380.
11. Audeau A, Han HW, Johnston MJ et al. Does human papilloma virus have a role in squamous cell carcinoma of the colon and upper rectum? Eur J Surg Oncol (EJSO) 2002; 28 (6): 657–660. doi: 10.1053/ejso.2002.1304.
12. Paquette C, Mills AM, Stoler MH. Predictive value of cytokeratin 7 immunohistochemistry in cervical low-grade squamous intraepithelial lesion as a marker for risk of progression to a high-grade lesion. Am J Surg Pathol 2016; 40 (2): 236–243. doi: 10.1097/PAS.0000000000000548.
13. Copur S, Ledakis P, Novinski D et al. Squamous cell carcinoma of the colon with an elevated serum squamous cell carcinoma antigen responding to combination chemotherapy. Clin Colorectal Cancer 2001; 1 (1): 55–58. doi: 10.3816/CCC.2001.n.006.
14. Rajan R, Baqar A, Menon T. An interesting case of primary squamous cell carcinoma of the colon with synchronous metastatic adenocarcinoma. Clin Case Rep 2014; 2 (6): 323–325. doi: 10.1002/ccr3.127.
15. Abdelqader A, Jabaji R, Albugeaey M et al. Squamous cell carcinoma of ascendenting colon: two cases. J Community Hosp Intern Med Perspect 2017; 7 (1): 53–55. doi: 10.1080/20009666.2017.1309339.
16. Zhao S, Guo J, Sun L et al. Gemcitabin-based chemotherapy in colon squamous cell carcinoma: A case report end literature review. [online]. Available from: https: //www.spandidos-publications.com/10.3892/ mco.2017.1178.
17. Petrelli NJ, Valle AA, Weber TK et al. Adenosquamous carcinoma of the colon and rectum. Dis Colon Rectum 1996; 39 (11): 1265–1268. doi: 10.1007/BF02055120.
Labels
Paediatric clinical oncology Surgery Clinical oncology
Article was published inClinical Oncology

2020 Issue 5-
All articles in this issue
- Současný pohled na možnosti léčby BRAF mutovaného kolorektálního karcinomu
- Dlouhé nekódující RNA a karcinom z renálních buněk
- Výzvy a riešenia v manažmente kardiotoxicity checkpoint inhibítorov
- Systémová liečba hepatocelulárneho karcinómu
- Nové trendy v neoadjuvantní léčbě lokálně pokročilého karcinomu rekta z pohledu chirurga – komentář
- Implementácia imunoterapie do liečby neuroblastómu – skúsenosti jedného centra s podávaním a manažovaním nežiaducich účinkov dinutuximabu
- Skvamocelulárny karcinóm hrubého čreva – kazuistika
- Extravazace (paravazace) cytostatik – aktualizované doporučení (2020) pro standardní péči v rámci České republiky ze spolupráce Sekce podpůrné léčby České onkologické společnosti ČLS JEP, České hematologické společnosti ČLS JEP, Onkologické sekce České asociace sester a Společnosti pro porty a permanentní katétry
- Editorial
- Entrektinib – tumor-agnostická léčba penetrující do centrálního nervového systému s prokázanou účinností i u pediatrické populace
- Aktuality z odborného tisku
- Prvý pacient s COVID-19 na Slovensku
- Clinical Oncology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Nové trendy v neoadjuvantní léčbě lokálně pokročilého karcinomu rekta z pohledu chirurga – komentář
- Současný pohled na možnosti léčby BRAF mutovaného kolorektálního karcinomu
- Extravazace (paravazace) cytostatik – aktualizované doporučení (2020) pro standardní péči v rámci České republiky ze spolupráce Sekce podpůrné léčby České onkologické společnosti ČLS JEP, České hematologické společnosti ČLS JEP, Onkologické sekce České asociace sester a Společnosti pro porty a permanentní katétry
- Systémová liečba hepatocelulárneho karcinómu
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

