-
Medical journals
- Career
Primární intrakraniální sarkomy, myxoidní meningeální sarkom – kazuistika a přehled literatury
Authors: D. Vrána 1; O. Kalita 2; L. Hrabálek 2; M. Matzenauer 1; M. Bartoušková 1; N. Rušarová 1; L. Tučková 3; Lenka Sedláčková 4
Authors‘ workplace: Onkologická klinika LF UP a FN Olomouc 1; Neurochirurgická klinika LF UP a FN Olomouc 2; Ústav klinické a molekulární patologie, LF UP a FN Olomouc 3; Radiologická klinika LF UP a FN Olomouc 4
Published in: Klin Onkol 2019; 32(3): 214-219
Category: Case Report
doi: https://doi.org/10.14735/amko2019214Overview
Východiska: Primární intrakraniální sarkomy představují vzácná onemocnění. S ohledem na chybějící randomizované studie vycházíme v léčebném algoritmu obvykle z extrapolace dat z extrakraniálních variant těchto sarkomů nebo pouze z publikovaných kazuistik, ovšem s vědomím specifik radioterapie v oblasti mozkové tkáně a omezeného průniku cytostatik přes hematoencefalickou bariéru. Základní léčebnou modalitu stále představuje chirurgická resekce, a to jak v případě primárních nádorů, tak event. recidivy. Nicméně vzhledem k intrakraniální lokalizaci nelze obvykle dosáhnout stejné radikality jako v případě extrakraniálních tumorů. Prognóza těchto typů nádorů i přes veškerou snahu zůstává bohužel neuspokojivá.
Případ: V naší kazuistice prezentujeme 69letou pacientku, která byla došetřována pro organický psychosyndrom a parézu levé horní končetiny. Magnetická rezonance prokázala rozsáhlou expanzi mozku frontálně vpravo s kolaterálním edémem. Byla indikována exstirpace tumoru s histologickým nálezem vzácného myxoidního meningeálního sarkomu. Časná recidiva v místě původního tumoru 4 měsíce po primární resekci byla následovaná reresekcí a adjuvantní radioterapií do 50 Gy na oblast lůžka tumoru, stejně jako další recidiva 19 měsíců po předchozí, která již však byla v jiné lokalitě. Systémová léčba zatím nebyla indikována. V současnosti je pacientka bez známek recidivy a pokračuje v observaci.
Závěr: Myxoidní meningeální sarkom představuje onemocnění s vysokým rizikem lokoregionální recidivy, u něhož v tuto chvíli neexistuje jednoznačné doporučení pro léčebný algoritmus.
Klíčová slova:
sarkomy – nádory mozku – radioterapie
Úvod
Jako primární intrakraniální sarkomy můžeme definovat intrakraniální sarkomy bez známek extrakraniálního postižení. Jiné práce tak označují nádory, které nejsou gliálního, neuronálního ani retikulárního původu a současně nejsou známky přítomnosti extrakraniálního sarkomu v době diagnózy [1]. Primární intrakraniální sarkomy představují v porovnání s extrakraniálními sarkomy a sekundárním metastatickým postižením mozku vzácné onemocnění a jsou téměř raritní u dospělých pacientů. I přes relativní vzácnost je však nutno na ně v diferenciální diagnostice intrakraniálních procesů myslet. Nádory mozku vč. intrakraniálních sarkomů jsou klasifikovány na základě doporučení World Health Organization z roku 2016, v němž však vlastní primární mezenchymální nádory představují heterogenní skupinu více než 20 nádorových podtypů. Nová klasifikace z roku 2016 zasáhla i sarkomy mozku, když např. hemangiopericytom a solitární fibrózní tumor jsou nyní klasifikovány jako jedna entita [2]. Histologicky nejčastější jsou v případě dětských nádorů rhabdomyosarkomy a chondrosarkomy, v případě primárních sarkomů dospělého věku je to hemangiopericytom/solitární fibrózní tumor, chondrosarkom, osteosarkom a leiomyosarkom [3–6]. Základní léčebnou modalitu stále představuje chirurgická resekce, a to jak v případě primárních nádorů, tak event. recidivy. Nicméně vzhledem k intrakraniální lokalizaci nelze dosáhnout stejné radikality jako u extrakraniálních nádorů, proto je na místě úvaha o indikaci adjuvantní léčby. Indikace radioterapie (s konvenční frakcionací, stereotaktická, protonová léčba) a systémové léčby je založena obvykle na extrapolaci dat z primárně extrakraniálně lokalizovaných nádorů, ovšem s vědomím specifik radioterapie v oblasti mozkové tkáně a omezeného průniku cytostatik přes hematoencefalickou bariéru. Stále častěji je využívána cílená terapie, kterou je možné s ohledem na efektivitu u extrakraniálních sarkomů využít i v případě sarkomů primárně intrakraniálních. Kawabata et al podávali pazopanib u 76letého pacienta s recidivujícím primárně intrakraniálním leiomyosarkomem s vyčerpanými možnostmi lokoregionální léčby a dosáhli stabilizace onemocnění [7]. Podobně byl pazopanib použitý u pacientů s hemangiopericytomem. Apra et al prezentovali kazuistiky dvou pacientů s meningeálním hemangiopericytomem léčených pazopanibem s parciální odpovědí na léčbu [8]. Cílená léčba je tedy zatím rezervována pro paliativní indikaci, postavení v neoadjuvantní či adjuvantní léčbě není definováno.
I když histologický nález těchto tumorů je různorodý, klinicky se nádory projevují v úvodu velmi podobně, nejčastěji epileptickými záchvaty, bolestmi hlavy či neurologickým deficitem, méně často jsou diagnostikovány jako vedlejší nález při provádění zobrazovacích vyšetření z jiných indikací.
Kazuistika
V naší kazuistice prezentujeme v době diagnózy 69letou pacientku, která byla došetřována pro levostrannou parézu horní končetiny a organický psychosyndrom. Dle vyšetření magnetickou rezonancí (magnetic resonance imaging – MRI) byla prokázána rozsáhlá expanze mozku frontálně vpravo s kolaterálním edémem (obr. 1). Následovala exstirpace tumoru s histologickým nálezem low-či intermediate-grade sarkomu (obr. 2). Doplněné druhé čtení potvrdilo diagnózu neobvyklého low-grade myxoidního meningeálního sarkomu. Histologicky šlo o nepravidelně myxoidně prosáklý vřetenobuněčný tumor, převážně s nízkou až střední buněčností, který imunohistochemicky vykazoval pozitivitu vimentinu, část buněk CD10 a zcela sporadické elementy velmi slabě epiteliální membránový antigen. Jednotlivé buňky byly D2-40 a CD68 pozitivní. Nádorové buňky byly negativní v barvení S100, GFAP, PR, AE1/3, CK20, CK7, CK18, CD138, kappa, lambda, SMA, desmin, caldesmon. Proliferační aktivita Ki67 byla kolem 5 %. Dle kontrolního vyšetření MRI s 4měsíčním odstupem bylo prokázáno progredující reziduum tumoru. Následná rekraniotomie potvrdila nález rezidua tumoru se stejným histologickým nálezem jako v případě primární resekce. U pacientky byla indikována adjuvantní radioterapie lůžka tumoru frontálně vpravo do 50 Gy v 25 frakcích s využitím 6MV lineárního urychlovače.
Image 1. Primární tumor frontálního laloku. 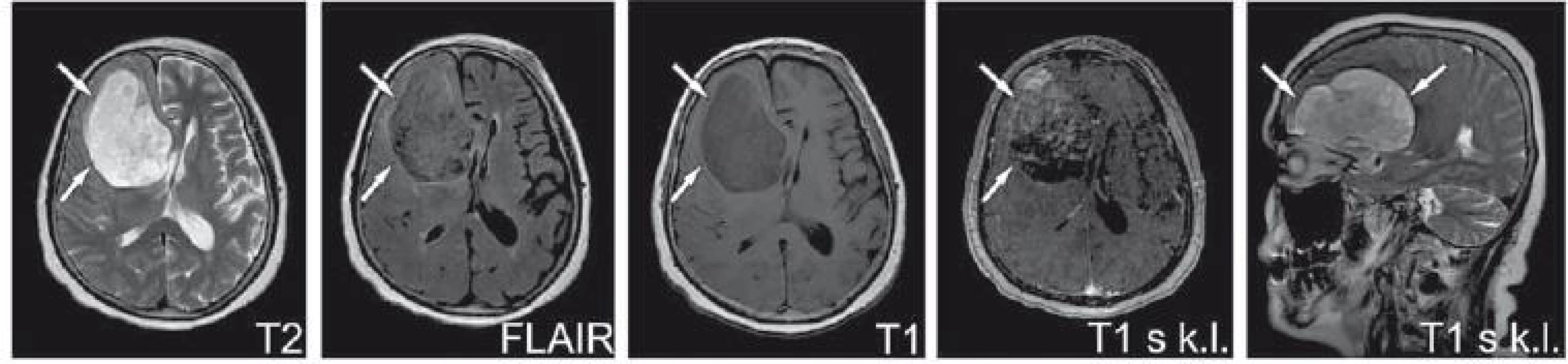
Image 2. Histologický nález primárního tumoru.
A. Průkaz kyselých mukopolysacharidů v tumoru. Alciánová modř, zvětšení 100×.
B. Přehledný snímek tumoru. Hematoxylin-eozin, zvětšení 40×.
C. Buněčnější partie tumoru. Hematoxylin-eozin, zvětšení 100×.
D. Méně buněčná partie tumoru. Hematoxylin-eozin, zvětšení 100×.
E. Okraj tumoru přecházející v nenádorovou mozkovou tkáň. Hematoxylin-eozin, zvětšení 100×.
F. Proliferační aktivita měřená indexem Ki67. Imunohistochemické barvení, zvětšení 100×.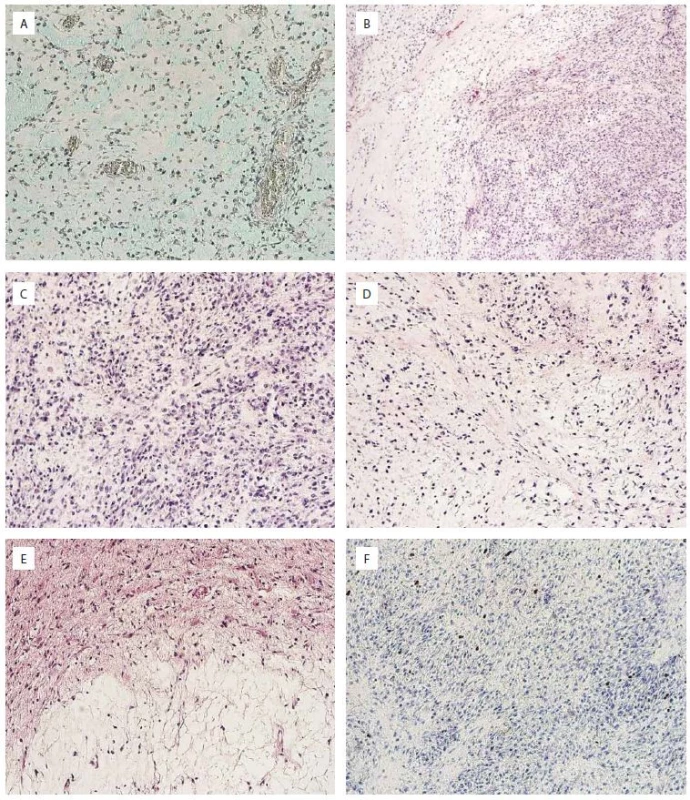
Následovala pečlivá dispenzarizace bez jednoznačných známek recidivy, až do doby 19 měsíců od posledního operačního výkonu, kdy byla v oblasti levé mozečkové hemisféry diagnostikována recidiva podobného charakteru jako primární tumor ve frontálním laloku (obr. 3). Pacientka proto podstoupila rekraniotomii s opětovným nálezem myxoidního meningeálního sarkomu. Následně byla indikována radioterapie lůžka tumoru mozečku do 50 Gy normofrakcionovaně, která proběhla bez větších komplikací. Systémová léčba zatím nebyla indikována, podobně jako v případě resekce primárního tumoru. Pacientka je nyní po radioterapii s reziduální lehkou parézou levé horní končetiny a přetrvávajícím organickým psychosyndromem. Bude pokračovat v observaci s 3měsíčními kontrolami MRI. Přešetření po ukončení radioterapie pozitronovou emisní tomografií / počítačovou tomografií a MRI mozku neprokázalo recidivu/generalizaci onemocnění.
Image 3. Recidiva tumoru v mozečku. 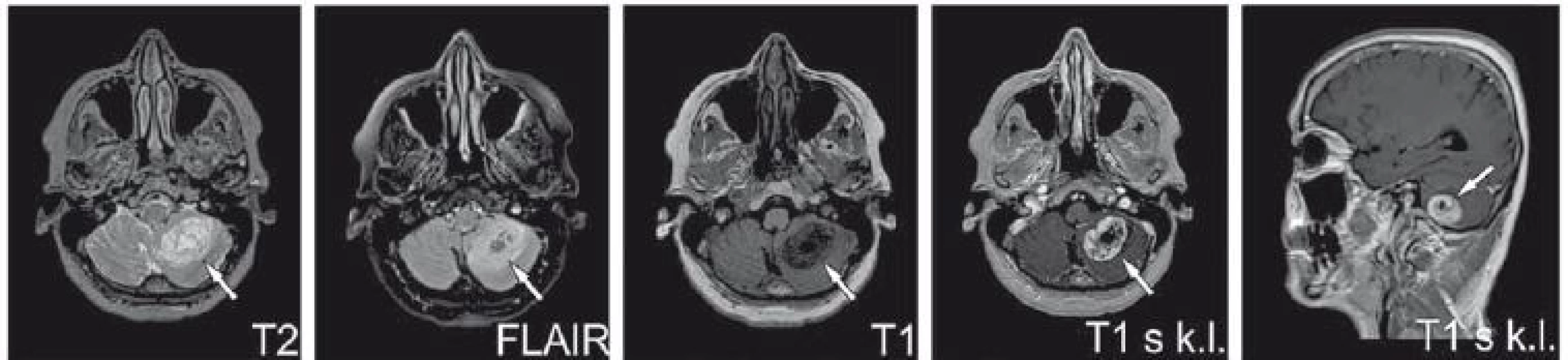
Diskuze
Primární intrakraniální sarkomy představují onemocnění s obecně špatnou prognózou i přes obvykle multimodální léčbu. Z rizikových faktorů pro vznik intrakraniálních nádorů jsou nejčastěji uváděny předchozí radioterapie, imunodeficit a některé hereditární nádorové syndromy (von Recklinghausenova choroba – neurofibromatóza typu I) [9,10]. S ohledem na nedostatek klinických studií vycházíme v léčebném algoritmu většinou z dat z léčby podobných histologických podtypů extrakraniálních sarkomů, event. pouze z publikovaných kazuistik, nicméně jak je uvedeno výše, je nutné zohlednit specifika intrakraniální lokalizace.
Z publikovaných dat (tab. 1) je možné shrnout, že v případě vyloučení generalizace je u synoviálních sarkomů nejčastějším postupem po chirurgické exstirpaci adjuvantní radioterapie do 60 Gy a adjuvantní chemoterapie na bázi ifosfamidu (Patel et al – doxorubicin, ifosfamid, mesna; Wushou et al – cisplatina, epirubicin, ifosfamid) [11,12]. V případě primárního intrakraniálního liposarkomu exstirpace se zvážením adjuvantní radioterapie [13,14]. U leiomyosarkomu byla indikována po resekci obvykle adjuvantní radioterapie do cca 60 Gy normofrakcionací se zvážením adjuvantní chemoterapie (vinkristin, ifosfamid, doxorubicin, etoposid) [7,15–18]. Extenzivní systémová léčba často v rámci specifických klinických studií (v některých případech i v kombinaci s intratekální chemoterapií) spolu s radioterapií celé kraniospinální osy byla indikována obvykle v případě primárních intrakraniálních Ewingových sarkomů, podobně jako v případě intrakraniálního rhabdomyosarkomu [19–22]. Osteosarkomy byly léčeny chirurgickou exstirpací, adjuvantní radioterapií s nebo bez chemoterapie [23–26]. V případě chondrosarkomů byla obvyklým postupem chirurgická exstirpace se zvážením adjuvantní radioterapie, avšak i v tomto případě zůstává riziko recidivy poměrně vysoké [27–29]. Li et al publikovali 37,3 % recidiv při mediánu sledování 47,8 měsíce ve skupině pacientů s primárně intrakraniálními chondrosarkomy [30]. V případě hemangiopericytomů / solitárních fibrózních tumorů je nejčastějším postupem chirurgická resekce a zvážení event. adjuvantní radioterapie, o které však v literatuře existují rozporuplná data [31]. Hemangiopericytomy představují onemocnění s relativně lepší prognózou, jak vyplývá ze systematického přehledu autorů Rutkowski et al, který zahrnoval 563 případů intrakraniálních hemangiopericytomů s mediánem přežití 13 let [32]. Fibrosarkomy představují další typ intrakraniálních sarkomů, u nichž je obvyklým postupem chirurgická resekce následovaná adjuvantní radioterapií [33]. Gaspar et al prezentovali soubor 9 pacientů s fibrosarkomem mozku. Pacienti byli léčeni chirurgickou resekcí a v 8 případech adjuvantní radioterapií (45–60 Gy). K lokoregionální recidivě došlo v 8 z 9 případů. S ohledem na tuto skutečnost autoři doporučují další navýšení dávky radioterapie až na 66 Gy (nicméně s vědomím, že ke generalizaci došlo u 50 % pacientů, by měla být zvažována také systémová léčba) [34]. Pro úplnost zmiňujeme gliosarkomy, které představují prognosticky nepříznivou variantu IDH nemutovaných glioblastomů, a nepředstavují tedy nádory mezenchymálního původu, které jsou předmětem tohoto článku. V našem případě myxoidního meningeálního sarkomu jsme se rozhodli pouze pro samostatnou adjuvantní normofrakcionovanou radioterapii lůžka tumoru po resekci, a to v případě exstirpace obou recidiv, jelikož se ozařovaná pole navzájem nepřekrývala. Zohlednili jsme také na absenci dat prokazujících efektivitu systémové léčby bez adjuvantní chemoterapie. V současnosti bohužel léčebná doporučení pro tento typ nádoru ve standardech European Society for Medical Oncology a National Comprehensive Cancer Network chybí.
Table 1. Přehled kazuistik primárních intrakraniálních sarkomů. 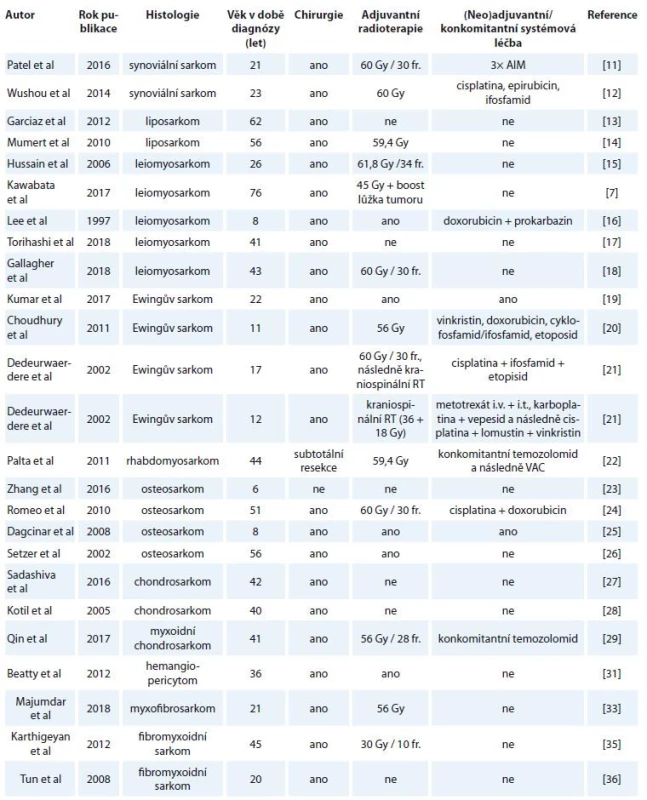
Gy – Gray, fr. – frakce, RT – radioterapie, AIM – doxorubicin, ifosfamid, mesna, VAC – vinkristin, aktinomycin D, cyklofosfamid Závěr
Myxoidní meningeální sarkom je vzácné nádorové onemocnění mozku, při němž chirurgická resekce spolu s adjuvantní radioterapií představuje potenciální léčebný postup, avšak s vysokým rizikem lokoregionální recidivy.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.Obdrženo: 3. 2. 2019
Přijato: 19. 2. 2019
doc. MUDr. David Vrána, Ph.D.
Onkologická klinika
LF UP a FN Olomouc
I. P. Pavlova 6
779 00 Olomouc
e-mail: davvrana@gmail.com
Sources
1. Maher OM, Khatua S, Mukherjee D et al. Primary intracranial soft tissue sarcomas in children, adolescents, and young adults: single institution experience and review of the literature. J Neurooncol 2016; 127 (1): 155–163. doi: 10.1007/s11060-015-2027-3.
2. Louis DN, Perry A, Reifenberger G et al. The 2016 World Health Organization classification of tumors of the central nervous system: a summary. Acta Neuropathol 2016; 131 (6): 803–820. doi: 10.1007/s00401-016-1545-1.
3. Benesch M, von Bueren AO, Dantonello T et al. Primary intracranial soft tissue sarcoma in children and adolescents: a cooperative analysis of the European CWS and HIT study groups. J Neurooncol 2013; 111 (3): 337–345. doi: 10.1007/s11060-012-1020-3.
4. UpToDate.com. Uncommon brain tumors. [online]. Available from: https: //www.uptodate.com/contents/uncommon-brain-tumors?search=brain%20tumors&topicRef=5180&source=see_link#H45.
5. Davis JL, Tihan, T, Kilpatrick, SE. Mesenchymal tumors of the central nervous system. In: Perry A, Brat DJ (eds). Practical surgical neuropathology: a diagnostic approach. 2nd ed. Radarweg: Elsevier 2018 : 299–322.
6. Kalita O, Cwiertka K, Vrána D et al. Multimodal therapy of recurrent malignant schwannoma. Klin Onkol 2016; 29 (5): 364–368. doi: 10.14735/amko2016364.
7. Kawabata Y, Aoki T, Yamamoto T et al. Pazopanib-mediated long-term disease stabilization after local recurrence and distant metastasis of primary intracranial leiomyosarcoma: a case report on the efficacy of pazopanib as a salvage therapy. NMC Case Rep J 2017; 5 (1): 1–7. doi: 10.2176/nmccrj.cr.2017-0048.
8. Apra C, Alentorn A, Mokhtari K et al. Pazopanib efficacy in recurrent central nervous system hemangiopericytomas. J Neurooncol 2018; 139 (2): 369–372. doi: 10.1007/s11060-018-2870-0.
9. Lafay-Cousin L, Lindzon G, Taylor MD et al. Successful treatment of primary intracranial sarcoma with the ICE chemotherapy regimen and focal radiation in children. J Neurosurg Pediatr 2016; 17 (3): 298–302. doi: 10.3171/2015.6.PEDS14709.
10. Merimsky O, Lepechoux C, Terrier P, et al. Primary sarcomas of the central nervous system. Oncology 2000; 58 (3): 210–214. doi: 10.1159/000012102.
11. Patel M, Li L, Nguyen HS et al. Primary intracranial synovial sarcoma. Case Rep Neurol Med 2016; 2016 : 5608315. doi: 10.1155/2016/5608315.
12. Wushou A, Zhao YJ, Shao ZM. Synovial sarcoma of the infratemporal fossa: a case report. Oncol Lett 2014; 8 (5): 2165–2170. doi: 10.3892/ol.2014.2436.
13. Garciaz S, Bouvier C, Roche PH et al. Primary dediffentiated liposarcoma of the dura mater: case report. Acta Neurochir (Wien) 2012; 154 (9): 1737–1738. doi: 10.1007/s00701-012-1449-3.
14. Mumert ML, Walsh MT, Jensen EM et al. Pleomorphic liposarcoma originating from intracranial dura mater. J Neurooncol 2010; 97 (1): 149–153. doi: 10.1007/s11060-009-0005-3.
15. Hussain S, Nanda A, Fowler M et al. Primary intracranial leiomyosarcoma: report of a case and review of the literature. Sarcoma 2006; 2006 : 52140. doi: 10.1155/SRCM/2006/52140.
16. Lee TT, Page LK. Primary cerebral leiomyosarcoma. Clin Neurol Neurosurg 1997; 99 (3): 210–212.
17. Torihashi K, Chin M, Yoshida K et al. Primary intracranial leiomyosarcoma with intratumoral hemorrhage: case report and review of literature. World Neurosurg 2018; 116 : 169–173. doi: 10.1016/j.wneu.2018.05.004.
18. Gallagher SJ, Rosenberg SA, Francis D et al. Primary intracranial leiomyosarcoma in an immunocompetent patient: case report and review of the literature. Clin Neurol Neurosurg 2018; 165 : 76–80. doi: 10.1016/j.clineuro.2017.12.014.
19. Kumar V, Singh A, Sharma V et al. Primary intracranial dural-based Ewing sarcoma/peripheral primitive neuroectodermal tumor mimicking a meningioma: a rare tumor with review of literature. Asian J Neurosurg 2017; 12 (3): 351–357. doi: 10.4103/1793-5482.185060.
20. Choudhury KB, Sharma S, Kothari R et al. Primary extraosseous intracranial Ewing’s sarcoma: case report and literature review. Indian J Med Paediatr Oncol 2011; 32 (2): 118–121. doi: 10.4103/0971-5851.89798.
21. Dedeurwaerdere F, Giannini C, Sciot R et al. Primary peripheral PNET/Ewing’s sarcoma of the dura: a clinicopathologic entity distinct from central PNET. Mod Pathol 2002; 15 (6): 673–678. doi: 10.1038/modpathol.3880 585.
22. Palta M, Riedel RF, Vredenburgh JJ et al. Primary meningeal rhabdomyosarcoma. Sarcoma 2011; 2011 : 312802. doi: 10.1155/2011/312802.
23. Zhang S, Ju Y, You C. A rare case of extensive primary meningeal osteosarcoma in childhood. Neurology 2016; 87 (13): 1420–1421. doi: 10.1212/WNL.0000000000003159.
24. Romeo E, Gisserot O, de Jaureguiberry JP et al. Meningeal chondroblastic osteosarcoma: case report and review of the literature. J Neurooncol 2010; 100 (2): 305–309. doi: 10.1007/s11060-010-0167-z.
25. Dagcinar A, Bayrakli F, Yapicier O et al. Primary meningeal osteosarcoma of the brain during childhood. Case report. J Neurosurg Pediatr 2008; 1 (4): 325–329. doi: 10.3171/PED/2008/1/4/325.
26. Setzer M, Lang J, Turowski B et al. Primary meningeal osteosarcoma: case report and review of the literature. Neurosurgery 2002; 51 (2): 488–492, discussion 492.
27. Sadashiva N, Sharma A, Shukla D et al. Intracranial extraskeletal mesenchymal chondrosarcoma. World Neurosurg 2016; 95 : 618.e1–618.e6. doi: 10.1016/j.wneu.2016.08.049.
28. Kotil K, Bilge T, Olagac V. Primary intradural myxoid chondrosarcoma: a case report and review in the lite-rature. J Neurooncol 2005; 75 (2): 169–172. doi: 10.1007/ s11060-005-1739-1.
29. Qin Y, Zhang HB, Ke CS et al. Primary extraskeletal myxoid chondrosarcoma in cerebellum: a case report with literature review. Medicine (Baltimore) 2017; 96 (47): e8684. doi: 10.1097/MD.0000000000008684.
30. Li D, Weng JC, Zhang GJ et al. Proposed treatment paradigm for intracranial chondrosarcomas based on multidisciplinary coordination. World Neurosurg 2018; 109: e517–e530. doi: 10.1016/j.wneu.2017.10.013.
31. Beatty Z, Bergman T. Meningeal hemangiopericytoma with intracranial metastases in an HIV-positive male: case report and review of the literature. Case Rep Oncol 2012; 5 (1): 159–163. doi: 10.1159/000337580.
32. Rutkowski MJ, Sughrue ME, Kane AJ et al. Predictors of mortality following treatment of intracranial hemangiopericytoma. J Neurosurg 2010; 113 (2): 333–339. doi: 10.3171/2010.3.JNS091882.
33. Majumdar K, Mandal S, Saran RK et al. Recurrent intracranial myxofibrosarcoma presenting as an extensive fronto-parieto-occipital SOL: an unusual sarcoma of meningeal origin. Clin Neurol Neurosurg 2013; 115 (3): 354–358. doi: 10.1016/j.clineuro.2012.05.030.
34. Gaspar LE, Mackenzie IR, Gilbert JJ et al. Primary cerebral fibrosarcomas. Clinicopathologic study and review of the literature. Cancer 1993; 72 (11): 3277–3281.
35. Karthigeyan M, Malik P, Garg S et al. Intracranial low grade fibromyxoid sarcoma with an atypical radiology. World Neurosurg 2019; 122 : 500–504. doi: 10.1016/j.wneu.2018.11.082.
36. Tun K, Ozen O, Kaptanoglu E et al. Primary intracranial low-grade fibromyxoid sarcoma (Evans tumor). J Clin Neurosci 2008; 15 (11): 1298–1301. doi: 10.1016/j.jocn.2007.07.085.
Labels
Paediatric clinical oncology Surgery Clinical oncology
Article was published inClinical Oncology

2019 Issue 3-
All articles in this issue
- MikroRNA v mozkomíšním moku jako biomarkery u pacientů s nádory mozku
- Sledování prognózy HPV pozitivních a negativních orofaryngeálních karcinomů v závislosti na léčebné modalitě
- Nanočásticemi modifikovaný apoferritinový nanotransportér pro cílený transport cytostatik
- Prevalence symptomů úzkosti a deprese a jejich vliv na kvalitu života u pacientů v paliativní onkologické léčbě – projekt PALINT
- Rhabdomyosarkom gluteus maximus – kazuistika, přehled literatury a terapeutické cíle
- Neoadjuvantní užití hypertermické izolované perfuze končetiny v léčbě nediferencovaného vřetenobuněčného sarkomu dolní končetiny s dosažením kompletní patologické odpovědi
- Primární intrakraniální sarkomy, myxoidní meningeální sarkom – kazuistika a přehled literatury
- Osamelosť pacientov v predterminálnom a terminálnom štádiu nádorovej choroby, sociálny rozmer zomierania
- Současný FIGO staging karcinomu děložního hrdla a léčba jednotlivých stadií
- Asociace TNF-α -308G>A polymorfizmu s citlivostí na karcinom děložního čípku a prsu – systematický přehled a metaanalýza
- Clinical Oncology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Současný FIGO staging karcinomu děložního hrdla a léčba jednotlivých stadií
- Rhabdomyosarkom gluteus maximus – kazuistika, přehled literatury a terapeutické cíle
- Prevalence symptomů úzkosti a deprese a jejich vliv na kvalitu života u pacientů v paliativní onkologické léčbě – projekt PALINT
- Osamelosť pacientov v predterminálnom a terminálnom štádiu nádorovej choroby, sociálny rozmer zomierania
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

