-
Medical journals
- Career
Paliativní chirurgická léčba nádorů pankreatu a periampulární oblasti
Authors: F. Čečka 1; B. Jon 1; J. Dvořák 2; R. Repák 3; Z. Šubrt 1; A. Ferko 1
Authors‘ workplace: Chirurgická klinika, LF UK a FN Hradec Králové 1; Klinika onkologie a radioterapie, LF UK a FN Hradec Králové 2; II. interní klinika, LF UK a FN Hradec Králové 3
Published in: Klin Onkol 2012; 25(2): 117-123
Category: Original Articles
Overview
Východiska:
Karcinom pankreatu je agresivní nádorové onemocnění, které má zvyšující se incidenci. Radikální resekce, která jediná je potenciálně kurabilní metodou léčby, je možná pouze u 20–30 % pacientů. Hlavními symptomy, které obtěžují pacienty s pokročilým neresekabilním karcinomem hlavy pankreatu a periampulární oblasti, jsou obstrukční ikterus při stenóze distálního choledochu, vysoký ileus při stenóze duodena a bolesti, zejména epigastria a v zádech. Smyslem paliativní léčby je zmírnění těchto obtíží.
Cílem našeho sdělení je zhodnotit vlastní výsledky paliativní chirurgické léčby maligního onemocnění pankreatu a periampulární oblasti.Soubor pacientů a metody:
Do souboru jsme zařadili pacienty s karcinomem pankreatu a periampulární oblasti, které jsme operovali na Chirurgické klinice FN Hradec Králové od 1. 1. 2006 do 31. 12. 2010. Všechny pacienty jsme indikovali k operaci se záměrem resekčního výkonu. U těch pacientů, u kterých byl během operace nález zhodnocen jako neresekabilní, jsme provedli paliativní operační výkon. U neresekabilního karcinomu hlavy pankreatu jsme vždy provedli gastro-entero anastomózu. V případě, že před operací karcinom hlavy pankreatu způsobil obstrukční ikterus při stenóze distální části žlučových cest a pokud to operační nález dovolil, našívali jsme hepatiko-jejuno anastomózu. Pokud měl pacient před operací bolesti v zádech, prováděli jsme též chirurgickou splanchnikektomii.Výsledky:
Za uvedené období 5 let jsme na našem pracovišti pro maligní onemocnění pankreatu a periampulární oblasti operovali 94 pacientů. Radikální resekci pro karcinom jsme provedli ve 45 případech. Paliativní spojkové operace jsme provedli ve 42 případech. Pouze exploraci jsme provedli u 7 pacientů. Pooperační komplikace u paliativních operací jsme zaznamenali u 15 pacientů (30,6 %), většina těchto komplikací byla nezávažných.Závěr:
Výhodou chirurgicky provedené hepatiko-jejuno anastomózy oproti zavádění endoskopických stentů je zejména lepší dlouhodobá průchodnost, proto je vhodné tuto operaci provádět u pacientů s delším předpokládaným přežitím. Morbidita spojkových operací je vcelku nízká a 30denní pooperační letalita v našem souboru nulová.Klíčová slova:
karcinom pankreatu – paliativní terapie – paliativní chirurgické výkony – přežití – kvalita životaÚvod
Karcinom pankreatu je agresivní nádorové onemocnění, které má zvyšující se incidenci. Podle Národního onkologického registru byla v roce 2006 hlášena hrubá incidence 19,2 na 100 000 za rok u mužů a 17,9 na 100 000 za rok u žen. Mortalita byla 17,7 na 100 000 za rok u mužů a 18,2 na 100 000 za rok u žen [1]. Mortalita dosahuje přibližně stejných hodnot jako incidence, což značí dlouhodobě infaustní prognózu. To je dáno především agresivní biologickou povahou onemocnění, pozdními příznaky a nízkou resekabilitou. Radikální resekce, která jediná je potenciálně kurabilní metodou léčby, je možná pouze u 20–30 % pacientů [2]. Většina pacientů má lokálně pokročilé nebo diseminované onemocnění již v době diagnózy a u nich je možná pouze paliativní nebo symptomatická léčba. Hlavními symptomy, které obtěžují pacienty s pokročilým neresekabilním karcinomem hlavy pankreatu a periampulární oblasti (karcinom Vaterské papily, distálního choledochu a duodena), jsou obstrukční ikterus při stenóze distálního choledochu, vysoký ileus při stenóze duodena a bolesti, zejména epigastria a v zádech [3]. Cílem paliativní léčby je zmírnění těchto obtíží. Přibližně 70 % pacientů má obstrukční ikterus v době zjištění diagnózy, proto i v rámci paliativní péče nabývá řešení obstrukčního ikteru největšího významu [4]. Obstrukční ikterus může vést k akutní cholangoitidě, dále může způsobit jaterní selhání a vést k závažné koagulopatii, čímž přímo ohrožuje život pacientů [5]. Bylo popsáno více metod paliativního řešení obstrukčního ikteru. V současné době se nejčastěji používá endoskopická drenáž žlučových cest při ERCP se zavedením plastového stentu a chirurgické našití hepatiko-jejuno anastomózy [6]. Endoskopická drenáž má všechny výhody miniinvazivního postupu a je většinou dobře tolerovaná. Nicméně největší nevýhodou této metody je riziko opakování obstrukčního ikteru při obstrukci stentu nebo jeho migraci. Další komplikací může být prorůstání nádoru a z toho vyplývající stenóza duodena, která zabrání opakovanému endoskopickému vyšetření a dalším výměnám stentů [7]. Endoskopická drenáž žlučových cest má celkově nižší morbiditu a letalitu, doba hospitalizace je kratší než při chirurgickém řešení ikteru.
Cílem našeho sdělení je zhodnotit vlastní výsledky paliativní chirurgické léčby maligního onemocnění pankreatu a periampulární oblasti.
Soubor pacientů a metody
Do souboru jsme zařadili pacienty s karcinomem pankreatu a periampulární oblasti, které jsme operovali na Chirurgické klinice FN Hradec Králové od 1. 1. 2006 do 31. 12. 2010. Všechny pacienty jsme indikovali k operaci se záměrem resekčního výkonu. U těch pacientů, u kterých byl během operace nález zhodnocen jako neresekabilní, jsme provedli paliativní operační výkon. Důvodem neresekability byla diseminace procesu po peritoneu, nově zjištěné metastatické postižení jater nebo lokálně pokročilý růst tumoru s infiltrací cévních struktur.
V těchto případech jsme prováděli paliativní spojkovou operaci, u neresekabilního karcinomu hlavy pankreatu jsme vždy provedli gastro-entero anastomózu. V případě, že před operací karcinom hlavy pankreatu způsobil obstrukční ikterus při stenóze distální části žlučových cest a pokud to operační nález dovolil, našívali jsme hepatiko-jejuno anastomózu. Na našem pracovišti provádíme paliativní spojkovou operaci nejčastěji formou dvou omega kliček (přední antekolická gastro-jejuno anastomóza a hepatiko-jejuno anastomóza), obě jsou spojeny Braunovou spojkou, celkem tedy 4 anastomózy. V některých případech provádíme hepatiko-jejuno anastomózu a gastro-jejuno anastomózu na kličku podle Rouxe, celkem 3 anastomózy. Tato druhá metoda je vhodná při menším tumoru a delším závěsu mezenteria. Výhodou této metody je menší počet anastomóz, nevýhodou je možný reflux žluče do žaludku. Pokud je ponechaný tumor velký, provádíme spojkovou operaci formou dvou omega kliček, gastro-jejuno anastomózu vždy antekolicky, hepatiko-jejuno anastomózu antekolicky nebo retrokolicky, tak aby nebyla anastomóza pod tahem.
Pokud měl pacient před operací bolesti v zádech, prováděli jsme též splanchnikektomii [8]. Jestliže byl karcinom lokalizován v těle nebo kaudě pankreatu a nezpůsoboval útlak duodena či žlučových cest, tak jsme paliativní spojky neprováděli. Pouze v případě bolestí před operací jsme provedli splanchnikektomii. Splanchnikektomii provádíme následujícím způsobem: po protětí pars hepatogastrica omenti minoris natneme zadní peritoneum mezi aortou a dolní dutou žílou. Za arteria hepatica communis vyhledáme ganglion coeliacum dextrum, které resekujeme. Přístup ke ganglion coeliacum sinistrum je možný po odtažení abdominálního jícnu vlevo, nicméně tento přístup je poměrně obtížný, s vyšším rizikem poranění jiných struktur, proto ganglion coeliacum sinistrum neresekujeme.
U pacientů jsme sledovali pooperační komplikace, 30denní pooperační letalitu, dobu hospitalizace, dlouhodobé výsledky průchodnosti hepatiko-jejuno anastomózy a celkovou dobu přežití. Pooperační komplikace jsme hodnotili podle Dinda, tab. 1 [9]. Přežití jsme zjišťovali ze zdravotní dokumentace pacientů, dotazem u praktického lékaře nebo u spádových zdravotnických zařízení.
Table 1. Komplikace podle Dinda. 
Výsledky
Za uvedené období jsme na Chirurgické klinice FN Hradec Králové pro maligní onemocnění pankreatu a periampulární oblasti operovali 94 pacientů. Průměrný věk všech pacientů byl 65 let. Radikální resekci pro karcinom jsme provedli ve 45 případech, z toho parciální duodenopankreatektomii 38× a levostrannou resekci pankreatu 7×. Totální duodenopankreatektomii jsme neprovedli v žádném případě.
Paliativní spojkové operace jsme provedli ve 42 případech. Z toho pouze gastro-entero anastomózu u 9 pacientů. Gastro-entero anastomózu s hepatiko-jejuno anastomózou u 33 pacientů. Pouze exploraci jsme provedli u 7 pacientů. Splanchnikektomii jsme provedli u 7 pacientů, z toho u spojkové operace ve 4 případech a u explorace ve 3 případech. U spojkových operací byla průměrná doba hospitalizace 12 dní, rozmezí 8–35 dní. U explorace byla průměrná doba hospitalizace 9 dní, rozmezí 7–12 dní.
Pooperační komplikace u paliativních operací jsme zaznamenali u 15 pacientů (30,6 %), většina těchto komplikací byla nezávažných – Dindo I a II, tj. neinfekční a infekční ranné komplikace, močové infekce, pooperační pneumonie lehkého stupně a jiné. Závažné pooperační komplikace Dindo III a IV měli pouze 3 pacienti (6,1 %). V jednom případě se jednalo o pooperační cholangoitidu, přechodně byla zavedena PTBD (perkutánní transhepatická biliární drenáž), hepatiko-jejuno anastomóza byla dobře průchodná. Po zlepšení stavu byla zevní drenáž odstraněna, další komplikace se neobjevily. Druhý pacient měl krvácení z gastro-jejuno anastomózy při plné antikoagulační léčbě nízkomolekulárním heparinem po náhradě aortální chlopně v minulosti. Krvácení bylo ošetřeno endoskopicky a po úpravě dávkování nízkomolekulárního heparinu se již neobnovilo. Třetí pacient měl 2. pooperační den fibrilaci komor, nejspíše na podkladě kardiální nestability při větším peroperačním přesunu tekutin. Byl úspěšně resuscitován a po zlepšení stavu propuštěn 23. pooperační den do domácího ošetřování. 30denní pooperační letalita v našem souboru pacientů se spojkovými operacemi byla nulová.
Dlouhodobá průchodnost hepatiko-jejuno anastomóz byla dobrá, žádný pacient neměl po operaci až do úmrtí obstrukční ikterus. Kromě jedné komplikace (akutní cholangoitidy řešené pomocí dočasně zavedené PTBD zmíněné výše) jsme další komplikace hepatiko-jejuno anastomóz nezaznamenali; leak nebo dehiscenci hepatiko-jejuno anastomózy jsme neměli u žádného pacienta. Dehiscenci gastro-entero anastomózy jsme též nepozorovali v žádném případě.
Dlouhodobé přežití pacientů jsme hodnotili podle Kaplan-Meiera. Medián přežití pacientů po paliativních spojkových výkonech a exploracích byl 10 měsíců. Více než 6 měsíců přežilo 31 z 49 pacientů (63,3 %). Jednoleté přežití bylo 30,6 %, tříleté přežití bylo 0 %.
Porovnání přežívání pacientů po radikálních a paliativních výkonech je patrné v grafu 1. K porovnání přežití pacientů v obou skupinách byl použit log-rank test. Mezi oběma skupinami byl zjištěn statisticky významný rozdíl, p < 0,01.
Diskuze
Karcinom pankreatu a periampulární oblasti je závažné onemocnění s poměrně špatnou prognózou. Jedinou potenciální kurativní modalitou léčby je radikální resekce. Resekční výkon oproti paliativním spojkám může významně prodloužit přežití (graf 1).
Graph 1. Porovnání přežití pacientů po radikální resekci (tmavá) a paliativní spojkové operaci (světlá). 
Při indikaci pacientů k operaci postupujeme podle obecně platného schématu uvedeného v grafu 2:
- Operaci indikujeme, pokud z vyšetřovacích metod (CT, ERCP, EUS, onkomarkery) vyplyne podezření na karcinom pankreatu nebo periampulární oblasti. Předoperační biopsii nevyžadujeme v případech, kdy je nález typický pro karcinom pankreatu. Tessler ukázal, že kombinace ztráty hmotnosti o více než 9 kg, sérové koncentrace bilirubinu nad 51 µmol/l a vyšší sérové koncentrace CA 19–9 má 100% specificitu k predikci malignity i bez předoperační biopsie [10]. Naopak u pacientů, kde jsou nálezy vyšetřovacích metod nejednoznačné, nebo dokonce protichůdné, vyžadujeme odběr biopsie, nejčastěji při endosonografii, méně často transabdominálně pod UZ kontrolou. Dále u rizikovějších pacientů klademe větší důraz na průkaz malignity před operací, abychom tak snížili počet resekcí pankreatu pro benigní léze u rizikových pacientů.
- Absolutně neresekabilní nádor se vyskytuje při metastatickém postižení jiných orgánů, nejčastěji jater, to může být patrné na CT vyšetřeních provedených před operací (obr. 1). U těchto pacientů chirurgickou exploraci neindikujeme. Diagnostická laparoskopie, která měla zlepšit zhodnocení lokoregionálního stagingu, nesplnila očekávání. Nieveen van Dijkum studoval efektivitu diagnostické laparoskopie u 297 pacientů a zjistil, že přínos tohoto postupu je menší, než bylo očekáváno [11]. Při otevřené chirurgické exploraci je možné lépe zhodnotit infiltraci cévních struktur a v indikovaných případech je možné resekovat tumor s infiltrovanou částí horní mezenterické žíly (VMS) nebo portální žíly en block [12]. Domníváme se, že je chybou neindikovat k operaci pacienty, u kterých je vysloveno pouhé podezření na infiltraci VMS nebo portální žíly na základě vyšetření CT nebo endosonografie.
Bylo navrženo několik klasifikací infiltrace VMS a portální žíly při zobrazovacích metodách. Klasifikace podle Loyera posuzuje konvexitu obrysu tumoru ve vztahu k žíle, viz tab. 2 [13]. Dále je možno posuzovat délku infiltrace žíly tumorem SMV (0 mm, < 5 mm, > 5 mm), cirkumferenci infiltrace žilních struktur (0°, 0–90°, 90–180°, nad 180°) [14].
Resekabilita nádoru se nejlépe posoudí až při chirurgické exploraci, a to zejména v hraničních případech. V indikovaných případech je možné provést en block resekci VMS nebo portální žíly s tumorem [12] (obr. 2). Přežití těchto pacientů je stejné jako u pacientů po resekci pankreatu bez resekce cév [15]. V některých případech je při chirurgické exploraci vysloveno podezření na infiltraci žíly tumorem, po provedené resekci se žílou en block se při definitivním histologickém vyšetření zjistí pouze zánětlivá reakce okolo tumoru, která imituje maligní infiltraci žilních struktur [15]. - Resekce pankreatu je náročný operační výkon, který má sice relativně nízkou pooperační letalitu, nicméně morbidita zůstává vysoká [16]. Při růstu incidence karcinomu pankreatu a stárnutí populace se stále častěji setkáváme s pacienty vyššího věku, kteří mají další různě závažné choroby (např. ICHS, CHOPN, renální insuficienci, DM atd.), a zvažujeme u nich resekci pankreatu. V těchto případech se neřídíme věkem, ale celkovým stavem pacientů. Vyšší věk sám o sobě není kontraindikací resekce pankreatu [17,18]. V rámci předoperačního vyšetření se jeví vhodná i zátěžová ergometrie, která dobře posoudí funkční rezervu pacienta.
- Indikace resekce pankreatu je závažné rozhodnutí, je nutné postupovat individuálně a pacienta pečlivě poučit o všech rizicích operace. Informovaný souhlas pacienta s operací je nezbytnou podmínkou.
Image 1. Rozsáhlý tumor těla pankreatu s infiltrací portální žíly, truncus coeliacus a žaludku (černá šipka). Patrné bilobární metastatické postižení jater (bílé šipky). Chirurgická léčba u tohoto pacienta není indikována. 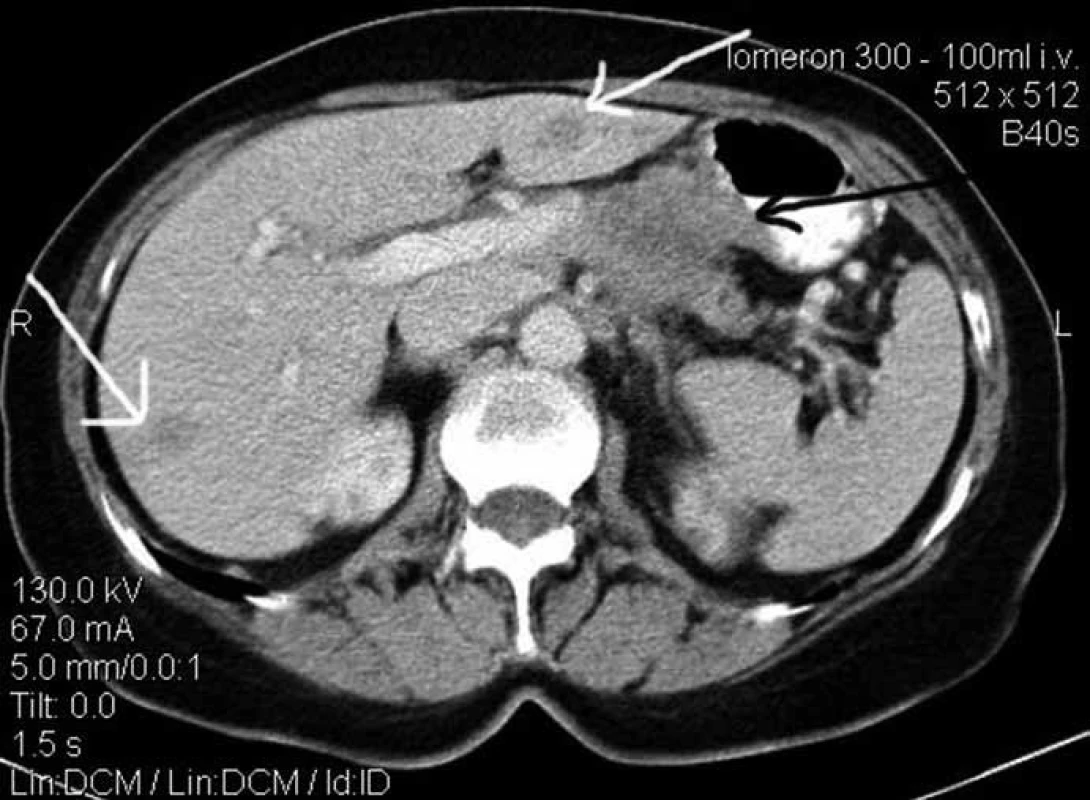
Image 2. Karcinom hlavy pankreatu s infiltrací vena mesenterica superior stupně D podle Loyera (černá šipka). Provedena parciální duodenopankreatektomie s resekcí vena mesenterica superior a náhradou štěpem vena saphena magna. 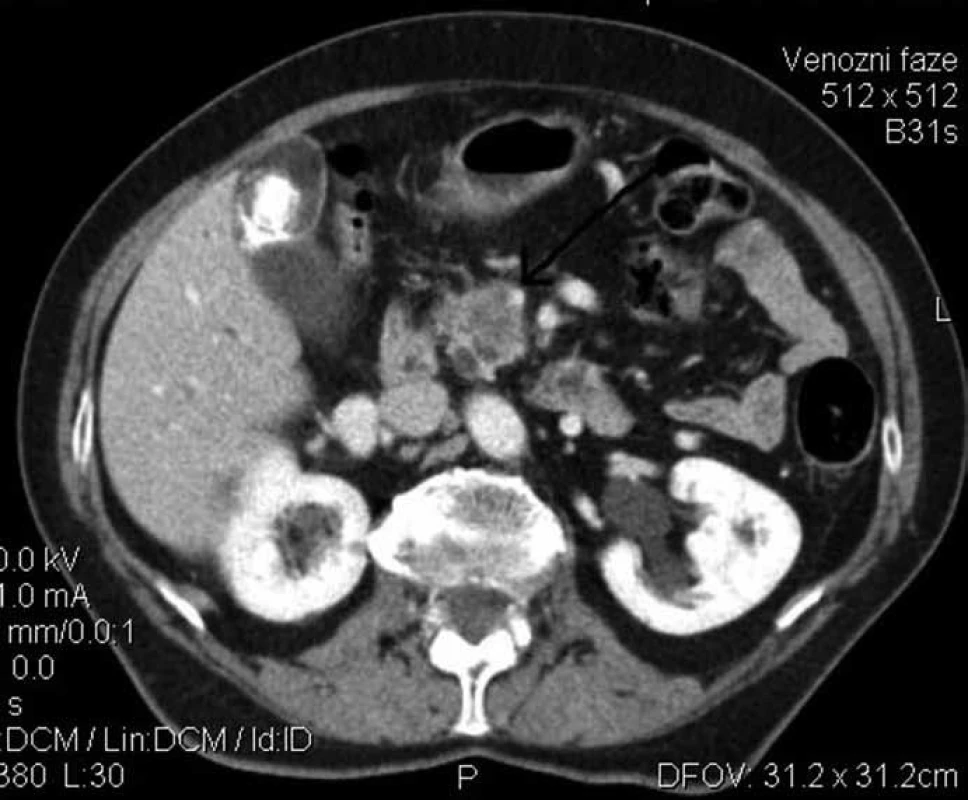
Table 2. Infiltrace v. mesenterica superior a v. portae podle Loyera. 
Všechny pacienty v uvedeném souboru pacientů jsme indikovali k operaci se záměrem radikální resekce, ovšem resekce byla možná pouze u 45 pacientů (47,9 %). Resekabilita v našem souboru pacientů byla vyšší, než je běžně udávaná resekabilita všech karcinomů pankreatu, protože jsme neoperovali pacienty s diseminací prokázanou v době diagnostiky onemocnění [19]. Pokud byl nádor hlavy pankreatu a periampulární oblasti při exploraci zhodnocen jako neresekabilní, prováděli jsme paliativní spojkové operace. Cílem paliativní léčby je zlepšit kvalitu života pacientů, tato léčba ovšem nemůže prodloužit přežití. V našem souboru byl medián přežití po spojkové operaci 10 měsíců, déle než 6 měsíců přežilo 63,3 % pacientů.
Přežití pacientů s neresekovaným tumorem v našem souboru bylo delší, než jsou běžně uváděná přežití karcinomu pankreatu a periampulární oblasti, protože se jednalo o vybranou skupinu pacientů. Všichni pacienti byli indikováni k operaci se záměrem radikální resekce, pacienti s prokázanou diseminací před operací nebyli do souboru zařazeni.
Závažné pooperační komplikace jsme zaznamenali u 3 pacientů (6,1 %), celkově mělo jakoukoliv komplikaci 15 pacientů (30,6 %). Morbidita v našem souboru je přijatelná a srovnatelná s podobnými soubory pacientů v jiných centrech [20]. Důležité je, že 30denní pooperační letalita byla nulová. Dále že chirurgické našití hepatiko-jejuno spojky zajistilo dobrou drenáž žlučových cest u všech pacientů. Žádný pacient neměl obstrukční ikterus až do své smrti. Komplikaci hepatiko-jejuno spojky jsme zaznamenali pouze v jednom případě (3 %).
Drenáž žlučových cest je hlavním cílem paliativní léčby u většiny pacientů s neresekabilním karcinomem hlavy pankreatu a periampulární oblasti. Endoskopická drenáž a chirurgická hepatiko-jejuno anastomóza jsou dvě nejčastější možnosti drenáže. Dosud jsou vedeny diskuze, která alternativa je pro pacienta výhodnější. Byly provedeny 4 randomizované studie, které porovnávaly výsledky endoskopické drenáže žlučových cest a chirurgické hepatiko-jejuno spojky [7,21–23].
V těchto studiích vykazovali pacienti s chirurgickou drenáží žlučových cest vyšší krátkodobou morbiditu a delší dobu hospitalizace, ale lepší dlouhodobou průchodnost anastomózy. Naproti tomu pacienti s endoskopicky založenou drenáží měli nižší morbiditu a iniciálně kratší dobu hospitalizace po drenáži. Nicméně 20–25 % mělo při dlouhodobém sledování komplikace, které vyplynuly z obstrukce stentu, tj. recidivující ikterus a cholangoitidu [24]. Interval průchodnosti plastového stentu je přibližně 70 dní [2]. V pozdější metaanalýze bylo uvedeno, že dostupné údaje nejsou dostatečné k definitivnímu závěru, která metoda by měla být preferována [25]. K nevýhodám uvedených studií patří fakt, že byly provedeny před delší dobou. V poslední době došlo ke zlepšení operačních technik, zavedení nových materiálů, zlepšení pooperační péče, které vedly k lepším výsledkům chirurgické léčby a snížení pooperační morbidity.
Novější studie udávají, že rozhodnutí o výběru metody drenáže žlučových cest by mělo být vedeno předpokládanou prognózou pacienta. Endoskopická drenáž je doporučována u pacientů, kteří mají diseminaci onemocnění nebo je u nich předpoklad přežití méně než 6 měsíců [3,24].
Jedna recentní studie dokonce uvádí, že chirurgická drenáž žlučových cest může mít výhodu v delším přežití pacientů oproti endoskopické drenáži. Důvodem je, že při chirurgické drenáži nedochází k recidivujícím cholangoitidám a sepsím u pacientů [2]. Nicméně tato studie byla retrospektivní a autoři ve studii nehodnotili rozsah onemocnění před terapií.
Delší průchodnost než plastové stenty by měl mít kovový stent. Byla publikována jedna retrospektivní studie porovnávající chirurgickou drenáž žlučových cest s drenáží pomocí kovového stentu [26]. V této studii se uvádí, že pacienti s kovovým stentem mají více pozdních komplikací (stenóza duodena, recidiva obstrukčního ikteru a cholangoitidy). Nevýhodou kovových stentů je nemožnost jejich odstranění, pokud způsobí komplikace [27].
Další výhodou chirurgické drenáže žlučových cest je možnost našití gastro-entero anastomózy v jedné době, tzv. double bypassu. Přibližně u 20 % pacientů s neresekabilním karcinomem hlavy pankreatu se postupně vyvine stenóza duodena. Provedení double bypassu v jedné době při porovnání s našitím pouze hepatiko-jejuno spojky účinně zabrání vzniku vysokého ileu. Morbidita a letalita obou operací je srovnatelná [4,28]. Pokud se ovšem gastro-entero anastomóza provádí až v době, kdy má pacient symptomatickou stenózu duodena, je morbidita vysoká a letalita dosahuje až 22 % [6]. Další relativně novou technikou léčby stenózy duodena je aplikace samoexpandibilních kovových stentů do duodena. Tato metoda je vhodná především u pacientů s krátkým předpokládaným přežitím [29]. Dosud nebyla provedena randomizovaná studie, která by porovnávala zavedení stentu do duodena s našitím gastro-entero anastomózy.
Léčba bolesti je nezbytnou součástí terapie pacientů s karcinomem pankreatu a periampulární oblasti. V průběhu onemocnění si stěžuje na bolesti více než 90 % pacientů. Léčba bolesti je nejprve farmakologická podle doporučení WHO. Nejdříve jsou podávána nesteroidní antiflogistika (NSAID), následně opiáty. Nicméně nežádoucí účinky těchto léků jsou výrazné a při progredující bolesti není farmakologická léčba dostačující. Dalším krokem v léčbě bolesti je intervence plexus coeliacus, při přerušení nervových drah z pankreatu se přeruší vnímání bolesti při karcinomu pankreatu. Blokáda plexus coeliacus může být provedena perkutánně pod CT kontrolou. Podle metaanalýzy 24 publikací s 1 145 pacienty, u kterých byla provedena neurolýza plexus coeliacus pod CT kontrolou, pro 70–80 % pacientů znamenala tato léčba dlouhotrvající přínos [30].
Další možností je neurolýza plexus coeliacus při endosonografii. Výsledky nerandomizovaných retrospektivních studií udávají úlevu od bolesti u 85–90 % pacientů [31,32]. Nicméně sledování pacientů v těchto studiích bylo pouze krátkodobé.
Při chirurgické exploraci je možné provést splanchnikektomii otevřeně, možností je buď chemická splanchnikektomie aplikací roztoku alkoholu, nebo přímá resekce ganglion coeliacus. Chemická splanchnikektomie se provádí aplikací 20 ml 50% alkoholu po obou stranách aorty v úrovni odstupu truncus coeliacus. Lillemoe provedl randomizovanou dvojitě zaslepenou studii, kdy porovnával chemickou splanchnikektomii aplikací alkoholu s aplikací placeba [28]. Chemická splanchnikektomie výrazně snížila bolesti pacientů. Oproti placebu signifikantně více pacientů netrpělo bolestí až do úmrtí (56 % vs 34 %). Zajímavým výsledkem této studie bylo, že pacienti s chemickou splanchnikektomií měli delší přežití než pacienti s placebem. Autoři to vysvětlují tím, že přetrvávající bolest vede k celkové deterioraci pacientů, a tím způsobuje časnější úmrtí.
Na našem pracovišti provádíme přímou splanchnikektomii, tj. resekci ganglion coeliacum, používáme techniku popsanou výše. Výhodou oproti chemické splanchnikektomii je přesná disekce ganglion coeliacum, která sníží riziko poranění jiných struktur, nevýhodou je mírné prodloužení operačního času. V našem souboru jsme provedli splanchnikektomii u 7 pacientů. U 4 pacientů (57 %) byl pozorován příznivý efekt výkonu, nicméně tento efekt byl pouze krátkodobý.
Další méně využívanou terapií bolesti u pacientů s karcinomem hlavy pankreatu je torakoskopická splanchnikektomie. V prospektivní studii 44 pacientů s karcinomem pankreatu nebo chronickou pankreatitidou byla provedena bilaterální torakoskopická splanchnikektomie, ta vedla k 50% ústupu bolestí během jednoho týdne po operaci [33]. Nicméně tato operace nese svá rizika, u 9 % pacientů byla vynuceně provedena torakotomie pro peroperační krvácení. Pro svá rizika nemůže být tato metoda považována za standardní metodu léčby bolesti u pacientů s karcinomem pankreatu.
Závěr
Diagnóza karcinomu pankreatu je velmi závažná. Jedinou šancí na dlouhodobé přežití je radikální resekce tumoru. Resekabilita karcinomu pankreatu se nejlépe pozná při chirurgické exploraci. Domníváme se, že je chybou neindikovat operační výkon u pacientů, u kterých je vysloveno podezření na infiltraci horní mezenterické žíly nebo portální žíly. Pacienti s hraničně resekabilním nádorem na CT a EUS by měli být indikováni k chirurgické exploraci a pokusu o resekci. Pokud je nádor peroperačně hodnocen jako neresekabilní, je možné provést paliativní spojkovou operaci: gastro-entero anastomózu a hepatiko-jejuno spojku v jedné době. Výhodou chirurgicky provedené hepatiko-jejuno anastomózy oproti zavádění endoskopických stentů je zejména lepší dlouhodobá průchodnost, proto je vhodné tuto operaci provádět u pacientů s delším předpokládaným přežitím. Morbidita spojkových operací je vcelku nízká a letalita v našem souboru nulová.
Práce byla podpořena výzkumným záměrem Ministerstva zdravotnictví České republiky MZO 00179906 a grantem IGA NS 9998-4.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do bi omedicínských časopisů.
MUDr. Filip Čečka, Ph.D.
Chirurgická klinika
LF UK a FN Hradec Králové
Sokolská 581
500 05 Hradec Králové
e-mail: filip.cecka@seznam.cz
Obdrženo: 23. 10. 2011
Přijato: 1. 11. 2011
Sources
1. Šálek C. Nové poznatky k epidemiologii nádorů pankreatu. Bull HPB 2004; 12(3): 86–90.
2. Distler M, Kersting S, Rückert F et al. Palliative treatment of obstructive jaundice in patients with carcinoma of the pancreatic head or distal biliary tree. Endoscopic stent placement vs. hepaticojejunostomy. JOP 2010; 11(6): 568–574.
3. van Heek NT, van Geenen RC, Busch OR et al. Palliative treatment in „peri“-pancreatic carcinoma: stenting or surgical therapy? Acta Gastroenterol Belg 2002; 65(3): 171–175.
4. van Heek NT, De Castro SM, van Eijck CH et al. The need for a prophylactic gastrojejunostomy for unresectable periampullary cancer: a prospective randomized multicenter trial with special focus on assessment of quality of life. Ann Surg 2003; 238(6): 894–902.
5. Abraham NS, Barkun JS, Barkun AN. Palliation of malignant biliary obstruction: a prospective trial examining impact on quality of life. Gastrointest Endosc 2002; 56(6): 835–841.
6. Köninger J, Wente MN, Müller MW et al. Surgical palliation in patients with pancreatic cancer. Langenbecks Arch Surg 2007; 392(1): 13–21.
7. Shepherd HA, Royle G, Ross AP et al. Endoscopic biliary endoprosthesis in the palliation of malignant obstruction of the distal common bile duct: a randomized trial. Br J Surg 1988; 75(12): 1166–1168.
8. Vobořil Z, Jon B. Splanchnikektomie při onemocněních pankreatu. Rozhl Chir 1994; 73(4): 154–156.
9. Dindo D, Demartines N, Clavien PA. Classification of surgical complications: a new proposal with evaluation in a cohort of 6336 patients and results of a survey. Ann Surg 2004; 240(2): 205–213.
10. Tessler DA, Catanzaro A, Velanovich V et al. Predictors of cancer in patients with suspected pancreatic malignancy without a tissue diagnosis. Am J Surg 2006; 191(2): 191–197.
11. Nieveen van Dijkum EJ, Romijn MG, Terwee CB et al. Laparoscopic staging and subsequent palliation in patients with peripancreatic carcinoma. Ann Surg 2003; 237(1): 66–73.
12. Gürlich R, Oliverius M, Lipár K et al. Výsledky jednoročního přežití u nemocných po resekci hlavy slinivky břišní s resekcí žil portomezenterické oblasti (PMO). Rozhl Chir 2009; 88(8): 417–421.
13. Loyer EM, David CL, Dubrow RA et al. Vascular involvement in pancreatic adenocarcinoma: reassessment by thin-section CT. Abdom Imaging 1996; 21(3): 202–206.
14. Phoa SS, Reeders JW, Stoker J et al. CT criteria for venous invasion in patients with pancreatic head carcinoma. Br J Radiol 2000; 73(875): 1159–1164.
15. Yekebas EF, Bogoevski D, Cataldegirmen G et al. En bloc vascular resection for locally advanced pancreatic malignancies infiltrating major blood vessels: perioperative outcome and long-term survival in 136 patients. Ann Surg 2008; 247(2): 300–309.
16. Winter JM, Cameron JL, Campbell KA et al. 1423 pancreaticoduodenectomies for pancreatic cancer: A single-institution experience. J Gastrointest Surg 2006; 10(9): 1199–1210.
17. Haigh PI, Bilimoria KY, DiFronzo LA. Early postoperative outcomes after pancreaticoduodenectomy in the elderly. Arch Surg 2011; 146(6): 715–723.
18. Lee MK, Dinorcia J, Reavey PL et al. Pancreaticoduodenectomy can be performed safely in patients aged 80 years and older. J Gastrointest Surg 2011; 14(11): 1838–1846.
19. Sener SF, Fremgen A, Menck HR et al. Pancreatic cancer: a report of treatment and survival trends for 100,313 patients diagnosed from 1985–1995, using the National Cancer Database. J Am Coll Surg 1999; 189(1): 1–7.
20. Kuhlmann KF, van Poll D, de Castro SM et al. Initial and long-term outcome after palliative surgical drainage of 269 patients with malignant biliary obstruction. Eur J Surg Oncol 2007; 33(6): 757–762.
21. Andersen JR, Sørensen SM, Kruse A et al. Randomised trial of endoscopic endoprosthesis versus operative bypass in malignant obstructive jaundice. Gut 1989; 30(8): 1132–1135.
22. Bornman PC, Harries-Jones EP, Tobias R et al. Prospective controlled trial of transhepatic biliary endoprosthesis versus bypass surgery for incurable carcinoma of head of pancreas. Lancet 1986; 1(8472): 69–71.
23. Smith AC, Dowsett JF, Russell RC et al. Randomised trial of endoscopic stenting versus surgical bypass in malignant low bileduct obstruction. Lancet 1994; 344(8938): 1655–1660.
24. Schwarz A, Beger HG. Biliary and gastric bypass or stenting in nonresectable periampullary cancer: analysis on the basis of controlled trials. Int J Pancreatol 2000; 27(1): 51–58.
25. Taylor MC, McLeod RS, Langer B. Biliary stenting versus bypass surgery for the palliation of malignant distal bile duct obstruction: a meta-analysis. Liver Transpl 2000; 6(3): 302–308.
26. Maosheng D, Ohtsuka T, Ohuchida J et al. Surgical bypass versus metallic stent for unresectable pancreatic cancer. J Hepatobiliary Pancreat Surg 2001; 8(4): 367–373.
27. Kaassis M, Boyer J, Dumas R et al. Plastic or metal stents for malignant stricture of the common bile duct? Results of a randomized prospective study. Gastrointest Endosc 2003; 57(2): 178–182.
28. Lillemoe KD, Cameron JL, Hardacre JM et al. Is prophylactic gastrojejunostomy indicated for unresectable periampullary cancer? A prospective randomized trial. Ann Surg 1999; 230(3): 322–328.
29. Shaw JM, Bornman PC, Krige JE et al. Self-expanding metal stents as an alternative to surgical bypass for malignant gastric outlet obstruction. Br J Surg 2010; 97(6): 872–876.
30. Eisenberg E, Carr DB, Chalmers TC. Neurolytic celiac plexus block for treatment of cancer pain: a meta-analysis. Anesth Analg 1995; 80(2): 290–295.
31. Giovannini M. Ultrasound-guided endoscopic surgery. Best Pract Res Clin Gastroenterol 2004; 18(1): 183–200.
32. Klapman JB, Chang KJ. Endoscopic ultrasound-guided fine-needle injection. Gastrointest Endosc Clin N Am 2005; 15(1): 169–177.
33. Ihse I, Zoucas E, Gyllstedt E et al. Bilateral thoracoscopic splanchnicectomy: effects on pancreatic pain and function. Ann Surg 1999; 230(6): 785–790.
Labels
Paediatric clinical oncology Surgery Clinical oncology
Article was published inClinical Oncology

2012 Issue 2-
All articles in this issue
- Agresívna fibromatóza: geneticko-biologické korelácie
- Agresívna fibromatóza: klinické aspekty
- Změny imunologické reaktivity u onkologických pacientů
- Prognostický význam morfologického hodnocení u mnohočetného myelomu
- Paliativní chirurgická léčba nádorů pankreatu a periampulární oblasti
- Tyreopatie u žien s karcinómom prsníka
- Klinický registr GIST
- MikroRNA vstupují do klinického testování
- Novinky v diagnostice a léčbě primárních nádorů mozku – závěry mezioborového setkání „Winter GLIO TRACK Meeting“ 2012
- Ionizujúcim žiarením indukované dlhodobé zmeny v hipokampe za experimentálnych podmienok
- Gastrointestinální stromální tumor duodena projevující se akutním krvácením do horního zažívacího traktu a léčený klínovitou resekcí
- Clinical Oncology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Agresívna fibromatóza: geneticko-biologické korelácie
- Agresívna fibromatóza: klinické aspekty
- Paliativní chirurgická léčba nádorů pankreatu a periampulární oblasti
- Tyreopatie u žien s karcinómom prsníka
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career


