-
Medical journals
- Career
Sjednocení a validace referenčních intervalů – pilotní studie
: L. Šprongl 1; H. Pláňková 1; D. Stejskal 2,3
: Centrální laboratoř, Šumperská nemocnice a. s. 1; Vědecko výzkumný institut Agel, pobočka Prostějov, Oddělení laboratorní medicíny Středomoravská nemocniční a. s. 2; Ústav lékařské chemie a biochemie, Lékařská fakulta, Univerzita Palackého Olomouc 3
: Klin. Biochem. Metab., 22 (43), 2014, No. 3, p. 132-137
Cíl studie:
Ověřit použitelnost referenčních intervalů ze zahraniční studie a použít je jako sjednocené pro síť laboratorních pracovišť.Materiál a metody:
Jako ověřované referenční intervaly byly použity údaje ze studie NORIP[1]. K ověření byly použity vzorky dárců krve, 100 vzorků od mužů a 100 vzorků od žen. Měření bylo prováděno maximálně do dvou hodin od odběru. Měření byla provedena za stejných podmínek (jedna kalibrace, stejná obsluha). Ověřovali jsme následující parametry: ALT, AST, GGT, ALP, Na, K, Ca, Urea, Kreatinin, Kyselina močová, Bilirubin celkový a Albumin.Výsledky:
Pro testované parametry jsme ověřili použitelnost referenčních intervalů ze studie NORIP [1] v našich podmínkách. Rozdíly referenčních intervalů námi zjištěných a výsledky ze studie NORIP byly řádově v jednotkách procent.Závěr:
Doporučujeme používat pro výše uvedené parametry referenční intervaly studie NORIP.Klíčová slova:
referenční intervaly, rozhodovací meze, biologická variabilita, referenční populace.Úvod
Referenční intervaly jsou považovány za nejrozšířenější nástroj pro interpretaci laboratorních výsledků vyšetřovaných jednotlivců. Základem je posoudit, jestli je vyšetřovaná osoba zdravá nebo u ní existuje podezření na přítomnost patologické odchylky. Obsah (koncentraci nebo aktivitu měřených parametrů) laboratorních výsledků, stejně jako v případě všech vědeckých dat, totiž nikdy nelze posuzovat izolovaně. Změřené výsledky musí být porovnávány s kohortou dat, která nacházíme u většiny zdravé populace. Z výše uvedených důvodů podávají referenční intervaly v laboratorní medicíně dokonce důležitější informaci než v mnoha jiných medicínských oborech. Často jsou tato data používána i jako diagnostická doporučení, a to v případě, že neexistuje jiný a efektivnější způsob, jak odlišit fyziologický a patologický stav. Zde je však potřeba zdůraznit, že existuje řada platných nadnárodních doporučení, která jsou zaměřena na lékařské rozhodovací meze. To je zcela jiná situace, kdy lékař řeší informaci o efektivitě terapie, její změně, atp. a neinterpretuje referenční rozmezí z hlediska přítomnosti jakékoliv patologické odchylky, ale výsledky u pacienta s definovanou patologií a z toho odvozuje možný dopad na efektivitu terapie, ev. její změnu.
Lze tedy zjednodušit, že referenční intervaly jsou v kombinaci s dalšími klinickými daty schopny posoudit zdravotní stav vyšetřované osoby. Dvě významné organizace - IFCC (International Federation of Clinical Chemistry and Laboratory Medicine) a CLSI (Clinical and Laboratory Standards Institute) – připravily doporučení, jak správně postupovat při tvorbě referenčních intervalů; obě doporučení jsou v zásadě ve shodě.
Tvorba referenčních intervalů měla svůj vývoj – v postupech i v názvosloví. Po druhé světové válce došlo k velkým změnám v nemocničních laboratořích. Zjednodušovalo se (a stávalo se dostupným) měření desítek parametrů u velkého počtu pacientů. Na druhé straně se s rozvojem měření objevila otázka, jak toto množství výsledků interpretovat. Jako první využili pravděpodobnostního rozložení k hodnocení výsledků Wotton a kol. v roce 1951 [2]. Sledovali 18 metod u pravděpodobně zdravých jedinců. Výsledkem bylo obvykle Gaussovo rozložení, avšak autoři nestanovili horní a dolní mez výpočtem, ale pozorováním. Se vzrůstajícím počtem dat bylo ale patrné, že rozložení se liší u různých skupin [3]. Dále se ukázaly rozdíly mezi laboratořemi [4], což bylo příčinou tvorby vlastních „normálních“ hodnot v jednotlivých laboratořích.
Dalším krokem bylo použití výsledků nemocničních pacientů s tím, že většina hodnot je „normální“ a tvoří Gaussovo rozdělení [5] a hodnoty zdravé populace se pohybují mezi limity 2,5. a 97,5. percentilu (95% interval spolehlivosti). Limity byly určovány extrapolací křivky z hodnot mezi 20 a 80 procenty.
Termín referenční hodnoty (intervaly) byl zvolen proto, aby se vyhnulo mnohoznačnosti slova normální [6, 7]. Následně experti IFCC definovali vhodnou terminologii, která by měla být používána [8]. Doporučené postupy ke stanovení byly vytvářeny opět experty IFCC [9], CLSI [10] použila tyto postupy do svých doporučení.
Referenční interval je tedy definován jako soubor hodnot mezi 2,5. a 97,5. percentilem dostatečně homogenního a početného souboru předpokládaně zdravých jedinců. Ceriotti [11] definuje referenční interval jako: Interval, který při aplikaci na populaci vyšetřovanou laboratoří korektně obsahuje většinu osob s charakteristikami odpovídajícími referenční skupině a vylučuje ostatní.
Při určení referenčních intervalů je základním problémem výběr referenčních jedinců a určení referenční populace. Podle doporučení IFCC je minimální velikost souboru 120 jedinců. Tuto velikost souboru lze považovat za minimální, zvětšování souboru vede ke zpřesnění výstupů, podle Ichihary je minimem 400 jedinců [12]. Jednotlivé laboratoře mohou vytvářet samostatné referenční intervaly s velkými obtížemi (ekonomická i časová náročnost). Obvykle se používá pouze postup pro ověřování referenčních intervalů, kde je minimem 20 výsledků [13]. Zdrojem dat k ověřování mohou být publikace v odborných časopisech, výsledky multicentrických studií na velkých počtech jedinců, případně i údaje výrobce.
Optimálním stavem by bylo dosažení všeobecně použitelných referenčních intervalů, závislých pouze na pohlaví, věku a rase. Toto „přání“ ale souvisí se standardizací metod v laboratoři [14]. Lze toho tedy dosáhnout zřejmě jen u parametrů s pokud možno nepřerušeným řetězcem metrologické návaznosti a s dobře definovaným složením [15]. Do této skupiny patří v současné době 65 analytů [16].
V současné době lze najít řadu prací, ať už věnovaných teorii referenčních intervalů [11, 17-23], obecné tvorbě referenčních intervalů [1, 24, 25], či tvorbě specifických referenčních intervalů pro děti a starší populaci [26-29]. Samozřejmě uvedené citace jsou pouze ukázkou, prací věnovaných již přímo stanovení určitých referenčních intervalů jsou desítky.
Cílem naší práce nebylo věnovat se teorii referenčních intervalů, ale najít cestu ke sjednocování těchto intervalů. Chtěli jsme otestovat možnost použití již známých hodnot získaných na velkých populačních souborech cestou jejich ověření a převzetí.
Materiál a metodika
Význam sjednocených referenčních intervalů stoupá jak s pohybem osob, tak s rostoucím počtem sítí zdravotnických zařízení. Není možné, aby byly jedny výsledky pacienta v jednom regionu, síti nemocnic nebo dokonce v jednom městě interpretovány různě. Proto jsme přistoupili ke sjednocování referenčních intervalů v naší síti laboratoří (AGEL), většinou navázaných na nemocnici. Výhodou je téměř ve všech případech stejná měřící technika, kterou v rámci naší sítě využíváme. Vzhledem k ekonomické náročnosti jsme nepřistoupili k tvorbě referenčních intervalů, ale k ověření možnosti převzít je z jiné velké studie. Vzhledem k tomu, že ani v naší síti zatím nedošlo k absolutní a úplné jednotnosti měřících systémů, nebylo možné použít údaje výrobců. Z dostupných výsledků multicentrických studií jsme zvolili výsledky tzv. studie NORIP (Nordic Reference Interval Project) [1]. V této studii jsou použity výsledky ze 102 laboratoří ze skandinávských zemí (Dánsko, Norsko, Finsko, Švédsko a Island) od 3035 dospělých osob.
Rozhodli jsme se v prvním kroku ověřit možnost převzetí referenčních intervalů pro 12 základních analytů v séru – 4 enzymy (ALT, AST, ALP, GGT), 2 elektrolyty (Na, K), 3 substráty (urea, kreatinin, kyselina močová), albumin, bilirubin a vápník. Toto spektrum jsme zvolili i vzhledem k faktu, že jde o nejfrekventovanější metody používané v rutinních biochemických laboratořích. Neověřovali jsme metody, kde existují lokální (národní) doporučené rozhodovací meze či cílové hodnoty. Pokud by byly meze referenčních intervalů ve shodě, převzali bychom tyto hodnoty i pro další měřené veličiny. Shoda znamená, aby odchylka výsledku horní a dolní meze referenčního intervalu nepřesáhla 2/3 TEa (Total error allowable – celková povolená chyba). K ověření bylo použito celkem 200 vzorků dárců krve, aby byl vzorek populace dostatečně reprezentativní (100 vzorků od mužů a 100 vzorků od žen, ve věku 19-58 let, vždy se jednalo o sérum). Vzorky byly získány od dárců prostřednictvím společnosti Transfúzní služba a.s. Šumperk, po předchozím podepsání informovaného souhlasu. U těchto osob předpokládáme, že splňují požadavky na tzv. referenční jedince – absolvují lékařské vyšetření a jako dárci krve by měli splňovat podmínky zdravé populace. Všechna měření proběhla se stejnou šarží diagnostik na jednu kalibraci. Měření probíhala ihned po obdržení vzorku (maximálně do dvou hodin od odběru), aby se eliminoval vliv doby od odběru, především u draselných iontů.
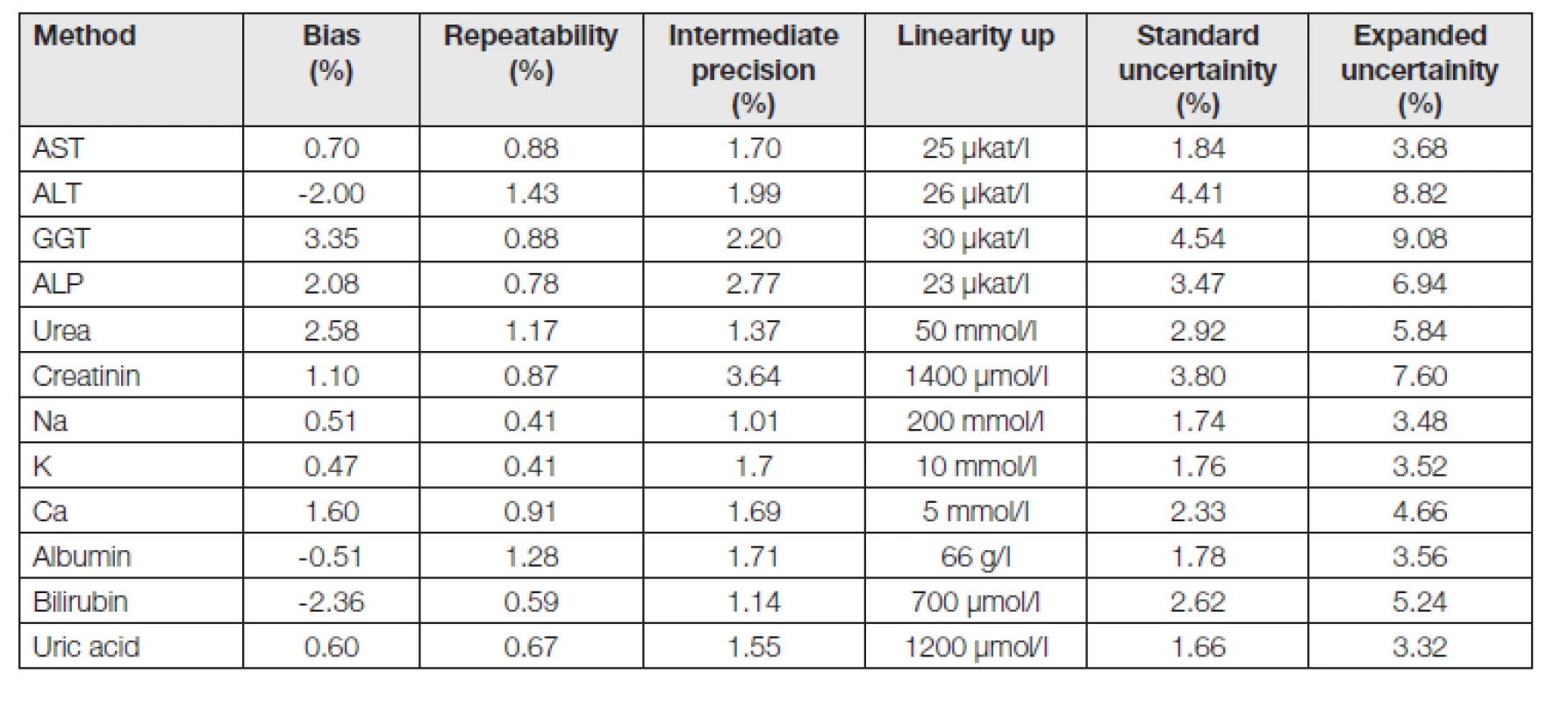
Měření proběhla na analyzátoru ADVIA 1800 (Siemens Healthcare, Tarrytown, USA) za použití určených kitů od stejného výrobce. V Tabulce 1 je přehled použitých kitů, v Tabulce 2 kalibrátory a jejich metrologická návaznost, v Tabulce 3 jsou analytické parametry metod získané při jejich verifikaci provedené dle platného doporučení [30].
1. Overwiev of the used methods 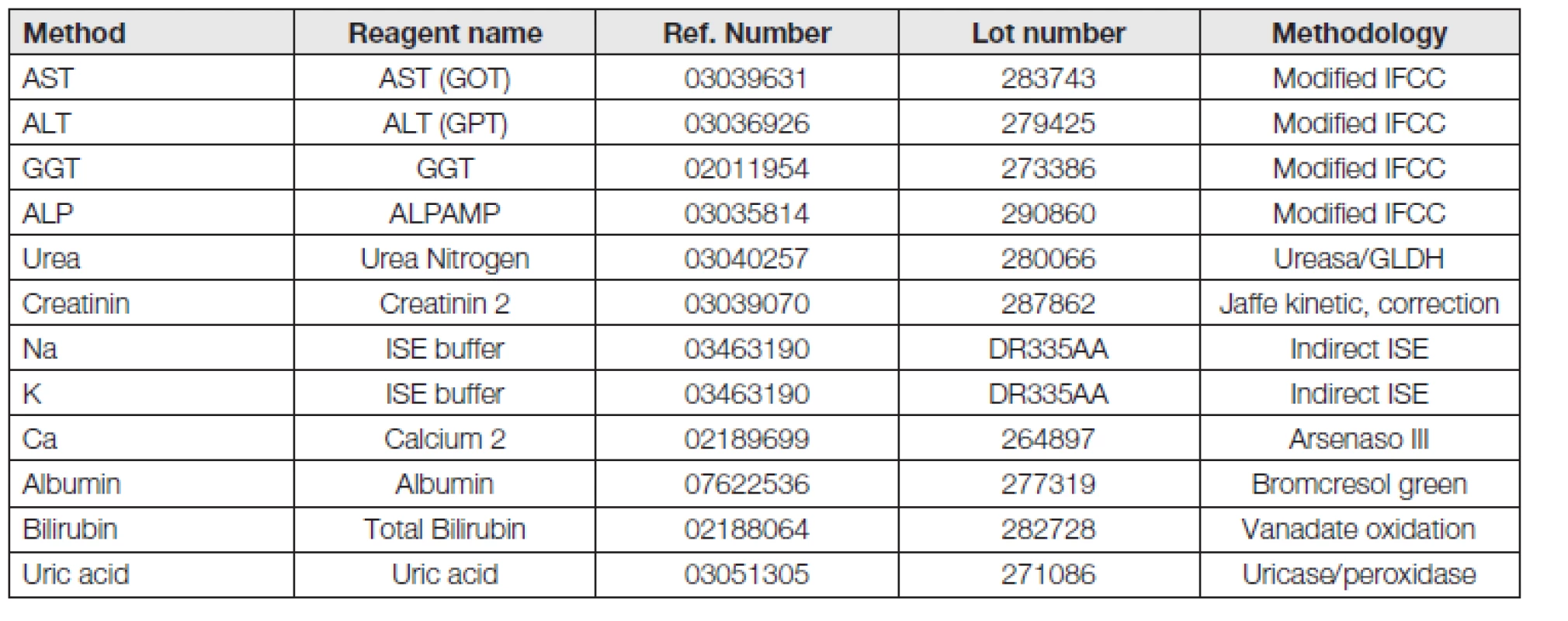
2. Calibration 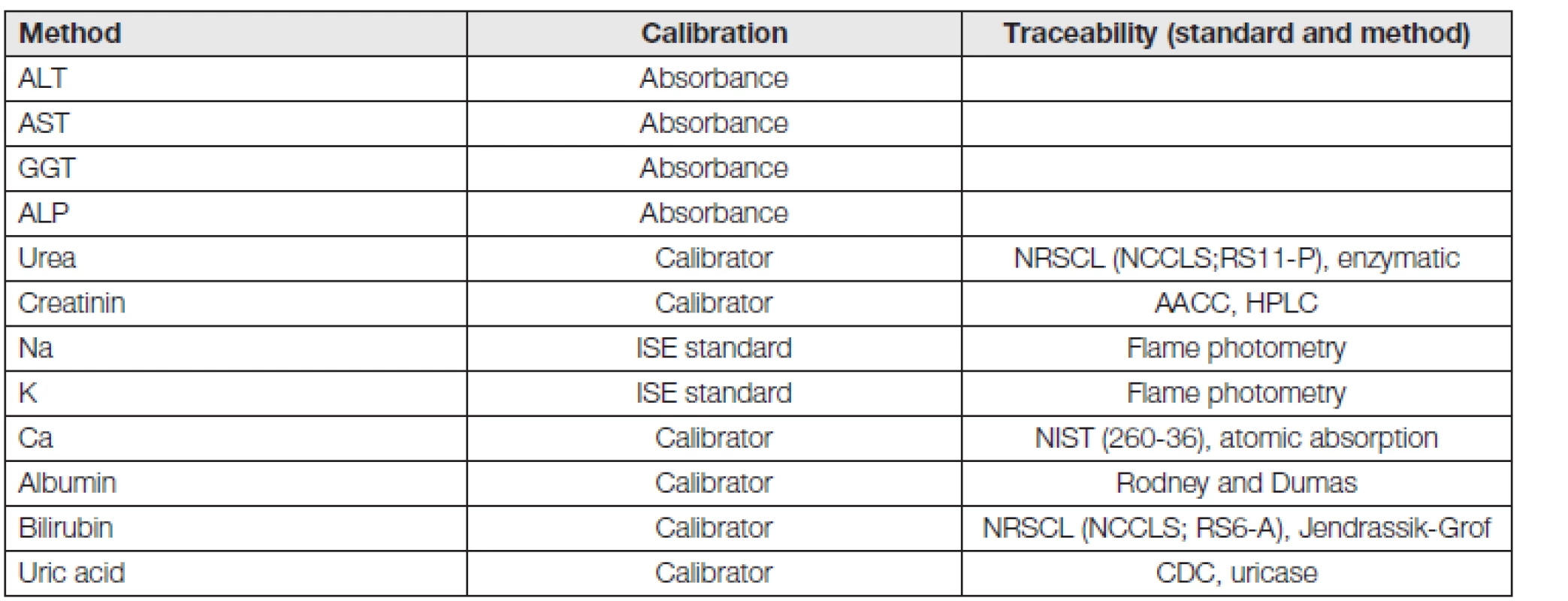
Remark: Calibrator - Chemistry Calibrator, produced by Siemens Healthcare, ref. 09784096 Pro statistické vyhodnocení byla použita neparametrická metoda pro určení horní a dolní meze referenčního intervalu (97,5. a 2,5. percentil). Jde o shodný postup se studií NORIP.
Výsledky a diskuse
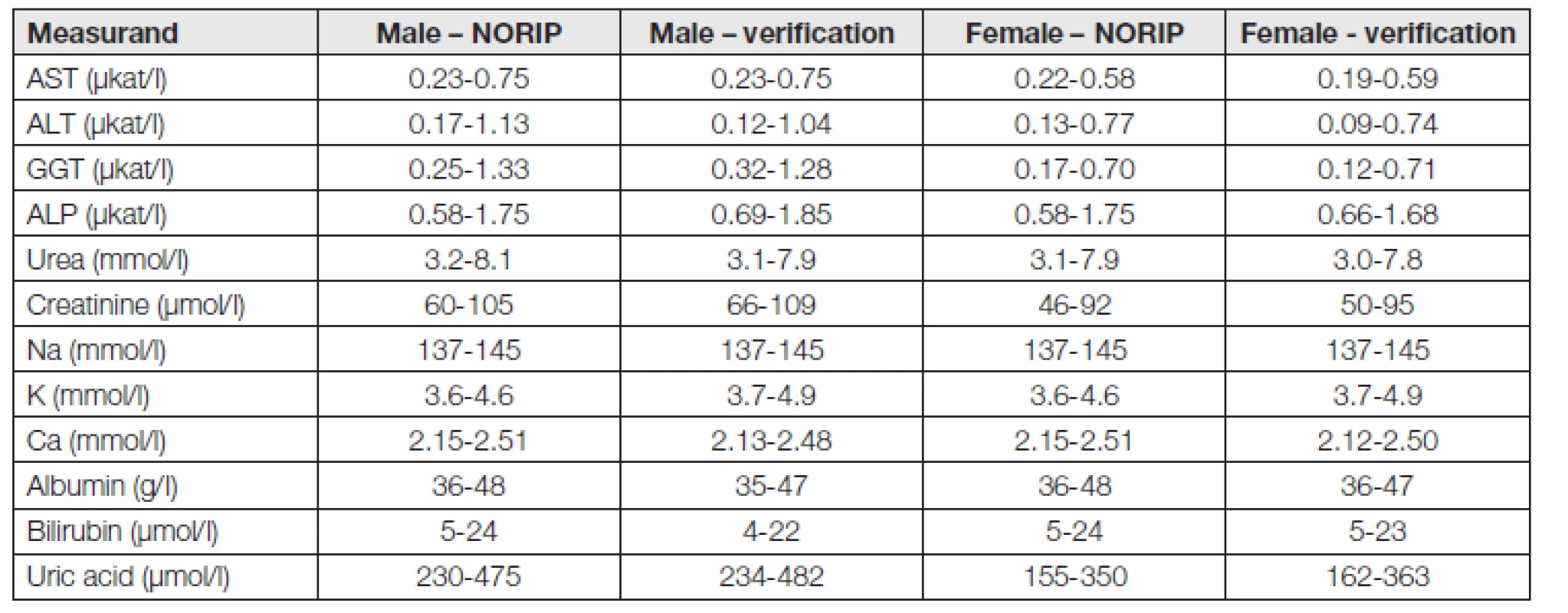
Ověřené referenční intervaly a hodnoty ze studie NORIP pro sérum jsou uvedeny v Tabulce 4. Odchylky od mezí v % a příslušné TEa [31] získané z biologických variabilit jsou uvedeny v Tabulce 5 pro muže a v Tabulce 6 pro ženy.
5. Limit diferencess and TEa – male 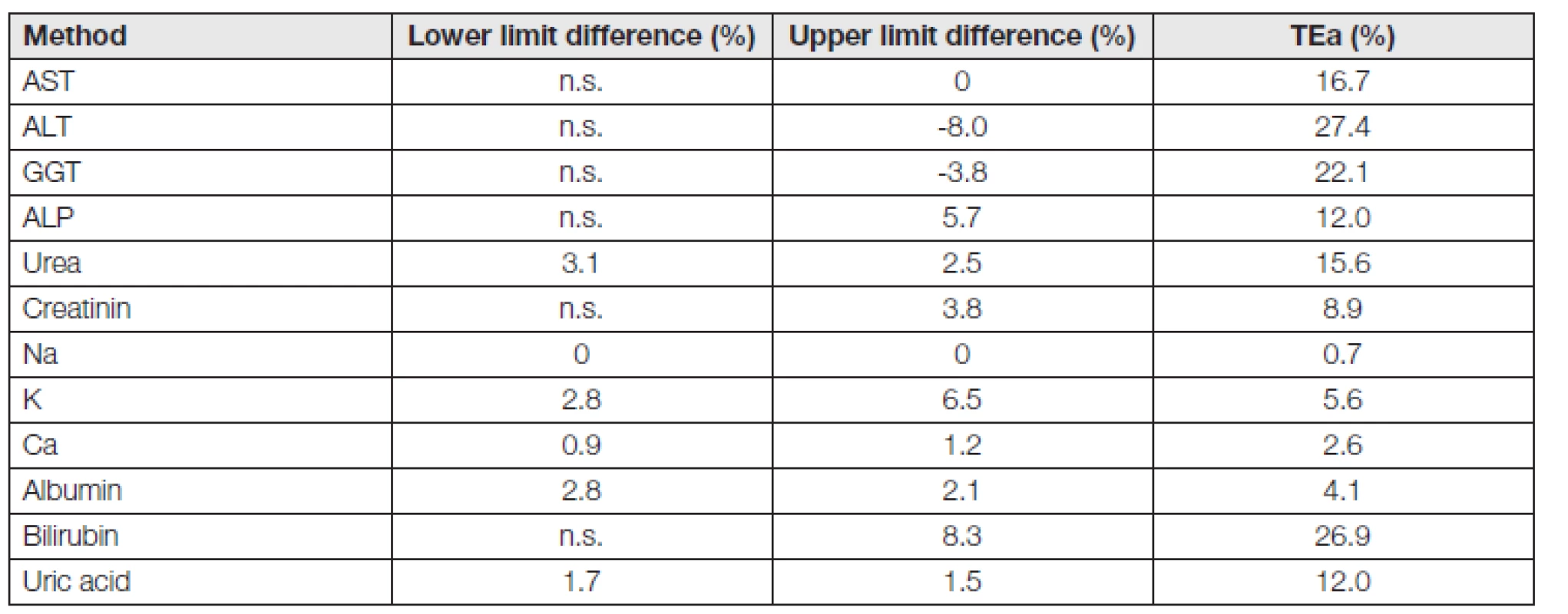
n.s. – clinical non significant 6. Limit diferencess and TEa – female 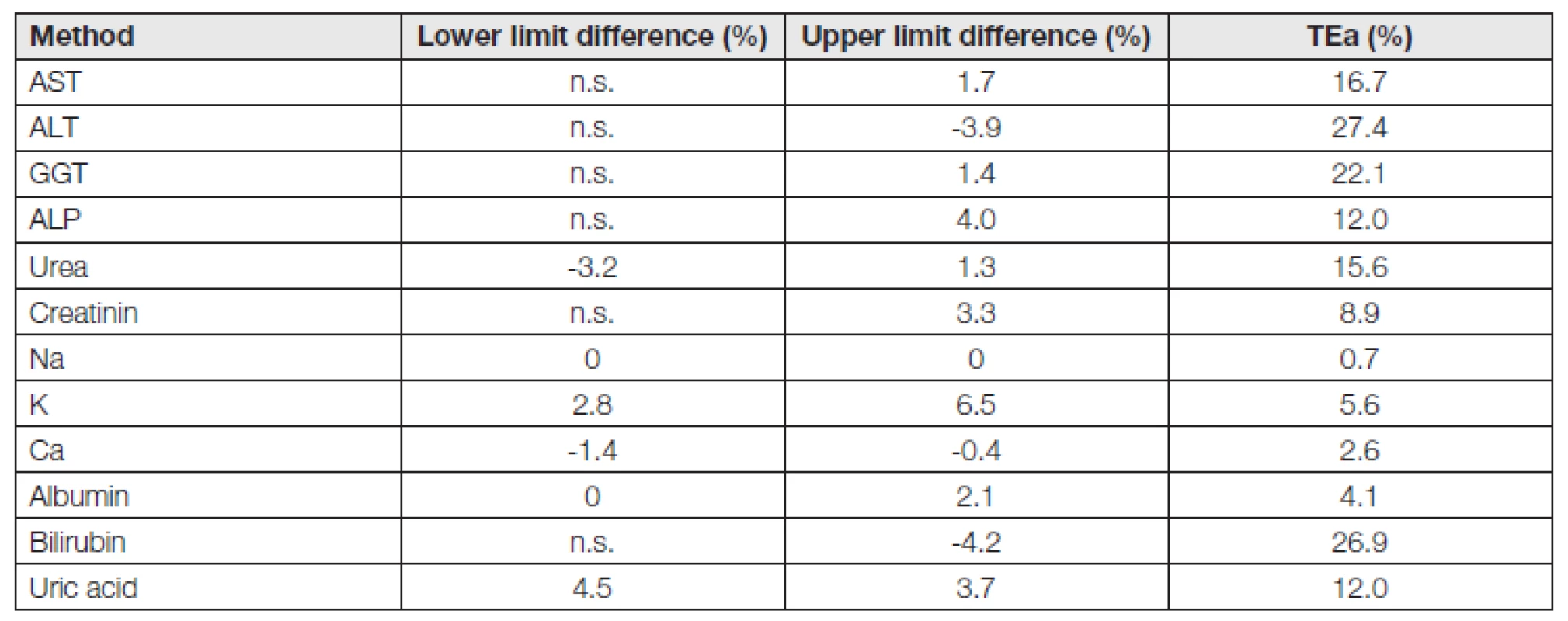
n.s. – clinical non significant Z výsledků je patrné, že u většiny ověřovaných metod v séru jsou výsledky téměř stejné či velmi podobné. U enzymů (AST, ALT, GGT a ALP), kde nás prakticky zajímá horní hranice referenčního intervalu (dolní hranice je z lékařského hlediska nevýznamná), je odchylka od 0 % (AST muži) po maximálně 8 % (ALT muži). I u ostatních metod se pohybují hranice referenčních intervalů od úplné shody (Na) po odchylky minimální. Z toho je patrné, že lze výsledky studie NORIP využít i v našich laboratořích. Případné problémy vznikající porovnáním s dosud používanými referenčními intervaly (hodnoty ALT a K) jsou dále diskutovány.
Pokud porovnáme odchylku našich výsledků od studie NORIP s TEa, je tato hodnota překročena pouze u horní hranice pro draselné ionty (výše zmíněn další rozbor).
Při porovnání s údaji publikovanými v učebnici Tietz Textbook of Clinical Chemistry and Molecular Diagnostics [32] najdeme řadu odchylek. Pro enzymy mimo ALP a pro bilirubin je zde používána pouze horní hranice referenčního intervalu. Shodné výsledky či odchylky do 10 % najdeme u Ca, Na, kreatininu, urey a kyseliny močové. U většiny enzymů jsou zde uvedené hodnoty nižší (ALT, AST, GGT), pouze pro ALP uvádí Tietzova učebnice vyšší hodnoty. To platí i pro bilirubin a albumin. Pro koncentraci draslíku v séru se naše hodnoty blíží údajům v Tietzově učebnici pro sérum, hodnoty ze studie NORIP spíše odpovídají hodnotám, uvedeným v Tietzově učebnici pro plazmu.
Při diskusích s kolegy na různých pracovištích v rámci naší sítě zdravotnických zařízení v ČR se intenzivně řešil problém, kdy někteří kolegové měli dojem, že navrhované hodnoty pro horní mez katalytické koncentrace jaterních enzymů (především ALT) jsou nízké a že v regionu bude mít příliš osob zvýšené hodnoty (tedy hodnoty vyšší než je horní mez referenčních intervalů). Toto tvrzení bylo sice relativně správné, ale podle našeho názoru pouze ukazuje a potvrzuje chybné nastavení referenčních intervalů v uvedených laboratořích. V žádném případě totiž nelze podle určité subpopulace měnit referenční intervaly pro zdravou populaci.
Dalším problematickým analytem, kolem kterého se vedla mnohaměsíční a často ostrá diskuse byla referenční mez pro stanovení koncentrace draslíku v séru. Zde se totiž zrcadlí především problém preanalytické fáze. Ve studii NORIP byly vzorky buď ihned změřeny, nebo okamžitě zmraženy na -80°C. Výsledky v tomto případě byly totožné pro sérum a plazmu. Hodnoty uvedené v Tietzově učebnici se významně liší pro sérum (3,5-5,1 mmol/l) a pro plasmu (3,4-4,4 mmol/l). Je možné a pravděpodobné, že zde došlo k prodlení od odběru do vlastní analýzy. Námi naměřené hodnoty se pohybují mezi koncentracemi zjištěnými v rámci studie NORIP a koncentracemi doporučenými v Tietzově učebnici. Měření kalémie v našem projektu neproběhlo bezprostředně, ale s minimálním zpožděním. Stojíme tedy před problémem, zdali akceptovat vliv preanalytické fáze, mnohdy i časově dlouhý interval mezi odběrem, centrifugací a měřením, nebo akceptovat skutečné referenční intervaly s tím, že může dojít ke zkreslení výsledků transportem.
Z uvedených důvodů jsme ověřovali procentuální zastoupení výsledků vyšších než hodnoty 4,6 mmol/l v séru ve dvou našich největších laboratořích, Laboratoře Agel a.s. a OLM (Oddělení laboratorní medicíny) Středomoravské nemocniční a.s. Tyto laboratoře provádí vyšetření ve větším zastoupení od ambulantních lékařů a vzorky sváží z Moravských regionů podle zásad správné laboratorní praxe. Opakovaným ověřením jsme zjistili, že hodnoty kalémie vyšší než uvedená referenční mez nalézáme u méně než 10 % vyšetřovaných. Jelikož nám nejsou známa komplexní anamnestická a klinická data, můžeme jen konstatovat, že počet testovaných osob s kalémií vyšší než horní mez referenčního intervalu významně nepřevyšoval (méně než 2% nárůst) počet klientů s hyperkalémií hodnocenou dle dřívějšího algoritmu (horní hranice referenčního intervalu 5,1 mmol/l). Zde jen pro zajímavost uvádíme, že v uvedených laboratořích jsou prováděna vyšetření pro řadu nefrologických pacientů a řadu pracovišť, kde jsou osoby léčené dialýzou.
Studie NORIP byla však zaměřená na klasické biochemické a hematologické metody. Hematologické referenční meze, referenční meze lipoproteinů, glykémie a HbA1c jsme sjednotili podle národních doporučení.
Jako problém se zatím jeví sjednocení referenčních mezí v imunochemii. Abychom to mohli provést, musíme zcela sjednotit používanou techniku, což je nyní naším cílem. V imunochemii tedy zatím využíváme jako referenční meze údaje výrobců s cílem omezení jejich počtu v našich laboratořích. Tyto údaje ověřujeme pravidly podle Westgarda [13].
Současně se chystáme ověřit některé údaje, podle kterých jsme připravili referenční rozmezí pro dětskou populaci a populaci seniorů nad 65 let věku [33,34].
Závěr
Naše práce prokázala možnost využití výsledků studie NORIP pro dospělou populaci v rámci České republiky. Na bázi ověřování jsme se rozhodli použít referenční intervaly pro dospělou populaci z této studie jako sjednocené referenční intervaly v síti laboratoří společnosti AGEL a.s. a to nejen pro ve studii ověřené, ale i pro ostatní metody. Domníváme se, že je to nezbytné řešení, které pomůže sjednotit a zefektivnit interpretaci výsledků a následné léčebně terapeutické rozhodování. Současně se domníváme, že by bylo záslužné využití identických referenčních intervalů pro uvedené základní analyty v rámci měst, regionů či celého státu. Sjednocování referenčních mezí pro metody s dostatečnou metrologickou návazností a analytickou kvalitou je jedním z úkolů a snah současné laboratorní medicíny
Na druhou stranu nesmíme při současné migraci osob opomenout vliv rasy na referenční intervaly. To zatím v našich oblastech zcela opomíjíme. Stejně tak, jak již bylo zmíněno, je problémem práce s referenčními intervaly u starší populace. Spolu se zvyšováním věku dožití se jeví nutností i v gerontologii třídit referenční intervaly podle věku.
Cílem práce nebylo věnovat se teorii referenčních intervalů, ale prakticky ověřit, zda lze sjednocovat referenční intervaly na bázi dostupných velkých studií. A ukázalo se, že touto cestou lze postupovat.
Do redakce došlo 24. 4. 2014
Adresa pro korespondenci:
Ing. Luděk Šprongl
Centrální laboratoř
Šumperská nemocnice a.s.
Nerudova 640/41
787 52 Šumperk
e-mail: ludek.sprongl@sun.agel.cz
Sources
1. Rustad, P. et al. The Nordic Reference Interval Project 2000: recommended reference intervals for 25 common biochemical properties. Scand. J. Clin. Lab. Invest., 2004, 64, p. 271-84
2. Wootton, I., King, E., Smith, J. The quantitative approach to hospital biochemistry. Br. Med. Bull., 1951, 7, p. 307-11
3. Wootton, I. Individual variation. Proc. Nutr. Soc., 1962, 21, p. 129-35
4. Belk, W., Sunderman, F. A survey of chemical analyses in clinical laboratories by William P. Belk and F. William Sunderman, Arch. Pathol. Lab. Med., 1988, 112(4), p. 320-6
5. Hofman, R. Statistics in the practice of medicine, JAMA 1963, 185, p. 864-73
6. Murphy, E., Abbey, H. The normal range: A common misuse, J. Chronic. Dis. 1967, 20, p. 79-88
7. Sunderman, F. J. Current concepts of „normal values“, „reference values“ and „discrimination values in clinical chemistry, Clin. Chem., 1975, 25 (8), p. 1873-7
8. Grasbeck, R. et al. Provisional recomendation on theory of reference values. Part1. The concept of reference values. Clin. Chem., 1979, 25 (8), p. 1506-8
9. PetitClerc, C., Solberg, H. E. International Federation of Clinical Chemistry. Approved recomandation on theo-ry of reference values. J. Clin. Chem. Biochem., 1987, 25, p. 639-644
10. CLSI. How to Define and Determine Reference Intervals in the Clinical Laboratory. Approved Guideline – Se-cond Edition. CLSI documnet C28-A2. Wayne PA: CLSI, 2000
11. Ceriotti, F. Prerequisites for use of common reference intervals, Clin. Biochem. Rev., 2007, 28, p. 115-121
12. Ichihara, K., Boyd, J. C. An appraisal of statistical procedures used in derivation of reference intervals. Clin. Chem. Lab. Med., 2010, 48 (11), p. 1537-1551
13. Westgard, J. O. Basic Method Validation, Westgard QC, 2008, p. 177-186
14. Müller M. M. Implementation of reference systém in laboratory medicine. Clin. Chem. 2000, 46, s. 1907-9
15. Panteghini, M. Traceability, Reference Systems and Result Comparability. Clin. Biochem. Rev., 2007, 28, p. 97-104
16. www.bipm.org/jctlm/
17. Petersen, P. H., Jensen E. A., Branslund I. Analytical performance, reference values and decision limits. A need to differentiate between reference intervals and decision limits and to define analytical quality specifications. Clin. Chem. Lab. Med., 2012, 50 (5), p. 819-831
18. Hawkins, R. C., Badrick, T. Reference interval studies: what is the maximum number of samples recommen-ded? Clin. Chem. Lab. Med., 2013, 51 (11), p. 2161-2165
19. Henny, J. Multicenter reference interval studies: a pro-mising perspective for the future? Clin. Chem. Lab. Med., 2013, 51 (7), p. 1335-1338
20. Katayev, A., Balzica, C., Seccombe, D. W. Establishing reference intervals for clinical laboratory test results: is there a better way? Am. J. Clin. Pathol., 2010, 133 (2), p. 180-186
21. Panteghini, M., Ceriotti, F. Obtaining reference intervals traceable to reference measurement systems: is it possible, who is responsible, what is strategy? Clin. Chem. Lab. Med., 2012, 50 (5), p. 813-817
22. Siest, G., Henny, J., Gräsbeck, R. et al. The theory of reference values: an unfinished symphony. Clin. Chem. Lab. Med., 2013, 51 (1), p. 47-64
23. Plebani, M., Lippi, G. Reference values and the journal: why the past is now present. Clin. Chem. Lab. Med., 2012, 50 (5), p. 761-763
24. Yamamoto, I., Hosogaya, S., Osawa, S. et al. Nationwide multicenter study aimed to establishment of common reference intervals for standardized clinical laboratory tests in Japan. Clin. Chem. Lab. Med., 2013, 51 (8), p. 1663-1672
25. Ichihara, K., Ceriotti, F., Tam, T. H. Tha Asian project for collaborative derivation of reference intervals: strategy and major results of standardized analytes. Clin. Chem. Lab. Med., 2013, 51 (7), p. 1429-1442
26. Pineda-Tenor, D., Laserna-Mendieta, E. J., Timón-Zapata, J. et al. Biological variation and reference change values of common clinical chemistry and haematologic laboratory analytes in the elderly population. Clin. Chem. Lab. Med., 2013, 51 (4), p. 851-862
27. Hilsted, L., Rustad, P., Aksglaede, L., Sørensen, K., Juul A. Recommended Nordic paediatric reference intervals for 21 common biochemical properties. Scand. J. Clin. Lab. Invest., 2013, 73 (1), p. 1-9
28. Daly, Ch., Liu, X., Grey, V. K. L., Hamid, J. S. A systematic review of statistical methods used in constructing pediatric reference intervals. Clin. Biochem., 2013, 46 (13-14), p. 1220-1227
29. Shaw, J. L., Binesh-Marvasti, T., Colantiano, D., Adeli, K. Pediatric reference intervals: challenges and recent initiatives. Crit. Rev. Clin. Lab. Sci., 2013, 50 (2), p. 37-50
30. Friedecký, B., Šprongl, L., Kratochvíla, J., Plzák, Z. Doporučení k provádění validace a verifikace analy-tických metod v klinických laboratořích. Klin. Biochem. Metab., 2011, 19 (1), p. 36 - 44
31. www.westgard.com
32. Burtis, C. A., Ashwood, E. R., Bruns, E.D. Tietz Textbook of Clinical Chemistry and Molecular Diagnostic, 2006, Elsevier Inc., St. Louis, ISBN 0-7216-0189-8
33. Soldin, J. S., Wong, E. C., Brugnara, C., Soldin, P.O. Pediatric Reference Intervals, 7th Edition, 2011, AACC Press, ISBN 9871594251017
34. Faulkner, R. W., Meites, S. Geriatric Clinical Chemistry, 1993, AACC Press, ISBN 9780915274659 Müller, M. M. Implementation of reference systém in laboratory medicine. Clin. Chem., 2000, 46, p. 1907-9
Labels
Clinical biochemistry Nuclear medicine Nutritive therapist
Article was published inClinical Biochemistry and Metabolism

2014 Issue 3-
All articles in this issue
- Positive association of adiponectin with adipocyte fatty acid binding protein in patients with unfavourable dyslipidemic phenotype
- Quality requirements for the determination of glycated hemoglobin HbA1c and possibilities of its application for diagnostic purposes
- Unification and validation of reference intervals – pilot study
- Comparison of creatinine clearance and estimated glomerular filtration rate in patients with chronic kidney disease
- Clinical Biochemistry and Metabolism
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Comparison of creatinine clearance and estimated glomerular filtration rate in patients with chronic kidney disease
- Unification and validation of reference intervals – pilot study
- Quality requirements for the determination of glycated hemoglobin HbA1c and possibilities of its application for diagnostic purposes
- Positive association of adiponectin with adipocyte fatty acid binding protein in patients with unfavourable dyslipidemic phenotype
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career