-
Medical journals
- Career
Diferenciální diagnostika hyponatremie
: J. Čáp
: IV. interní hematologická klinika LF UK a FN Hradec Králové
: Kardiol Rev Int Med 2015, 17(2): 178-180
: Internal Medicine
Hyponatremie se vyskytuje v klinické praxi často. Článek shrnuje základní mechanizmy regulace natremie a příčiny poklesu hladiny sodíku v séru. Je uveden diagnostický postup při zjištění hyponatremie a základní principy její terapie na základě současných guidelines a literatury.
Klíčová slova:
hyponatremie – diferenciální diagnóza – léčba
Sodík je hlavním faktorem určujícím osmolalitu extracelulární tekutiny. Protože voda může volně přecházet přes stěnu buněk, zvýšení osmolality vede k buněčné dehydrataci a její snížení k otoku buněk. Rychlý pokles osmolality vede k cytolýze. Další klinicky významnou osmoticky aktivní látkou, která nemůže volně přecházet do buněk, je glukóza.
Regulace osmolality, resp. natremie, je dána především regulací příjmu a výdeje vody. Osmoreceptory v hypotalamu jsou velmi citlivé na změnu osmolality a normálně zastaví sekreci antidiuretického hormonu (ADH) a pocit žízně při natremii pod 135 mmol/ l. To vede k vyloučení bezsolutové vody ledvinami a ke korekci natremie. K útlumu sekrece ADH nedojde, pokud je stimulována podněty presorickými (při nízkém tlaku) a objemovými (při intravaskulární hypovolemii např. při terapii srdečního selhání či jaterní cirhózy s ascitem diuretiky). Podmínkou útlumu je také normální sekrece kortikoidů. Vylučování sodíku močí je naopak do značné míry nezávislé na hladině sodíku v séru a je dáno především objemem intravaskulární tekutiny. Při hypovolemii se aktivuje systém renin‑angiotenzin‑aldosteron a vylučování sodíku klesá. Při expanzi objemu je naopak tato osa utlumena, je zvýšena hladina natriuretických faktorů, které vedou ke ztrátám sodíku [1].
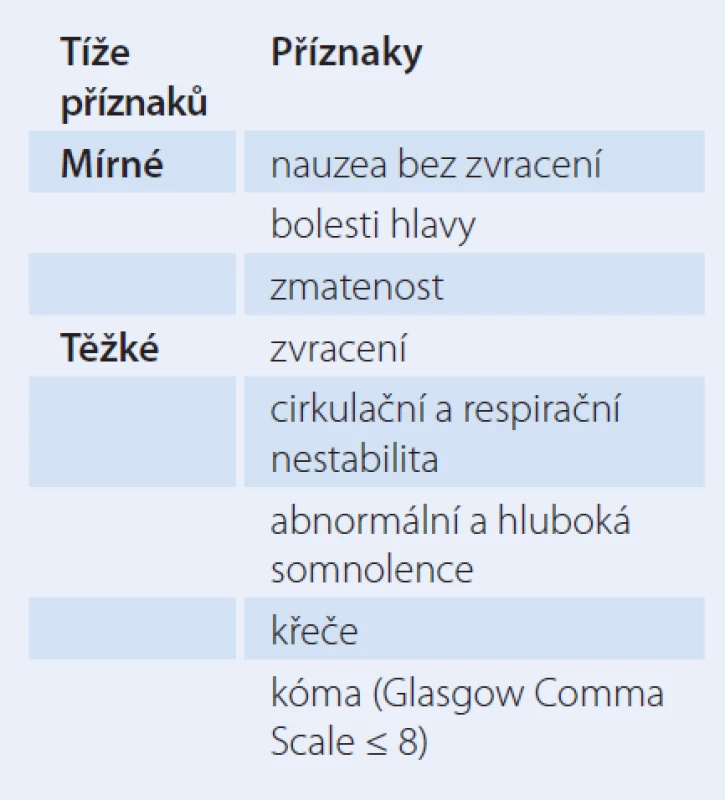
Hyponatremie je v klinické praxi častá. Vyskytuje se až u 30 % hospitalizovaných nemocných [2]. Většinou je mírná a asymptomatická. Příznaky hyponatremie závisí jednak na jejím stupni, ale hlavně na rychlosti jejího vzniku. Pokles osmolality vede ke zvětšení všech buněk v těle, příznaky jsou ale hlavně v důsledku postižení mozku – tedy neurologické. Podle recentních guidelines Evropské endokrinologické společnosti [3] se dělí na mírné a těžké (tab. 1).
I těžká hyponatremie může být asymptomatická. Buňky se totiž dokáží přizpůsobit během 24 – 48 hod poklesu osmolality zevního prostředí snížením koncentrace osmoticky aktivních látek v buňkách. Jde zejména o neionogenní osmoly – glutamát, taurin a myo ‑ inositol, které vystupují z buněk otevřením kanálů citlivých na objem buňky a dochází ke snížení expresi aktivních transportérů těchto látek do buňky. Nová syntéza transportérů může trvat až týden [4]. Astrocyty, které tvoří hematoencefalickou bariéru, dokáží mezibuněčným transportem rychle přijmout taurin z neuronů, takže chrání jejich objem, zatímco samy zduří. Během 24 hod se jejich objem postupně normalizuje vyplavením organických osmolů. Pokud potom dojde k rychlé korekci hyponatremie, podléhají astrocyty apoptóze s následnou poruchou hematoencefalické bariéry a demyelinizací [5].
Příčiny hyponatremie
Pseudohyponatremie
Je falešně nízká hladina sodíku zjištěná ve vzorku séra s vysokým obsahem lipidů nebo bílkovin. Při použití iontově selektivních elektrod je nyní méně častá. Osmolalita séra je normální.
Změna nastavení osmostatu
Je přítomna mírná hyponatremie, útlum sekrece adiuretinu nastává při nižší hladině sodíku, ale potom je normální. Fyziologicky je přítomen tento stav v těhotenství, kdy natremie bývá o 4 – 5 mmol/ l nižší.
Izotonická a hypertonická hyponatremie
Ne každá hyponatremie je spojena s hypoosmolalitou séra. Je‑li v séru vysoká hladina osmoticky aktivní látky, která volně neproniká do buněk (glukózy), je osmolalita normální nebo zvýšená. Přestup vody z nitrobuněčného prostoru způsobí diluční hyponatremii. Močovina volně prostupuje přes buněčnou stěnu, při renální insuficienci je proto přítomna hyperosmolalita séra, ale ne hyponatremie.
Hypotonická hyponatremie se snížením objemu extracelulární tekutiny
Jak bylo uvedeno výše, adiuretin je stimulován kontrakcí objemu i při snížené osmolalitě séra. Je to nepřiměřené vzhledem k osmolalitě, ale napomáhá to udržení intravaskulárního objemu. Ztráty tekutiny mohou být gastrointestinálním traktem. Při průjmech je koncentrace sodíku v moči velmi nízká, při ztrátách zvracením může být vyšší, protože alkalóza vede k vylučování bikarbonátu, který je doprovázen sodíkem. Ztráty kůže přicházejí při popáleninách (pomineme‑li cystickou fibrózu se ztrátou sodíku).
Ztráty močí jsou principem diuretické léčby. Hyponatremie častěji přichází po thiazidových diureticích a je obtížně vysvětlitelná jen kontrakcí objemu. Je možné, že thiazidy stimulují ADH [6]. Kličková diuretika působí hyponatremii vzácně, protože snižují koncentrační schopnost ledvin. Hypovolemie a ztráty sodíku močí jsou příčinou hyponatremie při nedostatku aldosteronu u primární insuficience nadledvin. Ztráty močí jsou samozřejmě možné při onemocněních ledvin (tubulární léze po chemoterapii, analgetická nefropatie, medulární cysty ledvin). Takzvané mozkové ztrácení sodíku (Cerebral salt wasting syndrome) bylo popsáno u onemocnění CNS jako u subarachnoidálního krvácení. Není jasné, zda je onemocnění způsobeno vyplavením mozkového natriuretického faktoru.
Ztráty do třetího prostoru mohou nastat při ileu, pankreatitidě, sepsi, po úrazu svalu.
Hypotonická hyponatremie s normálním objemem extracelulární tekutiny
Příčinou je diluční hyponatremie při poruše schopnosti ledvin vyloučit vodu v důsledku nepřiměřené sekrece ADH nebo nízkého příjmu sodíku.
Nejčastější je syndrom nepřiměřené sekrece ADH (SIADH). Vyskytuje se často u nádorů, zánětlivých afekcí mozku, plic, cévních příhod CNS a po řadě léků včetně opiátů, valproátu, karbamazepinu, některých antidiabeticích, antipsychoticích a antidepresivech. Jako příčina se také udávají anestezie, stres a zvracení. Často příčinu nezjistíme. Při kontinuální sekreci ADH se retinuje voda, mírně se zvýší extracelulární objem, ale postupně dochází k úniku z účinku ADH v důsledku sekrece natriuretických faktorů a suprese osy renin‑angiotenzin‑aldosteron (což zhoršuje hyponatremii zvýšením ztrát sodíku). Dochází také k downregulaci V2 receptorů a aquaporinu ‑ 2 v ledvinách [7].
Diagnostická kritéria se od dob prvního popisu v roce 1957 [8] prakticky nezměnila a jsou uvedena v tab. 2 (převzato z [3]). Jde vždy o diagnózu per exclusionem.
2. Diagnostická kritéria SIADH. 
Vysoký příjem vody vede k polyurii, psychogenní polydipsie většinou nepůsobí hyponatremii vzhledem ke schopnosti ledvin vyloučit okolo 20 l vody denně. Podmínkou této schopnosti je ovšem přítomnost minerálů. Protože v pivu je obsah sodíku malý, byla hyponatremie popsána u pijáků piva.
Hypotonická hyponatremie se snížením objemu extracelulární tekutiny
Hyponatremie se vyskytuje u 20 – 30 % nemocných se srdečním selháním NYHA III a IV [9] a je častá u nemocných s jaterní cirhózou a ascitem [10]. Stupeň hyponatremie v obou případech koreluje s mortalitou, ale není jasné, zda se na ní podílí nebo je jen ukazatelem těžšího postižení. Příčinou hyponatremie je snížení efektivního intravaskulárního objemu se stimulací ADH a uplatňuje se také léčba diuretiky. Podobným mechanizmem vzniká hyponatremie u nefrotického syndromu.
Diferenciální diagnóza
U nemocného s nízkou hladinou sodíku vyšetříme na prvním místě osmolaritu séra, která by měla být nízká (obr. 1). Je‑li normální nebo dokonce zvýšená, jsou přítomny jiné osmoticky aktivní látky – glukóza (diabetes) nebo močovina (renální insuficience). Současně zjistíme osmolaritu moči. Je‑li přiměřeně nízká (pod 100 mosmol/ kg) jde o nadměrný přísun tekutiny u pijáků piva nebo psychogenní polydipsii. Při nepřiměřeně zvýšené osmolaritě moči je stěžejním krokem posoudit efektivní intraarteriální objem krve (vyloučit objemovou stimulaci ADH). K tomu slouží hladina sodíku v moči, která je při objemové kontrakci nízká a při expanzi, včetně SIADH, vyšší – nad 30 mmol/ l. Obtížné je to posoudit při terapii diuretiky a spolehlivější se ukázala frakční exkrece kyseliny močové (při expanzi objemu > 12 %) [11]. Jsou‑li sodík v moči a exkrece kyseliny močové nízké, jde o kontrakci efektivního arteriálního objemu krve bez ohledu na to, je‑li přítomno převodnění (srdeční selhání, ascites) nebo ne (průjmy, diuretika, cerebrální ztrácení sodíku). Frakční exkreci vypočteme z koncentrace kyseliny močové ve vzorku moči (U_KM) a v séru (S_KM), známe‑li současně koncentraci kreatininu v séru (S_kreat) a v moči (U_kreat), podle vzorce:
1. Diferenciální diagnostika hyponatremie. 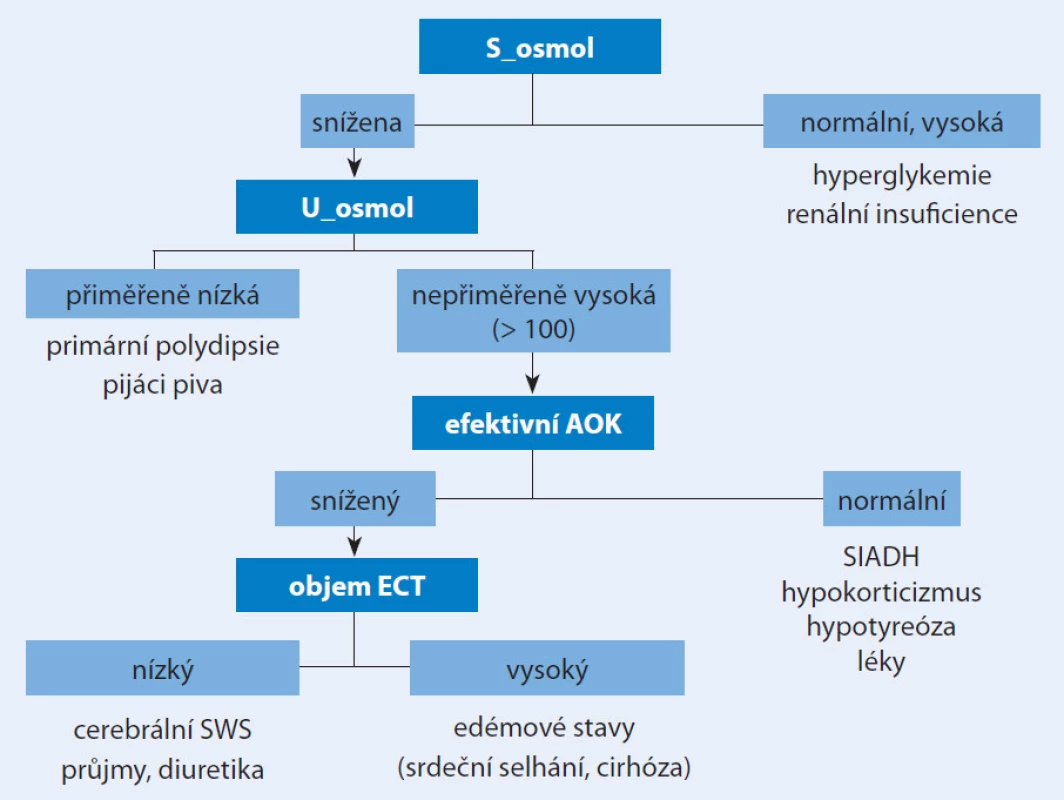
S_osmol – osmolarita séra, U_osmol – osmolarita moči, AOK – arteriální objem krve, ECT – extracelulární tekutina, SWS – salt wasting syndrome Léčba
Klinických guidelines byla publikována celá řada [12], v roce 2014 Evropskou endokrinologickou společností [3] a v roce 2015 v USA [1]. Jakkoli se v detailech liší, základním principem léčby je předpoklad, že hyponatremie, která působí výrazné klinické příznaky (zvracení, křeče, poruchu vědomí), trvá zřejmě krátkou dobu a je ji potřeba rychle korigovat, protože nebezpečí fatálního otoku mozku převyšuje hrozbu demyelinizace. Je doporučováno podat 100 – 150 ml 3% NaCl (tedy u nás nejlépe 3 × 10 ml ampule 10% NaCl do 100 ml F1/ 1)po dobu 20 min. Tato infuze se opakuje tak dlouho, dokud buď neodezní klinické příznaky, nebo nestoupne natremie o 5 mmol/ l za 6 hod [1], evropská guidelines dovolují 10 mmol/ l za 24 hod [3]. Vždy se infuze ukončuje při zmírnění příznaků a při vzestupu natremie na 130 mmol/ l. Zanedbáme‑li renální ztráty vody, potom podání 1 ml 3% NaCl na kg hmotnosti pacienta zvýší natremii o 1 mmol/ l [13]. Je však důrazně doporučeno neřídit se výpočty, ale častou kontrolou natremie. Rychlá korekce hyponatremie vede k myelinolýze. Dojde k ní poměrně často, a to proto, že příčina retence vody ustoupí a nemocný vyloučí rychle velké množství vody. Je doporučeno nepřekročit první den vzestup natremie o 10 mmol/ l Na+ a druhý den o 8 mmol/ l.
Proto bylo doporučeno používat při korekci těžké hyponatremie současně infuzi 3% NaCl a podání desmopressinu [14]. Tento postup není všeobecně přijat, ale v guidelines se zdůrazňuje, že při překročení tohoto limitu korekce hyponatremie se má podat voda a event. i desmopressin, aby se rychlý pokles Na+ korigoval.
Další postup jakož i léčba asymptomatické hyponatremie se řídí příčinou. Při dehydrataci podáme fyziologický roztok. Je‑li však naopak přítomen SIADH, fyziologický roztok vede k poklesu natremie. Pokud je součet koncentrace sodíku a draslíku v moči vyšší než 150 mmol/ l, není naděje, že bychom zkorigovali hyponatremii fyziologickým roztokem.
V terapii SIADH zůstává na prvním místě restrikce tekutin na 800 – 1 000 ml denně, což vede během několika dnů k váhovému úbytku 2 – 3 kg a k normalizaci natremie a výdeje sodíku močí (neadekvátní sekrece ADH se stane adekvátní nízkému příjmu vody). Pokud nemocný nedokáže příjem vody omezit, pomůže Furosemid. Účinné jsou inhibitory vazopresinového receptoru V2 – tolvaptan, conivaptan, lixivaptan. U chronického srdečního selhání tyto léky efektivně upravily natremii, ale nezlepšují přežití nemocných [15,16].
Závěr
Hyponatremie je v klinické praxi častá. Závažná a zejména rychle vzniklá vyžaduje urgentní léčbu, ale rychlá korekce naopak často způsobí poškození nemocného – myelinolýzu. Základní principy její diagnostiky a terapie by měl proto ovládat každý internista.
Doručeno do redakce: 6. 3. 2015
Přijato po recenzi: 2. 4. 2015
prof. MU Dr. Jan Čáp, CSc.
www.lfhk.cuni.cz
capj@lfhk.cuni.cz
Sources
1. Sterns RH. Disorders of plasma sodium – causes, consequences, and correction. N Engl J Med 2015; 372 : 55 – 65. doi: doi:10.1056/ NEJMra1404489.
2. Upadhyay A, Jaber BL, Madias NE. Epidemiology of hyponatremia. Semin Nephrol 2009; 29 : 227 – 238. doi: 10.1016/ j.semnephrol.2009.03.004.
3. Spasovski G, Vanholder R, Allolio B et al. Clinical practice guideline on diagnosis and treatment of hyponatraemia. Eur J Endocrinol 2014; 170: G1 – G47. doi: 10.1530/ EJE ‑ 13 ‑ 1020.
4. Strange K. Cellular volume homeostasis. Adv Physiol Educ 2004; 28 : 155 – 159.
5. Gankam Kengne F, Nicaise C, Soupart A et al. Astrocytes are an early target in osmotic demyelination syndrome. J Am Soc Nephrol 2011; 22 : 1834 – 1845. doi: 10.1681/ ASN.2010111127.
6. Friedman E, Shadel M, Halkin H et al. Thiazide‑induced hyponatremia. Reproducibility by single dose rechallenge and an analysis of pathogenesis. Ann Intern Med 1989; 110 : 24 – 30.
7. Verbalis JG. Whole ‑ Body volume regulation and escape from antidiuresis. Am J Med 2006; 119 (Suppl 1): S21 – S29. doi: 10.1016/ j.amjmed.2006.05.004.
8. Schwartz WB, Bennett W, Curelop S et al. A syndrome of renal sodium loss and hyponatremia probably resulting from inappropriate secretion of antidiuretic hormone. Am J Med 1957; 23 : 529 – 542. doi: 10.1016/ 0002 ‑ 9343(57)90224 ‑ 3.
9. Gheorghiade M, Abraham WT, Albert NM et al. Relationship between admission serum sodium concentration and clinical outcomes in patients hospitalized for heart failure: an analysis from the OPTIMIZE ‑ HF registry. Eur Heart J 2007; 28 : 980 – 988. doi: 10.1093/ eurheartj/ ehl542.
10. Kim WR, Biggins SW, Kremers WK et al. Hyponatremia and mortality among patients on the liver ‑ transplant waiting list. N Engl J Med 2008; 359 : 1018 – 1026. doi: 10.1056/ NEJMoa0801209.
11. Fenske W, Stork S, Koschker AC et al. Value of fractional uric acid excretion in differential diagnosis of hyponatremic patients on diuretics. J Clin Endocrinol Metab 2008; 93 : 2991 – 2997. doi: 10.1210/ jc.2008 ‑ 0330.
12. Nagler EV, Vanmassenhove J, van der Veer SN et al. Diagnosis and treatment of hyponatremia: a systematic review of clinical practice guidelines and consensus statements. BMC Med 2014; 12 : 1. doi: 10.1186/ s12916 ‑ 014 ‑ 0231 ‑ 1.
13. Sterns RH, Silver SM. Salt and water: read the package insert. QJM 2003; 96 : 549 – 552.
14. Sood L, Sterns RH, Hix JK et al. Hypertonic saline and desmopressin: a simple strategy for safe correction of severe hyponatremia. Am J Kidney Dis 2013; 61 : 571 – 578. doi: 10.1053/ j.ajkd.2012.11.032.
15. Konstam MA, Gheorghiade M, Burnett JC et al. Effects of oral tolvaptan in patients hospitalized for worsening heart failure: The everest outcome trial. JAMA 2007; 297 : 1319 – 1331. doi: 10.1001/ jama.297.12.1319.
16. Gilotra NA, Russell SD. Arginine vasopressin as a target in the treatment of acute heart failure. World J Cardiol 2014; 6 : 1252 – 1261. doi: 10.4330/ wjc.v6.i12.1252.
Labels
Paediatric cardiology Internal medicine Cardiac surgery Cardiology
Article was published inCardiology Review

2015 Issue 2-
All articles in this issue
- Sudden cardiac death
- Scoring systems in preventive cardiology
- Scoring systems in patients with acute coronary syndrome
- Scoring systems used in atrial fibrillation
- Scoring systems for venous thromboembolic disease
- Clinical classification and scoring systems in heart failure
- Role of echocardiography in the assessment of aortic stenosis and mitral regurgitation
- Direct versus indirect methods of determining the exercise intensity in cardiovascular rehabilitation
- Scoring systems used before cardiac surgery
- Primary hyperaldosteronism – the most common form of secondary hypertension
- Cushing’s syndrome and cardiovascular risk
- Iodine saturation in Czech Republic and globally – shortcomings and perspectives
- Acute conditions in medicine of thyroid gland
- Differential diagnosis of hyponatraemia
- The Endocrinology of aging – short overview
- Cardiology Review
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Clinical classification and scoring systems in heart failure
- Scoring systems for venous thromboembolic disease
- Differential diagnosis of hyponatraemia
- Acute conditions in medicine of thyroid gland
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career