-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Diferenciální diagnostika polyurie-polydipsie
Differential diagnosis of polyuria-polydipsia
In clinical practice, it is often difficult to distinguish psychogenic (or habitual) polydipsia from true organic polyuria.
First-line tests: urine chemistry, glycaemia: hyperglycaemia, glycosuria and ketonuria confirm diabetes mellitus. Kalemia and calcemia: chronic hypokalaemia or hypercalcaemia lead to loss of renal concentrating capacity. Plasma creatinine level and ultrasound imaging of the kidney: exclude renal impairment with possible loss of concentrating capacity. Serum and urine osmolality from samples as close in time as possible: incidental detection of high urine osmolality with normal serum osmolality is indicative of psychogenic polydipsia. Hyperosmolar serum and hypostenuric urine confirm diabetes insipidus (DI). The differential diagnosis needs to proceed further if the first line does not lead to a decision.
Second-line test: the fluid withdrawal test without desmopresin (DDAVP) administration. During the test are monitored diuresis, patient weight, urine osmolality of each portion during the test and the first portion of urine after its completion. The frequency of serum osmolality measurements during the test depends on the patient‘s condition and the diuresis being monitored. If diuresis decreases during the test and urine osmolality increases, we are probably approaching a diagnosis of psychogenic polydipsia and can reduce the frequency of serum osmolality testing. Persistent high diuresis of hypostenuric urine is suggestive of DI. In an infant with DI, even 3 hours of thirst can lead to hypernatremic dehydration! Terminate the test if one of the following conditions is met: 1. signs of dehydration; 2. uncontrollable thirst (ethical reason); 3. evidence of sufficient renal concentrating ability i.e. high urine osmolality. Usually we are satisfied with the finding of urine osmolality > 500 in infants and > 600 in toddlers and > 750 mOsm/kg in older children. If the condition for test termination is not met within 12 hours, patient non-cooperation is almost certain.
Third-line test: the fluid withdrawal test after DDAVP administration. It is used to differentiate between central and nephrogenic DI. The same test is used but after DDAVP administration. A decrease in diuresis and an increase in urine osmolality while maintaining serum osmolality is indicative of central DI.
Fourth-line examinations: in central DI, we perform CNS imaging by MR, assess other endocrine functions of the hypothalamic-pituitary axis, and add technetium skeletal scintigraphy to exclude osteolytic foci in Langerhans cell histiocytosis. A more precise diagnostic classification of nephrogenic DI is possible by molecular genetics.
Autoři: Votava Felix
Působiště autorů: Klinika dětí a dorostu, 3. lékařská fakulta, Univerzita Karlova a FN Královské Vinohrady, Praha
Vyšlo v časopise: Čes-slov Pediat 2024; 79 (1): 33-38.
Kategorie: Kapitoly k atestaci z pediatrie
doi: https://doi.org/10.55095/CSPediatrie2024/006Souhrn
V klinické praxi bývá problém odlišit návykovou (habituální či psychogenní) polydipsii od skutečné organicky podmíněné polyurie.
Vyšetření první linie: moč chemicky, glykemie – hyperglykemie, glykosurie a ketonurie potvrdí diabetes mellitus. Kalemie a kalcemie – chronická hypokalemie nebo hyperkalcemie vedou ke ztrátě koncentrační schopnosti ledvin. Hladina kreatininu v plazmě a ultrazvukové zobrazení urotraktu – vyloučí renální postižení s možnou ztrátou koncentrační schopnosti. Osmolalita séra a moči z časově co nejbližších vzorků – náhodné zachycení vysoké osmolality moče při normální osmolalitě séra svědčí pro návykovou polydipsii. Hyperosmolární sérum a hypostenurická moč potvrzují diabetes insipidus (DI). Pokud první linie nevede k rozhodnutí, je zapotřebí postupovat v diferenciální diagnostice dále.
Vyšetření druhé linie: Test s odnětím tekutin bez podání desmopresinu (DDAVP). Během testu monitorujeme diurézu, hmotnost pacienta, osmolalitu moče z každé porce během testu a první porce moče po jeho ukončení. Frekvence měření osmolality séra během testu závisí na stavu pacienta a sledované diuréze. Klesá-li během testu diuréza a vzrůstá osmolalita moče, blížíme se pravděpodobně k diagnóze psychogenní polydipsie a můžeme snížit frekvenci vyšetřování osmolality séra. Přetrvávající vysoká diuréza hypostenurické moči svědčí pro DI. U kojence s DI mohou i 3 hodiny žíznění vést k hypernatremické dehydrataci! Test ukončíme, je-li splněna jedna z následujících podmínek: 1. známky dehydratace; 2. nezvladatelná žízeň (etický důvod); 3. průkaz dostatečné koncentrační schopnosti ledvin, tj. vysoká osmolalita moče. Obvykle se spokojíme s nálezem osmolality moči > 500 u kojenců, resp. > 600 u batolat a > 750 mOsm/kg u starších dětí. Nenaplní-li se během 12 hodin podmínka pro ukončení testu, je téměř jistá nespolupráce pacienta.
Vyšetření třetí linie: Test s odnětím tekutin po podání DDAVP. Slouží k rozlišení mezi centrálním a renálním DI. Použijeme stejný test, ale po podání DDAVP. Snížení diurézy a zvýšení osmolality moči při zachování osmolality séra svědčí pro centrální DI.
Vyšetření čtvrté linie: Při centrálním DI provedeme zobrazení CNS pomocí MR, posoudíme ostatní endokrinní funkce osy hypotalamus–hypofýza a doplníme techneciovou scintigrafii skeletu k vyloučení osteolytických ložisek při histiocytóze z Langerhansových buněk. Přesnější diagnostické zařazení renálního DI je možné molekulárně geneticky.
Úvod
V klinické pediatrické praxi jsme občas postaveni před problém diferenciálně diagnosticky vyřešit symptom polyurie-polydipsie. Symptom se vyskytuje věkově nezávisle, napříč všemi věkovými kategoriemi dětství. Nesprávný vyšetřovací postup vystavuje pacienta riziku poškození neindikovanou léčbou (např. podáváním desmopresinu u návykové polydipsie) nebo oddálení rozhodnutí může vést k přehlédnutí závažného organického onemocnění. Smyslem je odlišit celkem frekventní benigní návykovou, habituální či psychogenní polydipsii od skutečné organicky podmíněné polyurie a následně zjistit její příčinu. Cílem článku je seznámit čtenáře, především mladé kolegy v postgraduálním vzdělávacím programu Pediatrie, s diferenciálně diagnostickým postupem.
Definice symptomu
Hranici pro zvýšený obrat tekutin za podmínek bazálního metabolismu spatřujeme v objemu nad 150 % věkově závislé normy. Orientačně je to příjem nad 200 ml / kg / 24 h s diurézou nad 120 ml / kg / 24 h u kojenců; nad 150 ml / kg / 24 h s diurézou nad 100 ml / kg / 24 h u batolat a dětí do 20 kg tělesné hmotnosti; a nad 110 ml / kg / 24 h s diurézou více než 70 ml / kg / 24 h u starších dětí s hmotností nad 20 kg. Do diferenciálně diagnostické rozvahy a vyšetřování se pouštíme často jen na základě pozorování rodičů o zvýšeném obratu tekutin, aniž bychom se opírali o přesné číselné vyjádření.
Klinické projevy
Pediatr může být konfrontován s pacientem s polyurií-polydipsií na základě stížnosti na velký obrat tekutin, noční pití a močení. Často rodiče upoutá sekundární enuréza, která se objevila po suchém intervalu. Může se vyskytnout stesk na neprospívání, nebo i ztrátu hmotnosti. Nápadné mohou být opakované stavy dehydratace bez jiných zevních příčin, které se speciálně u kojenců mohou projevit noční horečkou, typicky nad ránem. Stížnost může být i na absenci pocení či nápadně suchou kůži.
Fyziologie vodního hospodářství
Energetický metabolismus vyžaduje dynamickou rovnováhu mezi příjmem a výdejem tekutin (vody) s cílem zachovat osmolalitu plazmy (respektive extracelulární tekutiny, ECT) v rozmezí 282–295 mOsm/kg. Rozptyl je myšlen spíše interindividuálně, jedinec sám zachovává osmolalitu v užším pásmu cca ± 3 mOsm/kg. Na vyrovnané bilanci příjmu a výdeje vody se uplatňuje několik regulačních mechanismů, např. systém renin–angiotenziny–aldosteron, kde řídícím parametrem je průtok krve ledvinami jako výraz efektivního cirkulujícího objemu, či systém natriuretických peptidů, kde řídícím parametrem je objemová nálož (tlak) v centrálním žilním řečišti pro vyplavování ANP (atrial natriuretic peptide) či v mozku pro BNP (brain natriuretic peptide). Z hlediska možnosti rozvoje polyurie-polydipsie jako dominantního klinického příznaku mají největší význam 3 základní mechanismy:
Žízeň – je indukována osmoreceptory v hypotalamu, sice neměřitelná, ale je logické, že intenzita naléhavosti se zvyšuje s rostoucí osmolalitou plazmy.
Antidiuretický hormon, ADH (vazopresin) – nonapeptid (9 aminokyselin) je syntetizován v supraoptickém a paraventrikulárním jádru v hypotalamu. Pomocí bílkoviny neurofyzinu je dopravován nervovými vlákny do zadního laloku hypofýzy. Jedná se o tzv. neurosekreci. Ze zadního laloku hypofýzy je vyplavován do krevního oběhu především v závislosti na osmolalitě plazmy (uplatňují se i další podněty, např. snížení objemu ECT či bolest, stres). Cílovou tkání ADH jsou především buňky sběrných kanálků, částečně i distálního tubulu. Základní funkcí je zvýšení zpětné resorpce bezsolutové vody, tím snížení objemu moče a zvýšení její koncentrace (osmolality) a snížení osmolality plazmy. Název vazopresin upoutává i na jeho účinek vazokonstrikce v ledvinách a zvýšení krevního tlaku. Má však i jiné efekty zprostředkované V2 receptory – např. zvýšení glykogenolýzy a syntézy koagulačního faktoru VIII v játrech, což je terapeuticky využitelné u lehké formy hemofilie A (s bazální aktivitou faktoru VIII > 5 %). ADH zvyšuje i sekreci adrenokortikotropního hormonu (ACTH) z předního laloku hypofýzy, a tím i hladinu kortizolu. Je vyplavován pulzatilně s krátkým poločasem. Měření hladiny v krvi není použitelné pro klinické účely. V posledních letech je možné měřit v krvi hladinu C-terminálního segmentu ADH, tzv. kopeptin, který je stabilní a odráží míru sekrece ADH. Jeho stanovení má význam především pro průkaz zvýšené sekrece ADH.
Ledviny – membrána buněk sběrných kanálků není běžně prostupná pro vodu. Aktivace V2 receptoru a s ním spojeného G-proteinového komplexu vede k nárůstu intracelulárního cAMP a k syntéze a aktivaci speciálních transmembránových proteinů, tzv. akvaporinů, které prostup vody umožňují. Byla popsána řada typů akvaporinů. Na apikální membráně (na straně lumina kanálku) se exprimuje především akvaporin 2, který facilituje prostup vody směrem intracelulárním. Na bazální membráně působí především akvaporiny 3 a 4, které facilitují prostup vody směrem extracelulárním do osmoticky stratifikovaného intersticia dřeně ledviny (obr. 1). Výsledkem je pasivní přestup vody podle osmotického gradientu z lumina sběrného kanálku do intersticia dřeně ledviny a přestup vody do cév. Dojde k naředění plazmy, poklesu její osmolality, a tím jsou výsledný efekt ADH a regulační smyčka uzavřeny. Osmotická stratifikace intersticia ledvin přímo určuje maximální koncentrační schopnost ledvin a je závislá na věku. U novorozence je maximální dosažitelná osmolalita moče o málo vyšší než 400 mOsm/kg, v jednom roce 800–900 mOsm/kg, během dalších 3 let zvolna stoupá k hodnotám obvyklým u dospělých – 1200 mOsm/kg.
Obr. 1. Schéma funkce buněk sběrného kanálku ledvin 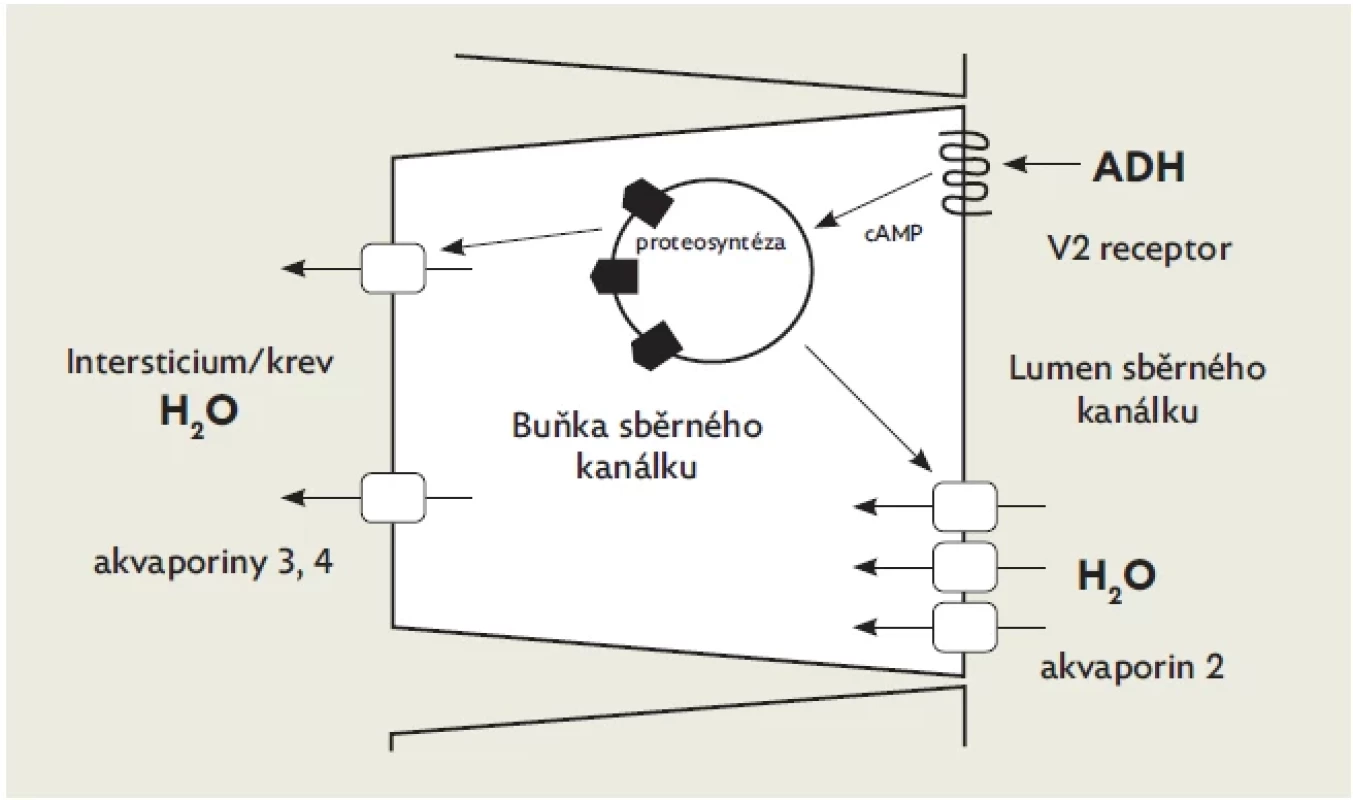
Obr. 2. Diagram diferenciálně diagnostického postupu polyurie-polydipsie 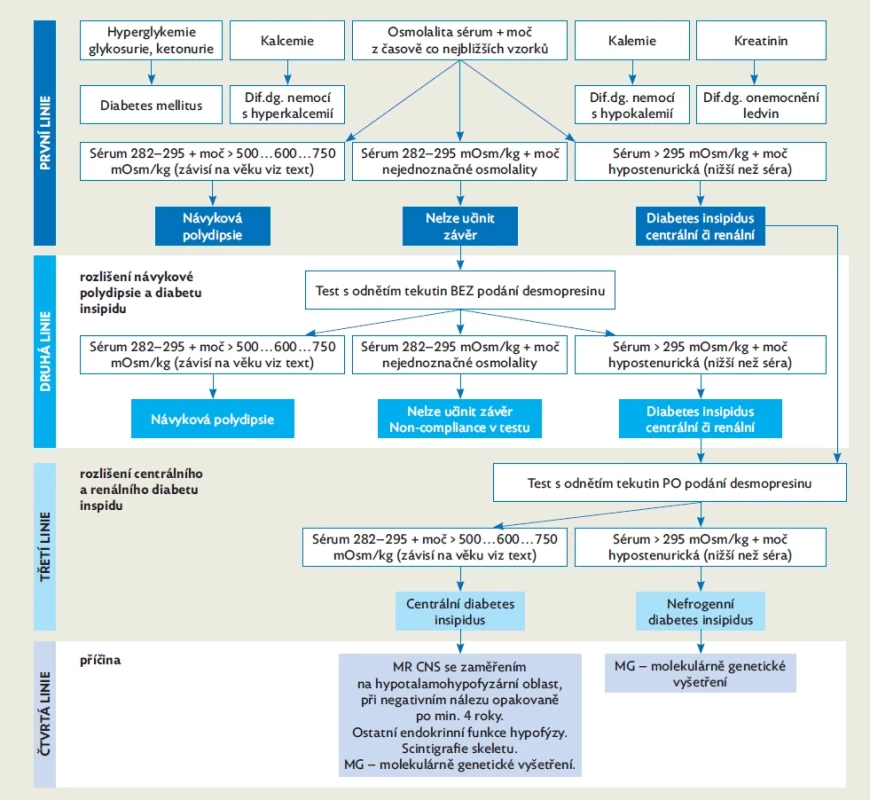
Základní princip diferenciálně diagnostického postupu
Příčinu hledáme v uvedených 3 regulačních mechanismech – žízni, ADH a ledvinách. Volíme postupně vyšetření navazujících linií – viz diagram (obr. 2). Nejdříve je třeba rozlišit častou návykovou či psychogenní habituální polyurii-polydipsii od častého diabetes mellitus a vzácnějšího diabetes insipidus, event. dalších vzácnějších organických příčin polyurie-polydipsie. Pokud prokážeme diabetes insipidus (DI), volíme další linii vyšetřování k rozlišení centrálního (neurohumorálního) DI a velmi vzácného renálního (nefrogenního) DI. Oba typy DI považujeme za symptom, takže pak následují vyšetření k upřesnění příčiny a diagnózy.
Obr. 3. MR zobrazení oblasti hypofýzy a hypotalamu – normální nález 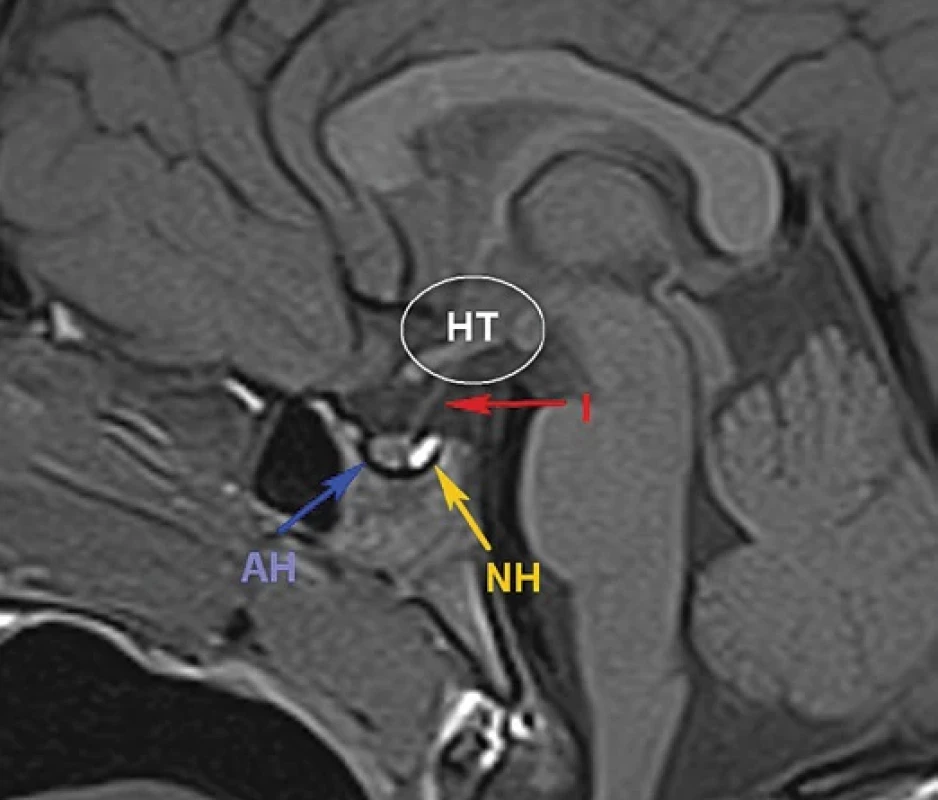
AH – adenohypofýza, HT – hypotalamus, NH – neurohypofýza Vyšetření první linie (než přistoupíme k testům s odnětím tekutin)
Moč chemicky a glykemie: vzhledem k vysoké frekvenci výskytu diabetes mellitus, a zvláště když upoutává typická krátká (jednotky dnů až týdnů) anamnéza (zvýšený obrat tekutin, hmotnostní úbytek, sekundární enuréza), event. i typický klinický obraz, který však nemusí být plně rozvinutý (dehydratace, acetonemický foetor, hyperpnoe, až i alterace vědomí), je moč chemicky a glykemie logicky prvním bezprostředním vyšetřením. Hyperglykemie, glykosurie a ketonurie potvrdí diabetes mellitus. Příčinou polyurie je glykosurie, která zvýší osmotický tlak moče ve sběrném kanálku ledviny do té míry, že se sníží efekt ADH a akvaporinů; z patofyziologického hlediska je tedy polyurie renální příčiny. Pokud vyloučíme diabetes mellitus, následují další testy první linie.
Kalemie a kalcemie: chronická hypokalemie (např. Gitelmanův či Bartterův syndrom) nebo hyperkalcemie (např. hyperparatyreóza, sarkoidóza, paraneoplasticky) vedou ke ztrátě koncentrační schopnosti ledvin kvůli porušené funkci buněk sběrného kanálku (refrakternost V2 receptoru na ADH).
Hladina kreatininu v plazmě a ultrazvukové zobrazení urotraktu: vyloučí chronické renální postižení s možnou ztrátou koncentrační schopnosti.
Osmolalita séra a moči z časově co nejbližších vzorků: v klinické praxi se osvědčuje hned při prvním kontaktu s pacientem při návštěvě v ambulanci či po přijetí na oddělení a vyloučení diabetes mellitus změřit osmolalitu séra a první možné porce moče. Nezřídka se může stát, že náhodně zachytíme vysokou osmolalitu moče při normální osmolalitě séra, což svědčí pro návykovou polydipsii. Naopak hyperosmolární sérum a hypostenurická moč potvrzují diabetes insipidus (DI). Je-li zachycena izo - nebo hypostenurická moč a normální osmolalita séra, jsou vyšetření nekonkluzivní. Pokud první linie nevede k rozhodnutí, je zapotřebí postupovat v diferenciální diagnóze dále.
Vyšetření druhé linie
Test s odnětím tekutin bez podání desmopresinu (DDAVP): dříve často nazývaný test žízněním. Smyslem testu je rozlišit návykovou polydipsii od diabetes insipidus. Konkrétní provedení může být variabilní dle místních zvyklostí, v literatuře lze najít různá schémata provedení. Pokud se jedná o kojence a batolata nebo by anamnéza svědčila pro možné opakované dehydratace během noci, test je rizikový rychlým rozvojem dehydratace a je třeba ho provádět za intenzivní zodpovědné monitorace, nezbytné je připravit monitorovací tabulku, vše vysvětlit ošetřujícímu personálu, rodičům a pacientovi. V praxi bývá někdy problémem zajistit kontrolu žíznění, především v případě psychogenní polydipsie. Osvědčuje se pacienta ponechat během testu na pomalé infuzi, např. 5 ml/h. Kanylu použijeme k odběrům a sníží se tím i možnost nespolupráce. Během testu monitorujeme v tabulce diurézu, hmotnost pacienta, osmolalitu moče z každé porce během testu a i z první porce moče po ukončení testu. Frekvence měření osmolality séra během testu závisí na stavu pacienta a sledované diuréze. Klesá-li během testu diuréza, blížíme se pravděpodobně k diagnóze návykové polydipsie a můžeme snížit frekvenci vyšetřování osmolality séra. Přetrvávající vysoká diuréza hypostenurické moči svědčí pro DI. U kojence s DI mohou v extrémním případě i 3 hodiny žíznění vést k hypernatremické dehydrataci! Test ukončíme, je-li splněna jedna z následujících podmínek:
1. známky dehydratace (úbytek hmotnosti, hyperosmolalita séra > 295 mOsm/kg);
2. nezvladatelná (nesnesitelná) žízeň (etický důvod);
3. průkaz dostatečné koncentrační schopnosti ledvin, tj. vysoká osmolalita moče. Obvykle se spokojíme s nálezem osmolality moči > 500 u kojenců, resp. > 600 u batolat a > 750 mOsm/kg u starších dětí. Nezapomenout poslat sérum na osmolalitu v momentě ukončení testu a první porci moče po ukončení testu. Nenaplní-li se během 12 či max. 16 hodin u starších dětí podmínka pro ukončení testu, je nejpravděpodobnější nespolupráce pacienta, teoreticky se může také jednat o inkompletní, parciální DI, který představuje diagnostický problém.
Hodnocení testu: hyperosmolární sérum (> 295 mOsm/kg) a hypostenurická moč svědčí pro diabetes insipidus. Normální osmolalita séra a dostatečný vzestup osmolality moče (věkově specificky, viz výše) prokazuje psychogenní návykovou polydipsii – může být i u kojenců! Normální osmolalita séra a izo - či hypostenurická moč svědčí pro nespolupráci (pacient během testu pil).
Vyšetření třetí linie
Test s odnětím tekutin po podání DDAVP: slouží k rozlišení mezi centrálním a renálním DI za podmínky, že byl DI skutečně vyšetřením prvé či druhé linie prokázán. Historickou zajímavostí je, že syntetický analog ADH – desmopresin (DDAVP) byl syntetizován a vyvinut v 60. letech 20. století v týmu Milan Zaorala v Ústavu organické chemie a biochemie Československé akademie věd. Byl u nás dříve i vyráběn pod názvem Adiuretin, nosní kapky. Použijeme stejný test s odnětím tekutin jako v druhé linii, ale po podání DDAVP. Před začátkem testu podáme DDAVP, v současnosti lze použít preparát Minirin Melt 60 µg sublingválně v dávce 1,5–3 µg/kg nebo subkutánní/intravenózní aplikaci 0,2–0,3 µg/kg (např. farmakum Octim). Průběh testu a hodnocení jsou stejné. Snížení diurézy a zvýšení osmolality moči při zachování osmolarity séra svědčí pro centrální DI.
Vyšetření čtvrté linie
Centrální i renální DI jsou pouhé symptomy. Je nutné pátrat po příčině. Při centrálním DI provedeme zobrazení CNS pomocí NMR, posoudíme ostatní endokrinní funkce osy hypotalamus–hypofýza a doplníme techneciovou scintigrafii skeletu k vyloučení osteolytických ložisek při histiocytóze z Langerhansových buněk. Přesnější diagnostické zařazení renálního DI je možné molekulárně geneticky.
Obr. 4. MR zobrazení oblasti hypofýzy a hypotalamu při geneticky podmíněném či idiopatickém deficitu ADH – absence zvýšeného signálu neurohypofýzy 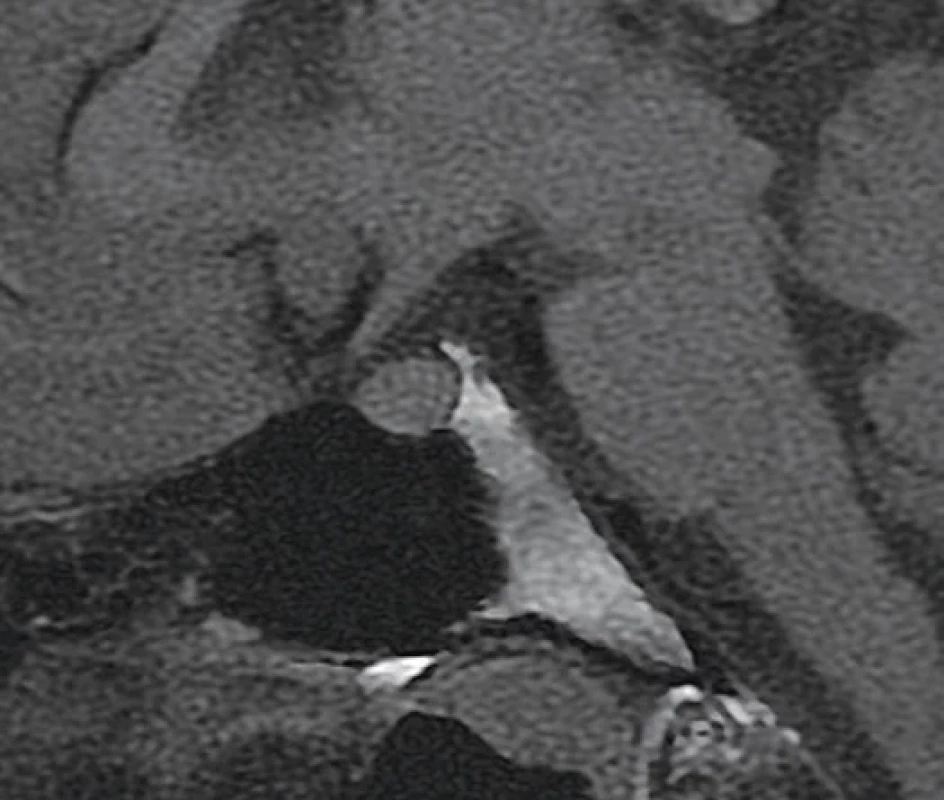
Obr. 5. MR zobrazení oblasti hypofýzy a hypotalamu – centrální diabetes insipidus na základě infiltrace hypotalamu/hypofýzy Langerhansovými buňkami – histiocytóza. Typickým časným nálezem je ztluštění stopky hypofýzy. 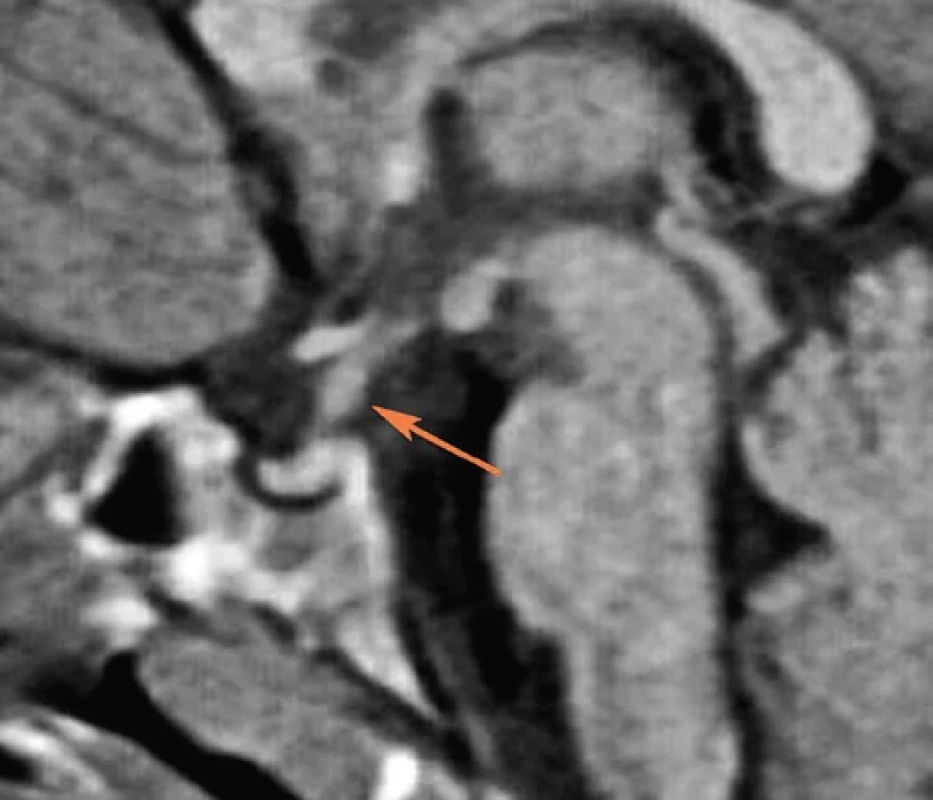
Příčiny centrálního, neurohumorálního diabetes insipidus
Vrozené příčiny: mutace genu (na 20. chromozomu) pro ADH nebo transportní neurofyzin. DI se může objevit v různém věku. Na MR typicky chybí hypersignální zobrazení zadního laloku hypofýzy (obr. 3 a 4). Vrozené vývojové vady CNS, např. septo-optická dysplazie či holoprosencefalie jsou spojeny s deficitem ADH. DI je i součástí některých syndromů – např. DIDMOAD (diabetes insipidus, diabetes mellitus, atrofie optiků a hluchota). Kongenitální CMV infekce či toxoplasmóza mohou být spojeny s centrálním DI.
Získané příčiny: tumory CNS, např. kraniofaryngeom, gliom optiku, dysgerminom hypotalamu. Centrální DI může být časným, až několik let ostatním symptomům přecházejícím symptomem histiocytózy I. typu z Langerhansových buněk. Typickým prvním nálezem na MR u histiocytózy bývá ztluštění stopky (infundibula) hypofýzy (obr. 5), které se objeví až i po letech trvání DI. Tento fakt je důvodem k pravidelnému opakování vyšetření hypotalamo-hypofyzární oblasti pomocí MR, většinou à 6 měsíců po min. 4 roky. DI může vzniknout po intrakraniálním krvácení po úraze či neurochorurgickém výkonu nebo po encefalitidě či granulomatózním procesem při sarkoidóze či tuberkulóze. Hypofýza může být infiltrována při leukemii. Je možná i autoimunitní příčina (hypofyzitida). U novorozenců může být centrální DI následkem asfyxie, intraventrikulárního krvácení, DIC zvláště ve spojení s meningitidou listeriové či streptokokové (skupiny B) etiologie.
Idiopatická příčina: až ve 20 % případů se nenajde příčina po 5 letech sledování.
Kromě odstranění příčiny se centrální DI léčí podáváním DDAVP v sublingvální formě. Dávkování se individualizuje dle bilance tekutin a s ohledem na možnou retenci vody s rizikem hyponatremického edému CNS.
Příčiny renálního, nefrogenního diabetes insipidus
Vrozené příčiny: X-vázaná recesivně dědičná mutace genu pro V2 receptor. Nebo se může jednat o autozomální recesivně či dominantně dědičné mutace genů (většinou 12. chromozom) pro akvaporiny. Renální DI je nebezpečný především v kojeneckém věku, kdy opakovanými hypernatremickými dehydratacemi může ireverzibilně poškodit CNS. Neexistuje specifická terapie. Důležité je udržet vyrovnanou bilanci tekutin. Polyurie se dá zmenšit dietou s nízkým obsahem sodíku a snížením glomerulární filtrace podáváním thiazidových diuretik. Pomáhá podávání amiloridu a nesteroidních antiflogistik.
Získané příčiny: renální insuficience např. při obstrukcích vývodných cest, infiltraci ledvin sarkoidózou či amyloidózou. Hypokalemie, hyperkalcemie a některá farmaka (lithium) zapříčiňují refrakternost V2 receptoru. |
Korespondenční adresa:
doc. MUDr. Felix Votava, CSc.
Klinika dětí a dorostu 3. LF UK a FN Královské Vinohrady
Šrobárova 1150 100 34 Praha 10
felix.votava@fnkv.cz
Zdroje
1. Partsch CJ, Mönig H, Sippell WG. Endokrinologická funkční diagnostika. Praha: Galén 2008.
2. Lebl J, Zapletalová J, Koloušková S, et al. Dětská endokrinologie. Praha: Galén 2004.
3. Hochberg Z. Practical Algoritms in Pediatric Endocrinology. Karger 2017.
4. Kliegman RM, St.Geme III JW. Nelson Textbook of Pediatrics. 21st Edition. Elsevier 2019.
5. Christ-Crain M, Gaisl O. Diabetes insipidus. Presse Med 2021; 50. Dostupné na: http://creativecommons.org/licenses/by-nc-nd/4.0/
6. Pedrosa W, et al. A combined outpatient and inpatient overnight water deprivation test is effective and safe in diagnosing patients with polyuria-polydipsia syndrome. Endocr Pract 2018; 24(11): 963–972.
7. Vaz de Castro PAS, et al. Nephrogenic diabetes insipidus: a comprehensive overview. J Pediatr Endocrinol Metab 2022; 35(4): 421–434.
8. Vergier J, et al. Rapid differential diagnosis of diabetes insipidus in a 7-month-old infant: The copeptin approach. Arch Pediatr 2018; 25(1): 45–47.
Štítky
Neonatologie Pediatrie Praktické lékařství pro děti a dorost
Článek vyšel v časopiseČesko-slovenská pediatrie
Nejčtenější tento týden
2024 Číslo 1- Horní limit denní dávky vitaminu D: Jaké množství je ještě bezpečné?
- Isoprinosin je bezpečný a účinný v léčbě pacientů s akutní respirační virovou infekcí
- Syndrom Noonanové: etiologie, diagnostika a terapie
-
Všechny články tohoto čísla
- Prevence poškození zdraví při sportu
- Současný pohled na prevenci infekční endokarditidy v dětství v České republice
- Z Lobkowiczké sbírky na Pražském hradě
- Porucha příjmu potravy kojenců a batolat
- Diferenciální diagnostika polyurie-polydipsie
- Úrazy břicha u dětí – identifikace, základní principy klinické rozvahy a léčby
- Co jsme psali
- Chemická pleurodéza s použitím jodovaného povidonu (Betadine) u vrozeného chylothoraxu: vlastní zkušenost a přehled literatury
- Cena ministra zdravotnictví za zdravotnický výzkum a vývoj
- 70 let Fakulty dětského lékařství Univerzity Karlovy v Praze
- Zemřel profesor MUDr. Bohumil Hučín, DrSc.
- Humor & poezie
- Editorial
- Preventivní kardiologie v pediatrii
- Prenatální kardiologie
- Česko-slovenská pediatrie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Diferenciální diagnostika polyurie-polydipsie
- Úrazy břicha u dětí – identifikace, základní principy klinické rozvahy a léčby
- Současný pohled na prevenci infekční endokarditidy v dětství v České republice
- Porucha příjmu potravy kojenců a batolat
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



