-
Medical journals
- Career
Roboticky asistovaná laparoskopická prostatektomie: kritické hodnocení výsledků
Authors: G. T. Gotto; J. A. Eastham
Authors‘ workplace: Urology Service, Department of Surgery, Memorial Sloan-Kettering Cancer Center, New York, USA
Published in: Urol List 2009; 7(4): 5-9
Overview
Roboticky asistovaná laparoskopická prostatektomie (RALP) si získává na popularitě navzdory nedostatku důkazů, které by prokazovaly její signifikantní výhodu oproti otevřené radikální prostatektomii (ORP). Ve Spojených Státech se RALP dokonce stala nejčastější metodou léčby klinicky lokalizovaného karcinomu prostaty. Autoři tohoto článku kriticky hodnotí výsledky ORP a RALP. K dispozici máme celou řadu údajů týkajících se onkologických a funkčních výsledků ORP a RALP, srovnáním obou metod se však doposud nezabývala žádná prospektivní randomizovaná studie. Malý počet prospektivních nerandomizovaných studií prokázal nekonzistentní výhody zlepšení některých výsledků jedné metody oproti druhé, což však lze přičítat spíše preferenci operatéra pro určitou techniku.
Klíčová slova:
výsledky, prostata, nádory prostaty, prostatektomie, robotikaÚVOD
Jen v USA představoval v roce 2008 karcinom prostaty 186 320 případů ze všech nově diagnostikovaných karcinomů a byl příčinou 28 660 úmrtí. To znamená, že jeden ze šesti mužů má riziko, že u něj bude v průběhu života diagnostikován karcinom prostaty, a jeden ze 34 pacientů na něj zemře. Karcinom prostaty představuje u mužů druhou nejčastější příčinu úmrtí na karcinom [1]. Možnost PSA screeningu vedla k významné změně stadia karcinomu při jeho detekci (stage migration), u více než 90 % pacientů je v době diagnózy přítomen klinicky lokalizovaný karcinom. Pro léčbu onemocnění ohraničeného na orgán máme k dispozici celou řadu modalit, které zahrnují jak techniky pozorného vyčkávání (watchful waiting) a aktivního sledování (active surveillance), tak kurativní techniky, mezi něž patří radikální prostatektomie, radioterapie (včetně brachyterapie), kryoterapie a fokusovaný ultrazvuk o vysoké intenzitě.
Techniku otevřené radikální prostatektomie poprvé popsal Millin v roce 1947 [2]. Prospektivní randomizovaná studie prokázala, že u pacientů s klinicky lokalizovaným karcinomem prostaty dosahuje ORP (ve srovnání s pozorným vyčkáváním) lepší doby přežití bez známek metastáz i mortality specifické pro karcinom prostaty – relativní riziko 0,65 [3]. Jedná se však o jedinou prospektivní randomizovanou studii srovnávající jakoukoliv léčbu klinicky lokalizovaného karcinomu prostaty s metodou pozorného vyčkávání nebo aktivního sledování. Doposud však nemáme k dispozici žádnou prospektivní randomizovanou studii, která by srovnávala účinnost dvou různých léčebných přístupů.
Techniku roboticky asistované laparoskopické prostatektomie (RALP) poprvé popsali Abbou et al v roce 2000 [4]. Krátce na to, v roce 2001, Binder et al publikovali svoji malou případovou studii [5]. Platforma robota da Vinci (Intuitive Surgical) poskytuje 3D vizi, zvětšení obrazu a díky technologii EndoWrist zdokonalení obratnosti pohybů [6]. Neexistují však žádné prospektivní randomizované studie, které by srovnávaly onkologický či funkční výsledek RALP s účinností jiných terapeutických modalit. Nicméně i navzdory absenci těchto údajů byla tato technika přijata jako „léčba první volby lokalizovaného karcinomu prostaty“ [6]. V roce 2007 byla v USA technika RALP užita při 63 % radikálních prostatektomií, v roce 2008 při více než 80 % [6]. Tento nárůst popularity lze přičítat marketingovým strategiím a tlaku na pacienty spíše než přítomnosti důkazů, které by prokazovaly benefit robotického přístupu k radikální prostatektomii oproti ostatním operačním přístupům.
TVRZENÍ
Webová stránka Intuitive Surgical uvádí následující potenciální výhody RALP oproti ORP
- zlepšení kontroly karcinomu
- rychlejší obnova potence a kontinence
- signifikantně menší bolestivost
- menší ztráta krve
- nižší výskyt komplikací
- méně častý vznik jizvení
- kratší doba hospitalizace
- rychlejší návrat k běžným denním činnostem [6]
Nejnovější hodnocení informací uvedených na webových stránkách center poskytujících RALP prokázala, že 45 % těchto zdrojů uvádí pouze výsledky zkopírované přímo z webové stránky Intuitive Surgical. Více než polovina webových stránek i navzdory nedostatku důkazů, které by toto tvrzení podpořily, uvádí, že míra ED je po RALP nižší než po ORP. Jedná se pouze o příklad toho, jakým způsobem jsou veřejnosti prezentovány informace o RALP, aniž by byly podpořeny řádným výzkumem založeným na důkazech [7].
Většina studií, v nichž jsou prezentovány výsledky RALP, pochází z individuálních center, kde se skupina urologů rozhodla upustit od provádění ORP a soustředit se pouze na techniku RALP. Existuje pouze malý počet center, v nichž by urologové školení v obou technikách prováděli stejný podíl ORP i RALP, což znesnadňuje srovnávání těchto dvou přístupů.
Tuto problematiku dále komplikují odlišnosti případů indikovaných k oběma přístupům a nekonzistentní definice výsledků a načasování.
DŮKAZY
Výskyt komplikací a rekonvalescence
Lepor et al v roce 2001 publikovali aktuální přehled výskytu komplikací po ORP ve velké studii zahrnující 1 000 pacientů. Míra výskytu peroperačních komplikací byla 0,8 %. Krevní transfuzi vyžadovalo 9,7 % pacientů. Během 30 dnů po ORP byla zaznamenána 0,4% míra výskytu plicní embolie (PE) a 0,5% míra výskytu infarktu myokardu (MI) s jediným pooperačním úmrtím způsobeným MI. Míra operační revize je 0,5 %. Průměrná doba hospitalizace byla 2,3 dnů, 1,5 % pacientů bylo opakovaně hospitalizováno po propuštění [8]. Catalona et al uvádějí ve své studii zahrnující 1 870 pacientů, kteří byli léčení pomocí ORP, 10% míru výskytu komplikací [9].
Ve studii provedené na základě údajů databáze SEER-Medicare z let 1992–1996 v naší instituci jsme zjistili úzkou souvislost mezi operatérem provádějícím ORP, objemem pacientů a pooperační morbiditou. Míra mortality 30 dnů po výkonu byla 0,5 %, míra výskytu závažných komplikací 28,6 % a míra výskytu pozdních mikčních komplikací 25,2 % [10]. Jedním z možných vysvětlení vyšší míry výskytu komplikací (ve srovnání s očekáváním) může být skutečnost, že tato databáze zahrnuje pouze starší pacienty, kteří využívají služeb Medicare, u nichž je pravděpodobnost přítomnosti komorbidit vyšší.
Je všeobecně známým faktem, že ztráta krve je po RALP díky venózní tamponádě, kterou způsobuje pneumoperitoneum, menší. Farnham et al prospektivně srovnávali ztrátu krve a nutnost krevní transfuze po RALP a ORP, které prováděl jediný operatér. U pacientů podstupujících RALP byla zaznamenána významně menší ztráta krve (191 vs 664 ml) [11].
Ficarra et al ve své prospektivní nerandomizované studii (zahrnující výkony v jediné instituci) srovnávali RALP s ORP. Průměrná délka výkonu byla kratší u ORP (135 min vs 185 min, p < 0,001). Ztráta krve během výkonu však byla při tomto zákroku významnější (500 vs 300 ml, p < 0,001), což mělo za následek vyšší míru aplikace krevní transfuze (14 % vs 1,9 %, p < 0,01). S ohledem na výskyt komplikací nebyl mezi oběma přístupy zaznamenán žádný významný rozdíl (ORP 9,7 % vs RALP 10,4 %) (p = 0,854) [12].
Studie zahrnující 5 923 pacientů (databáze SEER-Medicare) srovnávala jeden rok po výkonu výsledky ORP a minimálně invazivní RP (laparoskopická RP nebo LARP) při léčbě pacientů s klinicky lokalizovaným karcinomem prostaty, kteří operaci podstoupili v letech 2003–2005. Autoři prokázali srovnatelnou míru výskytu peroperačních a časných pooperačních komplikací. Specificky nebyl zaznamenán žádný rozdíl v míře výskytu obecných komplikací interního/chirurgického typu, komplikací spojených s výkonem (OR 0,93, 95 % CI: 0,77–1,14), genitourinárních/ střevních komplikací (OR 0,96, 95 % CI: 0,76–1,22), ani pooperační indikaci radiace nebo androgenní deprivace (případně aplikaci obou metod) (OR 0,80, 95 % CI: 0,60–1,08). Minimálně invazivní RP byla spojena s 35% kratší dobou hospitalizace (dva vs tři dny, p < 0,0001) a nižším výskytem obstrukce hrdla močového měchýře/močové trubice (OR 0,74, 95 % CI 0,58–0,94) [13].
Stav chirurgických okrajů
Tab. 1 uvádí přehled celkové míry výskytu pozitivních chirurgických okrajů v nejnovějších studiích týkajících se ORP a RALP. Míra výskytu pozitivních okrajů je vyšší (jak u ORP, tak i RALP) u onemocnění s vyšším patologickým stadiem.
Table 1. Stav chirurgických okrajů ve vybraných nejnovějších studiích týkajících se ORP a RALP. 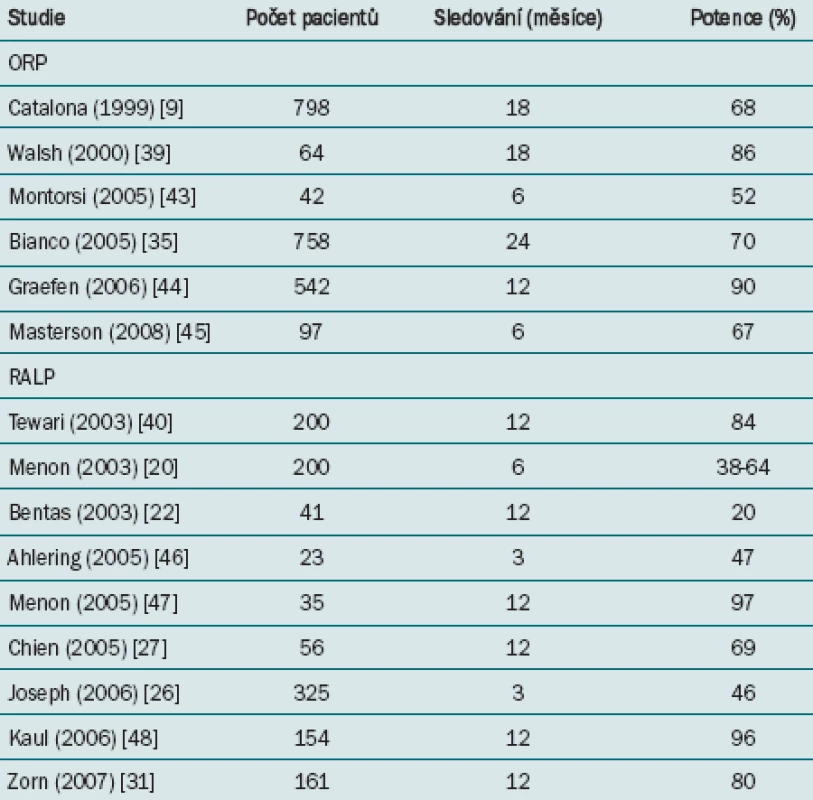
Smith et al ve své studii srovnávají incidenci pozitivních chirurgických okrajů při RALP a ORP. Ve srovnání s ORP byla incidence pozitivních chirurgických okrajů při RALP signifikantně nižší (15 % vs 35 %, p < 0,001). Pacienti podstu-pující RALP však měli před operací nižší hladinu PSA, klinické stadium i Gleasonovo skóre, což znesnadňuje jakékoliv přímé srovnání výsledků. Ficarra et al v podobné nerandomizované studii nezjistili u pacientů podstupujících léčbu nádorů ve stadiu pT2 pomocí ORP a RALP téměř žádný rozdíl ve výskytu pozitivních chirurgických okrajů (12,2 % vs 11,7 %, p = 0,70).
Parsons et al uskutečnili meta-analýzu pozorovacích studií, které srovnávají ORP a RALP. Nalezli celkem 13 studií zahrnujících dohromady 3 039 pacientů. Mezi oběma přístupy nebyl pozorován žádný významný rozdíl ve výskytu chirurgických okrajů (RR 0,88, 95 % CI 0,74–1,06, p = 0,17) [14].
Doba přežití bez biochemické recidivy (bPFS)
Srovnání doby přežití bez biochemické recidivy (bPFS) mezi jednotlivými studiemi je komplikované nejenom vzhledem k proměnlivé charakteristice jednotlivých případů, ale také vzhledem k odlišné definici recidivy a různě dlouhému trvání sledování.
Existuje pouze malý počet studií týkajících se RALP, které by zahrnovaly dostatečně dlouhé sledování umožňující zaznamenání bPFS, a to zejména vzhledem k tomu, že většina pacientů má onemocnění s nízkým rizikem (na základě klasifikace podle D´Amica), a u nichž pravděpodobně během pěti let nedojde k recidivě.
Bianco et al při sledování 1 746 pacientů, kteří podstoupili ORP pro léčbu klinicky lokalizovaného karcinomu prostaty, zaznamenali následující míru bPFS: 82 % po 5 letech, 77 % po 10 letech a 75 % po 15 letech [35]. Nielsen et al uvádějí podobné výsledky u 2 570 pacientů, kteří podstoupili ORP v letech 1985–2004 [36].
Dvě následující RALP studie zahrnující pouze krátkou dobu sledování uvádějí míru bPFS. Menon et al dosáhli u 1 142 pacientů sledovaných po dobu minimálně 12 měsíců (rozmezí: 12–66 měsíců, střední hodnota: 36 měsíců) [30] 91,6% bPFS. Zorn et al dosáhli u 300 pacientů sledovaných průměrně po dobu 17,1 měsíců 93,1% bPFS [31].
Kontinence
Míry kontinence dosažené při v současné době prováděných ORP a RALP jsou uvedeny v tab. 2.
Table 2. Míra kontinence ve vybraných studiích, které se zabývají RALP a ORP. 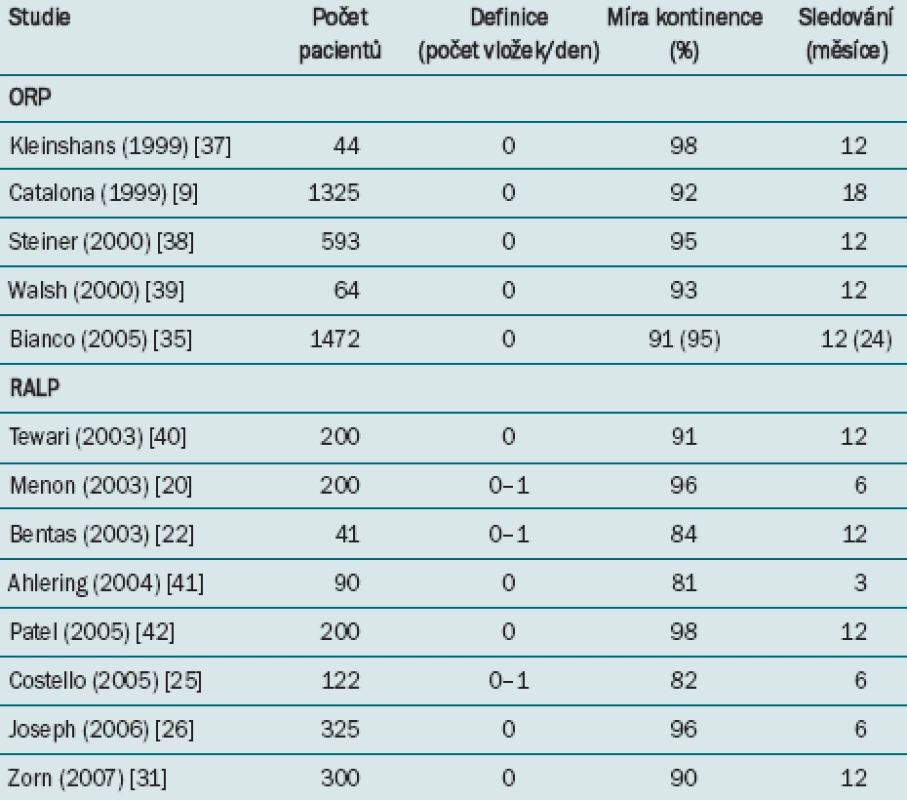
Parson et al ve své metaanalýze identifikovali čtyři studie zahrnující celkem 492 pacientů. Mezi oběma přístupy nebyl odhalen žádný významný rozdíl v míře kontinence (RR 1,07, 95 % CI 0,75–1,5, p = 0,70) [14].
Potence
Míra potence v nejnovějších studiích, které se zabývají ORP a RALP, je uvedena v tab. 3. Rozdílné definice a přístupy k hodnocení potence srovnání jednotlivých studií neskutečně komplikují. Výsledná měření užívaná ke stanovení potence čerpají z nevalidovaných dotazníků, hodnocení pohlavního styku, IIEF skóre a formálnějších druhů hodnocení. Pacienti jsou často klasifikováni jako potentní navzdory potřebě farmakologické léčby a/nebo užívání vakuových zařízení. Tato srovnání výsledků dále komplikují rozdíly ve smíšené charakteristice případů, která zahrnují do analýzy pouze pacienty podstupující bilaterální operaci se zachováním nervů a/nebo pouze mladší pacienty.
Table 3. Míra potence ve vybraných studiích, které se zabývají RALP a ORP. 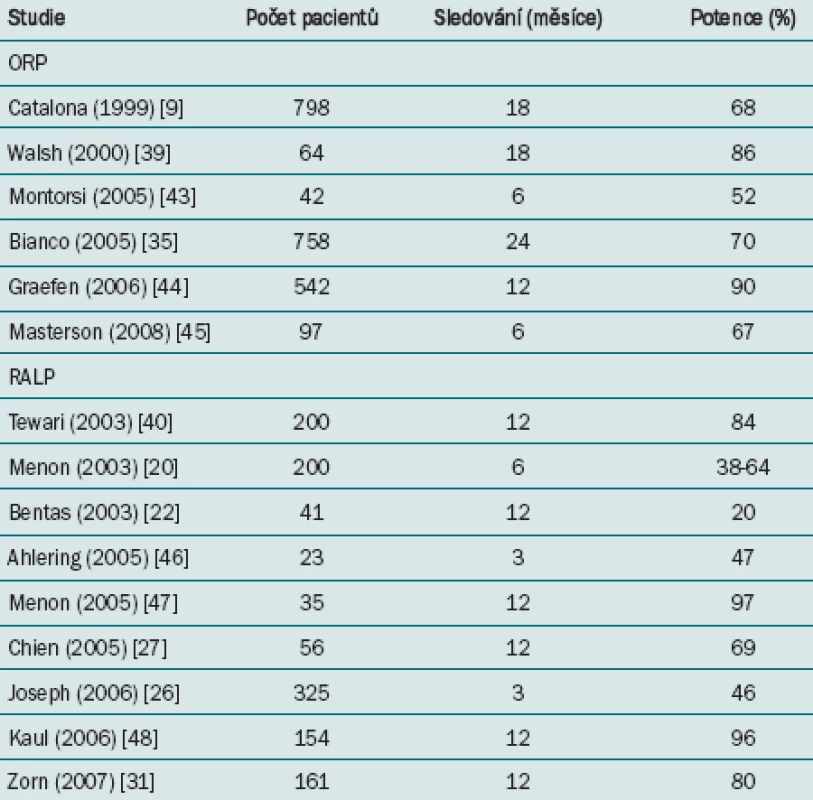
Parsons et al ve své meta-analýze identifikovali dvě studie zahrnující celkem 359 pacientů. V obou studiích byla užita rozdílná definice potence. Mezi oběma přístupy nebyl zaznamenán žádný signifikantní rozdíl v potenci (RR 1,28, 95 % CI 0,96–1,5, p = 0,09) [14].
Cena
Lotan et al prokázali, že ORP představuje cenově nejvýhodnější přístup k radikální prostatektomii. Odhadovaný cenový benefit oproti RALP byl 1 726 $ (v případě započítání pořizovací ceny robota da Vinci). Vyšší cena RALP byla přičítána pořizovací ceně zařízení, nákladům na udržování a užívání vybavení na jedno použití. Tuto nevýhodu nevyvážily ani kratší délka operace (140 vs 160 min), ani délka hospitalizace (1,2 vs 2,5/den) [49].
ZÁVĚR
Většina pacientů, u nichž byl diagnostikován klinicky lokalizovaný karcinom prostaty, jsou vhodnými kandidáty pro ORP nebo RALP. Oba přístupy jsou technicky náročné a funkční i onkologické výsledky jsou podmíněny zkušenostmi a kompetencemi operatéra [10,50–52].
Jedním z mála tvrzení týkajících se výsledku RALP uvedených na webové stránce Intuitive Surgical, která jsou podložena důkazy v literatuře, je, že „výsledky u jednotlivých pacientů se mohou lišit“ [6]. V případě obou přístupů jsou zručnost a operační technika mnohem důležitější než zvolený přístup. Kvalifikovaní operatéři v případě RALP prokázali, že modifikace operační techniky (zachování neurovaskulárního svazku bez použití tepelné energie, změna manipulace s dorzálním venózním komplexem nebo obnovení posteriorního rhabdosfinkteru uretry) vedou ke zlepšení výsledku [41,53–54].
Onkologické a funkční výsledky ORP a RALP se významně liší. Tento rozdíl je znatelný zejména v případě srovnávání výsledků jediného centra, které se zaměřuje pouze na jeden z těchto přístupů. Několik málo nerandomizovaných prospektivních studií prokazuje nekonzistentní zlepšení některých výsledků (jedné techniky oproti druhé), které však lze pravděpodobně přičítat preferenci operatéra pro danou techniku [12,40]. Parsons et al ve své metaanalýze nezjistili mezi oběma přístupy žádné významné rozdíly s ohledem na funkční ani onkologické výsledky [14].
Technika RALP je cenově náročnější než RRP. Z tohoto důvodu je nutné provedení dalších prospektivních studií s pečlivějším sledováním pacientů, které nám umožní posoudit, zda je tato vyšší cena oprávněná, nebo nikoliv.
James A. Eastham, MD
Urology Service, Department of Surgery
Memorial Sloan-Kettering Cancer Center
New York, USA
easthamj@mskcc.org
Sources
1. National Cancer Institute Website: www.cancer.gov. Last accessed: August 18th 2009.
2. Millin T. Retropubic Urinary Surgery: Baltimore, Williams, & Wilkins Co., 1947.
3. Bill-Axelson A, Holmberg L, Filen F et al. Radical prostatectomy versus watchful waiting in localized prostate cancer: the Scandinavian prostate cancer group-4 randomized trial. J Natl Cancer Inst 2008, 100 : 1144–1154.
4. Abbou CC, Hoznek A, Salomon L et al. [Remote laparoscopic radical prostatectomy carried out with a robot. Report of a case]. Prog Urol 2000; 10 : 520–523.
5. Binder J, Kramer W. Robotically-assisted laparoscopic radical prostatectomy. BJU Int 2001; 87(4): 408–410.
6. Intuitive Surgical Website: www.intuitivesurgical.com. Last accessed: August 18 2009.
7. Mulhall JP, Rojaz-Cruz C, Muller A. An analysis of sexual health information on radical prostatectomy websites. BJU Int 2009.
8. Lepor H, Nieder AM, Ferrandino MN. Intraoperative and postoperative complications of radical retropubic prostatectomy in a consecutive series of 1,000 cases. J Urol 2001; 166(5): 1729–1733.
9. Catalona WJ, Carvalhal GF, Mager DE et al. Potency, continence and complication rates in 1,870 consecutive radical retropubic prostatectomies. J Urol 1999; 162(2): 433–438.
10. Bianco FJ Jr, Riedel ER, Begg CB et al. Variations among high volume surgeons in the rate of complications after radical prostatectomy: further evidence that technique matters. J Urol 2005; 173(6): 2099 – 2103.
11. Farnham SB, Webster TM, Herrell SD et al. Intraoperative blood loss and transfusion requirements for robotic-assisted radical prostatectomy versus radical retropubic prostatectomy. Urology 2006; 67(2): 360–363.
12. Ficarra V, Novara G, Fracalanza S et al. A prospective, non-randomized trial comparing robot-assisted laparoscopic and retropubic radical prostatectomy in one European institution. BJU Int 2009; 104(4): 534–539.
13. Lowrance WT, Eastham JA, Jacks LM et al. Comparative Effectiveness of Surgical Treatments for Prostate Cancer: A Population-Based Analysis of Postoperative Outcomes (unpublished work).
14. Parsons JK, Bennett JL. Outcomes of retropubic, laparoscopic, and robotic-assisted prostatectomy. Urology 2008, 72(2): 412–416.
15. Hull GW, Rabbani F, Abbas F et al. Cancer control with radical prostatectomy alone in 1,000 consecutive patients. J Urol 2002; 167 : 528–534.
16. Harris MJ. Radical perineal prostatectomy: cost efficient, outcome effective, minimally invasive prostate cancer management. Eur Urol 2003; 44(3): 303–308.
17. Swindle P, Eastham JA, Ohori M et al. Do margins matter? The prognostic significance of positive surgical margins in radical prostatectomy specimens. J Urol 2005, 174(3): 903–907.
18. Eastham JA, Kuroiwa K, Ohori M et al. Prognostic significance of location of positive margins in radical prostatectomy specimens. Urology 2007, 70(5): 965–969.
19. Menon M, Shrivastava A, Sarle R et al. Vattikuti Institute Prostatectomy: a single-team experience of 100 cases. J Endourol 2003; 17(9): 785–790.
20. Menon M, Tewari A. Robotic radical prostatectomy and the Vattikuti Urology Institute technique: an interim analysis of results and technical points. Urology 2003; 61 4 Suppl 1): 15–20.
21. Wolfram M, Brautigam R, Engl T et al. Robotic-assisted laparoscopic radical prostatectomy: the Frankfurt technique. World J Urol 2003; 21(3): 128–132.
22. Bentas W, Wolfram M, Jones J et al. Robotic technology and the translation of open radical prostatectomy to laparoscopy: the early Frankfurt experience with robotic radical prostatectomy and one year follow-up. Eur Urol 2003; 44(2): 175–181.
23. Cathelineau X, Rozet F, Vallancien G. Robotic radical prostatectomy: the European experience. Urol Clin North Am 2004; 31(4): 693–699.
24. Sim HG, Yip SK, Lau WK et al. Early experience with robot-assisted laparoscopic radical prostatectomy. Asian J Surg 2004; 27(4): 321–325.
25. Costello AJ, Haxhimolla H, Crowe H et al. Installation of telerobotic surgery and initial experience with telerobotic radical prostatectomy. BJU Int 2005; 96(1): 34–38.
26. Joseph JV, Rosenbaum R, Madeb R et al. Robotic extraperitoneal radical prostatectomy: an alternative approach. J Urol 2006; 175 : 945–950.
27. Chien GW, Mikhail AA, Orvieto MA et al. Modified clipless antegrade nerve preservation in robotic-assisted laparoscopic radical prostatectomy with validated sexual function evaluation. Urology 2005; 66(2): 419–423.
28. Van Appledorn S, Bouchier-Hayes D, Agarwal D et al. Robotic laparoscopic radical prostatectomy: setup and procedural techniques after 150 cases. Urology 2006; 67(2): 364–367.
29. Borin JF, Skarecky DW, Narula N et al. Impact of urethral stump length on continence and positive surgical margins in robot-assisted laparoscopic prostatectomy. Urology 2007; 70(1): 173–177.
30. Menon M, Shrivastava A, Kaul S et al. Vattikuti Institute prostatectomy: contemporary technique and analysis of results. Eur Urol 2007; 51(3): 648–657.
31. Zorn KC, Gofrit ON, Orvieto MA et al. Robotic-assisted laparoscopic prostatectomy: functional and pathologic outcomes with interfascial nerve preservation. Eur Urol 2007; 51(3): 755–762.
32. Smith JA Jr, Chan RC, Chang SS et al. A comparison of the incidence and location of positive surgical margins in robotic assisted laparoscopic radical prostatectomy and open retropubic radical prostatectomy. J Urol 2007; 178(6): 2385–2389.
33. Patel VR, Palmer KJ, Coughlin G et al. Robot-assisted laparoscopic radical prostatectomy: perioperative outcomes of 1500 cases. J Endourol 2008; 22(10): 2299-2305.
34. Yee DS, Narula N, Amin MB et al. Robot-Assisted Radical Prostatectomy: Current Evaluation of Surgical Margins in Clinically Low-, Intermediate-, and High-Risk Prostate Cancer. J Endourol 2009; 23(9): 1461–1465.
35. Bianco FJ Jr, Scardino PT, Eastham JA. Radical prostatectomy: long-term cancer control and recovery of sexual and urinary function („trifecta“). Urology 2005; 66 (5 Suppl): 83–94.
36. Nielsen ME, Makarov DV, Humphreys E et al. Is it possible to compare PSA recurrence-free survival after surgery and radiotherapy using revised ASTRO criterion--„nadir + 2“? Urology 2008; 72 : 389–395.
37. Kleinhans B, Gerharz E, Melekos M et al. Changes of urodynamic findings after radical retropubic prostatectomy. Eur Urol 1999; 35(3): 217–221.
38. Steiner MS. Anatomic basis for the continence-preserving radical retropubic prostatectomy. Semin Urol Oncol 2000; 18(1): 9–18.
39. Walsh PC, Marschke P, Ricker D et al. Patient-reported urinary continence and sexual function after anatomic radical prostatectomy. Urology 2000; 55(1): 58–61.
40. Tewari A, Srivasatava A, Menon M et al. A prospective comparison of radical retropubic and robot-assisted prostatectomy: experience in one institution. BJU Int 2003; 92(3): 205–210.
41. Ahlering TE, Eichel L, Edwards RA et al. Robotic radical prostatectomy: a technique to reduce pT2 positive margins. Urology 2004, 64(6): 1224–1228.
42. Patel VR, Tully AS, Holmes R et al. Robotic radical prostatectomy in the community setting--the learning curve and beyond: initial 200 cases. J Urol 2005; 174(1): 269–272.
43. Montorsi F, Salonia A, Suardi N et al. Improving the preservation of the urethral sphincter and neurovascular bundles during open radical retropubic prostatectomy. Eur Urol 2005; 48(6): 938–945.
44. Graefen M, Walz J, Huland H. Open retropubic nerve-sparing radical prostatectomy. Eur Urol 2006; 49(1): 38–48.
45. Masterson TA, Serio AM, Mulhall JP et al. Modified technique for neurovascular bundle preservation during radical prostatectomy: association between technique and recovery of erectile function. BJU Int 2008; 101(10): 1217–1222.
46. Ahlering TE, Eichel L, Skarecky D. Rapid communication: early potency outcomes with cautery-free neurovascular bundle preservation with robotic laparoscopic radical prostatectomy. J Endourol 2005; 19(6): 715–718.
47. Menon M, Kaul S, Bhandari A et al. Potency following robotic radical prostatectomy: a questionnaire based analysis of outcomes after conventional nerve sparing and prostatic fascia sparing techniques. J Urol 2005; 174(6): 2291–2296.
48. Kaul S, Savera A, Badani K et al. Functional outcomes and oncological efficacy of Vattikuti Institute prostatectomy with Veil of Aphrodite nerve-sparing: an analysis of 154 consecutive patients. BJU Int 2006; 97(3): 467–472.
49. Lotan Y, Cadeddu JA, Gettman MT. The new economics of radical prostatectomy: cost comparison of open, laparoscopic and robot assisted techniques. J Urol 2004; 172 : 1431–1435.
50. Begg CB, Riedel ER, Bach PB et al. Variations in morbidity after radical prostatectomy. N Engl J Med 2002; 346(15): 1138–1144.
51. Eastham JA, Kattan MW, Riedel E et al. Variations among individual surgeons in the rate of positive surgical margins in radical prostatectomy specimens. J Urol 2003; 170 : 2292–2295.
52. Atug F, Castle EP, Srivastav SK et al. Positive surgical margins in robotic-assisted radical prostatectomy: impact of learning curve on oncologic outcomes. Eur Urol 2006; 49(5): 866–871.
53. Rocco F, Carmignani L, Acquati P et al. Early continence recovery after open radical prostatectomy with restoration of the posterior aspect of the rhabdosphincter. Eur Urol 2007; 52(2): 376–383.
54. Ahlering TE, Skarecky D, Borin J. Impact of cautery versus cautery-free preservation of neurovascular bundles on early return of potency. J Endourol 2006; 20(8): 586–589.
Labels
Paediatric urologist Urology
Article was published inUrological Journal

2009 Issue 4-
All articles in this issue
- Vývoj a implementace laparoskopické simulace na zvířecím modelu v rámci urologických tréninkových programů
- Jak lépe pracovat s odbornou literaturou
- Technika se zachováním cév při operaci striktury v proximální anteriorní části močové trubice: primární anastomóza a augmentovaná anastomóza
- Léčba hyperaktivního měchýře u žen
- Roboticky asistovaná laparoskopická prostatektomie: kritické hodnocení výsledků
- Srovnání peroperačního průběhu, časných komplikací a funkčních výsledků robotické a otevřené radikální prostatektomie
- Operační anatomie prostaty a pánevního dna pro účely provádění radikální prostatektomie a radikální cystektomie: nejdůležitější body pro dosažení onkologické bezpečnosti, kontroly močové kontinence a erektilní funkce
- Kryochirurgická operace lokalizovaného karcinomu prostaty v počátečním stadiu: přechod od léčby celé prostatické žlázy k fokální kryoablaci
- Možnosti léčby kostního postižení u karcinomu prostaty
- Roboticky asistované a laparoskopické urologické operační výkony ve Spojených Státech: současný stav
- Urological Journal
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Srovnání peroperačního průběhu, časných komplikací a funkčních výsledků robotické a otevřené radikální prostatektomie
- Operační anatomie prostaty a pánevního dna pro účely provádění radikální prostatektomie a radikální cystektomie: nejdůležitější body pro dosažení onkologické bezpečnosti, kontroly močové kontinence a erektilní funkce
- Roboticky asistovaná laparoskopická prostatektomie: kritické hodnocení výsledků
- Kryochirurgická operace lokalizovaného karcinomu prostaty v počátečním stadiu: přechod od léčby celé prostatické žlázy k fokální kryoablaci
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

