-
Medical journals
- Career
Trombotické mikroangiopatie
Authors: J. Novotný; M. Penka
Authors‘ workplace: Oddělení klinické hematologie FN Brno, Jihlavská 20, 625 00 Brno
Published in: Transfuze Hematol. dnes,26, 2020, No. 2, p. 80-90.
Category:
Overview
Trombotické mikroangiopatie představují skupinu heterogenních onemocnění, charakterizovaných diseminovanou tvorbou mikrotrombů v arteriolách a kapilárách s rezultující konzumpcí trombocytů, mikroangiopatickou hemolytickou anémií a potenciálním ischemickým poškozením orgánů. Diagnóza trombotických mikroangiopatií může být obtížná, jelikož se příznaky jednotlivých syndromů mohou překrývat. Pro trombotickou trombocytopenickou purpuru svědčí aktivita enzymu ADAMTS 13 (a disintegrin and metalloprotease with thrombospondin motif 13) pod 10 % s eventuálním průkazem IgG inhibitoru, hovoříme zde o autoimunní trombotické trombocytopenické purpuře. Vrozená trombotická trombocytopenická purpura vzniká na základě mutací v genu pro ADAMTS13 (Upshawův Schulmanův syndrom), kdy neprokazujeme přítomnost inhibitoru. Při snížené aktivitě ADAMTS13 dochází ke zvýšené koncentraci vysokomolekulárních multimerů von Willebrandova faktoru se zvýšenou afinitou k trombocytárním receptorům GPIb, což vede k agregaci krevních destiček. Terapii volby získané trombotické trombocytopenické purpury představuje vysokoobjemová výměnná plazmaferéza, obvykle s imunomodulační léčbou kortikoidy. U vrozené trombotické trombocytopenické purpury zpravidla postačí terapie plazmou bez plazmaferézy. Hemolyticko-uremický syndrom přichází nejčastěji jako typický hemolyticko-uremický syndrom v souvislosti s infekcí shiga toxiny produkující Escherichia coli. Shiga toxiny jsou toxické pro endotelie a navíc aktivují trombocyty. V popředí syndromu je výrazné poškození ledvin, mnohdy s nutností hemodialýzy. Onemocnění předcházejí hemoragické průjmy. Terapie je převážně podpůrná. Daleko méně častou formou je atypický hemolyticko-uremický syndrom na bázi dysregulace alternativní dráhy aktivace komplementu. Prokazujeme zde heterozygotní mutace v genech pro regulační proteiny této dráhy a/nebo v genech kódujících složky komplementu. U některých nemocných lze prokázat protilátky proti faktoru H. V popředí léčby těchto forem hemolyticko-uremického syndromu je indikace podání inhibitoru C5 složky komplementu v podobě eculizumabu. Sekundární trombotické mikroangiopatie vídáme při diseminovaných malignitách, po některých lécích, v graviditě a šestinedělí, u autoagresivních onemocnění, u defektu cobalaminu C (CblC), u poruchy diacylglycerol kinázy epsilon, u řady infekcí, u pacientů s transplantací hemopoetických kmenových buněk nebo solidních orgánů, u maligní hypertenze. Vždy je nutno od těchto syndromů odlišit syndrom diseminované intravaskulární koagulace, pro nějž svědčí prodloužené koagulační testy aPTT a PT.
Klíčová slova:
trombotická trombocytopenická purpura – hemolyticko-uremický syndrom – trombotické mikroangiopatie – HELLP syndrom – terapeutická plazmaferéza – eculizumab
Trombotické mikroangiopatie (TMAs) představují skupinu heterogenních onemocnění charakterizovaných diseminovanou tvorbou trombů v arteriolách a kapilárách s rezultující konzumpcí trombocytů, mikroangiopatickou hemolytickou anémií (MAHA) a potencionálním ischemickým poškozením orgánů (end organ injury) [1]. Trombotická trombocytopenická purpura (TTP) a hemolyticko-uremický syndrom (HUS) jsou prototypy TMAs, ačkoli TMAs se mohou manifestovat sekundárně při mnoha dalších systémových jednotkách, včetně maligní hypertenze, autoagresivních onemocnění, infekcí, polékových TMAs, malignit a porodnických komplikací [2, 3]. TMAs se mohou vyskytnout rovněž u pacientů s transplantací kmenových buněk krvetvorby a u transplantací solidních orgánů.
TROMBOTICKÁ TROMBOCYTOPENICKÁ PURPURA – CHOROBA MOSCHCOWITZOVÉ
Klasická trombotická trombocytopenická purpura (TTP) je způsobena přítomností vysokomolekulárních multimerů von Wilebrandova faktoru (ultra-large multimers of vWF – ULVWF) s rezultující tvorbou mikrotrombů destiček v arteriolách a kapilárách v důsledku interakce těchto multimerů s destičkovým glykoproteinem Ib (GPIb). Incidence TTP se odhaduje v poměru 3,7–4,4 na 1 milion obyvatel [4]. TTP byla poprvé popsána Eli Moschcowitzovou v roce 1924 [5]. Vysokomolekulární multimery vWF jsou po uvolnění z Weibelova-Paladeho tělísek (WP bodies) endotelií štěpeny enzymem ADAMTS13 (a disintegrin and metalloproteinase with thrombospondin motifs 13) na menší fragmenty. Nízká aktivita ADAMTS13 (pod 10 %) přichází jednak při mutacích v genu pro ADAMTS13 jako vrozená TTP – Upshawův-Schulmanův syndrom (USS) a častěji při výskytu protilátek proti ADAMTS13 – autoimunní TTP. Bylo popsáno více jak 100 kauzálních mutací v genu pro ADAMTS13 v homozygotní nebo compound heterereozygous formě [4].
Klinický obraz
Klasická TTP byla popsána pentádou příznaků (trombocytopenie s krvácivými projevy, MAHA, měnlivé neurologické příznaky, teplota, selhávání ledvin) [4], často však vídáme pentádu inkompletní – závažná trombocytopenie, MAHA, end organ failure. Mimo postižení CNS mohou být tangovány další orgány – ledviny, srdce, pankreas, gastrointestinální trakt apod. Jedná se o závažné onemocnění – mortalita TTP se i dnes pohybuje kolem 10–20 %, před zavedením terapeutické plazmaferézy se vyskytovala v 80 a více procentech. Závažné akutní selhávání ledvin s nutností hemodialýzy je vzácné a svědčí spíše pro HUS [6]. Klinické příznaky TTP jsou shrnuty v tabulce 1.
Table 1. Klinické příznaky TTP 
TIAs – tranzitorní ischemické ataky, GIT – gastrointestinální trakt, MAHA – mikroangiopatická hemolytická anémie, LDH – laktátdehydrogenáza, HUS – hemolyticko-uremický syndrom, AIM – akutní infarkt myokardu Pro MAHA svědčí nález schistocytů (více jak 1 %) v periferním nátěru s hyperbilirubinemií, vysokou hladinou LDH, poklesem haptoglobinu a negativním Coombsovým testem. Kardinálním vyšetřením u TTP je stanovení aktivity ADAMTS13 spolu se stanovením přítomnosti protilátek proti této proteáze (nejčastěji IgG4). Pro TTP svědčí aktivita ADAMTS13 pod 10 %. U vrozené TTP (USS) nacházíme nízkou hladinu ADAMTS13 (< 5–10 bez přítomnosti protilátek. Daleko častěji však protilátky detekujeme, hovoříme pak o autoimunní TTP (iTTP). Laboratorní stanovení aktivity ADAMTS13 detekují testy se substrátem v podobě intaktního vWF (Hemate P) nebo syntetizovaných oligopeptidů vWF. Nejpopulárnějšími testy jsou vyšetření na bázi fluorescence resonance energy transfer (FRET) se substráty v podobě peptidů FRETS-vWF73 a FRETS-vWF71. FRETS-vWF71 je citlivějším testem a na rozdíl od FRETS-vWF73 zde není interference s hyperbilirubinemií a hemoglobinemií. Čas stanovení těchto testů je cca 1 h [7]. Nadějným vyšetřením je test na bázi SELDI-TOF (surface enhanced laser desorption/ionization time-of flight) hmotnostní spektrometrie, který je však ve většině klinických laboratoří nedostupný [8]. Existuje celá řada komerčních testů stanovení ADAMTS13 a přítomnosti inhibitoru se zřejmými diskrepancemi mezi jednotlivými testy, neexistuje mezinárodní standard [9, 10].
Je třeba zdůraznit nutnost co nejrychlejší diagnózy a zejména co nejrychlejšího zahájení léčby plazmaferézami, tady v případě nedostupnosti rychlého stanovení ADAMTS13 i před potvrzením diagnózy. Optimální je standardizace postupu zahrnující zhodnocení nálezu na sklíčku z hlediska přítomnosti schistocytů a rychlé předání informace o suspektní MAHA žádajícímu lékaři. Odběr krve na stanovení aktivity ADAMTS13 nutno provést před zahájením léčby plazmaferézou.
Genetická vyšetření objasní možnou etiologii vrozené TTP (USS). Vrozené formy TTP se vyskytují u cca 5 % pacientů s TTP. Jedná se o autozomálně recesivní mutace, bylo jich popsáno více jak 100 (missense, nonssense, splice site, frameshift, delece nebo inserce). USS má bimodální distribuci – prvá epizoda TTP se objeví u dětí starých 2–5 let a druhý vrchol v časné dospělosti [4]. K manifestaci USS dochází často po vyvolávajících momentech – infekcích, v graviditě aj. Tíže poklesu aktivity ADAMTS13 má prognostický význam v podobě stupně postižení a možných recidiv. Gen pro ADAMTS13 se nachází na 9. chromozomu (9q34), má 29 exonů a obsahuje 37 kb. Syntéza ADAMTS13 probíhá hlavně v játrech.
U některých nemocných s chronicky sníženou aktivitou ADAMTS13 na základě vrozené či získané deficience může být pozorován mnohaletý bezpříznakový průběh, kdy k manifestaci TMA dojde na základě infekce nebo jiného vyvolávajícího faktoru (second hit), který vede ke zvýšenému uvolňování ULVWF. Pro aktivitu TMA svědčí cirkulující DNA a myeloperoxidáza [11].
Pokud jde o vazbu HLA na TTP, Amin Asnafi et al. diskutovali roli HLA-DRB1*11 a HLA-DQB1*02 v etiopatogenezi TTP [12].
Diferenciální diagnóza TTP
Od TTP nutno odlišit ostatní TMAs, zvláště typický hemolyticko-uremický syndrom (STEC-HUS) a atypický HUS – aHUS. V těhotenství přichází HELLP syndrom (hemolysis, elevated liver enzymes, low platelets), často spojený s preeklampsií. Dále je nutno odlišit syndrom diseminované intravaskulární koagulace (DIC), kde pomohou klasické koagulační testy (aPTT a PT), které jsou u TTP v normě. Všechny TMAs však mohou sekundárně přejít v DIC. V diferenciální diagnostice TTP je dále indikováno odlišení jiných trombocytopenií – imunní trombocytopenii (ITP), heparinem indukovanou trombocytopenii (HIT), pseudotrombocytopenii, Evansův syndrom, acute fatty liver in pregnancy (AFLP), sepsi, kardiopulmonární bypass. Častou diagnózou v graviditě je benigní těhotenská trombocytopenie v souvislostí s hemodilucí.
Sekundární TMAs vídáme u maligní hypertenze, po lécích, infekcích, u autoagresivních onemocnění, při malignitách apod. (tab. 2).
Table 2. Diferenciální diagnóza TMAs 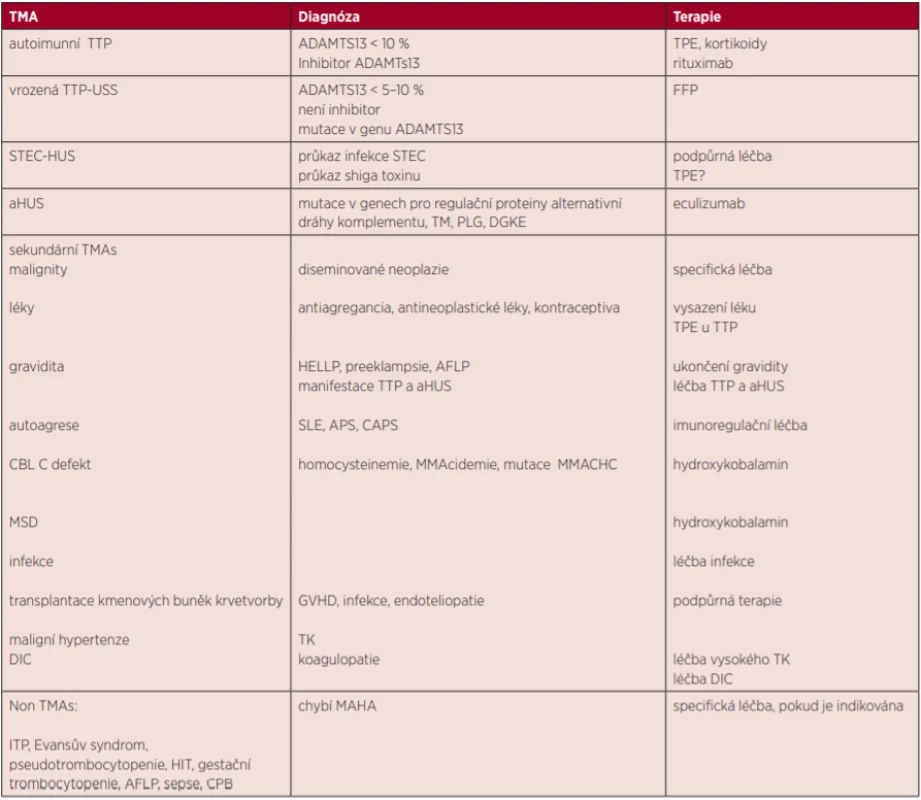
STEC – shiga toxin Escherichia coli, USS – Upshawův-Schulmanův syndrom, TMAs – trombotické mikroangiopatie, aHUS – atypický hemolyticko-uremický syndrom, TTP – trombotická trombocytopenická purpura, TPE – terapeutická léčebná plazmaferéza, SLE – systémový lupus erythematodes, APS – antifosfolipidový syndrom, CAPS – katastrofický APS, MMA – metylmalonic acid, MMACHC – metylmalonic aciduria and homocystinuria type C protein, GVHD – graft versus host disease, TK – tlak krevní, DIC – diseminovaná intravaskulární koagulace, TM – trombomodulin, PLG – plazminogen, DGKE – diacylglycerol kináza epsilon, MSD – defekt metionin syntetázy, AFLP – acute fatty liver in pregnancy, HIT – heparinem indukovaná trombocytopenie, CPB – kardiopulmonární bypass Terapie
Základním kamenem léčby získané autoimunitní TTP je terapeutická velkoobjemová výměnná plazmaferéza (therapeutic plasma exchange – TPE), kdy substituujeme 1–1,5 objemu pacientovy plazmy denně, což odpovídá cca 40–60 ml/kg [13]. Terapeutický efekt se projeví vzestupem počtu trombocytů, poklesem LDH v krvi a redukcí klinických příznaků. Mechanismem účinku TPE je eradikace inhibitoru ADAMTS13 a snížení koncentrace ULVWF s dodáním enzymu ADAMTS13. U vrozené TTP většinou postačí infuze čerstvé mražené plazmy bez nutnosti TPE [14]. Poločas ADAMTS13 je cca 2–3 dny. TPE často kombinujeme s podáním kortikoidů. Rituximab má své místo u pacientů s refrakterní, exacerbovanou nebo relabovanou TTP, i když existují doporučení pro up front použití u vysoce rizikových pacientů nebo při výrazném poklesu aktivity ADAMTS13 [1]. TPE postupně ukončujeme při vzestupu trombocytů nad 150 × 109/L dva dny po sobě. Významnou finanční úsporu představuje užití biosimilars rituximabu se srovnatelným klinickým efektem [15].
U rezistentní TTP (cca 10–15 % nemocných) je navíc možností indikovat TPE 2× denně, rituximab, cyklosporin, pulzy cyklofosfamidu, eventuálně bortezomib, který je zaměřen proti plazmocytům [13]. Dávkování bortezomibu odpovídá schématům terapie mnohočetného myelomu. Ve studiích se dále zkouší podání rekombinantního ADAMTS13, užití inhibitoru interakce ULVWF-destičkový glykoprotein Ib v podobě caplacizumabu [16], eventuálně lze indikovat splenektomii [17] u případů rezistentních na ostatní terapeutické modality. Caplacizumab je v ČR registrován a v dohledné době bude dostupný. Po vzestupu trombocytů nad 50 × 109/L je doporučena antitrombotická prevence aspirinem a/nebo LMWH [7]. Byl popsán příznivý efekt léčby ofatumumabem (anti-CD 20 druhé generace) u nemocné s hypersenzitivitou na rituximab [18]. U dvou nemocných s rezistentní TTP byl detekován příznivý léčebný účinek eculizumabu [19]. Indikace podání caplacizumabu byla podpořena studiemi TITAN a HERCULES [20]. Jelikož caplacizumab neovlivňuje primární patofyziologii onemocnění, dochází po jeho vysazení k exacerbaci nebo relapsu TTP. Nicméně caplacizumab výrazně zkrátí dobu uzavřené mikrocirkulace s významnými konsekvencemi pro „přežití“ orgánů a tkání. N-acetylcystein (NAC) modifikuje multimery ULVWF. Ve studiích Chena et al. vedlo podání NAC ke zmenšení multimerů VWF a k poklesu schopnosti VWF aglutinovat krevní destičky [21].
Závažný problém představuje recidivující TTP u nemocných s perzistujícím deficitem ADAMTS13. V terapii se zkouší postupy popsané u pacientů s primárně rezistentní TTP. Relaps TTP lze predikovat stanovením koncentrace imunitních komplexů ADAMTS13/IgG [22], v praxi spíše detekujeme opakující se významný pokles aktivity ADAMTS 13.
HEMOLYTICKO-UREMICKÝ SYNDROM
Hemolyticko-uremický syndrom (HUS) přichází buď ve formě typického, s infekcí asociovaného syndromu (STEC-HUS: Shiga toxin Escherichia coli), nebo jako atypický HUS – aHUS [23]. Nově se STEC-HUS označuje jako IA-HUS (infection-associated HUS) a aHUS jako CM-HUS (complement-mediated HUS). Na rozdíl od TTP není trombocytopenie většinou tak závažná (nad 30 × 109/L) a v popředí je výrazné postižení ledvin často s nutností hemodialýzy a s eventuální indikací transplantace ledviny. U STEC-HUS je příčinou endoteliopatie a aktivace trombocytů shiga toxiny, kterým předchází hemoragický průjem. STEC-HUS je daleko častější formou TMA než aHUS (85–90 %). U STEC-HUS se shiga toxiny (shiga toxin 1 a 2) vážou na receptor globotriaosylceramid (CD77, Gb3) na povrchu renálních endotelií [24]. Příčinou typického HUS může být i infekce Shigella dysenteriae sérotyp 1.
aHUS je vzácným onemocněním (incidence cca 0,5–2/milion), spojeným s dysregulací alternativní dráhy aktivace komplementu. Přichází u cca 5 % nemocných s HUS. Většina pacientů s aHUS vykazuje heterozygotní mutace v genech pro regulační proteiny této dráhy a/nebo v genech kódujících složky komplementu – buď loss of function (faktor H, faktor I, membrane cofactor protein (MCP/CD46), trombomodulin), nebo gain of function (C3, faktor B) [23]. U některých nemocných s aHUS byly prokázány protilátky proti faktoru H [23]. Uvedené mutace mají za následek hyperaktivaci alternativní cesty systému komplementu [25] s tvorbou MAC membrane attack complex C5b-C9 na povrchu endotelu a na trombocytech. Vrozené abnormality aktivace alternativní dráhy komplementu jsou detekovány u 70 % případů aHUS [26]. Mutace genu pro faktor H jsou zastoupeny přibližně v 30 % případů aHUS. Faktor H je hlavním regulačním faktorem alternativní dráhy komplementu a představuje kofaktorovou funkci pro serinovou proteázu v podobě faktoru I, který štěpí C3b a C4b. Autoprotilátky proti faktoru H jsou přítomny u cca 5–10 % případů aHUS [23]. Mutace v genu pro faktor I přicházejí u cca 10 % nemocných s aHUS. MCP/CD 46 je membránově vázaný kofaktor faktoru I a jeho mutace se vyskytují u až 15 % případů aHUS. Gain of function mutace C3 mají za následek hyperfunkci C3 konvertázy a jsou přítomny u cca 10 % pacientů s aHUS. Rovněž mutace faktoru B indukují hyperfunkci C3 konvertázy s výskytem u cca 4 % případů aHUS [23]. Defekty trombomodulinu jsou vzácné – vyskytují se pouze v cca 3 % případů. Je snížená aktivace TAFI na faktor TAFIa, který štěpí C3a a C5a [23].
K manifestaci aHUS často přichází v rámci second hit teorie v podobě infekcí, těhotenství apod. Mimo postižení ledvin může dojít k ischemickému poškození dalších orgánů – CNS, srdce, GIT apod. U postižení GIT může být detekován průjem, což znesnadní odlišení aHUS od STEC-HUS. aHUS se dále může manifestovat u řady infekcí, u maligních onemocnění, po lécích, u transplantací kmenových buněk krvetvorby, v průběhu těhotenství nebo u maligní hypertenze. Význam v etiopatogenezi aHUS mají i mutace v oblasti CFHR 1-5 (complement factor H-related proteins 1–5) zvláště CFHR 1 a 3.
Klinický obraz
V popředí klinického průběhu typického HUS – STEC-HUS je hemoragický průjem, který předchází manifestaci syndromu, s výskytem hlavně u dětí mladších 5 let. STEC-HUS má u dospělých horší prognózu. Nacházíme známky MAHA – schistocyty, vzestup LDH, pokles haptoglobinu, hyperbilirubinemii se vzestupem nekonjugovaného bilirubinu a trombocytopenii, která většinou není tak závažná jako u TTP (trombocyty nad 30 × 109/L) a výrazné poškození ledvin. U HUS i aHUS mohou být mimo závažné postižení ledvin i ischemická postižení dalších orgánů – CNS, srdce, GIT apod.
Laboratorní vyšetření
V popředí je detekce MAHA s trombocytopenií a selháváním ledvin s aktivitou ADAMTS13 nad 10 %, bez přítomnosti inhibitoru. Kultivačními a/nebo PCR testy lze detekovat infekci STEC, lze prokázat shiga toxiny v krvi nebo stolici [27]. Specializovaná vyšetření odhalí defekty alternativní dráhy systému komplementu u aHUS. Postižení orgánů se projeví vzestupem kreatininu, dále troponinu u kardiální léze atd. Pacienti s kardiálním defektem mají horší prognózu.
Diferenciální diagnóza
U jasného HUS nutno odlišit STEC-HUS od aHUS. Jinak platí diagnostika uvedená u TTP v tabulce 2.
Terapie
U STEC-HUS je hlavní terapií podpůrná léčba (hydratace, léčba hypertenze s eventuální hemodialýzou; antibiotická léčba je podle některých autorů kontraindikována). Někteří pacienti reagují na léčbu eculizumabem [28]. Shiga toxiny vážou faktor H, a mohou tak interferovat s jeho regulační funkcí aktivace komplementu [29].
Prognóza aHUS se dramaticky zlepšila se zavedením inhibitoru C5 složky komplementu v podobě eculizumabu. Nevyřešeným problémem terapie tímto inhibitorem je otázka vysazení eculizumabu, což je spojeno s rizikem rekurence aHUS [30]. U pacientů s protilátkou proti faktoru H je přístupem volby navíc terapeutická výměnná plazmaferéza TPE s eventuální imunosupresivní léčbou. Terapii eculizumabem lze monitorovat vyšetřením hladiny léku a/nebo stanovením aktivity komplementu (např. poměr C3 : CH50) s možností prodloužení nebo zkrácení intervalu podání eculizumabu [31]. Pacienti léčení eculizumabem jsou náchylní k infekcím enkapsulovanými bakteriemi, zvláště meningokoky, a doporučuje se vakcinace a antibiotická prevence těchto komplikací, navíc i vakcinace proti Haemophilus influenzae a pneumokokům. Byl popsán polymorfismus C5 zabraňující vazbě eculizumabu na C5. V těchto případech byl použit rekombinantní protein Coversin (alternativní C5 inhibitor) [32].
SEKUNDÁRNÍ TROMBOTICKÉ MIKROANGIOPATIE
Gravidita a šestinedělí
V graviditě a šestinedělí se mohou vyskytnout TTP i aHUS. Specifickou TMA v graviditě je HELLP syndrom (hemolysis, elevated liver enzymes, low platelets), kdy vedle eventuálního ukončení gravidity se zkoušela i léčba dexametazonem. Některé randomizované studie však neprokázaly účinnost steroidní terapie [33]. Nicméně u rozvinutého HELLP syndromu je dexametazon vnímán jako doporučený postup zlepšující vyzrávání plic novorozence i prognózu matky. HELLP syndrom je často manifestací v rámci preeklampsie se zvýšeným krevním tlakem a proteinurií [34]. V popředí klinického obrazu je bolest v pravém podžebří, mnohdy se známkami postižení i jiných orgánů. Afekce jater může vést i k hepatální ruptuře. Komplikacemi HELLP syndromu může být přechod v DIC, abrupce placenty, subkapsulární hematom až ruptura jater, selhání ledvin, plicní edém a postižení CNS ve smyslu ischemie či krvácení [35]. Jelikož v těhotenství dochází k aktivaci komplementu, byly publikovány kazuistiky podání eculizumabu u pacientek s HELLP syndromem [35].
Dále je nutno rovněž odlišit acute fatty liver of pregnancy (AFLP), kdy prokazujeme selhávání jater a prodloužené koagulační testy, pokles antitrombinu a albuminu a hypoglykemii [36].
Malignity
U hematologických i solidních neoplazií se může vyvinout sekundární TMA v podobě TTP/HUS postižení. Základem léčby v těchto případech je antineoplastická terapie. Nutno vždy odlišit syndrom DIC. TMAs u maligních onemocnění mohou být indukovány i při terapii cytostatiky (viz níže).
Léky
Bylo popsáno více jak 70 léků s možností indukovat TMAs [37].
Antiagregancia: ticlopidin a clopidogrel. U ticlopidinu je často výskyt inhibitoru ADAMTS13, pomůže zde vedle vysazení léku i TPE.
Antineoplastická léčba: mitomycin C, cisplatina, vincristin, gemcitabin, inhibitory calcineurinu – cyklosporin, tacrolimus, VEGF (vascular endothelial growth factor) inhibitory – bevacizumab, sunitinib, mTOR inhibitory: sirolimus, everolimus. Léčbou volby je vysazení léku a podpůrná terapie. U TMA po gemcitabinu byl popsán pozitivní efekt léčby eculizumabem [38]. Demirsoy et al. detekovali autoimunní TTP u pacienta s CML při terapii dasatinibem [39].
Kontraceptiva
Autoimunní onemocnění. Systémový lupus erythematodes, antifosfolipidový syndrom APS, dermatomyozitida. Základem léčby je terapie vyvolávajícího onemocnění. Mohou se zde však manifestovat jak TTP, tak i aHUS (second hit teorie). Katastrofický APS (CAPS) – jsou zde popsány pozitivní zkušenosti s terapií eculizumabem [40].
Vrozené poruchy metabolismu. Defekt kobalaminu C (Cbl C) je nejčastějším genetickým postižením metabolismu kobalaminu (vitamin B12) [41]. Absorpce, transport, skladování a intracelulární metabolismus Cbl C je komplexní, což se obráží ve vysokém počtu nejméně 21 genů regulujících tyto procesy u člověka [20]. Defekt Cbl C je způsoben mutacemi v genu Cbl C, který je umístěn na krátkém raménku 1. chromozomu (1p34.1). Gen je znám pod akronymem MMACHC (metylmalonic aciduria and homocystinuria type C protein), v současné době je popsáno více jak 80 mutací. Mutace jsou autozomálně recesivní. Vázne konverze cyanokobalaminu na esenciální kofaktory metylkobalamin a adenosylkobalamin. V plazmě je zvýšená koncentrace homocysteinu a kyseliny metylmalonové. V klinickém obraze nacházíme postižení nervového systému, jater, ledvin a kostní dřeně a jiných orgánů. V popředí mohou být projevy aHUS. Pacienti mají normální až zvýšenou koncentraci vitaminu B12. Mortalita je vysoká (cca 40 %). Mechanismus TMA není znám, avšak homocystein poškozuje endotelie. Lékem volby je intramuskulární aplikace vysokých dávek hydroxykobalaminu, navíc medikace betainu a kyseliny listové [41].
Defekt kobalaminu G: deficience metionin syntetázy (MSD) představuje vrozený defekt metabolismu kobalaminu s projevy megaloblastické anémie a neurologickými poruchami. Je zvýšená hladina homocysteinu. Hladina vitaminu B12 je v normě. Byl popsán HUS, reagující na léčbu hydroxykobalaminem intramuskulárně [42]. Mutace v genu pro metionin syntetázu jsou autozomálně recesivní.
Perniciózní anémie. Tran prokázal 68% výskyt perniciózní anémie u pacientů s deficiencí kobalaminu a projevy TMAs [43].
Infekce. Mohou být spouštěčem TTP i aHUS v rámci „second hit“ patofyziologie. Sekundární TMAs se mohou manifestovat po celé řadě infekcí, jak bakteriálních, tak virových, nutno vždy odlišit sepsi a DIC. Seznam možných vyvolávajících infekcí je zobrazen v tabulce 3.
Table 3. Infekce vyvolávající TMAs 
HIV – human immunodeficiency virus, CMV – cytomegalovirus, EBV – virus Ebsteina Barrové, HCV – virus hepatitidy C, HAV – virus hepatitidy A Neuraminidázou vyvolaný HUS. V etiopatogenezi této jednotky je infekce pneumokokem, kdy působením neuraminidázy je odkryt TF antigen (Thomsenův-Friedenreichův antigen) na erytrocytech a glomerulárním endotelu s následnou hemolýzou přirozenými anti-TF IgM protilátkami [23, 40]. Je pozitivní přímý Coombsův test. K manifestaci této jednotky dochází i při infekci influenzou A.
Transplantace hemopoetických kmenových buněk. Mechanismy potenciace TMAs v této situaci je pravděpodobně poškození endotelu radioterapií, chemoterapií, reakcí štěpu vůči hostiteli (GVHD), infekcí CMV. Terapie je symptomatická. U části nemocných byly prokázány genetické mutace systému komplementu s možností terapie eculizumabem [44]. TMAs se mohou objevit i u nemocných s transplantací solidních orgánů.
Maligní hypertenze vede k poškození endotelu. Terapií volby je agresivní léčba vysokého tlaku [45].
Diseminovaná intravaskulární koagulace (DIC)
K odlišení DIC poslouží globální koagulační testy (aPTT a PT), které jsou u non-DIC TMAs v normě. Všechny TMAs mohou však sekundárně vyústit v DIC [46]. U DIC dochází ke konzumpci ADAMTS 13, většinou je však aktivita enzymu nad 10 %.
Koagulační defekty. TMAs mohou být prokázány při vrozených defektech trombomodulinu a plazminogenu, tyto jednotky jsou velmi vzácné. Dochází k aktivaci koagulace a systému komplementu.
Diacylglycerol kináza epsilon (DGKE).Postižení funkce diacylglycerol kinázy epsilon (DGKE) je důsledkem recesivních mutací v genu pro DGKE. Pacienti se manifestují většinou v prvém roku života se známkami aHUS. Mechanismus vzniku TMA není přesně znám, u DGKE knock-out myší byly pozorovány poruchy metabolismu prostaglandinů v glomerulech ledvin [47]. Terapie je supportivní.
Monoklonální gamapatie. Ravindran et al. zaznamenali přítomnost monoklonální gamapatie u 13,7 % nemocných s TMA. Mechanismus indukce TMA není jasný [48].
Hadí jedy byly popsány TMAs po uštknutí hadem [49].
ZÁVĚR
TMAs jsou závažnými onemocněními spojenými i dnes s vysokou morbiditou a mortalitou. V současné době je největším přínosem v diagnostice i terapii TMAs stanovení aktivity enzymu ADAMTS13 a jeho IgG inhibitoru, což umožní odlišení vrozené i získané TTP od ostatních TMAs. U získané formy TTP je terapií volby velkoobjemová výměnná plazmaferéza (TPE). V oblasti diagnostiky a léčby aHUS došlo k posunu možností stanovením autozomálních mutací genů pro regulační proteiny alternativní dráhy aktivace komplementu s indikací podání inhibitoru C5 v podobě eculizumabu. U refrakterní TTP jsou k dispozici nové postupy, avšak závažná TTP s vysokým titrem inhibitoru ADAMTS13 má dnes i nadále za následek frekventní mortalitu (cca 10–20 %). U sekundárních TMAs většinou nejsou k dispozici specifické testy a terapie těchto jednotek spočívá v léčbě vyvolávající příčiny spolu s podpůrnou terapií. V patogenezi sekundárních TMAs mohou však hrát určitou roli dysbalance v systému komplementu a existují zde zprávy o dobré terapeutické odpovědi na eculizumab u některých refrakterních TMAs [50].
Seznam zkratek
ADAMTS13 – a disintegrin and metalloprotease with thrombospondin motif 13
AFLP – acute fatty liver in pregnancy
aHUS – atypický HUS
APS – antifosfolipidový syndrom
aPTT – aktivovaný parciální
CAPS – katastrofický APS
CFHR – complement factor H-related protein
CMV – cytomegalovirus
DGKE – diacylglycerol kináza epsilon
DIC – diseminovaná intravaskulární koagulace
FRET – fluorescence resonance energy transfer
GVHD – graft-versus host disease
HELLP – syndrom hemolysis, elevated liver enzymes, low platelets syndrom
HUS – hemolyticko-uremický syndrom
ITP – immunitní trombocytopenická purpura
MAC – membrane attack complex
MAHA – mikroangiopatická hemolytická anémie
MMACHC – metylmalonic aciduria and homocystinuria type C protein
MCP – membrane cofactor protein
PT – protrombinový čas
SELDI-TOF – surface enhanced laser desorption/ionization-time of flight
STEC – shiga toxin produkující E. coli
TMAs – trombotické mikroangiopatie
TPE – therapeutic plasma exchange
TTP – trombotická trombocytopenická purpura
ULVWF – ultralarge multimers of vWF
USS – Upshawův-Schulmanův syndrom
vWF – von Willebrandův faktor
Podíl autorů na přípravě rukopisu
JN – zpracoval rukopis
MP – provedl revizi rukopisu
Čestné prohlášení
Autoři práce prohlašují, že v souvislosti s tématem, vznikem a publikací tohoto článku nejsou ve střetu zájmů a vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou firmou.
Do redakce doručeno dne 22. 8. 2019.
Přijato po recenzi dne 12. 11. 2019.
MUDr. Jan Novotný, Ph.D.
Oddělení klinické hematologie FN Brno
Jihlavská 20
625 00 Brno
e-mail: novotnyjster@gmail.com
Sources
1. Saha M, Mc Daniel JK, Zheng XL. TTP: pathogenesis, diagnosis and potential novel therapeutics. J Thromb Hemost. 2017;15 : 1889–1900.
2. Caggl M, Aigner C, Sunder-Plassman G, Schmit A. Thrombotische mikroangiopathien. Med Klin Intensivmed Notfmed. 2016;111 : 434–439.
3. Salaj P. Thrombocytopenické purpury. Vnitř Lék. 2005;91 : 854–860.
4. Kremer Hovinga JA, Coppo P, Lämmle B, et al. TTP. Nat Rev/Dis Primers. 2017;3 : 1–17.
5. Moschcowitz E. Hyaline thrombosis of the terminal arterioles and capillaries: a hitherto undesribed disease. Proc N Y Pathol Soc. 1924;24 : 21–24.
6. Scully M, Hunt BJ, Benjamin S, et al. Guidelines on the diagnosis and management of TTP and other TMAs. Br J Haematol. 2012;158 : 323–335.
7. Muia J, Gao W, Haberichter SL, et al. An optimized fluorogenic ADAMTS13 assay with increased sensitivity for the incestigation of patients with TTP. Thromb Haemost. 2013;11 : 1511–1518.
8. Jin M, Cataland S, Bissel M, Wu HM. A rapid test for the dia-gnosis of TTP using SELDI-TOF-mass spectrometry. J Thromb Haemost. 2006;4 : 333–338.
9. Mackie I, Langley K, Chitolie A, et al. Discrepancies between ADAMTS13 activity assays in patients with TMAs. Thromb Hameost. 2013;109 : 488–496.
10. Peyvandi F, Palla R, Lotta A, et al. ADAMTS13 assays in TTP. Thromb Haemost. 2010;8 : 361–340.
11. Fuchs TA, Kremer Hovinga JA, Schatzberg D, et al. Circulating DNA and myeloperoxidase indicate disease activity in patients with TMAs. Blood. 2012;120 : 1157–1164.
12. Amin Asnafi A, Jalati MT, Pezeshki SMS, et al. The association between HLAs nad ITP, TTP and HIT. J Pediat Hematol Oncol. 2019;41 : 81–86.
13. Coppo P. Management of TTP. Transfus Clin Biol. 2017;24 : 148–158.
14. Čermáková Z, Blahutová Š, Kořístka M, et al. První zkušenosti jednoho centra s použitím přípravku Octaplas v léčbě pacientky s vrozenou formou TTP. Transfuze Hematol Dnes. 2012;18 : 162–164.
15. Stubbs MJ, Low R, McGuckin S, et al. Comparison of rituximab originator (MabThera) to biosimilar (Truxima) in patients with immune-mediated TTP. Br J Haematol. 2019;185 : 912–917.
16. Peyvandi F, Scully M, Kremer Hovinga JA, et al. Caplacuzimab for acquired TTP. N Engl J Med 2016;374 : 511–522.
17. Coppo P. Treatment of autoimmune TTP in the more severe forms. Transfus Apher Sci. 2017;56 : 52–56.
18. Al-Samkari H, Grace RF, Connors JM. Ofatumumab for acute treatment and prophylaxis of a patient with multiple relapses of acquired TTP. J Thromb Thrombolys. 2018;46 : 81–83.
19. Vigna E, Petrungaro A, Perri A, et al. Efficacy of eculizumab in severe ADAMTS 13 deficient TTP refractory to standard therapy. Transfus Apher Sci. 2018;57 : 247–249.
20. Dane K, Chaturvedi G. Beyond plasma exchange: novel therapies for TTP. Hematology. 2018;1 : 539–547.
21. Chen J, Reheman A, Gushiken FC, et al. N-acetylcysteine reduces the size and activity of VWF in human plasma and mice. J Clin Invest. 2011;121 : 593–603.
22. Mancini I, Ferrari B, Vaisecchi C, et al. ADAMTS 13-specific circulating complexes as potential predictors of relapse in patients with acquired TTP. Eur J Inter Med. 217;39 : 79–83.
23. Karpman D, Loos S, Tati R, Arvidsson I. HUS. J Inter Med. 2017;281 : 123–148.
24. Desch K, Motto D. Is there a shared pathophysiology for TTP and HUS? J Am Soc Nephrol. 2007;18 : 2457–2460.
25. Laurence J, Haller H, Mannuccio Mannucci P, et al. aHUS: Essential aspects of an accurate diagnosis. Clin Adv Hematol Oncol. 2016;14(S11):2–15.
26. Dixon BP, Gruppo RA. Atypical HUS. Pediat Clin N Am. 2018;65 : 509–525.
27. He X, Ardissino G, Patfield S, et al. An improved method for the sensitive detection of shiga toxin 2 in human serum. Toxins (Basel). 2018;10(2):59.
28. Fakhouri F, Loirat Ch. Anticomplement treatment in atypical and typical HUS. Semin Hematol. 2018;55 : 150–158.
29. Dixon BP, Gruppo RA. Atypical HUS. Pediat Cli N Am. 2018;65 : 509–525.
30. Sahutoglu T, Basturk T, Sakaci T, et al. Can eculizumab be discontinued in aHUS? Case report and review of the literature. Medicine. 2016;95 : 31–37.
31. Kerboua KE, Haiba F, Batouche D. C3:CH50 ratio as a proposed marker for eculizumab monitoring in aHUS. J Immunoasay Immunochem. 2017;38 : 178–189.
32. Wong EKS, Kavanagh D. Diseases of complement dysregulation – an overwiew. Semin Immunopathol. 2018;40 : 49–64.
33. Fonseca JE, Mendez F, Catano C, Arias F. Dexamethasone treatment dose not improve the outcome of women with HELLP sy.: a double-blind, placebo controlled, randomized clinical trial. Am J Obstet Gynecol. 2005;193 : 1591–1598.
34. Gumulec J, Šimetka O, Procházka M, et al. Diferenciální diagnostika trombocytopenie v graviditě. Vnitř Lék. 2010;56(S1):91–97.
35. Wallace K, Harris S, Adison A, Bean C. HELLP syndrome: Patho-physiology and current therapy. Curr Pharmaceut Biotechnol. 2018;19 : 816–826.
36. Thomas MR, Robinson S, Scully M. How we manage TMAs in pregnancy. Br J Haematol. 2016;173 : 821–830.
37. Wang XD, Zhang S, Li L, et al. Ticagrelor-induced TTP. A case report and review of the literature. Medicine. 2018;97 : 26–31.
38. Krishnappa V, Gupta M, Shah H, et al. The use of eculizumab in gemcitabine induced TMA. BMC Nephrol. 2018;19 : 26–31.
39. Demirsoy ET, Mehtap O, Atesoglu EB, et al. Dasatinib-induced immune mediated TTP. Transfus Apher Sci. 2018;57 : 222–224.
40. Akkeson A, Zetterberg E, Klintman J. At the cross section of TMA and aHUS: A narrattive review of differential diagnosis and a problematization of nomenclature. Therap Apher Dialys. 2017;21 : 304–319.
41. Beck BB, van Spronsen FJ, Diepstra A, et al. Renal TMA in patients with cblC defect: review of an under-recognized entity. Pediat Nephrol. 2017;32 : 733–741.
42. Vaisbich H, Braga A, Gabrielle M, et al. TMA caused by methionine synthase deficiency: diagnosis and teratment pifalls. Pediat Nephrol. 2017;32 : 1089–1092.
43. Tran PN, Tran MH. Cobalamine deficiency presenting with TMA features. A systematic review. Transfus Apher Sci. 2018;57 : 102–106.
44. Massias C, Vasu S, Cataland SR. None of above: TMA beyond TTP and HUS. Blood. 2017;129 : 2857–2863.
45. Villafuerte LHM, Pena PJM, Inigo GP, et al. Severe renal failure and TMA induced by malignant hypertension successfuly treated with spironolactone. Ann Cardiol Angiol. 2018;67 : 208–214.
46. Haram K, Mortensen JH, Mastrolia SA, Erez O. DIC in HELLP syndrome: how much we really know? Maternal Fetal Neonat Med. 2017;30 : 779–788.
47. Zhu J, Chaki M, Lu D, et al. Loss of DGKE in mice causes endothelial distress and impairs glomerulal Cox-2 and PGE2 production. Am J Physiol Renal Physiol. 2016;310:F895–F908.
48. Ravindran A, Go RS, Fervenza FC, Sethi S. TMA associated with monoclonal gammopathy. Kidney Int. 2017;91 : 691–698.
49. Rathnayaka N, Ranathunga PAN, Kularelne SA. TMA, HUS and TTP following Hump-nosed Pit Viper envenoming in Srí Lanka. Wilderness Environ Med. 2019;30 : 66–78.
50. Román E, Mendizábal S, Jarque I, et al. Secondary TMAs and eculizumab: a reasonable therapeutic option. Nefrologia. 2017;37 : 478–491.
Labels
Haematology Internal medicine Clinical oncology
Article was published inTransfusion and Haematology Today

2020 Issue 2-
All articles in this issue
- Editorial
- Trombotické mikroangiopatie
- Castlemanova nemoc, jedna z příčin chronické systémové zánětlivé reakce, někdy i retence tekutin, vaskulitid a poruch imunity – Mezinárodní diagnostická kritéria z roku 2017
- Léčba histiocytózy z Langerhansových buněk u dospělých osob
- Závěr života nemocných s nehodgkinským lymfomem, analýza souboru zemřelých během šesti let (2012–2017) na jednom pracovišti, integrace paliativní péče
- Skladování erytrocytů při nestandardní teplotě
- Theralite a mnohočetný myelom – známe už odpověď na efektivitu léčby nefrologa s hematologem?
- Překvapivý nález v kostní dřeni: co za ním je?
- Životní jubileum pana profesora Jiřího Mayera
- Transfusion and Haematology Today
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Castlemanova nemoc, jedna z příčin chronické systémové zánětlivé reakce, někdy i retence tekutin, vaskulitid a poruch imunity – Mezinárodní diagnostická kritéria z roku 2017
- Trombotické mikroangiopatie
- Překvapivý nález v kostní dřeni: co za ním je?
- Léčba histiocytózy z Langerhansových buněk u dospělých osob
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

