-
Medical journals
- Career
Neuroplasticita, restituce motorických funkcí a možnosti rehabilitace spastické parézy
Authors: O. Gál 1,2; M. Hoskovcová 1,2; R. Jech 2
Authors‘ workplace: Rehabilitační oddělení Neurologické kliniky a Centra klinických neurověd 1. LF UK a VFN v Praze 1; Centrum pro komplexní léčbu spasticity Neurologické kliniky a Centra klinických neurověd 1 . LF UK a VFN v Praze 2
Published in: Rehabil. fyz. Lék., 22, 2015, No. 3, pp. 101-127.
Category: Original Papers
Overview
Spastická paréza je významnou součástí klinického obrazu u většiny získaných poškození mozku. Příspěvek se nejprve věnuje reakci mozku na poškození a spontánním plastickým změnám v centrálním nervovém systému. Dále shrnuje recentní poznatky o rehabilitaci motorických funkcí po získaném poškození mozku v pseudochabém stadiu s důrazem na problematiku parézy, která v tomto stadiu dominuje. Ve druhé části je popsán klinický obraz jednotlivých typů zvýšené svalové aktivity (spasticita, spastická dystonie, flekční a extenční spasmy, spastická ko-kontrakce a spastické synkineze) a jsou definovány cíle rehabilitace ve spastickém stadiu s ohledem na současný stav poznání o možnostech indukce neuroplastických změn centrálního nervového systému. Popsány jsou terapeutické postupy ve vztahu ke třem hlavním příznakům léze horního motoneuronu, tj. svalovému zkrácení, svalové hyperaktivitě a streč-senzitivní paréze, a to včetně konceptu prof. Graciese Dohoda o reedukačním tréninku (Guided Self-rehabilitation Contract), který autoři prakticky využívají.
Klíčová slova:
zvýšená svalová aktivita, streč-senzitivní paréza, svalové zkrácení, neuroplasticita, dohoda o reedukačním tréninku1. REHABILITACE MOTORICKÝCH FUNKCÍ PO ZÍSKANÉM POŠKOZENÍ MOZKU V PSEUDOCHABÉM STADIU
1.1 Reakce na poškození mozku
Při získaném poškození mozku se spouští řada procesů, která společně s primárním poškozením ovlivňují klinický obraz. U cévních onemocnění mozku závisí vývoj funkčních a strukturálních ischemických změn na době trvání a poklesu perfúze (obr. 1). Při poklesu pod dolní hranici autoregulace dochází k oligémii, ale je zachována metabolická spotřeba v důsledku zvýšené extrakce kyslíku z krve a nedochází tak k žádným klinickým poruchám. Při dalším poklesu regionálního mozkového průtoku o více jak 50 % vzniká funkční reverzibilní dysfunkce (penumbra, neboli ischemický polostín), která je přítomna jen v akutním stavu a trvá pravděpodobně několik hodin. Při dalším poklesu pod 10-12 ml/100 g/min. dochází již k ireverzibilním strukturálním změnám, tj. mozkovému infarktu (10). Obecně lze říci, že u získaných poškození mozku reagují poškozené nervové dráhy retrográdní i ortográdní degenerací a u struktur, které jsou těmito drahami řízeny, lze pozorovat rozvoj denervační supersenzitivity. Při déletrvající denervaci funkčně souvisejících struktur se rozvíjí diaschisis, tedy hypofunkce a eventuální následná degenerace funkčně souvisejících neuronů, včetně odlehlých struktur, jakými jsou třeba α-motoneurony (107). Jejich úbytek na hemiparetické straně byl prokázán již v prvních třech měsících po CMP bez významnější progrese během dalších 9 měsíců (79). Ischemie mozkové tkáně vede rovněž ke vzniku mozkového edému. První fází v rozvoji otoku je cytotoxický edém, který postupně mizí a s různým časovým odstupem se s překryvem rozvíjí vazogenní edém v důsledku porušení hematoencefalické bariéry (10).
Image 1. Vývoj mozkového infarktu v závislosti na poklesu mozkové perfuze. (Modifikováno z Ambler, Bauer, 2010.) 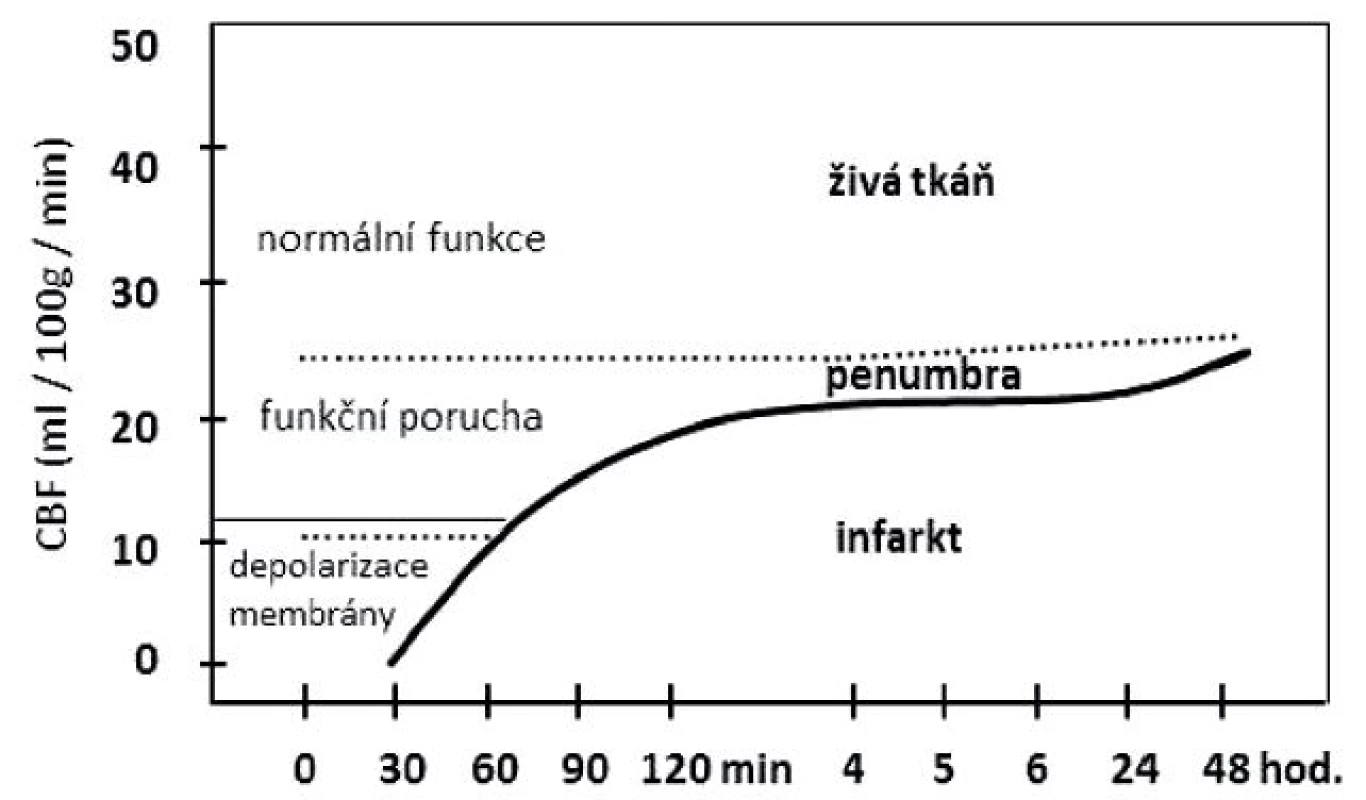
1.2 Plasticita a spontánní restituce motorických funkcí
Plasticita je definována jako schopnost adaptace na daný úkol v určitém prostředí. Jejím mechanismem je krátkodobě posílení synaptických spojení a dlouhodobě strukturální změny v organizaci a počtu spojů mezi neurony (177). V jádru těchto změn stojí dva procesy, a to dlouhodobá potenciace (long-term potentiation, LTP) a dlouhodobá deprese (long-term depression, LTD). Procesy vedoucí k LTP a LTD jsou dobře popsány u hippokampu, který je klíčovou strukturou pro formaci a vybavení určitých typů paměti (zejm. deklarativní). V případě, že stimulujeme Schafferovu kolaterálu CA3 pyramidových buněk a zaznamenáváme klidový postsynaptický potenciál CA1 pyramidové buňky, platí, že dochází k jeho navýšení za předpokladu, že je stimulace vysokofrekvenční a dostatečně intenzivní pro vyvolání postsynaptického potenciálu na CA1 pyramidové buňce (obr. 2). Kromě AMPA receptorů, na které se váže glutamát a které do buňky propouštějí Na+ ionty, se totiž glutamát váže také na NMDA receptory, které v případě současné depolarizace buněčné membrány umožňují vstup Ca2+. V případě, že je stimulace vysokofrekvenční, dochází k prudkému vzrůstu koncentrace Ca2+ iontů, což startuje procesy vedoucí nejprve k externalizaci nových AMPA receptorů, a tedy ke zvýšení senzitivity synapse. Při dlouhodobé stimulaci dochází k expresi proteinů, jež umožňují růst celé nové synapse (obr. 3). Jednoduše řečeno, je tedy LTP procesem dlouhodobého zvýšení synaptické síly mezi dvěma neurony (164). K LTD v těchto okruzích dochází naopak při nízkofrekvenční stimulaci o dostatečné intenzitě k vyvolání postsynaptické depolarizace. Nízký nárůst koncentrace Ca2+ iontů zde naopak vede ke kaskádě procesů, které ústí v internalizaci AMPA receptorů, a tedy ke snížení synaptické síly mezi oběma neurony (obr. 4). Předpokládá se, že tyto mechanismy leží v základu neuroplastických změn i v jiných oblastech CNS. Výzkum v této oblasti stále pokračuje a může se tedy v budoucnu ukázat, že popis těchto mechanismů nemusí být úplný.
Image 2. Dlouhodobá potenciace, LTP. (Převzato Purves, D. et al., Neuroscience 4ed 2014.) 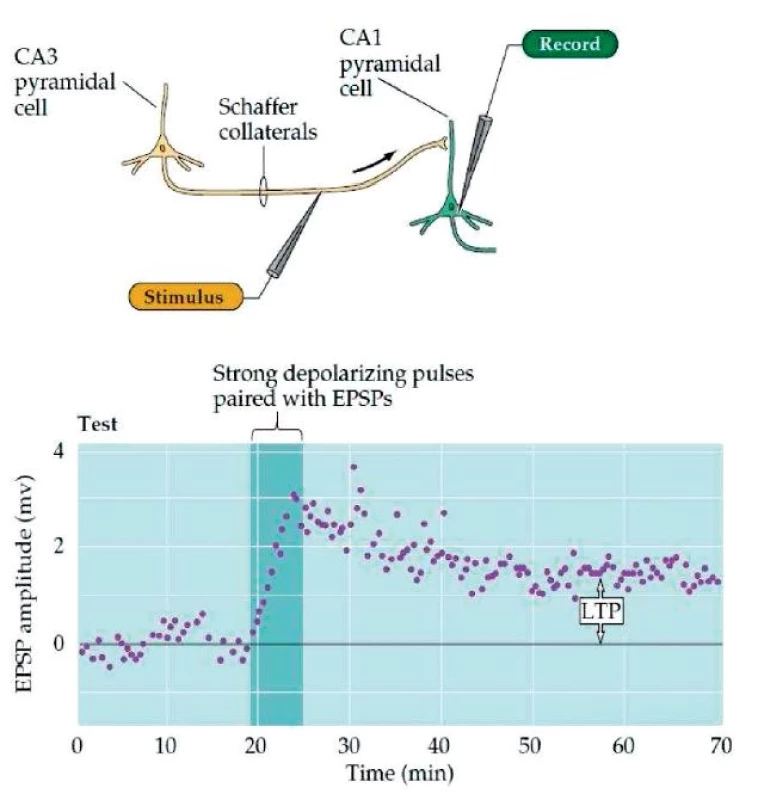
Image 3. Externalizace AMPA receptorů a růst nové synapse. (Převzato Purves, D. et al., Neuroscience 4ed 2014.) 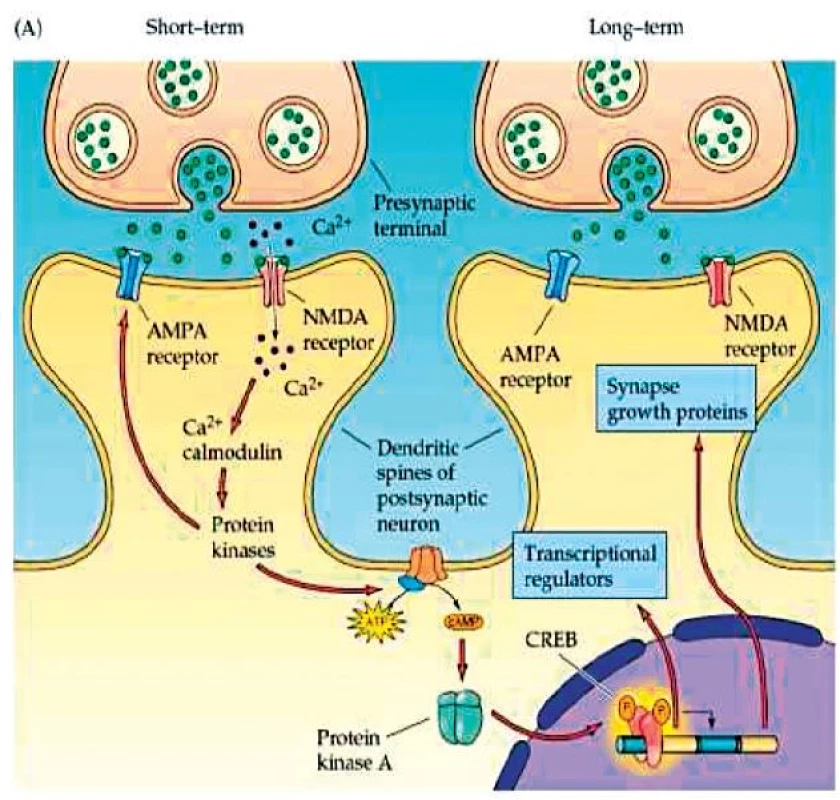
Image 4. Internalizace AMPA receptorů. (Převzato Purves, D. et al., Neuroscience 4ed 2014.) 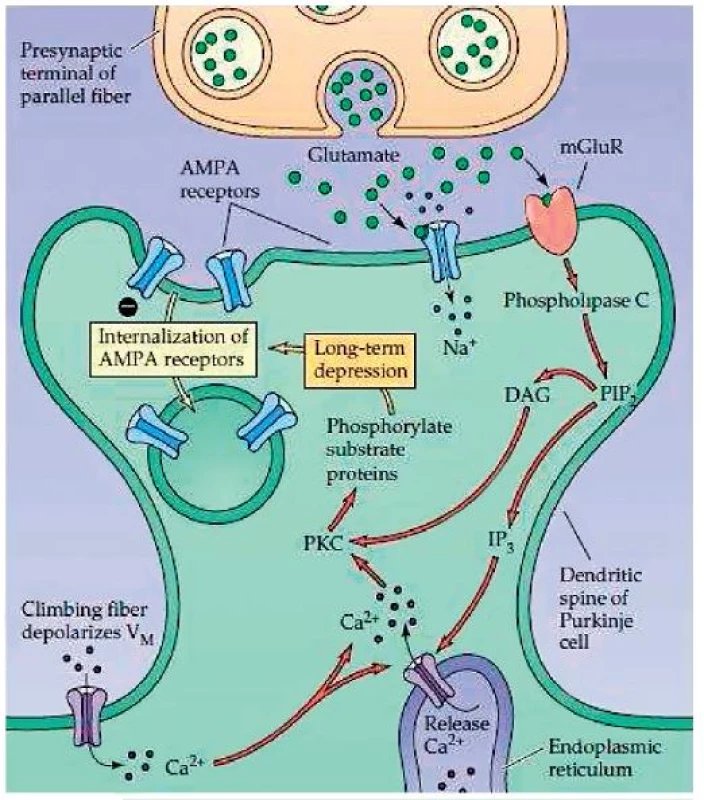
Spekuluje se o tom, že na principu LTP a LTD jsou vysoce pravděpodobně založeny jak veškeré typy motorického učení (41), tak jsou podkladem pro řadu procesů spontánní i indukované restituce motorických funkcí. Mechanismy spontánní restituce lze rozdělit na lokální, intra-hemisférické, inter-hemisférické a ostatní. Do lokálních patří reaktivní a regenerativní sprouting a synaptogeneze, jež byly prokázány přímo u kortikospinální dráhy (127, 146, 214). Intra-hemisférické změny zahrnují zvýšenou aktivaci sekundárních motorických oblastí (typicky premotorickou a suplementární motorickou oblast, motorické oblasti cingula a prefrontálního kortexu a některé oblasti parietální kůry (36, 203), přesun řízení na mimo-pyramidové dráhy (67), kortikální remapping (prokázaný např. mezi oblastmi ruky a ramene nebo ruky a obličeje) a aktivaci intaktní kortikální tkáně kolem léze (36, 203). Přesun řízení na mimo-pyramidové oblasti má závažné klinické důsledky, totiž ztrátu selektivního pohybu, zvýšenou námahu při iniciaci a provádění pohybu (v důsledku nižší schopnosti excitace α-motoneuronů těmito drahami) a diskrepanci ve schopnosti provedení pohybů v akrálních a proximálních částech končetin (v důsledku proximální projekce těchto drah). Distální pohyb může být totiž řízen pouze intaktními zkříženými vlákny kortiko-spinální dráhy a nezkříženými vlákny z kontralaterální nepostižené hemisféry (36). S tím souvisí právě inter-hemisférická reakce na lézi, tzn. supranormální aktivita kontralaterální (nepostižené) hemisféry. Jak ukázaly studie s trans-kraniální magnetickou stimulací (TMS), je tato hyperaktivita někdy přínosem u pacientů, kteří jeví celkově známky spíše špatné spontánní restituce. Lze předpokládat, že u nich je primární léze natolik rozsáhlá, že pro restituci motorických funkcí bude hrát klíčovou roli spíše reorganizace kontralaterální (nepostižené) primární motorické oblasti, která bude pohyb řídit přes nezkřížená vlákna kortiko-spinální dráhy, a případně přes zkřížená vlákna, která se sproutingem na míšní úrovni mohou podruhé „zkřížit“ a „napojit“ se na denervované α-motoneurony (203) (obr. 5). Byla také prokázána neogeneze spojů z kontralaterální hemisféry do mezencefala (obr. 5), kde je pak pohyb řízen přes rubro-spinální dráhu (36, 94). Naopak u pacientů s tendencí k dobré spontánní restituci může hyperaktivita kontralaterální hemisféry bránit dalšímu postupu restituce, protože má inhibiční spoje s poškozenými motorickými oblastmi druhé hemisféry, kde by mělo docházet k remappingu. U těchto pacientů je pak právě indikováno tlumení hyperaktivních oblastí pomocí TMS (203). Sám remapping může probíhat nejen v rámci sousedících oblastí poškozených částí primární motorické kůry, ale její funkci mohou převzít také kontralaterální dorzolaterální a bilaterálně ventrolaterální premotorická kůra či kontralaterální části mozečku (203). Konečně mezi ostatní mechanismy restituce patří obnova funkce v penumbře při její časné reperfúzi, stejně jako obnova funkce tkání „utlačených“ otokem při jeho ústupu.
Image 5. Schematické znázornění kortikospinální a kortikobulbární dráhy a jejich zkříženého sproutingu. (Převzato Chen, 2002.) 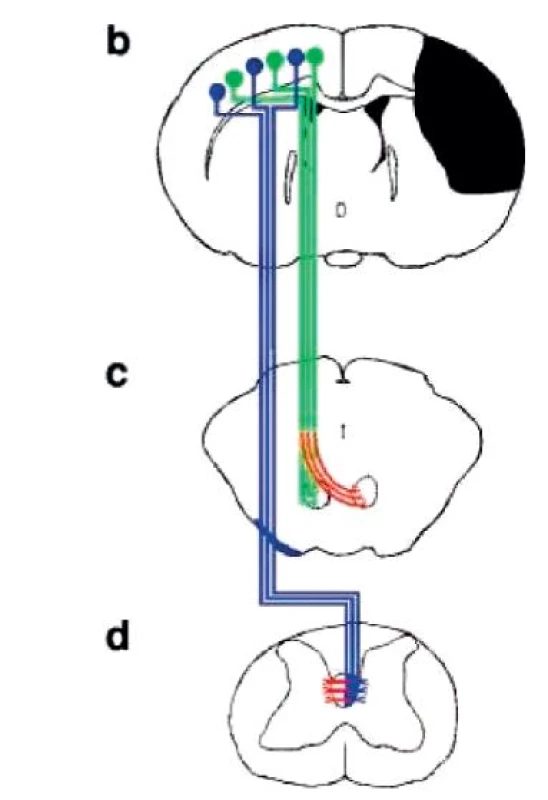
Přínos rehabilitace pro procesy spontánní restituce motorických funkcí není dosud dostatečně objasněn. Obecně lze říci, že za zlepšování pacientů v prvních týdnech po poranění mozku může z drtivé většiny čas (tzn. procesy spontánní restituce) a ne rehabilitační postupy (27). Nebyl dosud prokázán signifikantní rozdíl ve zlepšení motorických funkcí u pacientů s rehabilitací a bez ní v akutní fázi onemocnění. Zaznamenán byl pouze trend k vyšší míře zlepšení při časném zahájení rehabilitace. Z tohoto důvodu lze předpokládat synergický efekt spontánních a indukovaných plastických změn a na tomto předpokladu lze založit potřebu včasné rehabilitace (88). Na druhou stranu je z animálních modelů známo, že příliš intenzivní rehabilitace v prvních sedmi dnech po iktu vede k zvětšení objemu léze a zpožďuje restituci motorických funkcí (92). V akutní fázi je tedy třeba doporučit pouze střední intenzitu tréninku (123).
1.3 Cíle rehabilitace motorických funkcí v pseudochabém stadiu
1.3.1 Paréza
Paréza představuje nejvýznamnější faktor disability u syndromu centrálního motoneuronu (6). Kromě samotné centrální příčiny parézy přispívají k jejímu rozvoji také plastické změny na míšní a periferní úrovni. Mimo jiné dochází ke ztrátě vláken typu II ve prospěch vláken typu I, a tím vznikají obtíže s iniciací rychlých silových pohybů a s udržením konstantní svalové síly, i když zaznamenána byla i přeměna opačná (75, 149). Synaptickou degenerací α-motoneuronů dochází ke snížení počtu funkčních motorických jednotek, snížení rychlosti jejich pálení, k jejich abnormálnímu náboru a k dalším poruchám řízení motoriky. Pacienti s centrálním postižením jsou schopni využívat pouze neefektivní vzory svalové aktivace (76, 149). Tyto neurofyziologické poznatky nelze beze zbytku aplikovat u dospělých pacientů s DMO, i když centrální paréza jako taková se u nich pochopitelně manifestuje stejnými příznaky a minimálně v základu vyžaduje stejnou či podobnou terapii (18). Specifika práce se svalovou hyperaktivitou u dětských pacientů s DMO jsou uvedena v kapitole věnované této problematice.
Jakmile se začíná objevovat aktivní hybnost, pohyb se nerealizuje pouze v segmentu, ale aktivují se i další svaly v typických vzorcích („spastické synergie“), což je způsobeno převážně převedením řízení hybnosti na mimo-pyramidové dráhy (63). Míra aktivace dalších svalů obvykle odpovídá stupni nastupující spasticity. Vymizením spasticity a obnovením volní kontroly se zlepšuje i koordinace pohybu.
Při terapii paretických svalů v pseudochabém stadiu využíváme následující postupy:
Udržení svalové flexibility a kloubní integrity
Svalová flexibilita a kloubní integrita tvoří biomechanickou podmínku správného řízení svalové činnosti. Před vlastní terapií parézy vždy mobilizujeme klouby i měkké tkáně a provádíme cvičení na udržení rozsahů pohybu v kloubech. Aktivní i pasivní cvičeni kombinujeme s protažením do krajních poloh s respektem ke skapulohumerálnímu rytmu, tzn. při pohybu humerem pasivně navádíme do pohybu i lopatku. V opačném případě může i pasivní pohyb paží přispívat k rozvoji syndromu hemiparetického ramene.
Vzhledem k tomu, že i při intenzivní rehabilitaci tráví pacient drtivou většinu dne na lůžku, je třeba jej dynamicky polohovat podle jeho aktuálního stavu. V centrovaném postavení kloubů předpokládáme v pseudochabém stadiu ideální aferentaci do CNS, což je současně základem prevence senzorické deprivace a následků diaschisis, a v tomto smyslu jde i o svého druhu „terapii“ parézy. Základním principem polohování by mělo být neutrální (centrované) postavení v končetinových kloubech, které zajistí maximální přilnutí kloubních ploch a svalovou rovnováhu agonistů a antagonistů. V dalším průběhu onemocnění kombinujeme polohování vždy s protažením a následnou fixací končetiny nebo segmentu v určité poloze (manuálně, dlahou nebo pomocí přístroje). Při protahování rovněž dbáme na prevenci vzniku heterotopických osifikací. Obecně platí, že se řídíme subjektivním pocitem tahu ve svalu, který pacient udává, a nikdy nejdeme přes bolest (viz část 2.3.1). Důsledně dodržujeme fyziologické ROM, především u pacientů s poruchou čití. Dle možností pacienty instruujeme k autostrečinku, který bude v chronické fázi nezbytný, a není-li možný, využijeme polohovatelných ortéz nebo alespoň nafukovacích dlah, protože dodržení doporučené délky strečinku (alespoň 10 min. na každou svalovou skupinu – viz níže část 2.3.1) není v běžném nemocničním provozu možno zajistit s asistencí terapeuta.
Facilitační techniky a aktivace plegických a těžce paretických svalů
Podráždění z proprioceptorů či exteroceptorů může nahradit chybějící vzruchy z CNS a facilitovat příslušné interneurony nutné pro aktivaci daného periferního motoneuronu (199). Poruchu centrální iniciace signálu v descendentních drahách a jeho vedení poškozenými drahami lze nahradit aktivací alternativních korových oblastí a drah pomocí senzorických podnětů. Těchto principů využívá řada terapeutických postupů. Jedna z nejkomplexnějších technik, aplikujících multisenzorickou stimulaci CNS, je proprioceptivní neuromuskulární facilitace dle Kabata (PNF). Využívá facilitaci paretických svalů pomocí aktivace proprioceptorů protažením svalu před pohybem, aplikaci optimálního odporu, trakci nebo kompresi do kloubních ploch a specifický úchop končetiny, tj. taktilní vstup. Dále klade důraz na aktivní sledování pohybu ze strany pacienta (zrakový vstup) či provádění pohybů přesně dle vyřčených instrukcí (sluchový vstup). Tato technika vždy aktivuje příslušné svaly v synergických pohybových vzorcích, a proto lze využít fenoménu iradiace svalové síly ze silnějších svalových skupin do slabších. V neposlední řadě tvoří součást tohoto konceptu fenomén sukcesivní indukce, tj. zlepšeni podmínek kontrakce agonistů pomocí zlepšení předchozí aktivace antagonistů (srov. 7). Těchto principů využívá řada terapeutických postupů. Jejich přehled uvádí Umphred (196). Je však třeba si povšimnout, že řada těchto technik vychází ze vzájemně si protiřečících teoretických východisek. Některé syntetické postupy mají spíše snahu vyhýbat se zvýšenému svalovému napětí při provádění pohybu, dříve např. Bobath koncept (ozvuky tohoto přístupu lze nalézt ještě např. v Raine (165), i když Mayston (131) je již opatrnější), jiné tento fenomén v rámci sukcesivní indukce naopak s výhodou využívají, např. PNF či terapie podle Brunnstromové (28). Přesto nebyl zaznamenán žádný rozdíl mezi jejich efektem na funkci (16, 49, 185, 201).
U pacientů s plegií nebo velmi těžkou parézou se zprvu zaměřujeme na aktivaci svalu bez primárního požadavku na kvalitu pohybu (např. 175). Z hlediska evidence lze pro aktivaci plegických svalů doporučit intenzivní trénink pohybu v představě (mental imagery, mental practice (42, 160), blíže viz část 2.2), nebo zrcadlovou terapii (mirror therapy), která zvyšuje excitabilitu poškozené primární motorické kůry (42, 43) a ta se tak snáze aktivuje. Na základě animálních i humánních modelů by bylo možné se pokusit o využití kortikální reorganizace při sdruženém pohybu sousedících prstů, např. pomocí jejich svázání. Jak ukazují studie, je spojení kortikální reprezentace sousedních oblastí podmíněno časovou synchronicitou impulzů v těchto oblastech. Clark (32) zkoušel sešít u zdravých opic (Aotidae) sousední prsty, což vedlo ke změně jejich kortikální reprezentace ve smyslu jejich propojení. Již Clark spekuloval o časové synchronicitě aferentních impulzů jako příčině této reorganizace. Tato spekulace byla později znovu potvrzena v podobných experimentech (9). U lidí byla Mogilnerem (142) pozorována opačná kortikální reorganizace v reakci na chirurgické oddělení prstů u syndaktilie. V naší problematice by tedy bylo možné zkusit simulovanou syndaktilii pomocí svázání plegického prstu se sousedním paretickým prstem a jejich následná sdružená reedukace do doby, než se hybnost alespoň částečně obnoví.
Posilovací trénink
Podaří-li se sval aktivovat, pokoušíme se pomocí posilovacího tréninku o zlepšení parametrů jeho aktivity (síla, výkon a vytrvalost). K posílení dochází na základě neurální a muskulární adaptace. Neurální adaptace zahrnuje zvýšení excitability a konektivity příslušných kortikálních motorických oblastí a zlepšenou synchronizaci náboru motorických jednotek, přičemž tyto procesy jsou závislé na frekvenci a intenzitě stimulace neuroplastických procesů (viz část 1.2). Při zvolení zátěže, která převyšuje metabolickou kapacitu posilovaného svalu (princip přetížení), se objevují lokální změny ve svalu a kosti. Mezi tyto změny patří zvětšení počtu svalových vláken, zvýšení hladiny některých svalových enzymů, posílení ligament a šlach, zvýšení koncentrace minerálů v kostech aj. (100). Posilovací trénink musí být specifický. Na rozdíl od aerobního se při něm totiž zlepší pouze konkrétní trénovaný pohyb (např. posilovaní flexe v lokti s paží u těla zvýší svalovou sílu v této poloze, ale nezajistí stejně silnou flexi v lokti při abdukci v rameni). U aerobního tréninku se efekt přenáší i na jiné než trénované činnosti (např. jízda na kole zlepší i kardiovaskulární výkonnost při chůzi). Posilovat je třeba pravidelně, neboť za několik týdnů dochází k zániku vytrénované funkce (princip reverzibility). Svalovou sílu zvyšujeme aplikací vysokých zátěží s malým počtem opakovaní za krátký čas. Výkon trénujeme zvýšením zátěže nebo zkrácením času. Pro trénink vytrvalosti je nutno cvičit s malými zátěžemi, kdy se vyžaduje mnoho opakování za delší časový úsek. Pro řadu pacientů s centrálním typem parézy je často vhodné ovlivňovat nejprve svalovou vytrvalost a výkon a až později samotnou sílu. Posilovaní je možné s využitím vlastní hmotnosti i s náčiním, včetně přístrojové techniky (posilovací stroje). U pacientů bez schopnosti aktivního úchopu doporučujeme rukavice pro pasivní úchop. Při obtížích s fixací dolní končetiny na přístroji lze využít např. ortézu pro kotník a nohu (Ankle-Foot-Orthosis, AFO). Pacienti s těžším stupněm svalového oslabení cvičí v lehu či sedu. Využívají se techniky s vyloučením gravitace a s dopomocí při pohybu, jako jsou závěsné aparáty, různá mechanická a robotická zařízeni (Motomed, ReoGo aj.) či posuvné desky (Flowin aj.). Klasicky trénink kombinujeme s jednodušší (zrcadla) i komplexnější formou zpětné vazby (EMG, Kinect, Wii, virtuální realita aj.; k bližší diskusi o feedbacku a virtuální realitě srov. 2.2). Stále využíváme vizualizaci pohybu (cvičení v představě), která podporuje proces restituce motorické kontroly.
Vzhledem k množství dostupných technik si lze oprávněně klást otázku, kterou z nich zvolit pro dosažení maximálního efektu. Zdá se, že u pacientů s výraznou parézou není pravděpodobně typ posilovacího tréninku podstatný za předpokladu, že vede ke zvýšení svalové síly (tj. např. elektrostimulace, posilování v otevřených řetězcích se závažím, izometrické kontrakce, posilování na přístrojích atp.). Platí však, že od jistého prahu musí být trénink specifický vzhledem k požadované funkci (26).
Kombinovaný aerobní a posilovací trénink (tzv. aerobně-rezistentní trénink)
V současné době je doporučován klasický posilovací trénink v kombinaci s tréninkem aerobním (8, 39), je-li to u pacientů pro motorický deficit a další případné komorbidity možné. Je nutné provést zátěžovou spiroergometrii s přesnou indikací tréninkových parametrů. U pacientů s CMP je kontraindikováno posilování proti vysokému odporu a jsou vyloučena izometrická cvičení střední a vysoké intenzity. Pro rezistentní i aerobní trénink lze doporučit střídání více stanovišť, tj. formu kruhového tréninku (2, 3). Parametry posilovacího tréninku se obvykle pohybují v nízkých intenzitách, tj. 30–50 % maximální volní kontrakce, u aerobního tréninku kolem 40–60 %. Postupujeme vždy dle doporučení internisty.
1.3.2 Zkrácení a svalová hyperaktivita
V pseudochabém stadiu by se mohlo zdát, že zkrácení a svalová hyperaktivita nehrají žádnou roli. U pacientů je přítomné spíše snížení svalového napětí bez známek zkrácení a svalová hyperaktivita není přítomna z definice. K rozvoji kontraktur však může přispívat paréza, jelikož snižuje mobilitu končetiny. Pokud přetrvává déle, vede ke zkrácení tkání a nižšímu napětí a zatížení svalu. Dochází k atrofii svalových vláken, remodelaci pojivových nekontraktilních tkání se zvýšením tukové tkáně ve svalu, degenerativním změnám v přechodu mezi svalem a šlachou a k výraznější proliferaci kolagenu. Snižuje se rozsah pasivního protažení svalu („non-reflex stiffness“) a rozsah pohybu v kloubu s následným vznikem kontraktury. V animálních modelech bylo zjištěno, že po 6 hodinách imobilizace v plném zkrácení se významně snižuje syntéza svalových bílkovin. Toto snížení pravděpodobně zahajuje proces atrofie svalových vláken. Po 24 hodinách imobilizace se délka svalových vláken zkracuje o 60 % a po dvou dnech již dochází k nárůstu pojivového perimysia ve svalu (75). U reálných pacientů samozřejmě nevidíme tak rychlý průběh vzniku kontraktur, protože uvedená data jsou z animálních modelů v plném zkrácení svalu.
Z hlediska prevence možných budoucích kontraktur je tedy nutné ovlivňovat zkrácení již v časné fázi po získaném poškození mozku, jelikož rozvíjející se zkrácení bude potencovat svalovou hyperaktivitu mechanismem, jež bude popsán v části 2.3.1, a ta nadále prohlubuje parézu, jak bude vysvětleno v části 2.3.3.
Shrnutí: Cíle rehabilitace v pseudochabém stadiu
V pseudochabém stadiu se tedy primárně snažíme dosáhnout následujících cílů:
- Prevence senzorické deprivace a diaschisis, včetně trans-synaptické degenerace α-motoneuronů. Za tímto účelem používáme s výhodou veškeré syntetické postupy (tj. postupy na neurofyziologickém podkladě) ve snaze o aktivaci struktur funkčně spojených s lézí. Klíčové je zde také správné polohování dle zásad vývojové kineziologie, které lze v tomto smyslu definovat jako dlouhodobou optimalizaci aferentního vstupu tvořící základ pro multisenzorickou stimulaci.
- Prevence úbytku vláken typu II. Za tím účelem je třeba dle možností pacienta začít trénovat rychlé aktivní pohyby končetinami, a to bez primárního ohledu na „kvalitu“ prováděného pohybu.
- Využití terapeutického okna pro synergický efekt spontánní a indukované restituce. Jakkoliv není dosud tato souvislost prokázána, lze spekulovat o vzájemné potenciaci procesů spontánní a indukované restituce motorických funkcí a zacílení neuroplastických dějů na kortikální oblasti reprezentující trénované segmenty. Na druhou stranu je znovu třeba připomenout potenciální negativní efekt příliš intenzivního tréninku na spontánní restituci.
- Monitorace nástupu svalové hyperaktivity a zkrácení svalů. Jakmile se začne objevovat svalová hyperaktivita, je nutná okamžitá změna terapeutického přístupu, jak bude popsána v následující kapitole.
2. REHABILITACE MOTORICKÝCH FUNKCÍ PO ZÍSKANÉM POŠKOZENÍ MOZKU VE SPASTICKÉM STADIU
2.1 Klinický obraz spastické parézy
Léze centrálního motoneuronu vede k řadě klinických příznaků, které patří k některému ze základních symptomů triády paréza – zvýšená svalová aktivita – zkrácení svalu (63). Existuje i Jacksonův starší koncept, který klinické projevy centrální léze rozděluje na negativní a pozitivní příznaky. K negativním patří svalová slabost a ztráta koordinace volní motoriky u segmentů s částečně zachovanou inervací. K pozitivním patří zvýšení svalové rezistence při pasivním protažení, potažmo další projevy zvýšené svalové aktivity. Ať již přijmeme jakýkoliv model, v subjektivním obrazu pacienta dominuje paréza či plegie doprovázená abnormální posturou končetiny, která je výsledkem dysbalance svalového tonu agonistů a antagonistů. Při jednostranné supratentoriální lézi, např. při ischemii v karotickém povodí, vzniká typický obraz hemisyndromu s flekční posturou na horní a extenční na dolní končetině. Klasická trojflexe horní končetiny v prstech, zápěstí a lokti s pronací předloktí a doprovázená addukcí ramene je přitom jen jednou z variant postury při postižení v této lokalizaci. Na horní končetině se můžeme setkat s abdukcí ramene, extenzí lokte, supinovaným předloktím či s extendovanými prsty. Na dolní končetině zpravidla převažuje extenze kolene, plantární flexe s inverzí nohy, flexí prstů a extenzí palce. I zde existují výjimky s opačným klinickým obrazem postury. U spinálního typu léze, např. při transverzální míšní lézi, očekáváme spíše para-, mono-, tri - nebo kvadru - paretické postižení s dominující flexí dolních končetin v kolenou a kyčlích s addukcí stehen. Postura u spinálních lézí bývá navíc často měnlivá, kdy dolní končetiny přecházejí náhle z flexe do extenze a naopak (blíže viz příspěvek prim. Kříže).
Zvýšená svalová aktivita
Symptomy zvýšené svalové aktivity se po vzniku léze centrálního motoneuronu rozvíjejí postupně v horizontu týdnů až měsíců. S postupnou deliberací monosynaptických a polysynaptických míšních reflexů a po zapojení aberantní kortikální a míšní plasticity se tonus zvyšuje v podobě různých projevů, které mohou stávající motorickou poruchu dále zhoršit. Příznaky zvýšené svalové aktivity se přitom často navzájem kombinují, čímž vzniká komplexní klinický obraz, někdy souhrnně označovaný jako „spastic movement disorder“ (50). Zvýšenou svalovou aktivitu u centrálního typu léze je nutné klinicky odlišit od jiných patologických stavů doprovázených zvýšeným svalovým tonem. Jejich přehled přináší tabulka 1.
Table 1. Typy zvýšené svalové aktivity, které nepatří do obrazu spastické parézy. 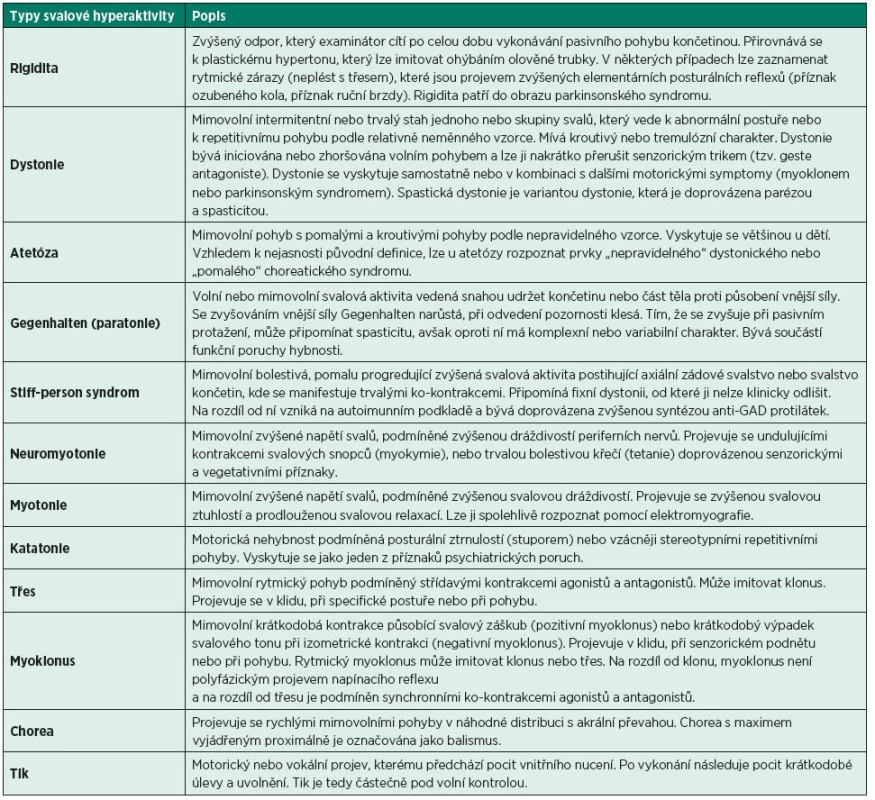
Spasticita
Spasticita je zvýšená svalová aktivita manifestující se nadměrnou excitabilitou napínacích reflexů. Při pomalém pasivním protažení lze sval protáhnout, zatímco při rychlém protažení vyšetřující cítí záraz („catch“), po kterém zvýšená aktivita mizí nebo částečně přetrvává do doby, kdy je pasivní pohyb ukončen. Čím rychleji je sval protažen, tím výraznější je jeho stah. Spasticita je tedy rychlostně vázané zvýšení svalového tonu (113), která, jak vplývá z definice, nemůže nikdy nastat v klidu, protože čistě spastický sval má nulovou klidovou aktivitu. Spasticita proto nemůže být zodpovědná za abnormální posturu končetiny. Spasticitu lze rozpoznat jen na základě subjektivního pocitu vyšetřujícího, neboť na pacientovi není vidět. Výjimkou je hyperreflexe napínacích reflexů, kterou vidět lze. Nutno doplnit, že rozlišujeme dva typy napínacích reflexů, fázické a tonické, jejichž práh je při spasticitě abnormálně snížen. Zjednodušeně řečeno, všechny monosynaptické napínací reflexy jsou fázické. Příkladem fázického reflexu je patelární reflex, kdy při poklepu dojde k náhlému protažení šlachy následované mohutnou, často polyfázickou kontrakcí čtyřhlavého stehenního svalu. Je-li práh dostatečně nízký, startuje se reflex samovolně a výsledkem je rytmický klonus (6-8 Hz), který jako jediný projev spasticity může u pacienta reálně přispívat k disabilitě. Tonické napínací reflexy na rozdíl od fázických nezávisejí na čase (a tedy rychlosti protažení), ale závisejí na intenzitě podnětu. Při tonickém reflexu je delší protažení svalu spojeno s vyšší intenzitou podnětu, a tedy s vyšší odezvou spastického svalu v podobě zvýšené svalové kontrakce. V extrémním případě spastická kontrakce přetrvává i při ukončení pasivního pohybu, tedy v situaci, kdy sval je dostatečně pasivně protažen. V takovém případě hovoříme o statickém napínacím reflexu (132), který se při opakování pohybu vyčerpává. Habituace znesnadňuje objektivní měření spasticity klinickými škálami (modifikovaná Ashworthova škála, Tardieuho škála), protože při opakovaném měření se skóre spasticity snižuje.
Spastická dystonie
Je dalším projevem zvýšené svalové aktivity u syndromu horního motoneuronu. Spastická dystonie je podmíněna mimovolním stahem paretických svalů za klidového stavu, což lze objektivizovat např. pomocí elektromyografie. Na rozdíl od spasticity je tedy na pacientovi vidět, protože je zodpovědná za abnormální posturu končetiny. Spastická dystonie významně přispívá k poruše funkce a pacientovi tak vadí daleko více než spasticita. Výsledná postura závisí na tom, zda převáží kontrakce flexorů nebo extenzorů. Klasické Wernicke-Mannovo držení s trojflexí horní a extenzí dolní končetiny je tedy projevem spastické dystonie. Pojem spastické dystonie byl zaveden pro typ svalové hyperaktivity při centrálním typu léze, který není vyprovokován externím podnětem a který se vyskytuje za situace bez volní svalové aktivity (48). Spastická dystonie je eferentního původu, protože nemizí ani po přetětí zadních kořenů. Dlouhodobě opakované pasivní protažení ji však potlačuje (76), takže nelze zcela akceptovat původní myšlenku, že spastická dystonie je na aferentním systému zcela nezávislá. Vedlejšími negativními projevy spastické dystonie je ztížené polohování a oblékání končetiny, nedostatečná hygiena (dlaně, axily, třísel) a v neposlední řadě nepříznivé sociální stigma, které díky abnormální postuře končetiny neujde pozornosti okolí. Důsledky spastické dystonie nemusejí být vždy negativní. Sevřenou nebo drápovitou ruku může pacient využít k přidržení láhve nebo nesení tašky, extenční postura dolní končetiny může zlepšovat její opěrnou funkci ve stoji a chůzi. Nutno dále podotknout, že ne každá postura je u syndromu centrálního motoneuronu podmíněna vždy jen spastickou dystonií. Může být zcela nebo částečně podmíněna zkrácením svalu, šlachy nebo retrakcí kloubního pouzdra.
Flekční a extenční spasmy
Imponují jako spastická dystonie, od které se však liší svým původem. Postihuje zejména flexory a vznikají na podkladě deliberace polysynaptických míšních reflexů. Oproti spastické dystonii jsou iniciovány aferentním podnětem, ke kterému je somatosenzorický systém díky sníženému prahu zvýšeně vnímavý (132). Na rozdíl od spasticity mají delší latenci a šíří se na další svalové skupiny. Lehký dotyk, zarostlý nehet, přeplněný močový měchýř nebo zánětlivá kožní iritace jsou pro jejich vznik dostatečně silným podnětem. Výsledkem je pomalu narůstající tonická křeč, která postihuje několik sousedních segmentů. Příkladem je mimovolní extenze palce nohy (striatální palec, Babinského příznak) nebo spastická trojflexe dolní končetiny po nociceptivním podnětu v oblasti planty. Flekční a extenční spasmy se vyskytují především u spinálních lézí, kde mívají charakter epizodických křečí. Mají tendenci k šíření na druhostrannou končetinu, mohou být bolestivé nebo omezovat sed, stoj či polohování.
Spastická ko-kontrakce
Pro správné provedení volního pohybu je kromě aktivace agonisty neméně důležitá relaxace antagonisty. V případě spastické ko-kontrakce je však antagonista kontrahován spolu s agonistou, což vede ke špatné koordinaci volního pohybu (200). Zatímco spastická dystonie se vyskytuje v klidu a lze na ni pohlížet jako na fixní dystonii, spastická ko-kontrakce se projevuje výhradně při aktivním pohybu a představuje ekvivalent mobilního typu dystonie (63). Spastická ko-kontrakce obvykle vadí pacientovi ze všech projevů zvýšené svalové aktivity nejvíce, protože se stupňuje se subjektivním úsilím a výrazně interferuje s volní motorickou činností. Primárním podnětem je volní pohyb, při kterém selhává mechanismus reciproční inhibice (37) a kdy je vzruch aberantně veden současně k agonistům i antagonistům téhož svalového segmentu. Svalové ko-kontrakce jsou dobře patrné při vykonávání střídavých pohybů, kdy např. aktivní flexe v lokti je provedena bez větších problémů, ale kdy extenze vázne kvůli současnému stahu m. triceps a m. biceps brachii.
Spastické synkineze
Jsou označované též jako asociované pohyby. Podobně jako spastické ko-kontrakce mají supraspinální původ a indukují se volním pohybem. Synkineze vznikne díky fenoménu „přetečení“ aktivity zřejmě již na kortikální úrovni, kdy se vzruch aberantně šíří na další, mnohdy vzdálené svalové segmenty. Tím vznikají neúčelné motorické synergie. Příkladem je současná elevace a abdukce ramene při pokusu o akrální pohyb prsty, vznik zrcadlových pohybů na kontralaterální končetině nebo asociovaný pohyb trupem či dolní končetinou při pohybu rukou.
2.2 Plasticita a indukovaná restituce motorických funkcí
Procesy indukované restituce motorických funkcí jsou analogické procesům spontánní restituce v tom, že je jejich podkladem především kortikální remapping a změny v interhemisférické rovnováze. Jsou ale zároveň podobné motorickému učení u zdravých jedinců v tom, že jde o řízenou a vynucenou změnu excitability a konektivity tréninkem stimulovaných motorických oblastí (27, 36, 177). Změny v interhemisférické rovnováze po tréninku byly experimentálně prokázány na fMRI u pacientů po iktu, kteří před terapií paretické končetiny aktivovali více ipsilaterální hemisféru při pokusu o pohyb, zatímco po terapii došlo k posunu kontralaterálním směrem (29). Za prokázanou lze rovněž považovat vynucenou změnu excitability a kortikální remapping. Např. při 3týdenním tréninku natažení a úchopu paretické horní končetiny po CMP byla na fMRI zaznamenána 420násobně vyšší aktivace kontralaterální senzomotorické kůry. Zajímavé však je, že k podobnému nárůstu aktivity nedošlo u kortikálních oblastí, které kódují izolovaný pohyb předloktím do supinace, a to přesto, že supinace horní končetiny je součástí trénovaného natažení horní končetiny a úchopu. Tím byla prokázána nutnost specifického tréninku (190). Mezi indukované změny v zapojení jednotlivých motorických drah pak mimo jiné (srov. 36) řadíme výše zmíněný sprouting zkřížených vláken kortikospinální dráhy z intaktní hemisféry na míšní úrovni ke kontralaterálním α-motoneuronům, stejně jako propojení primární motorické kůry intaktní hemisféry s nucleus ruber přes sprouting kortikobulbární dráhy (94). Za pouze spekulativní lze v současné době považovat možnost indukované neuronální neogeneze, která byla prokázána u neuronů zapojených primárně do lokálních okruhů a u interneuronů v čichovém bulbu a v hippokampu díky zásobě kmenových buněk v subventrikulární zóně (174). Na jiných místech, kde se v CNS vyskytují populace kmenových buněk (tj. v prosencefalu, mozečku, mezencefalu a v míše), však neogeneze nebyla pozorována (164).
Z množství terapií, které jsou v rehabilitaci používány, má pro indukci neuroplastických změn v současné době evidenci především několik postupů: CI-Terapie (Constraint induced /movement/ therapy; terapie indukovaná vynuceným pohybem), BWSTT (Body Weight Support Treadmill Training, trénink chůze na běžeckém pásu s odlehčením tělesné hmotnosti), některé roboticky asistované formy terapie, cvičení v představě a terapie pomocí virtuální reality. Dále je to poměrně široké spektrum technik zvaných task-oriented training (trénink zaměřený na specifický úkol), který zahrnuje řadu právě vyjmenovaných postupů, ale třeba také kruhový trénink nebo nácvik natažení (reaching) či postavování (11,167). Pro většinu těchto technik v podstatě platí, že:
- se soustředí na vysokou intenzitu terapie (zejm. CI-Terapie a task-oriented training),
- se soustředí na zahájení a provedení pohybu u pacientů s těžkým postižením (zejm. BWSTT, roboticky asistované formy terapie a cvičení v představě), nebo
- využívají herní (tj. smysluplné a zábavné) prvky pro zvýšení motivovanosti pacientů (především terapie pomocí virtuální reality a některé další roboticky asistované formy terapie).
Ad 1) Vysoce intenzivní terapie
Ze studií zaměřených na terapii chůze pomocí funkčního tréninku vyplývá, že tato forma terapie vede k indukci neuroplastických změn pouze za předpokladu, že trénovaný pohyb vykonáme více než 300x za jedno sezení (21), což je také v souladu s principy CI-Terapie (144). Jiné studie však uvádějí efekt při nižším počtu opakování, ovšem při zvýšení počtu cvičebních jednotek za den, např. 50 opakování reachingu pro sklenici s vodou (z důvodu smysluplnosti), 3x denně, po dobu 4 týdnů (11). Někteří autoři obecně hájí spíše specificitu tréninku proti excezivní intenzitě, jak ji známe např. z prvních verzí CI-Terapie (144, 192). Domnívají se, že i trénink o nižší intenzitě může vyvolat plastické změny za předpokladu, že je dostatečně specifický (154) či splňuje podmínky smysluplnosti, variability, opakování, zaměření na funkční celek a je terapeutem dostatečně podporovaný (91, podobně 207). Ve prospěch těchto názorů svědčí nepochybně proměna, kterou prošla CI-Terapie, která ustoupila z původních nároků na extrémní intenzitu tréninku (6h/den; 112) a proměnila se v méně náročnou modifikovanou CI-Terapii (mCIMT; 153; <3h/den; 148, 98), nebo dokonce v modifikovanou CI-Terapii s redukovanou intenzitou (intenzity-reduced mCIMT; 2h/den; 181). Přitom, jak se zdá, neztratila svou účinnost (56, 147, 155, 181, 193)1. Na druhou stranu platí, že trénink dvě hodiny denně, pět dnů v týdnu po dobu dvou týdnů, představuje stále vysoce intenzivní trénink v porovnání s běžnou rehabilitací v délce 45 minut, 2x týdně, jak je u nás běžné. Stejně tak je třeba upozornit na skutečnost, že dosud nepanuje jasná shoda na tom, co je vlastně intenzitou míněno. Jde o počet opakování pohybu za čas v rámci jednoho či vícero terapeutických sezení, nebo o množství vydané energie při tréninku (208)? Při snížení délky terapie tedy může být stále zachována dostatečná intenzita terapie jinými mechanismy, totiž zvýšením obtížnosti trénovaného pohybu, např. pomocí maximální rychlosti pohybu v maximálním rozsahu (11, 138). Za poměrně bezpečné východisko pro terapii v rámci těchto nejasností lze proto považovat opakované (115, 152), intenzivní (28, 88, 175, 208) provádění smysluplných (40, 107, 109, 169) úkolů, tj. takových, které alespoň částečně odrážejí pacientovy subjektivní cíle (11).
1 Terminologie zde však není ustálená. Za mCIMT lze považovat celou řadu modifikací CIMT, a proto někteří autoři udávají délku terapie mCIMT mezi 30min./den a 6h/den. Srov. (112).
Ad 2) Terapie umožňující začít a provést pohyb
Jak již bylo zmíněno v části 1.3.1, je cvičení v představě jednou z mála možností jak se pokusit o aktivaci těžce paretických až plegických svalů. Využití této terapie původně vzbuzovalo velká očekávání, ale provedené studie se dosud soustředily pouze na první dvě fáze zhodnocení efektu terapie dle MRC, tj. zjištění mechanismu účinku a pilotní studie (24). Podle nedávného Cochranského přehledu Pollocka a kol. (160), ale i dalších studií (42,198), existuje mírná evidence podle GRADE (moderate-quality evidence) pro účinnost této terapie na funkci a impairment horní končetiny (24), stejně jako pro efekt na ADL (24). Podobně jako u dalších diskutovaných technik je i pro cvičení v představě zcela klíčová intenzita tréninku, kde platí, že vyšší míra intenzity přinášela větší výsledky (15). Evidence také naznačuje, že zatímco v akutní fázi je cvičení v představě dokonce účinnější než konvenční terapie na zlepšení ADL (evidence 1a; 125, 126), v subakutním a chronickém stadiu jde spíše o doplňkovou terapii zvyšující celkový efekt léčby, ale sama není účinnější než konvenční terapie (54, 151, 168). Současně platí, že schopnost představovat si dostatečně plasticky motorické úlohy je relativně komplexní kognitivní úkon a řada pacientů toho není vzhledem k míře postižení schopna (11). Terapeut navíc nemůže v průběhu terapie posoudit, zda a v jaké kvalitě je představa vyvolána a tak může být u nevhodně vybraných pacientů efekt terapie spíše zklamáním.
Trendy k maximalizaci intenzity tréninku jsou patrné také při rehabilitaci chůze. Zlepšení chůze a mobility je jedním ze základních úkolů rehabilitace u neurologických pacientů a ze studií z posledních let vyplývá, že nejlepších výsledků by mohlo být dosaženo právě využitím opakovaného vysoce intenzivního a na specifický úkol orientovaného tréninku (58, 116, 117). Požadavky tohoto tréninku může za určitých okolností splňovat kondiční trénink. Pro zařazení kardiovaskulárního a kombinovaného tréninku (tj. kardiovaskulárního a posilovacího tréninku, včetně chůzových položek) do rehabilitačního programu po iktu existuje dostatečná evidence a tyto postupy umožňují především zvýšení rychlosti a vytrvalosti chůze (173). Není ovšem dostatek důkazů pro využití samostatného posilovacího tréninku (173), což poukazuje na význam intenzity (především u aerobních aktivit) a specificity tréninku.
Kromě terapie na treadmillu (TT) by další možností, jak aplikovat specifický a intenzivní trénink, mohlo být využití elektromechanického asistovaného tréninku chůze, který zahrnuje trénink na treadmillu s bezpečnostním závěsným zařízením (BWSTT), nebo pomocí robotických chůzových trenažérů. Mehrholz (137) definuje ve svém Cochranském review elektromechanické zařízení jako „jakékoliv zařízení, které elektromechanicky podporuje chůzový cyklus pomocí odlehčení tělesné hmotnosti a automatizuje terapeutický proces, včetně jakýchkoliv mechanických nebo počítačem řízených zařízení navržených pro zlepšení chůze, kromě přístrojů bez závěsného aparátu.“ TT byl původně základní součástí kondičního tréninku u zdravých jedinců. Postupně začal být na základě experimentálních animálních studií využíván i u osob po traumatickém spinálním poranění, CMP a dětí s DMO. Předpokládalo se, že výhodou TT by mohlo být ovlivnění celého chůzového cyklu, nikoliv pouze jeho izolovaných komponent, zlepšení rychlosti a vytrvalosti chůze a rovněž kardiovaskulární zdatnosti (176). Ke zvýšení bezpečnosti chůze a snížení zatížení dolních končetin odlehčením části tělesné hmotnosti se při tomto asistovaném tréninku začal využívat závěsný aparát (BWS; 59) a tento typ tréninku chůze se v praxi využívá již více než 20 let (93). BWSTT je vhodnou terapií pro pacienty s inkompletním spinálním poraněním, u kterých jsou částečně zachovány motorické funkce pod úrovní míšní léze a kteří mají potenciál ke zlepšení některých lokomočních funkcí. Při pravidelném provádění je vhodnou prevencí svalových atrofií, zlepšuje kondici, napomáhá zvýšení svalové síly a zlepšuje mobilitu a koordinaci (59). U osob po iktu jsou ovšem závěry jednotlivých studií hodnotících efekt BWSTT na lokomoci značně heterogenní. Např. Polese (159) uvádí, že u chodících pacientů po iktu zajišťuje mechanicky asistovaný trénink dostatečnou intenzitu „vynuceným“ způsobem, protože na treadmillu musí pacient provádět další a další kroky. Rovněž podle této studie BWSTT usnadňuje nácvik více fyziologického chůzového vzorce, protože vynucuje rytmicitu chůze, podporuje extenzi kyčle během stojné fáze a znesnadňuje kompenzační cirkumdukci dolní končetiny. Autoři dále zjistili, že u chodících osob má BWSTT, na rozdíl od nespecifického tréninku (nebo žádné terapeutické intervence), vliv na zvýšení rychlosti a dosažené vzdálenosti (159). U pacientů, kteří v průběhu jednoho měsíce po iktu nechodili, podle Ady (4) zvyšuje BWSTT nezávislost chůze na rozdíl od konvenční terapie chůze v terénu. Další práce naopak uvádějí, že po TT nebo BWSTT se nezávislost při chůzi příliš nezlepší (136), nebo že není příliš velký rozdíl v efektivitě BWSTT a konvenční terapie chůze v terénu (1). Podle posledního Cochranského přehledu umožňuje TT nebo BWSTT ve srovnání s jinými typy tréninku zvýšení rychlosti a vytrvalosti chůze především u osob, které na začátku tréninku chodily. Efekt cvičení byl nejvyšší v prvních třech měsících po iktu, kdežto v chronické fázi (tj. více než šest měsíců po iktu) byl tento efekt nižší. Výše zmíněný efekt nebyl prokázán u osob, které na začátku tréninku nechodily. Byl zjištěn i určitý trend ke zvýšení efektu terapie při vyšší frekvenci mechanického asistovaného tréninku, ale nebyl signifikantní. Pro zlepšení chůze by tedy měl být TT nebo BWSTT v klinické praxi využíván především u osob, které jsou schopné nezávislé chůze, a to ideálně časně (135). Podle současné evidence se zdá, že BWSTT je stejně efektivní jako ostatní terapie chůze (nikoliv superiorní) a neměl by být rutinně předepisován jako náhrada konvenční terapie chůze v terénu (59) nebo být používán jako jediná terapie s cílem zvýšení rychlosti a vytrvalosti chůze (136). Může být ovšem prostředkem jak zvýšit intenzitu tréninku orientovaného na určitý úkol a zajistit větší bezpečnost pro osoby se zhoršenou schopností chůze (1).
Nevýhodou TT, ale i BWSTT, může být velká náročnost pro terapeuty, kteří jsou nuceni asistovat především těžce postiženým jedincům a kontrolovat pohyby dolních končetin a trupu. Další nevýhodou může být nepřesnost generovaných chůzových vzorců ve srovnání s normální chůzí, která může mít za následek např. kompenzační pohyby v jiných segmentech a vysokou náročnost chůze (59). Tyto i další důvody vedly k rozvoji a vytvoření automatických elektromechanických zařízení. Jednou z možností je využití Lokomat systému, což je zařízení s elektronicky řízenými chůzovými ortézami pohybujícími symetricky oběma dolními končetinami podle před-programovaného chůzového vzorce. Tyto ortézy jsou kombinovány se speciálním závěsným zařízením odlehčujícím hmotnost těla a pohyblivým chůzovým pásem (34). Dalším systémem je Gait Trainer, tj. elektromechanické zařízení s dvěma řízenými plošinami pro obě dolní končetiny simulujícími jednotlivé fáze chůze, přičemž pacient je jištěn pomocí závěsného aparátu (84). Mezi novější zařízení lze zařadit HapticWalker, G-EO, Anklebot (MIT 2005), LOPES a AutoAmbulator (136). Z jednoho z posledních přehledů (133) vyplývá, že elektromechanicky asistovaný chůzový trénink v kombinaci s fyzioterapií zvyšují nezávislost při chůzi, ale jejich efekt není dostatečný k signifikantnímu zvýšení rychlosti a vytrvalosti chůze. Při interpretaci těchto výsledků je ovšem potřeba určité opatrnosti, protože někteří probandi na začátku studie již chodili nezávisle, ve studiích byly použity různé terapeutické přístroje, včetně funkční elektrické stimulace, a byly aplikovány rozdílné délky a frekvence terapie. V další aktualizaci Mehrholz (134) potvrzuje, že výše zmíněná kombinace terapií zvyšuje nezávislost chůze na rozdíl od osob, které absolvovaly chůzový trénink bez robotické rehabilitace. Zdá se, že z elektromechanické chůzové terapie více profitují pacienti v akutní a subakutní fázi (133) a ti, kteří v subakutní fázi po iktu nejsou schopni chůze (134). Schwartz (179) uvádí, že kombinace roboticky asistovaného tréninku s konvenční rehabilitační léčbou by mohla dále zvýšit efektivitu terapie chůze hlavně u osob v subakutní fázi po iktu a spinálním traumatickém poranění. Prozatím není znám optimální protokol robotického chůzového tréninku, ale zdá se, že delší doba a vyšší intenzita tréninku by mohly mít větší efekt na konečné výsledky funkčního tréninku chůze (179).
Ad 3) Terapie využívající feedback a herní prvky
Různé systémy využívající virtuální realitu (jako je eMagin Z800 3DVisor, Oculus Rift, Sony PlayStation 2 EyeToy, Xbox Kinect, Leap Motion, CAVE aj.) podporují procesy indukovaných neuroplastických změn maximálním zvýšením motivace a pozornosti pacienta mimo jiné prostřednictvím herních, tedy smysluplných pohybových prvků (11, 80, 95, 103, 105, 170)). Vliv pozornosti a motivace na procesy učení je zkoumán již delší dobu a spekuluje se zde o významu aktivity cholinergního systému bazálního telencefala (129, 186), resp. o gradientu opioidních receptorů v částech zrakové, sluchové a somatosenzorické kůry (170), který vede lidi k preferenci nových, rychlých a snadno interpretovatelných podnětů přitahujících pozornost (tzv. imerzní podněty). Detailní rozbor těchto mechanismů přesahuje možnosti této kapitoly. Velmi zjednodušeně lze tyto souvislosti přiblížit poukazem na fakt, že odvedení pozornosti od trénovaného úkolu narušuje nebo přímo zabraňuje neuroplastickým procesům (184) a naopak podání agonistů acetylcholinu tyto procesy urychluje (25, 139). Jak shrnuje Kleim (107), experimenty v této oblasti ukazují, že zájem o vykonávanou činnost je zprostředkován výše zmíněnou neurální sítí a její „oslovení“ je proto klíčové při snaze o indukci neuroplastických změn.
Klíčovým parametrem účinnosti takových systémů je jejich schopnost vzbudit subjektivní pocit přítomnosti ve virtuálním světě (prezence, ale někdy i immersion), jakkoliv je tento pojem ve většině literatury vyhrazen pro objektivní vlastnosti zařízení, které virtuální realitu vytvářejí (srov. 206, 178). Pocit přítomnosti ve virtuálním prostředí závisí z hlediska zařízení samého na řadě faktorů, mimo jiné na realističnosti a multimodalitě prostředí či na způsobu interakce pacienta s tímto prostředím (204). Významný je zde však přirozeně zmíněný faktor zábavy či smysluplnosti úkolů prováděných ve virtuálním prostředí, což je skutečnost běžně známá ze situací, kdy i poměrně triviální virtuální systémy (systémy s nízkou imerzí) dokáží pacienty maximálně vtáhnout do herního děje. Předpokládá se, že posílení pocitu přítomnosti ve virtuálním prostředí by mělo vést k lepšímu motorickému výkonu, jakkoliv tato souvislost nebyla dosud zřetelně prokázána (178).
Podle některých studií chroničtí pacienti po iktu vykazovali vyšší míru zlepšení ve stabilitě a chůzových parametrech po 30minutové terapii pomocí virtuální reality, kterou absolvovali navíc ke konvenční terapii, v porovnání s kontrolní skupinou bez virtuální reality (102). Podobně ve studii Mirelmana (141) byl pozorován vyšší efekt robotické terapie společně s virtuální realitou na rychlost chůze a maximální dosaženou vzdálenost, než stejné terapie bez užití virtuální reality. Konečně Jaffe (96) zaznamenal větší zvýšení rychlosti chůze u pacientů, kteří trénovali krok přes virtuální překážku, než u těch, kde byla překážka reálná. Ve studii s pacienty po CMP, kteří absolvovali virtuální TT, došlo navíc nejen ke zlepšení chůzových parametrů, ale byl zaznamenán rovněž transfer zvýšené rychlosti chůze do domácího prostředí (211). Tyto výsledky lze rovněž podpořit studiemi na zdravých operatérech, u nichž při virtuálním tréninku operačních dovedností dochází k transferu do reálného světa (78, 194), i když u dalších funkčních dovedností nebyl transfer dosud přesvědčivě prokázán (87). Autoři přehledových článků k problematice užití virtuální reality v rehabilitaci se v současné době shodují, že ačkoliv je evidence pro efekt virtuálního tréninku dosud limitovaná (především pro malé počty pacientů v jednotlivých studiích), jsou jejich výsledky dostatečně povzbudivé na to, aby ospravedlnily praktické užití virtuální reality v rehabilitaci a výzkum v této oblasti (22, 83, 122, 140, 166, 188). Praktickým problémem však zůstává skutečnost, že hry, běžně prodávané pro zdravou populaci, nejsou často pro pacienty se získaným poškozením mozku vhodné pro přílišnou motorickou náročnost, nesnadné ovládání apod. Programy vyvinuté speciálně pro pacienty jsou naopak často málo atraktivní a zábavné a nedostatečně realistické (114).
Herní prvky a feedback v sobě zahrnuje také většina roboticky asistovaných systémů pro rehabilitaci horní končetiny (11, 45, 130), kterých se v poslední době stále častěji využívá u neurologických pacientů s různým stupněm disability. Tato zařízení lze klasifikovat podle toho, na jaký segment horní končetiny se soustředí a jaké mají mechanické charakteristiky či podle míry asistence při cvičení, tj. zda pacient vykonává pasivní, aktivní neasistovaný, aktivní asistovaný nebo odporovaný či bimanuální pohyb (130). V současné době jsou pro rehabilitaci horní končetiny v klinické praxi používány mimo jiné tyto robotické systémy: MIT-Manus, MIME, BI-MANU-TRACK, Haptic Master, ARMin, Arm-Guide, REHAROB, NeReBot či T-WREX (130). Robotická rehabilitace se nejvíce soustřeďuje na jedince po iktu, protože jde o největší populaci pacientů se spastickou parézou. Byly ovšem publikovány i studie, hodnotící robotickou rehabilitaci horní končetiny u pacientů po traumatickém spinálním poranění, s roztroušenou sklerózou a s DMO (108). Zdá se, že největší výhodou robotické rehabilitace horní končetiny je specificita a intenzita tréninku (11, 45), možnost přesné asistence nebo kladení odporu během trénovaného pohybu (19) a reprodukovatelnost objektivního hodnocení terapie (108). Navíc v kombinaci s herními prvky a feedbackem je podporována motivace i pohodlí pacientů a terapeutů (11, 45). Podle současného stavu evidence lze tyto metody obecně považovat za stejně účinné jako konvenční terapii (111). V případě některých parametrů (hybnost proximálních segmentů, dosah v reachingu, nezávislost, ADL) se dokonce zdá, že jsou účinnější (128, 135) a jiné parametry (např. svalovou sílu) podle některých studií spíše neovlivňují (135). Podstatnou otázkou je v této souvislosti tedy spíše to, jak se tradiční i roboticky asistované přístupy v rehabilitaci horní končetiny mohou doplňovat (45).
Společným prvkem množství robotických systémů, řady virtuálně-reálných zařízení, ale i konvenční terapie, je využití zpětné vazby (feedbacku) k podpoře restituce motorických funkcí. Využití zpětné vazby obecně zlepšuje retenci nově naučených dovedností (31), pravděpodobně prostřednictvím vzniku nových senzorických paměťových stop (engramů) aktivací nepoužívaných synapsí při řízení pohybu, čímž se zlepšuje pozdější schopnost provést pohyb bez zpětné vazby (209). Rozlišujeme vnitřní a vnější typy zpětné vazby. Pomocí vnitřního feedbacku získává pacient z vlastních senzorických zdrojů smyslové informace o prováděném pohybu nebo úkolu a z nich se vytvářejí vnitřní reprezentace prováděného pohybu (187, 197). Zevní feedback představuje doplnění nebo náhradu vnitřního pomocí informací z vnějšího zdroje v průběhu prováděného pohybu, tj. nepatří sem instrukce dané před započetím pohybu (13). Do tohoto typu zpětné vazby lze zařadit feedback zaměřený na výsledek (knowledge of results) i na proces (knowledge of performance), ale i různé formy biofeedbacku (13). Feedbackem zaměřeným na výsledek rozumíme podání informace o výsledku pohybu nebo úkolu (např. že pacient uspěl ve sledovaném parametru na tolik a tolik procent). Tato forma zpětné vazby se ukazuje jako účinná tehdy, když je motivujícím faktorem a vyvolává u pacienta snahu o lepší kontrolu pohybu (156). Zpětná vazba zaměřená na proces podává pacientovi informace o způsobu provedení pohybu (např. že musí pacient provést požadovaný pohyb větší silou). Oproti zpětné vazbě zaměřené na výsledek, která vede ke zlepšení pouze v udávaném parametru, může feedback zaměřený na proces zlepšit více parametrů pohybu (31).
Pro vliv některých forem feedbacku na určité konkrétní parametry existují důkazy. Vizuální feedback dokáže podle studií ovlivnit schopnost a symetrii zatížení dolních končetin (14), rychlost chůze (124) nebo sílu dolních končetin (55). Auditorní feedback používají fyzioterapeuti podle výzkumů více jako nástroj pro motivaci pacienta než pro podávání informací o pohybu (191). Použití tohoto typu feedbacku je na rozdíl od vizuálního vhodnější pro zdůraznění temporálních parametrů trénovaného pohybu (90), typicky např. u chůze (13). Taktilní feedback je užíván spíše řídce. Kombinací auditorního, vizuálního a někdy i taktilního užívá výše pojednávaná virtuální realita.
Při užití různých forem feedbacku dosud neexistuje jasná shoda na výběru vhodných parametrů (13). Používaný feedback je navíc vždy třeba přizpůsobit motorickému i kognitivnímu postižení daného pacienta (13). Zdá se však, že z praxe a některých studií vyplývají některá obecná doporučení. Nadměrné využívání zpětné vazby sice může zlepšit výkon v prováděném pohybu, ale vede k vytvoření závislosti na zpětné vazbě, a naopak málo časté použití feedbacku zpomaluje proces motorického učení (197). Proto se doporučuje zpočátku volit spíše častější zpětnovazebnou stimulaci, ale brzy je potřeba snížit její frekvenci (177). Podobně lze proces učení v první fázi terapie usnadnit volbou zevních forem feedbacku, ale s postupem času bychom měli preferovat více vnitřní formy (149). Informace získávané z feedbacku by měly být multimodální, zábavné a motivující, aby dostatečně přitahovaly pacientovu pozornost, přičemž vynikajícím příkladem zábavného feedbacku je pořizování videonahrávek některými tanečními programy na konzoli Xbox Kinect. V neposlední řadě by měl být feedback pro pacienta snadno pochopitelný (13).
2.3 Cíle rehabilitace motorických funkcí ve spastickém stadiu
2.3 Cíle rehabilitace motorických funkcí ve spastickém stadiu
2.3.1 Kontraktury
Kontraktury jsou běžnou komplikací u nemocných s postižením centrálního motoneuronu. Klinicky vnímáme kontrakturu jako neschopnost dosažení plného pasivního i aktivního rozsahu pohybu v kloubu. Tento pojem zatím nemá definovánu přesnou míru omezení rozsahu pohybu. V literatuře se uvádí zkrácení, ztuhlost nebo neurčitě snížení rozsahu pohybu až po jeho úplnou ztrátu (104). Konceptuálně lze rozlišit myostatické kontraktury, kde dochází k adaptivním změnám ve smyslu snížení počtu sarkomer v sérii, pseudomyostatické kontraktury, kde se již zkracuje i délka jednotlivých sarkomer, arteogenní a periartikulární kontraktury, které jsou součástí intraartikulární patologie, a fibrotické kontraktury, u nichž došlo k nahrazení kontraktilních částí fibrotickými adhezemi, jizvou nebo heterotopickou kostní tkání (104).
Podle řady studií je incidence kontraktur u pacientů se syndromem horního motoneuronu značně alarmující. Např. Kwah a kolektiv uvádějí, že až u poloviny pacientů po iktu se do půl roku vyvine alespoň jedna kontraktura, přičemž incidence kontraktur v jednotlivých kloubech na horní i dolní končetině se pohybovala mezi 12 a 28 % (110). Sackley a kolektiv sledovali výskyt kontraktur v prvním roce po CMP a zjistili, že po 3 měsících má alespoň jednu kontraktu 43 % pacientů, v půl roce už 56 % a 1 rok od iktu až 67 % pacientů (172). V této studii navíc pod kontrakturou rozuměli omezení pasivního rozsahu pohybu alespoň o 30 % oproti zdravé straně. V případě pacientů s RS mělo podle Hoanga a kolektivu ze 156 pacientů průměrně 14,9 let od diagnostiky alespoň jednu kontrakturu 56 % z nich, přičemž ve 43,9 % případů se jednalo o kontrakturu v hlezenním kloubu (85). Ze studie také vyplynulo, že kontraktury jsou přítomny již v časném stadiu RS a jejich prevalence koreluje s progresí nemoci. U skupiny pacientů se spinálním poraněním bylo pozorováno, že mezi 3. a 12. měsícem po úrazu nedošlo k signifikantnímu zhoršení pasivní hybnosti v hlezenním kloubu, avšak spíše proto, že měli všichni kontraktury v hleznu již vstupně, tj. do tří měsíců (51). Dostupná jsou také heterogenní data pro pacienty s traumatickým poraněním mozku. Podle některých studií (180) se kontraktury v hleznu vyskytují pouze u 16,2 % pacientů, zatímco podle jiných u 47 % (47) či 56 % (158) nebo až u 84 % (212). Nepřekvapí také, že dystonická aktivita musculus triceps surae a musculus tibialis posterior je u těchto pacientů prediktorem rozvoje kontraktur v hleznu (180).
Svalová hyperaktivita obecně zhoršuje svalovou dysbalanci v segmentu a je považována za neurální příčinu zkrácení měkkých tkání a kontraktur. Všeobecně panuje názor, že spasticita může vest ke kontrakturám tímto mechanismem: sval se reflexně kontrahuje v důsledku spasticity a má tendenci zůstávat ve zkráceném postavení. Toto zkrácení způsobí změny vztahující se k délce svalu v komplexu sval-šlacha, zejména ztrátu sériově zapojených sarkomer. Snižuje se rozsah pohybu v kloubu a vzniká kontraktura (6). Redukce svalové hyperaktivity má proto u pacientů se syndromem centrálního motoneuronu také důležitou roli v prevenci kontraktur (75). U středního až těžkého stupně spasticity je proto snížení hyperaktivity nutné již z tohoto důvodu. V případě spastické dystonie je pohybový segment ve zkráceném postavení již od počátku a její přítomnost tak opět představuje vysoké riziko vzniku kontraktur. V tomto případě je indikována včasná aplikace botulotoxinu. Non-neurální příčinou kontraktur je adaptivní zkrácení svalu nebo svalových skupin a periartikulárních pojivových tkání (kloubního pouzdra, chrupavek a vazů) s následnou retrakcí a ztuhlostí. Konečným důsledkem kontraktur jsou deformity kloubů, bolest, poškození kožního krytu, omezení běžných aktivit a participace pacienta.
Prevencí a terapií zkrácení a kontraktur je obecně strečink. Přesný mechanismus účinku strečinku, a tedy ani přesná doporučení o jeho parametrech, nejsou dosud jasně objasněny (82, 104). Strečink vede ke zvýšení počtu svalových vláken (101) a současné angiogenezi, biomechanickým a dalším strukturálním změnám ve svalu, jako je produkce aktinu a myozinu a tvorba nových sarkomer (30, 52, 61). Není-li strečink aplikován po dostatečně dlouhou dobu, jsou tyto změny reverzibilní (44). Účinnost strečinku na kontraktilní část svalu je pravděpodobně limitována předchozí adaptací vaziva na zkrácení (97). Při dostatečně dlouhé aplikaci statického strečinku však lze dosáhnout i reorganizace nekontraktilních částí svalu (38, 205), a to především na bázi jejich parciální mikrotraumatizace s následným hojením v prodloužení (104).
Pro prevenci i terapii kontraktur u pacientů se spastickou parézou užíváme denní analytický prolongovaný statický progresivní strečink. Pacienti jsou však nejčastěji instruováni k provádění krátkodobého strečinku v řádu sekund až minut, který má prokázaný efekt na snížení streč reflexu, avšak tento výsledek mizí již po první kontrakci protahovaného svalu. U zdravých jedinců bylo prokázáno krátkodobé zvýšení svalové síly po takovém strečinku, ale u spastických svalů nebyl takový účinek pozorován. Předně však krátkodobý strečink nemá žádný efekt na nekontraktilní složku svalu, a proto není vhodný k prevenci a terapii kontraktur u pacientů se syndromem centrálního motoneuronu, protože nesplňují první podmínku strečinku u těchto pacientů, kterou je dostatečná délka protažení (17, 74).
Terapie, které splňují požadovanou délku protažení, tj. 20–30 min. na každý ohrožený nebo hyperaktivní sval 1–2x denně, 4–7x týdně (23, 99), však často nejsou dostatečně efektivní z jiného důvodu. Využití ortéz s tzv. funkčním postavením akra horní končetiny po celou noc prokazatelně nemá žádný efekt na vznik nebo terapii kontraktur (120), stejně jako polohování horní končetiny do středního postavení mezi vnitřní a zevní rotací (5), nebo strečink prováděný pacientem do 90° abdukce v ramenním kloubu a do cca 45° extenze zápěstí po dobu 30 minut 2x denně (195). Důvodem je nesplnění druhé podmínky správného strečinku u pacientů se syndromem horního motoneuronu, kterou je protažení svalu do maxima, kdy pacient již cítí tah, ale ještě ne bolest. Tato druhá podmínka je také naznačena ve zmíněné studii Ady a kolektivu, která výše popsaný strečink porovnávala s protažením do maximální zevní rotace v ramenním kloubu, které signifikantně snížilo vznik kontraktur (5), aniž by mu však zabránilo, pravděpodobně pro potřebu delšího trvání strečinku pro tuto svalovou skupinu (17). Z nutnosti protažení svalů do maxima také plyne potřeba analytických metod strečinku, protože při využití sdružených pohybů nedosáhneme maximálního protažení všech svalů (např. při současné extenzi zápěstí a prstů neprotahujeme do maxima mm. lumbricales, ale pouze flexor digitorum superficialis a profundus).
Potřeba dostatečně dlouhého protažení segmentu do maxima byla studována v případě ortéz na zápěstí horní končetiny, kde bylo porovnáváno polohování ve funkčním postavení a v maximálním protažení ve statické pozici. Výsledky neukázaly signifikantní rozdíl v rozsahu extenze v zápěstí ani u jedné z ortéz po 6 týdnech terapie (118, 119), a to z důvodu chybějící třetí podmínky správného strečinku u pacientů se syndromem horního motoneuronu, kterou je progrese maximálního protažení. Ortézy, které v této studii polohovaly zápěstí do maximální extenze, se velmi brzy po počátku jejich aplikace stávají neúčinné, protože se zápěstí již nenachází v maximálním protažení.
Nutnost zohlednění všech tří podmínek správného strečinku lze ověřit na sériové aplikaci imobilizačních obvazů, jejichž účinnost byla shrnuta v systematickém review Lanninem, avšak nebylo dostatek studií pro zhodnocení jejich dlouhodobého efektu (120). Moseley a kolektiv o rok později sledovali pacienty ještě čtyři týdny po ukončení sériové aplikace imobilizačních obvazů a zjistili, že efekt této terapie přestává být signifikantní již jeden den po jejím ukončení a za čtyři týdny již nebyl patrný vůbec (145). Z tohoto důvodu je nutné dodržet i čtvrtou podmínku správného strečinku u pacientů se syndromem horního motoneuronu, kterou je pravidelnost protahování, ideálně v denním režimu. Vzhledem k nevýhodám sériové aplikace imobilizačních dlah, k nimž patří akcentace nepoužívání končetiny, riziko poškození kůže a rozvoje edému (74), je třeba terapii pojmout jako autostrečink, kde pacient po stanovenou dobu zůstává ve statické poloze v maximálním protažení příslušné svalové skupiny. Délka a intenzita strečinku pro jednotlivé svaly nebyla dosud jednoznačně stanovena, v minimální variantě lze však z empirie a také na základě některých studií (srov. 17) doporučit alespoň 10, spíše však 30 minut na každou svalovou skupinu.
Dalším klíčovým parametrem strečinku je míra zatížení svalu v protažení. V této otázce nepanuje dosud jasná shoda. Z experimentů s parametry strečinku v animálních modelech po poranění míchy se zdá, že dlouhotrvající statický strečink s vysokým zatížením má větší efekt pro zvýšení rozsahu pohybu než statický strečink s nízkým zatížením svalu a/nebo kratší dobou trvání (143). Publikované humánní studie se zdají poukazovat ke stejným závěrům. Např. v případě tricepsu surae má strečink s vysokým zatížením (např. pomocí stoje) po dobu 30 minut vyšší účinnost než stejně dlouhý strečink se středním zatížením (20, 810). Jak již bylo řečeno, jasná doporučení stran kombinace délky strečinku, míry zatížení a dalších parametrů však dosud neexistují (17).
Většina běžně používaných technik v rehabilitaci pacientů se spastickou parézou uznává potřebu optimalizace „postavení kloubů a měkkých tkání za účelem dosažení správné svalové délky pro optimální funkci“ (35). V praxi však obvykle nejsou dodržovány parametry strečinku, tj. nejde o denní analytický prolongovaný statický progresivní strečink. Vzhledem k časové náročnosti této terapie je v podstatě nutné ji pojmout jako domácí program prováděný pacientem, případně s asistencí pečujících osob. Zahrnutí strečinku do terapie prováděné terapeutem lze proto v drtivé většině případů považovat za známku nedodržování potřebných parametrů. Programové soustředění na centrované postavení v kloubech, které má v řadě situací jasné oprávnění, je navíc ve spastickém stadiu založeno na zásadním omylu. Hlavním kinestetickým receptorem v lidském těle nejsou kloubní receptory, ale svalová vřeténka. Pro toto tvrzení existuje řada důkazů (k jejich diskusi srov. 162), od intaktního polohocitu a pohybocitu u pacientů s totální endoprotézou (77) nebo u zvířat s lézí zadních provazců na úrovni hrudní páteře (kde již není vedena informace z vřetének svalů dolních končetin, která se v oblasti horní bederní páteře odklání do spinocerebellárního traktu na rozdíl od informace z kloubních receptorů) (202), přes poruchy ve fungování polohocitu a pohybocitu založené na svalové tixotropii (163), až po iluzi pohybu končetiny při aplikaci vibrací na sval či jeho šlachu (53, 62). Argumentace správnou aferentací z kloubních receptorů při centrovaném postavení v kloubu je proto ve spastickém stadiu mylná. V centrovaném postavení kloubu vysílají svalová vřeténka hyperaktivních svalů informace o decentrované pozici v kloubu, a tyto informace jsou pro CNS daleko důležitější než informace z receptorů v kloubu. Naopak protahujeme-li více hyperaktivní a zkrácené svaly do maxima, budou jejich svalová vřeténka vysílat do CNS informaci o „centrovaném“ postavení, jakkoliv je protažením kloub jako takový decentrován. V pseudochabém stadiu, kde jsou svaly hypotonické, a jejich svalová vřeténka jsou proto hypoaktivní, představuje aferentace z kloubních receptorů naopak alespoň nějakou informaci do CNS, a polohování v centrovaném postavení v kloubu společně s aproximacemi do kloubu je proto zcela na místě. Ve spastickém stadiu však centrace v kloubu není to samé, co správná délka svalu, a systematické využívání imobilizace v centrovaném postavení u pacientů se spastickou parézou „může být důsledkem záměny terapie v ortopedii a neurologii.“ (74).
2.3.2. Svalová hyperaktivita
Zásadním primárním postupem lege artis ke snížení svalové hyperaktivity u pacientů se syndromem centrálního motoneuronu jsou denervační postupy (12, 57, 150), případně farmakoterapie (189), a nikoliv rehabilitace v monoterapii, která má na svalovou hyperaktivitu prokazatelně pouze krátkodobý účinek (46, 213). Rehabilitace a denervační postupy by však měly být indikovány současně, protože boj s centrální parézou je takříkajíc třeba vést na všech třech frontách zároveň, tj. 1. tlumit svalovou hyperaktivitu, 2. využívat vhodné rehabilitační postupy pro prevenci a léčbu vzniku kontraktur a současně 3. v rámci terapie parézy posilovat centrální kontrolu a periferní svalovou sílu oslabených agonistů (76). Rehabilitační postupy navíc mohou zvýšit a prodloužit účinnost aplikace botulotoxinu. Na lokální chemodenervaci je z hlediska rehabilitace třeba nahlížet především jako na prostředek pro vytvoření „terapeutického okna“ pro tonizaci a posílení více paretických agonistů, jež jsou před aplikací více hyperaktivním antagonistou inhibovány. V případě úspěchu takového postupu po odeznění účinku botulotoxinu tlumí „tonizovaný“ agonista nadále svalovou hyperaktivitu antagonisty, jež byl aplikován. Při správném protažení více hyperaktivního antagonisty také často dochází k utlumení svalové hyperaktivity svalů, jež by bez strečinku vyžadovaly aplikaci botulotoxinu, což může vést ke snížení celkové dávky botulotoxinu a/nebo umožní lepší zacílení chemodenervace na segmenty, které ji skutečně nezbytně vyžadují. Rehabilitaci je nutné zahájit ihned po aplikaci botulotoxinu a pokračovat kontinuálně do další aplikace.
Botulotoxin je neurotoxin produkovaný gramnegativní anaerobní bakteríí Clostridium botulinum. Existuje několik sérotypů botulotoxinu, z nichž se v léčbě používají typy A, B a E. Cílem aplikace botulotoxinu na poli spastické parézy není prohloubení parézy agonisty, ale snížení hyperaktivity (především spastické ko-kontrakce a dystonie) antagonisty. Molekula botulotoxinu se skládá z lehkého a těžkého řetězce a dalších proteinů. Těžký řetězec umožňuje navázání botulotoxinu na buněčnou membránu presynaptické části cholinergní synapse, a tak průnik toxinu do intracelulárních prostor. Lehký řetězec štěpí tzv. SNARE proteiny (tj. proteiny umožňující exocytózu acetylcholinu), čímž dojde k zablokování fúze synaptické vezikuly obsahující acetylcholin s buněčnou membránou. Tím je zablokován přenos vzruchu přes synapsi. Kromě toho dochází k degeneraci presynaptického zakončení, a tedy k denervaci svalu. S odstupem času však dochází k obnově funkce degenerovaných nervosvalových plotének a ke sproutingu motorického axonu. S latencí 3-5 měsíců tak dochází ke vzniku nové neuromuskulární ploténky, tedy k reinervaci. Efekt aplikace botulotoxinu je tedy vratný.
Tabulky 2 a 3 ukazují některé typické cíle v léčbě pomocí chemodenervace ve vztahu k obvyklým „spastickým vzorcům“.
Table 2. Cíle v léčbě pomocí chemodenervace ve vztahu k obvyklým „spastickým vzorcům“ na horní končetině. (Modifikováno z GRACIES, J. M., HEFTER, H., SIMPSON, D. M., MOORE, P.: Spasticity in Adults 2ed. In: MOORE, P., NAUMANN, M. (eds.): Handbook of Botulinum Toxin Treatment, Oxford, Blackwell Publishing, 2006.) 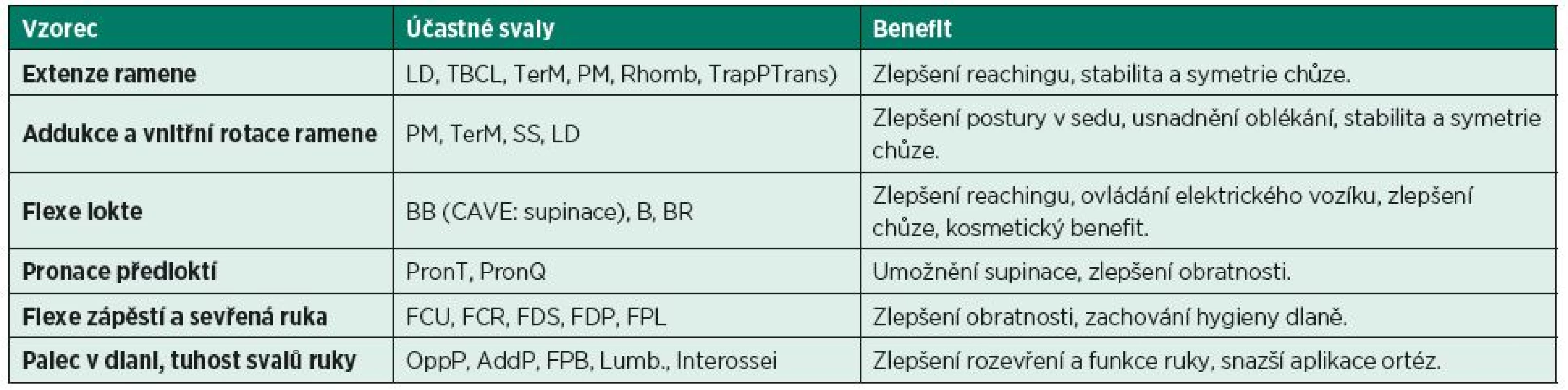
Zkratky: LD – latissimus dorsi, TBCL – triceps brachii caput longum, TerM – teres major, PM – pectoralis major, Rhomb – rhomboidei, TrapPTrans – trapezius pars transversa, SS - subscapularis, BB – biceps brachii, B – brachialis, BR – brachioradialis, PronT – pronator teres, PronQ –pronator quadratus, FCU – flexor carpi ulnaris, FCR – flexor carpi radialis, FDS – flexor digitorum superficialis, FDP – flexor digitorum profundus, FPL – lfexor pollicis longus, OppP – opponens pollicis, AddP – adductor pollicis, FPB – flexor pollicis brevis, Lumb. – lumbricales, Interossei – interossei palmares et dorsales Table 3. Cíle v léčbě pomocí chemodenervace ve vztahu k obvyklým „spastickým vzorcům“ na dolní končetině. (Modifikováno z GRACIES, J. M., HEFTER, H., SIMPSON, D. M., MOORE, P.: Spasticity in Adults 2ed. In: MOORE, P., NAUMANN, M. (eds.): Handbook of Botulinum Toxin Treatment, Oxford, Blackwell Publishing, 2006.) 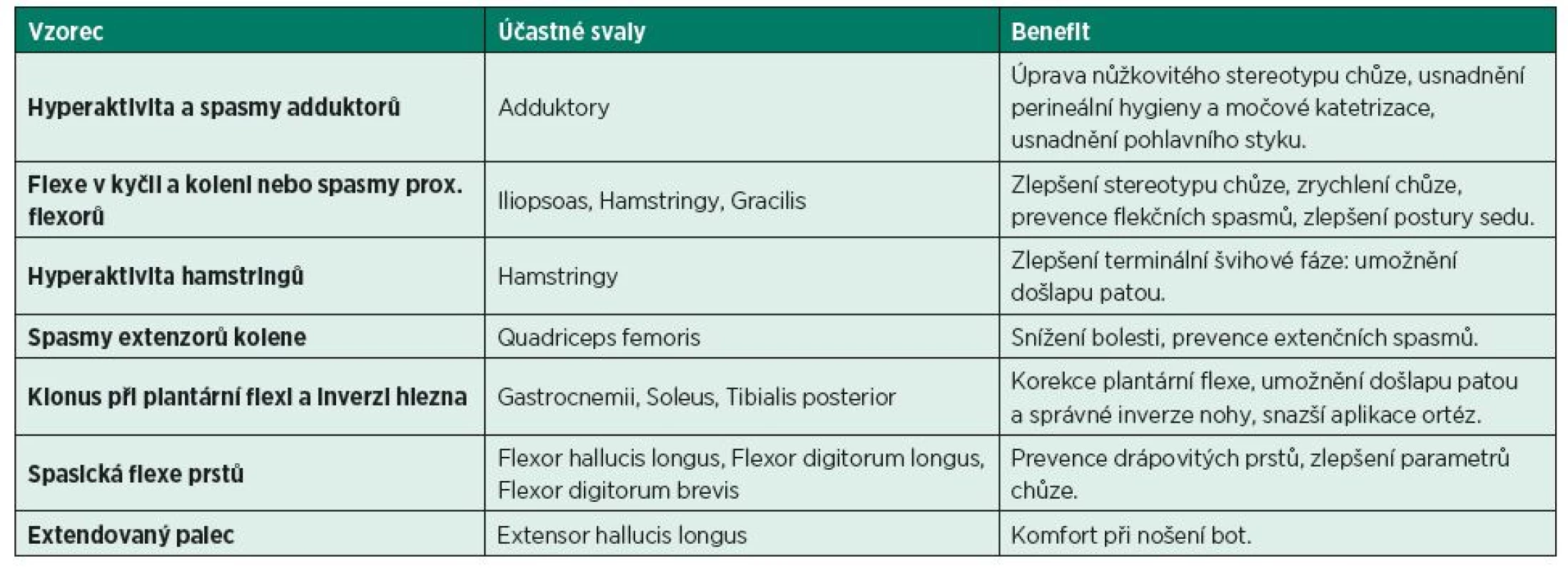
Jak uvádí Štětkářová (189), pro perorální léčbu spasticity neexistuje na rozdíl od botulotoxinu dostatek důkazů pro jejich efekt na spasticitu. Přesto jsou v praxi nejčastějším způsobem terapie. Mechanismus účinku jednotlivých léků se liší. Ovlivňují různé neuromediátory, jako je glutamát, noradrenalin, serotonin, GABA nebo glycin, a je proto třeba je indikovat s ohledem na symptomy, které se snažíme ovlivnit. Benzodiazepiny (alprazolam, oxazepam, tetrazepam, lorazepam, diazepam, chloradiazepoxid, klonazepam) zvyšují presynaptickou inhibici zvýšením afinity GABA-A receptorů k vlastnímu mediátoru GABA na kmenové a míšní úrovni, čímž snižují monosynaptické a polysynaptické reflexy. Benzodiazepiny doprovázejí významné nežádoucí účinky, zejména sedace při vyšších dávkách, snížení pozornosti a poruchy paměti. Při dlouhodobém užívání se navíc může objevit závislost s nepříjemnými abstinenčními příznaky při vysazení. Z této skupiny se klonazepam nejčastěji využívá u pacientů s DMO a při výskytu nočních spasmů u pacientů s RS. Tizanidin jako alfa-2 adrenergní agonista snižuje polysynaptickou reflexní aktivitu excitačních interneuronů. Oproti některým dalším antispastickým lékům má tizanidin relativně málo nežádoucích účinků. Jeho užití je doporučeno v kombinaci s dalšími léky, především na snížení tonu, frekvence spasmů a výskyt klonu. Mezi nejčastěji preskribovaná antispastika patří baklofen. Jde o GABA-B agonistu, který především svým presynaptickým působením snižuje na míšní úrovni monosynaptické a polysynaptické reflexy a inhibuje uvolňování glutamátu a aspartátu. Často je předepisován ke snížení tonu a ovlivnění spasmů u pacientů s RS, traumatickým poraněním mozku a DMO. Antiepileptika (klonazepam, gabapentin, pregabalin) se u pacientů se spastickou parézou využívají především spolu s dalšími antispastiky pro jejich schopnost snížit uvolňování glutamátu, i když jejich efekt na snížení spasticity nebyl dosud jednoznačně prokázán. Jejich užití je tak vhodné spíše při současném výskytu neuropatických bolestí. Kannabinoidy působí jako antagonisté NMDA receptorů a glutamátu. Nejčastěji se jich užívá na spasticitu u pacientů s RS, ale je třeba mít na paměti jejich nežádoucí účinky zejména při dlouhodobém užívání (porucha kognitivních funkcí).
2.3.3 Streč-senzitivní paréza
Centrální parézou rozumíme snížení schopnosti volního náboru motorických jednotek v důsledku poruchy descendentních motorických drah a tato porucha představuje první, bezprostřední motorický příznak získaného poškození mozku. Její součástí je mimo jiné nedostatečná synchronizace motorických jednotek a zvýšení prahu jejich aktivace (75). Ve chvíli, kdy se kromě parézy začne rozvíjet také svalová hyperaktivita, dochází k dalšímu prohloubení neschopnosti provést aktivní pohyb, a to na podkladě odporu protahovaných hyperaktivních antagonistů. Pro tento fenomén, který zahrnuje jak parézu agonistů, tak hyperaktivitu jejich antagonistů, je zaveden pojem streč-senzitivní parézy (76). Tento koncept vysvětluje běžně známý jev, kdy v důsledku chemodenervace hyperaktivního svalu dojde ke zvýšení aktivního rozsahu pohybu do opačného směru. Oslabení antagonisty botulotoxinem samozřejmě neléčí parézu agonisty ve vlastním slova smyslu, ale je terapií streč-senzitivní parézy agonisty. Míra svalové hyperaktivity antagonisty (především ko-kontrakce) je navíc dána nejen plastickými změnami, kterými CNS reaguje na lézi na spinální i supraspinální úrovni, ale je rovněž podmíněna excitabilitou jejich svalového vřeténka (68). Čím je antagonista zkrácenější, tím více je jeho svalové vřeténko excitabilní, a tím dříve a intenzivněji se bude sval ko-kontrahovat při pokusu o volní pohyb agonisty a bude tak dále prohlubovat jeho streč-senzitivní parézu. Nejen chemodenervace, ale i strečink antagonisty jsou proto způsoby jak léčit streč-senzitivní parézu agonisty. Lze tedy říci, že dokud dostatečně nezaléčíme svalovou hyperaktivitu antagonistů, nelze klinicky ani zhodnotit míru vlastní parézy agonisty. Kombinace chemodenervace a strečinku dle parametrů uvedených v části 2.3.1 je tak možné vnímat jako prostředky k otevření „terapeutického okna“ pro léčbu parézy agonistů, jak již bylo zmíněno. Postupujeme přitom s ohledem na principy, jež podmiňují indukované neuroplastické změny (viz část 2.2).
Již delší dobu se proto v rehabilitaci pacientů se syndromem horního motoneuronu prosazují koncepty, které se tolik nesoustředí na „kvalitu“ prováděného pohybu, ale daleko spíše na repetitivní, vysoce intenzivní trénink pohybu či pohybových komponent, spolu s užitím technik k ovlivnění biomechanických komponent pohybu, tj. především strečink (srov. 28, 88, 175, 208). Postupy různých terapeutických technik je proto třeba pozorně sledovat a hodnotit v kontextu správně pochopeného obrazu streč-senzitivní parézy. Nelze například zdánlivě nic namítnout proti tvrzení, že se terapie u pacientů se syndromem centrálního motoneuronu musí zaměřit na posilování, jelikož slabost je faktorem, který u těchto pacientů nejvíc přispívá k disabilitě (35). Primárním postupem při léčbě streč-senzitivní parézy je však, jak bylo řečeno, ovlivnění svalového zkrácení a hyperaktivity antagonisty a při užití posilování více paretických agonistů je třeba respektovat výše diskutovaný požadavek na intenzitu tréninku, a to bez ohledu na vyvolání patologických svalových vzorců, jimž se řada tradičních technik vyhýbá (např. 165), ačkoliv lze na základě evidence usuzovat, že to není nutné (183, 210). Podobně kladení důrazu na provádění pohybu ve funkčním kontextu (35) je jistě správné z toho pohledu, že je nutné pracovat na zlepšení funkčních dovedností pacienta v ADL a respektovat jeho subjektivní cíle v terapii. Neznamená to však, že jedinou terapeutickou možností je nácvik funkčních dovedností, protože i intenzivní analytické pohyby mají neuroplastický účinek a existuje u nich transfer do funkce (28, 33) jsou-li prováděny s ohledem na požadovanou funkci. Task-oriented training může sice také být účinný, ale jak bylo diskutováno výše, pouze při dostatečné délce terapie. To se však často vymyká reálným možnostem pacientů i terapeutů v běžném zdravotním provozu a finančním možnostem zdravotnického systému. Alternativní dosažení dostatečné intenzity tréninku pomocí zvýšení náročnosti úkolu pak opět často vede k pohybům v patologických vzorcích, které tradiční postupy odmítají. Správné pochopení problematiky streč-senzitivní parézy v kontextu neuroanatomických a neurofyziologických poznatků o pohybu konečně vrhá nové světlo na terapeutické priority. Zohlednění interakce segmentu a opěrné báze (rozuměj trupu), které v tradičních přístupech patří mezi nejvyšší priority (35) je sice důležité, ale vzhledem k tomu, že trupové svalstvo má oboustrannou inervaci, je trupová patologie v porovnání s končetinovou méně závažná a obvykle je spíše kompenzačním mechanismem nebo projekcí patologie končetinové, kterou je třeba řešit na prvním místě. Na dolních končetinách, kde je problematika instability (pro kterou je klíčové zhodnotit interakce segmentu a opěrné báze) zejména palčivá, je pak třeba se končetinovému svalstvu primárně věnovat z povahy chůze samé, protože opěrnou bází zde není primárně trup, ale akrum stojné končetiny. Ze studií navíc víme, že nejrychlejší a největší aktivace trupových svalů dosáhneme při rychlých pohybech končetinami (86), tedy že se trupovému svalstvu lze věnovat zprostředkovaně přes pohyby končetin.
Pro efekt intenzivního motorického tréninku a/nebo chemodenervace na streč-senzitivní parézu u různých diagnóz se spastickou parézou máme k dispozici určitou evidenci. Hu a kolektiv (89) zkoumali vliv roboticky asistované rehabilitace flexe a extenze v lokti na svalovou ko-kontrakci u chronických pacientů po CMP (n= 7). Každý pacient absolvoval 20 lekcí v rozsahu 90 min 3-5x týdně po dobu 7 týdnů. Hlavní sledovaný parametr byl index svalové ko-kontrakce, ale také MAS, FMA, MSS a svalová aktivita (pomocí zařízení Dynaserv motor) (182). Po tréninku došlo u těchto pacientů ke snížení excesivní svalové aktivace, spasticity a ko-kontrakce, stejně jako k signifikantnímu zlepšení ve výsledcích FMA a MSS. Podobně Gracies a kolektiv (72) zkoumali vliv aplikace botulotoxinu A do m. biceps brachii u pacientů s hemiparézou (n=18). Vyšetřovali spasticitu a zkrácení pomocí Tardieuho škály, izometrickou dynamometrii bicepsu, rychlost pronace a supinace předloktí měřenou potenciometrem a pEMG aktivitu měřenou při aktivním pohybu. Po aplikaci botulotoxinu došlo mimo jiné ke zrychlení extenze lokte o 25 % a ke zvýšení izometrické síly při extenzi o 20 %. Kombinaci obou postupů zkoumali Rodriguez a kolektiv (171), kteří chronickým pacientům po CMP (n=14) aplikovali botulotoxin do superficiálního a hlubokého flexoru prstů a předepsali jim domácí strečinkový program a cvičení na extenzory prstů. Výsledkem objektivizovaným pomocí MAS a měření aktivního rozsahu pohybu bylo signifikantní snížení tonu a zvětšení aktivního rozsahu pohybu. Za 4 měsíce, tj. po vymizení účinku botulotoxinu, sice došlo k návratu hodnot do nesignifikantního pásma, ale s další aplikací botulotoxinu se znovu objevilo pozorované zlepšení a nově také nesignifikantní trend ke kumulativnímu efektu. Konečně Giovannelli a kolektiv (60) vyzkoušeli podobný postup (aplikace botulotoxinu, strečink a aktivní cvičení) u pacientů s roztroušenou sklerózou (n=38) a porovnávali ho s kontrolní skupinou, u níž došlo pouze k aplikaci botulotoxinu. Podle MAS došlo u obou skupin k signifikantnímu snížení spasticity, ale u experimentální skupiny byl efekt vyšší. Jakkoliv tato evidence není dosud dostatečně průkazná, zejména proto, že jsou tyto studie provedeny na malém vzorku pacientů, lze ji považovat za slibnou, nově vznikající formu terapie. Výsledky těchto studií jsou navíc zcela v souladu s pilotními studiemi zkoumajícími efektivitu konceptu Dohoda o reedukačním tréninku (Guided self-rehabilitation contract, GSC; srov. část 4), jež shrnuje 4.
Table 4. Pilotní studie k účinnosti konceptu GSC. 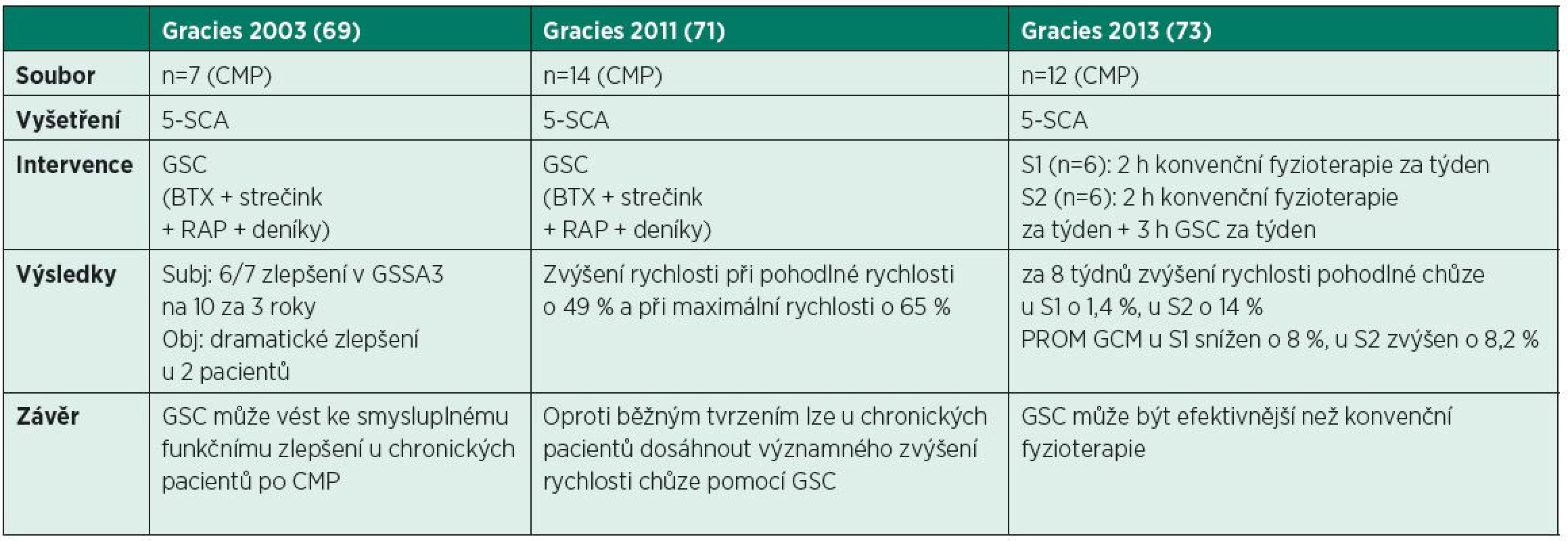
Na základě přesvědčivosti neurofyziologických a patofyziologických východisek této terapie a s ohledem na přímou i nepřímou evidenci pro zvolení těchto postupů při léčbě spastické parézy, využíváme na našem pracovišti koncept GSC. V současné době je organizace péče v našem Komplexním spastickém centru organizována v tříměsíčních cyklech (vzhledem k délce trvání účinku botulotoxinu). Pacient přichází poprvé na indikační seminář, kde je komplexně vyšetřen týmem složeným z neurologa, rehabilitačního lékaře a fyzioterapeuta. Na základě společné rozvahy jsou stanoveny priority terapie. V prvním cyklu není aplikován botulotoxin a pacienta pouze instruujeme o provádění strečinku (na více hyperaktivní antagonisty), případně rychlých střídavých pohybů (na více oslabené agonisty), je-li to možné. Důvodem je na jedné straně snaha o zlepšení klinického obrazu nefarmakologickými metodami před aplikací botulotoxinu z důvodu možného snížení aplikované dávky a/nebo kvůli lepší možnosti zaměřit budoucí aplikací cíleně na nejproblematičtější oblast (srov. výše část 3.3.2). Současně si ověřujeme spolupráci pacienta při cvičení, protože bez aktivního přístupu a dodržování předepsaného cvičení nelze od terapie očekávat dostatečný efekt. Pacient podepisuje informovaný souhlas, jež má formu „smluvní“ dohody v tom smyslu, že nedodržování předepsaného denního rehabilitačního tréninku může být důvodem pro ukončení účasti pacienta ve specializovaném programu našeho centra. Součástí pacientova závazku je také vedení denních záznamů o délce provádění předepsaného strečinku a počtu rychlých střídavých pohybů. Tříměsíční doba také dává prostor pro screening kognitivního deficitu a deprese, které mohou další terapii narušovat. V neposlední řadě jde o dobu, za níž se pacient blíže seznámí s novým terapeutickým režimem a má prostor diskutovat nejasnosti s terapeuty na kontrole za jeden měsíc od první návštěvy. Pokud pacient prokáže spolupráci a dostatečnou kognitivní způsobilost k absolvování terapeutického programu, je na začátku druhého cyklu znovu komplexně vyšetřen a podle tohoto vyšetření je aplikován botulotoxin a případně upraven terapeutický vzorec pro strečink a rychlé střídavé pohyby. Pacient je v tomto a dalších cyklech vždy kontrolován po měsíci, tj. na vrcholu dávky, kdy se ukáže, zda je vrcholový efekt botulotoxinu dostatečný pro posílení více paretických agonistů. Pacient je potom vyšetřen na začátku dalšího cyklu, tj. s odstupem tří měsíců, a toto vyšetření je porovnáváno se vstupním vyšetřením z předchozího cyklu. Ve vyšetření hodnotíme změnu úhlu pasivního a aktivního pohybu v kloubu, frekvenci rychlých střídavých pohybů, subjektivní vnímání funkce i výsledky v objektivních funkčních testech (srov. 63). V indikovaných případech naši pacienti současně s vedenou auto-terapií spastické parézy absolvují specializované skupinové či individuální programy (v běžném režimu 2x týdně) zaměřené na další symptomy svého onemocnění. Z nich je třeba vypíchnout alespoň dekondici, protože aerobní trénink mimo jiné prokazatelně podporuje indukované neuroplastické změny (157, 161) a napomáhá tak i vlastní terapii spastické parézy.
Shrnutí: Cíle rehabilitace ve spastickém stadiu
Ve spastickém stadiu se tedy primárně snažíme dosáhnout následujících cílů:
- Prevence úbytku vláken typu II. Za tím účelem je třeba trénovat rychlé pohyby končetinami, a to bez primárního ohledu na „kvalitu“ prováděného pohybu.
- Indukce neuroplastických změn. Pro nastartování procesů LTP je zásadní vysokofrekvenční stimulace o dostatečné intenzitě. V praxi to znamená, že je nutné využívat vysoce intenzivní formy terapie, tj. buď rozšířit délku trvání a frekvenci jednotlivých sezení terapie, nebo zvýšit náročnost trénovaných úkolů, např. pomocí maximálního rozsahu a rychlosti pohybu.
- Ovlivnění jasně definovaných cílů. Vyvolané neuroplastické změny probíhají vždy v příslušných, jasně definovaných oblastech, a proto je nutné terapii zaměřit pouze na několik málo konkrétních pohybů, aby byl její efekt maximální. Z tohoto důvodu musí být terapie specifická. Jasné stanovení cílů terapie pomůže zvolit segment vhodný pro trénink. Spolu s tím, jak v trénovaném segmentu dojde k případné obnově řízení pohybu, bude možné naučenou dovednost integrovat do funkčních činností, pokud trénovaný analytický pohyb od počátku odráží intendovanou funkční dovednost.
- Vhodná forma terapie pro dostatečnou retenci a transfer. Pro maximalizaci retence a transferu volíme u různých příznaků syndromu horního motoneuronu různé postupy s ohledem na způsob motorického učení, kterým příslušnou dovednost získáváme. V případě vlastní spastické parézy jsou vhodné i explicitní formy učení za podmínek specifikovaných v bodech 2 a 3.
- Primární zaměření terapie na antagonisty. U pacienta se spastickou parézou musíme vždy zahájit terapii ovlivněním a více hyperaktivních antagonistů pohybu v příslušných segmentech. Bez jejich dostatečného protažení a případné chemodenervace není možné efektivně (v některých případech dokonce vůbec) vyšetřit a terapeuticky oslovit více paretické agonisty.
- Normalizace tonu v segmentu. Společně s terapií zaměřenou na antagonisty se snažíme o tonizaci více paretických agonistů a reorganizaci CNS ve smyslu obnovy řízení pohybů vykonávaných těmito svaly.
3. GSC JAKO TERAPIE PRO CHRONICKÉ PACIENTY
Prof. Jean-Michel Gracies, M.D., Ph.D.
Département de Médecine Physique et de Réadaptation, Groupe Hospitalier Albert Chenevier - Henri Mondor, Créteil, Paříž, Francie
Deformující spastická paréza je syndrom, který zahrnuje slabost, zkrácení měkkých tkání a svalovou hyperaktivitu, včetně spasticity, tj. zvýšené reflexní odpovědi na fázický streč závislé na rychlosti protažení (68, 69, 70, 74, 75, 76). V návaznosti na lézi centrálních motorických drah se postupně objevují tyto tři hlavní faktory motorické poruchy, z nichž poslední dva brání aktivnímu pohybu:
I. streč-senzitivní paréza, kterou rozumíme snížení volního náboru motorických jednotek agonisty, které se zhoršuje při protažení antagonisty;
II. zkrácení měkkých tkání, o kterém mluvíme jak v souvislosti s postavením segmentu ve zkrácení, tak se sníženou extenzibilitou měkkých tkání;
III. svalová hyperaktivita, která zahrnuje:
a) spasticitu, což je zvýšená reflexní odpověď na fázický streč závislá na rychlosti pasivního protažení (63, 66);
b) spastickou dystonii, tj. dlouhodobou tonickou klidovou svalovou aktivitu, která je senzitivní na streč dystonického svalu;
c) spastickou ko-kontrakci, jíž rozumíme nepřiměřený stupeň kontrakce antagonisty při pokusu o volní kontrakci agonisty, senzitivní na streč ko-kontrahujícího se svalu.
Vzhledem k určujícím faktorům ko-kontrakce (aktivita agonisty a zkrácení či protažení antagonisty) by její terapie a terapie spastické parézy vůbec, měla logicky zahrnovat kombinaci těchto prvků:
I. Prolongovaný strečink všech hyperaktivních a zkrácených svalů, přičemž z dvojice hyperaktivního agonisty a antagonisty vybíráme ten více hyperaktivní a zkrácený. Tuto intervenci také případně kombinujeme s lokální chemodenervací, např. pomocí botulotoxinu, abychom rozbili bludný kruh hyperaktivita → zkrácení → hyperaktivita.
II. Intenzivní motorický trénink, tj. vysoký počet neasistovaných rapidních alterujících pohybů a funkčních cviků prováděných denně, cílených na méně hyperaktivní svaly, za účelem rozrušení bludného kruhu paréza → nepoužívání → paréza (76).
Recentní literatura jasně ukazuje, že:
- U hemiparetických pacientů je pro prevenci rozvoje zkrácení nutné provádět denně sub-maximální strečink hyperaktivních svalů po dobu delší, než 15 min. (5).
- Vysoký počet denně prováděných alterujících pohybů snižuje spastickou ko-kontrakci v trénovaném segmentu (89).
Posledních 50 let však nebylo při konvenční rehabilitaci chronických pacientů se spastickou parézou neobvyklé ji ukončit ve chvíli, kdy už se pacient takzvaně „nezlepší“. V zemích s nejvíce štědrým zdravotnictvím pak někteří pacienti mohli profitovat z období, kdy byla terapie na omezenou dobu obnovena, přičemž se tyto indikace obvykle řídily subjektivními kritérii. Tento systém je vzhledem k současným poznatkům o behaviorálně indukované plasticitě mozku a potenciálu ke zlepšení i v pozdních fázích spastické parézy nutno považovat za již zastaralý.
Vzhledem k současným finančním omezením ve zdravotnictví většiny zemí nemůže tento systém financovat fyzioterapeutickou a ergoterapeutickou péči v rozsahu a četnosti, které by byly vzhledem k výše řečenému potřeba. Proto představujeme alternativní metodu Dohody o reedukačním tréninku, která je způsobem, jak soustavně implementovat oba výše zmíněné rehabilitační principy, což může vést k významným funkčním zlepšením i v chronickém stadiu nemoci za předpokladu, že pacient nepřestane soustavně cvičit po dobu minimálně jednoho roku (5, 64, 69).
Na základě této dohody se z terapeuta stává kouč ve sportovním slova smyslu, který na pacienta dohlíží ve dvojím ohledu:
- technickém, kdy s ním vybírá potřebné cviky a vysvětluje mu je na pravidelných kontrolách, např. jednou za měsíc,
- psychologickém, aby dodržel svou část dohody, je-li k tomu kognitivně disponován, se pacient zavazuje, že:
- bude provádět předepsaný strečink a rychlé alterující pohyby denně po delší časový úsek,
- bude svůj výkon zaznamenávat písemně do deníku (64, 65, 68).
Jako doplněk této kvantifikované a monitorované domácí pohybové aktivity bude klinika pořádat pravidelné workshopy pro menší skupiny pacientů, které představují příležitost pro vzájemnou motivaci a další rozvoj technických dovedností potřebných pro trénink.
Pro účely naplnění této dohody jsme vyvinuli individuální reedukační deníky, které jsou součástí tréninkového manuálu pro pacienty a mohou sloužit jako návod pro cvičení v mezidobí mezi kontrolami nebo skupinovými instruktážemi.
Adresa ke korespondenci:
MUDr. Martina Hoskovcová
Rehabilitační oddělení Neurologické kliniky a Centra klinických neurověd 1. LF UK a VFN v Praze
Komplexní centrum pro léčbu spasticity Neurologické kliniky a Centra klinických neurověd 1. LF UK a VFN v Praze
e-mail: mhoskovcova@gmail.com
Sources
1. AASLUND, M. K., HELBOSTAD, J. L., MOE-NILSSEM, R.: Walking during body-weight-supported treadmill training and acute responses to varying walking speed and body-weight support in ambulatory patients post-stroke. Physiothe. Theory Pract., roč. 29, 2013, č. 4, s. 278-289.
2. ACSM: Exercise Management for Persons With Chronic Diseases & Disabilities. Illinois, Human Kinetics, 2009.
3. ACSM: Progression Models in Resistance Training for Healthy Adults. Med. Sci. Sports Exerc., roč. 41, 2009, č. 3, s. 687-708.
4. ADA, L., DEAN, C. M., VARGAS, J., ENNIS, S.: Mechanically assisted walking with body weight support results in more independent walking than assisted overground walking in non-ambulatory patients early after stroke: a systematic review. J. Physiother., roč. 56, 2010, č. 3, s. 153-161.
5. ADA, L., GODDARD, E., McCULLY, J., STAVRINOS, T., BAMPTON, J.: Thirty minutes of positioning reduces the development of shoulder external rotation contracture after stroke: a randomized controlled trial. Arch. Phys. Med. Rehabil., roč. 86, 2005, č. 2, s. 230-234.
6. ADA, L., O´DWYER, N., O´NEILL, E.: Relation between spasticity, weakness and contracture of the elbow flexors and upper limb activity after stroke: An observational study. Disabil. Rehabilit., roč. 28, 2006, č. 13-14, s. 891-897.
7. ADLER, S. S., BECKERS, D., BUCK, M.: PNF in Practice. Heidelberg, Springer, 2008.
8. ALEXANDER, M. A., MATTHEWS, D. J.: Pediatric rehabilitation. New York, Demos, 2010.
9. ALLARD, T., CLARK, S. A., JENKINS, W. M., MERZENICH, M. M.: Reorganization of somatosensory area 3b representations in adult owl monkeys after digital syndactyly. J. Neurophysiol., roč. 66, 1991, č. 3, s. 1048-1058.
10 AMBLER, Z., BAUER, J., KADAŇKA, Z.: Cévní onemocnění CNS. In: BEDNAŘÍK J., AMBLER Z., RŮŽIČKA E. a kol.: Klinická neurologie. Část speciální I, Praha, Triton, 2010.
11. ARYA, K. N., PANDIAN, S., VERMA, R., GARG, R. K.: Movement therapy induced neural reorganization and motor recovery in stroke: a review. J. Bodyw. Mov. Ther., roč. 15, 2011, č. 4, s. 528-537.
12. BAKER, J. A., PEREIRA, G.: The efficacy of Botulinum Toxin A for spasticity and pain in adults: a systematic review and meta-analysis using the Grades of Recommendation, Assessment, Development and Evaluation approach. Clin. Rehabil., roč. 27, 2013, č. 12, s. 1084-1096.
13. BARBOSA, D., SANTOS, C. P., MARTINS, M.: The application of cycling and cycling combined with feedback in the rehabilitation of stroke patients: A review. J. Stroke Cerebrovasc. Dis., roč. 24, 2015, č. 2, s. 253-273.
14. BARCLAY-GODDARD, R., STEVENSON, T., POLUHA, W. et al.: Force platform feedback for standing balance training after stroke. Cochrane Database Syst. Rev, roč. 4, 2004, CD004129.
15. BARCLAY-GODDARD, R. E., STEVENSON, T. J., POLUHA, W., THALMAN, L.: Mental practice for treating upper extremity deficits in individuals with hemiparesis after stroke. Cochrane Database Syst. Rev., roč. 5, 2011, CD005950.
16. BASMAJIAN, J. V., GOWLAND, C. A., FINLAYSON, M. A., HALL, A. L., SWANSON, L. R., STRATFORD, P. W., TROTTER, J. E., BRANDSTATTER, M. E.: Stroke treatment: comparison of integrated behavioral-physical therapy vs traditional physical therapy programs. Arch. Phys. Med. Rehabil., roč. 68, 1987, č. 1, s. 267-272.
17. BAYLE, N., GRACIES, J. M.: Management of deforming spastic paresis. In: SELZER M. E., CLARKE, S., COHEN, L. G., KWAKKEL, G., MILLER, R. H. (eds.): Textbook of Neural Repair and Rehabilitation 2ed, Cambridge. Cambridge University Press, 2014.
18. BAYLE, N., GRACIES, J. M.: The syndrome of deforming spastic paresis: pathophysiology, assessment and treatment. In: Shepherd, R.B. (ed.): Cerebral palsy in infancy. Edinburgh, Elsevier Ltd, 2014.
19. BELDA-LOIS, J. M., MENA-DEL HORNO, S., BERMEJO-BOSCH, I., MORENO, J. C., PONS, J. L., FARINA, D., IOSA, M. et al.: Rehabilitation of gait after stroke: A review towards a top-down approach. J. Neuroeng. Rehabil., roč. 8, 2011, s. 66.
20. BEN, M., HARVEY, L., DENIS, S., GLINSKY, J., GOEHL, G., CHEE, S., HERBERT, R. D.: Does 12 weeks of regular standing prevent loss of ankle mobility and bone mineral density in people with recent spinal cord injuries? J. Physiother., roč. 51, 2005, č. 4, s. 251-256.
21. BIRKENMEIER, R. L., PRAGER, E. M., LANG, C. E.: Translating animal doses of task-specific training to people with chronic stroke in 1-hour therapy sessions: a proof-of-concept study. Neurorehabil. Neural. Repair., roč. 24, 2010, č. 7, s. 620-635.
22. BOHIL, C. J., ALICEA, B., BIOCCA, F. A.: Virtual reality in neuroscience research and therapy. Nat. Rev. Neurosci., roč. 12, 2011, č. 12, s. 752-762.
23. BOVEND’EERDT, T. J., NEWMAN, M., BARKER, K., DAWES, H., MINELLI, C., WADE, D. T.: The effects of stretching in spasticity: A systematic review. Arch. Phys. Med. Rehabil., roč. 89, 2008, č. 7, s. 1395-1406.
24. BRAUN, S., KLEYNEN, M., VAN HEEL, T., KRUITHOF, N., WADE, D., BEURSKENS, A.: The effects of mental practice in neurological rehabilitation; a systematic review and meta-analysis. Front. Hum. Neurosci., roč. 7, 2013, s. 390.
25. BROWN, R. W., GONZALEZ, C. L., KOLB, B.: Nicotine improves Morris water task performance in rats given medial frontal cortex lesions. Pharmacol. Biochem. Behav., roč. 67, 2000, č. 3, s. 473-478.
26. BUCHNER, D. M., LARSON, E. B., WAGNER, E. H., KOEPSELL, T. D., DE LATEUR, B. J.: Evidence for a non-linear relationship between leg strength and gait speed. Age Ageing., roč. 25, 1996, č. 5, s. 386-391.
27. BUMA, F., KWAKKEL, G., RAMSEY, N.: Understanding upper limb recovery after stroke. Restor. Neurol. Neurosci., roč. 31, 2013, č. 6, s. 707-722.
28. BÜTEFISCH, C., HUMMELSCHEIM, H., DENZLER, P., MAURITZ, K. H.: Repetitive training of isolated movements improves the outcome of motor rehabilitation of the centrally paretic hand. J. Neurol. Sci., roč. 130, 1995, č. 1, s. 59-68.
29. CAREY, J. R., KIMBERLEY, T. J., LEWIS, S. M., AUERBACH, E. J., DORSEY, L., RUNDQUIST, P., UGURBIL, K. Analysis of fMRI and finger tracking training in subjects with chronic stroke. Brain., roč. 125, 2002, č. 4, s. 773-788.
30. CARSON, J. A., BOOTH, F. W.: Myogenin mRNA is elevated during rapid, slow, and maintenance phases of stretch-induced hypertrophy in chicken slow-tonic muscle. Pflugers Arch., roč. 435, 1998, č. 6, s. 850–858.
31. CIRSTEA, C. M., PTITO, A., LEVIN, M. F.: Feedback and cognition in arm motor skill reacquisition after stroke. Stroke, roč. 37, 2006, č. 5, s. 1237-1242.
32. CLARK, S. A., ALLARD, T., JENKINS, W. M., MERZENICH, M. M.: Receptive fields in the body-surface map in adult cortex defined by temporally correlated inputs. Nature., roč. 332, 1988, č. 6163, s. 444-445.
33. CLASSEN, J.: Rapid plasticity of human cortical movement representation induced by practice. J. Neurophysiol., roč. 79, 1998, č. 2, s. 1117-1123.
34. COLOMBO, G., JOERG, M., SCHREIER, R., DIETZ, V.: Treadmill training of paraplegic patients using a robotic orthosis. J. Reh. Dev., roč. 37, 2000, č. 6, s. 693-700.
35. CORNALL, C.: Is the Bobath approach relevant to neurophysiotherapy in 2010? A summary of the argument for the Bobath approach being relevant. CSP Bobath debate. www.acpin.net, 30. 3. 2015 19 : 43.
36. CRAMER, S. C., SUR, M., DOBKIN, B. H., O‘BRIEN, C., SANGER, T. D. et al.: Harnessing neuroplasticity for clinical applications. Brain, roč. 134, 2011, č. 6, s. 1591-1609.
37. CRONE, C., JOHNSEN, L. L., BIERING-SØRENSEN, F., NIELSEN, J. B.: Appearance of reciprocal facilitation of ankle extensors from ankle flexors in patients with stroke or spinal cord injury. Brain, roč. 126, 2003, č. 2, s. 495-507.
38. CUMMINGS, G. S., TILLMAN, L. J.: Remodeling of dense connective tissue in normal adult tissues. In: CURRIER D. P., NELSON R. M. (eds.): Dynamics of human biologic tissues. Philadelphia, FA Davies Comp., 1992.
39. DALGAS, U., STENAGER, E.: Exercise and disease progression in multiple sclerosis: can exercise slow down the progression of multiple sclerosis? Ther. Adv. Neurol. Disord., roč. 5, 2012, č. 2, s. 81-95.
40. DALY, J. J., RUFF, R. L.: Construction of efficacious gait and upper limb functional interventions based on brain plasticity evidence and model-based measures for stroke patients. ScientificWorld Journal., roč. 20, 2007, č. 7, s. 2031-2045.
41. DAYAN, E., COHEN, L. G.: Neuroplasticity subserving motor skill learning. Neuron., roč. 72, 2011, č. 3, s. 443-454.
42. de ALMEIDA OLIVEIRA, R., CINTIA DOS SANTOS VIEIRA, P., RODRIGUES MARTINHO FERNANDES, L. F. et al.: Mental practice and mirror therapy associated with conventional physical therapy training on the hemiparetic upper limb in poststroke rehabilitation: a preliminary study. Top Stroke Rehabil., roč. 21, 2014, č. 6, s. 484-494.
43. DECONINCK, F. J., SMORENBURG, A. R., BENHAM, A., LEDEBT, A., FELTHAM, M. G., SAVELSBERG, G. J.: Reflections on mirror therapy: A systematic review of the effect of mirror visual feedback on the Brain. Neurorehabil, Neural. Repair., roč. 29, 2015, č. 4, s. 349-361.
44. DeDEYENE, P. G.: Application of passive stretch and its implications for muscle fibres. Phys. Ther., roč. 81, 2001, č. 2, s. 819-827.
45. DEL-AMA, A. J., CUESTA, A., RAJASEKARAN, V., TRINCADO, F., IN, H., REINKENSMEYER, D.: Robotic rehabilitation: Ten critical questions about current status and future prospects answered by emerging researchers. In: Pons J. L., Toricelli D. (eds.): Emerging therapies in neurorehabilitation, Heidelberg, Springer-Verlag Berlin, 2014.
46. DEMETRIOS, M., KHAN, F., TURNER-STOKES, L., BRAND, C., McSWEENEY, S.: Multidisciplinary rehabilitation following botulinum toxin and other focal intramuscular treatment for post-stroke spasticity. Cochrane Database Sys.t Rev., roč. 6, 2013, CD009689.
47. DÉNES, Z.: Consequence of secondary complications during the rehabilitation of patients with severe brain injury. Orv. Hetil., roč. 150, 2009, č. 4, s. 165-169.
48. DENNY-BROWN, D.: The cerebral control of movement. Liverpool, Liverpool University Press, 1966.
49. DICKSTEIN, R., HOCHERMAN, S., PILLAR, T., SHAHAM, R.: Stroke rehabilitation. Three exercise therapy approaches. Phys. Ther., roč. 66, 1986, č. 8, s. 1233-1238.
50. DIETZ, V., SINKJAER, T.: Spastic movement disorder: impaired reflex function and altered muscle mechanics. Lancet Neurol., roč. 6, 2007, č. 8, s. 725-733.
51. DIONG, J., HARVEY, L. A., KWAH, L. K., CLARKE, J. L., BILSTON, L. E., GANDEVIA, S. C., HERBERT, R. D.: Gastrocnemius muscle contracture after spinal cord injury: a longitudinal study. Am. J. Phys. Med, Rehabil., roč. 92, 2013, č. 7, s. 565-574.
52. EGGINTON, S., ZHOU, A., BROWN, M. D. et al.: Unorthodox angiogenesis in skeletal muscle. Cardiovasc. Res., roč. 49, 2001, č. 3, s. 634–646.
53. EKLUND, G.: Position sense and state of contraction: the effects of vibration. J. Neurol. Neurosurg. Psychiatry, roč. 35, 1972, s. 606-611.
54. ERTELT, D., SMALL, S., SOLODKIN, A., DETTMERS, C., McNAMARA, A., BINKOFSKI, F., BUCCINO, G.: Action observation has a positive impact on rehabilitation of motor deficits after stroke. Neuroimage, roč. 36, 2007, č. S2, s. 164-173.
55. FERRANTE, S., AMBROSINI, E., RAVELLI, P. et al.: A biofeedback cycling training to improve locomotion: a case series study based on gait pattern classification of 153 chronic stroke patients. J. Neuroeng. Rehabil, roč. 8, 2011, s. 47.
56. FLEET, A., PAGE, S. J., MACKAY-LYONS, M., BOE, S. G.: Modified constraint-induced movement therapy for upper extremity recovery post stroke: What Is the evidence? Top Stroke Rehabil, roč. 21, 2014, č. 4, s. 319-331.
57. FOLEY, N., PEREIRA, S., SALTER, K., FERNANDEZ, M. M., SPEECHLEY, M., SEQEIRA, K., MILLER, T., TEASELL, R.: Treatment with botulinum toxin improves upper-extremity function post stroke: a systematic review and meta-analysis. Arch. Phys. Med. Rehabil., roč. 94, 2013, č. 5, s. 977-989.
58. FRENCH, B., THOMAS, L., LEATHLEY, M., SUTTON, CH., McADAM, J., FORSTER, A., LANGHORNE, P. et al.: Does repetitive task training improve finctional aktivity after stroke? A Cochrane systematic review and meta-analysis. J. Rehabil. Med., roč. 42, 2010, č. 1, s. 9-15.
59. GERVASIO, S., MACLEOD, C., ESTABAN-HERREROS, E. B., MENG, L., TEJADA, M. C.: Motor control and emerging therapies for improving mobility in patients with spasticity. In: Pons, J. L., Torricelli D. (eds.): Emerging therapies in neurorehabilitation, Heidelberg, Springer-Verlag, 2014.
60. GIOVANELLI, M., BORRIELLO, G., CASTRI, P., PROSPERINI, L., POZZILLI, C.: Early physiotherapy after injection of botulinum toxin increases the beneficial effects on spasticity in patients with multiple sclerosis. Clin. Rehabil., roč. 21, 2007, č. 4, s. 331-337.
61. GOLDSPINK, G.: Changes in muscle mass and phenotype and the expression of autocrine and systemic growth factors by muscle in response to stretch and overload. J. Anat., roč. 194, 1999, č. Pt 3, s. 323-334.
62. GOODWIN, G. M., McCLOSKEY, D. I., MATTHEWS, P. B.: The contribution of muscle afferents to kinaesthesia shown by vibration induced illusions of movement and by the effects of paralysing joint afferents. Brain, roč. 95, 1972, č. 4, s. 705-748.
63. GRACIES, J. M., BAYLE, N., VINTI, M., ALKANDARI, S., VU, P., LOCHE, C. M., COLAS, C.: Five-step clinical assessment in spastic paresis. Eur. J. Phys. Rehabil. Med., roč. 46, 2010, č. 3, s. 411-421.
64. GRACIES, J. M., BLONDEL, R., BAYLE, N., LOCHE, C., VU, P., COLAS, C.: Logique de Contrats d’Autorééducation Guidée dans la parésie spastique. Conception d’un manuel d’autorééducation. Ann. Phys. Rehabil. Med., roč. 53, 2010, s. e147.
65. GRACIES, J. M., BLONDEL, R., GAULT-COLAS, C., BAYLE, N.: Contrat d’Autorééducation Guidée dans la parésie spastique. Imprimeries APHP, ©Association Neurorééducation en Mouvement, 2010.
66. GRACIES, J. M., BURKE, K., CLEGG, N. J., BROWNE, R., RUSHING, C., FEHLINGS, D., MATTHEWS, D., TILTON, A., DELGADO, M. R.: Reliability of the Tardieu scale for assessing spasticity in children with cerebral palsy. Arch. Phy. Med. Rehab., roč. 91, 2010, č. 3, s. 421-428.
67. GRACIES, J. M., HEFTER, H., SIMPSON, D., MOORE, P.: Botulinum toxin in spasticity. In: MOORE P., NAUMANN M. (eds.): Handbook of Botulinum toxin. Oxford, Blackwell Science, 2002, s. 221-274.
68. GRACIES, J. M., WILSON, L., GANDEVIA, S. C., BURKE, D.: Stretched position of spastic muscles aggravates their co-contraction in hemiplegic patients. Ann. Neurol., roč. 42, 1997, č. 3, s. 438-439.
69. GRACIES, J. M.: Autoprise en charge du membre supérieur chez l’hémiplégique: expérience pilote d’un programme intensif d’étirements et de mouvements alternatifs rapides à domicile au long cours. Ann. Med. Phy., roč. 46, 2003, č. 7, s. 429.
70. GRACIES, J. M.: Evaluation de la spasticité – Apport de l’Echelle de Tardieu. Motricité Cérébrale, roč. 22, 2001, s. 1-16.
71. GRACIES, J. M.: Evaluation of walking speed (10m walking test) in patients with chronic hemiparesis after at least 3 consecutive botulinum neurotoxin injections while patients follow a guided self-rehabilitation contract, 26th Congress of Physical and Rehabilitation Medicine, 2011.
72. GRACIES, J. M.: Evidence for Increased Antagonist strength and movement speed following BTX injections in spasticity, Neurology, roč. 56, 2001, č. 8, s. A3.
73. GRACIES, J. M.: Guided Self-rehabilitation contracts and gait speed in chronic hemiparesis. A prospective study, 28th Congress of Physical and Rehabilitation Medicine, 2013.
74. GRACIES, J. M.: Pathophysiology of impairment in patients with spasticity and use of stretch as a treatment of spastic hypertonia. Phys. Med. Rehabil. Clin. N. Am., roč. 12, 2001, č. 4, s. 747-768.
75. GRACIES, J. M.: Pathophysiology of spastic paresis. I: Paresis and soft tissue changes. Muscle Nerve., roč. 31, 2005, č. 5, s. 535-551.
76. GRACIES, J. M.: Pathophysiology of spastic paresis. II: Emergence of muscle overactivity. Muscle Nerve., roč. 31, 2005, č. 5, s. 552-571.
77. GRIGG, P., FINERMAN, G. A., RILEY, L. H.: Joint-position sense after total hip replacement. J. Bone Joint Surg. Am., roč. 55, 1973, č. 5, s. 1016-1025.
78. GURUSAMY, K. S., AGGARWAL, R., PALANIVELU, L., DAVIDSON, B. R.: Virtual reality training for surgical trainees in laparoscopic surgery. Cochrane Database Syst. Rev., roč. 1, 2009, CD006575.
79. HARA, Y., MASAKADO, Y., CHINO, N.: The physiological functional loss of single thenar motor units in the stroke patients: when does it occur? Does it progress?. Clin. Neurophysiol., roč. 115, 2004, č. 1, s. 97-103.
80. HARRIS, K., REID, D.: The influence of virtual reality play on children‘s motivation. Can. J. Occup. Ther., roč. 72, 2005, č. 1, s. 21-29.
81. HARVEY, L. A., BYAK, A. J., OSTROVSKAYA, M., GLINSKY, J., KATTE, L., HERBERT, R. D.: Randomised trial of the effects of four weeks of daily stretch on extensibility of hamstring muscles in people with spinal cord injuries. Aust. J. Physiother., roč. 49, 2003, č. 3, s. 176-181.
82. HARVEY, L. A., GLINSKY, J. A., KATALINIC, O. M., BEN, M.: Contracture management for people with spoinal cord injuries. NeuroRehabilitation, roč. 28, 2011, č. 1, s. 17-20.
83. HENDERSON, A., KORNER-BITENSKY, N., LEVIN, M.: Virtual reality in stroke rehabilitation: a systematic review of its effectiveness for upper limb motor recovery. Top Stroke Rehabil., roč. 14, 2007, č. 2, s. 52-61.
84. HESSE, S., SARKODIE-GYAN, T., UHLENBROCK, D.: Development of an advanced mechanised gait trainer, controlling movement of the centre of mass, for restoring gait in non-ambulant subjects. Biomed. Tech., roč. 44, 1999, č. 7-8, s. 194-201.
85. HOANG, P. D., GANDEVIA, S. C., HERBERT, R. D.: Prevalence of joint contractures and muscle weakness in people with multiple sclerosis. Disabil. Rehabil., roč. 36, 2014, č. 19, s. 1588-1593.
86. HODGES, P. W., RICHARDSON, C. A.: Relationship between limb movement speed and associated contraction of the trunk muscles. Ergonomics, roč. 40, 1997, č. 11, s. 1220-1230.
87. HOLDEN, M. K.: Virtual environments for motor rehabilitation: review. Cyberpsychol Behav., roč. 8, 2005, č. 3, s. 187-211.
88. HOSP, J. A., LUFT, A. R.: Cortical plasticity during motor learning and recovery after ischemic stroke. Neural. Plast., 2011, 2011 : 871296.
89. HU, X.: Variation of muscle coactivation patterns in chronic stroke during robot-assisted elbow training. Arch. Phys. Med. Rehabil., roč. 88, 2007, č. 8, s. 1022-1029.
90. HUANG, H., WOLF, S. L., HE, J.: Recent developments in biofeedback for neuromotor rehabilitation. J. Neuroeng. Rehabil., roč. 3, 2006, s. 11.
91. HUBBARD, I. J., PARSONS, M. W., NEILSON, C., CAREY, L. M.: Task-specific training: evidence for and translation to clinical practice. Occup. Ther. Int., roč. 16, 2009, č. 3-4, s. 175-189.
92. HUMM, J. L., KOZLOWSKI, D. A., BLAND, S. T. et al.: Use-dependent exaggeration of brain injury: is glutamate involved? Exp. Neurol., roč. 157, 1999, č. 2, s. 349-358.
93. HUSSAIN, S., QUAN XIE, S., LIZ, G.: Robot assisted treadmill training: Mechanisms and training strategies. Med. Eng. Phys., roč. 33, 2011, č. 5, s. 527-533.
94. CHEN, P., GOLDBERG, D. E., KOLB, B., LANSER, M., BENOWITZ, L. I.: Inosine induces axonal rewiring and improves behavioral outcome after stroke. Proc. Natl. Acad. Sci. U S A., roč. 99, 2002, č. 13, s. 9031-9036.
95. JACK, D., BOIAN, R., MERIANS, A. S., TREMAINE, M., BURDEA, G. C., ADAMOVICH, S. V., RECCE, M., POIZNER, H.: Virtual reality-enhanced stroke rehabilitation. IEEE Trans. Neural. Syst. Rehabil. Eng., roč. 9, 2001, č. 3, s. 308-318.
96. JAFFE, D. L., BROWN, D. A., PIERSON-CAREY, C. D., BUCKLEY, E. L., LEW, H. L.: Stepping over obstacles to improve walking in individuals with poststroke hemiplegia. Journal of Rehabilitation Research & Development, roč. 41, 2004, č. 3A, s. 283-292.
97. JÄRVINEN, T. A., JÓZSA, L., KANNUS, P., JÄRVINEN, T. L., JÄRVINEN, M.: Organization and distribution of intramuscular connective tissue in normal and immobilized skeletal muscles. An immunohistochemical, polarization and scanning electron microscopic study. J. Muscle Res. Cell Motil., roč. 23, 2002, č. 3, s. 245-254.
98. KALLIO, K., NILSSON-WIKMAR, L., THORSÉN, A. M.: Modified constraint-induced therapy for the lower extremity in elderly persons with chronic stroke: Single-subject experimental design study. Top Stroke Rehabil., roč. 21, 2014, č. 2, s. 111-119.
99. KATALINIC, O. M., HARVEY, L. A., HERBERT, R. D.: Effectiveness of stretch for the treatment and prevention of contractures in people with neurological conditions: A systematic review. Phys. Ther., roč. 91, 2011, č. 1, s. 11-24.
100. KATCH, V. L., McARDLE, W. D. et al.: Essentials of exercise physiology. Philadelphia, Lippincott Williams & Wilkins, Baltimore, 2011.
101. KELLEY, G.: Mechanical overload and skeletal muscle fiber hyperplasia: a meta-analysis. J. Appl. Physiol., roč. 81, 1996, č. 4, s. 1584-1588.
102. KIM, J. H., JANG, S. H., KIM, C. S., JUNG, J. H., YUO, J. H.: Use of virtual reality to enhance balance and ambulation in chronic stroke: A double-blind, randomized controlled study. American Journal of Physical Medicine & Rehabilitation, roč. 88, 2009, č. 9, s. 693-701.
103. KING, M., HALE, L., PEKKARI, A., PERSSON, M., GREGERSSON, M., NILSSON, M.: An affordable, computerised, table-based exercise system for stroke survivors. Disabil. Rehabil. Assist. Technol., roč. 5, 2010, č. 4, s. 288-293.
104. KISNER, C., COLBY, J. A.: Stretching for impaired mobility. In: Therapeutic exercise foundations and techniques. 5ed. Philadelphia, F.A. Davis Company, 2007.
105. KIZONY, R., KATZ, N., WEISS, P.: Adapting an immersive virtual reality system for rehabilitation. Journal Vis. Comp. Anim., roč. 14, 2003, s. 1-7.
106. KLEIM, J. A., JONES, T. A.: Principles of experience-dependent neural plasticity: implications for rehabilitation after brain damage. J. Speech Lang Hear Res., roč. 51, 2008, č. 1, s. S225-239.
107. KLEIM, J. A., SCHWERIN, S.: Motor map plasticity: a neural substrate for improving motor function after stroke. In: CRAMER S. C., NUDO R. J. (eds): Brain repair after stroke. Cambridge, Cambridge University Press, 2010.
108. KOUTSOU, A. D., SUMMA, S., NASSER, B., MARTINEZ, J. G., THANGARAMANUJAM, M.: Upper limb neuroprostheses: Recent advances and future directions. In: PONS J. L., TORICELLI D. (eds.): Emerging therapies in neurorehabilitation, Heidelberg, Springer-Verlag Berlin, 2014.
109. KRAKAUER, J. W.: Motor learning: its relevance to stroke recovery and neurorehabilitation. Curr. Opin. Neurol., roč. 19, 2006, č. 1, s. 84-90.
110. KWAH, L .K., HARVEY, L. A., DIONG, J. H., HERBERT, R. D.: Half of the adults who present to hospital with stroke develop at least one contracture within six months: an observational study. J. Physiother., roč. 58, 2012, č. 1, s. 41-47.
111. KWAKKEL, G., KOLLEN, B. J., KREBS, H. I.: Effects of robot-assisted therapy on upper limb recovery after stroke: a systematic review. Neurorehabil. Neural. Repair., roč. 22, 2008, č. 2, s. 111-121.
112. KWAKKEL, G., VEERBEECK, J. M., VAN WEGEN, E. E. H., WOLF, S. L.: Constraint-induced movement therapy after stroke. Lancet Neuro., roč. 14, 2015, č. 2, s. 224-234.
113. LANCE, J. W.: Spasticity: disordered motor control. In: FELDMAN R.G., YOUNG R. R., KOELLA, W. P. (eds.): Symposium synopsis. Chicago, Yearbook Medical, 1980.
114. LANGE, B., FLYNN, S., CHANG, C.-Y., AHMED, A., GENG, Y., UTSAV, K., XU, M., SEOK, D., CHENG, S., RIZZO, A.: Development of an interactive rehabilitation game using the Nintendo (WiiFit) balance board for people with neurological injury. Topics Stroke Rehabil., roč. 15, 2010, č. 5, s. 345-352.
115. LANGHAMMER, B., STANGHELLE, J. K.: Bobath or motor relearning programme? A comparison of two different approaches of physiotherapy in stroke rehabilitation: a randomized controlled study. Clin. Rehabil., roč. 14, 2000, č. 4, s. 361-369.
116. LANGHORNE, P., BERNHARDT, J., KWAKKEL, G.: Stroke rehabilitation. Lancet., roč. 377, 2011, č. 9778, s. 1693-1702.
117. LANGHORNE, P., COUPAR, F., POLLOCK, A.: Motor recovery after stroke: A systematic review. Lancet Neurol., roč. 8, 2009, č. 8, s. 741-754.
118. LANNIN, N. A., ADA, L.: Neurorehabilitation splinting: theory and principles of clinical use. NeuroRehabilitation., roč. 28, 2011, č. 1, s. 21-28.
119. LANNIN, N. A., CUSICK, A., McCLUCKEY, A., HERBERT, R. D.: Effects of splinting on wrist contracture after stroke: a randomized controlled trial. Stroke, roč. 38, 2007, č. 1, s. 111-116.
120. LANNIN, N. A., HERBERT, R. D.: Is hand splinting effective for adults following stroke? A systematic review and methodologic critique of published research. Clin. Rehabil., roč. 17, 2003, č. 8, s. 807-816.
121. LANNIN, N. A., NOVAK, I., CUSICK, A.: A systematic review of upper extremity casting for children and adults with central nervous system motor disorders. Clin. Rehabil., roč. 21, 2007, č. 11, s. 963-976.
122. LAVER, K. E., GEORGE, S., THOMAS, S., DEUTSCH, J. E., CROTTY, M.: Virtual reality for stroke rehabilitation. Cochrane Database Syst. Rev., roč. 2, 2015, CD008349.
123. LEASURE, J. L., SCHALLERT, T.: Consequences of forced disuse of the impaired forelimb after unilateral cortical injury. Nebav. Brain Res., roč. 150, 2004, č. 1-2, s. 83-91.
124. LIN, S. I., LO, C. C., LIN, P.-Y. et al.: Biomechanical assessments of the effect of visual feedback on cycling for patients with stroke. J. Electromyogr. Kinesiol., roč. 22, 2012, č. 4, s. 582-588.
125. LIU, K. P., CHAN, C. C., LEE, T. M., HUI-CHAN, C. W. et al.: Mental imagery for promoting relearning for people after stroke: A randomized controlled trial. Arch. Phys. Med. Rehabil., roč. 85, 2004, č. 9, s. 1403-1408.
126. LIU, K. P., CHAN, C. C., WONG, R. S., KWAN, I. W., YAU, C. S., LI, L. S., LEE, T. M.: A randomized controlled trial of mental imagery augment generalization of learning in acute poststroke patients. Stroke, roč. 40, 2009, č. 6, s. 2222-2225.
127. LIU, Z., CHOPP, M., DING, X., CUI, Y., LI, Y.: Axonal remodeling of the corticospinal tract in the spinal cord contributes to voluntary motor recovery after stroke in adult mice. Stroke, roč. 44, 2013, č. 7, s. 1951-1956.
128. LUM, P. S., BURGAR, C. G., SHOR, P. C., MAJMUNDAR, M., VAN DER LOOS, M.: Robot-assisted movement training compared with conventional therapy techniques for the rehabilitation of upper-limb motor function after stroke. Arch. Phys. Med. Rehabil., roč. 83, 2002, č. 7, s. 952-959.
129. MARTINELLO, K., HUANG, Z., LUJAN, R., TRAN, B., WATANABE, M., COOPER, E. C., BROWN, D. A., SHAH, M. M.: Cholinergic afferent stimulation induces axonal function plasticity in adult hippocampal granule cells. Neuron., roč. 85, 2015, č. 2, s. 346-363.
130. MASIERO, S., POLI, P., ROSATI, G., ZANOTTO, D., IOSA, M., PAOLUCCI, S., MORONE, G.: The value of robotic systems in stroke rehabilitation. Expert Rev. Med. Devices., roč. 11, 2014, č. 2, s. 187-198.
131. MAYSTON, M.: The Bobath concept today. In: Syn´apse, 2001/Spring.
132. McGUIRE, J. R.: Spasticity and other signs of the upper motor neuron syndrome. In: BRASHEAR A., ELOVIC E. (eds.): Spasticity - Diagnosis and management. New York, Demos Medical Publishing LLC, 2011.
133. MEHRHOLZ, J., ELSNER, B., WERNER, C., KUGLER, J., POHL, M.: Electromechanical-assisted training for walking after stroke. Cochrane Database Syst. Rev., roč. 7, 2013, CD006185.
134. MEHRHOLZ, J., ELSNER, B., WERNER, C., KUGLER, J., POHL, M.: Electromechanical-assisted training for walking after stroke: Updated evidence. Stroke, roč. 44, 2013, č. 10, s. e127-128.
135. MEHRHOLZ, J., HÄDRICH, A., PLATZ, T., KUGLER, J., POHL, M.: Electromechanical and robot-assisted arm training for improving generic activities of daily living, arm function, and arm muscle strength after stroke. Cochrane Database Syst. Rev., roč. 6, 2012, CD006876.
136. MEHRHOLZ, J., POHL, M.: Rehabilitation robotics, orthotics, and prosthetics: lower limbs. In: SELZER M. E., CLARKE S., COHEN L. G..,KWAKKEL G., MILER R. H. (eds.): Textbook of neural repair and rehabilitation 2ed. Cambridge, Cambridge University Press, 2014.
137. MEHRHOLZ, J., WERNER, C., KUGLER, J., POHL, M.: Electromechanical-assisted training for walking after stroke. Cochrane Database Syst. Rev., roč. 4, 2007, CD006185.
138. MEIMOUN, M., BAYLE, N., BAUDE, M., GRACIES, J. M.: Intensity in the neurorehabilitation of spastic paresis. Rev. Neurol., roč. 171, 2015, č. 2, s. 130-140.
139. MEINTZSCHEL, F., ZIEMANN, U.: Modification of practice-dependent plasticity in human motor cortex by neuromodulators. Cereb Cortex., roč. 16, 2006, č. 8, s. 1106-1115.
140. MILLER, E. L., MURRAY, L., RICHARDS, L., ZOROWITZ, R. D., BAKAS, T., CLARK, P., BILLINGER, S. A.: American Heart Association council on cardiovascular nursing and the stroke council.: Comprehensive overview of nursing and interdisciplinary rehabilitation care of the stroke patient: A scientific statement from the American Heart Association. Stroke, roč. 41, 2010, č. 10, s. 2402-2448.
141. MIRELMAN, A., BONATO, P., DEUTSCH, J. E.: Effects of training with a robot-virtual reality system compared with a robot alone on the gait of individuals after stroke. Stroke, roč. 40, 2009, č. 1, s. 169-174.
142. MOGILNER, A., GROSSMAN, J. A., RIBARY, U., JOLIOT, M., VOLKMANN, J., RAPAPORT, D., BEASLEY, R. W., LLINÁS, R. R.: Somatosensory cortical plasticity in adult humans revealed by magnetoencephalography. Proc. Natl. Acad. Sci. U S A., roč. 90, 1993, č. 8, s. 3593-3597.
143. MORIYAMA, H., TOBIMATSU, Y., OZAWA, J., KITO, N., TANAKA, R.: Amount of torque and duration of stretching affects correction of knee contracture in a rat model of spinal cord injury. Clin. Orthop. Relat. Res., roč. 471, 2013, č. 11, s. 3626-3636.
144. MORRIS, D., TAUB, E., MARK, V.: Constraint-induced movement therapy: characterizing the intervention protocol. Eura Medicophys, roč. 42, 2006, č. 3, s. 257-268.
145. MOSELEY, A. M., HASSETT, L. M., LEUNG, J., CLARE, J. S., HERBERT, R. D., HARVEY, L. A.: Serial casting versus positioning for the treatment of elbow contractures in adults with traumatic brain injury: a randomized controlled trial. Clin. Rehabil., roč. 22, 2008, č. 5, s. 406-417.
146. NAKAGAWA, H., UENO, M., ITOKAZU, T., YAMASHITA, T.: Bilateral movement training promotes axonal remodeling of the corticospinal tract and recovery of motor function following traumatic brain injury in mice. Cell Death Dis., roč. 7, 2013, č. 4, s. e534.
147. NIJLAND, R., KWAKKEL, G., BAKERS, J., VAN WEGEN, E.: Constraint-induced movement therapy for the upper paretic limb in acute or sub-acute stroke: a systematic review. Int. J. Stroke, roč. 6, 2011, č. 5, s. 425-433.
148. NIJLAND, R., VAN WEGEN, E., VAN DER KROGT, H., BAKKER, C., BUMA, F., KLOMP, A., VAN KORDELLAR, J., KWAKKEL, G.: Characterizing the Protocol for early modified constraint-induced movement therapy in the EXPLICIT-stroke trial. Physiother. Res. Int., roč. 18, 2013, č. 1, s. 1-15.
149. O´SULLIVAN, S. ., SCHMITZ, T. J.: Physical rehabilitation. 5ed, Philadelphia, FA Davis Comp., 2007.
150. OLVEY, E. L., ARMSTRONG, E. P., GRIZZLE, A. J.: Contemporary pharmacologic treatments for spasticity of the upper limb after stroke: a systematic review. Clin. Ther., roč. 32, 2010, č. 14, s. 2282-2303.
151. PAGE, S., DUNNING, K., HERMANN, V., LEONARD, A., LEVINE, P.: Longer versus shorter mental practice sessions for affected upper extremity movement after stroke: A a randomized controlled trial. Clin. Rehabil., roč. 25, 2011, č. 7, s. 627-637.
152. PAGE, S. J., LEVINE, P., LEONARD, A.: Mental practice in chronic stroke: results of a randomized, placebo-controlled trial. Stroke, roč. 38, 2007, č. 4, s. 1293-1297.
153. PAGE, S. J., SISTO, S. A., LEVINE, P., JOHNSTON, M. V., HUGHES, M.: Modified constraint induced therapy: a randomized feasibility and efficacy study. J. R ehabil. Res. Dev., roč. 38, 2001, č. 5, s. 583-590.
154. PAGE, S. J.: Intensity versus task-specifi city after stroke: How important is intensity? Am. J. Phys. Med. Rehabil., roč. 82, 2003, č. 9, s. 730-732.
155. PEURALA, S. H., KANTANEN, M. P., SJÖGREN, T., PALTAMAA, J., KARHULA, M., HEINONEN, A.: Effectiveness of constraint-induced movement therapy on activity and participation after stroke: a systematic review and meta-analysis of randomized controlled trials. Clin. Reh., roč. 26, 2011, č. 3, s. 209-223.
156. PLATZ, T., WINTER, T., MÜLLER, N. et al.: Arm ability training for stroke and traumatic brain injury patients with mild arm paresis: A single-blind, randomized, controlled trial. Arch. Phys. Med. Rehabil, roč. 82, 2001, č. 7, s. 961-968.
157. PLOUGHMAN, M., AUSTIN, M. W., GLYNN, L., CORBETT, D.: The effects of poststroke aerobic exercise on neuroplasticity: a systematic review of animal and clinical studies. Transl. Stroke Res., roč. 6, 2015, č. 1, s. 13-28.
158. POHL, M., MEHRHOLZ, J.: A new shoulder range of motion screening measurement: its reliability and application in the assessment of the prevalence of shoulder contractures in patients with impaired consciousness caused by severe brain damage. Arch. Phys. Med. Rehabil., roč. 86, 2005, č. 1, s. 98-104.
159. POLESE, L. C., ADA, L., DEAN, C. M., NASCIMENTO, L. R., TEIXEIRA-SALMELA, L. F.: Treadmill training is effective for ambulatory adults with stroke: a systematic review. J. Phys., roč. 59, 2013, č. 2, s. 73-80.
160. POLLOCK, A., FARMER, S. E., BRADY, M. C., LANGHORNE, P., MEAD, G. E., MEHRHOLZ, J., van WIJCK, F.: Interventions for improving upper limb function after stroke. Cochrane databáze Syst. Rev., roč. 12, 2014, č. 11, CD010820.
161. PRAKASH, R. S., SNOOK, E. M., ERICKSON, K. I., COLCOMBE, S. J., VOSS, M. W., MOTL, R. W., KRAMER, A. F.: Cardiorespiratory fitness: A predictor of cortical plasticity in multiple sclerosis. Neuroimage., roč. 34, 2007, č. 3, s. 1238-1244.
162. PROSKE, U., GANDEVIA, S. C.: The proprioceptive senses: their roles in signaling body shape, body position and movement, and muscle force. Physiol. Rev., roč. 92, 2012, č. 4, s. 1651-1697.
163. PROSKE, U., MORGAN, D. L., GREGORY, J. E.: Thixotropy in skeletal muscle and in muscle spindles: A review. Prog. Neurobiol., roč. 41, 1993, č. 6, s. 705-721.
164. PURVES, D., AUGUSTINE, G. J., FITZPATRICK, D., HALL, W. C., LaMANTIA, A. S., McNAMARA, J. O., WILLIAMS, S. M.: Neuroscience 4ed, Sunderland, Sinauer Associates, Inc., 2014.
165. RAINE, S., MEADOWS, L., LYNCH-ELLERINGTON, M.: Bobath concept Theory and clinical practice in neurological rehabilitation. Chichester, Blackwell Publishing Ltd., 2009.
166. REINER, R.: Virtual reality for neurorehabilitation. In: DIETZ V., WARD N. (eds.): Oxford textbook of neurorehabilitation. Oxford, Oxford University Press, 2015.
167. RENSINK, M., SCHUURMANS, M., LINDEMAN, E., HAFTEINSDÓTTIR, T.: Task-oriented training in rehabilitation after stroke: Systematic review. J. Adv. Nurs, roč. 65, 2009, č. 4, s. 737-754.
168. RICCIO, I., IOLASCON, G., BARILLARI, M. R., GIMIGLIANO, R., GIMIGLIANO, F.: Mental practice is effective in upper limb recovery after stroke: a randomized single-blind cross-over study. Eur. J. Phys. Rehabil. Med., roč. 46, 2010, č. 1, s. 19-25.
169. RICHARDS, L., HANSON, C., WELLBORN, M., SETHI, A.: Driving motor recovery after stroke. Top. Stroke. Rehabil., roč. 15, 2008, č. 5, s. 397-411.
170. RIZZO, A., KIM, G. J.: A SWOT analysis of the field of virtual reality rehabilitation and therapy. Presence, roč. 14, 2005, č. 2, s. 119-146.
171. RODRIQUEZ, A. A.: Botulinum toxin injection of spastic finger flexors in hemiplegic patients. Am. J. Phys. Med. Rehabil., roč. 79, 2000, č. 1, s. 44-47.
172. SACKLEY, C., BRITTLE, N., PATEL, S., ELLINS, J., SCOTT, M., WRIGHT, C., DEWEY, M. E.: The prevalence of joint contractures, pressure sores, painful shoulder, other pain, falls, and depression in the year after a severely disabling stroke. Stroke, roč. 39, 2008, č. 12, s. 3329-3334.
173. SAUNDERS, D. H., SANDERSON, M., BRAZZELLI, M., GREIG, C. A., MEAD, G. E.: Physical fitness training for stroke patients. Cochrane Database Syst. Rev., roč. 10, 2013, CD003316.
174. SEITZ, R. J.: Brain events in the acute period of stroke in relation to subsequent repair. In: CRAMER S.C., NUDO R.J. (eds.): Brain repair after stroke. Cambridge, Cambridge University Press, 2010.
175. SHEPHERD, R. B. (ed.): Cerebral palsy in infancy. Edinburgh, Elsevier Ltd, 2014.
176. SHEPHERD, R. B., CARR, J.: Treadmill walking in neurorehabilitation. Neurorehabilitaion and Neural. Repair., roč. 13, 1999, s. 171-173.
177. SHUMWAY-COOK, A., WOOLLACOTT, M.: Motor control: translating research into clinical practice, 4ed., Philadelphia, Lippincott Williams & Wilkins, 2012.
178. SCHUEMIE, M. J., VAN DER STRAATEN, P., KRIJN, M., VAN DER MAST, C. A.: Research on presence in virtual reality: a survey. Cyberpsychol. Behav., roč. 4, 2001, č. 2, s. 183-201.
179. SCHWARTZ, I., MEINER, Z.: Robotic-assisted gait training in neurological patients: Who may benefit? Ann. Biomed. Eng., 2015, Feb 28. [Epub ahead of print].
180. SINGER, B. J., JEGASOTHY, G. M., SINGER, K. P., ALLISON, G. T., DUNNE, J. W.: Incidence of ankle contracture after moderate to severe acquired brain injury. Arch. Phys. Med .Rehabil., roč. 85, 2004, č. 9, s. 1465-1469.
181. SMANIA, N., GANDOLFI, M., PAOLUCCI, S., IOSA, M., IANES, P., RECCHIA, S., GIOVANZANA, C., MOLTENI, F., AVESANI, R. et al.: Reduced-intensity modified constraint-induced movement therapy versus conventional therapy for upper extremity rehabilitation after stroke: A multicenter trial. Neurorehabilitation and Neural Repair., roč. 26, 2012, č. 9, s. 1035-1045.
182. SONG, R., TONG, K. Y., HU, X. L., TSANG, V. S., LI, L.: The therapeutic effects of myoelectrically controlled robotic system for persons after stroke – a pilot study. Engineering in Medicine and Biology Society (EMBS=06). 28th Annual International Conference of the IEEE; 2006, Aug, New York (NY), s. 4945-4948.
183. STEFAN, K., KUNESCH, E., COHEN, L. G., BENECKE, R., CLASSEN, J.: Induction of plasticity in the human motor cortex by paired associative stimulation. Brain, roč. 123, 2000, č. 3, s. 572-584.
184. STEFAN, K., WYCISLO, M., CLASSEN, J.: Modulation of associative human motor cortical plasticity by attention. J. Neurophysiol., roč. 92, 2004, č. 1, s. 66-72.
185. STERN, P. H., McDOWELL, F., MILLER, J. M., ROBINSON, M.: Effects of facilitation exercise techniques in stroke rehabilitation. Arch. Phys. Med. Rehabil., roč. 51, 1970, č. 9, s. 526-531.
186. STERN, S. A., ALBERINI, C. M.: Mechanisms of memory enhancement. Wiley Interdiscip Revm Syst, Biol, Med., roč. 5, 2013, č. 1, s. 37-53.
187. SUBRAMANIAN, S. K., MASSIE, C. L., MALCOLM, M. P. et al.: Does provision of extrinsic feedback result in improved motor learning in the upper limb poststroke? A systematic review of the evidence. Neurorehabil. Neural. Repair., roč. 24, 2010, č. 2, s. 113-124.
188. SVEISTRUP, H.: Motor rehabilitation using virtual reality. J. Neuroeng. Rehabil., roč. 1, 2004, č. 1, s. 10.
189. ŠTĚTKÁŘOVÁ, I., EHLER, E., JECH, R.: Spasticita a její léčba. Praha, MaxdorfJessenius, 2012.
190. TAKAHASHI, C. D., DER-YEGHIAIAN, L., LE, V., MOTIWALA, R. R., CRAMER, S. C.: Robot-based hand motor therapy after stroke. Brain., roč. 131, 2008, č. 2, s. 425-437.
191. TALVITIE, U.: Socio-affective characteristics and properties of extrinsic feedback in physiotherapy. Physiother. Res. Int, roč. 5, 2000, č. 3, s. 173-189.
192. TAUB, E., USWATTE, G., MARK, V. W., MORRIS, D. M., BARMAN, J., BOWMAN, M. H., BRYSON, C., DELGADO, A., BISHOP-McKAY, S.: Method for enhancing real-world use of a more affected arm in chronic stroke: transfer package of constraint-induced movement therapy. Stroke, roč. 44, 2013, č. 5, s. 1383-1388.
193. THRANE, G., FRIBORG, O., ANKE, A., INDREDAVIK, B.: A meta-analysis of constraint-induced movement therapy after stroke. J. Rehabil. Med., roč. 46, 2014, č. 9, s. 833-842.
194. TORKINGTON, J., SMITH, S. G., REES, B. I., DARZI, A.: Skill transfer from virtual reality to a real laparoscopic task. Surg. Endosc., roč., 15, 2001, č. 10, s. 1076-1079.
195. TURTON, A. J., BRITTON, E.: A pilot randomized controlled trial of a daily muscle stretch regime to prevent contractures in the arm after stroke. Clin. Rehabil., roč. 19, 2005, č. 6, s. 600-612.
196. UMPHRED, D. A.: Neurological rehabilitation. St. Louis, Mosby, 2012.
197. VAN VLIET, P. M., WULF, G.: Extrinsic feedback for motor learning after stroke: what is the evidence? Disabil. Rehabil, roč. 28, 2006, č. 13-14, s. 831-840.
198. VEERBEEK, J. M., VAN WEGEN, E., VAN PEPPEN, R., VAN DER WEES, P. J., HENDRIKS, E., RIETBERG, M., KWAKKEL, G.: What is the evidence for physical therapy poststroke? A systematic review and meta-analysis. PLOS One., roč. 9, 2014, č. 2, s. e87987.
199. VÉLE, F.: Kineziologie. Praha, Triton, 2006.
200. VINTI, M., COUILLANDRE, A., HAUSSELLE, J., BAYLE, N., PRIMERANO, A., MERLO, A., HUTIN, E., GRACIES, J. M.: Influence of effort intensity and gastrocnemius stretch on co-contraction and torque production in the healthy and paretic ankle. Clin. Neurophysiol., roč. 123, 2013, č. 3, s. 528-535.
201. WAGENAAR, R. C., MEIJER, O. G., VAN WIERINGER, P. C., KUIK, D. J., HAZENBERG, G. J., LINDEBOOM, J. et al.: The functional recovery of stroke: a comparison between neuro-developmental treatment and the Brunnstrom method. Scand. J. Rehabil. Med., roč. 22, 1990, č. 1, s. 1-8.
202. WALL, P. D., NOORDENBOS, W.: Sensory functions which remain in man after complete transection of dorsal columns. Brain, roč. 100, 1977, č. 4, s. 641-653.
203. WARD, N. S.: Human brain mapping of the motor system after stroke. In: CRAMER S.C., NUDO R.J. (eds): Brain repair after stroke. Cambridge, Cambridge University Press, 2010.
204. WEISS, P. L., KIZONY, R. FEINTUCH, U., RAND, D., KATZ, N.: Virtual reality application in neurorehabilitation. In: SELZER M.E., CLARKE S., COHEN L.G., KWAKKEL G., MILLER R. H. (eds.): Textbook of neural repair and rehabilitation 2ed. Cambridge, Cambridge University Press, 2014.
205. WILLIAMS, P. E., GOLDSPINK, G.: Connective tissue changes in immobilised muscle. J. Anat., roč. 138, 1984, č. 2, s. 343-350.
206. WITMER, B. G., SINGER, M. J.: Measuring presence in virtual environments: A presence questionnaire. Presence, roč. 7, 1998, s. 225-240.
207. WOLF, S. L., NEWTON, H., MADDY, D., BLANTON, S., ZHANG, Q., WINSTEIN, C. J., MORRIS, D. M., LIGHT, K.: The excite trial: relationship of intensity of constraint induced movement therapy to improvement in the wolf motor function test. Restor. Neurol. Neurosci., roč. 25, 2007, č. 5-6, s. 549-562.
208. WOLF, S. L., WINSTEIN, C. J.: Intensive physical therapeutic approaches to stroke recovery. In: CRAMER S. C., NUDO R. J. (eds.): Brain repair after stroke. Cambridge, Cambridge University Press, 2010.
209. WOLF, S. L.: Electromyographic biofeedback applications to stroke patients. A critical review. Phys. Ther., roč. 63, 1983, č. 9, s. 1448-1459.
210. XERRI, C., MERZENICH, M. M., PETERSON, B. E., JENKINS, W.: Plasticity of primary somatosensory cortex paralleling sensorimotor skill recovery from stroke in adult monkeys. J. Neurophysiol., roč. 79, 1998, č. 4, s. 2119-2148.
211. YANG, Y. R., TSAI, M. P., CHUANG, T. Y., SUNG, W. H., WANG, R. Y.: Virtual reality-based training improves community ambulation in individuals with stroke: A randomized controlled trial. Gait and Posture., roč. 28, 2008, č. 2, s. 201-206.
212. YARKONY, G. M., SAHGAL, V.: Contractures. A major complication of craniocerebral trauma. Clin. Orthop. Relat. Res., roč. 219, 1987, s. 93-96.
213. YELNIK, A. P., SIMON, O., PARRATTE, B., GRACIES, J. M.: How to clinically assess and treat muscle overactivity in spastic paresis. J. Rehabil. Med., roč. 42, 2010, č. 9, s. 801-807.
214. ZAAIMI, B., EDGLEY, S. A., SOTEROPOULOS, D. S., BAKER, S. N.: Changes in descending motor pathway connectivity after corticospinal tract lesion in macaque monkey. Brain., roč. 135, 2012, č. 7, s. 2277-2289.
Labels
Physiotherapist, university degree Rehabilitation Sports medicine
Article was published inRehabilitation & Physical Medicine

2015 Issue 3
Most read in this issue- Spasticita u dětské mozkové obrny (DMO)
- Neuroplasticita, restituce motorických funkcí a možnosti rehabilitace spastické parézy
- Rameno v kostce – III. část
- Spasticita a roztroušená skleróza
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

