-
Medical journals
- Career
Analoga gonadoliberinu v léčbě infertility
: I. Crha; R. Hudeček; Martin Huser
: Gynekologicko-porodnická klinika, LF MU a FN Brno
: Prakt Gyn 2011; 15(3-4): 152-156
: Review Article
Cílem práce je aktuální přehled racionálního využití analog gonadoliberinu (GnRH = gonadotropin releasing hormone) při terapii poruch plodnosti žen. Pro rešerši průkazných dokumentů byly použity databáze Cochrane Library Reviews and Protocols, Database of Abstractsof Reviews of Effects (DARE) a MEDLINEplus a léčebné postupy Centra asistované reprodukce Gynekologicko-porodnické kliniky. GnRH-analoga jsou využívána při léčbě endometriózy, děložních myomů, v protokolech ovariální stimulace pro metody asistované reprodukce a pro ochranu ovarií při gonadotoxické léčbě. GnRH-analoga mají velký přínos pro terapii poruch plodnosti žen.
Klíčová slova:
GnRH analoga – triptorelin – neplodnost – endometrióza – myomatózaÚvod
Historicky prvním krokem pro pochopení řízení aktivity gonád byl poznatek, že poškození předního laloku hypofýzy vede ke genitální atrofii [1], který byl učiněn začátkem 20. století. GnRH dekapeptid byl izolován a jeho struktura upřesněna v roce 1971. Při substituci jednotlivých aminokyselin byl objeven význam jednotlivých úseků pro stabilitu, vazbu na receptory a aktivaci gonadotrofních buněk štítné žlázy [2]. Modifikací na pozicích 6 a 10 byla vytvořena analoga, která měla mnohonásobně zvýšenou aktivitu a poločas odbourávání.
V roce 1978 bylo objasněno úvodní zvýšení gonadotropinů (flare-up) a následné potlačení (downregulation) GnRH-receptorů hypofýzy při aplikaciGnRH agonistů [3]. V roce 1980 bylo poprvé publikováno pulzatilní podání nízkých dávek GnRH agonistů u ženy s hypogonadotropním hypogonadizmem, které vedlo k těhotenství [4]. Počátkem 80. let byla aplikace GnRH agonistů použita také pro prevenci předčasného zvýšení luteinizačního hormonu (LH) při stimulaci ovarií [5]. Během necelých deseti let se stimulační protokol s využitím GnRH agonistů stal základem každodenní praxe IVF, signifikantně snížil podíl zrušených cyklů a zlepšil výsledky a flexibilitu časování odběru oocytů [6].
V roce 2001 byla do klinické praxe zavedena třetí generace GnRH antagonistů – ganirelix a cetrorelix, pro které je charakteristický rychlý nástup suprese a rychlé obnovení receptorů po ukončení jejich aplikace.
GnRH analoga a jejich schopnost velmi účinně a reverzibilně kontrolovat sekreci gonadotropinů hypofýzy přinesla také nové možnosti léčby onemocnění, která vedou k alteraci reprodukčních funkcí. Výrazně zlepšila léčbu endometriózy, děložních myomů. Suprese aktivity ovaria pomocí GnRH agonistů se stala také základem ochrany reprodukce u žen podstupujících gonadotoxickou léčbu [7]. Cílem této práce je aktuální přehled racionálního využití analog gonadoliberinu při terapii poruch plodnosti žen.
GnRH analoga v řízené ovariální stimulaci
Prevence předčasného peaku LH
Před zavedením GnRH analog do klinického použití byla základem stimulace aplikace folikulostimulačního hormonu (FSH) v kombinaci s klomifencitrátem. Předčasný peak LH vedl ke zrušení 20–25 % cyklů, pregnancy rate se pohybovala kolem 6 % zahájených cyklů [8]. GnRH analoga se podílela na výrazném zlepšení výsledků, farmaceutický průmysl přinesl širokou nabídku účinných látek (tab. 1) v různé formě a s různým podáním – aplikace podkožní injekce 1× denně, depotní injekce, nosní sprej. Systematický přehled výsledků v „Cochrane Database” neprokázal signifikantní rozdíly mezi depotní a denní formou podání [9]. Velká pozornost byla věnována optimálnímu protokolu podávání. Při krátkém protokolu se využívá zvýšená sekrece (flare up) FSH indukovaná GnRH agonisty, které jsou podávány současně s exogenním FSH (obr. 1).Po ústupu zvýšené sekrece v dalších dnech je navozen útlum LH a sníženo riziko předčasného peaku.
1. GnRH-analoga používaná při léčbě endometriózy. 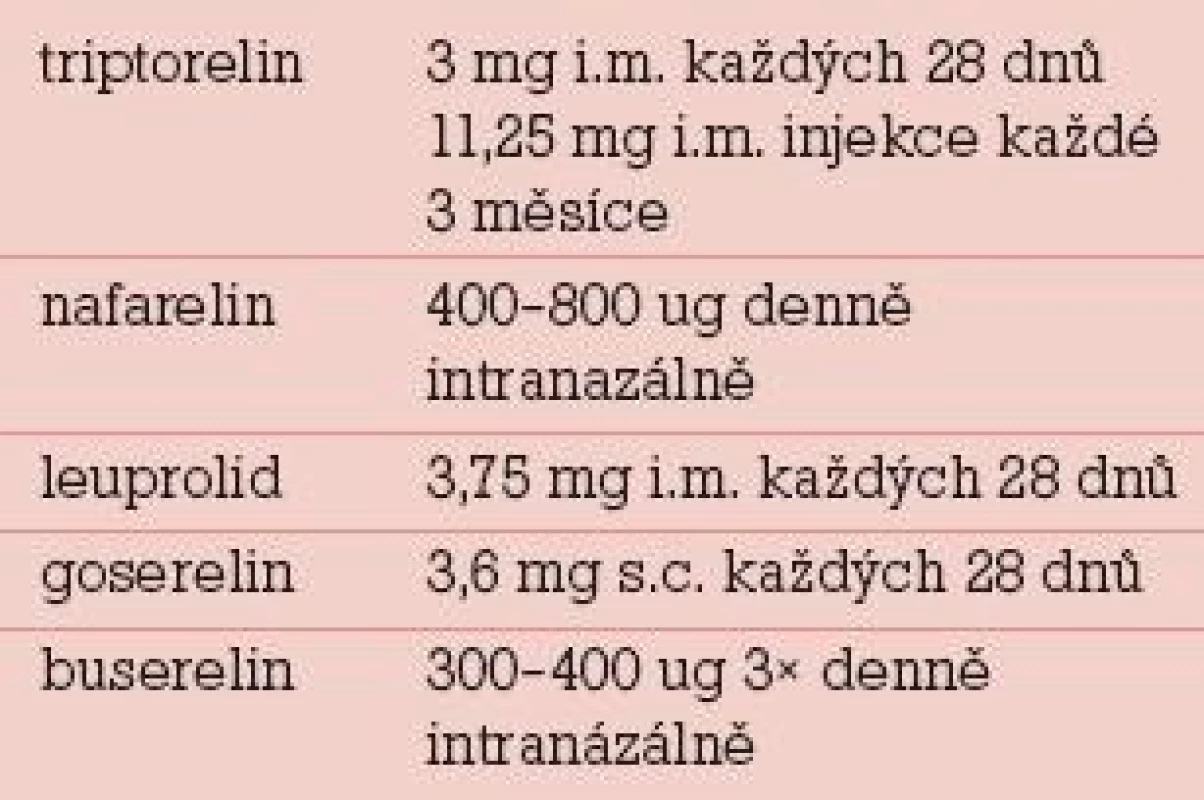
1. Schéma aplikace GnRH analog a folikulostimulačního hormonu v krátkém protokolu. 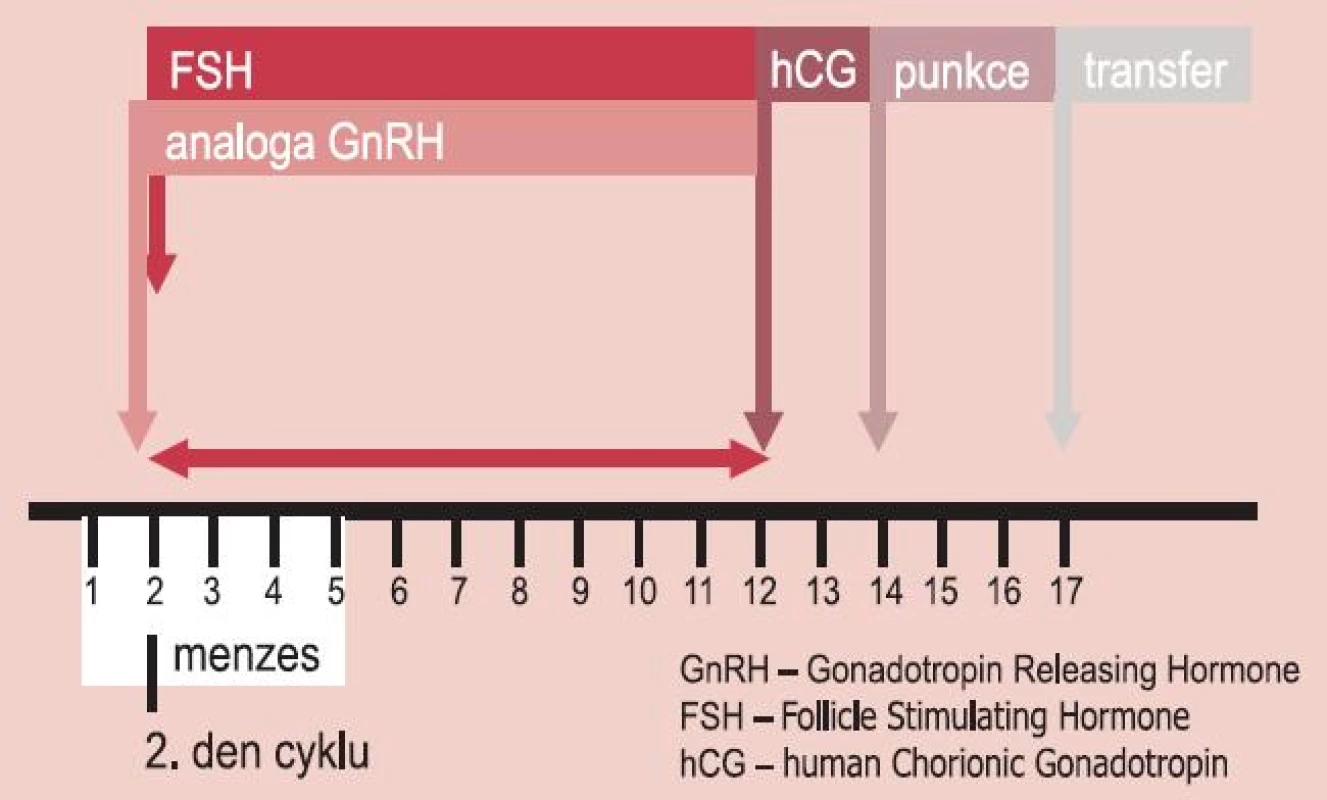
V dlouhém protokolu je aplikace GnRH agonistů zahájena v luteální fázi cyklu před podáváním FSH a pokračuje až do aplikace hCG před odběrem oocytů (obr. 2). V tomto protokolu je potlačení sekrece gonadotropinů delší. U žen s nižší ovariální rezervou bývá nižší odpověď vaječníků na stimulaci.
2. Schéma aplikace GnRH analog a folikulostimulačního hormonu v dlouhém protokolu. 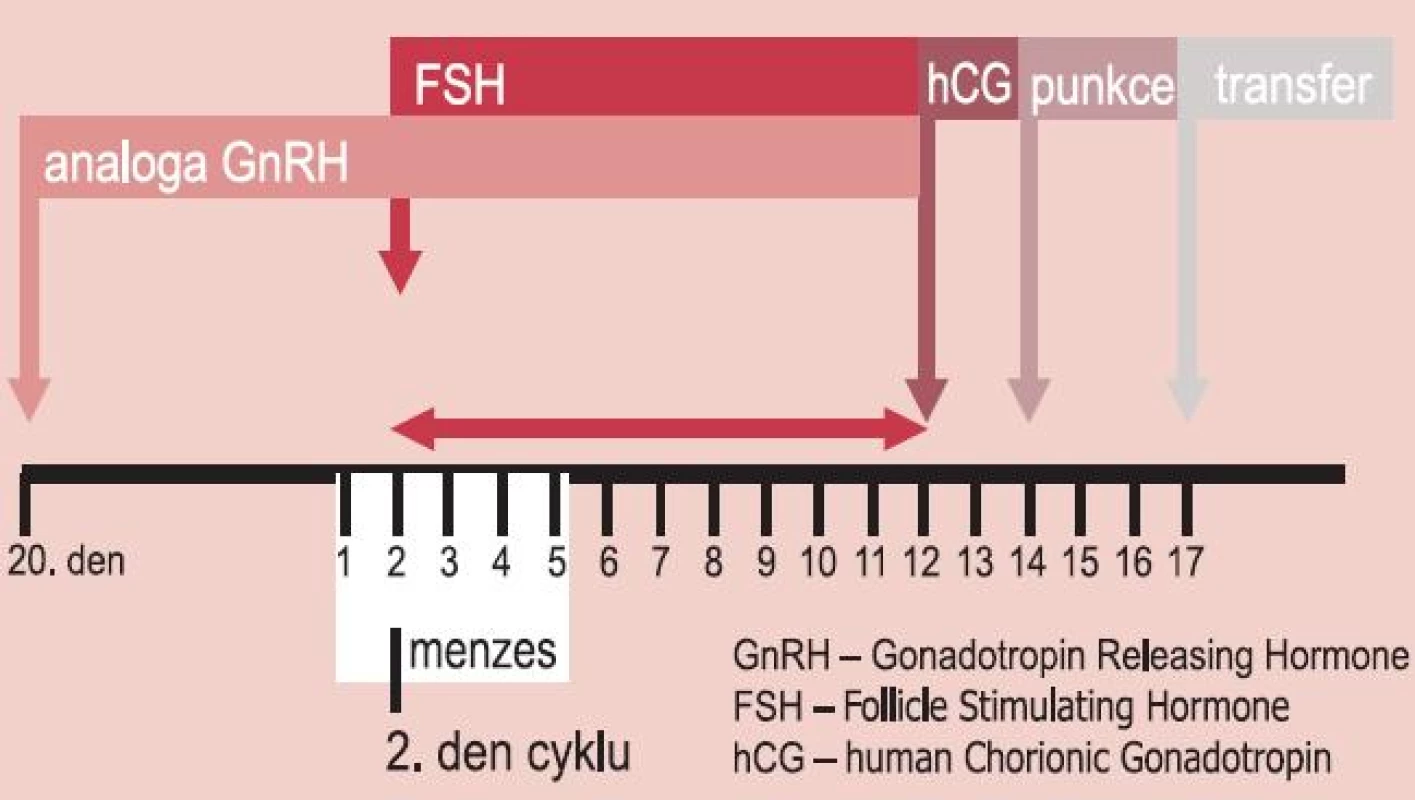
Paletu možných aplikačních protokolů snižujících riziko předčasného peaku LH rozšířily v roce 2001 GnRH antagonisté ganirelix a cetrorelix. Jsou podávány jako depotní forma většinou od 8. nebo 9. dne cyklu, případně po 24 hod od 6. dne cyklu nebo od nálezu folikulu s průměrem 14mm. K výhodám protokolů s antagonisty patří kratší délka stimulace, nižší dávka FSH a nižší riziko hyperstimulace [10]. V některých studiích bylo ale prokázáno mírné snížení počtu folikulů, oocytů a počtu těhotenství [11].
Indukce preovulačního peaku LH
V nestimulovaných cyklech je peak LH signálem pro ovulaci a obnovu meiotického dělení – maturaci oocytu. Pulzatilní sekrece LH také podporujerozvoj a správnou funkci žlutého tělíska. Nejčastějším a nejdostupnějším přípravkem, kterým LH nahrazujeme, je hCG.
Ve stimulačních protokolech s GnRHantagonisty je možné indukovat preovulační peak LH pomocí injekce GnRH analoga, která uvolní z hypofýzy potřebné množství LH. Tento postup může eliminovat podíl hCG na rozvoji ovariálního hyperstimulačního syndromu.
GnRH analoga v léčbě endometriózy
Poruchy plodnosti jsou kromě bolesti klasickým symptomem endometriózy. V souvislosti s rozvojem laparoskopie se zlepšil a usnadnil průkaz endometriálních lézí, epidemiologické studie prokázaly signifikantní souvislost mezi přítomností endometriózy a poruchou plodnosti. Významným krokem při získávání nových poznatků o endometrióze byl rozvoj technik asistované reprodukce. U žen s endometriózou podstupujících léčbu metodou in vitro fertilizace (IVF) byly prokázány horší výsledky než u fertilních žen bez endometriózy, včetně vyšších těhotenských ztrát a komplikací v průběhu gravidity [12].
Podezření na endometriózu vyplývá především z anamnestických údajů. Je třeba cíleně pátrat po symptomech endometriózy – bolestech, délce snahy o těhotenství, výskytu endometriózy v rodině. Při gynekologickém vyšetření mohou být patrná ložiska endometriózy na čípku (tzv. blepsy), při postižení zadních vazů zjišťujeme jejich citlivost a nodulární ztluštění. Pro adenomyózu je typické zvětšení a bolestivost dělohy, při endometriomech býváhmatná rezistence v oblasti adnex. Ultrazvukové vyšetření prokazuje především endometriomy, které mají charakteristickou jemně anisoechogenní strukturu. Pro vyšetření extraperitoneálních a hlubokých ložisek endometriózy bývá využívána magnetická nukleární rezonance. Z laboratorních vyšetření bývají zvýšeny hladiny tumor markeru CA-125, což je antigen exprimovaný na povrchu buněk derivovaných z coelomového epitelu. Novou perspektivu představuje vyšetření senzitivních nervových vláken v endometriu. V publikované studii predikovala kombinovaná analýza neurálníchmarkerů PGP, VIP a SP přítomnost minimální a mírné endometriózy s 95% senzitivitou, 100% specifitou a 97,5% přesností [13].
Pro stanovení diagnózy je nutná vizualizace endometriálních lézí, případně biopsie a histologické vyšetření (obr. 3). Laparoskopie je tak standardem diagnostiky endometriózy.
3. Typické ložisko endometriózy v oblasti zadního vazu děložního. 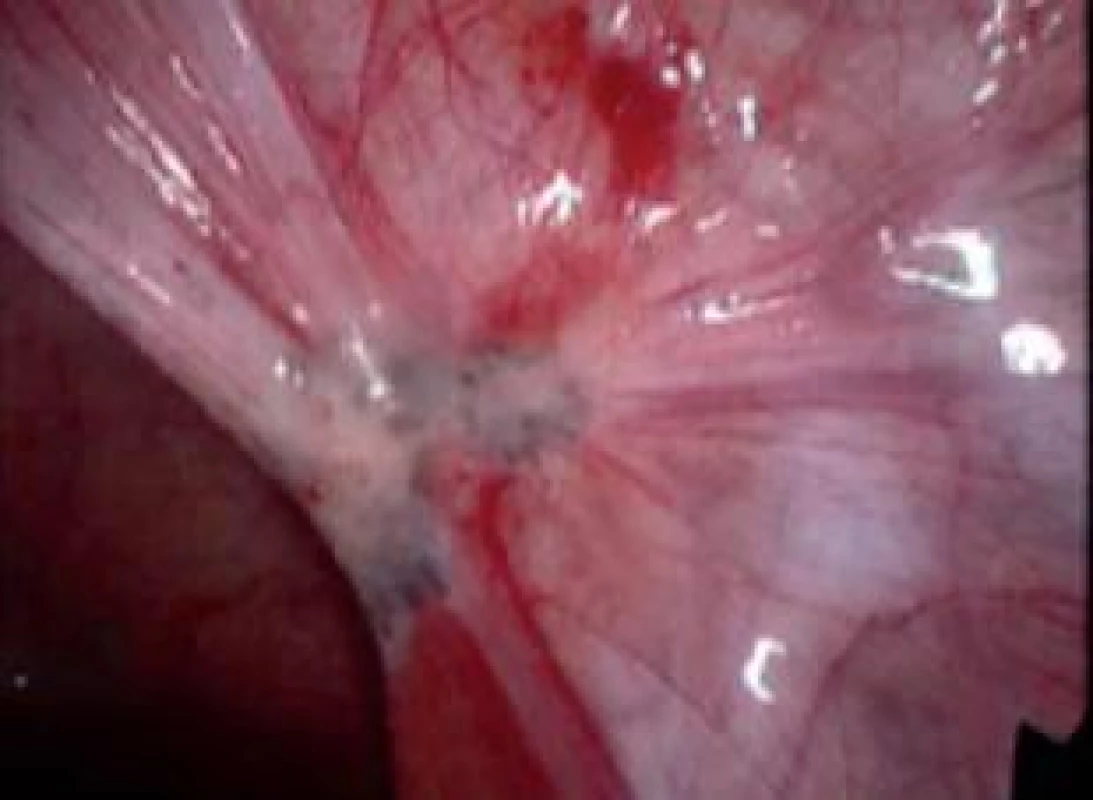
V souvislosti s poruchou plodnosti je nutné v kontextu s výsledky ostatních vyšetření a s ohledem na další známé příčiny neplodnosti stanovit racionální postup léčby. Využívá se chirurgická a medikamentózní léčba endometriózy a metody asistované reprodukce.
Základním principem hormonální léčby je blokáda produkce ovariálních estrogenů s následnou atrofií endometriálního ložiska. Odpověď na terapii závisí na přítomnosti steroidních receptorů, vaskularizaci léze a její velikosti. V současné době jsou pro blokádu funkce ovarií a navození hypoestrinního stavu nejčastěji používány GnRH agonisté. Jejich zavedení otevřelo novou cestu v léčbě endometriózy. Přehled látek používaných pro medikamentózní léčbu endometriózy a jejich aplikace je uveden v tab. 1. Indikací blokády ovarií je rozsáhlá endometrióza, okluze vejcovodů způsobená endometriózou, endometriální cysty (v kombinaci s chirurgickou léčbou), neúspěch IVF či algické symptomy endometriózy.
Některá ložiska endometriózy mohou být na hormonální léčbu rezistentní. Na rezistenci endometriózy na medikamentózní léčbu se podílí především autonomní produkce estradiolu, která je dána zvýšenou expresí a aktivitou aromatázy v ektopicky uloženém endometriu [14]. Při selhání léčby GnRH analogy může být účinná léčba inhibitory aromatázy – např. anastrozol a letrozol.
Podle současných doporučení ESHRE [15] není samotná hormonální blokáda ovarií v případech minimální a mírné endometriózy signifikantně účinná pro dosažení těhotenství [16]. Vzhledem k tomu, že při této léčbě dochází prokazatelně k ústupu endometriózy, zlepšení bolesti a zprůchodnění vejcovodu okludovaného endometriální lézí, je otázkou, proč by nemělo dojít také ke zlepšení plodnosti. Jedním z vysvětlení může být skutečnost, že při velkém počtu a proměnlivosti faktorů ovlivňujících plodnost je velmi obtížné efekt léčby přesně a spolehlivě změřit a statisticky analyzovat. Využití této léčebné modality v souvislosti s infertilitou tak vyžaduje zodpovědné posouzení všech okolností – možných faktorů neplodnosti, rozsahu a algických projevů endometriózy, výsledků asistované reprodukce a rizika vedlejších účinků. Kombinaci chirurgického výkonu a hormonální blokády volíme v případech rozsáhlé aktivní endometriózy nebo endometriálních cyst. Samotná hormonální terapie nevede k odstranění endometriomů.
Léčba závažnějších případů endometriózy vyžaduje dostatek zkušeností, odpovídající technické zázemí a možnost mezioborové spolupráce. V České republice byla vytvořena síť center pro léčbu endometriózy, která jsou schopna zajistit adekvátní diagnostiku a terapii nejzávažnějších případů tohoto onemocnění (obr. 4).
4. Přehled Center pro léčbu endometriózy v České republice. 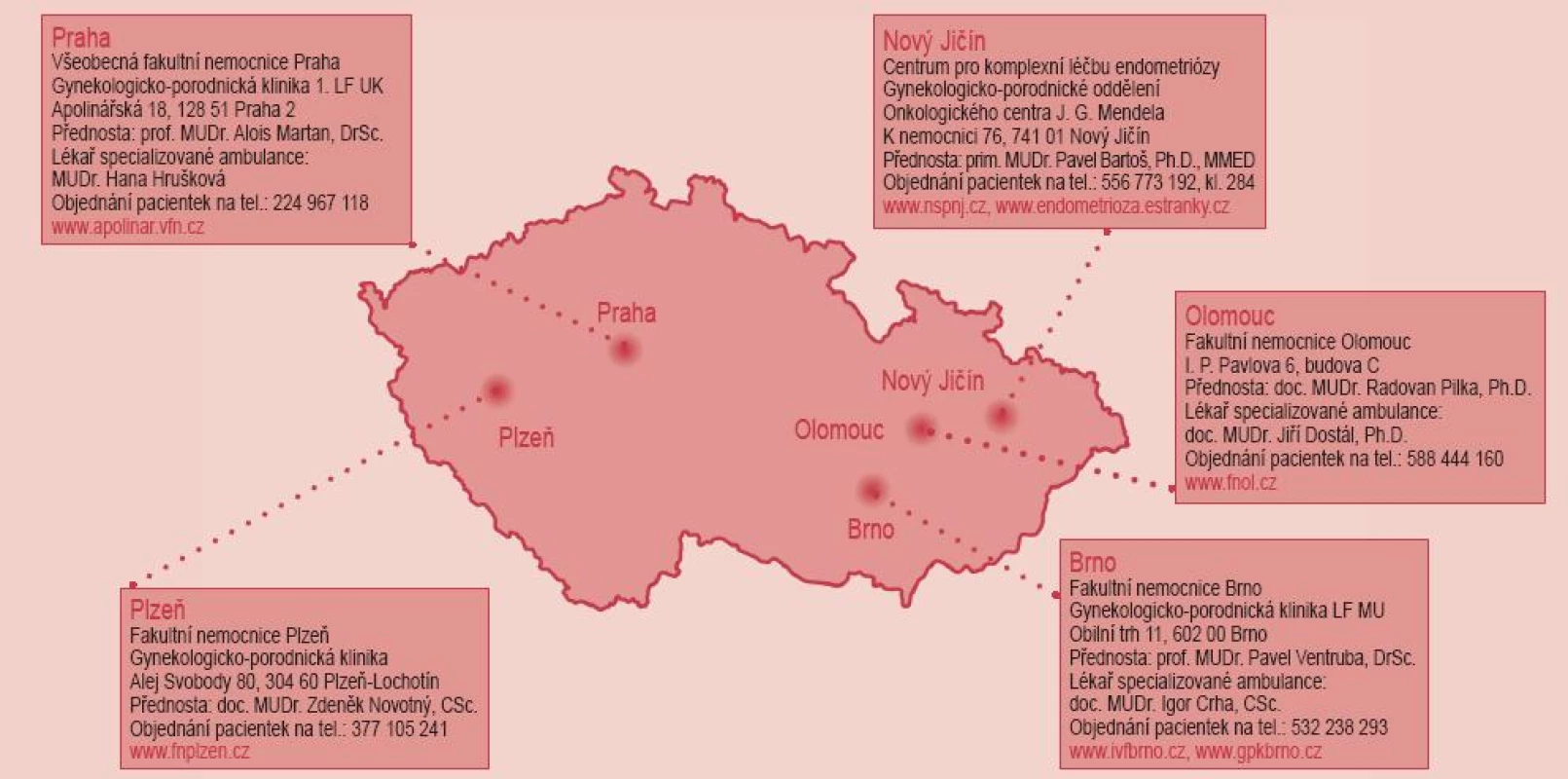
GnRH analoga v léčbě děložních myomů
Myom je mezenchymový nádor vznikající proliferací hladké svaloviny a vaziva. Je nejčastější nádorem děložního těla, který lze diagnostikovat u 30–50 % žen ve věku mezi 30 a 50 lety [17]. Jde o hormonálně závislý nádor, v jehož tkáních lze prokázat estrogenní i progesteronové receptory. Bez hormonální stimulace (v menopauze nebo po léčbě GnRH analogy) myomy většinou regredují.
V současné době v souvislosti se změnami životního stylu (např. těhotenství a porody ve vyšším věku) bývají děložní myomy mnohem častěji diagnostikovány u žen gravidních nebo graviditu plánujících. Také metody asistované reprodukce dnes umožňují otěhotnět ženám podstatně starším než v minulosti, což přináší častější výskyt myomů u koncepci plánujících a těhotných žen. Proto je velmi důležité racionálně posoudit možnosti léčby, její přínos a rizika. V posledních letech se touto problematikou zabývala řada prací. Věnovaly se novým poznatkům jak z oblasti základního výzkumu (molekulární genetika, etiopatogeneze), tak z oblasti klinické (nové možnosti konzervativní i operační léčby, vztah myomů k poruchám plodnosti) [17].
Aplikace GnRH analog představuje velmi účinnou modalitu v terapii děložních myomů. GnRH analoga navozují reverzibilní hypoestrinní stav, který vede ke zmenšení objemu myomu i celé dělohy (v průměru o 35–65 % v průběhu prvních tří měsíců léčby). Tento efekt je časově limitován, po vysazení léčby a obnovení ovariální sekrece estrogenů se myomy opět zvětšují. Proto se většinou kombinuje aplikace GnRH analog s chirurgickým výkonem. Tento postup má řadu výhod – – především zlepšení anatomických podmínek pro odstranění myomů a menší prokrvení dělohy, což snižuje invazivitu výkonu. Podrobný přehled vlivu děložní myomatózy na reprodukční funkce a možnosti léčby byl prezentován nedávno [18].
Ochrana ovarií v průběhu gonadotoxické léčby
Chemoterapie používaná v léčbě zhoubných onemocnění působí zejména na pravidelně a rychle se množící buňky, mezi něž řadíme i zárodečné buňky vaječníků. Působením depotních GnRH analog je možné reverzibilně blokovat folikulární aktivitu a navodit klidový stav ovarií. Bylo prokázáno, že zárodečné buňky ve vaječnících ovlivněných těmito léky jsou méně citlivé na chemoterapii.
Aplikace GnRH analog v průběhu chemoterapie statisticky signifikantně snížila riziko předčasného ovariálního selhání (POS) u žen léčených pro Hodgkinův lymfom. Při celkovém srovnání bylo ve skupině žen s aplikací GnRH analog během chemoterapie prokázáno statisticky signifikantně méně případů POS než v kontrolním souboru v obou sledovaných obdobích 6 a 12 měsíců po ukončení chemoterapie. Při analýze rizika vzniku POS v závislosti na cytotoxicitě použitého režimu chemoterapie byly statisticky signifikantní výsledky lepší u méně agresivních léčebných protokolů. Studie tedy prokázaly malý ochranný vliv aplikace GnRH-a na funkci ovarií při nutnosti použití vysokodávkovaných a kombinovaných chemoterapeutických režimů v pokročilých stadiích onkologického onemocnění. Proto se v těchto případech doporučuje tuto metodu kombinovat s jinou formou ochranné léčby [7,19].
Dalším příznivým účinkem aplikace GnRH analog během chemoterapie je výrazná redukce intenzity a četnosti menstruačního krvácení či nepravidelného krvácení z rodidel u často pancytopenických žen s nutností podání substituce erytrocytů či dalších krevních derivátů. Takto vzniklá významná ekonomická úspora při léčbě krevními deriváty byla několikanásobně vyšší než vynaložené náklady na podpůrnou léčbu GnRH analogy. Jejich bezpečnost byla opakovaně prokázána. Další výhodou tohoto postupu je možnost kombinace s ostatními metodami ovariální ochrany – zejména laparoskopickým odběrem ovariální tkáně [19]. Je nutné si uvědomit, že suprese ovariální funkce pomocí GnRH analog nastupuje až po 7–10 dnech po jejichaplikaci. Během této krátké doby dochází naopak v důsledku „flare-up“ fenoménu k aktivaci folikulogeneze, a tudíž ke zvýšení senzitivity ovaria k cytotoxickému účinku chemoterapie. Aplikaci GnRH analog je nutno zahájit dostatečně brzy, nejlépe asi 10 dnů před začátkem chemoterapie. K potlačení nežádoucího „flare-up“ fenoménu po aplikaci GnRH-analoga je možné využít také semi-depotních antagonistů GnRH. Plánování a časování podpůrné léčby GnRH analogy ve spolupráci s onkologem je tedy velmi důležité již od prvního dne diagnózy nádorového onemocnění.
Závěr
GnRH analoga představují racionální a účinnou léčbu poruch plodnosti.
Podpořeno Grantem IGA MZ ČR NS/9661-4.
Doručeno do redakce: 22. 7. 2011
Přijato po recenzi: 2. 8. 2011
doc. MUDr. Igor Crha, CSc.
Gynekologicko-porodnická klinika, LF MU a FN Brno
icrha@fnbrno.cz
Sources
1. Ascheim S, Zondek B. Hypophysenvorderlappenhormone und ovarialhormon im Harn von Schwangeren. Kim Wochenschr 1927; 6 : 1322.
2. Schally AV. Luteinizing hormone-releasing hormone analogs: their impact on the control of tumorigenesis. Peptides 1999; 20(10): 1247–1262.
3. Conn PM, Crowley WF Jr. Gonadotropin-releasing hormone and its analogs. Annu Rev Med 1994; 45 : 391–405.
4. Leyendecker G, Wildt L, Hansmann M. Pregnacies following chronic intermittent (pulsatile) administration of Gn-RH by means of a portable pump (“Zyklomat”) – a new approach to the treatment of infertility in hypothalamic amenorrhoea. J Clin Endocrinol Metab 1980; 51(5): 1214–1216.
5. Porter RN, Smith W, Craft IL et al. Induction of ovulation for in-vitro fertilisation using buserelin and gonadotropins. Lancet 1984; 2(8414): 1284–1285.
6. Smitz J, Devroey P, Camus M et al. The luteal phase and early pregnancy after combined GnRH-agonist/HMG treatment for superovulation in IVF or GIFT. Hum Reprod 1988; 3(5): 585–590.
7. Huser M, Crha I, Ventruba P et al. Prevention of ovarian function damage by a GnRH analogues during chemotherapy in Hodgkin lymphoma patients. Hum Reprod 2008; 23(4): 863–868.
8. Stanger JD, Yovich JL. Reduced in-vitro fertilization of human oocytes from patients with raised basal luteinizing hormone levels during the follicular phase. Br J Obstet Gynaecol 1985; 92(4): 385–393.
9. Albuquerque LE, Saconato H, Maciel MC. Depot versus daily administration of gonadotrophin releasing hormone agonist protocols for pituitary desensitization in assisted reproduction cycles. Cochrane Database Syst Rev 2005; 1: CD002808.
10. Tarlatzis BC, Kolibianakis EM. GnRH agonists vs antagonists. Best Pract Res Clin Obstet Gynaecol 2007; 21(1): 57–65.
11. Al-Inany H, Aboulghar M. GnRH antagonist in assisted reproduction: a Cochrane review. Hum Reprod 2002; 17(4): 874–885.
12. Crha I, Juránková E. Poruchy plodnosti podmíněné endometriózou. Gynekol Prax 2006; 4 : 203–208.
13. Bokor A, Kyama CM, Vercruysse L et al. Density of small diameter sensory nerve fibres in endometrium: a semi-invasive diagnostic test for minimal to mild endometriosis. Hum Reprod 2009; 24(12): 3025–3032.
14. Bulun SE, Zeitoun KM, Takayama K et al. Molecular basis for treating endometriosis with aromatase inhibitors. Hum Reprod Update 2000; 6(5): 413–418.
15. Kennedy S, Berqqvist A, Chapron C et al. ESHRE guideline for the diagnosis and treatment of endometriosis. Hum Reprod 2005; 20(10): 2698–2704.
16. Hughes E, Fedorkow D, Collins J et al. Ovulation suppression for endometriosis. Cochrane Database Syst Rev 2003; 3: CD000155.
17. Mára M, Holub Z et al. Děložní myomy – moderní diagnosti a léčba. Praha: Grada 2009.
18. Krajčovičová R, Hudeček R. Vliv děložní myomatózy na reprodukční funkce. Prakt Gyn 2010; 14(4): 154–163.
19. Huser M, Crha I, Hudecek R et al. Ovarian tissue cryopreservation - new opportunity to preserve fertility in female cancer patients. Eur J Gynaecol Oncol 2007; 28(4): 249–256.
Labels
Paediatric gynaecology Gynaecology and obstetrics Reproduction medicine
Article was published inPractical Gynecology

2011 Issue 3-4-
All articles in this issue
- Genetic prediction of osteoporosis in clinical practice
- Prevention of postpartum hemorrhage in caesarean section with carbetocin
- Applications of GnRH analogues in infertility treatment
- Targeted – biological treatment of ovarian cancer
- Sperm analysis by fluorescence in situ hybridization
- Preventing hereditary risk of breast and ovarian cancer
- Sayana – the new face of the traditional depot medroxyprogesterone acetate
- Caesarean section – with what anaesthesia?
- Management of recurrent ovarian cancer
- Spontaneous abortions in Slovakia from 1997 to 2009
- The reasons for severe ovarian hyperstimulation syndrome in patients requiring hospitalisation
- Surgical techniques and legislative framework for female sterilization in the Czech Republic
- Cornual pregnancy carried to full term
- Prolapsus uteri at vaginae totalis with Mayer’s pessary
- 13th World Congress on Menopause
- Aromatase inhibitors in breast cancer: review and possible benefits in premenopausal women
- Practical Gynecology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Prolapsus uteri at vaginae totalis with Mayer’s pessary
- Applications of GnRH analogues in infertility treatment
- Cornual pregnancy carried to full term
- The reasons for severe ovarian hyperstimulation syndrome in patients requiring hospitalisation
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

