-
Medical journals
- Career
Laparoskopická sutura perforovaného peptického vředu – rutina, nebo cílený výběr pacientů?
Authors: L. Tulinský 1,2; M. Mitták 1,2; J. Hrubovčák 1,2; M. Kepičová 1,2; P. Ihnát 1,2; L. Martínek 1,2
Authors‘ workplace: Chirurgická klinika Fakultní nemocnice Ostrava 1; Katedra chirurgických studií, Lékařská fakulta, Ostravská univerzita 2
Published in: Rozhl. Chir., 2022, roč. 101, č. 7, s. 326-331.
Category: Original articles
doi: https://doi.org/10.33699/PIS.2022.101.7.326–331Overview
Úvod: Vředová choroba gastroduodena patří mezi nejčastěji se vyskytující onemocnění proximální části zažívacího traktu. Její komplikace jsou relativně časté, nejvážnější je perforace peptického vředu s roční incidencí asi 10 případů na 100 tisíc obyvatel a mortalitou 10–40 %. Jedinou možností léčby je chirurgická sutura perforace, kterou lze provést laparoskopickým přístupem nebo otevřeně. Cílem studie bylo porovnat krátkodobé výsledky laparoskopické a otevřené sutury akutní perforace peptického vředu a zhodnotit přesnost skórovacího systému dle Boeya ke stanovení rizikovosti pacientů v české populaci.
Metody: Retrospektivní studie provedená na chirurgické klinice Fakultní nemocnice Ostrava. Pacienti podstoupili akutní laparoskopickou nebo otevřenou suturu perforovaného peptického vředu v letech 2017–2021.
Výsledky: Do studie bylo zařazeno 60 pacientů. Laparoskopicky byl výkon proveden u 43,3 % pacientů, laparotomicky u 56,7 %. Průměrná pooperační morbidita byla 70,0 %. Mírné komplikace byly zaznamenány u 23,3 % pacientů, závažné u 16,7 % pacientů. Pacienti po laparoskopické sutuře vykazovali vyšší výskyt mírných i závažných komplikací (26,9 % vs. 20,6 % a 19,2 % vs. 14,7 %), ale i vyšší výskyt nekomplikovaného pooperačního průběhu. Celková pooperační mortalita byla 30,0 % (laparoskopie 15,4 %, laparotomie 41,2 %). Výsledky studie potvrdily odhadované vstupní riziko úmrtí stanovené dle Boeyova skóre.
Závěr: Laparoskopická sutura vředu může být metodou volby u pacientů bez nebo s nízkými rizikovými faktory. Laparoskopicky operovaní pacienti vykazovali vyšší výskyt lehkých i závažných komplikací. Vyšší mortalita pacientů po otevřené sutuře souvisí s jejich horším počátečním klinickým stavem. Předoperační stanovení rizika mortality pomoci Boeyova skóre je přesné a ke zvolení operačního přístupu výhodné.
Klíčová slova:
mortalita – perforovaný peptický vřed – laparoskopická sutura – laparotomická sutura – Boey skóre
ÚVOD
Vředová choroba gastroduodena (VCHGD) patří mezi nejčastěji se vyskytující onemocnění proximální části zažívacího traktu. Celosvětový výskyt nekomplikovaného peptického vředu je asi 90 případů na 100 000 obyvatel za rok [1]. V České republice je roční incidence s celosvětovým průměrem identická. Prevalence VCHGD v populaci je asi 5 % [2]. Komplikace jsou relativně časté. Ke krvácení z vředu dochází asi v 50 % případů VCHGD, k perforaci v 10 %. Celosvětová průměrná roční incidence akutní perforace peptického vředu (PPV), včetně České republiky, je tedy asi 9–10 případů na 100 000 obyvatel [1]. Hlavní rizikovou skupinou jsou ženy nad 60 let. Všeobecně známými rizikovými faktory jsou kouření, etylismus a užívání NSAID [3].
Mortalita PPV se pohybuje kolem 10–40 % [4,5], výrazně se však liší zejména v závislosti na věku a stavu pacienta před přijetím do nemocnice. Všeobecnou rizikovost pacienta lze klasifikovat podle mnoha obecných skórovacích systémů (např. ASA, APACHE II atp.). Vhodněji můžeme použít klasifikační systémy cílené pro pacienty s PPV: Boeyovo, Hacettepovo, Jabalpurovo skóre nebo peptic ulcer perforation score (PULP) [6]. V současnosti je pro nejpřesnější a nejjednodušší stanovení rizika pooperační mortality a morbidity u pacientů s akutní PPV považován skórovací systém dle Boeya [7,8].
Jedinou možností léčby PPV je chirurgická sutura perforace, kterou lze provést laparoskopickým přístupem nebo otevřeně. Volba operačního přístupu se liší v závislosti na předoperačním klinickém stavu pacienta a preferencích operatéra. V poslední době pozorujeme vzrůstající tendenci používat i v této akutní indikaci miniinvazivní přístup.
Cílem předkládané studie bylo porovnat krátkodobé výsledky laparoskopické (LS) a otevřené sutury (OS) akutní perforace peptického vředu a zhodnotit přesnost skórovacího systému dle Boeya ke stanovení rizikovosti pacientů v české populaci.
METODY
Jednalo se o retrospektivní studii, do které bylo zařazeno 60 pacientů chirurgické kliniky Fakultní nemocnice Ostrava. Pacienti podstoupili akutní laparoskopickou nebo otevřenou suturu perforovaného peptického vředu v letech 2017–2021. Z analýzy byli vyloučeni pacienti operovaní elektivně a pacienti s neúplnými údaji v nemocničním informačním systému.
Operační postup
Všem pacientům byla před výkonem podána antibiotická profylaxe dle doporučených postupů, po výkonu bylo v antibiotické terapii pokračováno terapeuticky. Bez ohledu na operační přístup bylo místo perforace suturováno vždy jednotlivými vstřebatelnými stehy. Po dokončení sutury byla provedena omentoplastika a následná kompletní břišní laváž ředěným jodovým roztokem s následnou drenáží silikonovým drénem. Laparoskopická revize byla provedena vždy ze tří vstupů (v supraumbilikální oblasti a obou mezo - až hypogastriích), otevřená revize cestou horní střední laparotomie. Všem pacientům byla poskytnuta standardní perioperační péče.
Sběr dat
Demografické a klinické údaje všech pacientů ve studii (věk, pohlaví, BMI, ASA klasifikace, lokalizace vředu), typ operace, operační revize a pooperační morbidita byly extrahovány z elektronické zdravotní dokumentace. Předoperační klinický stav pacientů byl hodnocen podle Boeyova skóre (Tab. 1). Jako trvání perforace byla definována doba mezi nástupem bolesti nebo akutní exacerbací chronické bolesti a přijetím do nemocnice. Jako předoperační šok byl považován vstupní systolický krevní tlak <100 mmHg. Mezi závažné komorbidity bylo řazeno systémové onemocnění srdce, plic, jater nebo ledvin, malignita a diabetes mellitus [7]. Pooperační komplikace byly hodnoceny podle Clavien-Dindo klasifikace [9]. Jako mírné byly označeny komplikace 1. a 2. stupně, jako závažné komplikace 3. a 4. stupně. Komplikace 5. stupně odpovídaly mortalitě.
Table 1. Boeyovo skóre
Tab. 1: Boey score
Statistická analýza
Získaná data byla analyzována pomocí metod deskriptivní statistiky. Pro statistický popis souboru byl použit průměr a směrodatná odchylka, pro kvantitativní hodnoty t-test, pro kategorické hodnoty Chí-kvadrát test. Jako statisticky významná byla považována hladina významnosti α=0,05 a hodnoty p<0,05.
VÝSLEDKY
Do studie bylo zařazeno 60 pacientů po sutuře perforovaného vředu. Laparoskopicky byl výkon proveden u 26 (43,3 %) pacientů, laparotomicky u 34 (56,7 %) pacientů. Základní demografické a klinické atributy studovaných pacientů jsou uvedeny v Tab. 2. Celkově se jednalo o 25 (41,7 %) žen a 35 (58,3 %) mužů; průměrný věk byl 65,8±14,8 roku (v rozmezí 32 až 93 let). Celkem 13 (21,7 %) pacientů bylo předoperačně charakterizováno jako ASA I–II, 28 (46,7 %) jako ASA III a 19 (31,7 %) jako pacienti s vysokým rizikem ASA IV–V; rozdíl v zastoupení skupin nebyl statisticky významný (p=0,148).,
Table 2. Demografická a klinická data pacientů ve studii
Tab. 2: Demographics and clinical data of study patients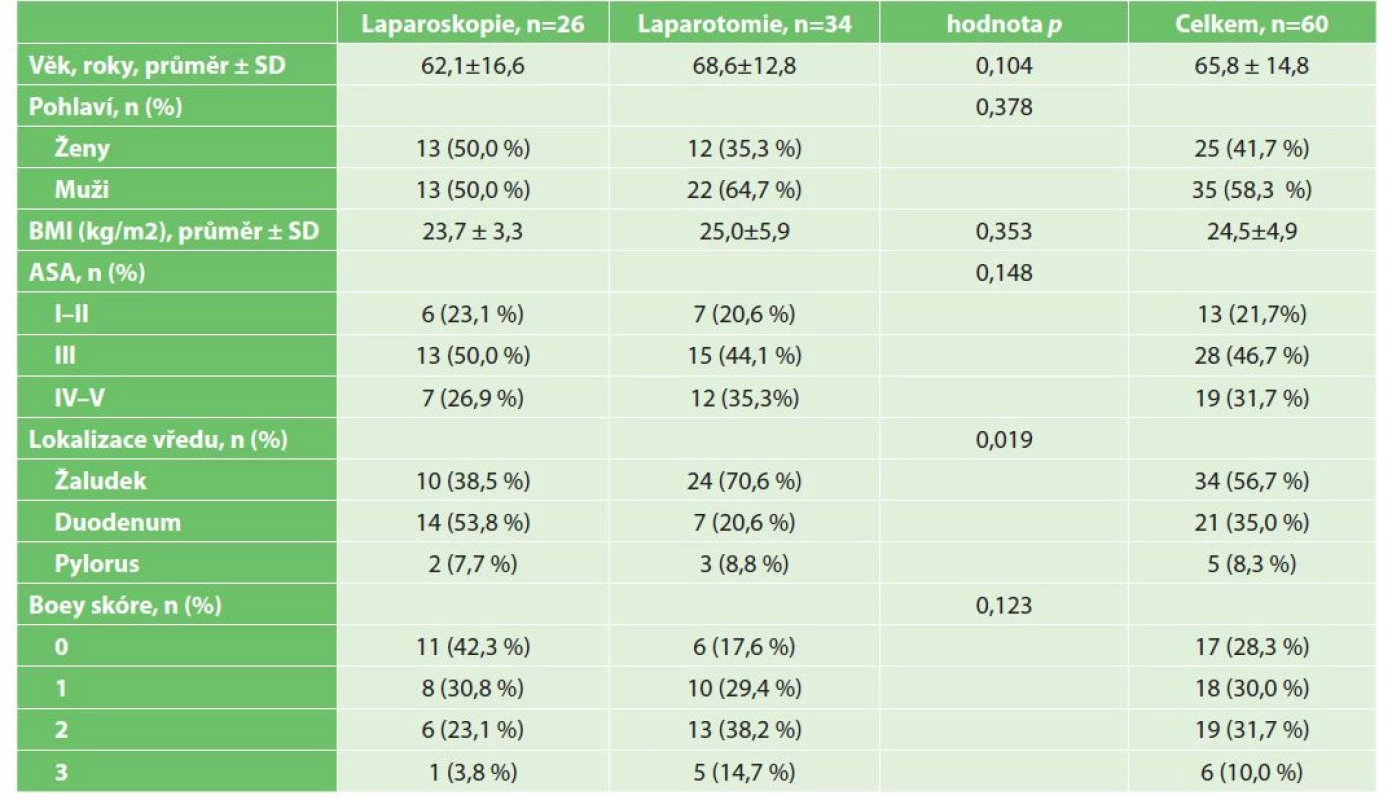
Žaludeční vřed byl nalezen u 34 (56,7 %) pacientů, duodenální u 21 (35,0 %) a vřed v pylorické oblasti u 5 (8,3 %) pacientů. Rozdíl v lokalizaci vředu mezi oběma studijními skupinami byl statisticky významný (p=0,019). Po přijetí do nemocnice mělo 17 (28,3 %) pacientů Boeyovo skóre 0, 18 (30,0 %) pacientů mělo skóre 1, 19 (31,7 %) skóre 2 a 6 (10,0 %) skóre 3. Ve skupině laparoskopických revizí mělo 11 (42,3 %) pacientů Boeyovo skóre 0, 8 (30,8 %) pacientů skóre 1, 6 (23,1 %) skóre 2 a pouze 1 (3,8 %) pacient měl skóre 3. Naopak ve skupině pacientů operovaných otevřenou technikou mělo 6 (17,6 %) pacientů Boeyovo skóre 0, 10 (29,4 %) pacientů skóre 1, 13 (38,2 %) skóre 2 a 5 (14,7 %) pacientů dokonce Boeyovo skóre 3. Rozdíl ve výchozím klinickém stavu pacientů mezi studovanými skupinami ale není statisticky významný (p=0,123).
Tab. 3 uvádí perioperační a krátkodobé pooperační výsledky pacientů. Celková průměrná délka operace byla 59,0±22,8 min. (rozsah 25–129 min., LS 58,2±19,9 min., OS 59,6±25,0 min.). Rozdíl mezi sledovanými skupinami nebyl statisticky významný (p=0,806). Průměrná doba hospitalizace byla 12,6±7,7 dne (rozmezí 3–35 dnů, LS 12,3±7,7 dne, OS 12,7±7,8 dne); rozdíl mezi skupinami studie nebyl statisticky významný (p=0,859).
Table 3. Perioperační a pooperační výsledky pacientů ve studii
Tab. 3: Intraoperative and postoperative outcomes of study patients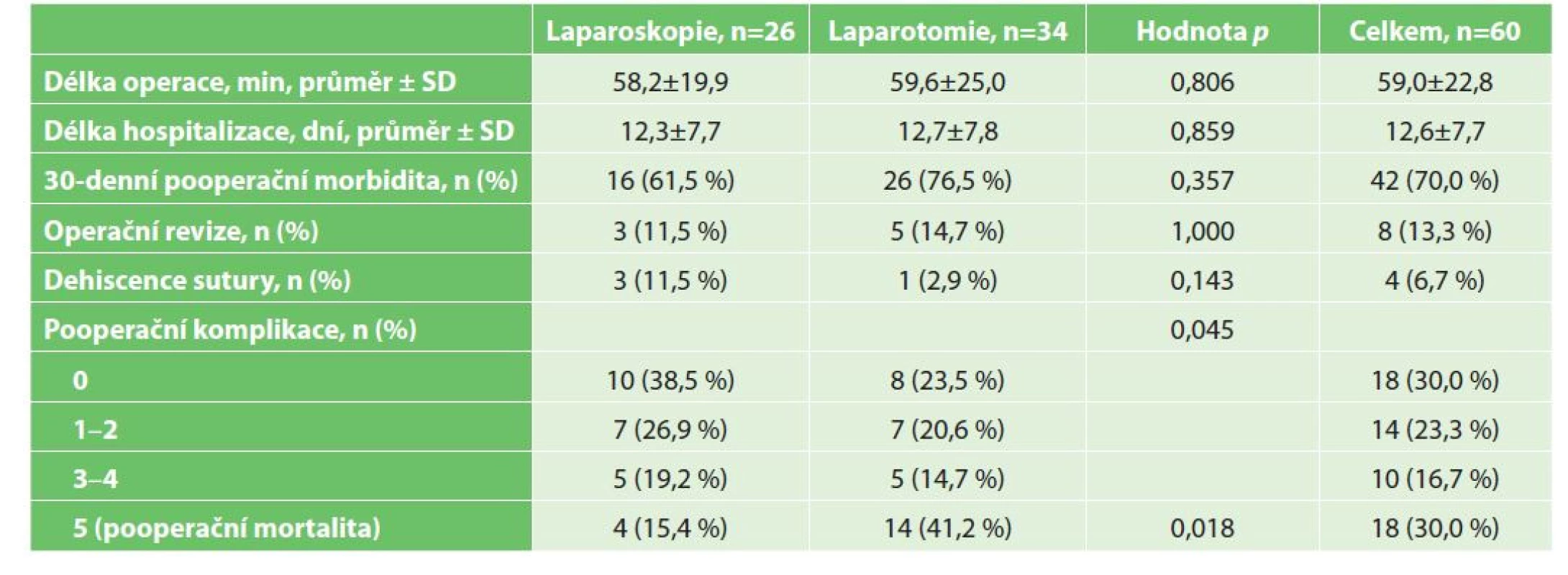
Průměrná 30denní pooperační morbidita byla 70,0 % (celkem 42 pacientů, LS 61,5 %, OS 76,5 %). Celkově byly komplikace mírného stupně (Clavien-Dindo 1–2) zaznamenány u 14 (23,3 %) pacientů, závažné komplikace (Clavien-Dindo 3–4) u 10 (16,7 %) pacientů. Pacienti po LS vykazovali oproti pacientům po OS vyšší výskyt mírných i závažných komplikací (26,9 % vs. 20,6 % a 19,2 % vs. 14,7 %), ale i vyšší procento nekomplikovaného pooperačního průběhu (38,5 % vs. 23,5 %). Rozdíl mezi těmito skupinami byl statisticky významný (p=0,045). Celková pooperační mortalita pacientů v naší studii byla 30,0 %. Mortalita pacientů operovaných laparoskopicky byla 15,4 % (4 pacienti), ve skupině pacientů operovaných otevřeně dosahovala 41,2 % (14 pacientů). Rozdíl v mortalitě u obou skupin byl statisticky významný (p=0,018).
Chirurgickou revizi bylo nutno provést celkem u 8 (13,3 %) pacientů. Po LS se revidovali 3 (11,5 %) pacienti, po OS 5 (14,7 %) pacientů. Důvodem revize byla u 4 (6,7 %) pacientů dehiscence sutury místa perforace vředu. U LS bylo toto u všech 3 (11,5 %) revidovaných pacientů, u OS se pro dehiscenci revidoval jen 1 (2,9 %) pacient. Rozdíl mezi počtem revizí a dehiscencí není mezi oběma skupinami statisticky významný (p=1,000 a p=0,143).
Detailní rozložení komplikací stratifikovaných podle vstupního rizika pacientů (podle Boeyova skóre) ukazuje Tab. 4. Ve skupině pacientů s rizikem Boey 0 nemělo žádné komplikace 11 (64,7 %) pacientů, komplikace mělo 5 (29,4 %) pacientů (4 mírné, 1 závažná). Ve skupině pacientů Boey 1 neměli komplikace 4 (22,2 %) pacienti, komplikace postihly 11 (61,1 %) pacientů (6 mírných, 5 závažných). Ve skupině Boey 2 neměli komplikace 3 (15,8 %) pacienti, komplikace mělo 7 (36,9 %) pacientů (4 mírné, 3 závažné). Ve skupině Boey 3 nebyl žádný pacient bez komplikací. Jeden pacient měl závažnou komplikaci, zbytek pacientů ve skupině v pooperačním období umřelo (5 pacientů, 83,3 %). Mortalita stoupala dle skupin rizikovosti pacientů (Boey 0 – 5,9 %, Boey 1 – 16,6 %, Boey 2 – 47,4 % a Boey 3 – 83,3 %). Vzhledem k malé citlivosti statistických testů při n<5 nebyla významnost těchto rozdílů statisticky měřitelná.
Table 4. Rozložení komplikací podle vstupního rizika pacientů (Boeyova skoré)
Tab. 4: Distribution of complications according to patients‘ initial risk (Boey score)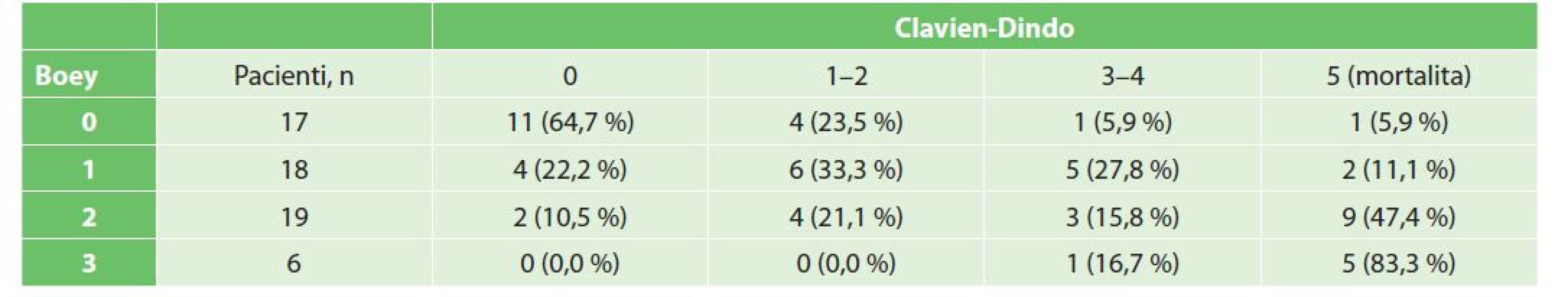
Celková pooperační mortalita pacientů v naší studii byla 30,0 %. Mortalita pacientů operovaných laparoskopicky byla 15,4 % (4 pacienti), ve skupině pacientů operovaných otevřeně dosahovala 41,2 % (14 pacientů) (Tab. 3). Tabulka 5 ukazuje detailní rozložení mortality podle vstupního rizika pacientů a operačního přístupu. Ve skupině pacientů operovaných laparoskopicky bylo 11 pacientů s Boey skóre 0, žádný z těchto pacientů neumřel. Ze 7 pacientů Boey 1 umřeli 2 (28,6 %) pacienti, ze 6 pacientů Boey 2 umřel 1 (16,7 %) pacient. Jeden pacient umřel i ve skupině Boey 3, kde byl v této kategorii sám a vytvořil tak úmrtnost 100 %. Ve skupině pacientů operovaných otevřeným přístupem bylo 6 pacientů s Boey skóre 0, z těchto pacientů 1 (16,7 %) umřel. Z 10 pacientů Boey 1 umřel 1 (10,0 %), z 13 pacientů Boey 2 umřelo 8 (61,5 %) pacientů a z 5 pacientů Boey 3 umřeli 4 (80,0 %) pacienti. Rozdíl v mortalitě u obou skupin byl statisticky významný (p=0,018).
Table 5. Mortalita podle vstupního rizika pacientů (Boeyova skoré) a operačního přístupu
Tab. 5: Mortality according to patients‘ initial risk (Boey score) and surgical approach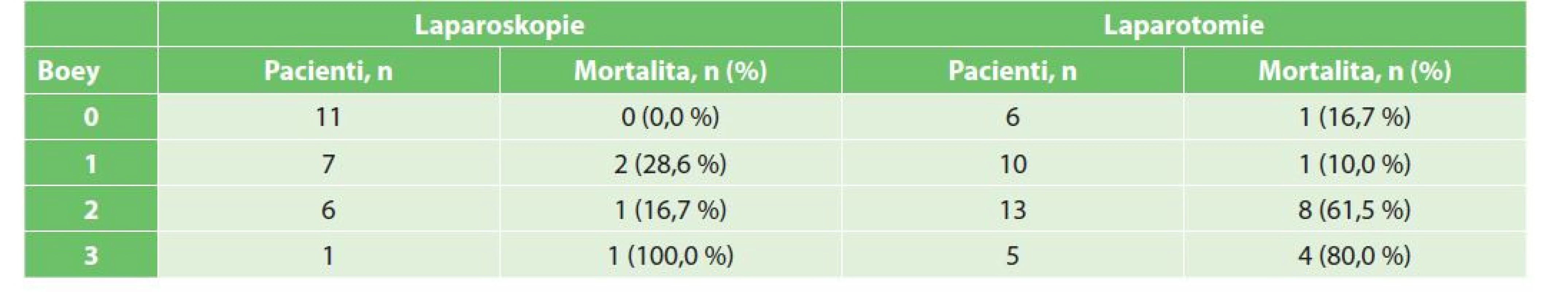
DISKUZE
Jedinou adekvátní léčbou PPV je sutura místa perforace. V minulosti se tento výkon prováděl dominantně laparotomickým přístupem. S úspěšným zaváděním laparoskopie do elektivní operativy se vytvořil předpoklad užití miniinvazivity i v akutních indikacích. Laparoskopická sutura (LS) PPV byla poprvé popsána v roce 1990 [10], od té doby se poměr laparoskopických přístupů každým rokem zvyšuje. Wright a kol. [11] zaznamenali na souboru 5361 pacientů v letech 2007–2010 podíl laparoskopie pouze 2,6 %. Davenport a kol. [12] ve své studii na 4210 pacientech uvádějí nárůst četnosti LS ze 4,5 % v roce 2010 na 11,4 % v roce 2016. V České republice referovali Starý a kol. [13] již v roce 2008 podíl LS 31 % v jejich souboru 51 pacientů. Poslední světové studie uvádějí četnost laparoskopických operací u PPV 10–50 % [14,15,16,17]. Naše studie měla podíl laparoskopie 43 %, což je v souladu s těmito závěry a potvrzuje vzestup LS v akutních indikacích i v České republice.
LS v akutní terapii PPV byla v mnoha studiích potvrzena jako rovnocenná metoda. Pereira a kol. [15] a Quah a kol. [18] poukázali na to, že pokud jde o morbiditu, mortalitu, operační dobu a dobu hospitalizace, LS vykazuje podobné nebo lepší výsledky než sutura vředu provedená otevřeně. Naopak Varcus a kol. [19] v roce 2018 popsali, že riziko dehiscence LS vředu může být až třikrát vyšší. Tato zjištění jsme potvrdili i v naší studii, kdy míra dehiscence laparoskopicky provedené sutury byla třikrát vyšší než u jejího provedení otevřeně. Očekávanou stejnou úmrtnost obou skupin jsme naopak nepotvrdili. Mortalita ve skupině laparotomicky operovaných pacientů byla třikrát vyšší než ve skupině laparoskopické. Toto zjištění souvisí s rozdílnými vstupními charakteristikami naší studijní skupiny, jak je popsáno dále.
Pro objektivizaci počátečního klinického stavu pacientů bylo zvoleno Boeyovo skóre [8]. To je mnohými autory považováno za nejpřesnější a nejjednodušší systém pro stanovení rizika mortality u pacientů s akutní PPV [5,6,20,21]. Náš soubor pacientů ukázal, že k laparoskopii chirurgové indikovali převážně pacienty s nižším Boeyovým skóre (Boey 0–1). Rizikovější pacienty (Boey 2–3) ponechávali k otevřené revizi. Laparoskopicky operovaní pacienti tak měli v průměru menší vstupní riziko než pacienti operovaní otevřeně. To mělo za následek statisticky významný rozdíl v mortalitě mezi oběma skupinami, kde mortalita otevřené revize byla téměř třikrát vyšší než mortalita laparoskopického přístupu (p=0,018).
Boey a kol. už v roce 1987 určili čtyři úrovně rizika pacientů, u kterých se mortalita progresivně zvyšovala s vyšším stupněm klasifikace (Boey 0–3 : 0 %, 10 %, 45,5 % a 100 %). Boeyovo odhadované skóre bylo hodnoceno v řadě následných studií. Přesnost rizika úmrtí se pohybovala v rozmezí 85–95 % [2,3,4,5,6], což lze považovat za adekvátní přesnost systému. V české literatuře popisovali Boeyův systém jako přínosný Satinský a kol. [22] v roce 2012, kdy svou přehledovou práci podložili výsledky několika zahraničních autorů. Naše studie ukázala výsledky velice podobné výše uvedenému (mortalita ve skupinách Boey 0–3 : 6 %, 17 %, 47 % a 83 %) a potvrdila tak deklarovanou přesnost Boeyova skórovacího systému i v české populaci.
Jak je popsáno výše, z hlediska pooperační morbidity lze LS považovat za ekvivalent OS. Někteří autoři [23] však uvádějí, že suturu perforace nelze při laparoskopii dotáhnout tak kvalitně jako při otevřeném přístupu, což vede k vyššímu riziku následné dehiscence. Tuto domněnku vyvrátili Zhou a kol. [24] ve své studii v roce 2009 a později Wilhelmsen a kol. [25] v roce 2015. V našich skupinách není rozdíl mezi poměrem revizí a dehiscencí po laparoskopické a otevřené sutuře statisticky významný. U LS však byla dehiscence sutury téměř čtyřikrát častější než u OS. Na základě našich výsledků můžeme připustit, že dehiscence sutury vředu může být u LS mnohem častější.
Data z naší studie neobsahují informace o velikosti vředu. Mnoho studií popisuje, že větší vředy nejsou pro LS vhodné [26,27,28,29]. Neexistuje však žádný obecně uznávaný názor, který by definoval indikaci LS dle velikosti vředu. Lee a kol. [26] a Sue a kol. [27] uvedli, že velikost vředu >10 mm je nezávislým rizikovým faktorem, který předpovídá zvýšené riziko dehiscence laparoskopicky prováděné sutury. Bohužel kvůli nedostatečným informacím v našem souboru jsme tento parametr vyhodnotit nemohli.
Hlavním omezením studie je retrospektivní a nerandomizovaný design. Studie má však dostatečný počet pacientů a byla provedena na jediném pracovišti zkušenými chirurgy. U všech pacientů byly zachovány standardní chirurgické a pooperační postupy, které zaručovaly snížení rizika zkreslení výsledků.
Rozdíly ve věku pacientů, ASA klasifikaci a Boey skóre mezi studijními skupinami byly statisticky významné. Tato limitace souvisí s nerandomizovaným designem studie. Chirurgové volili operační přístup podle objektivního stavu pacienta. Starší pacienti, pacienti s vyšším ASA a Boey skóre jsou obecně rizikovější, proto v naší studii chirurgové volili přehlednější postup – otevřenou suturu.
ZÁVĚR
Laparoskopická sutura perforovaného peptického vředu může být metodou volby u pacientů bez nebo s nízkými rizikovými faktory. Mezi skupinami studie byly statisticky významné rozdíly ve věku, ASA a Boey skóre, což naznačuje, že k LS jsou obecně indikováni méně rizikoví pacienti. Laparoskopicky operovaní pacienti vykazovali vyšší výskyt lehkých i závažnějších komplikací. Vyšší mortalita pacientů s OS souvisí s jejich horším počátečním klinickým stavem. Předoperační stanovení rizika mortality pomoci Boeyova skóre je přesné a ke zvolení operačního přístupu výhodné. Riziko dehiscence sutury vředu je u LS vyšší než u OS.
Seznam zkratek:
APACHE II – acute physiology and chronic health evaluation II
ASA – American Society of Anesthesiologists
LS – laparoskopická sutura
NSAID – nesteroidní protizánětlivé léky
OS – otevřená (laparotomická) sutura
PPV – perforace peptického vředu
PULP – peptic ulcer perforation score
VCHGD – vředová choroba gastroduodena
Konflikt zájmů
Autoři článku prohlašují, že nejsou v souvislosti se vznikem tohoto článku ve střetu zájmů a že tento článek nebyl publikován v žádném jiném časopise, s výjimkou kongresových abstrakt a doporučených postupů.
MUDr. Lubomír Tulinský, Ph.D.
Chirurgická klinika Fakultní nemocnice
Ostrava 17. listopadu 1790
708 52 Ostrava
e-mail: lubomir.tulinsky@fno.cz
ORCID: 0000-0003-3100-5990
Sources
1. Lin KJ, García Rodríguez LA, Hernández - Díaz S. Systematic review of peptic ulcer disease incidence rates: do studies without validation provide reliable estimates? Pharmacoepidemiology and Drug Safety 2011 May 27;20(7):718–728. doi:10.1002/pds.2153.
2. Dítě P. Vředová nemoc žaludku a dvanáctníku, současné léčebné trendy. Interní Med. 2006; 8(5):231–234.
3. Wakayama T, Ishizaki Y, Mitsusada M, et al. Risk factors influencing the short-term results of gastroduodenal perforation. Surgery Today 1994 Aug;24(8):681–687. doi:10.1007/BF01636772.
4. Christensen S, Riis A, Nørgaard M, et al. Short-term mortality after perforated or bleeding peptic ulcer among elderly patients: a population-based cohort study. BMC Geriatrics 2007 Apr 17;7(1). doi:10.1186/1471-2318-7-8.
5. Noguiera C, Silva AS, Santos JN, et al. Perforated peptic ulcer: Main factors of morbidity and mortality. World Journal of Surgery 2003 Jul 1;27(7):782–787. doi: 10.1007/s00268-003-6645-0.
6. Thorsen K, Søreide JA, Søreide K. Scoring systems for outcome prediction in patients with perforated peptic ulcer. Scandinavian Journal of Trauma, Resuscitation and Emergency Medicine 2013;21(1):25. doi:10.1186/1757-7241-21-25.
7. Lohsiriwat V, Prapasrivorakul S, Lohsiriwat D. Perforated peptic ulcer: Clinical presentation, surgical outcomes, and the accuracy of the boey scoring system in predicting postoperative morbidity and mortality. World Journal of Surgery 2008 Oct 29;33(1):80–85. doi:10.1007/s00268 - 008-9796-1.
8. Boey J, Choi SK, Alagaratnam TT, et al. A prospective validation of predictive factors. Annals of Surgery 1987 Jan;205(1):22–32. doi:10.1097/00000658 - 198701000-00005.
9. Clavien PA, Barkun J, de Oliveira ML, et al. The Clavien-Dindo classification of surgical complications. Annals of Surgery 2009 Aug;250(2):187–196. doi:10.1097/ SLA.0b013e3181b13ca2.
10. Nathanson LK, Easter DW, Cuschieri A. Laparoscopic repair/peritoneal toilet of perforated duodenal ulcer. Surgical Endoscopy 1990 Dec;4(4):232–233. doi:10.1007/BF00316801.
11. Wright GP, Davis AT, Koehler TJ, et al. Cost-efficiency and outcomes in the treatment of perforated peptic ulcer disease: Laparoscopic versus open approach. Surgery 2014 Oct;156(4):1003 – 1008. doi:10.1016/j.surg.2014.06.047.
12. Davenport DL, Ueland WR, Kumar S, et al. A comparison of short-term outcomes between laparoscopic and open emergent repair of perforated peptic ulcers. Surgical Endoscopy 2018 Jul 11;33(3):764–772. doi:10.1007/s00464-018-6341-7.
13. Starý L, Vysloužil K, Klementa I, et al. Laparoskopické ošetření perforovaného vředu gastroduodena. Miniinvazívna chirurgia 2008;12(1):5–8.
14. Jayaraman SS, Allen R, Feather C, et al. Outcomes of laparoscopic vs open repair of perforated peptic ulcers: An ACSNSQIP study. Journal of Surgical Research 2021 Sep;265 : 13–20. doi:10.1016/j. jss.2021.02.030.
15. Pereira A, Santos Sousa H, Gonçalves D, et al. Surgery for perforated peptic ulcer: Is laparoscopy a new paradigm? Minimally Invasive Surgery 2021 May 12;2021 : 1–6. doi:10.1155/2021/8828091.
16. Fransvea P, Costa G, Lepre L, et al. Laparoscopic repair of perforated peptic ulcer in the elderly: An interim analysis of the FRAILESEL Italian Multicenter Prospective Cohort Study. Surgical Laparoscopy, Endoscopy & Percutaneous Techniques 2020 Jul 14;31(1):2–7. doi:10.1097/ SLE.0000000000000826.
17. Pelloni M, Afonso-Luís N, Marchena-Gomez J, et al. Comparative study of postoperative complications after open and laparoscopic surgery of the perforated peptic ulcer: Advantages of the laparoscopic approach. Asian Journal of Surgery 2022 Apr;45(4):1007–1013. doi:10.1016/j. asjsur.2021.08.059.
18. Quah GS, Eslick GD, Cox MR. Laparoscopic repair for perforated peptic ulcer disease has better outcomes than open repair. Journal of Gastrointestinal Surgery 2018 Nov 21;23(3):618–625. doi:10.1007/ s11605-018-4047-8.
19. Varcus F, Paun I, Duta C, et al. Laparoscopic repair of perforated peptic ulcer. Minerva Surgery 2018 Apr;73(2). doi:10.23736/s0026-4733.18.07603-4.
20. Chung KT, Shelat VG. Perforated peptic ulcer – an update. World Journal of Gastrointestinal Surgery 2017;9(1):1. doi:10.4240/wjgs.v9.i1.1.
21. Menekse E, Kocer B, Topcu R, et al. A practical scoring system to predict mortality in patients with perforated peptic ulcer. World Journal of Emergency Surgery 2015 Feb 21;10(1). doi:10.1186/s13017 - 015-0008-7.
22. Satinský I. Perforovaný peptický vřed – předoperační rizika, pooperační morbidita a mortalita, profylaxe v intenzivní péči a doporučení. Anesteziologie a intenzivní medicína 2012,
23.5 : 259–263. 23. Lunevicius R, Morkevicius M. Systematic review comparing laparoscopic and open repair for perforated peptic ulcer. British Journal of Surgery 2005 Sep 20;92(10):1195–1207. doi:10.1002/ bjs.5155.
24. Zhou C, Wang W, Wang J, et al. An updated meta-analysis of laparoscopic versus open repair for perforated peptic ulcer. Scientific Reports. 2015 Sep 9;5(1). doi:10.1038/srep13976.
25. Wilhelmsen M, Møller MH, Rosenstock S. Surgical complications after open and laparoscopic surgery for perforated peptic ulcer in a nationwide cohort. British Journal of Surgery 2015 Jan 21;102(4):382–387. doi:10.1002/bjs.9753.
26. Lee FYJ, Leung KL, Lai PBS, et al. Selection of patients for laparoscopic repair of perforated peptic ulcer. British Journal of Surgery 2001 Jan;88(1):133–136. doi:10.1046/j.1365-2168.2001.01642.x.
27. Siu WT, Leong HT, Law BKB, et al. Laparoscopic repair for perforated peptic ulcer. Annals of Surgery 2002 Mar;235(3):313 – 319. doi:10.1097/00000658-200203000 - 00001.
28. Lau W-Y, Leung K-L, Kwong K-H, et al. A randomized study comparing laparoscopic versus open repair of perforated peptic ulcer using suture or sutureless technique. Annals of Surgery 1996 Aug;224(2):131 – 138. doi:10.1097/00000658-199608000 - 00004.
29. Siu WT, Chau CH, Law BKB, et al. Routine use of laparoscopic repair for perforated peptic ulcer. British Journal of Surgery 2004 Feb 20;91(4):481–484. doi:10.1002/ bjs.4452.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2022 Issue 7-
All articles in this issue
- Mikrobiologie v chirurgii
- Diagnosis and treatment of surgical skin and soft tissue infections – current status
- Microbiological analysis of peritoneal fluid samples from patients with perforated peptic ulcer – retrospective observational study
- Infections associated with vascular reconstruction procedures at the Department of Surgery in Pilsen in retrospect
- Laparoscopic repair of perforated peptic ulcer – routine procedure or targeted patient selection?
- Benign stenosis of common bile duct after Roux Y gastrectomy
- Giant aggressive intra-abdominal desmoid-type fibromatosis – case report
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Diagnosis and treatment of surgical skin and soft tissue infections – current status
- Giant aggressive intra-abdominal desmoid-type fibromatosis – case report
- Laparoscopic repair of perforated peptic ulcer – routine procedure or targeted patient selection?
- Benign stenosis of common bile duct after Roux Y gastrectomy
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

