Spontánní retroperitoneální hematom – naše zkušenosti s aktivním chirurgickým přístupem
Authors:
L. Mitáš 1; T. Nevrtal 1; L. Kunovsky 1,2; Z. Kala 1; J. Kamelander 3; V. Čan 1; T. Andrašina 4; M. Penka 3; I. Penka 1
Authors‘ workplace:
Chirurgická klinika, Fakultní nemocnice Brno, Lékařská fakulta Masarykovy univerzity
1; Interní gastroenterologická klinika, Fakultní nemocnice Brno, Lékařská fakulta Masarykovy univerzity
2; Oddělení klinické hematologie, Fakultní nemocnice Brno, Lékařská fakulta Masarykovy univerzity
3; Klinika radiologie a nukleární medicíny, Fakultní nemocnice Brno, Lékařská fakulta Masarykovy univerzity
4
Published in:
Rozhl. Chir., 2019, roč. 98, č. 1, s. 23-26.
Category:
Case Report
Overview
Spontánní retroperitoneální hematom je závažnou komplikací antikoagulační a antiagregační terapie, jejíž incidence vzhledem ke zvyšujícímu se počtu pacientů s touto medikací v posledních letech narůstá. V dostupné literatuře je popisována celá řada kazuistik, které v drtivé většině případů doporučují při oběhové stabilitě pacienta konzervativní postup, popřípadě radiologické ošetření zdroje krvácení selektivní embolizací. Chirurgická revize je často uváděna jako metoda poslední volby při selhání konzervativní terapie, neúspěšnosti nebo nedostupnosti radiologické intervence u pacientů se známkami pokračujícího krvácení či při rozvoji břišního kompartment syndromu.
V naší kazuistice prezentujeme případ masivního retroperitoneálního krvácení u pacienta na antikoagulační terapii pro hlubokou žilní trombózu řešený primárně chirurgicky.
Klíčová slova:
retroperitoneální hematom − krvácení − antikoagulační léčba − chirurgie
Úvod
Spontánní retroperitoneální hematom (SRH) je definován jako krvácení do retroperitoneálního prostoru bez jakékoliv předchozí souvislosti s traumatem, chirurgickým výkonem, miniinvazivním výkonem či jinou základní patologií [1]. Již v roce 1969 Hodin et al. publikovali článek, v němž popisují vznik spontánního retroperitoneálního krvácení jako komplikaci antikoagulační terapie [2]. V posledních letech se udává, že až 66,3 % pacientů s diagnostikovaným SRH užívalo antikoagulační terapii [1]. Incidence SRH je udávána v rozmezí 0,5–6,6 % [3,4]. Jedná se tedy o méně častou, ale o to závažnější komplikaci antikoagulační terapie zatíženou vysokou morbiditou a mortalitou [5].
Mechanismus vzniku SRH není znám, ale existuje celá řada hypotéz jako difuzní arterioskleróza drobných arterií a arteriol, heparinem indukovaná imunitní mikroangiopatie či nerozpoznané mikrotrauma [6].
Mezi klinické příznaky jsou řazeny bolest v podbřišku a v lumbální oblasti, nauzea, zvracení, femorální neuropatie, anurie, hypotenze, tachykardie, až známky hypovolemického šoku či příznaky nitrobřišního kompartment syndromu (ACS) s postupným selháváním orgánů a možným letálním průběhem [6].
Stěžejním radiodiagnostickým vyšetřením v diagnostice SRH je CT angiografie. V tomto případě má vysokou senzitivitu, je snadno dostupná a může lokalizovat aktivní extravazaci kontrastní látky. Pokud je na CT angiografii viditelný aktivní zdroj krvácení, je terapeutickou metodou volby selektivní embolizace s cíleným ošetřením tohoto zdroje [6]. Pokud aktivní leak kontrastní látky na CT nenacházíme, odvíjí se další terapeutický postup od klinického stavu pacienta, známek pokračujícího krvácení a jeho rozsahu.
Kazuistika
61letý muž s četnými komorbiditami, s aktuálně probíhající antikoagulační terapií nízkomolekulárním heparinem (LMWH – low molecular weight heparin) (Fraxiparine 1 ml á 12 hod. při váze 110 kg) pro hlubokou trombózu femorální žíly vpravo, byl přivezen na urgentní příjem Fakultní nemocnice Brno pro kolapsový stav, dušnost a bolesti břicha. Při příjmu byl naměřen krevní tlak 90/60 mmHg, sinusová tachykardie 130 pulzů/minutu, objektivně byl pacient apatický s výraznou palpační bolestivostí v celé pravé polovině břicha. Naměřené vstupní laboratorní hodnoty byly: International normalized ratio (INR) 1,44, activated partial thromboplastin time (aPTT) 1,13, hladina hemoglobinu 72 g/l (předchozí hodnota před 48 hodinami byla 126 g/l), leukocyty 19x109/l, trombocyty 170x109/l, anti-Xa aktivita 0,88 kIU/l. Vstupně bylo na urgentním příjmu provedeno ultrazvukové vyšetření břicha, kde byl popsán v pravém hypogastriu pod úrovní ledviny a částečně i perirenálně objemný útvar smíšené echogenity velikosti minimálně 10 cm, bez zřetelného prokrvení, v diferenciální diagnostice na prvním místě již zkoagulovaný retroperitoneální hematom. Byla zahájena volumoterapie krystaloidy a koloidy (4 % Gelaspan). Po stabilizaci krevního oběhu bylo vzhledem ke klinickému stavu a výsledku ultrazvukového vyšetření provedeno urgentní CT angiografické vyšetření břicha, na kterém byl viditelný aktivní leak krvácení v pravém mezogastriu bez přesné lokalizace zdroje s retroperitoneálním hematomem jdoucím ze subhepatální úrovně až do oblasti pravého tříselného vazu (Obr. 1 a 2).
Fig. 1: CT (coronal scan): hematoma of the retroperitoneum
on the right with visible bleeding in the mediocaudal
part (indicated by an arrow)
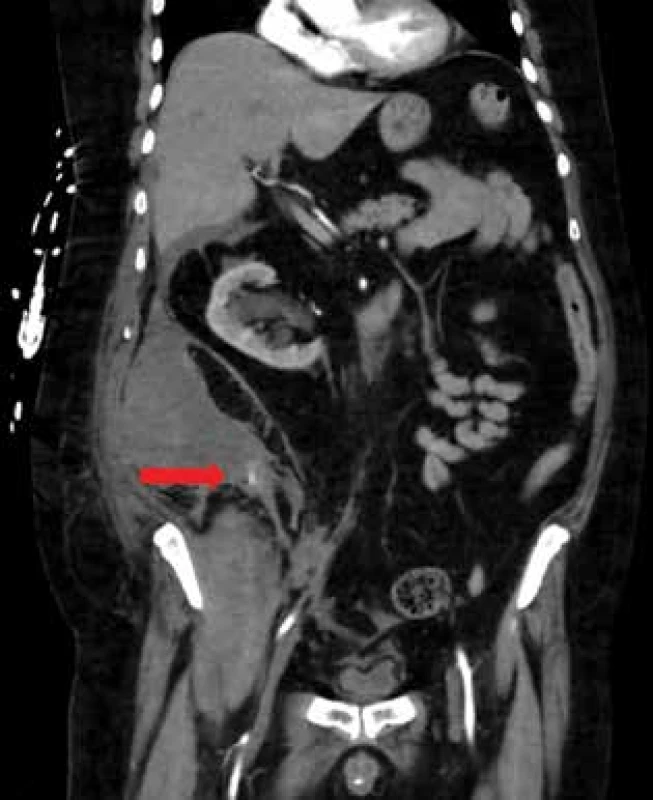
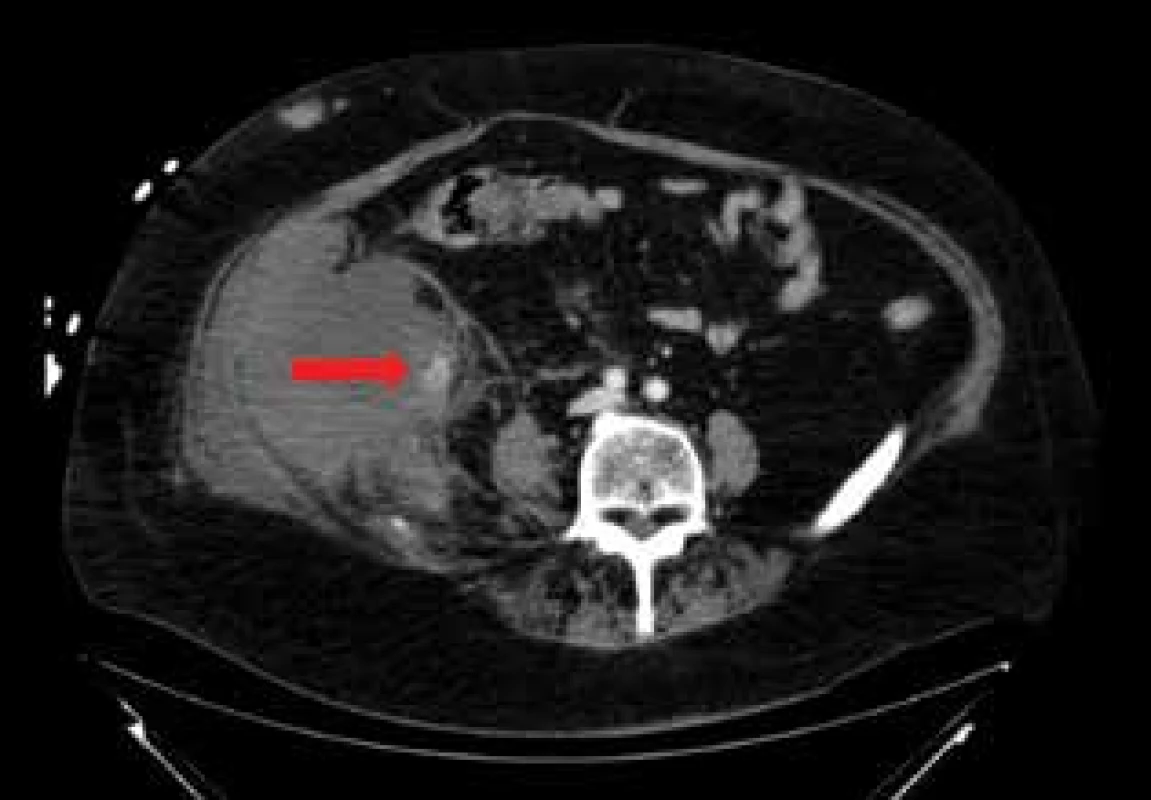
Fig. 2: CT (transversal scan): hematoma of the retroperitoneum
on the right with visible bleeding in the mediocaudal
part (indicated by an arrow)
Vzhledem ke zhoršujícímu se klinickému stavu pacienta s prohlubující se hypotenzí a známkám masivního krvácení byla indikována urgentní operační revize. S ohledem na probíhající léčbu terapeutickými dávkami LMWH byl konzultován hematolog a doporučena korekce 500 j Ocplexu, 2 ampulemi Dicynone, 1 g Exacylu a vzhledem k terapeutické hladině anti-Xa bylo podáno i 1000 jednotek Protamin hydrochloridu. Dále byly aplikovány 2 transfuzní jednotky erymasy k substituci hemoglobinu. Během operační revize z pravého retroperitoneálního přístupu ze střídavého řezu v pravém hypogastriu, bylo evakuováno asi 1000 ml krve a koagul, bez patrného chirurgicky ošetřitelného zdroje krvácení, proto byla provedena tamponáda 4 břišními rouškami. Během operace bylo podáno dalších 6 transfuzních jednotek erymasy a 4 plazmy. Po operaci byl pacient přeložen k monitoraci na Kliniku anesteziologie a resuscitační medicíny Fakultní nemocnice Brno, kde bylo pokračováno v péči o pacienta s klinickým obrazem hemoragického šoku s následnou postupnou stabilizací stavu. Za 48 hodin od primární operace byl proveden second look s extrakcí roušek bez nálezu pokračujícího krvácení. Byla tedy provedena drenáž a definitivní uzávěr břišní stěny po anatomických vrstvách. Pacient byl následně 7. den po primární operaci přeložen ve stabilizovaném stavu na interní oddělení, kde byl další pooperační průběh bez komplikací.
Diskuze
SRH je definován jako krvácení bez jakéhokoliv zjevného vyvolávajícího traumatu či patologie. Jedná se o méně časté onemocnění, které je však téměř vždy zaznamenáno u pacientů s antikoagulační nebo antiagregační terapií, koagulopatií a u dialyzovaných nemocných [6].
LMWH jsou považovány za bezpečné a efektivní v profylaxi i léčbě akutního koronárního syndromu, non-Q infarktu myokardu, žilní trombózy a plicní trombembolické choroby [3,7]. Jejich podání však není zcela bez rizika. V literatuře byly po aplikaci LMWH publikovány případy závažného krvácení do břišní stěny, jater, stehna, musculus psoas, retroperitonea, ale i do oblasti spinální a epidurálního prostoru [8]. Riziko závažných krvácivých komplikací při této medikaci je zvýšené dále u pacientů vyššího věku, se zhoršenými renálními funkcemi, v dávkách LMWH blížících se 1 mg/kg hmotnosti pacienta (100 IU/kg) a při souběžné medikaci léků ovlivňujících krevní srážlivost [3,9,10].
V našem případě šlo o masivní krvácení do oblasti pravého retroperitonea u 61letého polymorbidního pacienta, kterému bylo podáváno celkem 19 000 IU ve dvou dávkách na 110 kg tělesné hmotnosti v rámci terapie hluboké žilní trombózy v oblasti femorální žíly vpravo. Dávka tedy odpovídala 172 IU/kg.
Ve většině publikovaných prací je terapie SRH konzervativní, spočívající v přerušení antikoagulační či antiagregační medikace, úpravě koagulopatie, objemové resuscitaci a v případě nutnosti i podání krevních transfuzí [6].
Vysazení, přerušení či převedení pacienta na jinou formu antiagregační a antikoagulační terapie by však mělo být provedeno vždy po konzultaci indikujícího lékaře a hematologa, aby byla zvážena veškerá rizika jak trombotických, tak krvácivých komplikací u pacienta v dané situaci. Nutný je tedy individuální přístup a interdisciplinární spolupráce v řešení těchto závažných stavů.
V případě selhání konzervativní terapie je další možností chirurgická či radiologická intervence [6].
Konzervativní postup je preferován u pacientů vyššího věku, v případě stabilního oběhu i hladiny hemoglobinu, neprogredujícího ohraničeného hematomu a v případě, že není prokázán aktivní leak na zobrazovacích metodách [11]. Pokud je na CT angiografii prokázán aktivní zdroj krvácení v arteriální či venózní fázi, je indikována selektivní embolizace, jejíž výhodou je nižší invazivita v porovnání s operačním výkonem a možnost selektivního ošetření zdroje. Publikovaná technická úspěšnost embolizace při spontánním krvácení je 75–100 %, klinická úspěšnost pak 57−69 %. Rekurence aktivního krvácení po provedené embolizaci se v literatuře pohybuje od 16 do 25 % [12].
Chirurgická terapie je dle publikovaných prací indikována u pacientů, u kterých přetrvává oběhová nestabilita nebo známky pokračujícího krvácení přes adekvátní hrazení tekutin a krevních převodů, a pokud je radiologická intervence nedostupná nebo neúspěšná. Další indikací je pak rozvoj kompartment syndromu s kardiální, respirační či renální insuficiencí nebo femorální neuropatií [4,6].
Za nevýhody chirurgického přístupu jsou považovány: možné zhoršení krvácení při ztrátě tamponujícího efektu při otevření retroperitoneálního prostoru, rizika plynoucí z invazivního zákroku u pacienta v závažném stavu a dále velmi často neúspěšná lokalizace zdroje krvácení [11,13]. V případě nenalezení chirurgického zdroje krvácení a přítomnosti difuzního sáknutí ze tkání při koagulopatii je pak nejčastěji užívána tamponáda břišními rouškami [4,9]. V případě rozvoje ACS pak může být kromě evakuace hematomu nutná i dekompresní laparotomie [9]. Výhodou chirurgického řešení oproti konzervativní léčbě a radiologické intervenci je evakuace hematomu [6] jako prevence ACS a možných infekčních komplikací. V dostupné literatuře téměř chybějí data o dalším vývoji často objemných hematomů řešených konzervativně či jen radiologickou intervencí.
I přes agresivní terapii zůstává mortalita SRH vysoká a může dosahovat až 33 % [14], v případě rozvoje ACS až 62 %, většinou na podkladě multiorgánového selhání či sepse [15,16].
Vzhledem k výše uvedeným poznatkům se na našem pracovišti kloníme v případě rozsáhlých retroperitoneálních hematomů se známkami pokračujícího krvácení k aktivnímu chirurgickému přístupu s evakuací hematomu, ošetřením zdroje krvácení (pokud je nalezen) a drenáží, či v případě difuzního krvácení s tamponádou břišními rouškami, které jsou následně extrahovány za 24−48 hodin. Tento postup byl zvolen i v námi prezentovaném případu s dobrým efektem a nekomplikovaným pooperačním průběhem u pacienta s masivním krvácením pod obrazem hemoragického šoku.
Závěr
SRH patří mezi závažné komplikace antikoagulační a antiagregační medikace, jehož incidence narůstá. Je nutné na něj pomýšlet v diferenciální diagnostice u pacientů léčených touto medikací a vyšetřovaných pro známky krvácení, bolesti břicha a lumbalgie. Včasná diagnostika a adekvátní léčba jsou nezbytné ke snížení vysoké morbidity a mortality tohoto onemocnění. I když hlavním požadavkem je v těchto situacích zástava krvácení a stabilizace pacienta, je nutné brát v úvahu i riziko trombotických komplikací při přerušení medikace s možnými fatálními následky. Interdisciplinární spolupráce s konzultací hematologa je tedy nezbytná.
Seznam zkratek
ACS − abdominal compartment syndrome − břišní kompartment syndrom
aPTT − activated partial thromboplastin time − aktivovaný parciální tromboplastinový čas
CT − computed tomography − počítačová tomografie
INR − International normalized ratio − mezinárodní normalizovaný poměr
LMWH − low molecular weight heparin − nízkomolekulární heparin
SRH − spontánní retroperitoneální hematom
Konflikt zájmů
Autoři článku prohlašují, že nejsou v souvislosti se vznikem tohoto článku ve střetu zájmů a že tento článek nebyl publikován v žádném jiném časopise.
MUDr. Lumír Kunovský, Ph.D.
Chirurgická klinika, FN Brno Bohunice, LF MU
Jihlavská 20
625 00 Brno
e-mail: kunovsky.lumir@fnbrno.cz
Sources
-
Sunga KL, Bellolio MF, Gilmore RM, et al. Spontaneous retroperitoneal hematoma: Etiology, characteristics, management, and outcome. J Emerg Med 2012;43:e157–61.
-
Hodin E, Dass T. Spontaneous retroperitoneal hemorrhage complicating anticoagulant therapy. Ann Surg 1969;170:848–51.
-
Ernits M, Mohan PS, Fares LG, et al. A retroperitoneal bleed induced by enoxaparin therapy. Am Surg 2005;71:430–3.
-
Chan YC, Morales JP, Reidy JF, et al. Management of spontaneous and iatrogenic retroperitoneal haemorrhage: conservative management, endovascular intervention or open surgery? Int J Clin Pract 2008;62:1604–13.
-
Chan-Tack KM. Fatal spontaneous retroperitoneal hematoma secondary to enoxaparin. South Med J 2003;96:58–60.
-
Won DY, Kim SD, Park SC, et al. Abdominal compartment syndrome due to spontaneous retroperitoneal hemorrhage in a patient undergoing anticoagulation. Yonsei Med J 2011;52:358–61.
-
Besir FH, Gul M, Ornek T, et al. Enoxaparin-associated giant retroperitoneal hematoma in pulmonary embolism treatment. N Am J Med Sci 2011;3:524–6.
-
Vayá A, Mira Y, Aznar J, et al. Enoxaparin-related fatal spontaneous retroperitoneal hematoma in the elderly. Thromb Res 2003;110:69–71.
-
Quartey B, Nelson J. Massive spontaneous retroperitoneal hemorrhage induced by enoxaparin and subsequent abdominal compartment syndrome requiring surgical decompression: A case report and literature review. Int J Case Rep Imag 2011;2:14–8.
-
Fernández-Ruiz M, Guerra-Vales JM. Enoxaparin-induced retroperitoneal haematoma in patients with renal insufficiency. Swiss Med Wkly 2010;140:122–3.
-
Butt MU, Buzsaki LA, Smyth SS, et al. Deep vein thrombosis complicated by spontaneous iliopsoas hematoma in patient with septic shock. Am J Case Rep 2017;18:1148–52.
-
Dohan A, Darnige L, Sapoval M, et al. Spontaneous soft tissue hematomas. Diagn Interv Imaging 2015;96:789–96.
-
Dondelinger RF, Trotteur G, Ghaye B, et al. Traumatic injuries: radiological hemostatic intervention at admission. Eur Radiol 2002;12: 979–93.
-
Triscott J, Mercer S, Tian PG, et al. Retroperitoneal haematoma associated with enoxaparin use in an elderly woman with chronic kidney disease. BMJ Case Rep 2015. Available from: doi:10.1136/bcr-2015-211699.
-
Hunter JD, Damani Z. Intra-abdominal hypertension and the abdominal compartment syndrome. Anaesthesia 2004; 59: 899–907.
-
Moore AF, Hargest R, Martin M, et al. Intra-abdominal hypertension and the abdominal compartment syndrome. Br J Surg 2004;91:1102–10.
Labels
Surgery Orthopaedics Trauma surgeryArticle was published in
Perspectives in Surgery

2019 Issue 1
Most read in this issue
- Spontánní retroperitoneální hematom – naše zkušenosti s aktivním chirurgickým přístupem
- Mezenteriální divertikly tenkého střeva jako příčina náhlé příhody břišní
- Timing ERCP u akutní biliární pankreatitidy
- Současná léčba difuzních peritonitid – je kvadrantová laváž stále aktuální?
