-
Medical journals
- Career
Malígny fibrózny histiocytóm ako raritná príčina akútnej končatinovej ischémie
: J. Pobehová 1; M. Zavacká 1; P. Závacký 2; P. Pobeha 3; M. Koščo 4; M. Frankovičová 1
: Klinika cievnej chirurgie, LF Univerzity P. J. Šafárika a VÚSCH, Košice prednosta: prof. MUDr. M. Frankovičová, PhD. 1; I. Chirurgická klinika UNLP a LF P. J. Šafárika, Košice Prednosta: prof. MUDr. J. Radoňak, PhD. 2; LF Univerzity P. J. Šafárika, Košice dekan: prof. MUDr. D. Pella, PhD. 3; Angiologické oddelenie Kliniky kardiológie, VÚSCH, a. s., Košice prednosta: prof. MUDr. G. Valočik, PhD. 4
: Rozhl. Chir., 2017, roč. 96, č. 5, s. 218-223.
: Case Report
Malígny fibrózny histiocytóm (MFH) patrí medzi zriedkavé zhubné ochorenia srdca a aorty. Symptomatológia ochorenia závisí od lokalizácie, veľkosti, stupňa invazivity a tvorby metastáz. V literárnych zdrojoch nachádzame pomerne málo prípadov akútnej embolizácie tumoróznych más do arteriálneho systému viscerálnych a končatinových tepien. V prezentovanej kazuistike popisujeme prípad pacienta s akútnou ischémiou oboch dolných končatín, ktorej príčinou boli tromboembolické masy s bunkami malígneho fibrózneho histiocytómu. Tento nádor má v literárnych zdrojoch popisovanú nepriaznivú prognózu, čo potvrdzuje aj tento prípad.
Kľúčové slová:
akútna končatinová ischémia − periférna embolizácia − Fogartyho embolektómia − malígny fibrózny histiocytómÚVOD
Akútna končatinová ischémia (ALI − acute limb ischemy) vzniká náhlym poklesom, alebo zhoršením prietoku krvi končatinou, čo ohrozuje jej životaschopnosť. Napriek výraznému pokroku v diagnostike a liečbe môže byť zdrojom mnohých komplikácií, ktoré v prípade nepriaznivého vývoja môžu vyústiť do straty končatiny alebo viesť k smrti [1,2]. Závažnosť prejavov akútnej končatinovej ischémie závisí primárne od lokalizácie, trvania a rozsahu uzáveru tepny, ako aj od kapacity kolaterálneho obehu zabezpečiť perfúziu periférnych tkanív. Hlavné príčiny vzniku sú embolizácia a trombóza tepnového riečiska dolných končatín. Včasná diagnostika príčiny a lokalizácie uzáveru tepny s následnou úspešnou revaskularizáciou sú nevyhnutnou podmienkou pre priaznivú prognózu postihnutej končatiny, ako aj celkového stavu pacienta [2].
Etiológia
Akútny uzáver natívnej tepny môže byť spôsobený embolizáciou v mieste bifurkácie, trombózou v teréne aterosklerotických zmien, pri hyperkoagulačných stavoch, arteritíde, uvoľnením trombotických más z aneuryzmy. Zriedkavejšie sa popisuje ako príčina vzniku ALI entrapment syndróm arteria poplitea a cystická degenerácia adventície.
V prípade etiológie uzáverov tepnových náhrad sa pri protetických bypassoch uvádza ako najčastejšia príčina intimálna hyperplázia v anastomózach. Pri autológnych náhradách bývajú príčinou stenózy v mieste poškodenia žily, alebo pozostatok hrotu chlopne v in-situ grafte.
V literárnych zdrojoch sa ako zriedkavá príčina ALI popisuje embolizácia nádorovými hmotami u nádorov srdca a aorty. Emboly sa zvyčajne zachytávajú v oblastiach, kde sa arteriálne riečisko vetví, prípadne v miestach zúženia, a pri takzvanej prachovej mikroembolizácii dochádza k roztriešteniu embolických hmôt do drobných periférnych tepien.
Diagnostika
Základom diagnostiky ALI sú anamnestické údaje, fyzikálne vyšetrenie s palpáciou pulzov na končatinách, zobrazovacie metódy (ultrasonografia, DSA, CT AG, MRI).
V klinickom obraze sa ALI prejaví šiestimi typickými príznakmi: paresthesia – tŕpnutie, pain – bolesť, pallor – bledosť, pulslessness – chýbanie pulzácií, paralysis – paralýza a poikilothermia – chlad.
Hodnotenie senzitívneho a motorického deficitu v diagnostike je smerodajné pre klasifikáciu ochorenia, ako aj pre ďalší diagnosticko-terapeutický postup.
Tab. 1 popisuje štandardné zobrazovacie techniky v diagnostike tohto ochorenia. Včasná diagnostika príčiny a lokalizácie uzáveru tepny s následnou úspešnou revaskularizáciou sú nevyhnutnou podmienkou pre priaznivú prognózu postihnutej končatiny, ako aj celkového stavu pacienta [2].
1. Špeciálne prístrojové vyšetrovacie metódy pri ALI DK Tab. 1: Special diagnostic methods of ALI 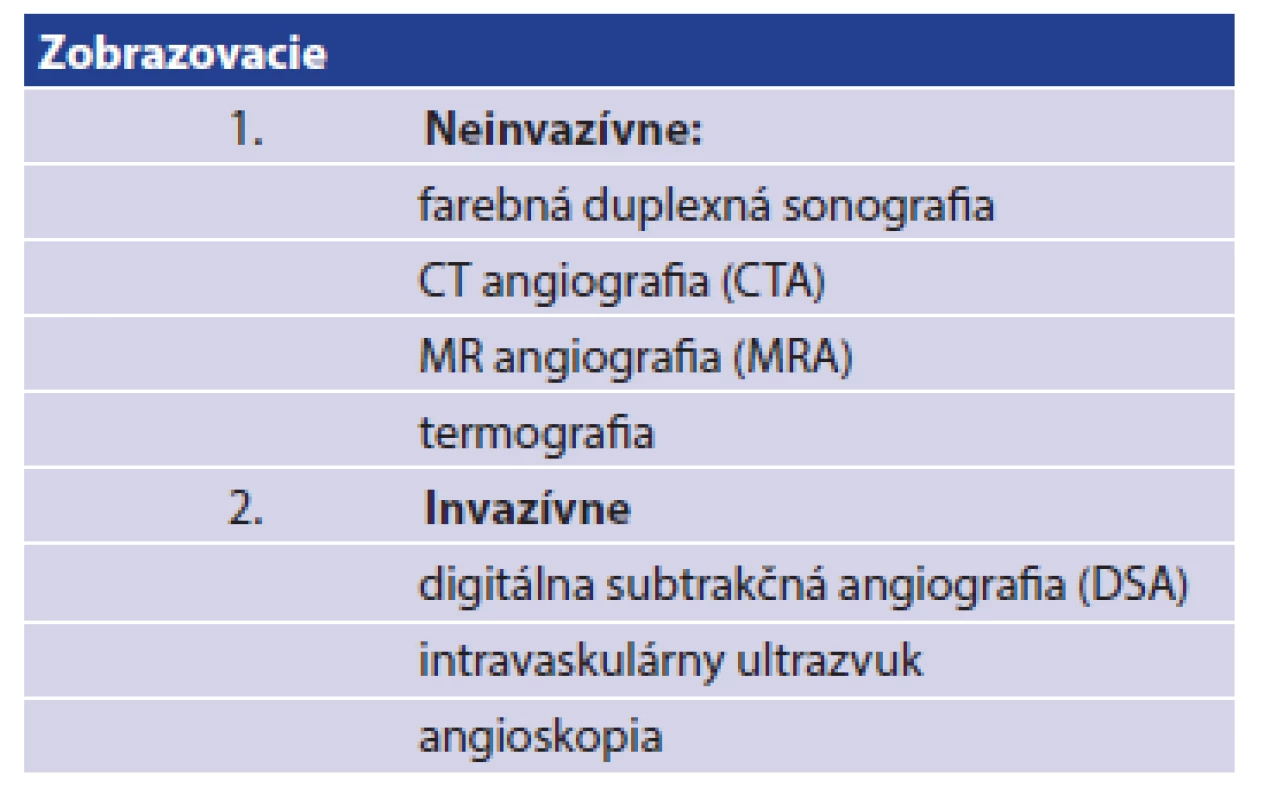
Voľba terapeutickej modality akútnej končatinovej ischémie závisí od lokalizácie tepnového uzáveru, od klinického štádia ochorenia, od preferencie pacienta, ako aj od skúseností a technického vybavenia daného pracoviska (Tab. 2). Mortalita spojená s akútnym periférnym tepnovým uzáverom je vysoká, v priemere dosahuje 10–25 % [3,4].
2. Modality liečby akútnej končatinovej ischémie Tab. 2: Treatment options of acute limb ischemy 
Najdôležitejším liečebným bodom konzervatívneho postupu pri ALI je aplikácia prvotnej dávky heparínu, ktorá zabráni progresii trombózy v periférnom riečisku a spomalí nástup ireverzibilných ischemických zmien.
Indikácia chirurgickej revaskularizácie závisí od klinického obrazu ALI, od komorbidít pacienta a od etiológie akútnej končatinovej ischémie. Embolické uzávery sa často dajú vyriešiť embolektómiou, kým riešením trombotických uzáverov môže byť endarterektómia alebo bypassová rekonštrukcia [2,5]. Operácia u väčšiny pacientov s embolickým uzáverom marginálnej tepny dolnej končatiny sa začína transfemorálnym prístupom cez arteriotómiu v oblasti arteria femoralis communis (AFC), čo umožňuje cievny prístup pre balónikovú katétrovú trombektómiu od bifurkácie aorty až po členok. Zriedkavo je potrebné zabezpečiť podkolenný prístup [3,6,7]. V prípade absencie výtokového traktu, alebo neprítomnosti periférneho Doppler signálu po trombembolektómii, je potrebné realizovať angiografiu postihnutej končatiny za účelom zváženia ďalšieho postupu. Potreba vykonať amputáciu pri ischémii trvajúcej menej ako 4 hodiny je v 3 % prípadov, pri ischémii medzi 4 a 6 hodinami v cca 10 %, v trvaní 6−12 hodín v cca 25 % a pri ischémii trvajúcej viac ako 12 hodín stúpa riziko amputácie na 50−60 % [8].
KAZUISTIKA
64ročný muž, dlhoročný aktívny fajčiar (5 až 6 cigariet denne), hypertonik, bol v máji 2015 v urgentnom režime preložený zo spádového chirurgického oddelenia na Kliniku cievnej chirurgie Východoslovenského ústavu srdcovej a cievnej chirurgie (VÚSCH), a.s., Košice, s náhle vzniknutou slabosťou a pokojovými bolesťami oboch dolných končatín. Anamnesticky udával bolesti nôh pri chôdzi v trvaní dvoch týždňov.
Z pridružených ochorení sa okrem artériovej hypertenzie liečil na vredovú chorobu gastroduodena, bilaterálnu nefrolitiázu a polyglobulický syndróm. Pri príjme bol pacient afebrilný, obe dolné končatiny boli chladné, bledé, s mramorovou kožou. Vykonaná CT angiografia v spádovej nemocnici preukázala oklúziu oboch spoločných iliackých tepien. Pred prevozom bol na spádovom chirurgickom oddelení podaný nízkomolekulárny heparín (LMWH) v terapeutickej dávke. Pri vstupnom fyzikálnom vyšetrení boli obe dolné končatiny chladné, bledé, predkolenia a akrá mramorové s rozvinutým senzomotorickým deficitom, ochlpenie končatín bolo zachované, končatiny boli bez kožných defektov a gangrény, pulzácie neboli hmatné na aa. femorales, aa. poplitae, ani na periférii bilaterálne. Pri vstupnom ultrasonografickom vyšetrení ciev bol vizualizovaný len krátky úsek infrarenálnej časti brušnej aorty, ktorá nebola dilatovaná, s prítomným preokluzívnym tokom. Spoločné panvové tepny (aa. iliacae communes – AIC) a vonkajšie panvové tepny (aa. iliacae externae – AIE) boli bez toku krvi. Stav bol angiológom a cievnym chirurgom zhodnotený ako akútny bilaterálny končatinový uzáver tepien s uzáverom spoločných a vonkajších iliackých artérií, siahajúci až do oblasti bifurkácie abdominálnej aorty, klasifikovaný ako štádium ALI - Rutherford IIb, vyžadujúci si neodkladnú operačnú revíziu (viď. Obr. 1,2).
Obr. 1, 2: Angiografický nález pred chirurgickým riešením Fig. 1, 2: DSA before the Surgical Treatment 
Vo vstupnom laboratórnom obraze dominovala anémia (6,90 g/dl), zvýšený počet trombocytov (500x109/l), leukocytóza (27,01x109/l), hodnoty zrážacích parametrov preukázali zvýšenú viskozitu krvi. Vyšetrenie vnútorného prostredia dokumentovalo hyperglykémiu 12,1mmol/l a retenciu dusíkatých metabolitov kreatinínu (122 μmol/l) a urey (11,00 mmol/l). Po predoperačnej príprave, hemosubstitúcii, profylaktickom podaní antibiotík (Vulmizolin 4x1 g iv.) a nízkomolekulárneho heparínu ( LMWH) bol pacient operovaný.
V celkovej anestézii bola realizovaná trombektómia iliackých tepien vpravo, AFC, AFS a AP a krurálnych tepien na oboch stranách. Trombotické masy extrahované z končatinových tepien boli odoslané na histologické vyšetrenie. Snaha o spriechodnenie iliackých tepien na ľavej dolnej končatine bola neúspešná aj po opakovaných prienikoch Fogartyho katétrami. Konzultovaný intervenčný angiológ indikoval digitálnu subtrakčnú angiografiu (DSA), na ktorej bol nález primeraného toku tepien od a. iliaca communis až po trojcievny výtokový trakt na predkolení vpravo, avšak vľavo bola a. iliaca communis priechodná iba v úseku 2 cm s trombotickým uzáverom a chýbaním náplne ciev distálne od uzáveru (viď. Obr. 3).
1. Trombus v a.iliaca externa l.sin. Fig. 3: Trombus inside a. iliaca externa l.sin. 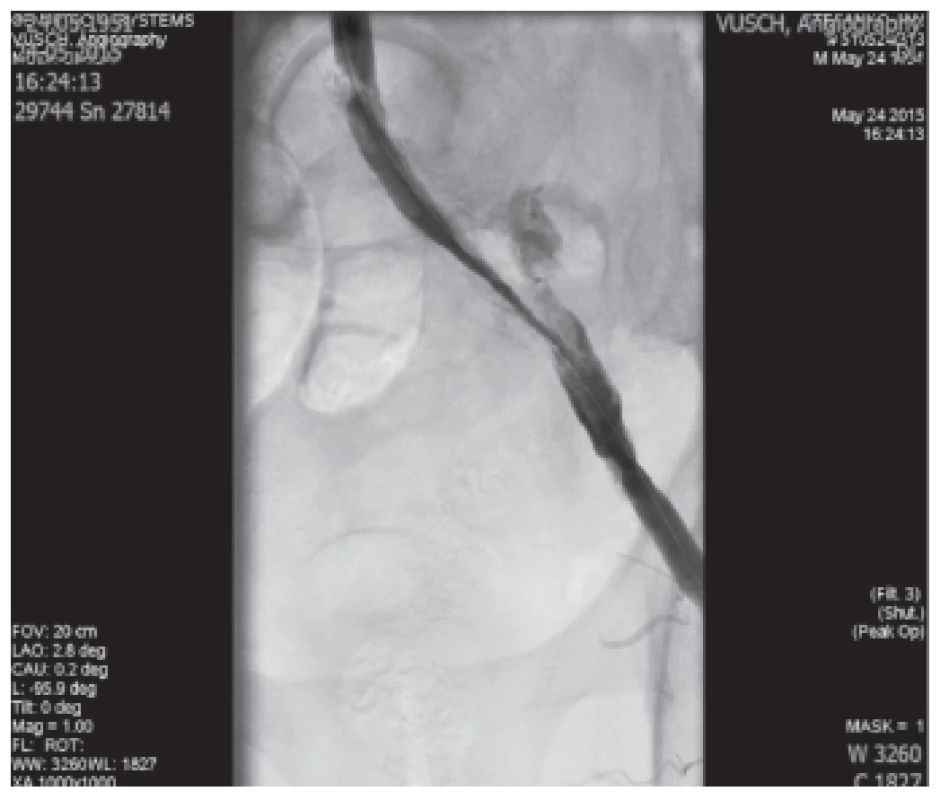
Intervenčný angiológ spriechodnil iliacké tepny vľavo mechanickou trombektómiou, s implantáciou stentgraftu do a. iliaca externa vpravo pre vzniknutý paravazát (viď. Obr. 4, 5, 6). Následne pre proximálne vzniknuté disekcie cievnej steny doplnil perkutánnu transluminálnu angioplastiku (PTA) a stent do a. iliaca communis vľavo s priaznivým efektom.
2. Umiestnenie katétra pre mechanickú trombektómiu AIE l.sin. Fig. 4: Catheter placement for mechanical thrombectomy AIE l.sin. 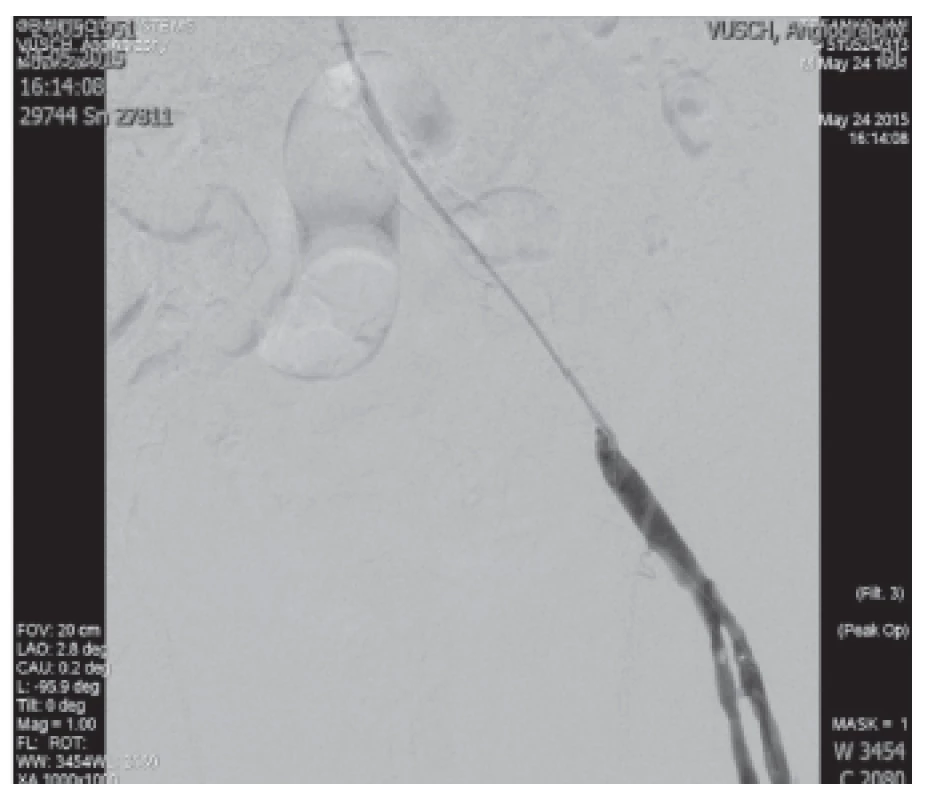
3. Implantácia stentgraftu do AIE l.sin. Fig. 5: Implantation of the stentgraft in AIE l.sin. 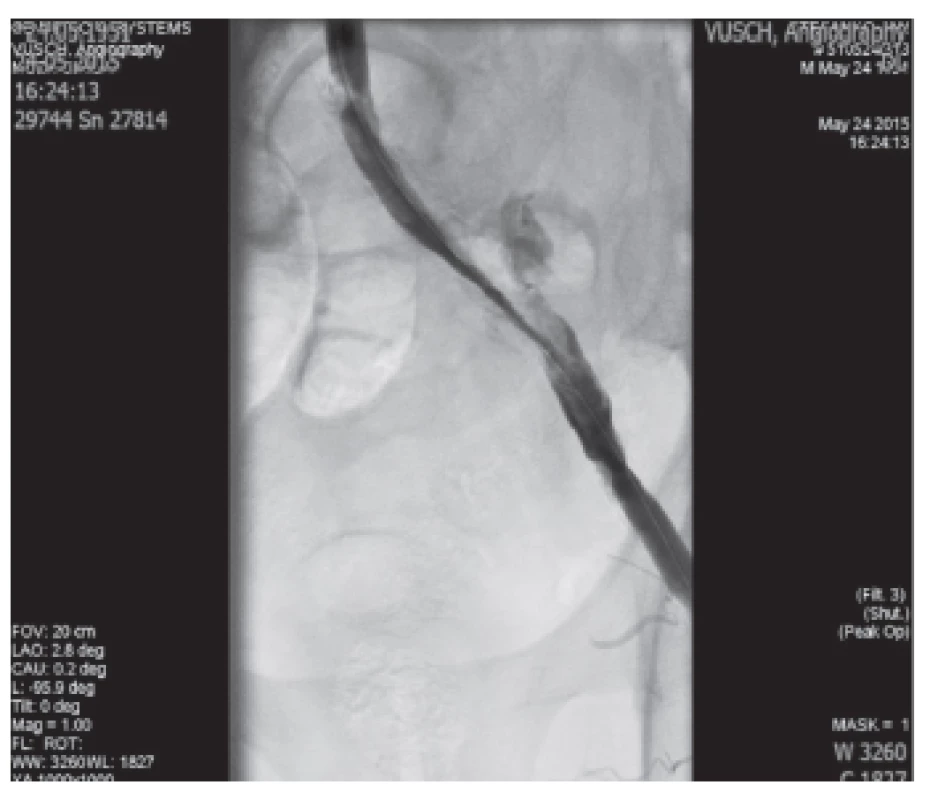
4. Implantácia balón-expandibilného stentu do AIE l.sin. Fig. 6: Implantation of the baloon expandible stent in AIE l.sin. 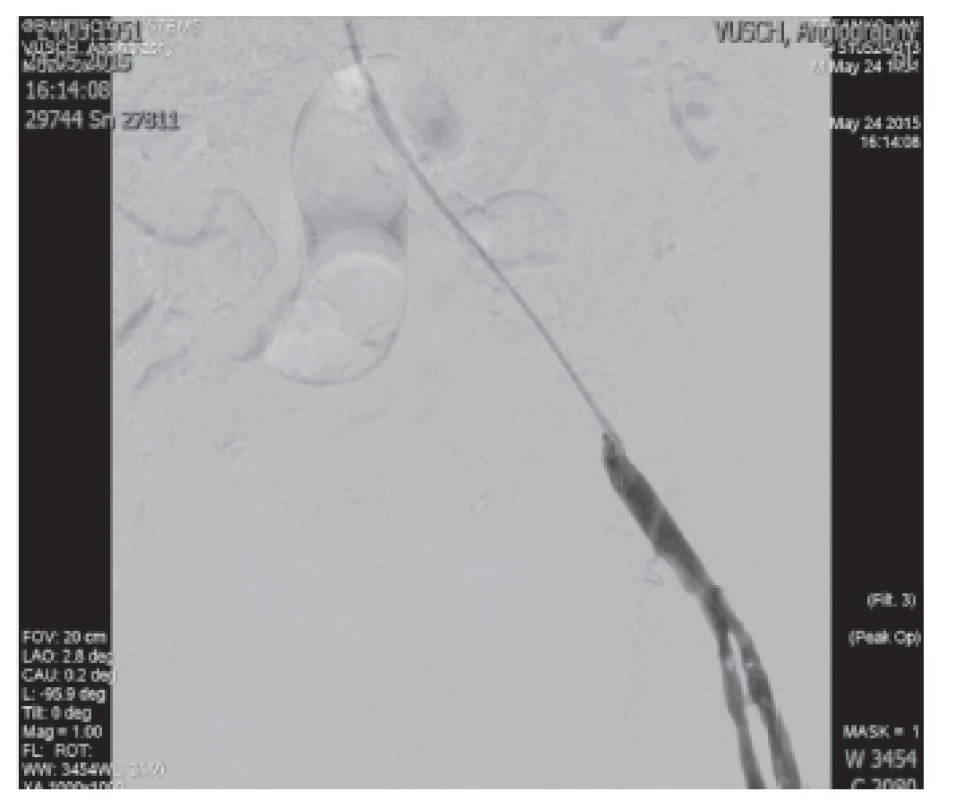
Pacient bol po výkone za účelom stabilizácie celkového stavu a pre kontinuálny monitoring preložený na Kliniku anesteziológie a intenzívnej medicíny (KAIM) VÚSCH, a.s. Priebeh tejto hospitalizácie bol komplikovaný rozvojom akútnej končatinovej reperfúzie tepien ľavej dolnej končatiny, preto bola angiochirurgom do 24 hodín indikovaná a vykonaná urgentná fasciotómia z ventrálnej, dorzálnej i laterálnej strany. Pooperačné straty do drénov boli minimálne, doplnené infúziami koloidných roztokov, erytrocytárnymi masami a čerstvou plazmou. Postupne dochádza k úprave parametrov vnútorného prostredia. V klinickom obraze pacienta dominovali bolesti dolných končatín. Tie boli teplé, s prekrvenými akrálnymi časťami. Pacient bol následne liečený penicilínovými antibiotikami a antitrombotickou trojkombináciou: LMWH, Clopidogrel, kyselina acetylsalicylová (ASA) a vazodilatačnými infúziami. Pooperačný priebeh sa naďalej komplikoval hepatorenálnym zlyhávaním pri reperfúznom syndróme, s pravdepodobným podielom nefropatie navodenej kontrastnou látkou. Napriek vyrovnanej bilancii tekutín, prevencii hypotenzie a redukcii nefrotoxických látok vrátane antibiotík (Unasyn 2x1,5 g i.v.), došlo u pacienta k rozvoju pľúcneho edému a respiračnému zlyhávaniu, preto bol pacient opakovane preložený na Kliniku anesteziológie, VÚSCH, a.s., kde bola začatá umelá pľúcna ventilácia a hemodialýza. Vzhľadom na náhle a dramatické zhoršenie stavu, bola ľavá dolná končatina amputovaná až po nevyhnutnej stabilizácii celkového stavu na 4. pooperačný deň. V priebehu ďalšieho ošetrovacieho dňa dochádza k postupnému obnoveniu spontánnej diurézy a odpojenia od umelej pľúcnej ventilácie. Postupne dochádza k stabilizácii stavu, ktorá umožnila postupnú rehabilitáciu. Pacient bol po 12 dňoch preložený na spádové chirurgické oddelenie za účelom pokračovania v konzervatívnej terapii, kde však dochádza k opätovnému zhoršeniu zdravotného stavu a exitu na kardiorespiračné zlyhanie v teréne multiorgánovej dysfunkcie.
Až po ukončení našej hospitalizácie získavame definitívne výsledky histopatologického vyšetrenia trombotických hmôt z tepien oboch dolných končatín, kde po opakovanom vyšetrení vrátane imunohistochémie, bol identifikovaný recentný zmiešaný trombus a z väčšej časti nekroticky zmenené štruktúry malígneho mezenchymálneho novotvaru. Per exclusionem išlo o malígny fibrózny histiocytóm (MFH).
DISKUSIA
Primárne malígne neoplázie srdca sú zriedkavé tumory, ktoré tvoria 25 % všetkých primárnych nádorov srdca [9,10,11]. Prevalencia primárnych sarkómov srdca, zistená na základe veľkých štúdií pitevných nálezov zo 6 nemocníc v USA [9], je 0,0017 % a celková globálna incidencia 0,001−0,03 % [12,13]. MFH je nediferencovaným sarkómom s pleiomorfnými a epiteloidnými bunkami a malým množstvom viacjadrových buniek. U väčšiny zdokumentovaných tumorov popisovaných v literárnych zdrojoch bola histologická vzorka získaná, tak ako aj v našom prípade, z periférneho embolu. Definitívnu diagnózu potvrdila až pitva.
Do roku 1991 bolo popísaných iba 29 prípadov tumorov aorty, z toho 26 malígnych sarkómov a 3 benígne tumory [14], väčšina postihnutých pacientov bola mužského pohlavia (68 %) [15].
Zahraničné literárne zdroje uvádzajú nasledujúce lokalizácie tumoru získané pri nekropsii: ascendentná aorta a oblúk – 1 prípad, hrudná aorta − 9 prípadov [16,17], brušná aorta – 14 prípadov, na hrudnej a brušnej aorte súbežne – 5 prípadov [18,19,20,21,22]. Histologicky tumor zaberal v 20 prípadoch iba aortálnu intimu, v 7 presahoval až do adventície, v 2 prerastal celou stenou a šíril sa do okolia [17,23,24].
Wright a kolektív [24] rozdelili MFH na základe rozsahu a lokalizácie do dvoch skupín. Prvú tvorí MFH pôvodom a lokalizáciou z tunica intima aorty, ktorá zasahuje intimu cievy a klinicky sa prezentuje embolizujúcimi metastázami. V druhej skupine je uvádzaný myxoidný malígny fibrózny histiocytóm, ktorý býva lokalizovaný v tunica adventitia alebo media a klinicky sa prejavuje kompresívnym syndrómom.
Symptómy nádoru závisia na lokalizácii, veľkosti, stupni invazivity a tvorbe metastáz. Tie sa šíria vaskulárnou cestou predovšetkým do viscerálnych orgánov, kde embolizujúce masy uzatvárajú tepny najčastejšie v oblasti aa. mesentericae a a. poplitea. V prípade uvádzanom v našej kazuistike išlo o akútny uzáver oboch dolných končatín prakticky od aortálnej bifurkácie smerom distálne, na čom sa pravdepodobne podieľala aj apozičná trombóza. Ďalšie cesty šírenia metastáz sú najčastejšie do pečene, svalov, kostí, mozgu a pľúc [25,26,27,28,29].
Štandardom v diagnostike primárneho tumoru zostávajú zobrazovacie metódy: echokardiografické vyšetrenie: transtorakálne (TTE), transezofageálne (TEE), CT, MRI vyšetrenie, ktoré napomáhajú lokalizovať metastázy tumoru. V našom prípade nebolo primárne ložisko tohto zriedkavého tumoru dodiagnostikované z dôvodu jednak ťažkých pooperačných komplikácií (dlhodobá umelá pľúcna ventilácia a podpora obehu na Klinike anesteziológie a intenzívnej medicíny, pridružené renálne zlyhanie, realizované fasciotómie dolných končatín pre kompartment syndróm ako dôsledok dlhotrvajúcej bilaterálnej akútnej končatinovej ischémie, až po amputáciu), ako aj z dôvodu dostupnosti histologického nálezu, ktorý sme dostali až po preklade pacienta na spádové chirurgické oddelenie, ktoré bolo o výsledku informované. Následné dodiagnostikovanie prípadu vyššie uvedenými zobrazovacími metódami a začatie adekvátnej liečby nádoru sa už nerealizovalo v dôsledku úmrtia pacienta.
Viaceré publikácie uvádzajú, že tento nádor srdca a aorty je veľmi invazívny a s veľmi zlou prognózou [25,26,27]. Štandardnou liečbou ochorenia je resekcia celého tumoru, s následnou rádio a chemoterapiou. Napriek adekvátnej liečbe uvádzajú dostupné štúdie priemerné prežívanie len 22,2±6,1 mesiaca po resekcii tumoru, jednoročné prežívanie sa dosiahne u 82,5 % pacientov, dvojročné u 41,3 % pacientov [30].
V literatúre sú spomenuté kauzistické prípady. Podobne ako v našom prípade, popísal Tejada a kol. (1991) [15] prípad 69 ročného pacienta s prejavmi akútnej končatinovej ischémie v trvaní cca 10 hodín, s angiograficky dokumentovaným uzáverom oboch popliteálnych tepien. Zo vzoriek z bilaterálnej embolektómie bol histologicky potvrdený MFH. Autori doplnili CT a MRI vyšetrenie, ktorými dokázali lobulárne exofyitické masy tumoru intraluminálne v aorte, bez extra-aortálnej tenzie. Primárny tumor bol chirurgicky odstránený s aortálnou náhradou v dostupnom úseku, avšak po výkone bol stav pacienta komplikovaný paraplégiou, pneumóniou, renálnym zlyhaním a exitoval do 6 mesiacov po stanovení primárnej diagnózy. Nekropsia potvrdila emboly aj v hepatálnych a splenickej tepne, viacnásobné infarkty pečene, staršie infarkty mozgu a mozočka. V prípade nášho pacienta nebol primárny tumor histologizovaný, pretože pitva na žiadosť príbuzných realizovaná nebola.
Ako najnovší v literatúre publikovaný prípad je uvádzaná kazuistika autorov Sun a kol. (2015) [31], kde uviedli prípad 37 ročnej pacientky s 3 mesačnou anamnézou dyspnoe a následným dvojdňovým akútnym zhoršením stavu. Echokardiograficky boli v ľavej komore preukázané masy veľkosti 5x2,3 cm, ktoré počas diastoly zasahovali do mitrálnej chlopne, spôsobujúc mitrálnu stenózu. Doplnené röntgenologické (RTG) a CT vyšetrenia nepotvrdili tumorózne masy v inej oblasti. Diagnóza MFH bola potvrdená histologicky z resekátu. Po resekcii nádoru podstúpila pacientka chemoterapiu, avšak po mesiaci došlo k nebolestivej recidíve na vulve vľavo. Napriek extirpácii útvaru a ďalšej chemoterapii pacientka taktiež do 6 mesiacov exitovala.
ZÁVER
Malígny fibrózny histiocytóm je zriedkavý nádor srdca a aorty so zlou prognózou. Prejavy môžu byť kombináciou symptomatológie primárneho nádoru v srdci a aorte a zároveň z metastatického šírenia. V literatúre sa ale popisuje aj periférna embolizácia nádorových hmôt do končatinových tepien vedúca k akútnej končatinovej ischémii a táto etiológia, hoci raritná, by nemala byť opomenutá cievnym chirurgom a angiológom pri manažmente pacienta s akútnou končatinovou ischémiou.
Konflikt záujmov
Autori článku vyhlasujú, že nie sú v súvislosti so vznikom tohto článku v konflikte záujmov a že tento článok nebol publikovaný v žiadnom inom časopise.
MUDr. Jana Pobehová, PhD.
Klinika cievnej chirurgie LF UPJŠ a VÚSCH, a.s.,
Ondavská 8
040 11 Košice
e-mail: jana.pastvova@post.cz
Sources
1. Štvrtinová V, Choroby ciev. Bratislava, SAP 2008 : 896.
2. Cronenwett J, Johnston KW. Rutherford´s vascular surgery. 6th ed., Saunders 2005 : 5678−86.
3. Becquemin J, Kovarsky S. Arterial emboli of the lower limbs: Analysis of risk factors for mortality and amputation. Ann Vasc Surg 1995;9 : 32.
4. Jivegard L, Holm J, Schersten T. Acute limb ischemia due to arterial embolism or thrombosis: influence of limb ischemia versus pre-existing cardiac disease on postoperative mortality rate. J Cardiovasc Surg (Torino) 1988;29 : 32−6.
5. Abbott W, Maloney R, McCabe C, et al. Arterial embolism: A 44-year perspective. Am J Surg 1982;143 : 460.
6. Eason J, Mills J, Beckett W. Hypercoagulable states in arterial thromboembolism. Surg Gynecol Obstet 1992;174 : 211.
7. Čertík B. Akutní končetinová ischemie. Praha, Grada Publishing 2003 : 147.
8. Karetova M, Staněk J. Angiologie pro praxi. Praha, Maxdorf Jessenius 2001 : 311.
9. Straus R, Merliss R. Primary tumor of the heart. Arch Pathol 1945;39 : 74–8.
10. Neragi-Miandoab S, Kim J, Vlahakes GJ. Malignant tumours of the heart: A review of tumour type, diagnosis and therapy. Clin Oncol 2007;19 : 748−56.
11. Burke AP, Cowan D, Virmani R. Primary sarcomas of the heart. Cancer 1992;69 : 387–95.
12. McAllister H, Fenoglio J. Atlas of tumor pathology. 2nd series. Fascicle 15 American Registry of Pathology/Armed Forces Institute of Pathology, Washington, D.C. 1978 : 1–3.
13. Yu K, Liu Y, Wang H, et al. Epidemiological and pathological characteristics of cardiac tumors: A clinical study of 242 cases. Interact Cardiovasc Thorac Surg 2007;6 : 636–9.
14. Crawford ES, Crawford JL. Diseases of the Aorta. Baltimore/London, Williams & Wilkins 1984 : 450−66.
15. Tejada E, Becker GJ, et al. Malignant myxoid emboli as the presenting feature of primary sarcoma of the aorta (Myxoid malignant fibrous histiocytoma): A case report and review of the literature. Clin Cardiol 1991;14 : 425−30.
16. Schmid E, Port SJ, Carroll RM, et al. Primary metastazing aortic endothelioma. Cancer 1984;54 : 1407−11.
17. Chen KTK. Primary malignant fibrous histiocytorna of the aorta. Cancer 1981;48 : 840−4.
18. Kattus AA, Longmire WP, Cannon, et al. Primary intraluminal tumor of the aorta producing malignant hypertension. Successful surgical removal. N Engl J Med 1960;262 : 694−700.
19. Kimbrell OC, Kaasa LJ. Primary intraluminal aortic myxoma with involvement of several vertebrae. J Am Med Assoc 1973;226 : 350−460.
20. Karhoff B. Primärtumor der Aorta. Zentralblatt für Allgemeine Pathologie und Pathologische Anatomie 1952 : 46−89.
21. Smeloff EA, Recce JM, Masters JH. Primary inlraluminal malignant tumor of the aorta. Am J Cardiol 1965;15 : 107−10.
22. Zeitlhofer J, Holzner JH, Krepler P. Primäres Fibromyxosarkom der Aorta. Krebsarzt 1963;18 : 259−69.
23. Weinberg DS, Maini BS. Primary sarcoma of the aorta associated with a vascular prosthesis: A case report. Cancer 1980;46 : 398−402.
24. Wright EP, Virmani R, Glick AD, et al. Aortic intimal sarcoma with embolic metastases. Am Surg Pathol 1985;9 : 890−7.
25. Oh SJ, Yeom SY, Kim KH. Clinical implication of surgical resection for the rare cardiac tumors involving heart and great vessels. J Korean Med Sci 2013;28 : 717–24.
26. Hsieh SC, Chen CY, Chan WP. Malignant fibrous histiocytoma of the heart: A case report. Acta Cardiol 2010;65 : 85–7.
27. Sheikh AA, Ahmad M, Lone AR, et al. Cardiac metastasis in malignant fibrous histiocytoma. Saudi Med J 2008;29 : 1041–3.
28. Milicic D, Juretic, A, Bulum, J, et al. Primary malignant fibrous histiocytoma of the heart with skeletal muscles metastases. J Card Surg 2007;22 : 513–6.
29. Pimentel J, Fernandes AC, Silva R, et al. Brain metastases of a malignant fibrous histiocytoma presenting as an acute cerebral hemorrhage. Clin Neuropathol 2001;20 : 64–9.
30. Bakaeen FG, Reardon MJ, Coselli JS, et al. Surgical outcome in 85 patients with primary cardiac tumors. Am Surg 2003;186 : 641–7.
31. Sun J, Liu R, Wang W, et al. Primary cardiac malignant fibrous histiocytoma with vulvar metastases: A case report. Oncology Letters 2015;10 : 3153−6.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2017 Issue 5-
All articles in this issue
- Malignant fibrous histiocytoma as a rare cause of acute limb ischemia
- Thoracoscopic, epicardial ablation of atrial fibrillation using the COBRA Fusion system as the first part of hybrid ablation
- Autologous cranioplasty with a bone flap preserved subcutaneously in the mesogastrium
- Combined treatment of early tracheobronchopleural fistula after right tracheal sleeve pneumonectomy
- Leiomyoma of external iliac vein
- Current possibilities to influence surgical site infection
- Colorectal cancer in senior patients – are we doing it well?
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Autologous cranioplasty with a bone flap preserved subcutaneously in the mesogastrium
- Current possibilities to influence surgical site infection
- Malignant fibrous histiocytoma as a rare cause of acute limb ischemia
- Thoracoscopic, epicardial ablation of atrial fibrillation using the COBRA Fusion system as the first part of hybrid ablation
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

