-
Medical journals
- Career
Hrudní drenážní systémy a komplikace s drenáží spojené
: T. Bohanes; M. Szkorupa
: I. chirurgická klinika LF UP a FN Olomouc, přednosta: doc. MUDr. Č. Neoral, CSc.
: Rozhl. Chir., 2013, roč. 92, č. 11, s. 672-678.
: Various Specialization
Práce je určena k postgraduálnímu vzdělávání lékařů.
Úvod:
Součástí hrudní drenáže je připojení drénu na některý ze systémů hrudní drenáže. Hrudní drenáž může být přitom spojena s určitými specifickými komplikacemi.Cíl:
Cílem práce je přehledně vysvětlit rozdělení a principy jednotlivých systémů hrudní drenáže, které můžeme rozdělit na pasivní (chlopňové systémy a vodní zámek) a aktivní hrudní sání. Zvláštní metodou je balancovaná hrudní drenáž. Dále práce pojednává o nejčastějších komplikacích při hrudní drenáži, kterými jsou protrahovaný vzduchový únik, multifaktoriální plicní edémy, fibrilace síní a empyém pohrudniční dutiny.Závěr:
Volba vhodného drenážního systému je významným faktorem úspěšnosti hrudní drenáže včetně pravděpodobnosti výskytu komplikací. Znalost vhodných postupů řešení komplikací hrudní drenáže, včetně užití i případně méně standardních postupů, umožňuje řešit i značně komplikované stavy.Klíčová slova:
hrudní drenáž – hrudní drén – pneumothorax – hrudní sání – protrahovaný vzduchový únik – plicní edém – reexpanzní plicní edém – podtlakový plicní edémÚvod
Zavedený hrudní drén není možné nechat otevřený. Výjimkou je pouze tenzní pneumotorax, nemáme-li k dispozici vodní zámek nebo Heimlichovu chlopeň. Jak vyplývá z patofyziologie a logiky věci, v důsledku dýchacích pohybů hrudníku by docházelo otevřeným drénem k nasávání vzduchu do pohrudniční dutiny. To by pochopitelně za normálních okolností vedlo k vzniku otevřeného pneumothoraxu s kolapsem plíce, v případě fixace plíce srůsty nebo stavu po pneumonektomii pak minimálně k riziku kontaminace drénované dutiny mikroorganismy zvenčí. Právě vyřešení problematiky drenážního systému Bülauem v roce 1875 [1] otevřelo brány pro intervence v hrudníku, protože do té doby právě výše zmíněné problémy drenáž hrudníku v podstatě znemožňovaly.
Drenážní systémy
Drenážním systémem u hrudní drenáže rozumíme jakékoliv zařízení připojené na hrudní drén, které zabraňuje proudění vzduchu zvenčí do drénu, a tedy do pohrudniční dutiny, aniž přitom zamezuje proudění vzduchu a tekutiny z pohrudniční dutiny ven. Tento systém pak může být pouhou jednosměrnou záklopkou (chlopní), pasivním drenážním systémem s vodním zámkem nebo systémem, využívajícím aktivní sání. Zvláštním typem pasivního systému je pak ještě tzv. balancovaná drenáž.
Pasivní systém s vodním zámkem
Prototypem pasivní drenáže v hrudní chirurgii je systém vodního zámku nebo též Bülauova drenáž. Zde je vzduch a tekutina z pohrudniční dutiny vypuzována při zvýšeném intrapleurálním tlaku v expiriu do drenážního systému. Aby nedošlo k návratu obsahu drénu zpět do pohrudniční dutiny, prochází drén přes tzv. vodní zámek. Ten tvoří láhev, otevřená navenek, kde je konec drénu jdoucí od pacienta, ponořen 2–3 cm pod úroveň hladiny tekutiny v láhvi (jde o sterilní vodu, případně roztok dezinfekční látky) (Obr. 1). Přetlak v pohrudniční dutině, který převýší odpor vodního zámku, tedy ony 2–3 cm vodního sloupce), způsobí únik vzduchu do láhve a z ní navenek. Tekutina odtéká do drenážní láhve. Při inspiriu dochází pak pouze k nasávání sterilní tekutiny z láhve do drénu, takže do pohrudniční dutiny nemůže proniknout potenciálně kontaminovaný vzduch z okolí. Láhev musí být umístěna pod úrovní lůžka nemocného, čímž dochází rovněž k zapojení gravitace. Při zvednutí láhve nad úroveň lůžka by naproti tomu hrozilo nasátí tekutiny z láhve do pohrudniční dutiny.
1. Bülauova drenáž (drenážní systém s vodním zámkem) Fig. 1: Bülau drainage (water seal drainage system) 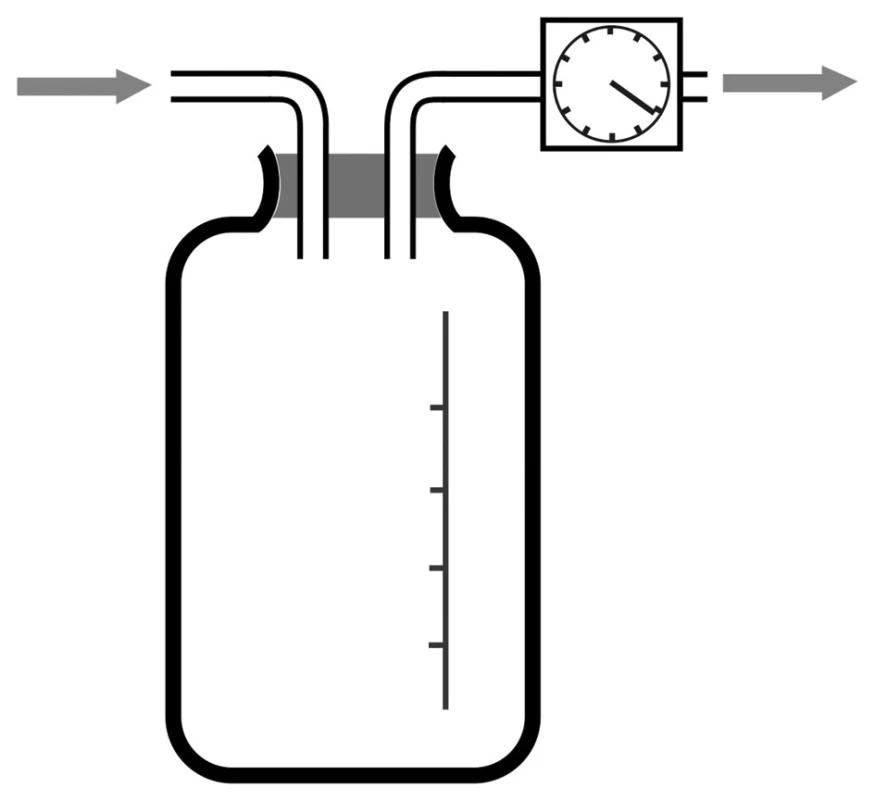
Tento typ drenáže je základním drenážním systémem užívaným po pneumonektomii, kde je nepřípustné užití aktivního drenážního systému s hrudním sáním, lze jej ale využít i u nekomplikovaných pneumothoraxů či jednoduchých plicních resekcí. Hlavním nebezpečím tohoto systému v základním uspořádání je to, že hromadění tekutiny vytékající z hrudníku v láhvi zvyšuje hloubku ponoření přívodné části drénu. Tím narůstá odpor, který vodní zámek klade, a může dojít k situaci, že drenáž přestane být pro velký odpor účinná. V takovém případě je vhodné vložit před láhev s vodním zámkem ještě jednu sběrnou láhev, která je určena pouze pro sběr tekutiny.
Pasivní chlopňové systémy
Prototypem tohoto rovněž pasivního drenážního systému je Heimlichova chlopeň. Je pojmenována po americkém chirurgovi Henrym Jay Heimlichovi, který její použití popsal v roce 1968 [2]. Funkčně jde o jednocestný ventil tvořený gumovou chlopní, která je umístěna uvnitř průhledné plastové trubice napojené na sběrný sáček (Obr. 2). Takto může proudit vzduch a tekutina z pohrudniční dutiny navenek, ale chlopeň zabraňuje zpětnému nasátí do drénu. Méně dokonalou chlopeň si můžeme snadno zhotovit z ustřiženého prstu rukavice s malým otvorem, fixovaného ligaturou k hrudnímu drénu. Jako chlopeň funguje tento systém stejně dokonale, ale neumožňuje pochopitelně jímat tekutinu jdoucí z hrudníku (Obr. 3).
2. Heimlichova chlopeň Fig. 2: Heimlich valve 
3. Princip funkce Heimlichovy chlopně a) výdech – vzduch uniká otvorem blízko vrcholu chlopně; b) nádech – podtlak způsobí kolaps chlopně, a tedy uzavření otvoru. Fig. 3: Principle of the Heimlich valve a) expiration – air goes out through a small opening near the valve top, b) inspiration – the negative pressure causes the collapse of the valve and occlusion. 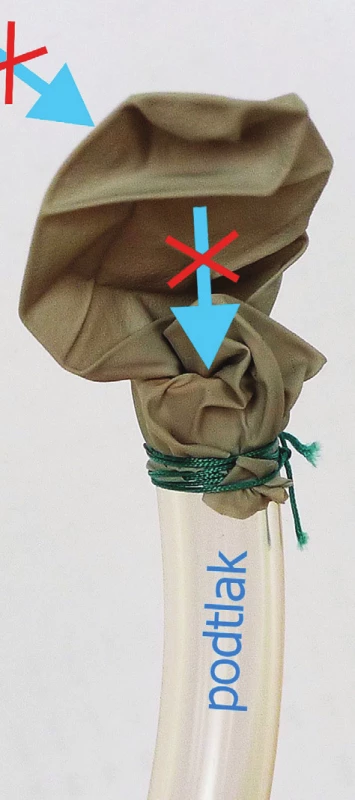
Heimlichova chlopeň umožňuje ambulantní léčbu i u nemocných s prolongovaným vzduchovým únikem, většinou se dnes užívají různé firemní modifikace, jako např. Pneumostat™. Ten má i malou komůrku umožňující sběr drénovaného výpotku. Nevýhodou těchto systémů je relativně vyšší cena, než by odpovídalo jednoduchosti řešení.
Aktivní drenážní systémy
V řadě případů výše uvedené pasivní systémy nejsou dostatečné k dosažení reexpanze plíce a je třeba využít aktivní sání. V tomto případě připojujeme hrudní drén na sběrnou láhev, v níž vytváří podtlak mechanická pumpa (obvykle je láhev napojena na centrální sání), úroveň podtlaku v systému nastavujeme manometrem (Obr. 4). V klasickém (a zároveň i bezpečnějším) provedení se ovšem aktivní drenážní systém sestavuje jako dvou - nebo třílahvový systém, kdy je mezi drén a manometr vložen ještě systém několika láhví s definovanou funkcí (Obr. 5a,b). První láhví v systému může být sběrná láhev, avšak ve dvoulahvovém systému tato chybí. Následuje láhev s funkcí vodního zámku (podobně jako u Bülaovy drenáže, zaručuje tedy, že i při odpojení zdroje sání nemůže dojít k nasávání okolního vzduchu do pohrudniční dutiny). Třetí láhev má funkci regulace maximálního podtlaku. Podle hloubky ponoření trubičky vycházející navenek dojde při překročení odporu vodního sloupce v trubičce k nasávání vzduchu zvenčí a tím ke snížení podtlaku v systému. Můžeme tedy mít na manometru nastavenu jakkoliv vysokou hodnotu podtlaku. Jeho úroveň v systému, a tedy i v pohrudniční dutině, je určena pouze hloubkou zanoření této regulační trubičky, protože při překročení nastaveného tlaku dochází k probublávání vzduchu v této třetí láhvi a redukci podtlaku v systému. Probublávání vzduchu v láhvi zároveň indikuje správnou regulační funkci systému.
4. Nejjednodušší systém pro hrudní sání – sběrná láhev a manometr pro nastavení úrovně podtlaku Fig. 4: The simplest system for chest suction – collection bottle and manometer for setting the negative pressure level 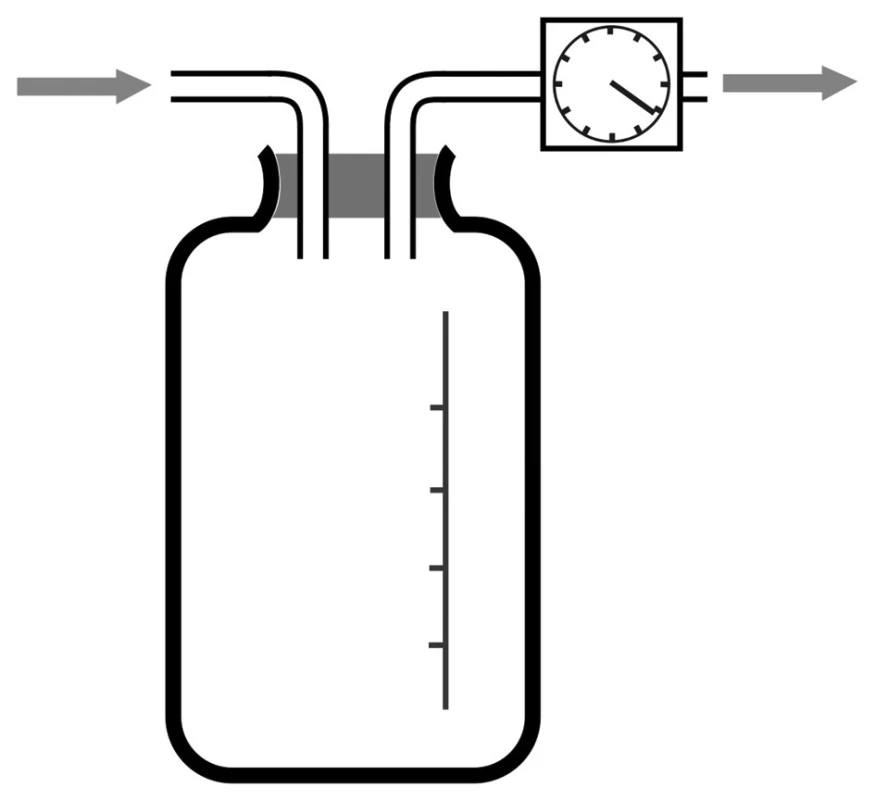
5. Vícelahvový systém pro hrudní sání a) dvoulahvový systém; b) třílahvový systém. Fig. 5: Multi-bottle system for chest suction a) two-bottle system ;b) three-bottle system. 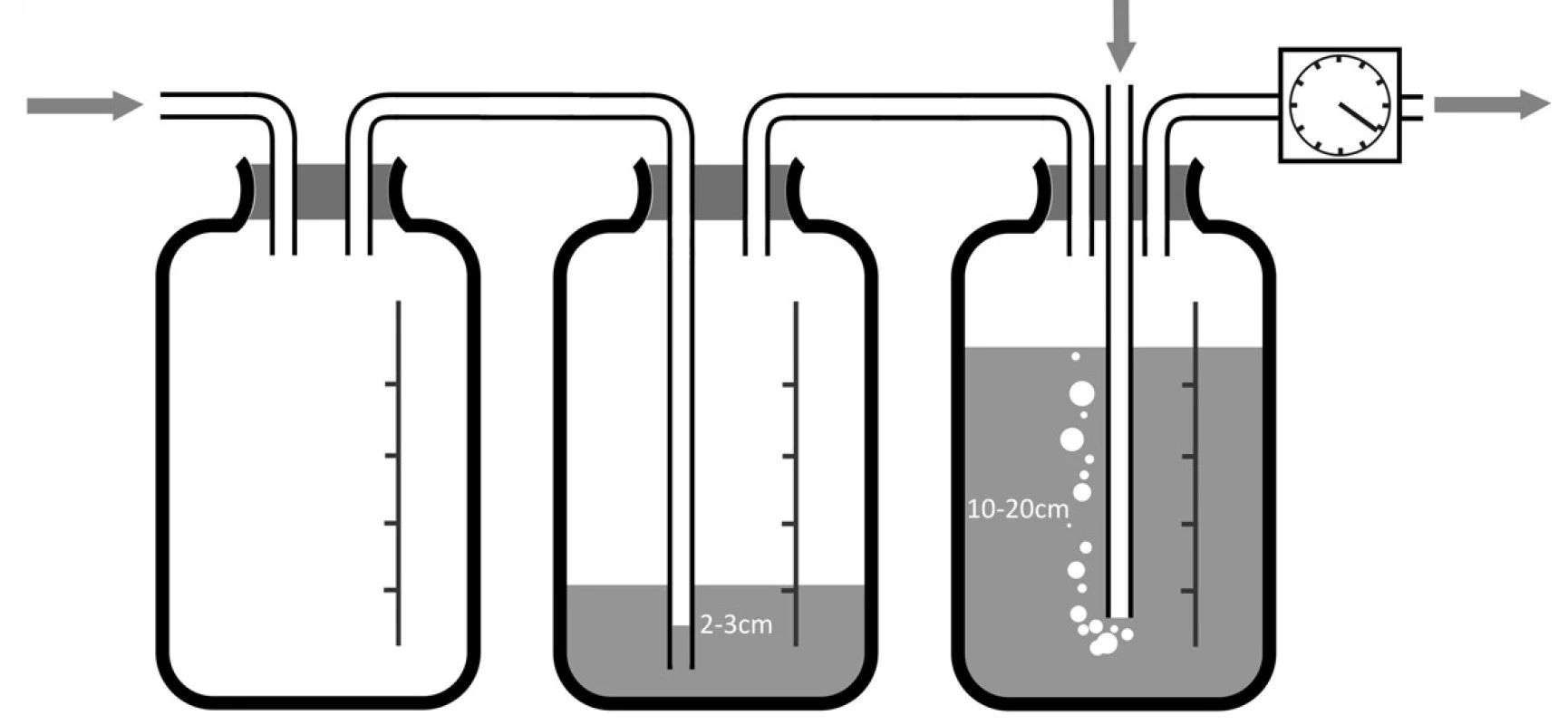
V moderní době jsou výše uvedené dvoj - či třílahvové systémy integrovány do jednorázových krabicových systémů, v nichž jsou jednotlivé láhve transformovány do komůrek se stejnou funkcí. Tyto systémy jsou z hlediska obsluhy a hygienického hlediska mnohem vhodnější než systémy lahvové, nevýhodou je ovšem poměrně vyšší cena. Určitou výhodou těchto systémů bývá i integrovaný průtokoměr vzduchu systémem, který orientačně umožňuje kvantifikovat úroveň vzduchového úniku skrze systém na stupnici 1..x, což je o něco přesnější než „bublemetrie“ pouhým okem podle množství bublin procházejících hadicemi drenážního systému (Obr. 6).
6. Krabicový systém pro hrudní sání (zde Atrium Oasis ™) Fig. 6: Water seal box system (Atrium Oasis™ in this case) 
Nejpokročilejším systémem jsou dnes přenosné osobní pumpy, jež fungují na stejném principu jako svrchu popsaný systém tvořený zdrojem sání, manometrem a sběrnou nádobou. Tyto přístroje (Medela Thopaz™, Atmos Thorax™ aj.) poskytují při zachování aktivnosti systému plnou mobilitu díky bateriím s několikahodinovou možností na síti nezávislého provozu. Funkčnost systému je hlídána jednoduchým počítačem, který je schopen analyzovat provoz systému a vyhlásit alarm v případě jakéhokoliv problému. Významnou výhodou systémů je rovněž integrovaný průtokoměr, který umožňuje kvantifikovat zcela přesně v ml/min velikost vzduchového úniku včetně uložení historie a možnosti grafického vyjádření, všechna data mohou být přenesena do PC a tam dále zpracovávána. Tyto pumpy jsou do jisté míry limitovány co do dosažitelného podtlaku a vzduchového průtoku, nicméně stačí pro naprostou většinu nemocných po hrudní drenáži, především se vzduchovým únikem (větší odpady tekutiny jsou pro jejich nasazení méně vhodné, ale to především z finančních důvodů pro cenu a relativně malý objem sběrných nádob). Vstupní pořizovací náklady na přístroj jsou pochopitelně vyšší, vlastní provozní režie je pak ale přijatelná.
7. Přenosná pumpa pro hrudní sání Medela Topaz™ v provozní pozici na JIP lůžku Fig. 7: The Medela Topaz™ mobile chest suction pump in the operating position with an ICU bed 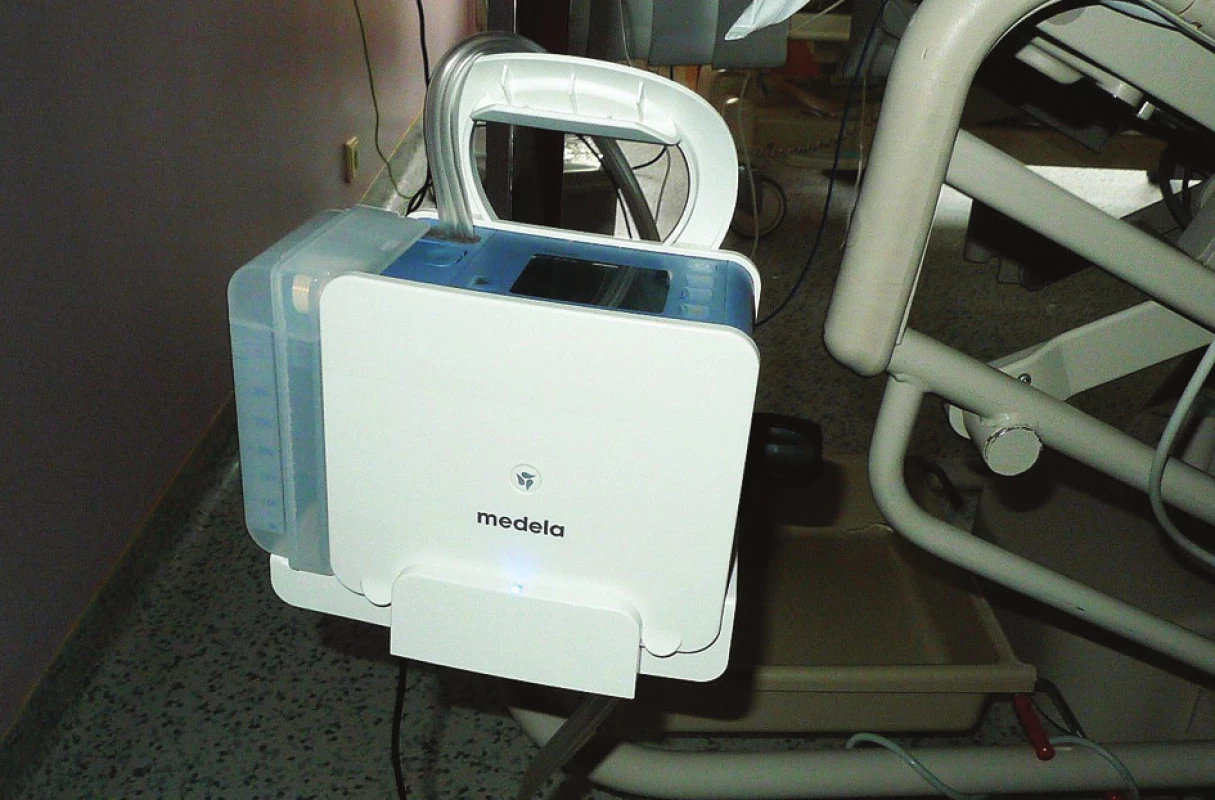
Balancovaná drenáž
Jde o zvláštní typ pasivní drenáže, uplatňovaný především u pacientů po pneumonektomii. Poprvé byla publikována Laforetem a Boydem v roce 1964 [3]. Výhodou této metody je, že napomáhá udržet tlakové poměry v pleurální dutině v poměrně fyziologickém rozmezí (dle nastavení např. -13 až +1cm H2O). To napomáhá udržovat fyziologické postavení mediastina. Důležité je, že uvedené rozmezí tlaku v pohrudniční dutině je udržováno automaticky. Systém využívá tří nádob (nebo komůrek ve firemním krabicovém systému) (Obr. 8), kdy první láhev je sběrná, druhá má funkci vodního zámku a třetí slouží k regulaci podtlaku podobně jako v případě systému s aktivním sáním. V okamžiku, kdy podtlak v pohrudniční dutině překročí nastavenou hodnotu, tj. kdy zároveň dochází k přetahování mediastina na operovanou stranu se všemi negativními důsledky, dojde k nasátí vzduchu z vnějšího prostředí do systému. To vede ke zvýšení tlaku v pohrudniční dutině a úpravě postavení mediastina. Nevýhodou je riziko kontaminace systému a pleurální dutiny, jakkoliv toto riziko patrně není velké, zvláště při použití filtrů na vstupu. Některými autory bývá tato metoda drenáže favorizována, mimo jiné pro snížené riziko postpneumonektomického plicního edému [4,5,6,7,8], avšak i u pacientů po pneumonektomiích převažuje spíše užívání Bülauovy drenáže s důrazem na časné odstranění drénu [9].
8. Systém pro balancovanou drenáž Fig. 8: Balanced drainage system 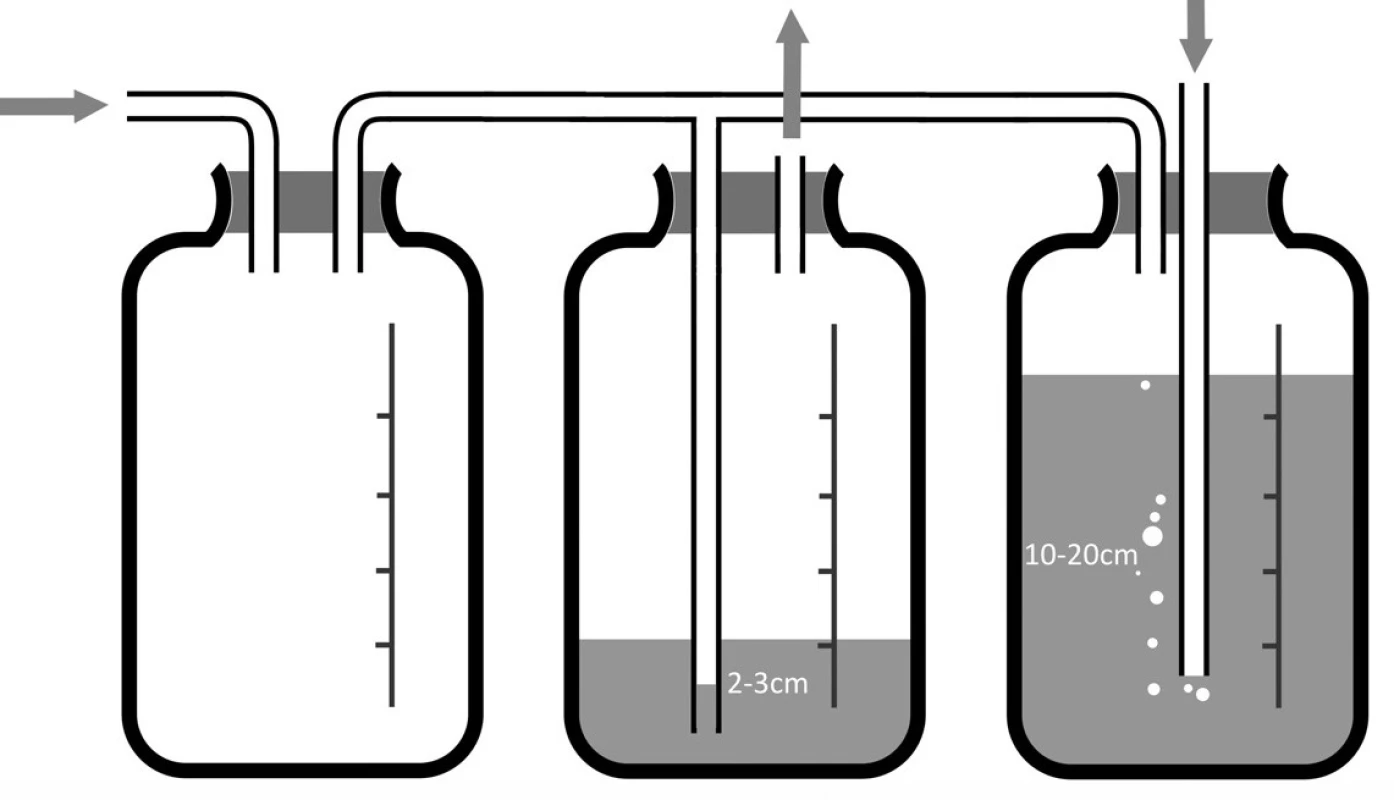
Úroveň podtlaku užívaná v aktivních drenážních systémech
Obvykle doporučované rozmezí podtlaku pro aktivní drenážní systémy bývá 10–20 cm H2O [9] s maximální hodnotou v případě nedostatečné reinflace plíce až 30 cm H2O. Vyšší hodnoty podtlaku se obvykle považují za nebezpečné pro riziko sáním vyvolané redistribuce tekutiny v plících a vzniku unilaterálního podtlakového edému. Některé krabicové drenážní systémy tak povolují maximální hodnotu podtlaku 40 cm H2O. Na druhou stranu například přenosné osobní pumpy, představující nejpokročilejší systémy pro hrudní drenáž, umožňují nastavit podtlaky značně větší, např. Medela Thopaz™ až 100 cm H2O. Na pracovišti autorů bývaly dokonce v minulosti rutinně užívány podtlaky 100–200 cm H2O, ve vybraných speciálních indikacích až 300 cm H2O, aniž to způsobilo zásadní komplikace. V zásadě lze zkušenosti shrnout tak, že i tyto vyšší podtlaky jsou bezpečné. Jakkoliv k určité redistribuci tekutin až mírné formě edému (dle hodnocení RTG dokumentace) docházelo asi u 15 % pacientů ze skupiny nemocných po plicních resekcích, klinicky signifikantní projevy unilaterálního edému byly zaznamenány pouze u 0,5 % nemocných. Ve všech těchto případech mohla být ovšem etiologie edému podstatně komplexnější a nelze ji jednoznačně svádět na použití vyšších podtlaků (viz níže). Přesto lze pro běžné užívání v klinické praxi jednoznačně doporučit užívání rozmezí 10–20 cm H2O, které lze považovat obecně za bezpečné i bez kontinuální monitorace fyziologických funkcí, jež je jednoznačně vhodná v případech potřeby použití vyšších podtlaků.
Komplikace hrudní drenáže
Zatímco komplikace spojené se zavedením hrudního drénu jsou popsány v předchozím příspěvku, tato část pojednává o komplikacích spojených s déletrvající hrudní drenáží. Je třeba zdůraznit, že detailní popis problematiky komplikací hrudní drenáže by vydal na samostatný článek, a je tedy nutné z prostorových důvodů tyto komplikace probrat jen v krátkosti. Autorům nezbývá než zájem čtenáře o hlubší proniknutí do této problematiky odkázat na další literaturu.
Protrahovaný vzduchový únik a pneumothorax
Protrahovaný vzduchový únik lze definovat jako pokračující vzduchový únik trvající delší dobu, než je pro daný stav obvyklé. Po resekčních výkonech na plíci se za protrahovaný vzduchový únik považuje jeho trvání 7 a více dnů [10]. Často se protrahovaný vzduchový únik vyskytuje zároveň s pneumothoraxem, tj. v situaci, kdy nedojde ke kompletní reexpanzi plíce, jelikož oba patologické stavy mají vzájemnou souvislost. Při dosažení reexpanze dojde k uzavření a zalepení otvorů v plicním parenchymu díky kontaktu s nástěnnou pleurou a tak zároveň vymizí vzduchový únik.
Prvním opatřením, které je třeba udělat, je vyloučit možnost přisávání vzduchu podél drénu zvenčí. K tomu může dojít zejména při drénu zavedeném nedostatečně hluboko (někdy může být dokonce poslední otvor drénu již v hrudní stěně) a při příliš široké incizi pro drén v hrudní stěně. V této situaci lze někdy zasunout drén hlouběji, popřípadě stehem utěsnit otvor v kůži kolem drénu, ale často se problém manipulací s drénem vyřešit nepodaří. Pak je nutná extrakce drénu a případně redrenáž.
Pokud není plíce plně reexpandována, je třeba se zaměřit na reexpanzi plíce. Zde může pomoci zvýšení podtlaku v sání, čímž plicní parenchym aktivně táhneme k hrudní stěně. Dalším podpůrným prvkem terapie je dechová rehabilitace, především různé cviky s dýcháním proti odporu, což rovněž napomáhá k reexpanzi plíce jejím nafukováním. Na tomto místě je třeba poznamenat, že tyto metody mohou na druhou stranu zvýrazňovat a prodlužovat trvání vzduchového úniku. Podle našich zkušeností je v tomto případě ale prioritní dosažení reexpanze plíce.
Pokud trvá vzduchový únik v případě reexpandované plíce, pak je možné potencovat tvorbu srůstů mezi viscerálním a parietálním listem pleury za pomoci některé metody k vyvolání pleurodézy. Obecně lze doporučit a je v poslední době používána především aplikace autologní krve do pleurální dutiny [9,11] nebo 40% roztoku glukózy. Glukóza je s velkým úspěchem používána na pracovišti autorů. Je třeba varovat před použitím talkové pleurodézy. Talek má jistě svoje nezastupitelné místo mezi metodami pleurodézy v případě maligních výpotků, ale v případě perzistující alveolo-pleurální píštěle není jeho použití vhodné pro riziko aspirace z pleurálního prostoru. Taková aspirace je nepříjemná v případě krve či glukózy, avšak v případě talku by mohla patrně skončit i fatálně.
Plicní edém
Plicní edém je poměrně vzácnou, nicméně potenciálně poměrně závažnou komplikací doprovázející hrudní drenáž. Nejde vždy o komplikaci drenáže samotné, jelikož poškození plíce, které edém vyvolává, vzniká obvykle ještě v období před nasazením hrudní drenáže. Jde především o edémy vzniklé na podkladě ischemicko-reperfuzního poškození plíce při selektivních ventilacích, kde dochází k poškození endotelu na podkladě ischemie v kolabované plíci, alveolární distenze při vysokoobjemové plicní ventilaci, toxického efektu kyslíku. Poškození plíce pak bývá označováno jako akutní trauma plic (ALI/ARDS) a mívá vysokou závažnost [9,12].
Jednoznačným důsledkem hrudní drenáže není ani reexpanzní plicní edém (RPE), což je unilaterální edém vzácně komplikující hrudní drenáž, při níž se snažíme dosáhnout reexpanze dlouhodobě kolabované plíce při PNO, atelektáze či fluidothoraxu. Incidence RPE je nízká, jelikož v řadě velkých studií, zabývajících se řešením spontánního PNO, nebyl RPE vůbec zaznamenán [13], nicméně RPE je komplikací závažnou s mortalitou až 20 %. Rizikovými faktory jsou zejména věk (čím mladší pacient, tím vyšší riziko), ženské pohlaví, velikost kolapsu plíce, kolaps trvající déle než 24 hodin, rychlá reexpanze plíce do 10 minut a evakuace více než 2000 ml výpotku. Projevy jsou zejména kašel, případně tachykardie, hypotenze, nauzea, zvracení a cyanóza. Většinou se přitom RPE vyvíjí v první hodině reexpanze [14]. Etiologie je patrně rovněž v poškození endotelu s jeho následnou zvýšenou permeabilitou během ischemicko-reperfuzního poranění plíce [15]. Prevencí této potenciálně závažné komplikace může být pomalá reexpanze plíce, což sice nemusí určitému edému zabránit, ale minimálně sníží závažnost projevů. V kontextu výše uváděných rizikových faktorů na pracovišti autorů prodlužujeme reexpanzi rizikové plíce (tj. velký kolaps dlouhotrvající) až na 4 hodiny (např. evakuace výpotku po 500 ml za hodinu).
Jako důsledek hrudní drenáže s aktivním sáním lze jednoznačně označit pouze podtlakový plicní edém (NPPE). Ten se obecně popisuje jako důsledek excesivního odsávání z dýchacích cest (při bronchoskopii, odsávání katétrem z plic tracheostomií či endotracheální kanylou), pak se může jednat i o oboustranný edém. Vyskytuje se zvláště v případech parciální obstrukce dýchacích cest (stenóza, hlenové zátky), která ztěžuje vyrovnání tlaku s atmosférickým tlakem. Byl avšak popsán i jeho výskyt unilaterálně ve vazbě na hrudní drenáž [16], čemuž odpovídá i zkušenost autorů z výskytu radiologických známek edému u pacientů po resekcích, kteří byli vystaveni vyšším podtlakům při hrudním sání. Z fyziologického pohledu lze edém snadno vysvětlit porušenou rovnováhou na kapilární membráně, která vede ke zvýšenému kapilárnímu leaku. Edém je ale i při vystavení vysokým podtlakům zpravidla klinicky nevýznamný, jde jen o vedlejší radiologický nález, který radiologové obvykle popisují jako perzistující fluidothorax. Porovnáním vývoje RTG obrazu a odpadu z drénu lze ale usoudit na jinou povahu zastínění hemithoraxu na straně drénu a po zrušení sání nebo snížení podtlaku dochází k vyčištění snímku. Z toho lze usuzovat na zásadní podíl sání na vzniku takového obrazu. Závažnost této poruchy tekutinové rovnováhy v plicích pak spočívá pouze v možnosti její kombinace s některým z výše uvedených edémů. Tím dojde ke zhoršení už tak potenciálně závažného stavu nemocného.
Fibrilace síní
Fibrilace síní (FS) se vyskytuje v nízkém procentu u nemocných po hrudní drenáži či menších výkonech na plíci do rozsahu subsegmentální resekce. Naproti tomu její výskyt stoupá u pacientů po anatomické plicní resekci počínaje lobektomií, kde se uvádí výskyt 12,5–46 %. Obvykle k ní dochází mezi 2.–3. pooperačním dnem a trvá 4–18 hodin. Ve třetině případů dochází po verzi na sinusový rytmus v průběhu dvou dnů k rekurenci [9]. Existují pochopitelně pacienti, kteří jsou ke vzniku FS náchylnější, rizikovými faktory jsou věk nad 60 let, mužské pohlaví, hypertenze, ICHS a FS v anamnéze [17]. Porovnání incidence FS 6,1 % po abdominálních operacích s 20 % po plicních výkonech [9] ukazuje ale, že rizikové faktory jsou méně podstatné a příčina je v samotném hrudníku. Tou je patrně vlastní intervence v oblasti srdce a plicních žil, kdy se může vyskytovat ektopická aktivita v oblasti ústí plicních žil [9]. FS může způsobovat i jiná iritace v oblasti hrudníku a mediastina, například dráždění myokardu tlakem hrudního drénu nebo v důsledku tlakové nestability mediastina při hrudním sání.
V terapii se uplatňují s dobrým efektem antiarytmika, zejména amiodaron či propafenon. Alternativou k jimi vyvolané kardioverzi je kontrola srdeční frekvence pomocí dioxinu, betablokátorů, diltiazemu či verapamilu [9].
Empyém
Možnost sekundární kontaminace pleurální dutiny cestou drénu je spíše vzácnou komplikací hrudní drenáže. Jak vyplývá z předchozího textu, v zásadě by k ní v případě správného managementu hrudní drenáže nemělo dojít. Pouze při použití balancované drenáže (viz výše) nelze z principu metody tuto komplikaci ani při správném použití zcela vyloučit. Na druhou stranu rovněž nelze zcela vyloučit kontaminaci šířící se podél drénu. Dalším rizikovým faktorem pro vznik empyému jsou všechny případy, při nichž dochází k proplachům drénu, typicky při jeho ucpání nebo při aplikaci roztoku k dosažení pleurodéze drénem. Z tohoto důvodu je třeba všechny aplikace do drénu indikovat uvážlivě a zejména zprůchodňování drénu proplachy spíše vyloučit.
Pokud k této komplikaci dojde, terapie je analogická jako u hrudního empyému z jiné příčiny.
Závěr
Hrudní drenáž v rukou zkušeného odborníka je poměrně bezpečná a snadná metoda s velkým terapeutickým potenciálem při řešení nejrůznějších patologií pleurální dutiny. Z tohoto důvodu není třeba se jí bát, jakkoliv na druhou stranu je třeba její indikaci vždy citlivě a individuálně zvažovat s ohledem na porovnání přínosu a rizik. Je ovšem nesporné, že komplikovanější případy hrudních drenáží patří do rukou zkušeného hrudního chirurga, pro nějž je hrudní drenáž a péče o drénované pacienty denním chlebem a který je zběhlý i v řešení nejrůznějších mimořádných stavů a komplikací s drenáží spojených.
MUDr. Tomáš Bohanes, PhD.
I. chirurgická klinika LF UP a FN Olomouc
I. P. Pavlova 6
775 20 Olomouc
e-mail: tomas.bohanes@fnol.cz
Sources
1. Bülau H. Für die Heber-Drainage bei Behandlung des Empyems. Ztschr Klin Med 1891;18 : 31.
2. Heimlich HJ. Valve drainage of the pleural cavity. Dis Chest 1968;5 : 282–7.
3. Laforet EG, Boyd TF. Balanced drainage of the pneumonectomy space. Surg Gynecol Obstet 1964;118 : 1051–4.
4. da Rosa JF. Balanced drainage system. Ann Thorac Surg 1982; 34 : 477.
5. Bennett EV Jr. Balanced postpneumonectomy drainage systém. Ann Thorac Surg 1982;34 : 728–9.
6. Deslauriers J, Aucoin A, Grégoire J. Postpneumonectomy pulmonary edema. Chest Surg Clin N Am 1998; 8 : 611–31.
7. Deslauriers J, Grégoire J. Techniques of pneumonectomy. Drainage after pneumonectomy. Chest Surg Clin N Am 1999;9 : 437–8.
8. Alvarez JM, Tan J, Kejriwal N, et al. Idiopathic postpneumonectomy pulmonary edema: hyperinflation of the remaining lung is a potential etiologic factor, but the condition can be averted by balanced pleural drainage. J Thorac Cardiovasc Surg 2007;133 : 1439–47.
9. Stolz A, Pafko P, et al. Komplikace v plicní chirurgii. Praha, Grada Publishing 2010.
10. Stolz A, Schutzner J, Lischke R, et al. Predictors of prolonged air leak following pulmonary lobectomy. Eur J Cardiothorac Surg 2005;27 : 334–6.
11. Ozpolat B. Autologous blood patch pleurodesis in the management of prolonged air leak. Thorac Cardiovasc Surg 2010;58 : 52–4.
12. Timby J, Reed C, Zeilender S, Glauser FL. „Mechanical“ causes of pulmonary edema. Chest 1990;98 : 973–9.
13. Myšíková D, Šimonek J, Stolz A, Lischke R. Reexpanzní plicní edém po drenáži dlouhotrvajícího spontánního pneumothoraxu – kazuistika. Rozhl Chir 2013;92 : 333–6.
14. Mahfood S, Hix WR, Aaron BL, Blaes P, Watson DC. Reexpansion pulmonary edema. Ann Thorac Surg 1988;45 : 340–5.
15. Sivrikoz MC, Tuncozgur B, Cekman M, et al. The role of tissue reperfusion in the reexpansion injury of the lung. Eur J Cardiothorac Surg 2002;22 : 721–7.
16. Memtsoudis SG, Rosenberger P, Sadovnikoff N. Chest tube suction-associated unilateral negative pressure pulmonary edema in a lung transplant patient. Anesth Analg 2005;101 : 38–40.
17. Harpole DH, Decamp MM, Henderson WG, et al. Prognostic models of thirty-day mortality and morbidity after major pulmonary resection. J Thorac Cardiovasc Surg 1999;117 : 969–79.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2013 Issue 11-
All articles in this issue
- Multiple endocrine neoplasia type 1 syndrome with special emphasis on pancreatoduodenal tumours – a case report analysis
- Laparoscopic lavage and drainage in the management of acute diverticulitis: Is it time to move on?
- Reconstruction of complex abdominal wall defects using the component separation technique
- Minimally invasive video-assisted operations for heart disease
- Heparin-induced thrombocytopenia in a patient with acute thrombosis, acute aortic dissection and acute lower limb ischaemia
- Difficult differential diagnosis of malignant melanoma – case reports
- Chest drainage – physiological and pathophysiological aspects and indications
- Chest drainage methods
- Chest drainage systems and the complications associated with drainage.
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Chest drainage systems and the complications associated with drainage.
- Chest drainage methods
- Chest drainage – physiological and pathophysiological aspects and indications
- Reconstruction of complex abdominal wall defects using the component separation technique
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career



