-
Medical journals
- Career
Obnova aktivní extenze nohy při paréze peroneálních nervů
: P. Špiroch; I. Čižmář; J. Freiwald; J. Palčák
: Traumatologické oddělení FN Olomouc
: Rozhl. Chir., 2012, roč. 91, č. 3, s. 151-157.
: Original articles
Úvod:
Paréza nervus peroneus communis je nejčastější periferní obrnou postihující dolní končetinu. Jde o invalidizující postižení, kdy noha je ve flekčním a supinačním postavení a pacient není schopen aktivní extenze a pronace nohy, ani extenze prstů. Šlachový transfer, který obnovuje aktivní extenzi hlezna, je považován za metodu volby při paréze peroneálních nervů, pokud nedojde ke klinicky uspokojivé reinervaci.Materiál a metodika:
Do souboru bylo zařazeno 14 pacientů léčených na Traumatologickém oddělení FNO buď pro parézu společného či hlubokého peroneálního nervu, nebo pro izolovanou lézi předního tibiálního svalu. K obnovení pohybu byly využity aktivní svaly, a to v 13 případech zadní tibiální sval a v jednom případě dlouhý peroneální sval. Šlachy těchto svalů byly zakotveny na dorzum nohy.Výsledky:
U všech pacientů došlo k obnově aktivní extenze nohy, v průměru na 12,3° (4–20), s dostatečnou svalovou silou. Při hodnocení Stanmorovým skórovacím systémem bylo hodnocení vynikající, mezi 87–100 body.Závěr:
Při šlachovém transferu musculus tibialis posterior nebo musculus peroneus longus dochází k obnově aktivní extenze nohy. Důsledkem tohoto rekonstrukčního výkonu je lehké omezení celkové hybnosti hlezna. Funkčně výhodnější pro pacienta je provádět transfer s lehce větším předpětím, tak aby bylo dosaženo po operaci dostatečné extenze hlezna.Klíčová slova:
Peroneální paréza – šlachový transfer – šlacha tibialis posterior – equinovarózní deformita nohyÚvod
Paréza nervus (n.) peroneus communis je nejčastější monoparézou na dolní končetině [1]. Spontánní návrat funkce při peroneální paréze není příliš častý. Při revizi a sutuře nervu při jeho otevřeném poranění lze návrat funkce očekávat jen asi v 36 % případů [2, 3]. Pokud nedojde k obnově funkce postižených svalů, je jediným řešením obnovy aktivního pohybu šlachový transfer. Při šlachovém transferu se používá funkční, dobře inervovaný sval k náhradě funkce nefunkčního, většinou antagonistického svalu. Člověk má schopnost naučit se používat přenášený sval k opačnému pohybu, než ke kterému byl původně určen (flexor jako extenzor, abduktor jako adduktor atp.). V této práci hodnotíme funkční výsledek rekonstrukce extenze nohy náhradou funkčními flexory.
Celosvětově nejčastější příčinou peroneální parézy je lepra, leprózní neuritida [4, 5]. K postižení peroneálního nervu v tomto případě dochází v průběhu kolem hlavičky fibuly, proto vzniká paréza n. peroneus communis (NPC). Z dalších neúrazových příčin může být paréza peroneálních nervů již od dětského věku, při mozkových obrnách, při peroneálních svalových dystrofiích a atrofiích, spastických paraparézách, spina bifida a atypické svalové dystrofii, Friedreichově ataxii a při chorobě Charcot-Marie-Toothové [6]. Při úrazech dochází k poranění n. peroneus communis nejčastěji v průběhu kolem hlavičky fibuly, kdy může být přerušen při otevřených ranách, rozdrcení nebo při dlouhodobém tlaku u sníženě mobilních pacientů. Jeho poškození vzniká při zlomeninách proximální tibie a fibuly, při luxacích kolenního kloubu přímým tlakem kostních fragmentů nebo trakcí. Často je NPC poškozen ischemií při compartment syndromu bérce. Peroneální paréza vzniká také při luxacích kyčle a zlomeninách pánve, kdy peroneální část n. ischiadicus je vulnerabilnější než tibiální. Iatrogenně se paréza n. peroneus communis popisuje jako komplikace trakce za tuberositas tibiae, exstirpací ganglií nebo jiných tumorů v oblasti kolene a při operačních výkonech, jako jsou artroskopie kolene či operace varixů. Klinicky jako paréza n. peroneus communis se může projevit radikulopatie L5 při výhřezu meziobratlové ploténky L4/L5 a L5/S1 [3, 7, 8 , 9, 10].
Klinicky se paréza NPC projevuje flexí a supinací nohy (equinovarózním postavením), flekčním postavením prstů, které vzniká výpadkem extenze a tahem m. tibialis posterior (TP) s nemožností aktivní extenze a pronace hlezna [11]. Při poranění n. peroneus profundus (NPP) je jen flekční postavení nohy s nemožností aktivní extenze nohy a prstů, výpadkem funkce přední svalové skupiny svalů bérce. Pronaci zajišťují m. peroneus longus (PL) a m. peroneus brevis (PB). Při poškození n. peroneus superficialis (NPS) je noha ve varózní deformitě výpadkem funkce obou pronátorů nohy (PL a PB), extenzi zajišťuje funkční přední svalová skupina. Přepadávání nohy a prstů způsobuje poruchu chůze, tzv. čapí chůzi, kdy pacient vysoko zvedá kolena, aby nezakopával o flektovanou nohu a prsty. Ke kompenzaci lze použít ortézu, peroneální pásku, která udržuje hlezno v 90°.
Materiál a metodika
Soubor pacientů
Do studie byli zahrnuti pacienti s nemožností nebo omezením extenze nohy při paréze NPC, NPP a při izolované dysfunkci m. tibialis anterior (TA). Pro toto postižení bylo na Traumatologickém oddělení FN Olomouc operováno od září 2006 do prosince 2010 celkem 14 pacientů. Jednalo se o 4 ženy a 10 mužů (Tab. 1).
1. Data pacientů Tab. 1: Patient data 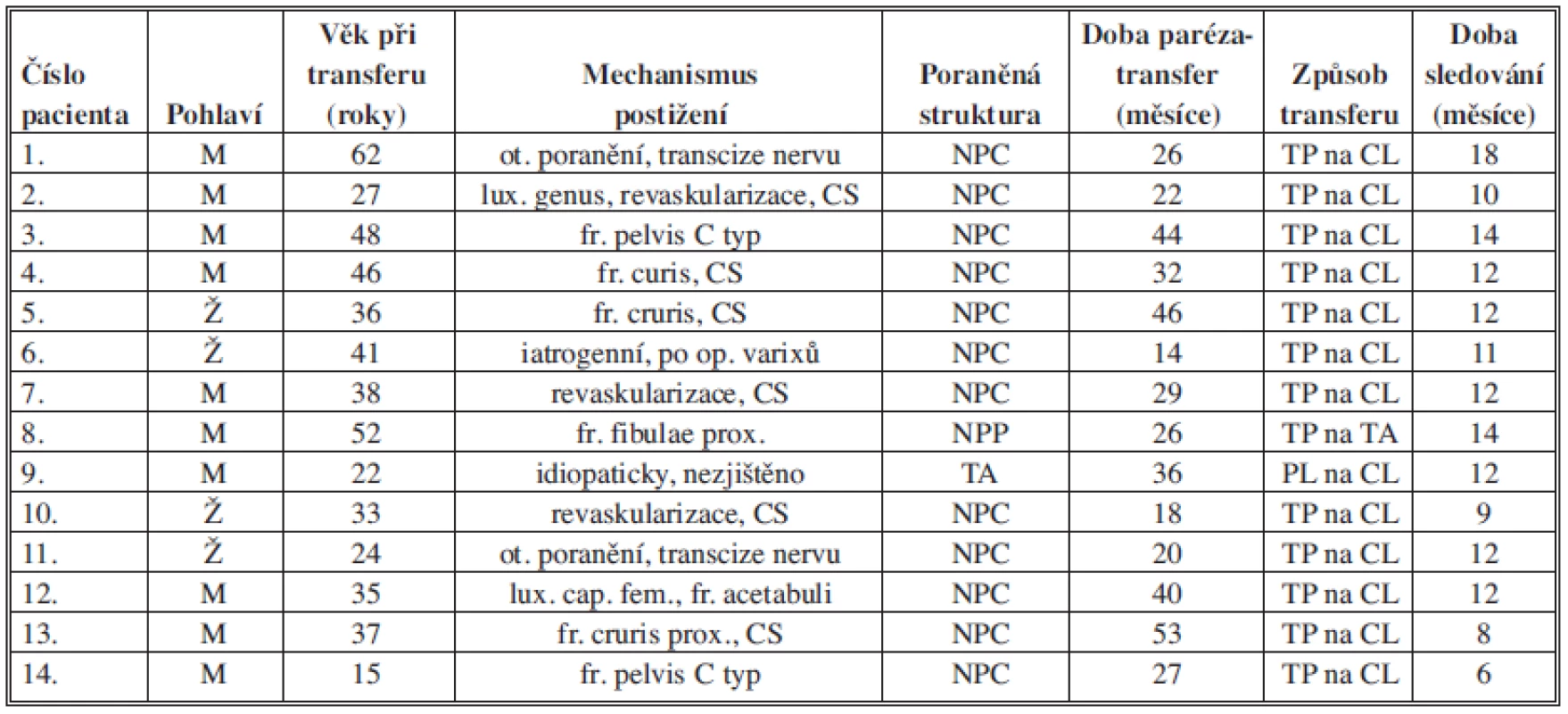
Legenda pod tabulku (CS – compartment syndrom, NPC – nervus peroneus communis, NPP – nervus peroneus profundus, TA – musculus tibialis anterior, TP – musculus tibialis posterior, CL – os cuneiforme laterale) Ve 12 případech byl postižen NPC, v jednom případě NPP a v jednom případě byla izolovaná léze TA. Věkový průměr při transferu byl 36,9 (15–62) roku. Minimální doba sledování byla 6 měsíců, průměrná 11,6 (6–18) měsíce. U dvou pacientů, kteří utrpěli otevřené poranění, byla provedena revize a sutura nervu. Průměrná doba mezi poškozením nervu a transferem byla 30,9 (14–53) měsíce. Nejkratší doba, 14 měsíců, byla u pacientky s jistým ztrátovým poraněním nervu, kdy návrat funkce nebylo možno očekávat. U všech ostatních byla dodržena minimální doba 1,5 roku od poranění. Opakovaně bylo prováděno EMG vyšetření, kdy podmínkou k provedení transferu byl stacionární stav, bez reinervačních změn v průběhu posledních 6 měsíců. Pacient č. 9 s izolovaným defektem TA měl jako jediný zachovanou aktivní extenční aktivitu, ale oslabenou svalovou sílu se snadnou unavitelností a musel využívat peroneální pásku. Pacient č. 8 nebyl schopen aktivní extenze, noha byla ve flekčním postavení, ale vzhledem k funkčnosti peroneálních svalů nebyla přítomna varózní deformita. U ostatních pacientů bylo equinovarózní postavení nohy bez aktivní extenze a pronace. U 10 pacientů byla pasivní extenze větší než 10° z neutrální pozice v hlezenním kloubu, u 4 byla nižší (Tab. 2).
2. Předoperační a pooperační aktivní a pasivní rozsah hybnosti hlezna Tab. 2: Pre-operative and postoperative active and passive ankle range of motion 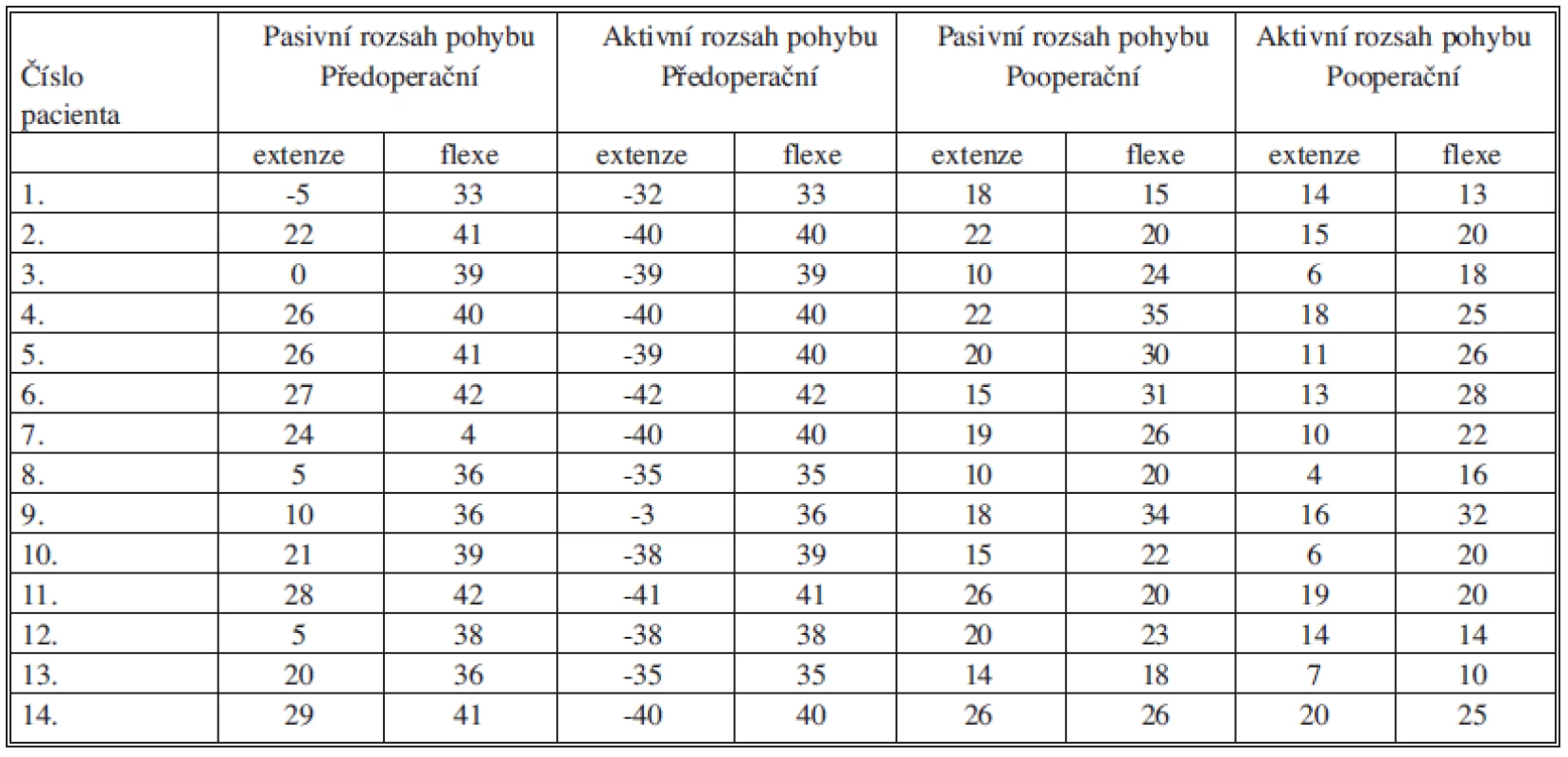
U pacientů s lézí NPC a NPP byla použita technika popsaná Mayerem [12] a Watkinsem [6], tedy transfer TP přes interoseální membránu na dorzum nohy. U pacienta č. 9 byl k transferu použit sval PL.
U pacientů s parézou NPC a NPP byla vypreparována šlacha TP na mediální straně nohy a odetnuta od úponu na os naviculare a ossa cuneiformia pedis. Následně byla protažena do incize na mediální straně bérce (Obr. 1). Z incize na ventrální straně bérce bylo preparováno podél laterální strany tibie k interoseální membráně, která byla perforována v rozsahu 3–4 cm. Tímto otvorem byla šlacha TP protažena na přední stranu bérce (Obr. 2). U pacientů s parézou NPC byla šlacha TP protažena pod extenzorovými retinakuly na dorzum nohy, kde byla kotvou fixována do os cuneiforme laterale ve 20° extenzi hlezna (Obr. 3). U pacientů 1, 3, 12, kteří měli předoperačně pasivní extenzi 10° a nižší, bylo současně provedeno prodloužení Achillovy šlachy Z-plastikou k umožnění pasivního pohybu alespoň 20° extenze.
1. Vypreparovaná šlacha m. tibialis posterior protažena do incize na mediální straně bérce Fig. 1: The dissected posterior tibial tendon inserted into the incision on the medial side of the shank 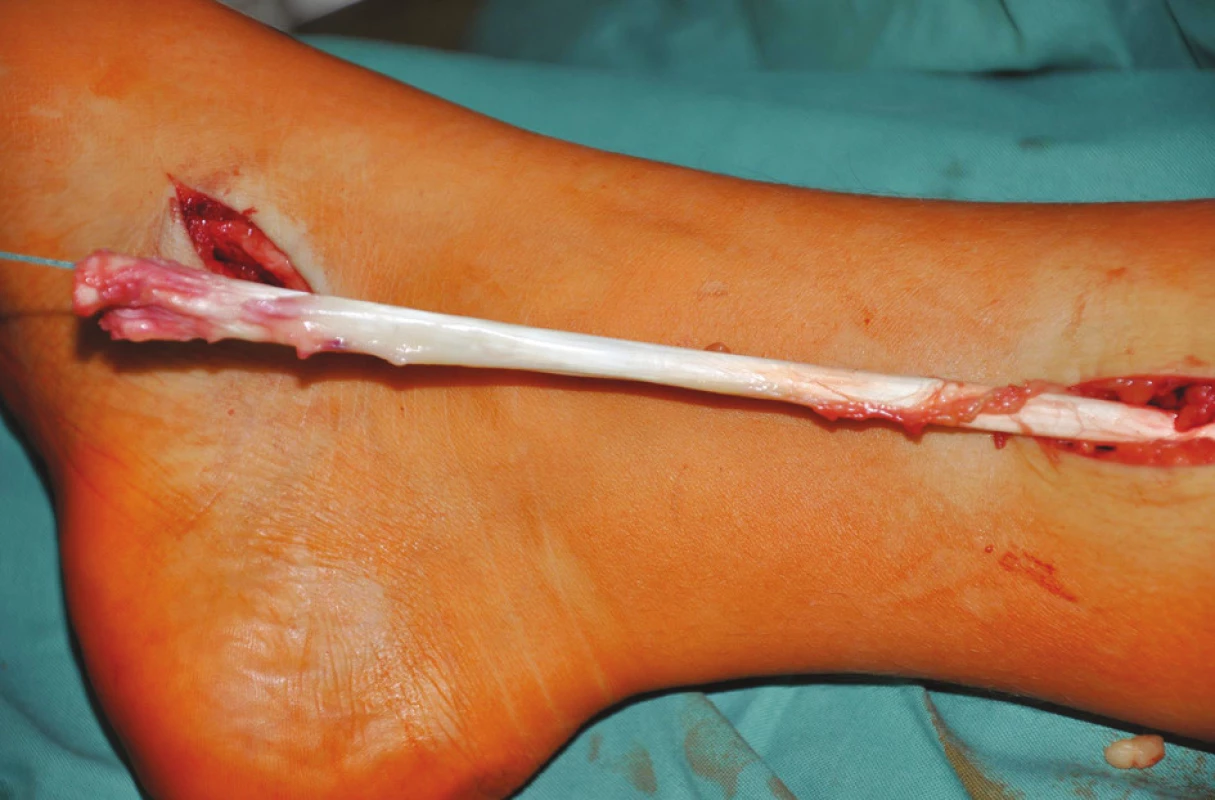
2. Šlacha m. tibialis posterior po protažení přes interoseální membránu na ventrální stranu bérce Fig. 2: The posterior tibila tendon inserted through membrana interossea cruris onto the ventral side of the shank 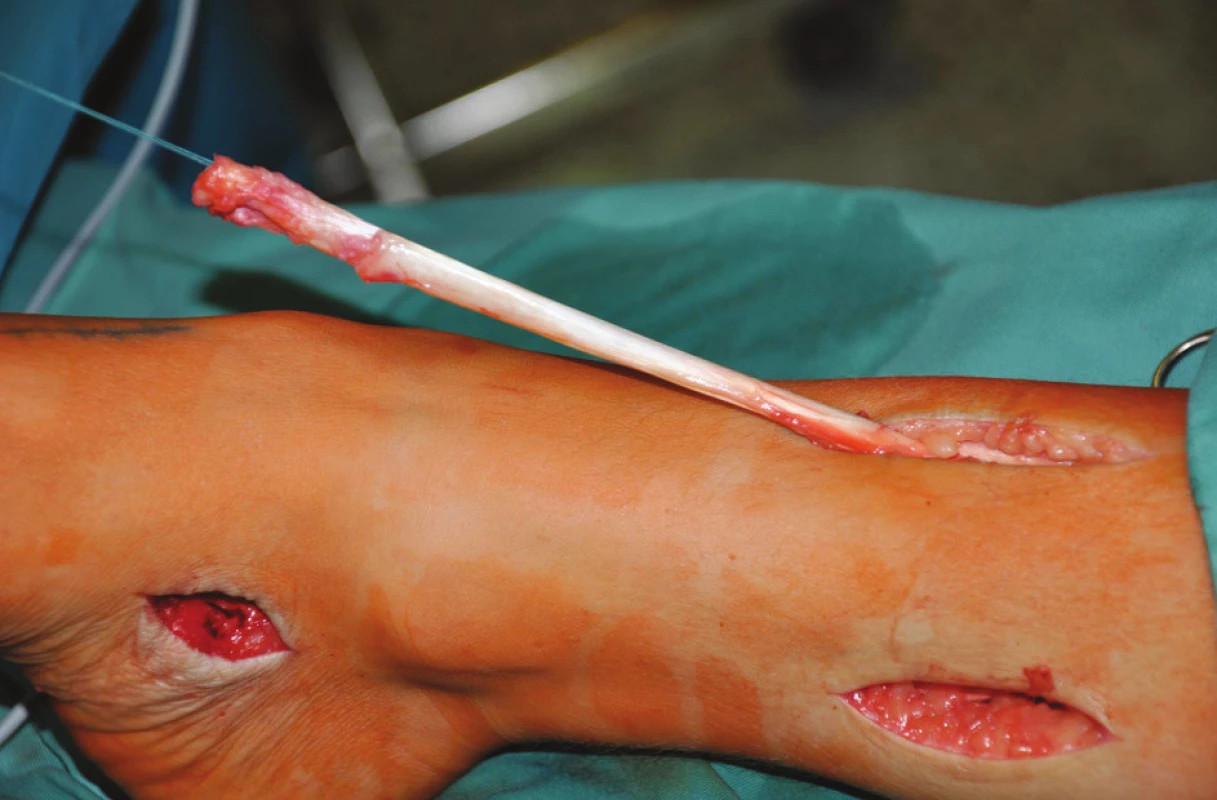
3. Ukotvení šlachy m. tibialis posterior do os cuneiforme laterále Fig. 3: Anchoring the posterior tibial tendon into the lateral cuneiform bone 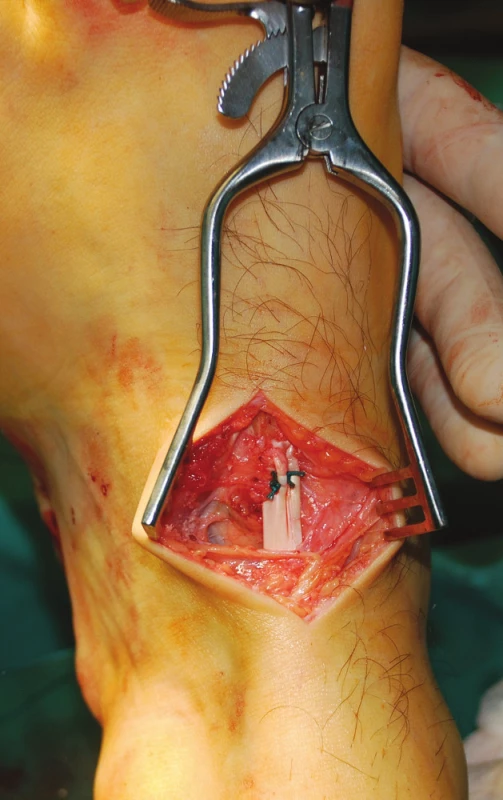
U pacienta č. 8 byla šlacha TP našita side to side v délce 5 cm ve 20° extenzi hlezna k distálnímu pahýlu šlachy TA. Současně pro omezení pasivní extenze byla prodloužena Achillova šlacha.
U pacienta č. 9 bylo potřeba posílit extenzi nohy transpozicí šlachy PL, která byla přenesena na dorzum nohy na os cuneiforme laterale.
Po výkonu byla přiložena fixace ve 20° extenzi hlezna po dobu 6 týdnů. Následně byla zahájena rehabilitace za hospitalizace s nácvikem chůze a postupnou zátěží končetiny.
Hodnocení
K analýze předoperačních a pooperační dat byl použit Stanmorův skórovací systém [13]. Tento skórovací systém hodnotí bolest, a to jak klidovou, tak pozátěžovou, potřebu ortézy, peroneální pásky k chůzi, obuv, kterou je pacient schopen na končetině nosit, a to jednak preference stejného nebo jiného typu obuvi než na nepostižené končetině a případný rozdíl velikostí obuvi. Dalším kritériem je funkční stav, kdy pacient hodnotí omezení při běžných denních, pracovních, rekreačních a sportovních aktivitách. Svalová síla extenze se hodnotí podle stupnice vydané Medical Research Council [2]. Standardním goniometrem měříme stupně aktivní a pasivní extenze, přičemž Stanmorův skórovací systém hodnotí jen aktivní pohyb. Posledním hodnoceným kritériem je postavení nohy při došlapu a deformita nohy. Maximální hodnota výsledku tohoto skórovacího systému je 100 bodů, přičemž výsledek 85–100 bodů je hodnocen jako vynikající, 70–84 bodů jako dobrý, 55–69 bodů jako uspokojivý a nižší než 55 bodů jako špatný.
Výsledky
Po operačním výkonu se nevyskytly žádné časné pooperační komplikace, všechny rány se zhojily per primam.
U všech pacientů byla možná aktivní extenze hlezna, průměrně 12,3° (4–20) (Tab. 2), kdy předoperačně měl možnost aktivní extenze jen pacient č. 9, a to jen do –3°. U třinácti pacientů, kterým byl transferován TP, došlo k omezení jak aktivní, tak pasivní flexe, kdy omezení aktivní flexe bylo průměrně o 48 % (27–71) oproti předoperační aktivní flexi hlezna. U pacienta č. 9, kterému byl transferován PL, bylo omezení flexe hlezna jen o 11 %.
U devíti pacientů, kteří udávali předoperačně mírnou nebo střední bolest, došlo pooperačně k jejímu vymizení nebo zmírnění. U 5 pacientů, kteří byli již předoperačně bez bolestivostí, se bolest pooperačně neobjevila. Po šlachovém transferu žádný z pacientů nepotřebuje kompenzační pomůcku, peroneální pásku. U 13 pacientů (93 %) došlo ke zlepšení v parametru preferovaného typu obuvi, jen u jednoho pacienta (7 %) se tento parametr nezměnil. Osm pacientů (57 %) udávalo možnost vykonávat normální denní aktivity, zaměstnání i trávení volného času, 5 pacientů (36 %) udávalo omezení v rekreačních a sportovních aktivitách a 1 pacient (7 %) udával omezení i při běžných denních činnostech. Při měření svalové síly mělo 6 pacientů (43 %) dostatečnou svalovou sílu extenze nohy proti silnému odporu a 8 pacientů (57 %) mělo dostatečnou svalovou sílu proti mírnému odporu. Poslední hodnocené kritérium, postavení a držení nohy, bylo u 7 pacientů (50 %) správné, noha byla bez deformity a pacienti došlapovali celou nohou. U druhé poloviny pacientů se hodnocený parametr nezměnil, došlapovali celým chodidlem, ale byla patrna mírná deformita nohy.
Výsledný součet bodů byl mezi 87 a 100 body (Tab. 3), takže u všech pacientů bylo hodnocení v pásmu vynikajícího výsledku. Tři pacienti (21 %) dosáhli maximálního počtu 100 bodů. Při statistickém zhodnocení předoperačního a pooperačního stavu Studentovým T-testem je rozdíl ve všech hodnocených kritériích včetně konečného součtu statisticky významný.
3. Hodnocení výsledků Stanmorovým skórovacím systémem Tab. 3: Postoperative results by Stanmore scoring system 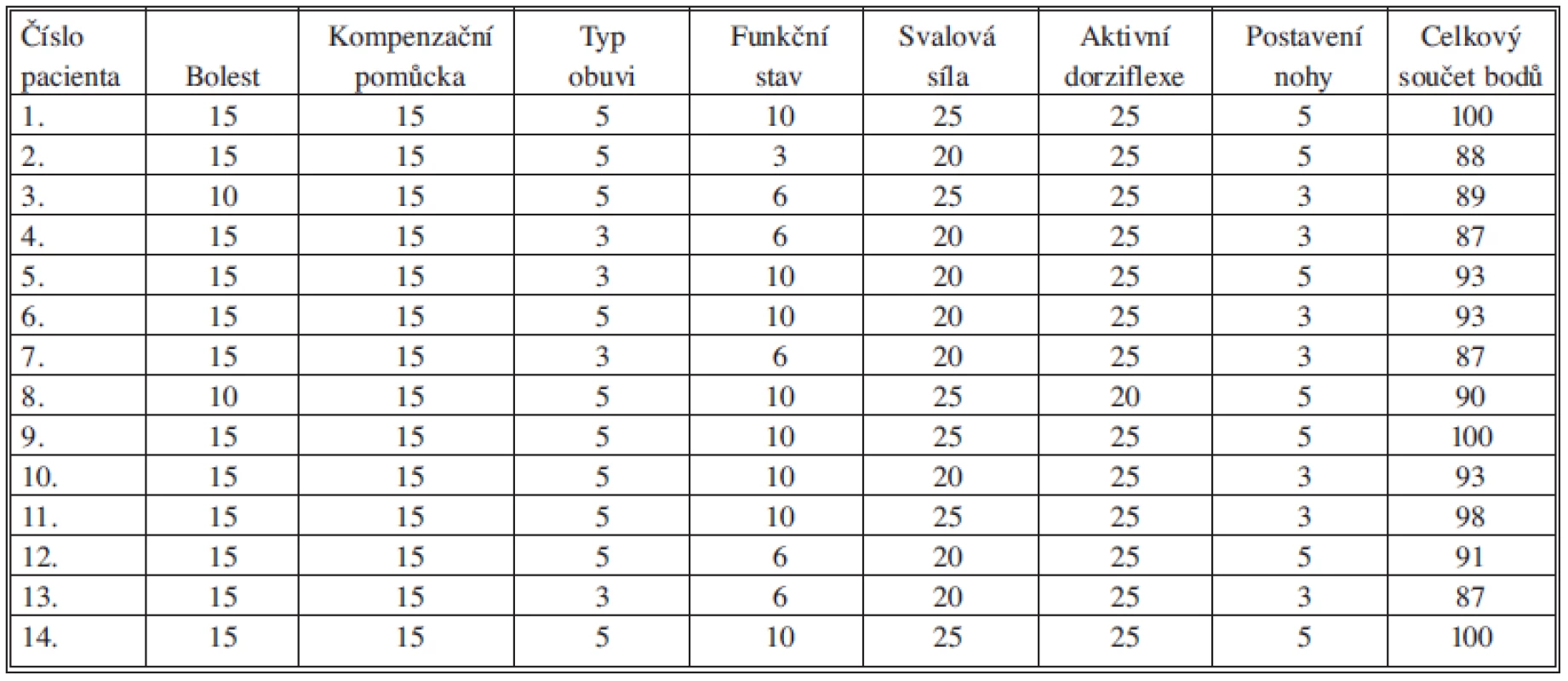
Diskuze
Při výpadku funkce svalu nebo určité skupiny svalů, nejčastěji při postižení periferních nervů, a dobré funkci jiných svalů příslušné oblasti končetiny má šlachový transfer tři cíle. Prvním je obnovení nebo zvýšení síly postiženého pohybu, druhým je zmenšení nebo odstranění deformujících sil působících na končetinu a třetím je zvýšení stability postiženého kloubu při zátěži a odstranění nutnosti používat kompenzační pomůcky [14]. Kromě transferů, které jsou svou podstatou dynamické chirurgické výkony umožňující pohyb, mohou být prováděny i tzv. statické chirurgické výkony, které upraví postavení postižené části končetiny do lepší funkční pozice, čímž sice zlepší celkovou funkci končetiny, ale neobnoví ztracený pohyb, případně zmenší nebo úplně zruší pohyb stávající. Statickými výkony jsou artrodézy, osteotomie a tenodézy. Nevýhodou statických výkonů je jejich nevratnost. Proto by měly být používány statické výkony buď jako podpora dynamických výkonů při fixovaných deformitách končetin, nebo po selhání transferu, nebo v případech, kdy není transfer indikován, například při významném degenerativním postižení kloubu, při difuzních periferních neuropatiích, při mozkových a neuromuskulárních chorobách, nebo při poranění vícečetných nervů na končetině s nepřítomností funkční donorské šlachy k transferu. Dynamické výkony, transfery, při kterých se změní průběh svalu přemístěním jeho distálního úponu, se zlepší funkce končetiny a především dojde k obnově aktivního pohybu. Jejich indikací je v současné době především léčba poúrazových nervových paréz [15].
První práce zabývající se šlachovými transfery na dolní končetině je z roku 1933 [16], kdy Ober popisuje povrchový, cirkumtibiální transfer TP. Další práce, Mayera [12], vychází v roce 1937 a je v ní popsán transfer TP přes interoseální membránu na dorzum nohy k obnově aktivní extenze nohy.
Při paréze NPC je noha v equinovarózním postavení. Největší obtíží pacientů je přepadávání špičky nohy, kdy o ni při chůzi zakopávají a jsou nuceni při chůzi vysoko zvedat koleno (tzv. čapí chůze), běh není možný vůbec. Závažný problém pro pacienta představuje nestabilita hlezenního kloubu, projevující se opakovanými podvrtnutími a pády, především při chůzi v nerovném terénu. Je tedy potřeba obnovit extenzi nohy, zabránit varózní deformitě nohy způsobované tahem TP a zvýšit stabilitu hlezna. Toho dosáhneme transferem TP na dorzum nohy, do neutrálního bodu nohy, na os cuneiforme laterale. Při paréze NPP jsou pronosupinační síly v rovnováze, a je tedy potřeba obnovit jen extenzi v hleznu. Toho je možno dosáhnout i artrodézou hlezna, nebo tenodézou TA, ovšem funkčně výhodnější je dynamický proces, kdy je zachován volní pohyb, šlachový transfer [17, 18]. K zachování rovnováhy pronosupinačních sil působících na nohu, je v tomto případě šlacha TP přemístěna na mediální stranu dorza nohy.
Vzhledem k tomu, že je jen asi třetinová pravděpodobnost návratu funkce n. peroneus communis po revizi a ošetření jeho přímého poranění, je na některých pracovištích k rychlejšímu návratu funkce prováděn šlachový transfer v jedné době s ošetřením nervu [19] jako prevence možných kontraktur a deformit nohy tahem zadní svalové skupiny. V našich případech jsme dodrželi minimální dobu 1,5 roku od vzniku parézy a EMG v rozmezí 6 měsíců bez reinervačních změn. Jen u pacientky s jistou ztrátou nervu byl transfer proveden dříve. Proti vzniku kontraktur a deformit probíhala řízená rehabilitace hlezna a nohy s udržením maximální možné pasivní hybnosti hlezna. Výše zmíněná práce Ferraresiho neřeší tu třetinu případů, u níž dojde k návratu funkce NPC a tím ke vzniku svalové dysbalance nohy. Námi prezentovaný postup dává možnost k reinervaci, návratu pohybu, zabrání vzniku deformity a při přetrvávající plegii obnoví aktivní pohyb šlachovým transferem.
K co nejlepšímu funkčnímu výsledku šlachového transferu je důležité správné předpětí transferované šlachy [11, 20]. Při technikách, při kterých je šlacha TP našívána na šlachu TA, je možné nastavení předpětí. Některými autory je preferováno mírné nebo střední napětí suturovaných šlach, kdy hlezno je maximálně v 90°. Jinými autory [21] je preferováno vysoké napětí šlachy, kdy je hlezno v okamžiku sutury v 10–20° extenzi. Při reinzerci šlachy TP do kosti, do os cuneiforme laterale, je vzhledem k tomu, že šlacha TP má hraniční délku situace ohledně předpětí jednodušší, hlezno musí být v okamžiku inzerce šlachy v 10–20° extenzi. Pokud je předpětí větší, dochází vzhledem k malé pohybové exkurzi TP k tzv. tenodeznímu účinku, je omezena flexe hlezna. Je otázkou, co pacienti vnímají jako větší problém, jestli omezení extenze, nebo flexe. Pro chůzi i běh je důležitá možnost dostatečné extenze, a to alespoň 10°. V našich případech jsme proto prováděli větší předpětí šlachy, hlezno bylo v 10–20° extenze a u všech pacientů došlo k omezení flexe. Všichni pacienti byli s výsledkem spokojeni, byli schopni rychlé chůze a běhu a nikdo z nich nepozoroval jako problém omezení flexe. A při srovnání výsledků Stanmorova skórovacího systému jsou naše výsledky lepší než při našití šlachy s nižším předpětím [22]. Pilný a kol. [23] prezentuje stejný operační postup, avšak s menším předpětím transferované šlachy. V hodnocení nepoužívá komplexní Stanmorův systém, ale hodnotí jen možnost extenze hlezna a výborné výsledky udává jen u 64 % pacientů. Z toho vyplývá, že provádět transfer s větším předpětím je úspěšnější.
Při transferu TP je možné použití dvou cest, kudy je šlacha vedena. Jednak je to tzv. cirkumtibiální cesta, kdy je šlacha provlékána podkožím podél mediální strany tibie na přední stranu bérce. Druhou je tzv. transinteroseální cesta, použitá v našich případech, kdy je šlacha provlékána na přední stranu bérce přes otvor v interoseální membráně. V biomechanické studii [24] vychází transinteroseální, námi použitá, technika jako výhodnější, cesta je kratší a zajistí větší svalovou sílu. Otvor v membráně musí být dostatečně velký, šlacha jím musí procházet v tupém úhlu a před inzercí nebo suturou musí být zkontrolováno, zda není ve svém průběhu přetočena. Na přední straně bérce je možné šlachu k místu úponu vést buď v hloubce, pod extenzorovými retinakuly, anebo povrchově nad nimi. Tímto se zabývala biomechanická studie [25], se závěrem, že při provlečení šlachy povrchově, nad retinakuly, je výrazně účinnější pohyb než při transferu pod retinakuly. Tato změna v námi použité technice by mohla zlepšit celkový rozsah hybnosti hlezna, v našem případě do flexe.
V Srinivasanově práci z roku 1968 [5] je poprvé popsána technika transferu, kdy je našívána šlacha ke šlaše. V tomto případě je šlacha TP rozdělena, po přesunutí na přední stranu bérce, na dvě části. Jedna část je našita na šlachu EHL a druhá na šlachu EDL a m. peroneus tertius, k vyvážení pronosupinace nohy. Současně popisuje nevýhody a technické obtíže při fixaci šlachy TP do kosti a hraniční délku šlachy TP. Další práce [15, 18], ve kterých jsou použity modifikace Srinivasanovy techniky, uvádějí dobré výsledky. Inovaci těchto technik přinesla až v roce 2008 Vigasiova práce [22], kdy je přemístěno místo úponu TA provrtáním kuneiformních kostí z mediální strany na dorzum os cuneiforme laterale a šlacha TA po přerušení na muskulotendinózním přechodu je tímto otvorem provlečena a na přední straně bérce sešita se šlachou TP. Problematické u této techniky může být poškození kloubů mezi kuneiformními kostmi, které může působit bolesti. Výhodou technik TtT (tendon to tendon) je možnost nastavení předpětí, které u fixace šlachy TP do kosti není. Proto je tato technika variantou při problémech s délkou šlachy TP, kdy by byla nutnost nadměrného předpětí ve více než 20° extenzi hlezna a případů, kdy je indikován transfer na distální pahýl TA v původním umístění. Kotvení šlachy do kosti, námi použitou technikou implantací Mitek kotev do os cuneiforme laterale, je dostatečně spolehlivé, pevné, v udržení šlachy vnořené do kosti až do doby jejího vhojení. Slibná se v posledních letech jeví technika kotvení šlachy do kosti, používaná dříve hojně při plastice LCA, použitím endobuttonu. Zatím byly publikovány práce, které popisují použití endobuttonu při refixaci ruptury distálního úponu m. biceps brachii [26], kdy je tento způsob fixace šlachy do kosti v biomechanické studii vyhodnocen jako nejpevnější [27]. Použití při šlachových transferech TP nebylo prozatím publikováno.
Možností, jak posílit extenzi nohy a obnovit extenzi prstů a palce, je přenést spolu s TP ještě jednu šlachu. Nejvhodnější je transfer šlachy m. flexor digitorum longus (FDL) na extenzory prstů a palce. Je důležité ponechání m. flexor hallucis longus (FHL), protože jeho síla je důležitá v odrazové fázi kroku. Ve studiích [22], které prováděly transfer FDL, ztráta funkce TP a FDL nepřinesla žádnou ztrátu, pokud jde o sílu a rozsah pohybu prstů nohy. V našich případech nebylo vnímáno přetrvávající flekční postavení prstů a nohy jako negativum, i když k dalšímu posílení extenze nohy by tento transfer byl přínosný.
V pooperační péči není shoda v literatuře, co se týče imobilizace končetiny. Rozmezí je 5 dní až 8 týdnů. Časnou rehabilitaci, již 5 dní po operačním zákroku, popisují autoři z Indie a Nepálu [28], kdy je transfer prováděn pro leprózní postižení různými technikami TtT. Popisované výsledky jsou lepší než při imobilizaci 40 dní. Druhým extrémem je 8 týdnů, popsaných již Oberem v roce 1933 [16]. Naše doba imobilizace, 6 týdnů, je kompromisem a nejčastěji udávanou dobou imobilizace. Nezaznamenali jsme ani jedno vytržení šlachy z kosti při námi prováděné imobilizaci po dobu 6 týdnů.
Musculus tibialis posterior je hlavním dynamickým stabilizátorem mediální nožní klenby a hlavním supinátorem zadní části nohy [29]. Z tohoto důvodu by se dal očekávat zvýšený výskyt sekundárního plochonoží u pacientů, kteří podstoupili transfer TP, ztrátou jeho funkce. Tím dochází ke zvýšení tlaku na statické stabilizátory podélné nožní klenby, z nichž hlavním je plantární kalkaneonavikulární vaz. Ovšem není tomu tak, popsané případy získaného plochonoží po transferu TP jsou raritní. Při normálním kroku je potřeba inverzí, tahem TP, zablokovat příčné tarzální klouby, a přeměnit tak původně pružnou nohu v pevnou, rigidní, která umožní odraz. Normálním antagonistou m. tibialis posterior je m. peroneus brevis, který provádí pronaci zadní části nohy [30, 31, 32]. Jako nejpravděpodobnější důvod, proč nedochází ke vzniku plochonoží, je současná ztráta funkce TP (transferem) i peroneus brevis (poraněním NPC, nebo NPS), čímž vznikne nová dynamická rovnováha [31]. Yeap [33] s tím nesouhlasí a prokazuje, že plochonoží nevzniká ani u pacientů po šlachovém transferu TP při zachovalé funkci peroneálních svalů. Raritní vznik plochonoží po transferu vysvětluje predispozičními faktory a předoperačně nediagnostikovanou dysfunkcí m. tibialis posterior a počínajícím plochonožím. V našem souboru se po dobu sledování podélné plochonoží neobjevilo, nicméně pacient by měl být předoperačně na toto riziko, i když malé, upozorněn.
Závěr
Nemožnost nebo oslabení extenze nohy v hleznu je invalidizující stav, který znemožní rychlejší chůzi nebo běh. Obnova aktivní extenze transferem TP nebo PL je metodou volby, kdy obnovená extenze nohy umožní běžné aktivity, návrat k pracovním i sportovním činnostem. Po těchto transferech dochází vždy k částečnému omezení hybnosti hlezna do flexe pro menší pohybový rozsah transferovaných flexorů. Omezení flexe však není pacienty vnímáno negativně. Popsané techniky jsou jednoduché a mají velmi dobré funkční výsledky.
MUDr. Petr Špiroch
Mošnerova 18a
779 00 Olomouc
e-mail: spirda@email.cz
Sources
1. Mont M, Dellon AL, Chen F, et al. The operative treatment of peroneal nerve palsy. J Bone Joint Surg Am 1996;78 : 863–869.
2. Clawson DK, Seddon HJ. The results of repair of the sciatic nerve. J Bone Joint Surg Br 1960;42 : 05–212.
3. Kim DH, Murovic JA, Tiel RL, Kline DG. Management and outcomes in 318 operative common peroneal nerve lesions at the Louisiana State University Health Sciences Center. Neurosurgery 2004;54 : 1421–1429.
4. Shah RK. Tibialis posterior transfer by interosseous route for the correction of foot drop in leprosy. Int Orthop 2009;33 : 1637–1640.
5. Srinivasan H, Mukherjee SM, Subramaniam RA. (1968) Twotailed transfer of tibialis posterior for correction of drop-foot in leprosy. J Bone Joint Surg Br 1968;50 : 623–628.
6. Watkins MB, Jones JB, Ryder CT Jr., Brown TH Jr. Transplantation of the posterior tibial tendon. J Bone Joint Surg Am 1954;36 : 1181–1189.
7. Herman J, Sekanina Z, Utikal P, et al. Peroneal nerve injury during varicose veins surgery. Int Angiol 2009;28 : 458–460.
8. Johnson DS, Sharma DP, Bangash IH. Common peroneal nerve palsy following knee arthroscopy. Arthroscopy 1999;15 : 773–774.
9. Khan R, Birch R. Latropathic injuries of peripheral nerves. J Bone Joint Surg Br 2001;83 : 1145–1148.
10. Niall DM, Nutton RW, Keating JF. Palsy of common peroneal nerve after traumatic dislocation of the knee. J Bone Joint Surg Br 2005;87 : 664–667.
11. Carayon A, Bourrel P, Bourges M, Touze M. Dual transfer of the posterior tibial and flexor digitorum longus tendons for drop foot: report of thirty-one cases. J Bone Joint Surg Am 1967;49 : 144–148.
12. Mayer, L. The physiological method of tendon transplantation in the treatment of paralytic drop-foot. J Bone Joint Surg Am 1937;19 : 389–394.
13. Yeap JS, Singh D, Birch R. A method for evaluating the results of tendon transfers for foot drop. Clin Orthop Relat Res 2001; 383 : 208–213.
14. Mulier T, Moens P, Molonaers G, et al. Split posterior tibial tendon transfer through the interosseous membrane in spastic equinovarus deformity. Foot Ankle Int 1995;16 : 754–759.
15. Rodriguez RP. The Bridle procedure in the treatment of paralysis of the foot. Foot Ankle 1992;13 : 63–69.
16. Ober FR. Tendon transplantation in the lower limbs. New Engl J Med 1933;209 : 52–59.
17. De Marchi F, Malerba F, Montrasio Alfieri U, et al. M. Tibialis posterior tendon transfer through the interosseal membrane in paralysis of the common peroneal nerve. Foot Ankle Surg 2000;6 : 19–25.
18. Yeap JS, Birch, R, Singh D. Long-term results of tibialis posterior tendon transfer for drop-foot. Int Orthop 2001;25 : 114–118.
19. Ferraresi S, Garozzo D, Buffatti P. Common peroneal nerve injuries: results with one-stage nerve repair and tendon transfer. Neurosurg Rev 2003;26 : 175–179.
20. Hove LM, Nilsen PT. Posterior tibial tendon transfer for dropfoot: 20 cases followed for 1–5 years. Acta Orthop Scand 1998;69 : 608–610.
21. Andersen JG. Indications and contra-indications in reconstructive surgery in leprosy. Lepr Rev 1963;34 : 127–131.
22. Vigasio A, Marcoccio I, Patelli A, et al. New Tendon Transfer for Correction of Drop-foot in Common Peroneal Nerve Palsy. Clin Orthop Relat Res 2008;466 : 1454–1466.
23. Pilný J, Čižmář I, Ehler E, Dráč P. Transpozice šlachy m. tibialis posterior - efektivní řešení parézy peroneálních svalů. Česk Slov Neurol N 2009;(72)105 : 279–283.
24. Goh JC, Lee PY, Lee EH, Bose K. Biomechanical Study on Tibialis Posterior Tendon Transfers. Clinical Orthopaedics & Related Research 1995;319 : 297–302.
25. D’Astous JL, MacWilliams BA, Kim SJ, Bachus KN. Superficial Versus Deep Transfer of the Posterior Tibialis Tendon. Journal of Pediatric Orthopaedics 2005;25 : 245–248.
26. Ranelle RG. Use of the Endobutton in repair of the distal biceps brachii tendon. Proc (Bayl Univ Med Cent), 2007;20 : 235–236.
27. Mazzocca AD, Burton KJ, Romeo AA, et al. Biomechanical evaluation of 4 techniques of distal biceps brachii tendon repair. Am J Sports Med 2007;35 : 252–258.
28. Rath S, Schreuders TAR, Selles RW. Early postoperative active mobilisation versus immobilisation following tibialis posterior tendon transfer for foot-drop correction in patients with Hansen’s dinase. Journal of Plastic, Reconstructive & Aesthetic Surgery 2010;63 : 554–560.
29. Mann RA. Flatfoot in adults. In: Mann, RA., Coughlin MJ., editors: Surgery of the foot and ankle. 7th ed. St. Louis, Mosby, 1999 : 733–767.
30. Mann RA, Thompson FM. Rupture of the posterior tibial tendon causing flat foot: surgical treatment. J Bone Joint Surg Am 1985;67 : 556–561.
31. Mizel, MS, Temple HT, Scranton PE Jr., et al: Role of the peroneal tendons in the production of the deformed foot with posterior tibial tendon deficiency. Foot Ankle Int 1999;20 : 285–289.
32. Vertullo CJ, Nunley JA. Acquired Flatfoot Deformity Transfer for Peroneal Nerve Injury: A Case Report. J Bone Joint Surg Am 2002;84 : 1214–1217.
33. Yeap JS, Singh D, Birch R. Tibialis posterior tendon dysfunction: a primary or secondary problem? Foot Ankle Int 2001;22 : 51–55.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2012 Issue 3-
All articles in this issue
- Screening of breast carcinoma screening in the Czech Republic requires cooperation with surgeons
- Malignant tumors of the esophagus in the Czech Republic
- NOSE (Natural Orifice Specimen Extraction) in laparoscopic colorectal surgery
- Osteosynthetic material breakage in patients treated with DHS for proximal femoral fracture
- Restoration of active foot extension following peroneal nerve palsy
- Rates of complications after laparoscopic cholecystectomy depending on the coagulation technique – a comparative study
- Retrogastric bronchogenic cyst
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Restoration of active foot extension following peroneal nerve palsy
- Retrogastric bronchogenic cyst
- Osteosynthetic material breakage in patients treated with DHS for proximal femoral fracture
- Screening of breast carcinoma screening in the Czech Republic requires cooperation with surgeons
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

