-
Medical journals
- Career
Diagnostika heterotopické žaludeční sliznice horního jícnu a její vliv na sliznici hrtanu
Authors: M. Enter 1; J. Syrovátka 1; M. Merenda 2
Authors‘ workplace: Oddělení ORL a chirurgie hlavy a krku, Nemocnice AGEL Nový Jičín a. s. 1; Interní oddělení, Nemocnice AGEL Nový Jičín a. s. 2
Published in: Otorinolaryngol Foniatr, 72, 2023, No. 3, pp. 136-142.
Category: Original Article
doi: https://doi.org/10.48095/ccorl2023136Overview
Úvod: Heterotopická žaludeční sliznice proximálního jícnu, inlet patch (IP), představuje ostrůvek sliznice nacházející se distálně od horního jícnového svěrače. Její buňky mohou být schopny produkovat kyseliny a trávicí enzymy. Metodika: Prospektivní studie v období let 2020 a 2021 sleduje pacienty souborů A nebo B, kteří podstoupili gastroskopické vyšetření nebo vyšetření přímou ezofagoskopií v celkové anestezii. V souboru C jsme ORL videoendoskopickým vyšetřením hodnotili vliv IP na sliznici hrtanu. Výsledky: Prevalence IP byla stanovena na 4,87 %. Zachyceno bylo 40 IP z 821 provedených vyšetření. V souboru C nebylo zjištěno výraznější postižení sliznice hrtanu u pacientů s IP. Závěr: Prevalence IP v novojičínském regionu byla 4,87 %. V našem souboru nebylo zjištěno vyšší postižení sliznic hrtanu u pacientů s IP. Na IP je nutné pomýšlet u pacientů s laryngofaryngeálním refluxem bez efektu konzervativní terapie jako možnou příčinu obtíží. V léčbě extraezofageálního refluxu, špatně ovlivnitelného konzervativní terapií je vhodné doplnit gastrofibroskopické vyšetření se zaměřením na průkaz IP a jeho biopsii.
Klíčová slova:
heterotopická žaludeční sliznice – inlet patch – GERD – extraezofageální reflux – rigidní ezofagoskopie
Úvod
Heterotopická žaludeční sliznice oblasti horního jícnu, v anglické terminologii inlet patch (IP), představuje ostrůvek sliznice nacházející se distálně od horního jícnového svěrače. Nejčastěji zmiňovaná teorie vzniku předpokládá embryonální původ během transformace epitelu v 11. embryonálním týdnu. Proximální část jícnu je poslední oblastí transformace, což může vysvětlovat zvýšený výskyt heterotopické žaludeční sliznice právě v této oblasti [1–5]. Buňky této sliznice jsou schopny produkovat kyselinu chlorovodíkovou i trávicí enzymy. Tato schopnost vede k možným projevům laryngofaryngeálního refluxu (LPR) u pacientů s IP [1, 2, 5–7].
Prevalence IP v proximálním jícnu se pohybuje v rozmezí 0,1–15 % [1, 2, 5, 7–15]. IP se typicky nachází 1–5 cm distálně od horního jícnového svěrače v průměrné vzdálenosti 15–21 cm od řezáků [2, 4, 5, 16, 17]. Na sliznici vypadá jako sametově růžově až lososově zbarvený ostrůvek oválného nebo okrouhlého tvaru s přesně ohraničenými okraji od okolní sliznice jícnu (obr. 1, 2). Velikost bývá od několika milimetrů do několika centimetrů a jejich počet se nejčastěji udává v rozmezí 1–4 lézí [2, 5, 7, 18]. Symptomatologie je předurčena velikostí léze, jejich počtem a schopností produkovat kyseliny. IP bývá většinou klinicky němý, obtíže jsou popisovány u 6–20 % pacientů s prokázanou lézí [6, 10]. Studie poukazují na spojitost s vyšším výskytem symptomů laryngofaryngeálního refluxu u pacientů s IP [1, 7, 9, 12, 16, 18] s nejvyšší koincidencí až v 73 % případů [5]. IP jsou všeobecně považovány za benigní léze, proto jejich nález při endoskopii nevyžaduje rutinní odběr biopsie [2, 6]. Mezi popisované komplikace patří slizniční prstence až striktury, častější uváznutí sousta, vředy, krvácení, perforace, tracheoezofageální fistula a raritně maligní transformace [1–4, 7, 11, 16, 19]. V současnosti neexistují standardizované léčebné strategie u pacientů s diagnostikovaným IP [3]. Asymptomatičtí pacienti s náhodným nálezem IP nevyžadují léčbu. U pacientů s příznaky LPR se v terapii uplatňují konzervativní i chirurgické (endoskopické) přístupy.
Materiál a metodika
Do sledovaných skupin v této prospektivní práci byli zařazeni všichni pacienti splňující kritéria, kteří podstoupili vyšetření v Nemocnici AGEL Nový Jičín a.s. v období mezi 1. 1. 2020 a 31. 8. 2021. Pro účely práce byly vytvořeny tři skupiny pacientů (A–C).
Soubor A – gastrofibroskopické vyšetření
Do prvního souboru byli zařazeni všichni pacienti, kteří v rozhodném období podstoupili gastrofibroskopické vyšetření cestou gastroenterologické ambulance. Vyšetření prováděl jeden lékař se znalostí výskytu IP. Vyšetření bylo prováděno v bílém světle bez bioptického ověření léze. Do sledovaného souboru bylo zařazeno 799 pacientů. Ze souboru byli vyloučeni pacienti s akutním krvácením v horním GIT, impaktovaným cizím tělesem v jícnu a pooperační kontroly po onkochirurgickém nebo bariatrickém výkonu, kde nebyla zachována fyziologická kontinuita jícnu.
Soubor B – přímé vyšetření jícnu videoendoskopem v celkové anestezii
Do souboru bylo zařazeno 22 pacientů, kteří podstoupili přímé vyšetření jícnu v celkové anestezii na oddělení ORL a chirurgie hlavy a krku. Vyšetření prováděl jeden lékař, za použití rigidního ezofagoskopu (R.WOLF 300 × 14 ×10 mm), pod videoendoskopickou kontrolou (R.WOLF 0°, 495 mm, Lumina) v bílém světle. Do souboru nebyli zařazeni pacienti, kteří podstoupili ezofagoskopii pro nález cizího tělesa.
Soubor C – ambulantní ORL vyšetření
Do souboru byli zařazeni pacienti s nálezem IP (ze souborů A i B), kteří souhlasili s vyšetřením ORL lékařem. Vyšetření podstoupilo 17 pacientů se záchytem IP ze souborů A a B. Před vyšetřením byl pacienty vyplněn dotazník Reflux Symptom Index (RSI) (tab. 1) [20–22]. Navazující videoendoskopické vyšetření v bílém světle bylo provedeno stejným L2 ORL lékařem. Nález byl hodnocen podle Reflux Finding Score (RFS) (tab. 2) [20–22] a byla pořízena fotodokumentace ke kontrole nálezu.
Table 1. Refl ux symptom index (RSI).
Tab. 1. Refl ux Symptome Index (RSI).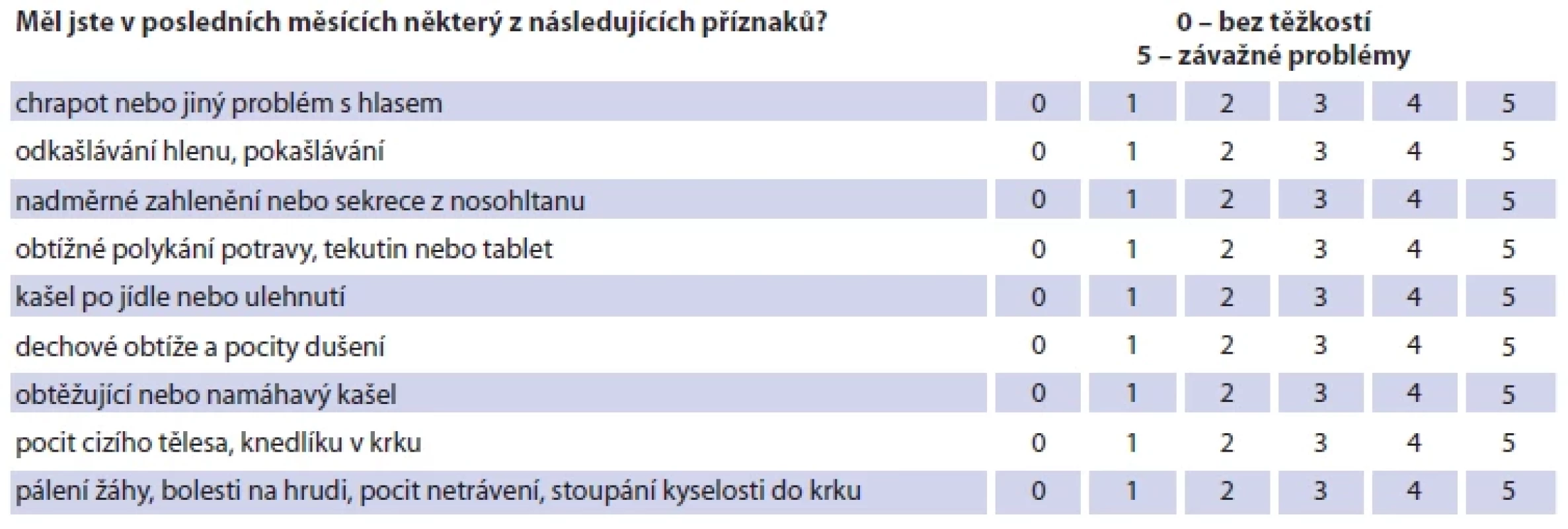
Table 2. Refl ux fi nding score (RFS).
Tab. 2. Refl ux Finding Score (RFS).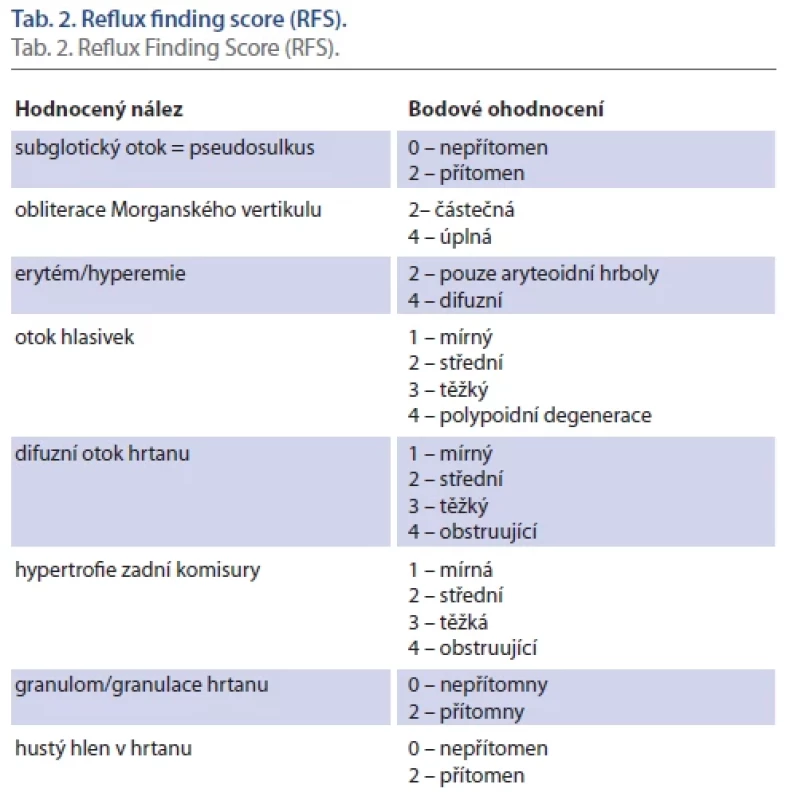
Výsledky
Prevalence IP novojičínského regionu je 4,87 % (graf 1). Ve sledovaném období 20 měsíců bylo vyšetřeno 821 pacientů splňujících kritéria pro zařazení do souboru A nebo B. IP jsme diagnostikovali u 40 z nich. Mezi diagnostikovanými pacienty bylo 18 mužů (45 %) a 22 žen (55 %). Průměrný věk pacientů s IP byl 52 let v rozpětí 27–78 let (graf 2). V souboru bylo zachyceno 33 pacientů (82,5 %) s jedním ostrůvkem heterotopické žaludeční sliznice a 7 (17,5 %) se dvěma ostrůvky. Více než dva ostrůvky nebyly pozorovány.
Graph 1. Prevalence IP na Novojičínsku.
Graph 1. Prevalence of IP in Nový Jičín region.
Graph 2. Histogram věku pacienta s IP.
Graph 2. Age histogram of patients with IP.
Soubor A – gastrofibroskopické vyšetření
Ve sledovaném období podstoupilo gastrofibroskopické vyšetření 799 pacientů, kteří splňovali kritéria pro zařazení do skupiny a vyšetření u nich provedl stejný lékař. Prevalence IP v souboru byla 4,76 %. Počet pacientů s diagnostikovaným IP byl 38, z toho 16 mužů (42,1 %) a 22 žen (57,9 %). Průměrný věk byl 52 let v rozpětí 27–77 (graf 3).
Graph 3. Soubor A s IP, histogram věku.
Graph 3. Age distribution in IP patients, group A.
Soubor B – přímé vyšetření jícnu
Do souboru bylo zařazeno 22 pacientů, kteří podstoupili přímé vyšetření jícnu v celkové anestezii za hospitalizace na ORL oddělení. Záchyt IP byl u 2 pacientů, 1 muže a 1 ženy. Prevalence IP v souboru byla 9,1 % (graf 4). V souboru bylo 20 mužů (91,9 %) a 2 ženy (9,1 %) s věkovým průměrem 62 let v rozmezí 44–78 let. Nejčastější indikací k přímému vyšetření jícnu byla onkologická onemocnění v ORL oblasti (mimo jícen) a dispenzarizace po jejich léčbě (77,27 %).
Graph 4. Soubor B, prevalence při přímé ezofagoskopii.
Graph 4. Group B, prevalence in esophagoscopy.
Soubor C – ambulantní vyšetření ORL
Do souboru bylo zařazeno 17 pacientů (42,5 %) z celkem 40 s diagnostikovaným IP, kteří souhlasili s následným ORL vyšetřením. V souboru bylo 5 mužů (29,4 %) a 12 žen (70,6 %) s věkovým průměrem 49 let v rozpětí 27–77 let. V rámci vyšetření byl pacienty vyplněn RSI dotazník s bodovým rozmezím 0–45. Průměrný výsledek byl 7,7 bodu, medián 8, s rozpětím výsledků 0–27 bodů. Dotazník byl hodnocen pozitivně 15 pacienty (88,2 %), 2 pacienti neudávali žádné subjektivní obtíže a jejich bodový součet RSI činil 0. Pouze u 4 pacientů (23,5 %) byl součet RSI vyšší než 13 a poukazoval na velkou pravděpodobnost, že obtíže byly způsobeny extraezofageálním refluxem (EER) [23, 24]. Nejčastěji udávanými obtížemi podle dotazníku RSI byly obtěžující tvorba hlenů a pocit knedlíku v krku, shodně udávány 10 pacienty (58,8 %). Pocit knedlíku v krku byl častěji udáván s vyššími bodovými hodnotami a jeho průměrná hodnota činila 1,29 (tab. 3).
Table 3. Soubor C, výsledky dotazníku RSI.
Tab. 3. Group C, RSI results.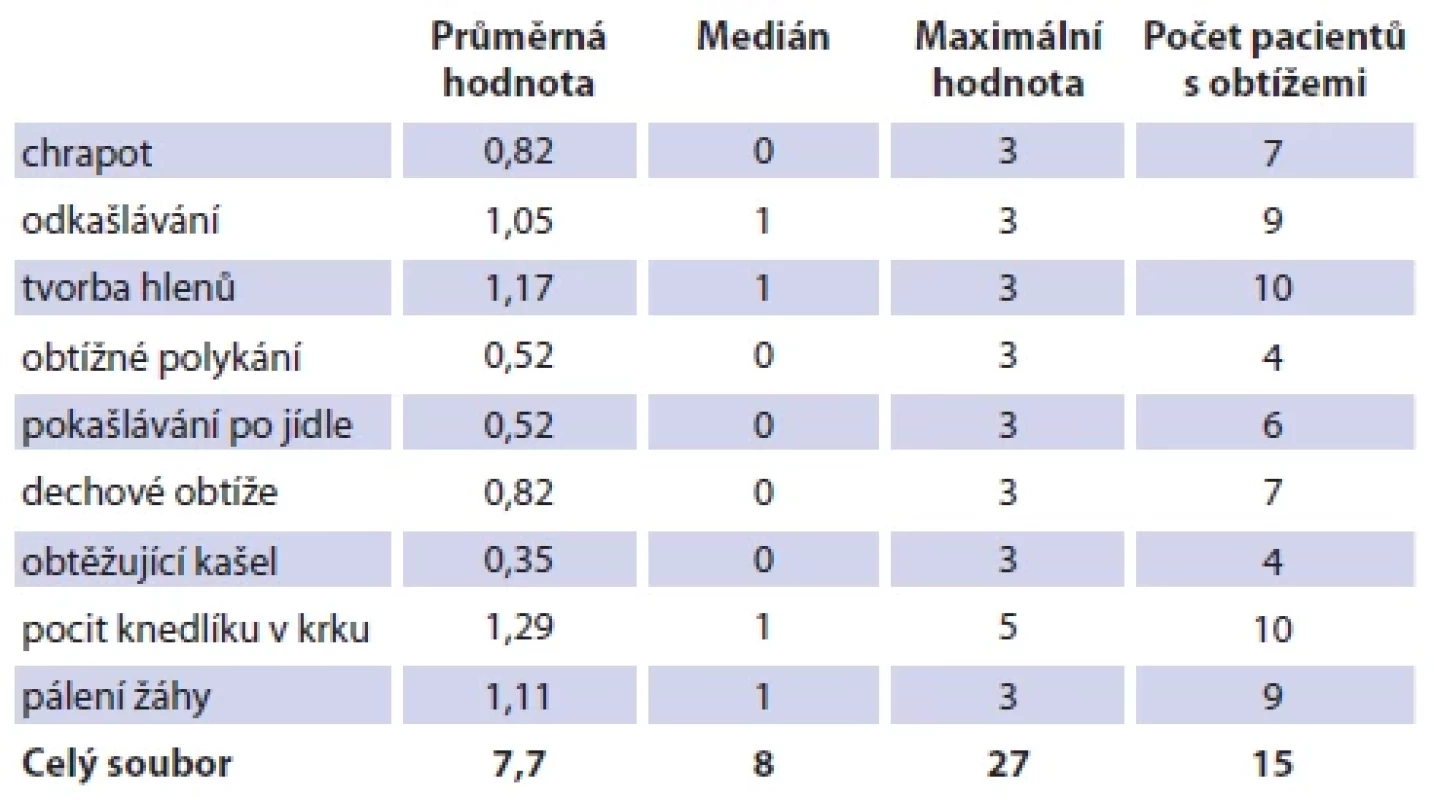
Videoendoskopickým ORL vyšetřením byla hodnocena oblast hrtanu podle RFS s rozpětím hodnot 0–26. Průměrná hodnota RFS byla 3,17 s mediánem 3 a rozpětím výsledků 0–14 (tab. 4). Hodnota vyšší než 1 byla zaznamenána u 12 pacientů (70,5 %). Nejčastější patologie byla hypertrofie zadní komisury pozitivně hodnocena u 9 pacientů (52,9 %). Součet RFS > 7, který předpokládá, že hrtanový nález je způsoben EER [20, 21], byl pouze u 1 pacienta (5,88 %). U všech 4 pacientů s RSI > 13 a předpokládanou příčinou obtíží v EER byla hodnota RFS < 7 v rozpětí 0–6. V rámci souboru C jsme neprokázali přímou souvislost mezi výskytem IP a subjektivně udávanými symptomy EER pomocí RSI ani významný vliv IP na sliznici hrtanu hodnocenou videoendoskopicky podle RFS.
Table 4. Soubor C, výsledky Refl ux fi nding score.
Tab. 4. Group C, Refl ux Finding Score.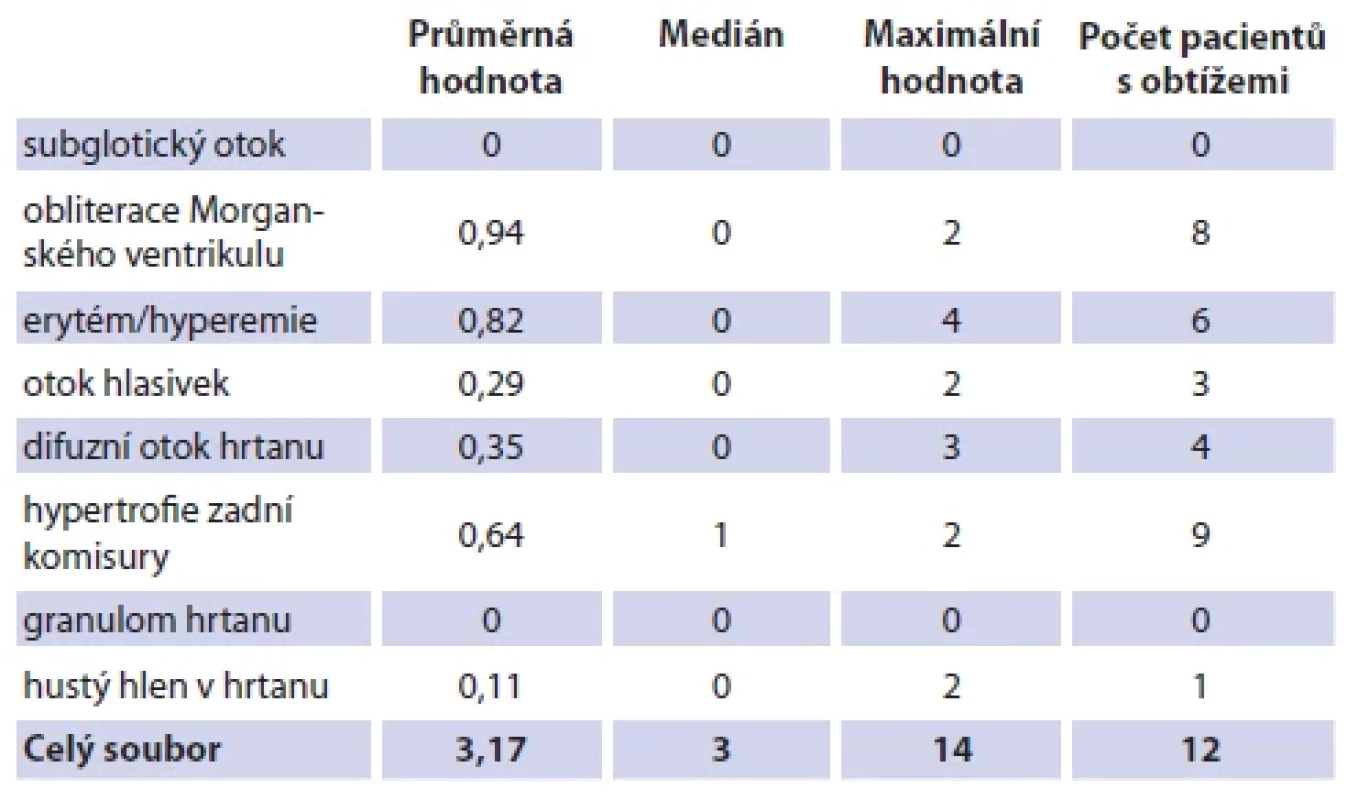
Diskuze
Vznik IP
Heterotopická žaludeční sliznice oblasti horního jícnu představuje ostrůvek sliznice nacházející se distálně od horního jícnového svěrače. První zmínka o IP v horním jícnu je v pitevní studii z roku 1805, kde je popisován jako aberantní sliznice žaludku [23]. U IP se předpokládá embryonální původ. Nejčastěji zmiňovaná teorie udává, že po rekanalizaci jícnu je jeho povrch pokryt cylindrickým epitelem. V 11. embryonálním týdnu (24. týden těhotenství) dochází k postupné přeměně cylindrického epitelu v dlaždicobuněčný. Proces začíná v prostřední části jícnu a šíří se do obou směrů – proximálně i distálně. Proximální část jícnu bývá poslední částí transformace, což může vysvětlovat zvýšený výskyt heterotopické žaludeční sliznice právě v této oblasti [1–4]. Méně pravděpodobná teorie předpokládá metaplastickou transformaci dlaždicobuněčného epitelu v cylindrický působením chronického zánětu na podkladě kyselého refluxu [5]. Třetí teorie předpokládá rupturu uzavřené jícnové cysty, která vede ke vzniku retenční cysty s následnou transformací v epitel cylindrický [2, 5, 24]. Patogeneze heterotopické žaludeční sliznice v GIT není dodnes úplně vysvětlena, protože její výskyt je popisován v průběhu celé délky trávicí trubice s největší incidencí v oblasti Meckelova divertiklu [4, 5, 16]. Histopatologicky se nejčastěji jedná o cylindrickou sliznici bohatou na oxyntické buňky. Tyto buňky jsou schopny produkovat kyselinu chlorovodíkovou i trávicí enzymy. To může vést ke klinickým projevům LPR spojovaným s nálezem IP [2, 5–7]. IP bývá nejčastěji diagnostikováno pomocí gastrofibroskopie v bílém světle nebo ve světelném modu Narrow Band Imaging (NBI).
Diagnostika
Prevalence IP se uvádí 1–15 % a není ovlivněna etnickou příslušností nebo geografickou polohou studované populace [6, 13, 14, 17]. Největší vliv na záchytu IP má povědomí lékaře provádějícího vyšetření a pečlivé vyšetření oblasti horního jícnu [2, 8, 9, 13, 14, 17]. Prevalence IP na Novojičínsku byla 4,87 % u pacientů v souborech A i B. Výsledek odpovídá rozpětí prevalence, která je popisována v literatuře [5, 6, 9, 12–15]. Některé publikace uvádí prevalenci nižší 1–2 % [14, 15], jiné obdobnou 4,7 % [13] a některé vyšší, až 10 % u vyšetření v bílém světle [5, 9, 12]. Nejvyšší prevalenci, až 14,5 % [17], udávají studie prováděné v zobrazení polarizovaným světlem NBI, které výrazně zvyšuje detekci IP [13, 17]. Prevalence v souboru A při gastroskopickém vyšetření byla 4,76 %, zatímco v souboru B při přímé ezofagoskopii v celkové anestezii byla dokonce 9,1 %. Rozdílná prevalence v našich souborech je způsobena rozdílnou velikostí souborů, 799 pacientů (soubor A), resp. 22 pacientů (soubor B), resp. Předpokládáme, že při obdobné velikosti souborů by byl rozdíl prevalence mezi soubory minimální. Další příčinou rozdílných výsledků by mohlo být důslednější vyšetření horního jícnu v celkové anestezii. Při vyšetření v anestezii je dostatek času na prohlédnutí oblasti výskytu IP a jeho diagnostika pod endoskopickou kontrolou. Při rigidní ezofagoskopii není běžné použití endoskopické kontroly a léze může být přehlédnuta. V běžné praxi tak může být naopak větší záchyt IP při gastrofibroskopickém vyšetření než při rigidní ezofagoskopii. Při gastrofibroskopickém vyšetření, které trvá průměrně 5–10 minut, však může být léze také přehlédnuta. Při vyšetření se oblast horního jícnu prohlíží jako poslední těsně před vytažením gastrofibroskopu z jícnu. Přítomnost gastrofibroskopu v oblasti horního jícnu vyvolá dávivý reflex pacienta a lékař raději výkon ukončí dříve, než aby provedl důsledné vyšetření této oblasti. Ve studiích je popsán vyšší záchyt IP u endoskopistů, kteří jsou seznámeni s problematikou IP a oblast horního jícnu prohlížejí důkladně [2, 5, 6, 8, 9, 13, 17]. V naší studii gastrofibroskopické i ORL vyšetření prováděl stejný lékař, seznámený s výskytem IP. Tímto jsme snížili riziko přehlédnutí léze pro neznalost. Pokud by bylo při diagnostice v obou souborech využito zobrazení NBI, byla by prevalence IP pravděpodobně vyšší, protože bylo prokázáno, že modus NBI zvyšuje detekci malých IP až 3× v porovnání s vyšetřením v bílém světle [8, 13, 14, 17]. V našem souboru 40 diagnostikovaných pacientů jsme lézi prokázali u 18 mužů (45 %) a 22 žen (55 %). Naše data odpovídají rozsáhlým souborům, kde také nebyla pozorována rozdílná prevalence IP mezi pohlavím [5, 16].
Klinické projevy
IP jsou považovány za benigní a často asymptomatické léze, proto jejich nález při endoskopii nevyžaduje rutinní odběr biopsie [2, 6, 7, 10]. Mezi literaturou popisované komplikace IP patří slizniční prstence až striktury, častější uváznutí sousta, vředy, krvácení, perforace a tracheoezofageální fistula [2–4, 7, 11, 16]. V 0,1–1,5 % případů jsou popisovány maligní transformace v adenokarcinom jícnu, nejčastěji metaplasticko-dysplastickou transformací sliznice [1, 2, 16, 19]. Basseri et al. popisují kazuistiku vlivu IP na vznik karcinomu hrtanu [11]. V našem souboru pacientů nebyla popsána žádná komplikace související s IP.
Ve studiích bývá spojován vyšší výskyt symptomů LPR s přítomností IP u 10–73 % případů [1, 5, 7, 10, 16]. Další studie naopak neprokázaly přímou souvislost mezi IP a příznaky LPR [6, 10, 17]. V našem souboru C udávalo příznaky LPR > 1 podle dotazníku RSI 15 ze 17 pacientů (88,2 %) s průměrnou hodnotou 7,7 bodu. Podle Zeleníka et al. lze EER předpokládat u pacientů s hodnotou RSI > 13 [20]. V našem souboru udávali 4 pacienti výsledek RSI > 13 (23,52 %), naznačující souvislost příznaků s EER. Fibroskopické vyšetření hrtanu u těchto pacientů bylo hodnoceno podle RFS < 7. Tento výsledek neprokázal vliv IP na sliznici hrtanu a souvislost s příznaky LPR v souboru. Důkazem o vlivu IP na LPR a sliznici hrtanu u našich pacientů s RSI > 13 by mohlo být provedení 24hodinové dvoukanálové pH-metrie, která v některých studiích prokázala EER v horním jícnu a v hrtanu a zároveň normální pH v oblasti dolního jícnového svěrače [11, 16, 25]. Toto vyšetření v naší studii nebylo prováděno. Domníváme se, že u pacientů s prokázaným IP bez efektu konzervativní léčby by měla být doplněna duální pH-metrie v rámci další diagnostiky obtíží.
Práce Weickerta et al. popisuje skupinu pacientů s nálezem IP a příznaky LPR nereagujícím na běžnou terapii inhibitory protonové pumpy (PPI). Po histologickém vyšetření bylo prokázáno, že u těchto pacientů ve sliznici IP nebyly přítomny buňky produkující kyseliny nebo enzymy, ale buňky produkující hlen [10]. Tato nadměrná produkce hlenu ve sliznici IP by mohla být příčinou obtíží i našich pacientů, kteří neměli průkaz působení kyselin a trávicích enzymů na sliznici hrtanu. Toto je pouze naše domněnka, protože jsme neprováděli rutinní biopsii ani pH-metrii při diagnostice IP. Mezi nejčastější příznaky LPR (tab. 1) u pacientů s diagnostikovaným IP patří pocit knedlíku v krku [7, 12, 25] a obtěžující kašel, který bývá častější u větších lézí [5, 16]. V našem souboru C byly oba příznaky zaznamenány nejčastěji, a to u 10 ze 17 pacientů (58,82 %) (tab. 3). Studie Peitze et al. a Latose et al.souvislost mezi IP a příznaky LPR neprokázaly [6, 17]. V našem souboru nebyl rovněž vliv IP na příznaky LPR a sliznici hrtanu prokázán. V případě přetrvávajícího LPR a potvrzeném IP by provedení biopsie mohlo pomoci s dalším terapeutickým postupem.
Léčba
V současnosti neexistují standardizované léčebné strategie u pacientů s diagnostikovaným IP [3]. Asymptomatičtí pacienti s náhodným nálezem IP nevyžadují léčbu. U pacientů s příznaky LPR, jako je kašel, pocit knedlíku v krku, bolesti v krku, chrapot, zahlenění apod. [20], se v terapii uplatňují medikamentózní nebo endoskopické přístupy. V konzervativní terapii je užíván stejný přístup jako u EER. Je doporučována dieta, inhibitory protonové pumpy, případně prokinetika [3]. Terapie PPI je nejčastěji volena jako diagnosticko-terapeutický test s užitím omeprazolu 20 mg 2× denně. Délka léčby se různí od 4–8 týdnů [25] po 3–6 měsíců [20]. Při nedostatečném efektu je možné navýšit omeprazol na 40 mg 2× denně [3, 20]. Při přetrvání obtíží je vhodné zvážit doplnění pH-metrie k průkazu tvorby kyselin v horním jícnu. Při histologickém průkazu heterotopické sliznice horního jícnu, pozitivním nálezu na pH-metrii a přetrvávajících obtížích po konzervativní terapii trvající déle než 2 měsíce je možné přistoupit k endoskopickému řešení argonovou plazmako - agulací. Tato metoda je široce dostupná na gastroenterologických pracovištích. Úlevový efekt nastává do 8 týdnů od výkonu, ale léčba je spojena s rizikem vzniku stenóz [24]. Další metodou je radiofrekvenční ablace, kde je popisována úspešnost léčby až 80 %, nízký výskyt komplikací a dlouho trvající efekt [18].
Závěr
Inlet patch je v rámci ORL oboru vzácně diskutovaná a velmi málo diagnostikovaná léze, která může mít vliv na stav sliznic ORL oblasti. Ve studovaném souboru pacientů byla zjištěna prevalence IP 4,87 %. Při gastroskopickém vyšetření 4,76 % a při přímém vyšetření jícnu 9,1 %. Většina pacientů byla asymptomatická a neudávala typické obtíže spojované s LPR. V našem souboru jsme neprokázali souvislost mezi výskytem IP, subjektivně udávanými symptomy EER zjištěnými dotazníkem RSI nebo vliv IP na sliznici hrtanu hodnocenou RFS. V případě neúspěšné konzervativní léčby příznaků EER by neměla být diagnóza IP opomíjena. U pacientů s obtížně léčitelným EER by v diagnostice mělo být doplněno gastrofibroskopické vyšetření se zaměřením na výskyt IP a jeho biopsie. Při průkazu IP by měla být provedena dvoukanálová pH-metrie. V případě biop - ticky ověřené léze IP s potvrzeným kyselým refluxem v oblasti horního jícnu je možností terapie endoskopická ablace ložiska heterotopické žaludeční sliznice horního jícnu. Osvěta k výskytu IP je nutná jak mezi lékaři ORL, tak gastroenterology, a vyžaduje jejich vzájemnou mezioborovou spolupráci.
Prohlášení o střetu zájmu
Autor práce prohlašuje, že v souvislosti s tématem, vznikem a publikací této práce není ve střetu zájmů a vznik ani publikace nebyly podpořeny žádnou farmaceutickou firmou.
ORCID autorů
M. Enter ORCID 0009-0005-4570-9827,
J. Syrovátka ORCID 0009-0005-5381-6315.
Přijato k recenzi: 3. 10. 2022
Přijato k tisku: 25. 11. 2022
MU Dr. Michal Enter
Oddělení ORL a chirurgie hlavy a krku
Nemocnice AGEL Nový Jičín a.s.
Otorinolaryngol Foniatr 2023; 72(3): 136 – 142
Purkyňova 2138/ 16
741 01 Nový Jičín
Sources
1. Orosey M, Amin M, Cappell MS. A 14-Year Study of 398 Esophageal Adenocarcinomas Diagnosed Among 156,256 EGDs Performed at Two Large Hospitals: An Inlet Patch Is Proposed as a Significant Risk Factor for Proximal Esophageal Adenocarcinoma. Dig Dis Sci 2018; 63(2): 452–465. Doi: 10.1007/ s10620-017-4878-2.
2. Linter R, Kubát J, Mezera V et al. Neobvyklý případ dysfagie horního typu. Gastroent Hepatol 2020; 74(3): 250–255. Doi:10.14735/ amgh2020250.
3. Ciocalteu A, Popa P, Ionescu M et al. Issues and controversies in esophageal inlet patch. World J Gastroenterol 2019; 25(30): 4061–4073. Doi: 10.3748/ wjg.v25.i30.4061.
4. Rahden BH von, Stein HJ, Becker K et al. Heterotopic gastric mucosa of the esophagus: literature-review and proposal of a clinicopathologic classification. Am J Gastroenterol 2004; 99(3): 543–551. Doi: 10.1111/ j.1572-0241.2004.04082.x.
5. Chong VH, Jalihal A. Heterotopic gastric mucosal patch of the esophagus is associated with higher prevalence of laryngopharyngeal reflux symptoms. Eur Arch Otorhinolaryngol 2010; 267(11): 1793–1779. Doi: 10.1007/ s00405 - 010-1259-2.
6. Latos W, Sieroń-Stołtny K, Kawczyk-Krupka A et al. Clinical evaluation of twenty cases of heterotopic gastric mucosa of upper esophagus during five-year observation, using gastroscopy in combination with histopathological and microbiological analysis of biopsies. Contemp Oncol 2013; 17(2): 171–175. Doi:10.5114/ wo.2013.34376.
7. Cock C, Hamarneh Z. Gastric inlet patches: symptomatic or silent? Curr Opin Otolaryngol Head Neck Surg 2019; 27(6): 453–462. Doi: 10.1097/ MOO.0000000000000581.
8. Maconi G, Pace F, Vago L et al. Prevalence and clinical features of heterotopic gastric mucosa in the upper oesophagus (inlet patch). Eur J Gastroenterol Hepatol 2000; 12(7): 745–749. Doi: 10.1097/ 00042737-200012070-00005.
9. López-Colombo A, Jiménez-Toxqui M, Gogeascoechea-Guillén PD et al. Prevalence of esophageal inlet patch and clinical characteristics of the patients. Rev Gastroenterol Mex 2019; 84(4): 442–448. Doi: 10.1016/ j.rgmx.2018.07.003.
10. Weickert U, Wolf A, Schröder C et al. Frequency, histopathological findings, and clinical significance of cervical heterotopic gastric mucosa (gastric inlet patch): a prospective study in 300 patients. Dis Esophagus 2011; 24(2): 63–68. Doi: 10.1111/ j.1442-2050.2010.01091.x.
11. Basseri B, Conklin JL, Mertens RB et al. Heterotopic gastric mucosa (inlet patch) in a patient with laryngopharyngeal reflux (LPR) and laryngeal carcinoma: a case report and review of literature. Dis Esophagus 2009; 22(4): E1–E5. Doi: 10.1111/ j.1442-2050.2008.00915.x.
12. Chong VH. Cervical inlet patch: an important cause of Globus pharyngeus. Eur Arch Otorhinolaryngol 2018; 275(12): 3101–3102. Doi: 10.1007/ s00405-018-5132-z.
13. Cheng CL, Lin CH, Liu NJ et al. Endoscopic diagnosis of cervical esophageal heterotopic gastric mucosa with conventional and narrow--band images. World J Gastroenterol 2014; 20(1): 242–249. Doi:10.3748/ wjg.v20.i1.242.
14. Chung CS, Lin CK, Liang CC et al. Intentional examination of esophagus by narrow-band imaging endoscopy increases detection rate of cervical inlet patch. Dis Esophagus 2015; 28(7): 666–672. Doi: 10.1111/ dote.12252.
15. Sahin G, Adas G, Koc B et al. Is cervical inlet patch important clinical problem? Int J Biomed Sci 2014; 10(2): 129–135.
16. Chong VH. Clinical significance of heterotopic gastric mucosal patch of the proximal esophagus. World J Gastroenterol 2013; 19(3): 331–338. Doi: 10.3748/ wjg.v19.i3.331.
17. Peitz U, Vieth M, Evert M et al. The prevalence of gastric heterotopia of the proximal esophagus is underestimated, but preneoplasia is rare – correlation with Barrett‘s esophagus. BMC Gastroenterol 2017; 17(1): 87. Doi: 10.1186/ s12876-017-0644-3.
18. Dunn JM, Sui G, Anggiansah A et al. Radiofrequency ablation of symptomatic cervical inlet patch using a through-the-scope device: a pilot study. Gastrointest Endosc 2016; 84(6): 1022–1026. Doi: 10.1016/ j.gie.2016.06.037.
19. Dziadkowiec KN, Sánchez-Luna SA, Stawinski P et al. Adenocarcinoma Arising From a Cervical Esophageal Inlet Patch: The Malignant Potential of a Small Lesion. Cureus 2020; 12(7): e9284. Doi: 10.7759/ cureus.9284.
20. Zeleník K, Komínek P, Stárek I et al. Extraezofageální reflux (2. část). ORL manifestace a léčba. Otorinolaryngol Foniatr 2008; 57(3): 151–158.
21. Zeleník K, Kopřivová H, Stárek I et al. Reflux Finding Score. Otorinolaryngol Foniatr 2010; 59(1): 28–31.
22. Zeleník K, Kopřivová H, Komínek P. Extraezofageální reflux: porovnání základních diagnostických metod (Reflux symptom index, Reflux finding score, diagnosticko-terapeutický test, pH-metrie). Otorinolaryngol Foniatr 2011; 60(2): 71–77.
23. Schmidt FFA. De mammalium oesophage atque ventriculo. Inaugural dissertation. Halle in off Bathenea. 1805.
24. Bajbouj M, Becker V, Eckel F et al. Argon plasma coagulation of cervical heterotopic gastric mucosa as an alternative treatment for globus sensations. Gastroenterology 2009; 137(2): 440–444. Doi: 10.1053/ j.gastro.2009.04.053.
25. Rusu R, Ishaq S, Wong T et al. Cervical inlet patch: new insights into diagnosis and endoscopic therapy. Frontline Gastroenterol 2018; 9(3): 214–220. Doi: 10.1136/ flgastro-2017-100855.
Labels
Audiology Paediatric ENT ENT (Otorhinolaryngology)
Article was published inOtorhinolaryngology and Phoniatrics
2023 Issue 3-
All articles in this issue
- Sledování pacientů s nádory hlavy a krku: soubor doporučení České kooperativní skupiny pro nádory hlavy a krku
- Editorial
- Rinosinusitida jako komplikace FESS: je prospěšná antibiotická profylaxe?
- Využití fluoresceinu ke zlepšení senzitivity flexibilního endoskopického vyšetření polykání
- Diagnostika heterotopické žaludeční sliznice horního jícnu a její vliv na sliznici hrtanu
- Poleptání jícnu a žaludku – nejnovější pohled na diagnostiku a léčbu
- Cervikofaciálny podkožný emfyzém po preventívnej dentálnej hygiene – kazuistika
- Warthinův tumor nosohltanu – kazuistika a přehled literatury
- Prof. MU Dr. Arnošt Pellant, DrSc. – 80letý
- Prof. MU Dr. Pavel Komínek, Ph.D., MBA – 65letý
- Otorhinolaryngology and Phoniatrics
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Poleptání jícnu a žaludku – nejnovější pohled na diagnostiku a léčbu
- Cervikofaciálny podkožný emfyzém po preventívnej dentálnej hygiene – kazuistika
- Rinosinusitida jako komplikace FESS: je prospěšná antibiotická profylaxe?
- Diagnostika heterotopické žaludeční sliznice horního jícnu a její vliv na sliznici hrtanu
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

