-
Medical journals
- Career
Zkušenosti se sekundární implantací hlasových protéz na Klinice otorinolaryngologie a chirurgie hlavy a krku ve Fakultní nemocnici Olomouc v letech 2016–2021
Authors: P. Beláková; M. Brož; Richard Salzman
Authors‘ workplace: Klinika otorinolaryngologie a chirurgie hlavy a krku LF UP a FN Olomouc
Published in: Otorinolaryngol Foniatr, 72, 2023, No. 1, pp. 15-22.
Category: Original Article
doi: https://doi.org/10.48095/ccorl202315Overview
Úvod: Totální laryngektomie je jedna z možností léčby pacientů v pokročilém stadiu karcinomu hrtanu. Tento výkon je spojen s výrazným ovlivněním kvality života pacientů po operaci, kteří přichází o možnost přirozené tvorby hlasu vedoucí k psychologické i sociální stigmatizaci. Nejmodernější a nejvíce preferovaná možnost náhrady hlasu je implantace hlasové protézy. Implantovat lze primárně, v průběhu totální laryngektomie, anebo sekundárně s časovým odstupem od operace. Na našem pracovišti jsme zahájili sekundární implantaci hlasových protéz v květnu 2016. Metodika: Retrospektivní studie má za cíl vyhodnotit průměrný interval výměn hlasových protéz, četnost a důvody výměn u pacientů se sekundárně implantovanou hlasovou protézou na Klinice otorinolaryngologie a chirurgie hlavy a krku ve Fakultní nemocnici Olomouc v období od května 2016 do konce června 2021. Výsledky: Ve sledovaném souboru 17 pacientů se sekundárně implantovanou hlasovou protézou jsme provedli celkem 94 výměn. Průměrná životnost hlasové protézy je v našem souboru pacientů 127 dnů. Nejčastější indikací k výměně protézy bylo protékání v 52 % případů. Závěr: Životnost protéz v našem souboru je delší než uváděná v literatuře. Protékání je nejčastější indikací k výměně protézy.
Klíčová slova:
hlasová protéza – totální laryngektomie – karcinom hrtanu
Úvod
Totální laryngektomie (TLE) je operační zákrok, který se provádí u pokročilých stadií karcinomu hrtanu jako jedna z léčebných modalit. Tento rozsahem výjimečný chirurgický zákrok má pochopitelně pro pacienta četné nežádoucí následky. Mezi hlavní patří trvalá tracheostomie a ztráta přirozeného hlasu, které výrazně zhoršují kvalitu života pacientů, což má za následek sociální a psychologické stigma. K dalším často opomíjeným následkům patří porucha vnímání chuti a čichu [1].
Schopnost mluvit a komunikovat je jedinečnou lidskou schopností a je zásadní pro mnoho činností každodenního života. V současné době existují tři hlavní metody hlasové rehabilitace: jícnová řeč, elektrolarynx a řeč pomocí tracheoezofageální píštěle (TeP) s implantovanou hlasovou protézou (HP) [2].
Jícnový hlas – ructus neboli říhnutí je nejpřirozenější náhradní hlasový mechanizmus po TLE. Zvuk při něm vzniká na principu vibrací v místě horního jícnového svěrače při aktivním unikání vzduchu z jícnu. Vzduch se do jícnu dostává jícnovou insuflací – polykáním vzduchu, poté je uvolňován z jícnu kontrolovaným způsobem. Vzduchový sloupec je veden přes zbytkový artikulační aparát, kde je upraven tak, aby vytvořil srozumitelný hlas. Výhodou je, že ructus nezaměstnává ruce pacienta, také nehrozí aspirace vzhledem k odděleným dýchacím a polykacím cestám. Jícnový hlas je ale nepřirozeně hluboký, monotónní, neumožňuje plynulou výslovnost víceslabičných slov. Výuka je náročná a dlouhodobá, její úspěšnost je relativně nízká [2, 3].
Elektrolarynx představuje jednu z dalších alternativ hlasu po TLE. Tato elektromechanická pomůcka ve tvaru válečku se při řeči přikládá zevně na spodinu dutiny ústní. Pacient vytváří řeč pouhou artikulací s využitím zvukové energie elektrolaryngu. Manipulace a použití přístroje jsou jednoduché, zvládne je většina pacientů. Nevýhodou je, že zaměstnává ruku pacienta, navíc má nepřirozený robotický zvuk při komunikaci [3].
Hlasová protéza představuje v současnosti hlavní způsob tvorby náhradního hlasu po TLE (obr. 1). Využívá podobně jako jícnový hlas vibrace sliznice ezofagohypofaryngeálního přechodu. Na rozdíl od ructu ale pacient využívá k vytvoření fonace podobně jako při přirozené mluvě proud vzduchu z plic. HP představuje ventil, který umožňuje přesměrovat proud vzduchu z plic opět do horních cest dýchacích, pokud si pacient při výdechu uzavře tracheostomii. Ventil je jednocestný, takže protéza přitom brání před zatékáním slin a potravy do dolních cest dýchacích. HP lze zavést primárně v průběhu TLE, nebo sekundárně s časovým odstupem. Výhodou protézy je jednoduchý nácvik hlasu, vysoká úspěšnost hlasové rehabilitace. Ve srovnání s jícnovou řečí kvalita a srozumitelnost řeči je u HP výrazně lepší [3]. K nevýhodám patří, že většina pacientů při fonaci musí používat ruku. Výjimkou jsou handsfree sady, které ale u nás nehradí zdravotní pojišťovna. O protézu je nutné pečovat, pravidelně ji čistit. I přes nynější vysokou biokompatibilitu použitých materiálů HP stále dochází k určitým problémům a komplikacím, které vyžadují relativně časté výměny HP a tedy návštěvu lékaře [3].
Image 1. Implantovaná hlasová protéza v tracheostomatu pacienta po totální laryngektomii.
Fig. 1. Voice prosthesis implanted in a patient after total laryngectomy.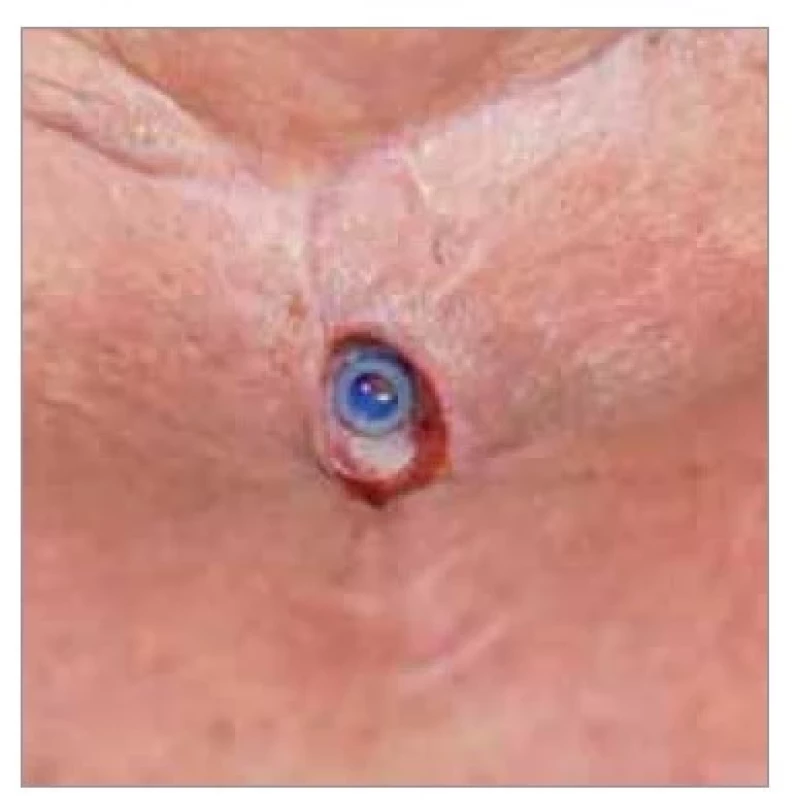
Vlivem trvalého mikrobiálního osídlení silikonového povrchu protézy, zejména kvasinkami, dochází k její postupné biodegradaci, která zapříčiní poruchu těsnosti HP. Následně může docházet k protékání protézy s nutností její výměny. Obstrukce HP je méně častou komplikací, která má za následek zhoršení fonace, může vzniknout ucpáním HP sekretem nebo naléháním protézy na zadní stěnu jícnu. Řešením je výměna protézy za menší velikost. Při zvolení nevhodné velikosti HP může dojít k prosakování kolem ní. Obtékání vzniká také v důsledku atrofií tkáně kolem TeP, která způsobí její rozšíření. Pokud zavedení těsnicího kroužku nevede k utěsnění píštěle, je nutné shunt zmenšit. Zmenšení lze provést stažením píštěle stehem nebo aplikací výplně (tuk, kolagen) do jejího okolí, event. dočasným odstraněním protézy s vyvoláním slizniční reakce tvorba granulací poleptáním, kauterizací [4]. Nutnost uzávěru píštěle lalokem je vzácná. V okolí protézy často vznikají granulace, které můžou mít vliv na zhoršení fonace. Granulace lze ošetřovat leptáním, nebo elektokauterizací. Dislokace protézy způsobí zhoršení fonace, protože dýchací a polykací cesty nejsou poté dostatečně propojeny. Dislokace nebo vypadnutí HP může vzniknout při neodborné manipulaci, například při čištění protézy většinou v terénu chronické zánětlivé reakce na cizí těleso. Protéza může být tedy spolknuta, nebezpečnější je však její aspirace. Zcela raritně může vzniknou perforace jícnu a mediastinitida.
Na klinice ve Fakultní nemocnici Olomouc jsme zahájili sekundární implantaci hlasových protéz v květnu 2016. Primární implantace vykonáváme od července 2020 po získání dostatečných zkušeností s HP.
Cílem práce bylo zhodnotit soubor pacientů po totální laryngektomii se sekundárně implantovanou hlasovou protézou na Klinice otorinolaryngologie a chirurgie hlavy a krku ve Fakultní nemocnici Olomouc.
Metodika
Retrospektivním sledováním nemocných po totální laryngektomii jsme vytvořili soubor pacientů se sekundárně implantovanou hlasovou protézou na Klinice otorinolaryngologie a chirurgie hlavy a krku ve Fakultní nemocnici Olomouc v období od května 2016 do června 2021. U všech hodnocených pacientů byla sekundárně zavedena protéza Provox Vega© (Atos Medical, Švédsko).
V sledovaném souboru jsme hodnotili věk pacientů, pohlaví, časové období, kdy byla po totální laryngektomii zavedena hlasová protéza, zda pacient podstoupil radioterapii (RT), resp. chemoradioretapii (ChRT), celkový počet výměn HP u jednotlivých pacientů, v jakém časovém odstupu byly nutné výměny hlasových protéz, příčinu výměny protézy, nutnost hospitalizace a celkové anestezie při jednotlivých výměnách, komplikace po zavedení hlasové protézy.
Zjištěné výsledky jsme porovnávali s literaturou získanou literární rešerší z databáze MedLine.
Výsledky
Popis souboru
Ve sledování máme nyní celkem 27 pacientů s implantovanou HP, z nich je 10 implantováno primárně. Vzhledem ke krátké době sledování a malému počtu výměn HP nebyly primárně implantovaní pacienti zařazeni do studie. Všech 17 pacientů se sekundárně implantovanou HP bylo zařazeno do studie. Všechny základní informace o sledovaném souboru jsou shrnuty v tab. 1.
Table 1. Charakteristika pacientů ve sledovaném souboru sekundárních implantací.
HP – hlasová protéza, ChRT – chemoradioterapie, M – muž, RT – radioterapie, TLE – totální laryngektomie, Ž – žena
Tab. 1. Characteristics of patients in the monitored group of secondary implants.
HP – voice prosthesis, ChRT – chemoradiotherapy, M – male, RT – radiotherapy, TLE – total laryngectomy, Ž – female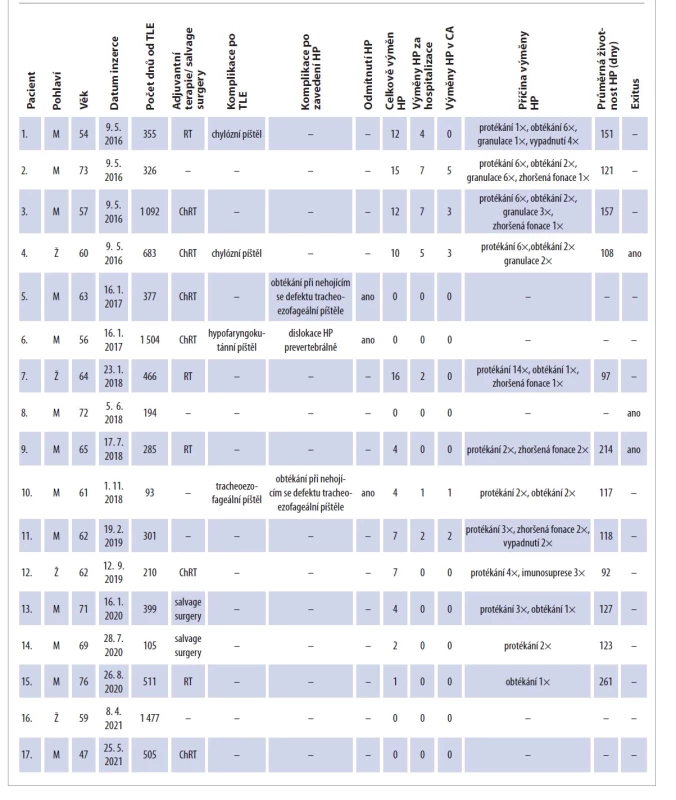
Ze 17 pacientů bylo celkem 13 mužů a 4 ženy. Věkový průměr v čase stanovení diagnózy maligního onemocnění vyžadujícího totální laryngektomii byl 63 let, nejmladšímu pacientovi bylo 47 let a nejstaršímu 76 let.
Adjuvantní RT nebo ChRT absolvovalo 10 pacientů. Další 2 pacienti podstoupili TLE jako salvage surgery po předchozí onkologické léčbě. Celkem 12 pacientů z našeho souboru absolvovalo léčbu zářením před implantací HP.
Průměrný počet dnů od provedení TLE k implantaci HP byl 523. Nejkratší doba od TLE k zavedení HP byla 93 dnů, naopak nejdelší byla 1 504 dnů. Pacienti, kteří podstoupili TLE po květnu 2016, kdy jsme zahájili program implantací HP na naší klinice, měli HP implantovanou průměrně 408 dnů od provedení TLE.
Životnost protéz a četnost výměn
Průměrný časový interval mezi jednotlivými výměnami byl 127 dnů. Nejdelší životnost hlasové protézy v našem souboru byla 433 dnů, naopak nejkratší interval mezi výměnami byl pouze 8 dnů.
Ve sledovaném období bylo provedeno v našem souboru pacientů celkem 94 výměn, do této hodnoty nejsou započteny prvotní implantace. Pět pacientů ve sledovaném souboru nemělo od implantace žádnou výměnu HP, jeden z pacientů náhle umřel krátce po prvotní implantaci na interní onemocnění, u dvou pacientů se vyskytla po zavedení HP závažná komplikace, a protéza musela být odstraněna, další znovuzavedení pacienti odmítli. Poslední dva pacienti byli implantováni v roce 2021, tedy ke konci sledování souboru, výměna HP tedy u nich ještě neproběhla.
Protékání bylo nejčastější příčinou výměny HP, a to ve 49 případech, tedy v 52 %. Druhou nejčastější příčinou výměny HP bylo obtékání, které jsme zaznamenali 17× (18 %).
Zpočátku jsme obtékání řešili dočasným vytažením HP, zajištěním polykacích cest nazogastrickou sondou (NGS), dýchacích cest tracheostomickou kanylou s balónkem, která brání aspiracím, a do TeP jsme vložili Nelatonův katétr, který zamezil úplnému zatažení píštěle. Po pár dnech, v našem případě 3–7 dnech podle klinického nálezu, pokud došlo k mírnému stažení píštěle, jsme opětovně zavedli HP, což jsme využívali v prvním roce od zahájení programu implantace HP, a to u 5 výměn HP pro obtékání. Obtékání lze řešit i aplikací tzv. těsnicích kroužků. Použili jsme těsnicí kroužky Provox® XtraFlange. Většinou bylo dostatečné zavedení jednoho těsnicího kroužku, v několika případech byly aplikovány 2 těsnicí kroužky a jednou vyřešily obtékání až 3 těsnicí kroužky. Ve dvou případech si obtékání vyžádalo uzavření TeP, což bude popsáno blíže v popisu komplikací.
Další příčiny výměny HP byly tvořící se granulace v tracheostomatu kolem hlasové protézy, které výrazně ovlivnily její funkčnost (12 případů, tedy 12,7 %), zhoršená fonace (7 případů) a nakonec spontánní vypadnutí protézy, které jsme zaznamenali v 6 případech. Sedm pacientů, kterým byla provedena výměna z důvodů zhoršení fonace, mělo zavedenou špatnou velikost HP. Po výměně za menší velikost došlo ke zlepšení fonace. U jedné imunosuprimované pacientky provádíme pravidelné výměny HP každé 3 měsíce z důvodu prevence infektu, i když HP je zcela funkční (3 výměny).
Celkem 14 výměn (15 %) bylo provedeno v celkové anestezii, nutnost hospitalizace byla u 28 výměn (30 %). Celkovou anestezii jsme využili převážně při výskytu granulací kolem protézy, kdy byly v apnoické pauze sneseny granulace elektrokauterem a následně provedena výměna protézy. Ve dvou případech byla výměna spojena s dalším výkonem vyžadujícím celkovou anestezii – exstirpace uzliny a kontrolní endoskopie. Dále jsme provedli výměnu HP v celkové anestezii při dislokaci HP do polykacích cest, kdy byla HP vytažena z hypofaryngu. Dvakrát u nefonujících pacientů, kdy byla HP povytažena a fistula v oblasti přední stěny jícnu byla téměř zatažena.
Závažné komplikace
Se závažnou komplikací po implantaci HP jsme se setkali celkem u 3 pacientů, kterým musela být HP odstraněna a další znovuzavedení odmítli. V prvním případě se jednalo o pacienta po TLE komplikované vznikem hypofaryngokutánní píštěle. Po prolongovaném hojení se nakonec zhojil bez nutnosti chirurgické revize. Pacient absolvoval adjuvantní ChRT. Po dosažení remise došlo postupně k rozvoji dysfagických obtíží. Na zobrazovacím rentgenu (rtg) polykacího aktu byla poté zjištěna stenóza jícnu. Pacient absolvoval opakovaně dilataci jícnu s dobrým efektem. S odstupem byl pacient doporučen k implantaci HP, po jejím zavedení došlo k dobrému fonačnímu zisku. Po necelých 3 týdnech nastalo zhoršení fonace a po několika dalších dnech si pacient všiml, že protéza v tracheostomatu chybí. Navíc došlo k rozvoji dysfagie. Při použití zobrazovacích metod se hlasová protéza našla dislokovaná v prevertebrální oblasti C5–C6 (obr. 2), navíc v okolí se známkami tvořící se abscesové dutiny. Následně přes rozdilatovanou tracheoezofageální píštěl byla provedena incize zadní stěny jícnu, evakuován tvořící se absces a extrahována protéza. Po zhojení pacient další znovuzavedení hlasové protézy odmítl.
Image 2. CT snímek – sagitální pohled. Hlasová protéza dislokovaná prevertebrálně – označeno šipkou (převzato z Korpová et al. [25]).
Fig. 2. CT image of a sagittal view. Voice prosthesis deployed prevertebrally – marked with an arrow (source from Korpová et al. [25]).![CT snímek – sagitální pohled.
Hlasová protéza dislokovaná prevertebrálně
– označeno šipkou (převzato
z Korpová et al. [25]).<br>
Fig. 2. CT image of a sagittal view. Voice
prosthesis deployed prevertebrally –
marked with an arrow (source from
Korpová et al. [25]).](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image_pdf/92e7b8964ed6f1987e0529a6f8b102b9.jpg)
Ve druhém případě byla HP zavedena do tracheoezofageální píštěle spontánně vytvořené jako komplikace po TLE, která přetrvávala po prolongovaném hojení. Spontánní píštěl byla v místě, kde standardně zavádíme HP. Po zavedení HP do této píštěle došlo ke zmírnění obtíží, pacient přestal aspirovat, zlepšila se mu kvalita života. Pacient absolvoval celkem 4 výměny HP, kdy průměrný interval mezi jednotlivými výměnami byl cca 117 dnů. Po 4. výměně však došlo k rozšíření píštěle a HP výrazně obtékala. Nepomohla již ani aplikace těsnicích kroužků, HP byla tedy odstraněna a pacientovi byla zavedena dočasně NGS. Vzhledem k tomu, že nedošlo ke spontánnímu uzavření píštěle, byla provedena chirurgická revize – parciální resekce cervikální trachey v oblasti tracheostomatu a uzavření píštěle jícnu.
Obdobně jsme museli postupovat i u třetího pacienta, kterému po dvou týdnech od zavedení HP začala protéza výrazně obtékat. Protéza byla vytažena a pacientovi byla dočasně zavedena NGS. Píštěl ani po týdnech neměla tendenci ke zmenšení, proto byl pacient indikován k parciální resekci cervikální trachey v oblasti tracheostomatu a plastice jícnu s uzavřením píštěle jícnu.
Diskuze
Tracheoezofageální řeč byla poprvé popsána v roce 1859 Czermakem a jeho kolegy jako potenciální modalita pro alaryngeální komunikaci [5]. Autor popsal dívku s laryngeální stenózou, která dosáhla hlasu tím, že odklonila proudění vzduchu od tracheostomie k jazyku. Zajímavé je, že tato informace byla uvedena o několik let dříve, než byla provedena první TLE Billrothem v roce 1873. Gussenbauer popsal první případ vytvoření srozumitelné řeči po totální laryngektomii, když vybavil Billrothova prvního pacienta po TLE zařízením namontovaným na tracheostomii – trubici s portem zasahujícím do hltanu [6]. Během následujících 100 let bylo testováno množství různých technik k dosažení řeči řízené plícemi. Jednalo se o protetické laryngeální náhrady, totální laryngektomii s funkčním tracheoezofageálním zkratem a různé neoglotické postupy s tracheofaryngeálním spojením. Všechny tyto pokusy byly v různé míře omezené komplikacemi, jako je aspirace, odmítnutí protéz, rozpad rány nebo uzavření shuntu [7]. Ve snaze překonat tyto problémy Singer a Blom v roce 1980 popsali endoskopickou techniku pro zavedení chlopňové tracheoezofageální protézy, která umožňuje průchod vzduchu z tracheostomie do hltanu, ale zároveň brání vdechnutí potravy a tekutiny [8]. Na jejich principu se implantují HP dodnes. Postupem času i samotné hlasové protézy procházejí vývojem.
K docílení úspěšné tracheoezofageál - ní řeči musí být zavedení HP bezpečně proveditelné, pacient musí být motivován a mít dostatečnou plicní rezervu, protože tracheoezofageální řeč vyžaduje vyšší hnací tlaky vzduchu než standardní laryngeální řeč. Fyzicky by měl pacient být manuálně obratný i vizuálně schopný, aby zvládl uzavřít tracheostomii a péči o protézu, která vyžaduje pravidelné čištění. Při běžných komplikacích, které se často vyskytují, musí být schopen docházet pravidelně na kontroly k výměně protéz.
Implantace HP je většinou proveditelná a jen výjimečně narážíme na relativní kontraindikace, jako je nepříznivá anatomie pacienta, omezující kyfóza nebo tuhé tkáně krku změněné radiační fibrózou. U jedné naší pacientky se hlasovou protézu nepodařilo zavést pro projizvení v oblasti hypofaryngo-ezofageálního přechodu, které neumožňovalo zavést rigidní ezofagoskop dostatečně hluboko k tracheostomii, navíc byl omezen záklon hlavy.
Dalším z důležitých hledisek je velikost tracheostomie, průměr menší než přibližně 1,5 cm může způsobit problémy s čištěním a výměnou protéz [9].
Implantaci provádíme v celkové anestezii. Při prvotní implantaci zavádíme protézu dlouhou 10 mm vzhledem k předpokládanému edému v oblasti píš - těle. Při první výměně zavádíme protézu o délce 8 mm a při dalších výměnách již délku protézy volíme podle šířky stěny píštěle (nejčastěji 6 nebo 8 mm).
Výměny HP se běžně provádí ambulantně bez nutnosti anestezie. V našem souboru 14 z celkem 94 výměn (15 %) bylo provedeno v celkové anestezii. Výměnu za hospitalizace jsme provedli u 28 pacientů (30 %). Zpočátku, přibližně rok a půl od zahájení programu HP, jsme každou výměnu prováděli za hospitalizace z důvodu nedostatku zkušeností. Celkovou anestezii jsme využili často při výskytu granulací kolem protézy, kdy byly v apnoické pauze sneseny granulace elektokauterem a následně provedena výměna HP.
Lewin et al. zjistili medián životnosti HP u 390 pacientů pouze 70 dní [10]. Kress et al., kteří ve své práci srovnávali životnost vícero typů protéz, zjistili průměrnou životnost 108 dnů (medián 74 dnů). U modelu Provox Vega®, který používáme i my, zjistil průměrnou životnost 107 dnů a medián 92 dnů [11]. Mayo-Yáñez et al. uvádějí průměrnou životnost u stejného typu HP 124 dnů [12]. Starší práce od Delsupehe et al. uvádějí průměr kolem 15 týdnů (105 dnů) [13]. V naší studii byl průměrný interval mezi výměnami delší, až 127 dnů, co může být způsobeno menší velikostí našeho souboru.
Netěsnost způsobující protékání je nejčastější indikací k její výměně [8, 14]. V našem souboru byla tato příčina výměny HP u 52 % výměn, což je méně, než uvádí literatura. Lewin at al. ve své práci udávají až 69 %, Mayo-Yáñez et al. 64 % [10, 12]. Menší četnost protékání v naší studii si vysvětlujeme malou skupinou pacientů našeho souboru. U primárních implantací, které v této studii zařazené nejsou, jsme zatím provedli pouze 10 výměn HP, z nich 9 bylo pro protékání a 1 pro obtékání HP. Netěsnost HP vzniká ukládáním mikrobiálního a kvasinkového biofilmu v oblasti chlopně HP, což způsobuje její selhání a následné protékání [15]. Při častém protékání lze použít typ protézy Provox® ActiValve®, která má vnitřní chlopeň z fluoroplastu omezující tvorbu biofilmu. Navíc obsahuje magnety, které zamezují nechtěnému protékání přes chlopeň. Tato protéza není na našem trhu zatím hrazena zdravotní pojišťovnou.
Druhou nejčastější indikací výměny HP v našem souboru bylo obtékání. Na našem pracovišti jsme při zvětšení TeP odstranili dočasně HP a pacientům zavedli NGS. Do TeP jsme vložili Nelatonův katétr o velikosti 8 Charrier a zavedli tracheostomickou kanylu s balónkem. Po pár dnech, kdy došlo k mírnému stažení TeP, jsme opětovně zavedli HP. Tento postup jsme využívali ze začátku, přibližně v prvním roce po zahájení programu implantací HP. Nyní obtékání řešíme spíše aplikací těsnicích kroužků, které jsme dříve neměli k dispozici. Standardně stačí použití jednoho nebo dvou těsnicích kroužků, při nutnosti užití vícero kroužků je lepší spíše změnit velikost HP. Při obtékání lze také využít HP Provox Vega© XtraSeal©, která má navíc na jícnové straně přídatnou těsnicí manžetu bránící obtékání. Tento typ HP jsme zatím na naší klinice nepoužili.
Z dalších možností, kterou lze TeP zmenšit, je sutura nebo injekční augmentace resorbovatelným nebo neresorbovatelným materiálem do okolí píštěle [4, 9]. S danými postupy nemáme na našem pracovišti zkušenosti.
Ve dvou případech, kdy píštěl neměla tendenci se zatahovat ani po aplikaci těsnicích kroužků, ani po dočasném vytažení HP, pacienti absolvovali parciální resekce cervikální trachey v oblasti tracheostomatu a uzavření píštěle jícnu suturou. Podle dostupné literatury lze po chirurgickém uzavření TeP provést další tracheoezofageální punkci s vložením nové HP po 3–4 měsících [4]. Oba naši pacienti ale odmítli další znovu - zavedení HP.
Třetí nejčastější indikací k výměně HP byly granulace kolem HP, a to u 12 případů. Pacienty s recidivujícími granulacemi kolem TeP s potřebou časté výměny protézy a s neuspokojivými vokálními výsledky sledovali ve své práci Cocuzza et al. U 49 % sledovaných pacientů byl prokázán gastroezofageální reflux. Po zaléčení terapeutickou dávkou inhibitorů protonové pumpy došlo u 38 % pacientů k vymizení nebo zmenšení objemu granulací, v 60 % došlo k zlepšení hlasu a ve 40 % došlo k prodloužení životnosti HP [16].
Účinky RT na TeP jsou podle údajů uvedených v literatuře sporné. Radioterapie pravděpodobně zvyšuje riziko komplikací v oblasti TeP, zejména zvětšení píštěle a vznik obtékání kolem HP. Za základní patofyziologický mechanizmus je považována tkáňová fibróza neofaryngu vyvolaná zářením s následným vznikem atrofie stěny průdušnice [14, 17–20]. Elving et al. zkoumali 101 pacientů po TLE a zjistili, že aplikace radiačních dávek 60 a více Gy na oblast primárního nádoru byla spojena se zkrácením životnosti protéz [17]. V práci Boscolo-Rizzo et al. byla životnost HP u pacientů po RT o 40 dnů kratší [18]. Existuje však také řada mezinárodních studií, které nenalezly souvislost mezi radioterapií a vznikem netěsností kolem protézy [14, 19, 20].
V našem souboru 12 pacientů absolvovalo RT nebo ChRT před sekundární implantací HP. Deset z nich absolvovalo adjuvantní RT po TLE. Dva pacienti podstoupili TLE jako salvage surgery. Neprokázali jsme u nich kratší životnost protéz ani vliv na rozvoj komplikací.
Setkali jsme se se závažnou komplikací, kdy HP vycestovala prevertebrálně s následným rozvojem abscesové dutiny [21]. Ze zpětného pohledu je ke zvážení, zda pacient byl správně indikován k zavedení HP. V terénu stenózy jícnu zřejmě nebyl normotonus v oblasti neofaryngu a horního jícnu, což je jeden z nejdůležitějších předpokladů k úspěšné implantaci HP. Naštěstí po provedení incize zadní stěny jícnu, evakuaci tvořícího se abscesu a vytažení HP se pacient zhojil bez komplikací. Horší výsledek popisují Oztruk et al. ve své kazuistice, kdy u pacienta došlo po výměně HP ke vzniku abscesové dutiny v oblasti krční páteře, která způsobila kvadruplegii [22].
Text práce je zaměřen pouze na pacienty se sekundárně implantovanými HP, kteří mají na našem pracovišti delší dobu sledování. Aktuálně je nabízena možnost primární implantace HP každému pacientovi, který podstupuje TLE. Vzhledem ke krátké době sledování a pouze minimu výměn HP nebyla tato skupina pacientů zařazena do studie.
Metaanalýza z roku 2017, srovnávající primární a sekundární zavedení HP, neprokázala statisticky významné rozdíly v celkové míře komplikací nebo hlasových výstupech, i když naznačovala vyšší riziko hypofaryngokutánní píštěle po primárním zavedení HP [23].
Barauna Neto et al. v přehledu literatury udávají, že u pacientů po sekundární implantaci je riziko obtékání kolem protézy nižší než po primárním zavedení HP [24]. Luu et al. ve své systematické přehledové práci rozdíl v komplikacích mezi primárními a sekundárními implantacemi nenašli [25].
Z uvedených studií vyplývá, že stran komplikací je o něco málo bezpečnější sekundární zavedení. Je však nutno připomenout, že po primárním zavedení je zkráceno období, kdy pacient není schopen komunikace. Již po 10 dnech od zavedení může pacient zahájit hlasovou rehabilitaci [3, 9]. V našem souboru měli pacienti implantovanou HP průměrně 523 dnů od provedení TLE, což je významně delší zásah do kvality života než u pacientů po primárním zavedení. Relativně dlouhá doba od operace po implantaci je na našem pracovišti dána tím, že se sekundární implantací čekáme na dokončení onkologické terapie a vyloučení časné recidivy.
Závěr
Implantace hlasové protézy je moderní způsob rehabilitace hlasu po TLE, umožňující aktivní život bez sociální izolace. Životnost v našem souboru sekundárně implantovaných pacientů byla průměrně 127 dnů. Nejčastější indikací k výměně HP je její netěsnost, tedy protékání. S implantací HP plánujeme dále pokračovat.
Prohlášení o střetu zájmů
Prohlašuji, že v souvislosti s tématem, vznikem a publikací tohoto článku nejsem ve střetu zájmů a vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou firmou. Toto prohlášení se týká i všech spoluautorů.
Grantová podpora
Podpořeno MZ ČR – RVO (FNOL, 00098892) a interním grantem Univerzity Palackého v Olomouci IGA LF 2021-21.
ORCID autorů
P. Beláková ORCID 0000-0001-8417-8970,
M. Brož ORCID 0000-0003-1378-1478.
R. Salzman ORCID 0000-0001-5705-5510.
Přijato k recenzi: 30. 11. 2021
Přijato k publikaci: 13. 6. 2022
MUDr. Petra Beláková
Klinika otorinolaryngologie a chirurgie hlavy a krku, LF UP a FN Olomouc
Zdravotníků 248/7 779 00 Olomouc
Sources
1. Galli A, Giordano L, Biafora M et al. Voice prosthesis rehabilitation after total laryngectomy: Are satisfaction and quality of life maintained over time? Acta Otorhinolaryngol Ital 2019; 39 (3): 162–168. Doi: 10.14639/0392-100X - 2227.
2. Kaye R, Tang CG, Sinclair CF. The electrolarynx: Voice restoration after total laryngectomy. Med Devices Evid Res 2017; 10 : 133–140. Doi: 10.2147/MDER.S133225.
3. Dršata J a kol. Foniatrie – hlas. 1. vyd. Havlíčkův Brod: Tobiáš 2011.
4. Lorenz KJ. The development and treatment of periprosthetic leakage after prosthetic voice restoration: a literature review and personal experience. Part II: conservative and surgical management. Eur Arch Otorhinolaryngol 2015; 272 (3): 661–672. Doi: 10.1007/s00405-014-33 93-8.
5. Czermak J. Uber die sprache bei luftdichter Verschliessung des Kehlkopfes. Sitzungsbericbte der Akademie der Wissenschaften in Wien Mathematischnaturwissenschaftliche Klasse 1858; 35 (2): 65–72.
6. Gussenbauer C. Ueber die erste durch Th. Billroth am Menschen ausgeführte Kehlkopf-Exstirpation und die Anwendung eines künstlichen Kehlkopfes. Arch Klin Chir Berlin 1874; 17 : 343–356.
7. Bien S, Rinaldo A, Silver CE et al. History of voice rehabilitation following laryngectomy. Laryngoscope 2008; 118 (3): 453––458. Doi: 10.1097/MLG.0b013e31815db 4a2.
7. Singer MI, Blom ED. An endoscopic technique for restoration of voice after laryngectomy. Ann Otol 1980; 89 : 529–553. Doi: 10.1177/000 348948008900608.
9. Zenga J, Goldsmith T, Bunting G et al. State of the art: Rehabilitation of speech and swallowing after total laryngectomy. Oral Oncol 2018; 86 : 38–47 Doi: 10.1016/j.oraloncology.2018.08. 023.
10. Lewin JS, Baumgart LM, Barrow MP et al. Device Life of the Tracheoesophageal Voice Prosthesis Revisited. JAMA Otolaryngol Head Neck Surg 2017; 143 (1): 65–71. Doi: 10.1001/ jamaoto.2016.2771.
11. Kress P, Schäfer P, Schwerdtfeger FP et al. Are modern voice prostheses better? A lifetime comparison of 749 voice prostheses. Eur Arch Otorhinolaryngol 2014; 271 (1): 133–140. Doi: 10.1007/s00405-013-2611-0.
12. Mayo-Yáñez M, Cabo-Varela I, Dovalo-Carballo L et al. Provox 2 (®) and Provox Vega (®) device life-time: a case-crossover study with multivariate analysis of possible influential factors and duration. Eur Arch Otorhinolaryngol 2018; 275 (7): 1827–1830. Doi: 10.1007/s00 405-018-5008-2.
13. Delsupehe K, Zink I, Lejaegere M et al. Prospective randomized comparative study of tracheoesophageal voice prosthesis: Blom-Singer versus Provox. Laryngoscope 1998; 108 (10): 1561–1565. Doi: 10.1097/00005537-1998100 00-00026.
14. LaBruna A, Huo J, Klatsky I et al. Tracheoesophageal puncture in irradiated patients. Ann Otol Rhinol Laryngol 1995; 104 (4): 279–281. Doi: 10.1177/000348949510400404.
15. Buijssen KJ, van der Laan BF, van der Mei HC et al. Composition and architecture of biofilms on used voice prostheses. Head Neck 2012; 34 (6): 863–871. Doi: 10.1002/hed.21 833.
16. Cocuzza S, Bonfiglio M, Chiaramonte R et al. Gastroesophageal reflux disease and postlaryngectomy tracheoesophageal fistula. Eur Arch Otorhinolaryngol 2012; 269 (5): 1483–1488. Doi: 10.1007/s00405-012-1938-2.
17. Elving GJ, van Weissenbruch R, Busscher HJ et al. The influence of radiotherapy on the lifetime of silicone rubber voice prostheses in laryngectomized patients. Laryngoscope 2002; 112 (9): 1680–1683. Doi: 10.1097/000 05537-200209000-00028.
18. Boscolo-Rizzo P, Marchiori C, Gava A et al. The impact of radiotherapy and GERD on in situ lifetime of indwelling voice prostheses. Eur Arch Otorhinolaryngol 2008; 265 (7): 791–796. Doi: 10.1007/s00405-007-0536-1.
19. Op de Coul BM, Hilgers FJ, Balm AJ et al. A decade of postlaryngectomy vocal rehabilitation in 318 patients: a single Institution‘s experience with consistent application of provox indwelling voice prostheses. Arch Otolaryngol Head Neck Surg 2000; 126 (11): 1320–1328. Doi: 10.1001/archotol.126.11. 1320.
20. Trudeau M, Schuller D, Hall D. The effects of radiation on tracheoesophageal puncture. A retrospective study. Arch Otolaryngol Head Neck Surg 1989; 115 (9): 1116–1117. Doi: 10.1001/archotol.1989.01860330106 028.
21. Korpová A, Brož M, Salzman R. Dislokace hlasové protézky do prevertebrálního prostoru – vzácná komplikace. Otorinolaryngol Foniatr 2020; 69 (1): 35–39.
22. Ozturk K, Erdur O, Kibar E. Permanent quadriplegia following replacement of voice prosthesis. J Craniofac Surg 2016; 27 (8): 741–743. Doi: 10.1097/SCS.0000000000003083.
23. Chakravarty PD, McMurran, AEL, Banigo A et al. Primary versus secondary tracheoesophageal puncture: Systematic review and meta-analysis. J Laryngol Otol 2018; 132 (1): 14–21. Doi: 10.1017/S0022215117002390.
24. Barauna Neto JC, Dedivitis RA, Aires FT et al. Comparison between Primary and Secondary Tracheoesophageal Puncture Prosthesis: A Systematic Review. ORL J Otorhinolaryngol Relat Spec 2017; 79 (4): 222–229. Doi: 10.1159/000477970.
25. Luu K, Chang BA, Valenzuela D et al. Primary versus secondary tracheoesophageal puncture for voice rehabilitation in laryngectomy patients: A systematic review. Clin Otolaryngol 2018; 43 (5): 1250–1259. Doi: 10.1111/coa.13 138.
Labels
Audiology Paediatric ENT ENT (Otorhinolaryngology)
Article was published inOtorhinolaryngology and Phoniatrics
2023 Issue 1-
All articles in this issue
- Editorial
- An accuracy of whisper hearing test together with screening otoacoustic emissions in the detection of hearing loss
- Experience with secondary voice prostheses implantations at the Department of Otorhinolaryngology and Head and Neck Surgery at the Olomouc University Hospital in 2016–2021
- Functional evaluation of laryngoscopic examination and its relation to voice quality and voice range profile parameters
- Heerfordt’s syndrom – a rare manifestation of sarcoidosis from an ENT perspective
- Schwannoma of the mastoid part of the facial nerve
- Myiasis of the ear as a rare cause of otorrhea
- Sedmdesátiny doc. MUDr. Jana Vokurky, CSc.
- Kurz „Chirurgie kůže hlavy a krku pro pokročilé“
- Multidisciplinárny Workshop Dysfágia
- XIX. česko-slovenský kongres mladých otorinolaryngológov
- Otorhinolaryngology and Phoniatrics
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Experience with secondary voice prostheses implantations at the Department of Otorhinolaryngology and Head and Neck Surgery at the Olomouc University Hospital in 2016–2021
- An accuracy of whisper hearing test together with screening otoacoustic emissions in the detection of hearing loss
- Functional evaluation of laryngoscopic examination and its relation to voice quality and voice range profile parameters
- Heerfordt’s syndrom – a rare manifestation of sarcoidosis from an ENT perspective
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

