-
Medical journals
- Career
Erdheimova-Chesterova choroba – kazuistika
Authors: Pilarčíková K. 1; Sláviková K. 2; Plank L. 3; Puchertová M. 4; Babinec M. 1; Barta T. 1; M. Profant 1
Authors‘ workplace: Klinika ORL, chirurgie hlavy a krku LF UK a UN Bratislava 1; Rádiológia s. r. o., Bratislava 2; Ústav patologickej anatómie, JLF UK v Martine 3; Ústav patologickej anatómie, LF SZU, Bratislava 4
Published in: Otorinolaryngol Foniatr, 70, 2021, No. 3, pp. 177-180.
Category: Case Reports
doi: https://doi.org/10.48095/ccorl2021177Overview
Erdheimova-Chesterova choroba (ECD) patrí medzi malígne polyostotické sklerotické formy non-Langerhansovej histiocytózy. Pri abnormálnej proliferácii patologických histiocytov „penovitých buniek“ napadnuté štruktúry hypertrofujú, zvyšujú svoju denzitu, objavuje sa jazvenie. Choroba postihuje najmä diafýzy a metafýzy dlhých kostí dolných končatín s typickým prejavom bolesti. Podľa WHO je choroba klasifikovaná ako histiocytózna neoplázia. Referujeme o 74-ročnej pacientke s expanzívnym ložiskom v oblasti horného klivu a sfenoidálnej kosti vpravo. Histologické vyšetrenie potvrdilo túto zriedkavú chorobu, ktorou trpí asi len 600 pacientov na svete.
Klíčová slova:
Erdheim-Chester – penovité histiocyty – skleróza – fibróza
Úvod
Keď sa na našom pracovisku objavil histologický výsledok excízie z oblasti rinobázy s podozrením na Erdheimovu-Chesterovu chorobu, ostali sme všetci prekvapení, nikdy sme o takej diagnóze nepočuli. Myslíme si, že o tejto zriedkavej diagnóze je vhodné informovať našu odbornú verejnosť spracovaním kazuistiky pacientky.
Erdheimova-Chesterova choroba (ECD) je veľmi zriedkavá, v literatúre opísaná asi u 600 ľudí na svete. Patrí medzi malígne polyostotické sklerotické formy non-Langerhansovej histiocytózy. Prvý prípad zaznamenal americký patológ William Chester v roku 1930 vo Viedni, počas návštevy svojho rakúskeho kolegu Jakoba Erdheima [1].
Vyskytuje sa prevažne u 40–70-ročných mužov. Je charakterizovaná abnormálnou proliferáciou patologických histiocytov „penovitých buniek“, produkujúcich prozápalové cytokíny v rôznych orgánoch. Následkom nekontrolovateľného zápalového procesu napadnuté štruktúry hypertrofujú, zvyšujú svoju denzitu, objavuje sa jazvenie. Postihuje najmä diafýzy a metafýzy dlhých kostí dolných končatín s typickým prejavom bolesti (členky, kolená). Až 50 % tvoria extraskeletálne prejavy: dyspnoe a zlyhávanie pľúc (interlobulárna a pleurálna fibróza), polyúria, polydipsia a hypopitiutarizmus (fibróza hypofýzy), zlyhávanie obličiek (fibróza perinefritického tuku „hairy kidney“), ataxia a závraty (fibróza cerebela), exoftalmus, xantómy, retroperitoneálna fibróza, aortálna fibróza („coat aorta“). Prítomné môžu byť aj B symptómy typické pre hematologické ochorenia, a to subfebrílie, nočné potenie, úbytok hmotnosti, patologická únava [2–5].
Image 1. A, B – nahromadenie histiocytov s objemnou penistou cytoplazmou (označené šípkou, farbenie hematoxylín-eozín, zväčšenie 100x, 400x), C, D – imunohistochemický dôkaz CD68 v histiocytoch (zväčšenie 100x, 400x).
Fig. 1. A, B – accumulation of histiocytes with voluminous penile cytoplasm (marked by arrow, hematoxylin-eosin staining, magnification 100x, 400x), C, D – immunohistochemical evidence of CD68 in histiocytes (magnification 100x, 400x).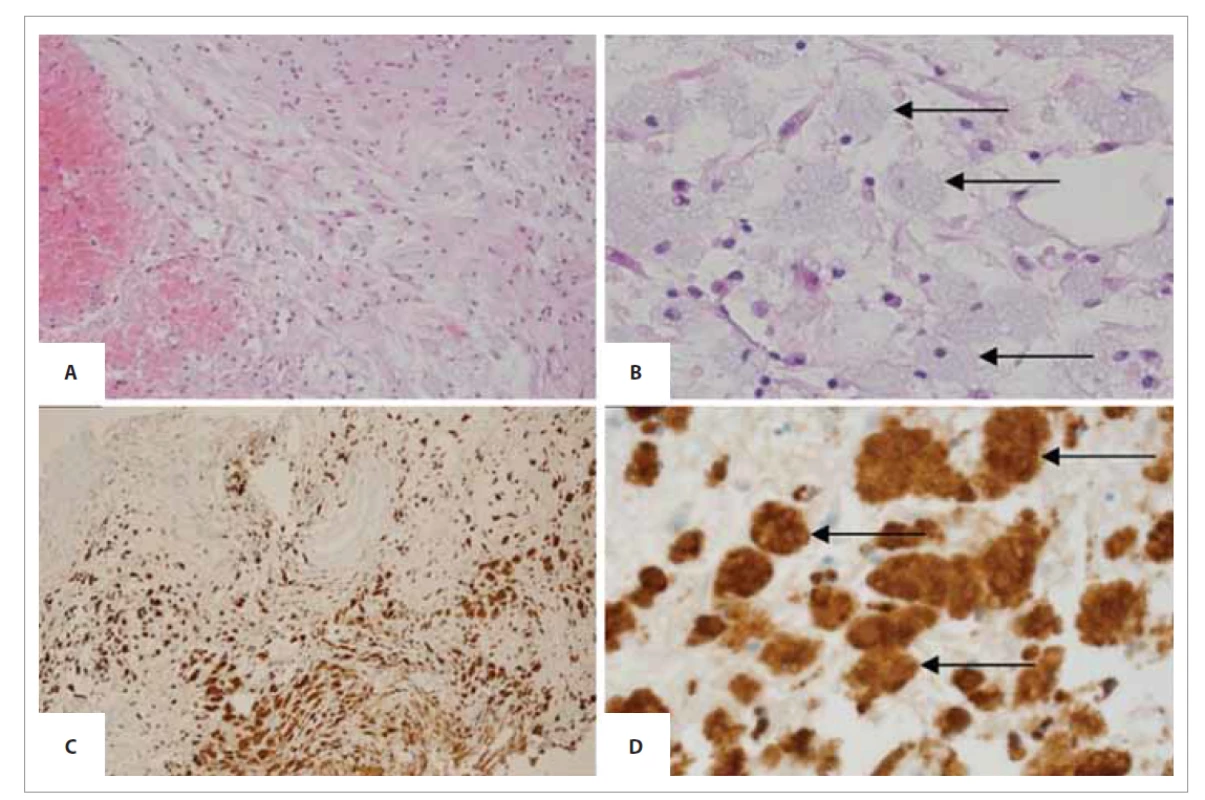
Kazuistika
V januári 2020 bola odoslaná na naše pracovisko 74-ročná pacientka, sledovaná od roku 2015 neurológmi pre expanzívne ložisko v oblasti klivu a sfenoidálnej kosti vpravo verifikované na CT obraze (obr. 2). Pacientka mávala nešpecifické závratové stavy, bez cefaley, ataxie či inej neurologickej a vegetatívnej symptomatológie. Lekári pripisovali problémy nálezu nekompenzovanej arteriálnej hypertenzie a arytmie.
Image 2. Expanzia v oblasti horného klivu dorzálne a inferiórne od klinovej dutiny vpravo.
Fig. 2. Expansion in the area of the upper clavicle dorsally and inferiorly from the wedge cavity to the right.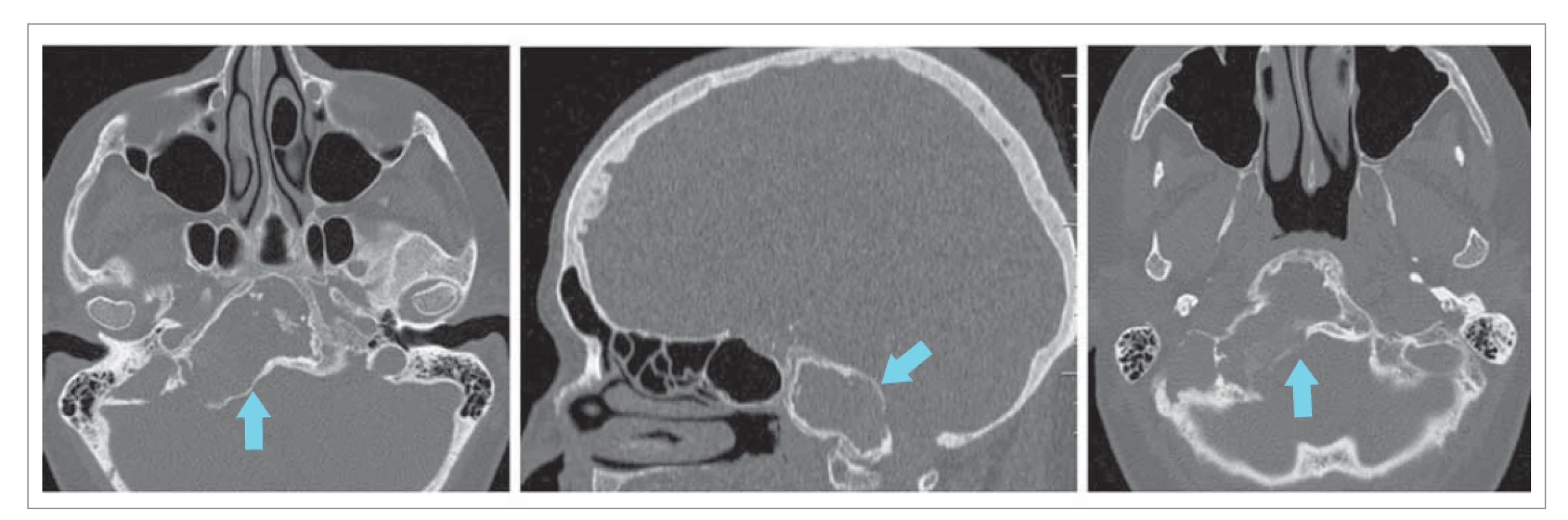
V roku 2019 prekonala závratový stav so synkopou. Neurológ indikoval MR mozgu, ktoré zobrazilo progresiu daného patologického nálezu oproti CT vyšetreniu z roku 2015 asi o 20 % (obr. 3). V diferenciálnej diagnóze sa uvažovalo o chondromyxoide, chondróme, prípadne menej pravdepodobnom chondrosarkóme.
Image 3. Expanzia v oblasti horného klivu, zvýšený signál v T2, izointenzívny signál v T1 zvyšuje intenzitu signálu v T1 s kontrastom.
Fig. 3. Expansion in the upper cliff region, increased signal in T2, isointensive signal in T1 increases the signal intensity in T1 with contrast.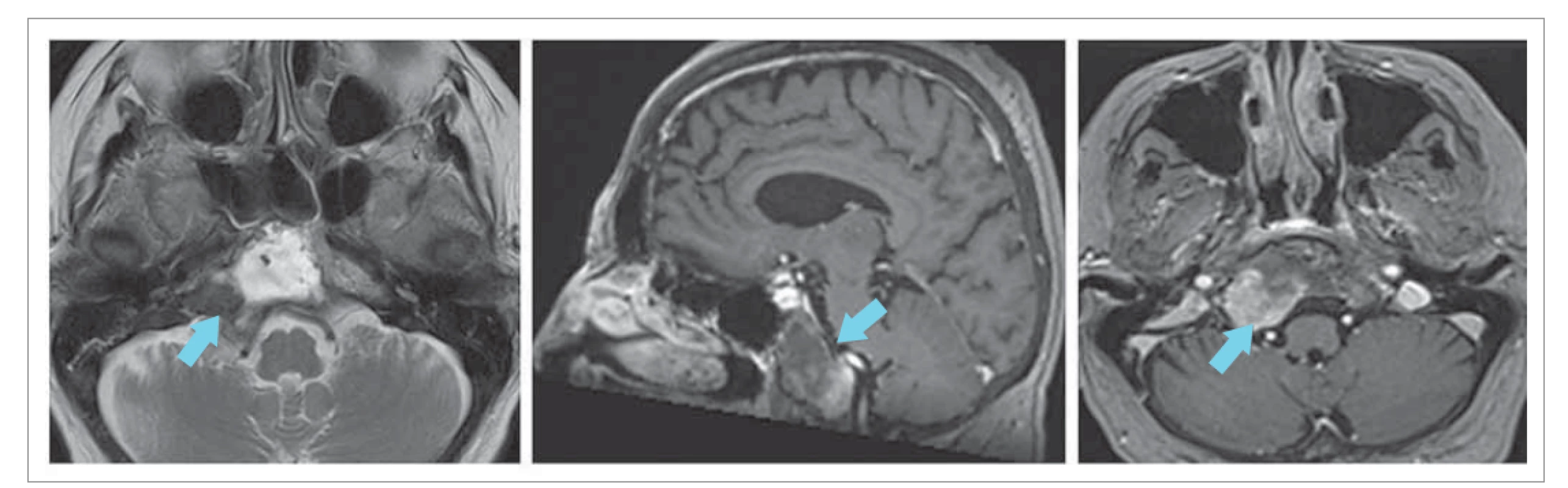
Neurochirurg následne odporučil histologizáciu procesu rinobázy transnazálnou excíziou z daného útvaru. Vo februári 2020 sme transfenoidálne odobrali časť útvaru na histologické vyšetrenie. Histologický nález vylúčil chondróm, chondromyxoid či chondrosarkóm a patológ uvažoval o diagnóze Erdheimova-Chesterova choroba (ECD). Pre limitovaný objem materiálu a nejednoznačné závery sa rozhodlo o rebiopsii, ktorú sme urobili v auguste 2020. Vzhľadom na zriedkavé skúsenosti s ECD bol materiál konzultovaný viacerými patológmi. Histologický nález sa posudzoval multidisciplinárne v korelácii s klinickými príznakmi a laboratórnymi vyšetreniami. Koncom augusta 2020 v definitívnom histologickom závere sa patológ priklonil k záveru, že sa jedná o ECD.
Následné PET-CT nezobrazilo iné ložiská ECD. U pacientky bola indikovaná cielená radiačná liečba na ECD ložisko v oblasti klivu a sfenoidálnej kosti vpravo 8 frakcií rádioterapie po 2,5 Gy v najvyššej zvládnuteľnej dávke, vzhľadom na komorbidity pacientky (podobný protokol ako pri paragangliómoch). Chemoterapia sa nepodala. Pacientka bola v dobrom klinickom stave prepustená domov. Pri nestabilnom krvnom tlaku a arytmii o pár dní zakrvácala do mozočka vľavo s následnou hospitalizáciou na neurologickom oddelení. Pri prijatí bol opísaný nystagmus II. stupňa, ataxia doprava a dorzálne, vomitus, schvátenosť, imobilita. Po dvoch týždňoch sa stav pacientky zlepšil a bola prepustená v stabilizovanom stave už len s miernou ataxiou, mobilná, bez paretických prejavov. Pre ECD je pacientka naďalej v starostlivosti onkológov a neurológov.
Diskusia
Podľa dostupnej literatúry príčina ECH nie je doposiaľ známa. Podľa WHO je choroba klasifikovaná od roku 2016 ako histiocytózna neoplázia a u viac ako 50 % pacientov sa zistila mutácia génu BRAF V600E [3, 4, 6].
Stanovenie diagnózy vyžaduje multidisciplinárny prístup. Posudzujú sa rádiologické, laboratórne, histologické a imunohistochemické (IHC) kritériá. HRCT hrudníka, dutiny brušnej, malej panvy zachytí fibrózu orgánov, osteosklerotické ložiská kostí. Laboratórne sa zistia zvýšené zápalové parametre (CRP, leukocyty, trombocyty, fibrinogén) [4, 7]. V histologickom obraze sú početné penovité histiocyty s okolitou fibrózou, obrovské viacjadrové bunky tuotonoidného typu. Tieto elementy podľa IHC preparátu vykazujú výraznú expresiu CD68+, ale S100, CD1a sú negatívne. Birbekove granuly (typické pre Langerhansové histiocytózy) nie sú prítomné [8]. Histologický obraz ukazuje obr. 1. Je zjavné, že bremeno diagnózy spočíva v správnom vyhodnotení histologického nálezu.
V diferenciálnej diagnóze treba uvažovať o Rosai-Dorfmanovej chorobe (sinusová histiocytóza s masívnou lymfonodopatiou) a o iných histiocytózach [9, 10].
Vzhľadom k výnimočnému výskytu tejto choroby v ORL praxi, nie je terapeutický postup štandardizovaný. Chirurgická resekcia ložiska, za účelom zmenšenia objemu, sa využíva pri závažných resekabilných orbitálnych a intrakraniálnych ložiskách. Okrem chirurgickej resekcii tumoru je možná liečba vysokými dávkami kortikosteroidov, interferónom-alfa, cyklosporínom, anakinrou (imunosupresívum, blokátor receptoru pre interleukín 1), kladribinom (cytostatikum, fagocytuje monocyty), vemurafenibom (inhibítor BRAF V600E), vysokými dávkami chemoterapie [4, 7, 11, 12]. Rádioterapia vo vyšších dávkach približne 20 Gy sa využíva väčšinou pri izolovaných intrakraniálnych a orbitálnych ložiskách ECD, ale dosiahnutie dlhodobej stabilizácie je zriedkavé [13, 14].
Prognóza je variabilná, závisí od rozsahu a distribúcie patologických zmien [7]. Francúzska štúdia z roku 2011 pri liečbe ECD interferónom-alfa uvádza 5-ročné prežívanie u 68 % pacientov z 53 liečených pacientov [15]. Odkedy sa pacienti združujú v ECD Global Aliance and ECD Referral Care Center sa vedomosti o chorobe rozširujú, štúdie a klinické prípady sú dostupnejšie [7].
Záver
Izolované patologické procesy v oblasti rinobázy, sfenoidálnej dutiny, klivu, tureckého sedla nie sú výnimočné. Pri nejasnej diagnóze z klinického nálezu a obrazovej dokumentácie otorinolaryngológ a neurochirurg obvykle žiadajú histologizáciu transnazálnym prístupom. V diferenciálnej diagnóze treba myslieť aj na možnosť Erdheimovej-Chesterovej choroby, ktorá sa diagnostikovala u našej pacientky.
Prehlásenie o strete záujmov
Prehlasujem, že v súvislosti s témou, vznikom a publikáciou tohto článku nie som v strete záujmov a vznik ani publikácia článku nebola podporená žiadnou farmaceutickou firmou. Toto prehlásenie sa týka aj všetkých spoluautorov.
ORCID autora
M. Profant ORCID 0000-0002-3986-6376.
Prijaté k recenzii: 30. 11. 2020
Prijaté k tlači: 4. 1. 2021
prof. MUDr. Milan Profant, CSc.
Klinika ORL, chirurgie hlavy a krku
LF UK a UN Bratislava
Antolská 11
851 07 Bratislava
Sources
1. Estrada-Veras JI, O‘Brien KJ, Boyd LC et al. The clinical spectrum of Erdheim-Chester disease: an observational cohort study. Blood Adv 2017; 1 (6): 357–366. Doi: 10.1182/blood advances.2016001784.
2. Ozkaya N, Rosenblum MK, Durham BH et al. The histopathology of Erdheim-Chester disease: a comprehensive review of a molecularly characterized cohort. Mod Pathol 2018; 31 (4): 581–597. Doi: 10.1038/modpathol.2017. 160.
3. Munoz J, Janku F, Cohen PR et al. Erdheim-Chester disease: characteristics and management. Mayo Clin Proc 2014;.89 (7): 985–996. Doi: 10.1016/j.mayocp.2014.01.023.
4. Adam Z, Petrášová H, Řehák Z et al. Hodnocení pětileté léčby Erdheimovy-Chesterovy nemoci anakinrou – kazuistika a přehled literatury. Vnitř Lék 2016; 62 (10): 820–832.
5. Sedrak P, Ketonen L, Hou P et al. Erdheim-Chester disease of the central nervous system: new manifestations of a rare disease. AJNR Am J Neuroradiol 2011; 32 (11): 2126–2131. Doi: 10.3174/ajnr.A2707.
6. Haroche J, Charlotte F, Arnaud L et al. High prevalence of BRAF V600E mutations in Erdheim-Chester disease but not in other non-Langerhans cell histiocytoses. Blood 2012; 120 (13): 2700–2703. Doi: 10.1182/blood - 2012-05-430140.
7. Diamond EL, Dagna L, Hyman DM et al. Consensus guidelines for the diagnosis and clinical management of Erdheim-Chester disease. Blood 2014; 124 (4): 483–492. Doi: 10.1182/blood-2014-03-561381.
8. Adam Z, Krejčí M, Vorlíček J et al. Přehled maligních hematologických nemocí, 2. dopln. a zcela přeprac. vyd. Praha: Grada 2008.
9. Becker MR, Gaiser T, Middel P et al. Clinicopathologic challenge. Destombes-Rosai-Dorfman disease (DRDD) (sinushistiocytosis with massive lymphadenopathy). Int J Dermatol 2008; 47 (2): 125–127. Doi: 10.1111/j.1365 - 4632.2008.03376.x.
10. Razanamahery J, Diamond EL, Cohen-Aubart F et al. Erdheim-Chester disease with concomitant Rosai-Dorfman like lesions: a distinct entity mainly driven by MAP2K1. Haematologica 2020; 105 (1): e5–e8. Doi: 10.3324/haematol.2019.216937.
11. Adam Z, Řehák Z, Koukalová R et al. PET-CT dokumentovaná kompletní 4letá remise Erdheimovy-Chesterovy nemoci po léčbě kladribinem. Vnitř Lék 2014; 60 (5–6): 499–511.
12. Alfieri A, Gazzeri R, Galarza M et al. Surgical treatment of intracranial Erdheim-Chester disease. J Clin Neurosci 2010; 17 (12): 1489–1492. Doi: 10.1016/j.jocn.2010.03.062.
13. Mascalchi M, Nencini P, Nistri M et al. Failure of radiation therapy for brain involvement in Erdheim-Chester disease. J Neurooncol 2002; 59 (2): 169–172. Doi: 10.1023/a: 1019649201324.
14. Miller RC, Villa S, Kamer S et al. Palliative treatment of Erdheim-Chester disease with radiotherapy: a Rare Cancer Network study. Radiother Oncol 2006; 80 (3): 323–326. Doi: 10.1016/j.radonc.2006.07.034.
15. Arnaud L, Hervier B, Neel A et al. CNS involvement and treatment with interferon-alpha are independent prognostic factors in Erdheim-Chester disease: a multicenter survival analysis of 53 patients. Blood 2011; 117 (10): 2778–2782. Doi: 10.1182/blood-2010-06-294108.
Labels
Audiology Paediatric ENT ENT (Otorhinolaryngology)
Article was published inOtorhinolaryngology and Phoniatrics

2021 Issue 3-
All articles in this issue
- Odborný časopis Otorinolaryngologie a foniatrie slaví 70 let
- Akutní závrať v pohotovostní službě ORL lékaře
- Hodnocení řeči u pacientů po kochleární implantaci – Motol Speech Scale
- Vrozené vývojové vady vnitřního ucha
- Gastrický choristom hypofaryngu u novorozence
- Erdheimova-Chesterova choroba – kazuistika
- Sklerotizace krčních cyst alkoholem pod ultrasonografickou kontrolou jako alternativa operačního řešení
- Komentář ke článku „Hodnocení řeči u pacientů po kochleární implantaci – Motol Speech Scale“
- Odpověď autorů na komentář ke článku „Hodnocení řeči u pacientů po kochleární implantaci – Motol Speech Scale“
- Odešel prim. MUDr. Jiří Sušický
- Vzpomínka na MUDr. Luďka Šefce
- Vzpomínka na doc. MUDr. Miloslava Hroboně, CSc.
- Problematika roztroušené sklerózy v otoneurologické ambulanci, mezioborová spolupráce otoneurologa a neurologa
- Otorhinolaryngology and Phoniatrics
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Vrozené vývojové vady vnitřního ucha
- Akutní závrať v pohotovostní službě ORL lékaře
- Sklerotizace krčních cyst alkoholem pod ultrasonografickou kontrolou jako alternativa operačního řešení
- Hodnocení řeči u pacientů po kochleární implantaci – Motol Speech Scale
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

