-
Medical journals
- Career
Diagnostika a další péče o pacienty s tyreoidálními uzly: doporučení American Thyroid Association 2015 modifikované pro podmínky České republiky
Authors: Jan Jiskra
Authors‘ workplace: 3. interní klinika – klinika endokrinologie a metabolismu 1. LF UK a VFN v Praze
Published in: Čas. Lék. čes. 2017; 156: 241-251
Category: Review Article
Overview
Tyreoidální uzly jsou časté. Naprostá většina z nich jsou uzly benigní bez hormonální nadprodukce. Základním vyšetřením u tyreoidálních uzlů je vyloučení tyreoidální dysfunkce a ultrazvuk ke správnému posouzení, které uzly mají být vyšetřeny aspirační biopsií tenkou jehlou (FNAB) s následnou cytologií. V indikaci k FNAB se zvažují zejména velikost uzlu, vzhled uzlu při vyšetření ultrazvukem a klinické rizikové faktory. Z důvodu lepší standardizace dalšího postupu a zlepšení péče o pacienty s minimalizací nežádoucích důsledků z podhodnocení (přehlédnutá malignita) i nadhodnocení (zbytečné operace) by měl být výsledek FNAB kategorizován podle rizika malignity. Jako nejvhodnější se k tomuto účelu jeví tzv. klasifikace Bethesda, ačkoliv ani ona, zejména z důvodu problematické kategorie III, není optimální.
Klíčová slova:
tyreoidální uzel, karcinom štítné žlázy, ultrazvuk, aspirační biopsie tenkou jehlou, klasifikace BethesdaÚvod
Prevalence tyreoidálních uzlů je vysoká (až 76 % u běžné neselektované populace) a s nárůstem počtu prováděných zobrazovacích metod v oblasti krku stále stoupá. Většinou tedy jde o náhodné nálezy – incidentalomy. Zhoubných nádorů je mezi náhodně diagnostikovanými uzly maximálně 5–10 %. Kromě toho se ukazuje, že papilární karcinom (u nás nejčastější, představuje 80–90 % všech zhoubných nádorů štítné žlázy) náhodně diagnostikovaný jako mikrotumor (< 1 cm) bez známek extratyreoidální invaze má u většiny pacientů (> 90 %) dokonce i bez léčby velmi dobrou prognózu, danou jeho indolentním chováním.
Růst tumoru je zejména u starších osob ve většině případů pomalý a tumor progreduje do klinicky manifestního stadia jen u malého podílu pacientů. Proto je všeobecný trend ke konzervativnějšímu a méně invazivnímu postupu, což se týká jak terapie, tak diagnostiky. Klíčovým nástrojem schopným určit, které uzly vyžadují aspirační biopsii tenkou jehlou (FNAB) s následnou cytologií (FNAC) a které uzly stačí sledovat, je ultrazvuk (UZ).
Na druhou stranu je třeba mít na paměti, že malé procento (< 5 %) papilárních mikrokarcinomů má od počátku agresivní chování s extratyreoidální invazí a často i vzdálenými metastázami. Naštěstí se ale jedná o vzácné případy. Odlišit agresivní varianty od indolentních forem v počáteční fázi (ještě před extratyreoidální invazí) zobrazovací metody neumějí. Přínosem může být molekulárně genetické vyšetření na základě FNAB, kde především mutace BRAF je negativním prognostickým markerem u papilárního karcinomu štítné žlázy (PTC). U každého pacienta s tyreoidálním uzlem/uzly se má zhodnotit anamnéza a symptomy (klinické rizikové faktory), provést palpační vyšetření krku včetně vyšetření lymfatických uzlin a má být proveden specializovaný UZ štítné žlázy a krku a TSH v séru.
Table 1. Kategorizace tyreoidálního uzlu na ultrazvuku podle ATA 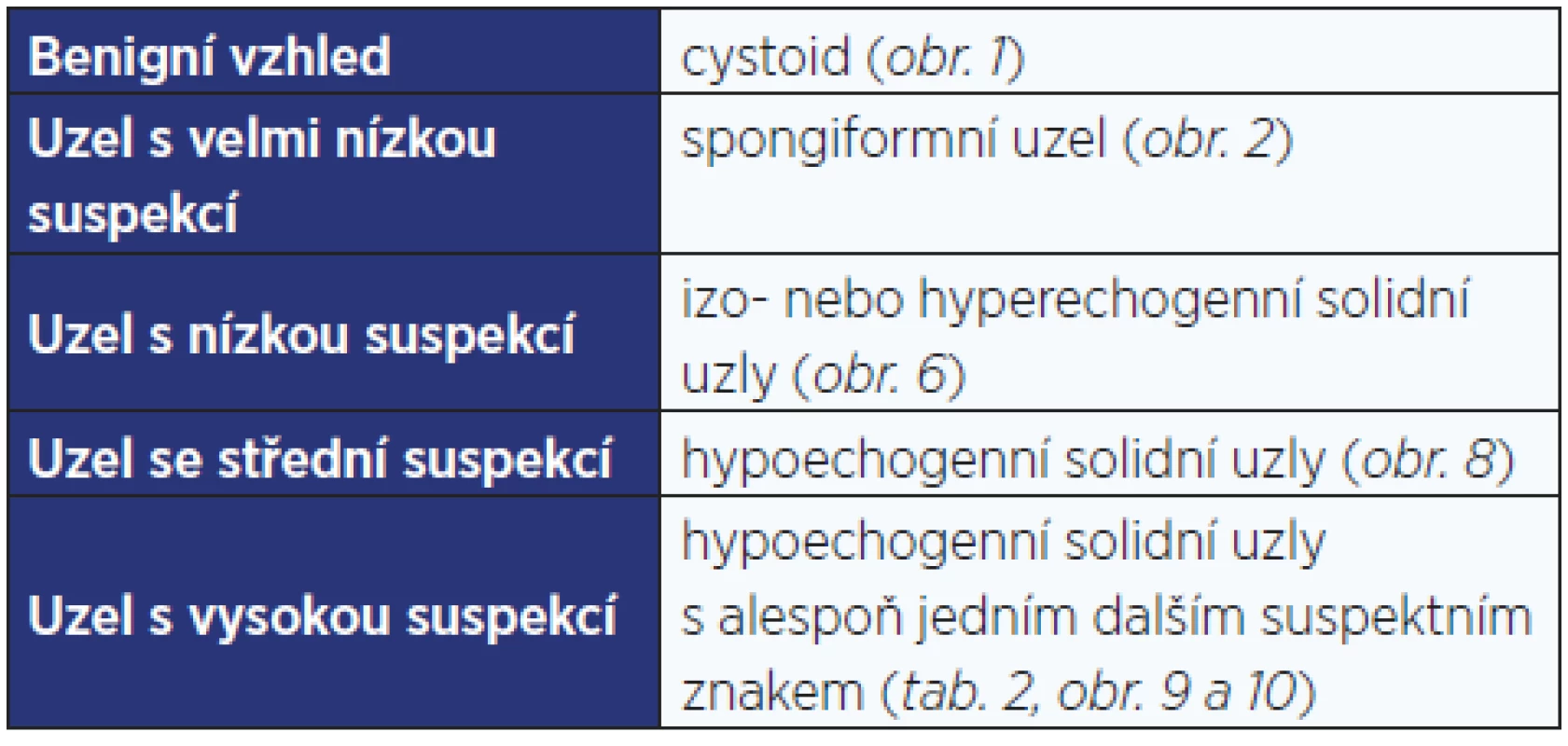
Pozn.: Podrobný popis jednotlivých kategorií je v textu. Podobnou podrobnější klasifikací je TIRADS (Thyroid Image-Reporting and Data System), která ale nebyla dosud odbornými společnostmi oficiálně přijata. 1. Indikace k FNAB a kategorizace ultrazvukového nálezu při prvním vyšetření
V indikaci k FNAB se zvažuje:
- UZ charakter uzlu (většinu uzlů lze zařadit do jedné z 5 kategorií – 1) a UZ suspektní známky malignity (tab. 2);
- velikost (> 1 cm, > 1,5 cm, > 2 cm);
- patologické lymfatické uzliny na krku a jiné známky extratyreoidální invaze (viz bod 8);
- klinické rizikové faktory (tab. 3)
Table 2. Ultrazvukové suspektní známky malignity tyreoidálního uzlu 
Pozn.: 1 Solidní uzel s nehomogenní texturou charakteru „sůl a pepř“ (střídají se nepravidelné oblasti nižší a vyšší echogenity, někdy až charakteru chobotů odlišné echogenity, které budí dojem nepravidelně smíchané soli a pepře, obr. 11); jde o obraz maligního růstu. 2 Nutno odlišit od situace, kdy má uzel špatně definovaný okraj a setřelé ohraničení proti okolí, což je běžné u benigních uzlů v polynodózní strumě (obr. 12). 3 Odlišit od koloidních agregací a hyperechogenních sept v spongiformních uzlech a cystoidech (obr. 3 a 4). Table 3. Klinické rizikové faktory malignity tyreoidálního uzlu 
Pozn.: 1 Na základě recentních dat se u diferencovaných tyreoidálních mikrokarcinomů klinicky významný maligní charakter uzlu manifestuje častěji u mladších osob (< 40 let), naopak u starších osob (≥ 60 let) ve většině případů diferencovaný mikrokarcinom neprogreduje do klinicky významného onemocnění. 1.1 Kategorie „Benigní vzhled uzlu (cystoid)“
Jde o cystoidy, riziko malignity je téměř nulové (obr. 1). Diagnostická FNAB není indikovaná s výjimkou případů, kdy UZ není schopen s jistotou odlišit, že jde o dutinu vyplněnou tekutinou nebo o silně hypoechogenní až anechogenní uzel. Evakuační FNAB je indikována pouze u symptomatických cystoidů nebo z kosmetických důvodů. Asymptomatické cystoidy ≤ 1 cm není třeba kontrolovat UZ, u asymptomatických cystoidů > 1 cm není shoda, zda mají být kontrolovány UZ; pokud ano, pak ne dříve než za 2 roky.
Image 1. Benigní vzhled uzlu (cystoid). 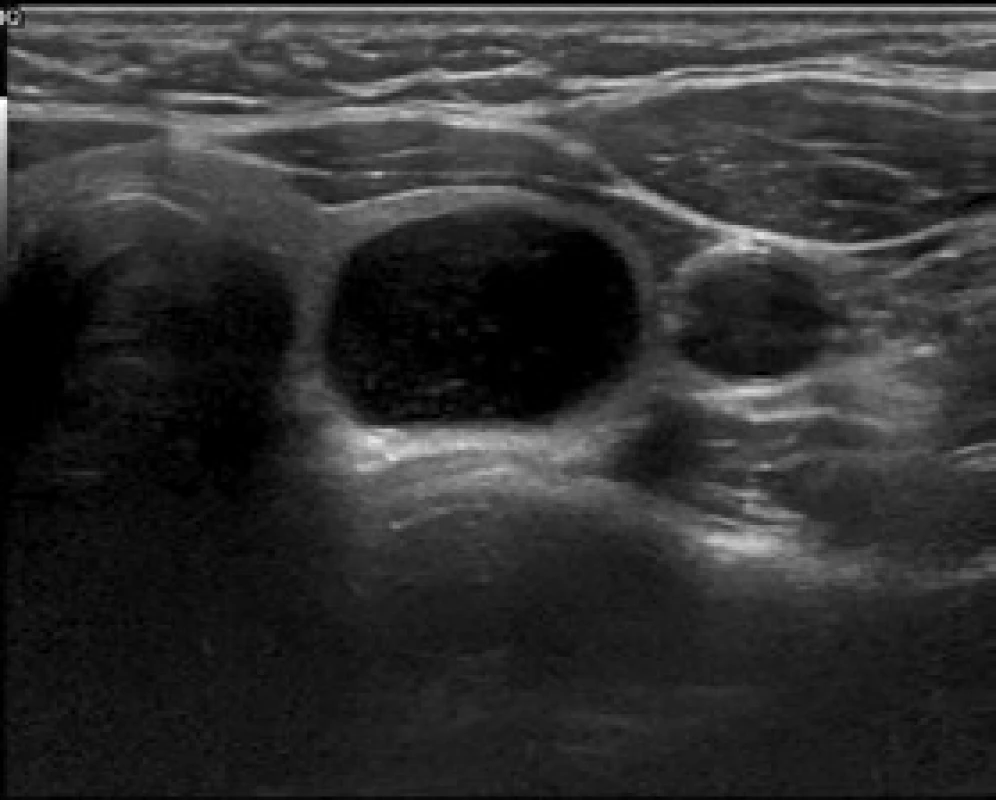
Riziko malignity < 1 %. 1.2 Kategorie „Uzel s velmi nízkou suspekcí“
Riziko malignity uzlů s velmi nízkou suspekcí je < 3 %. Patří sem tzv. spongiformní uzel, pro který je v UZ obrazu typický vzhled mycí houby, v řezu jsou patrné mnohočetné drobné či větší anechogenní dutiny vyplněné tekutinou (koloidem), oddělené hyperechogenními septy (obr. 2). V anechogenních dutinách nebo při jejich stěnách jsou často přítomné koloidní agregace (obr. 3), které se mohou někdy spolu s hyperechogenními septy (obr. 4) zaměnit za mikrokalcifikace. Koloidní agregace bývají okrouhlého tvaru (mikrokalcifikace jsou naopak často třískovité) a mívají tzv. artefakt ocasu komety (obr. 3).
Image 2. Příklady uzlů s velmi nízkou suspekcí (spongiformní uzly). 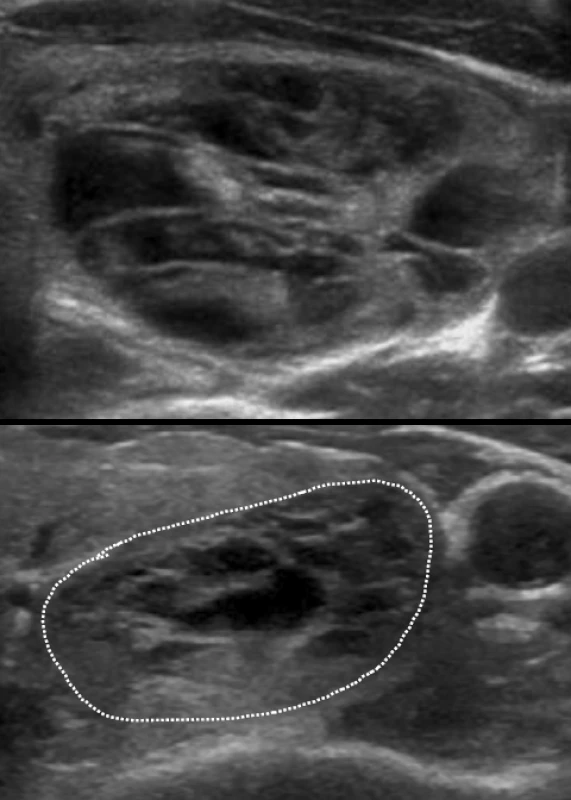
Riziko malignity < 3 %. Image 3. Koloidní agregace v cystoidu (A, comet tail artefact) a spongiformním (B) uzlu. 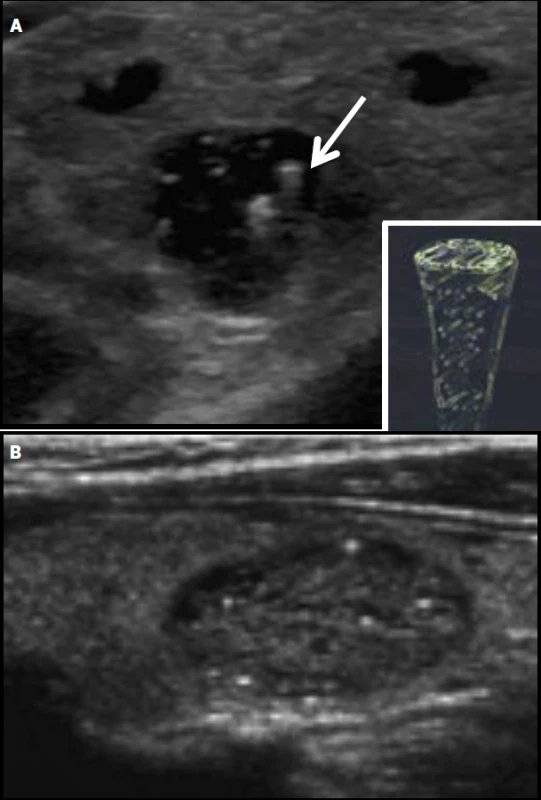
Riziko malignity < 1 %, resp. < 3 %. Image 4. Hyperechogenní septa ve spongiformním uzlu. 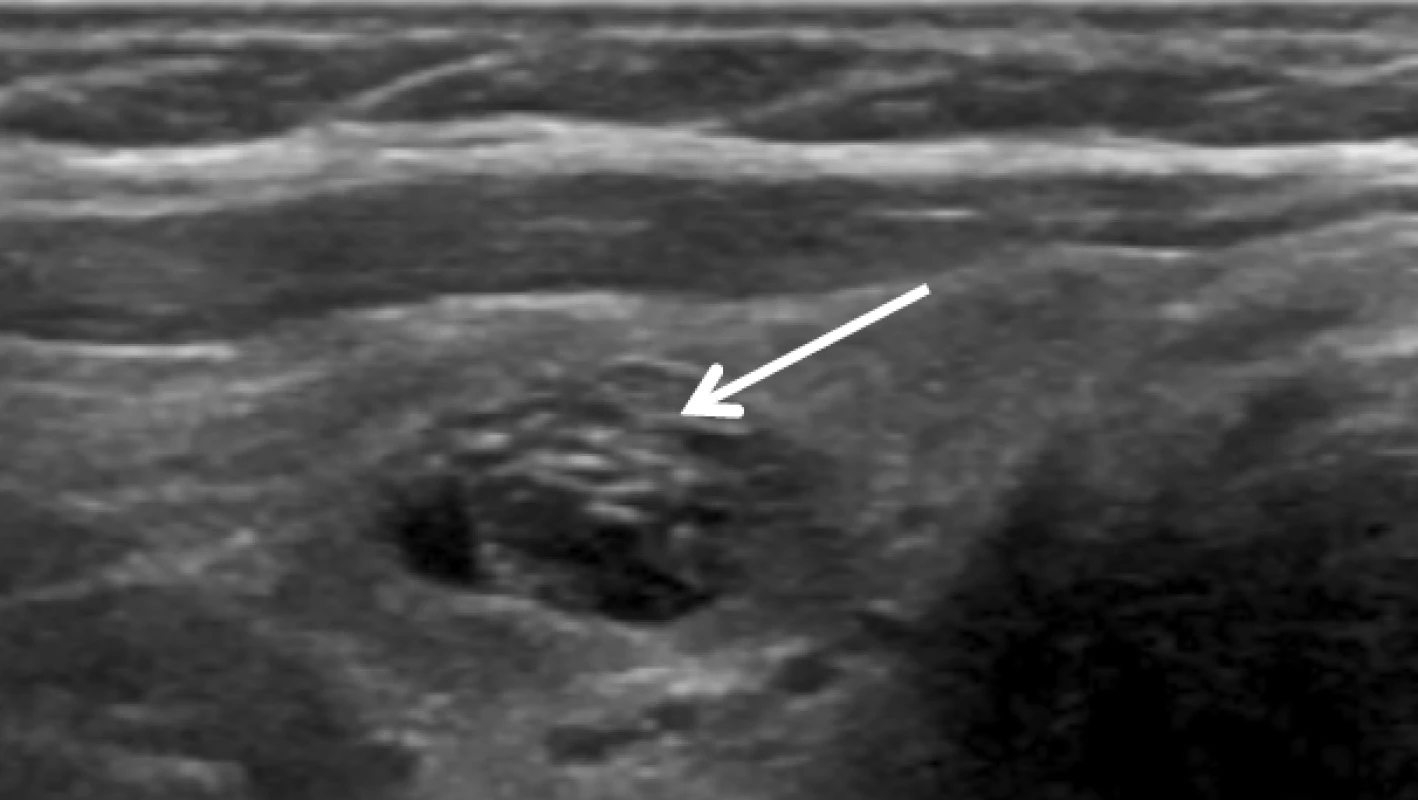
Riziko malignity < 3 %. Mikrokalcifikace jsou na rozdíl od hyperechogenních sept a koloidních agregací přítomné v solidních uzlech (obr. 9A). U uzlů s velmi nízkou suspekcí ≤ 2 cm není FNAB indikovaná, pokud nejsou známky extratyreoidální invaze a/nebo patologické lymfatické uzliny. V závislosti na ostatních rizikových faktorech (tab. 3), komorbiditách, očekávané délce života a preferenci pacienta se FNAB zvažuje u uzlů > 2 cm, avšak i v těchto případech je lze jen sledovat. Asymptomatické uzly ≤ 1 cm s nízkou suspekcí není třeba kontrolovat UZ, u asymptomatických uzlů > 1 cm není shoda, zda mají být kontrolovány UZ; pokud ano, pak ne dříve než za 2 roky.
Pozn.: malé spongiformní uzly (< 1 cm) s drobnými cystoidními dutinkami je někdy obtížné odlišit od hypoechogenních solidních uzlů, zejména pokud UZ nemá dostatečnou rozlišovací schopnost, která je daná zejména frekvencí (nejméně 12 MHz), počtem měničů sondy, případně možností harmonického zobrazení.
1.3 Kategorie „Uzel s nízkou suspekcí“
Riziko malignity činí 5–10 %.
Patří sem:
- solidní nebo hyperechogenní uzel (nemá charakter spongiformního uzlu) izoechogenní s pravidelným okrajem, často s hypo - či anechogenním lemem (obr. 5);
- smíšený uzel, který má v různém poměru zastoupenou solidní izo - nebo hyperechogenní komponentu a cystoidní komponentu (obr. 6);
- izo - nebo hyperechogenní uzel v terénu chronické lymfocytární tyreoiditidy (je izoechogenní s okolním zánětlivě změněným parenchymem a často je obtížné najít jeho přesné hranice) (obr. 7).
Image 5. Uzel s nízkou suspekcí. 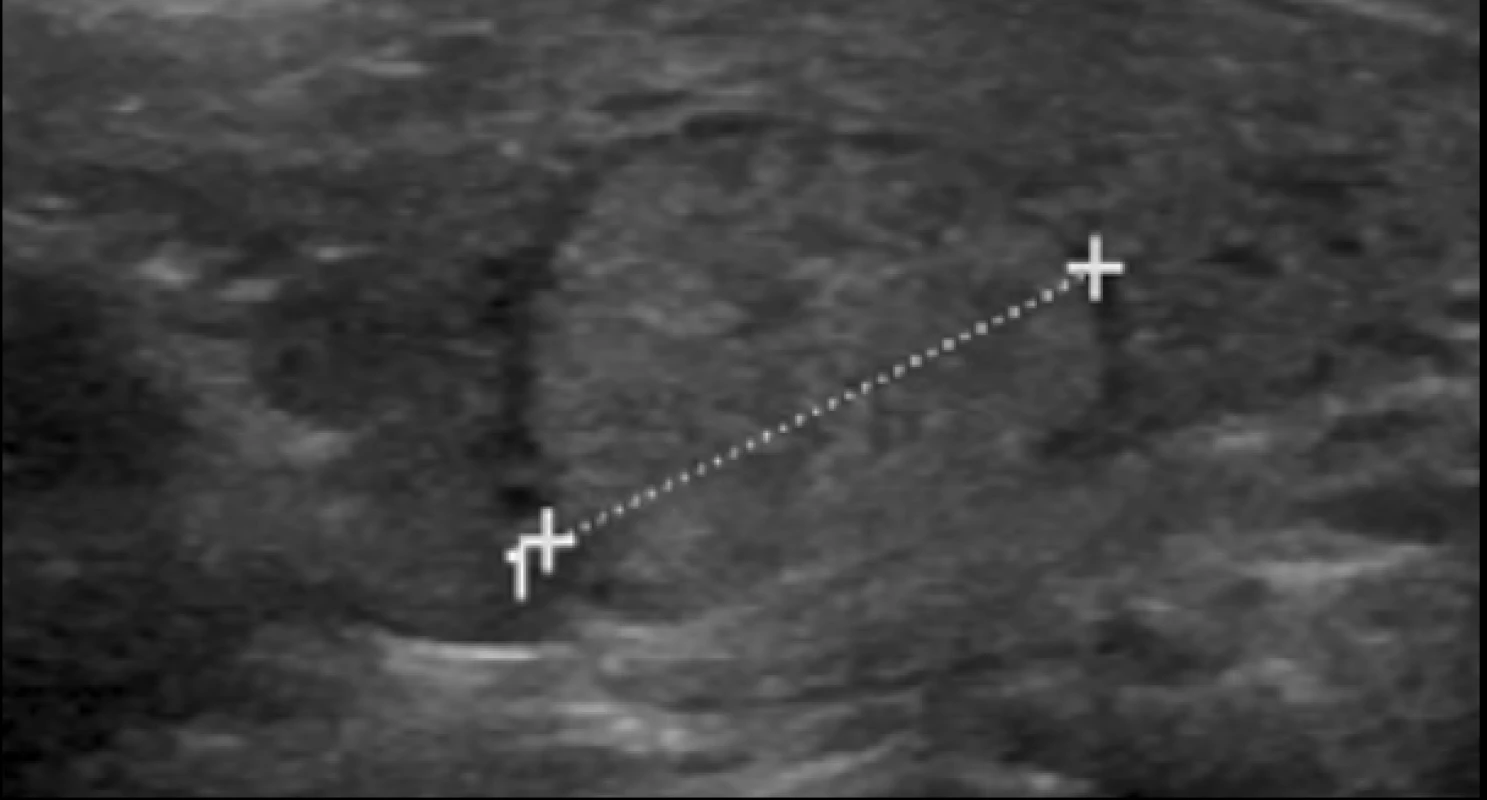
Riziko malignity 5–10 %. Image 6. Smíšený solidně-cystoidní uzel s nízkou suspekcí 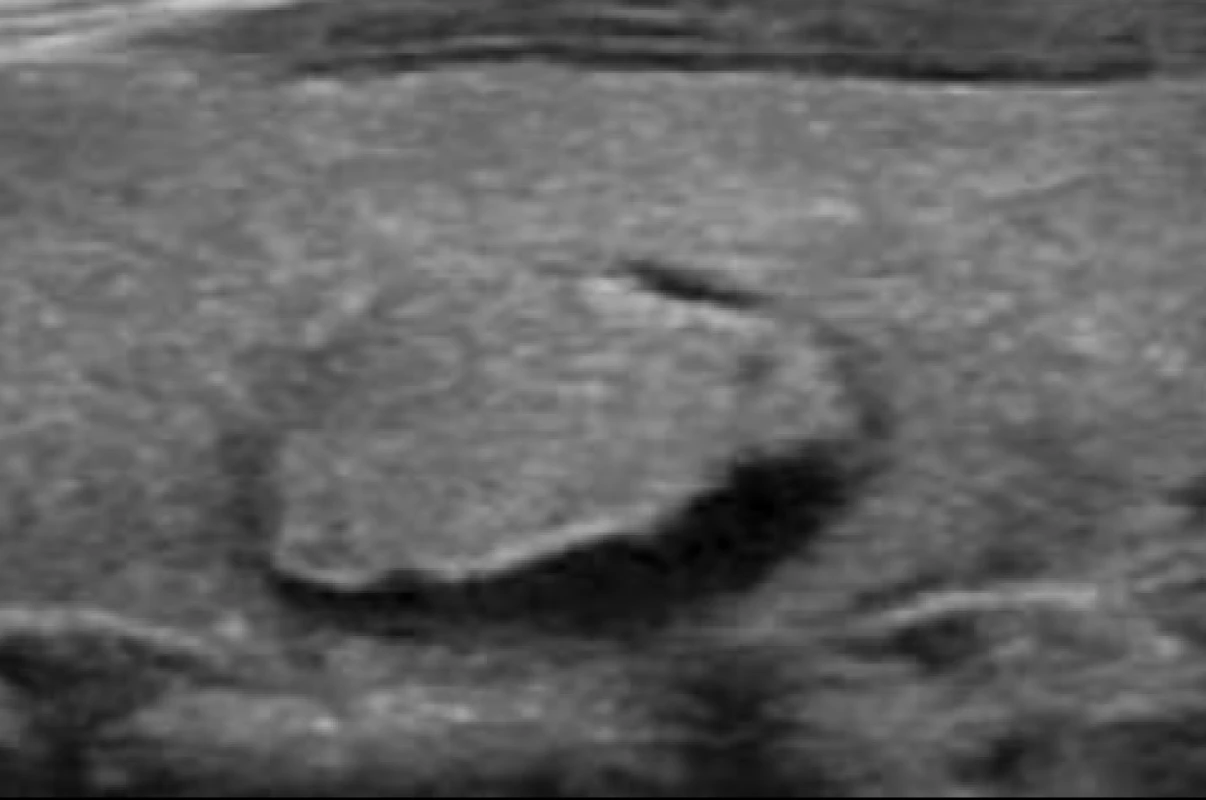
Image 7. Uzel s nízkou suspekcí v terénu chronické lymfocytární tyreoiditidy. . 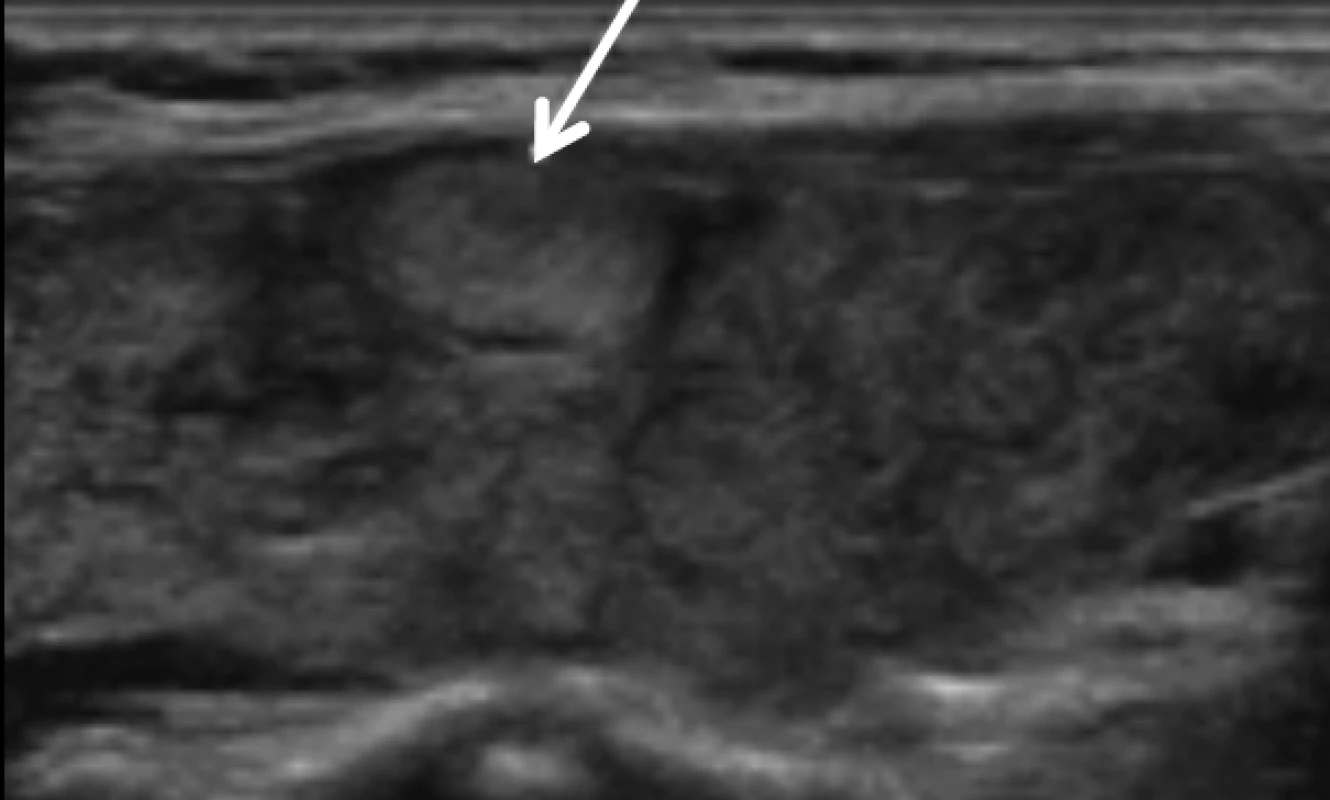
Riziko malignity 5–10 % Tyto uzly jsou indikovány k FNAB:
- při velikosti > 1,5 cm;
- jsou-li přítomné známky extratyreoidální invaze nebo patologické lymfatické uzliny, protože by mohlo jít o vzácný agresivní folikulární/onkofolikulární karcinom invazivní i při malé velikosti (většinou se naštěstí folikulární/onkofolikulární karcinomy stávají invazivními až při dosažení určité velikosti (obvykle > 2 cm).
1.4 Kategorie „Uzel se střední suspekcí“
Riziko malignity činí 10–20 %.
Patří sem:
- pravidelný solidní hypoechogenní uzel (obr. 8);
- solidní hypoechogenní komponenta smíšeného uzlu (echogenita je zřetelně nižší než okolní tyreoidální parenchym) bez dalších UZ suspektních znaků (tab. 2).
Image 8. Příklady uzlů se střední suspekcí (solidní hypoechogenní, bez další suspektních znaků). 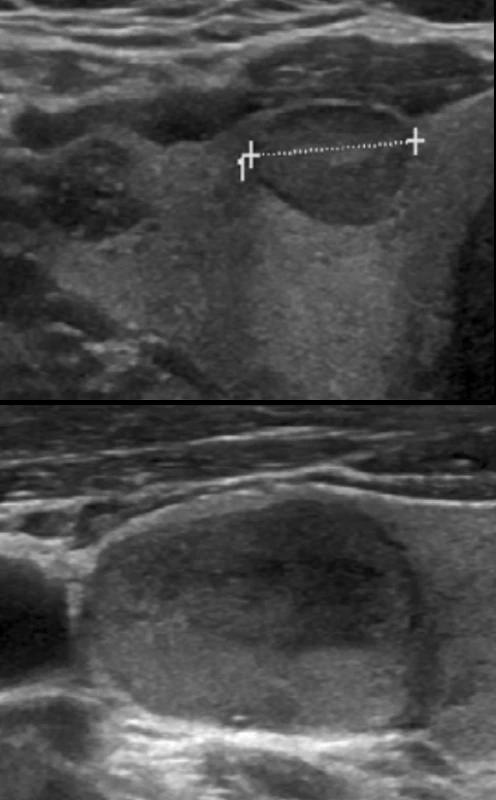
Riziko malignity 10–20 %. Tyto uzly jsou indikovány k FNAB:
- při velikosti >1 cm;
- jsou-li přítomné známky extratyreoidální invaze nebo patologické lymfatické uzliny.
1.5 Kategorie „Uzel s vysokou suspekcí“
Riziko malignity činí 70–90 %.
Patří sem:
- solidní hypoechogenní uzel nebo solidní hypoechogenní komponenta smíšeného uzlu (echogenita je zřetelně nižší než okolní tyreoidální parenchym) s alespoň jedním dalším UZ suspektním znakem: nepravidelný okraj uzlu (infiltrativní, makro - či mikrolobulární), mikrokalcifikace, uzel vyšší než širší v transverzální rovině, přerušovaná obvodová (rim) kalcifikace (tab. 2, obr. 9);
- solidní uzel s nehomogenní texturou charakteru „sůl a pepř“ (nepravidelné se střídají oblasti nižší a vyšší echogenity, někdy až charakteru chobotů odlišné echogenity, které budí dojem nepravidelně smíchané soli a pepře, 10).
Tyto uzly jsou indikovány k FNAB:
- při velikosti > 1 cm (při velikosti ≤ 1 cm je třeba zvažovat FNAB zejména u mladších či jinak rizikových osob);
- jsou-li přítomné známky extratyreoidální invaze nebo patologické lymfatické uzliny.
Pozn.: infiltrativní, makro - či mikrolobulární okraj uzlu je třeba odlišit od „špatně definovaného“ okraje uzlu, kdy nelze určit jeho přesné hranice. To je časté u benigních mnohočetných uzlů u polynodózní strumy/přestavby (obr. 11) nebo v terénu chronické lymfocytární tyreoiditidy (obr. 7).
Image 9. Příklady uzlů s vysokou suspekcí (A – solidní, hypoechogenní, nepravidelný tvar, tkáňové mikrokalcifikace, extratyreoidální invaze ventrálním směrem; B – solidní hypoechogenní, nepravidelný tvar, C – vyšší než širší v transverzální rovině). 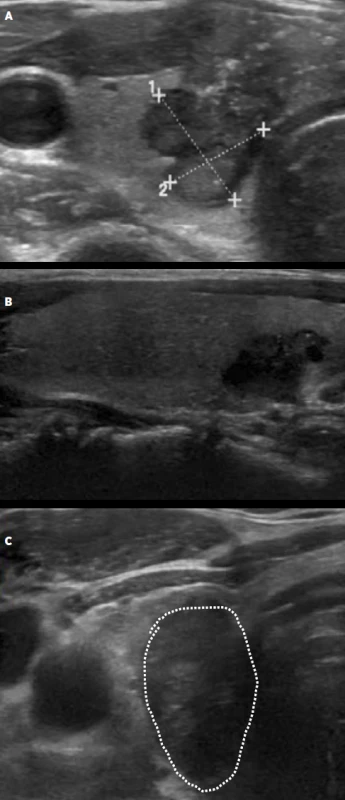
Riziko malignity 70–90 %. Image 10. Příklady uzlů s vysokou suspekcí charakteru „sůl a pepř“. Střídají se nepravidelné oblasti nižší echogenity (plné šipky) a vyšší echogenity (přerušované šipky), někdy až charakteru chobotů odlišné echogenity, které budí dojem nepravidelně smíchané soli a pepře). 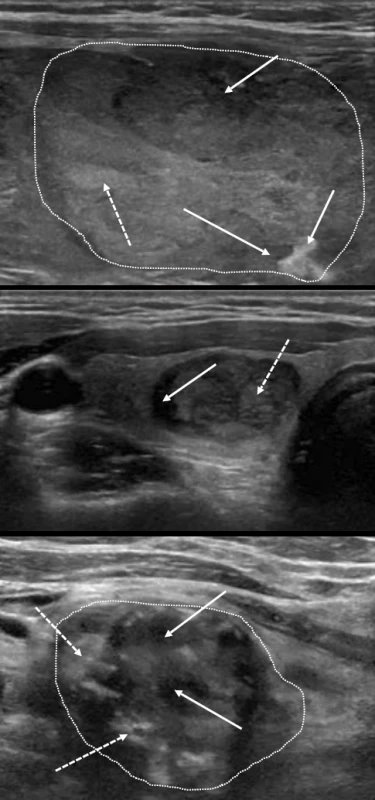
Riziko malignity 70–90 %. Image 11. Špatně definovaný okraj většinou mnohočetných uzlů bez dalších suspektních známek (nelze přesně určit jejich hranice). Jeden uzel přechází v druhý a normální parenchym je uzly zcela nahrazen uzly. 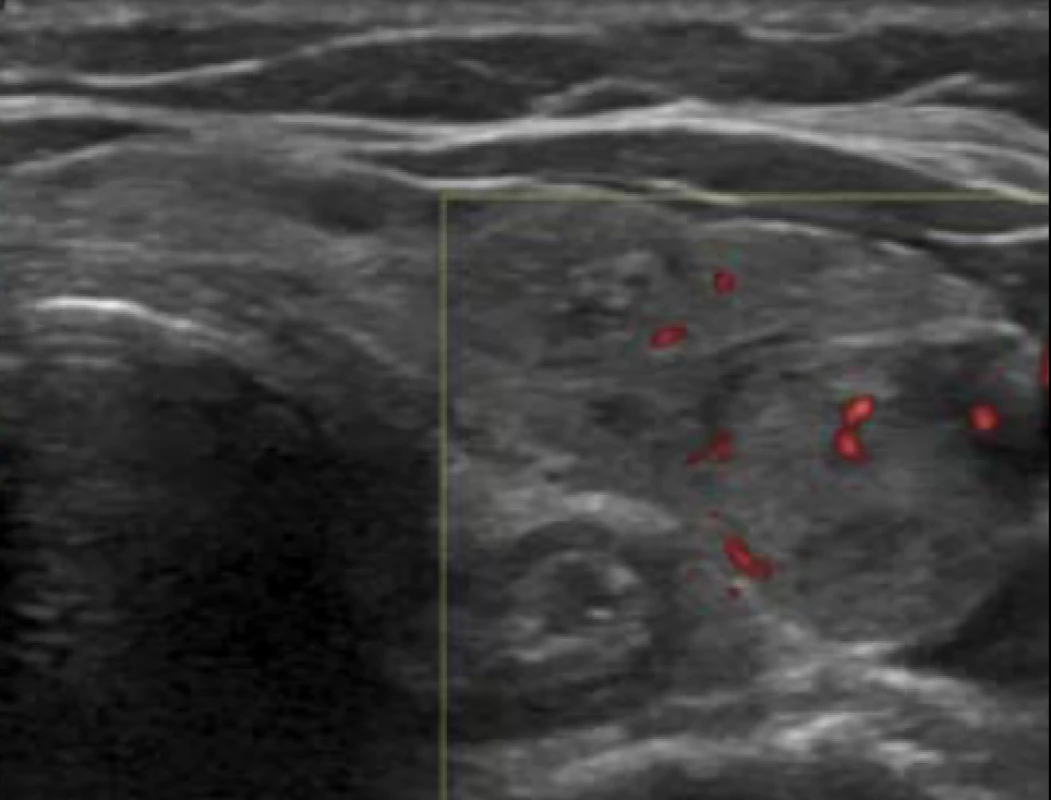
Riziko malignity 5–10 %. 1.6 Kategorie „Neurčitý/nezařaditelný uzel“
Uzel nelze zařadit do žádné z výše uvedených kategorií. Důvodem je špatná vyšetřitelnost daná nízkou kvalitou přístroje, habitem pacienta (nemožnost záklonu hlavy, vysoká vrstva tuku na krku apod.), nevhodným uložením uzlu (např. retrosternálně zasahující uzel) nebo nevhodnými podmínkami vyšetření (orientační vyšetření u lůžka s nemožností zatemnění místnosti apod.), eventuálně nezkušeností/nízkou erudicí vyšetřujícího.
Tyto uzly jsou indikovány k FNAB při velikosti > 1 cm nebo je indikován superkonziliární UZ.
1.7 Indikace k FNAB u mnohočetných uzlů
Každý uzel > 1 cm by měl být posuzován zvlášť podle stejných pravidel jako u solitárních uzlů. Individuální riziko malignity pro pacienta je u solitárních uzlů stejné jako u mnohočetných uzlů. U mnohočetných uzlů s nízkou nebo velmi nízkou suspekcí, které kompletně nahrazují normální parenchym (klasická polynodózní přestavba/struma), je riziko malignity nízké. V těchto případech se provádí FNAB největšího uzlu, pokud je > 2 cm, alternativním postupem jsou UZ kontroly bez FNAB (iniciálně za 1–2 roky a dále za 3–5 let).
2. Další postup u uzlů, které nesplňují kritéria pro FNAB
Je uveden přehledně v tab. 4.
Table 4. Další postup u uzlů, které nesplňují kritéria pro indikaci FNAB 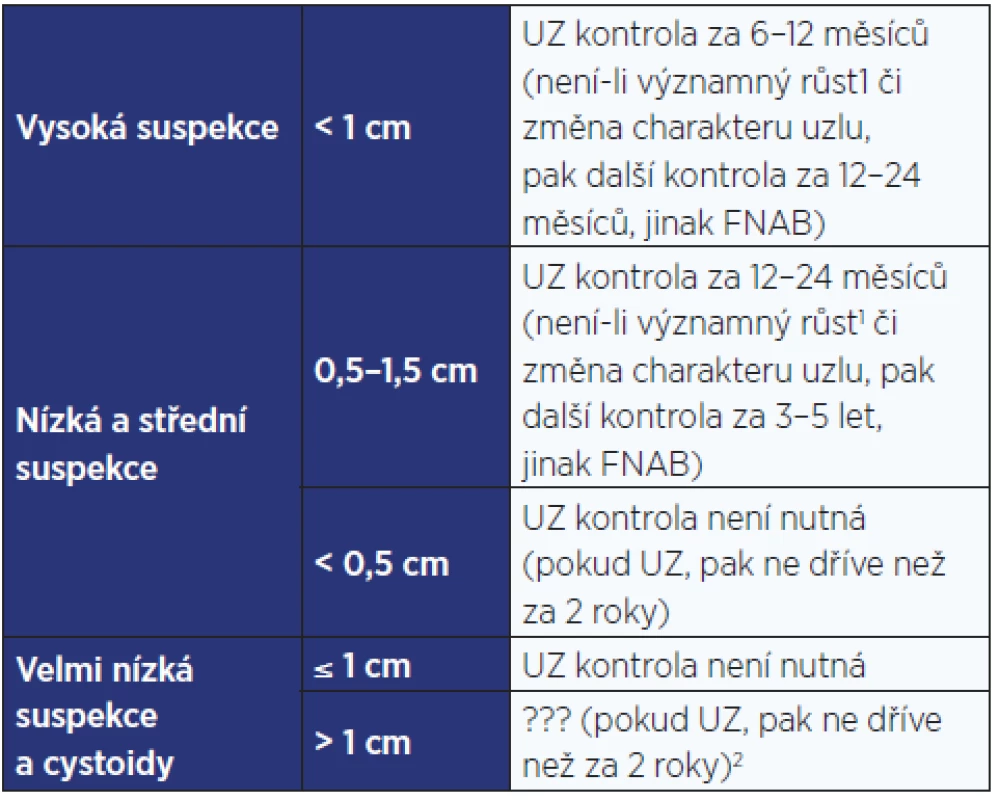
Pozn.: 1 Viz tab. 11. 2 Není jasné, zda je u asymptomatických cystoidů a uzlů s velmi nízkou suspekcí > 1 cm UZ kontrola vůbec nutná, u symptomatických uzlů se UZ kontrola provádí podle klinické potřeby. 3. Kategorizace výsledku FNAB a další postup
Z důvodu lepší standardizace dalšího postupu a zlepšení péče o pacienty s minimalizací nežádoucích důsledků z podhodnocení (přehlédnutá malignita) i nadhodnocení (zbytečné operace) by měl být výsledek FNAB kategorizován podle rizika malignity. Jako nejvhodnější se k tomuto účelu jeví tzv. klasifikace Bethesda (tab. 5), ačkoliv ani ona, zejména z důvodu problematické kategorie III, není optimální. Další postup u jednotlivých kategorií Bethesda je podrobně popsán v tab. 6–10. Zjednodušeně řečeno, ve většině případů u kategorií Bethesda I a III opakujeme FNAB, u kategorie II sledujeme uzel ultrazvukem a v případě významného růstu uzlu (tab. 11) a/nebo změny charakteru uzlu indikujeme opakování FNAB; u kategorie IV indikujeme operaci (hemi - nebo totální tyreoidektomii) zejména s cílem histologického ověření uzlu a u kategorií V a VI indikujeme totální tyreoidektomii jako terapeutický výkon.
Table 5. Bethesda klasifikace cytologických nálezů u tyreoidálních uzlů 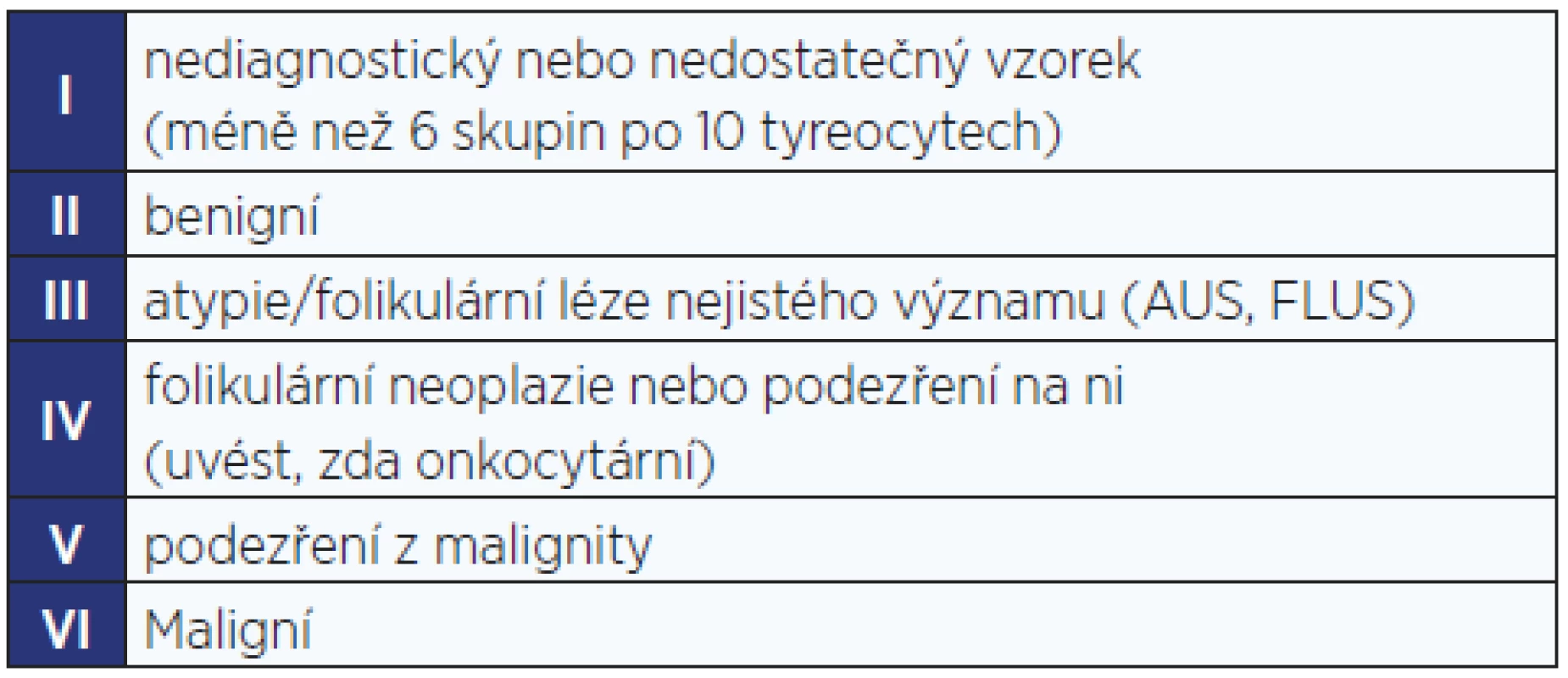
Table 6. Další postup u výsledku FNAB Bethesda I. Riziko malignity činí 2–4 %1. 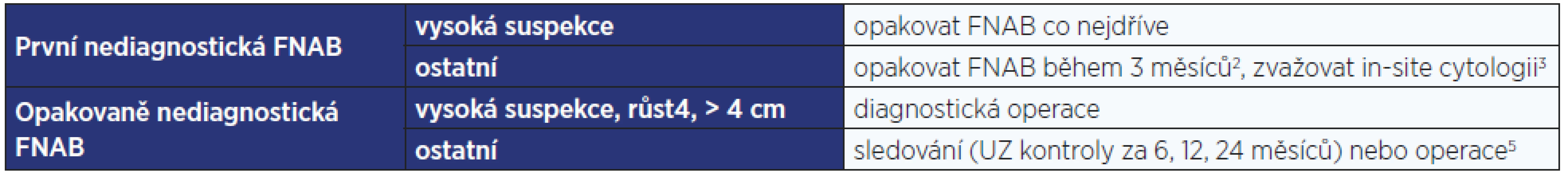
Pozn.: 1 Celkové riziko malignity je v kategorii Bethesda I relativně malé (1–2 %); u uzlů, které byly operovány, bylo 9–32 %, což je ale ovlivněno selekčním zkreslením. 2 Podle některých autorů je vhodné opakovat FNAB ne dříve než za 3 měsíce, z důvodu možného rizika falešně pozitivního nálezu při reparativních změnách po předchozí punkci; dostatek důkazů pro tento postup ale není. 3 Zhodnocení reprezentativnosti vzorku přítomným patologem během FNAB. 4 Kritéria významného růstu jsou uvedeny v tab. 11. 5 Zvážit lze v těchto případech i poměr rizik, nákladů a benefitů core-cut biopsie (je málo senzitivní pro papilární karcinom) nebo molekulárního vyšetření, pro efektivitu těchto metod však není dostatek dat. Table 7. Další postup u výsledku FNAB Bethesda II. Riziko malignity činí průměrně 1–2 %1. 
Pozn.: 1 Průměrný podíl falešně negativních 1–2 % lze hodnotit jako relativně malý; pokud je FNAB ze stejného uzlu hodnocena ≥ 2× jako Bethesda kategorie II, je riziko malignity minimální. 2 Efektivita UZ k hodnocení růstu jako indikátoru přehlédnuté malignity není známá (spíše je limitovaná), nicméně kontrolní UZ obvykle provádíme (iniciálně za 2 roky a dále za 3–5 let, pokud je uzel stabilní, nebo dříve, pokud dojde k progresi). 3 UZ provádíme pouze u rostoucích uzlů nebo když se objeví příznaky z lokálního tlaku; UZ kontroly s cílem hodnotit riziko malignity nejsou indikované. Table 8. Další postup u výsledku FNAB Bethesda III. Riziko malignity činí 6–48 %1. 
Pozn.: 1 Riziko malignity v kategorii Bethesda III je odlišné v jednotlivých centrech (průměrně 16 %) a významně závisí na erudici cytopatologa. 2 Protože riziko malignity je v jednotlivých centrech u kategorie Bethesda III velmi variabilní (6–48 %), závisí postup na zkušenostech centra (např. v centru s rizikem malignity 48 % je namístě operace, naopak v centru s rizikem malignity 6 % lze uzel sledovat UZ); riziko malignity ovšem stoupá, pokud je kategorie Bethesda III stanovena opakovaně. Table 9. Další postup u výsledku FNAB Bethesda IV. Riziko malignity činí 14–33 %. 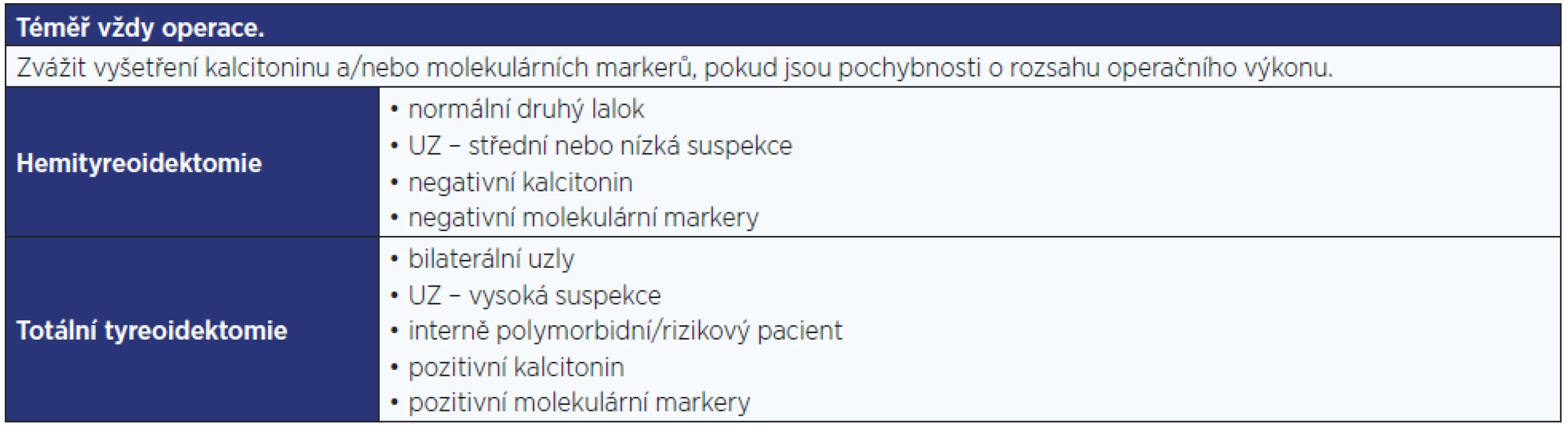
Table 10. Další postup u výsledku FNAB Bethesda V a VI. Riziko malignity činí 53–87 % u Bethesda V a 94–100 % u Bethesda VI. 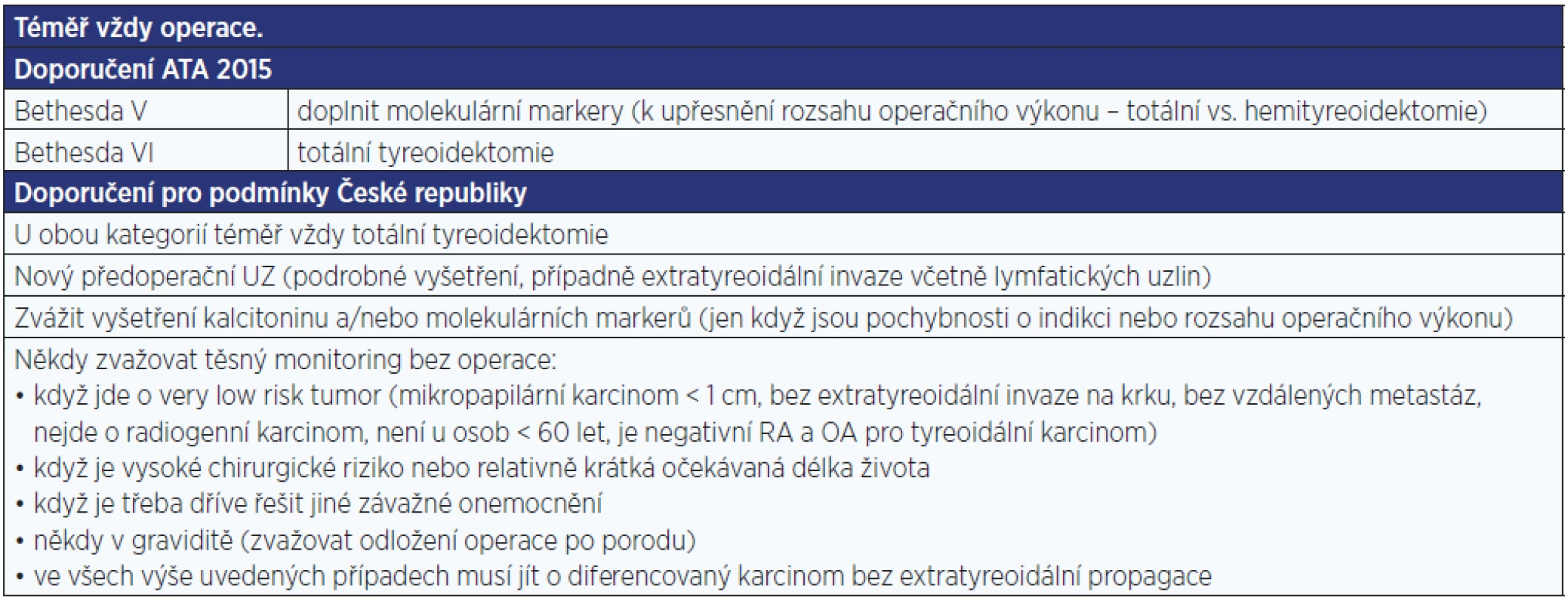
Table 11. Kritéria významného růstu uzlu 
4. Tyreoidální stimulační hormon v séru
Je-li TSH suprimovaný, doplní se fT3, fT4, protilátky proti receptoru TSH v séru a scintigrafie 99mTc-technecistanem (123I u nás není běžně k dispozici) a dále se pokračuje v léčbě hypertyreózy dle zvyklostí. Je-li uzel hyperfunkční a hyperakumulující, je riziko malignity sice minimální a podle ATA FNAB není nutná, v podmínkách České republiky se většinou i přesto indikace k FNAB řídí velikostí a UZ charakterem uzlu.
Je-li TSH zvýšený, léčíme hypotyreózu. Vyšší riziko malignity bylo v retrospektivních studiích prokázáno i u uzlů s TSH v horním pásmu normy, nicméně nejsou důkazy, že by léčba levothyroxinem s cílem snížit TSH do dolního pásma normy toto riziko snížila, a proto ji nelze u eutyroidních pacientů rutinně doporučit.
5. Molekulární diagnostika
ATA doporučuje zvážit molekulární vyšetření z FNAB u pacientů s kategorií Bethesda III a IV. U kategorií V a VI může molekulárně genetické vyšetření přispět k odhadu agresivity u PTC, pokud jsou pochybnosti o indikaci či radikalitě chirurgického výkonu. ATA však současně uvádí, že není známa efektivita ani nákladová efektivita molekulárně genetického vyšetření z FNAB, a důrazně také doporučuje, aby bylo prováděno výhradně v certifikovaných laboratořích.
Existují dva základní přístupy k molekulárnímu vyšetření z FNAB (tab. 12). Prvním je průkaz různé exprese většího množství genů – např. gene expression classifier (GEC, s analýzou 167 genů) a druhým je detekce mutací či přeskupení v hlavních příčinných genech (BRAF, NRAS, HRAS, KRAS, RET/PTC1, RET/PTC3 a PAX8/PPARγ) pomocí real-time PCR či sekvencí, např. využitím komerčně nabízených panelů. V ČR je na specializovaných pracovištích v praxi dostupné využití panelů, které sice nemají dostatečnou senzitivitu, aby v kategoriích III a IV spolehlivě vyloučily malignitu a uchránily tak před operací, lze je však v těchto kategoriích zvážit k odhalení přehlédnutého PTC, což může změnit radikalitu operačního výkonu (z diagnostické hemityreoidektomie na totální tyreoidektomii). ATA u kategorií III a IV vyšetření pomocí komerčních panelů nedoporučuje a preferuje zvažovat GEC, který má lepší senzitivitu, avšak není v ČR dostupný. Panely genů či samostatné stanovení mutace BRAF lze také zvažovat u cytologie s výsledkem PTC (Bethesda V či VI) jakožto významného prognostického markeru agresivity a horší prognózy.
Table 12. Možnosti preoperačního vyšetření molekulárních markerů 
Pozn.: 1 V ČR dostupné ve specializovaných centrech. 2 Např. při zvažování preventivní disekce krčních lymfatických uzlin v centrálním kompartmentu apod. 3 Nelze použít k vyloučení malignity, lze ho však v těchto kategoriích zvážit k odhalení případného přehlédnutého papilárního karcinomu, což může změnit radikalitu operačního výkonu (z diagnostické hemityroidektomie na totální tyreoidektomii), byť nákladová efektivita takového postupu není známá. 4 V ČR není dostupný. Pokud je klinické podezření na medulární karcinom a diagnózu se nepodaří stanovit jinak (FNAB, sérový kalcitonin), lze zvažovat vyšetření kalcitoninu z FNAB nebo molekulární vyšetření somatických mutací v protoonkogenu RET (příčina až 50 % sporadických a téměř 100 % familiárních MTC) z FNAB ve specializovaném centru.
6. Elastografie a další pomocné zobrazovací techniky
Elastografie je aktuálně považována za pomocnou vyšetřovací metodu, která vychází z teoretického předpokladu, že benigní uzly jsou měkké a maligní tuhé (obr. 12). Diagnostická přesnost elastografie byla v provedených studiích velmi variabilní. V jedné studii byla dokonce horší než u konvenčního B-mode ultrazvuku. Nevýhodou elastografie je velká interpersonální variabilita a fakt, že dostatečná spolehlivost metody je pouze u vybraných uzlů – obvykle u solidních v jinak normální štítné žláze.
Image 12. Elastograficky tuhý (A) a měkký (B) uzel 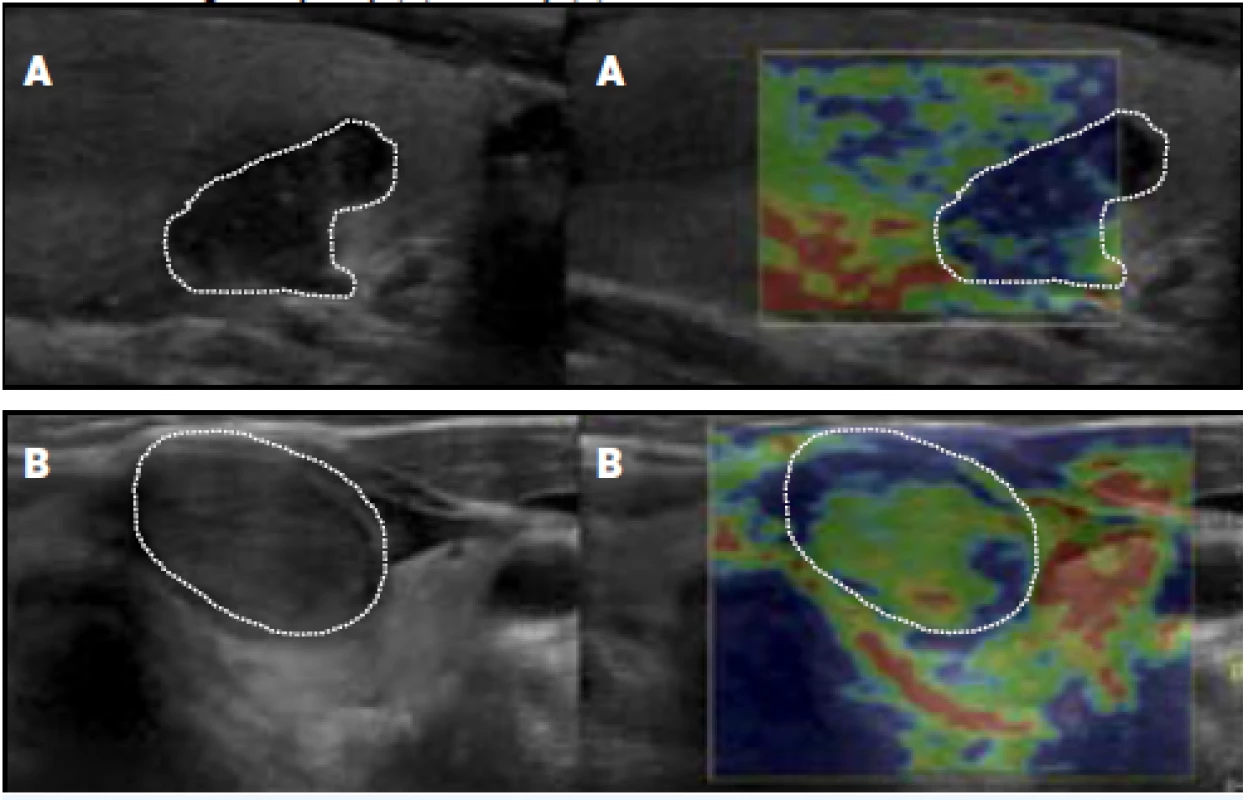
Podle našich zkušeností je elastografie přínosná zejména u solidních uzlů velikosti 0,5–2 cm, u kterých jsou pochybnosti, zda indikovat FNAB, nebo není jasný další postup při nediagnostické FNAB. Naopak není přínosná u uzlů v terénu polynodózní strumy a/nebo autoimunitní tyreoiditidy, příliš malých (< 1 cm) a příliš velkých (> 3 cm), s mikrokalcifikacemi, v těsném vztahu k průdušnici a často ani u uzlů u pacientů příliš astenických nebo naopak obézních, kdy přesnému vyšetření brání anatomické poměry. Elastografie rozhodně nenahrazuje konvenční B-mode ultrazvuk a měla by se provádět pouze u vybraných vhodných uzlů, kde lze očekávat relativně spolehlivý výsledek.
Hodnocení intenzity a charakteru vaskularizace uzlu není u tyreoidálních uzlů dostatečně spolehlivé a ATA je mezi rizikové faktory nezařazuje. Význam má ověření úplné absence vaskularizace u benigních cystoidů. Podobně absence anechogenního lemu není dle ATA považována za rizikový faktor, nicméně platí, že jeho přítomnost svědčí pro benigní uzel (často u kategorie „uzel s nízkou suspekcí“, bod 1.3).
V preoperační diagnostice je doporučeno CT s kontrastem nebo MRI krku jako pomocná metoda u pacientů s klinicky lokálně pokročilým tumorem (s klinicky zjevnou invazí do okolí a do krčních lymfatických uzlin).
V preoperační diagnostice s cílem zhodnocení rizika malignity tyreoidálních uzlů se nedoporučuje provádět 18FDG-PET ani scintigrafii z důvodu nedostatečné přesnosti.
7. Kalcitonin
Z důvodu nedostatku dat nedal panel ATA 2015 doporučení rutinně vyšetřovat sérový bazální kalcitonin u tyreoidálních uzlů, ale ani ho nestanovovat. Vyšetření bazálního kalcitoninu bez stimulačního testu není dostatečně efektivní, přináší příliš velké množství výsledků v nediagnostickém pásmu a podle některých studií vedlo ke zbytečným operacím.
Další problém je s referenčními mezemi a cut-offs, které nejsou standardizované. V současné době není dostupný pentagastrin, takže se ke stimulaci používá kalcium, avšak standardizace kalciového testu není optimální. Referenční meze a navrhované cut-offs bazálního a stimulovaného kalcitoninu jsou uvedeny v tab. 13, nicméně mohou se lišit v závislosti na použité metodě. Aktuálně nelze doporučit rutinní vyšetřování bazálního kalcitoninu u všech uzlů, avšak provádí se v případě klinického či cytologického podezření na medulární karcinom štítné žlázy (MTC) a může být užitečné k upřesnění rozsahu výkonu u uzlů, které jsou indikované k operaci (Bethesda IV, V a VI), eventuálně v případě diagnostických rozpaků (opakovaně Bethesda I či III).
Table 13. Referenční meze a cut-offs pro pozitivní kalcitonin 
Pozn.: 1 Pozitivní výsledek testu znamená buď medulární karcinom štítné žlázy (MTC), nebo hyperplazii C buněk (CCH); hyperplazie C buněk je sice prokázanou prekancerózou u nositelů mutace v protoonkogenu RET, avšak u osob bez mutace není její klinický význam jasný a není prokázané, že jde o prekancerózu. 2 Pentagastrin není k dispozici. Pokud je klinické podezření na MTC a diagnózu se nepodaří stanovit jinak (FNAB, sérový kalcitonin), lze zvažovat vyšetření kalcitoninu z FNAB nebo molekulární vyšetření somatických mutací protoonkogenu RET (příčina až 50 % sporadických a téměř 100 % familiárních MTC) z FNAB ve specializovaném centru.
8. Suspektní lymfatické uzliny na krku a jiné známky extratyreoidální invaze
Ultrazvuk lymfatických uzlin hodnotí velikost a strukturu. Z hlediska strukturálních změn rozlišujeme uzliny benigního, neurčitého a suspektního charakteru (tab. 14, obr. 13). Přibližné cut-offs pro patologické velikosti lymfatických uzlin jsou uvedeny v tab. 15, nicméně samotné zvětšení neznamená automaticky infiltraci a je třeba současně hodnotit velikost i charakter. Metastázy tyreoidálního karcinomu se typicky nacházejí v kompartmentech VI, II, III, IV a V (obr. 14).
Table 14. Ultrazvuková charakteristika krčních lymfatických uzlin 
Image 13. Ultrazvukový obraz lymfatické uzliny benigního (A), neurčitého (B) a maligního (C) charakteru 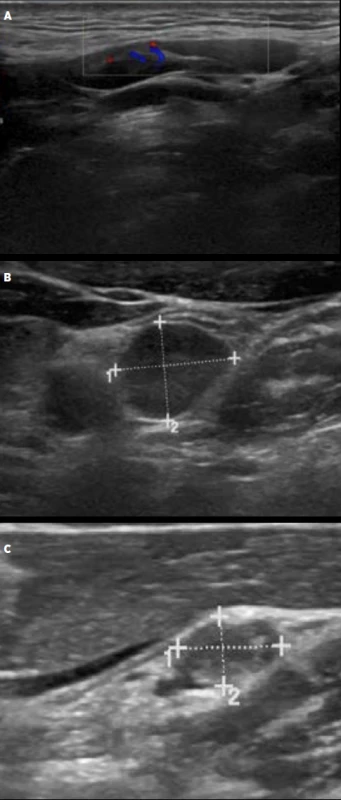
Image 14. Kompartmenty krčních lymfatických uzlin 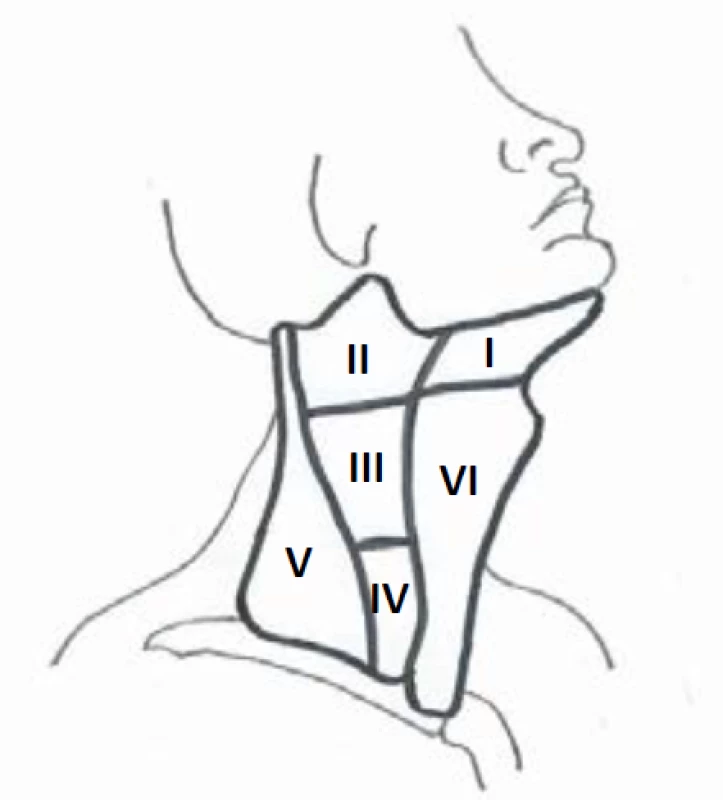
V předoperační diagnostice je u zvětšených suspektních lymfatických uzlin indikovaná FNAB z uzliny a cytologické vyšetření, případně stanovení tyreoglobulinu z uzliny. Na rozdíl od pacientů po tyreoidální ablaci, kde byla dle ATA 2015 za cut-off pro pozitivní tyreoglobulin v uzlině navržena hodnota 1 ng/ml, je v preoperační diagnostice vyšetření tyreoglobulinu z punktátu uzliny obtížně hodnotitelné. Podle jedné z prací byl cut-off při normální štítné žláze 32 ng/ml, což ovšem nelze považovat za hodnotu obecně platnou.
Table 15. Cut-offs velikosti pro patologické lymfatické uzliny na krku 
9. Terapie benigních tyreoidálních uzlů a cystoidů
Supresní terapie levothyroxinem se u benigních tyreoidálních uzlů u eutyroidních pacientů nedoporučuje, protože má větší rizika než prospěch. V terénu tyreoidálních uzlů je na místě léčba hypotyreózy včetně subklinické (zejména je-li příčinou chronická lymfocytární tyreoiditida), pokud nepřeváží rizika terapie levothyroxinem (opatrnost je nutná zejména u starších pacientů). U osob s TSH v horním pásmu normy lze u rostoucích uzlů a/nebo symptomatických uzlů a/nebo uzlů v terénu chronické lymfocytární tyreoiditidy zvažovat i izohormonální (euthyroxinemickou) terapii.
U symptomatických benigních uzlů je třeba zvažovat chirurgické řešení (alternativní postupy, jako jsou radiofrekvenční či laserová ablace nebo ablace vysokofrekvenčním ultrazvukem se provádějí pouze v některých centrech a jejich efektivita a nákladová efektivita nejsou známé). Asymptomatické uzly se někdy doporučují operovat při velikosti > 4 cm, dostatečná data pro tento postup však nejsou k dispozici.
Symptomatické recidivující cystoidy a uzly s dominantní cystoidní složkou s benigní FNAB ze solidní složky lze jako alternativu operace po předchozí evakuaci sklerotizovat alkoholem (v některých centrech je sklerotizace cystoidů metodou první volby). Pokud jsou cystoidy evakuovány, doporučuje se odeslat aspirovanou tekutinu k cytologickému vyšetření, ačkoliv výtěžnost je mnohem horší než u nátěru na sklíčko a nejsou k dispozici kritéria pro reprezentativnost ani data o přesnosti a spolehlivosti tohoto vyšetření. Asymptomatické cystoidy stačí sledovat.
Seznam použitých zkratek:
ATA American Thyroid Association
FNAB tenkojehlová aspirační biopsie
FNAC tenkojehlová aspirační cytologie
UZ ultrazvuk
TSH tyreoidální stimulační hormon
fT4 volný thyroxin
fT3 volný trijodthyronin
18FDG-PET pozitronová emisní tomografie s 18fluorodeoxyglukózou
PTC papilární karcinom štítné žlázy
MTC medulární karcinom štítné žlázy
Adresa pro korespondenci:
doc. MUDr. Jan Jiskra, Ph.D.
3. interní klinika 1. LF UK a VFN v Praze
U Nemocnice 1
128 08 Praha 2
Tel.: 224 962 919, 224 962 958
e-mail: jan.jiskra@lf1.cuni.cz
Sources
1. Haugen BR, Alexander EK, Bible KC et al. 2015 American Thyroid Association management guidelines for adult patients with thyroid nodules and differentiated thyroid cancer: the American Thyroid Association Guidelines Task Force On Thyroid Nodules And Differentiated Thyroid Cancer. Thyroid 2016; 26(1): 1–133.
2. Leenhardt L, Erdogan MF, Hegedus L et al. 2013 European Thyroid Association guidelines for cervical ultrasound scan and ultrasound-guided techniques in the postoperative management of patients with thyroid cancer. Eur Thyroid J 2013; 2(3): 147–159.
Labels
Addictology Allergology and clinical immunology Angiology Audiology Clinical biochemistry Dermatology & STDs Paediatric gastroenterology Paediatric surgery Paediatric cardiology Paediatric neurology Paediatric ENT Paediatric psychiatry Paediatric rheumatology Diabetology Pharmacy Vascular surgery Pain management Dental Hygienist
Article was published inJournal of Czech Physicians

-
All articles in this issue
- Nadměrný růst u dětí a dospělých: nový klinický pohled, nové geny, nové fenotypy
- Diagnostika a další péče o pacienty s tyreoidálními uzly: doporučení American Thyroid Association 2015 modifikované pro podmínky České republiky
- Adrenokortikální insuficience
- Hypogonadismus u mužů a jeho léčba
- Léčba hypofyzárních adenomů
- Biologické aspekty ADHD (hyperkinetické poruchy) a poruch chování v dětském a adolescentním věku, vybrané preventivní aspekty
- Journal of Czech Physicians
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Hypogonadismus u mužů a jeho léčba
- Nadměrný růst u dětí a dospělých: nový klinický pohled, nové geny, nové fenotypy
- Adrenokortikální insuficience
- Diagnostika a další péče o pacienty s tyreoidálními uzly: doporučení American Thyroid Association 2015 modifikované pro podmínky České republiky
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

