-
Medical journals
- Career
Chirurgické techniky v době nedostatku dárců
Authors: M. Oliverius
Authors‘ workplace: Klinika transplantační chirurgie IKEM Praha, přednosta MU Dr. Jiří Froněk, Ph. D., FRCS
Published in: Vnitř Lék 2013; 59(8): 682-685
Category:
Overview
Od doby první úspěšné transplantace v České republice uplynulo 30 let. Počet výkonů a jejich potřeba trvale narůstá. Vzhledem k trvalému nedostatku dárců bylo vyvinuto mnoho nových technik, které mají za úkol zvýšit počet jaterních štěpů vhodných k transplantaci, a zároveň tak snížit počet úmrtí pacientů na čekací listině. Nejaktuálnější je tato potřeba v oblasti transplantace jater dětí, zejména nejmenších váhových skupin. Práce se zabývá jednotlivými technikami a jejich dostupností v Čechách. Mezi nejčastěji používané patří jaterní redukce a SPLIT jater. Dále bylo provedeno několik úspěšných domino transplantací a transplantací od žijícího dárce. Jiné techniky používané ve světě (transplantace od dárce s nebijícím srdcem, duální transplantace a transplantace auxiliární) dosud provedeny nebyly.
Klíčová slova:
transplantace jater – redukce jater – SPLIT jater – domino transplantace – příbuzenská transplantaceÚvod
Transplantace jater (TxJ) je standardní léčebnou metodou pro nemocné s nezvratným selháním jater (end stage liver disease – ESLD). První úspěšnou transplantaci jater provedl Thomas E. Starzl v roce 1963 v Denveru [1]. O 20 let později – dne 7. února 1983 – provedl první transplantaci jater v bývalém Československu prof. V. Kořístek v Brně. Československo se tak stalo 5. evropskou zemí, kde byl program transplantací zahájen [2]. První nemocní zařazení na čekací listinu (waiting list – WL) k transplantaci byli pacienti s nádory, kteří pro rozsah svého onemocnění nebyli indikováni k jiným způsobům léčby. S postupným rozvojem metody a zlepšujícími se výsledky byli na WL zařazování pacienti s mnoha dalšími onemocněními, která vedla k ESLD, případně pacienti s akutním selháním jater (fulminant hepatic failure – FHF). Velmi záhy vznikl prohlubující se rozdíl mezi počtem nemocných na WL a nedostatkem jaterních štěpů vhodných k transplantaci. Zároveň se zvyšovala úmrtnost nemocných na WL nebo jejich vyřazení (tzv. drop out) pro progresi základního onemocnění (nejčastěji nádoru) v průběhu dlouhé doby čekání. Tato situace byla alarmující zejména u nejmenších dětí a příjemců hraničních váhových kategorií. To vedlo ke vzniku nových metod, které mají za cíl zvýšit počet dostupných štěpů vhodných k transplantaci, a tak umožnit většímu počtu nemocných podstoupit tento život zachraňující výkon. Přes zapojení všech různých technik, o kterých pojednává následující článek, se nepodařilo tento problém úplně vyřešit dodnes, i když mortalita na WL významně poklesla. Práce se zabývá jednotlivými metodami, které se dnes u nás a ve světě používají a slouží k zvýšení počtu jaterních štěpů vhodných k TxJ.
Redukce jater
Koncem 80. let 20. století je TxJ uznávanou léčebnou metodou s výbornými výsledky a 5leté přežívání pacientů přesahuje 70 %. Počet nemocných, kteří umírají na WL pro nedostatek dárců, se obecně snižuje, nikoli však u dětí, zejména v nejnižších váhových kategoriích (pod 10 kg). Z těchto důvodů, na základě znalostí jaterní anatomie popsané Couinaudem, přicházejí Bismuth a Houssin s novou koncepcí redukce celého štěpu pro potřeby nejmenších příjemců [3]. Technika se rychle rozšířila a byla postupně adoptována po celém světě [4 – 6]. Díky tomu úmrtnost dětí na WL rapidně poklesla z původních 15 – 50 % referovaných v různých centrech až pod 5 % na počátku 20. století [7]. V Čechách byla první transplantace redukovaným štěpem provedena v roce 1995 a od roku 2007 jsou transplantovány všechny děti i těch nejmenších váhových kategorií s výbornými výsledky [8]. Do konce roku 2012 bylo provedeno celkem 72 transplantací u pacientů mladších 18 let.
Technika redukce spočívá v rozdělení jaterního štěpu s tím, že jedna jeho část je použita k transplantaci (obr. 1). Prvním úskalím je výběr vhodného dárce (z hlediska věku, délky pobytu na jednotce intenzivní péče, nezbytné inotropní podpory a výsledků aktuální laboratoře). Rozhodující je správně zvolený poměr mezi hmotností dárce a hmotností získaného redukovaného štěpu, z hlediska hmotnosti dětského příjemce. V případě nedostatečného objemu může vzniknout tzv. „small for size“ syndrom s fatálními následky [9].
Image 1. Schéma redukce jater a redukovaný štěp jater se segmenty II + III. 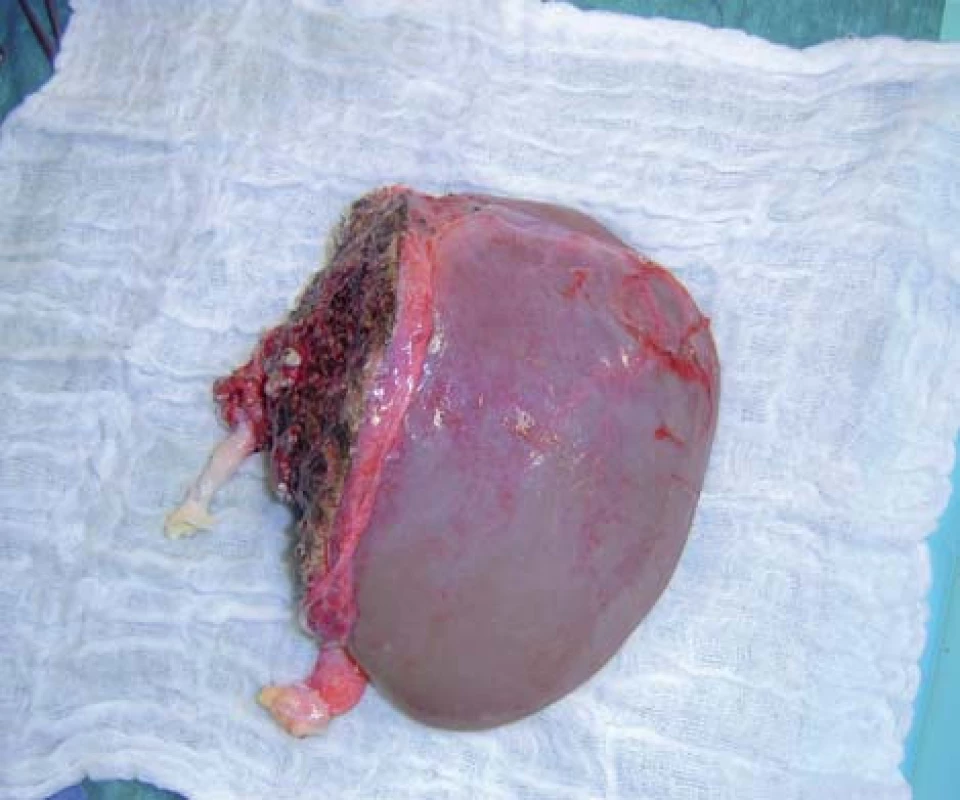
Split jater
Logickým pokračováním ve vývoji při hledání dostatečného zdroje štěpů pro transplantace byl vznik „splitování“ jaterního parenchymu. Dárcovská játra jsou rozdělena na dvě části, z nichž každá je použita k transplantaci (obr. 2). Na rozdíl od redukce z jednoho dárce profitují 2 příjemci. Obvykle je split použit pro kombinaci dospělý a dítě, nicméně možností je i transplantovat vzniklé štěpy 2 příjemcům nižších váhových kategorií. První split provedli v Německu Pichlmayr et al [10]. Rozdělení jater lze provést přímo v těle dárce tzv. „in situ split“ [11] nebo dnes častěji používanou metodou rozdělení jater ve studeném roztoku po odběru „ex situ split“ [12,13]. Podle potřeby lze získat kombinaci 2 štěpů skládajících se ze 2 + 6 jaterních segmentů nebo 2 štěpů po 4 segmentech. Tím se zvyšuje množství příjemců vhodných pro tyto štěpy. Podobně jako u redukce je důležité předem určit minimální potřebný objem jaterní tkáně. Metoda je náročná nejen na techniku, ale i logistiku provedení. V České republice je její využití zatím minimální.
Image 2. Schéma splitu jater na segmenty II–IV a segmenty V–VIII. Peroperační nález splitu in situ (v těle dárce). 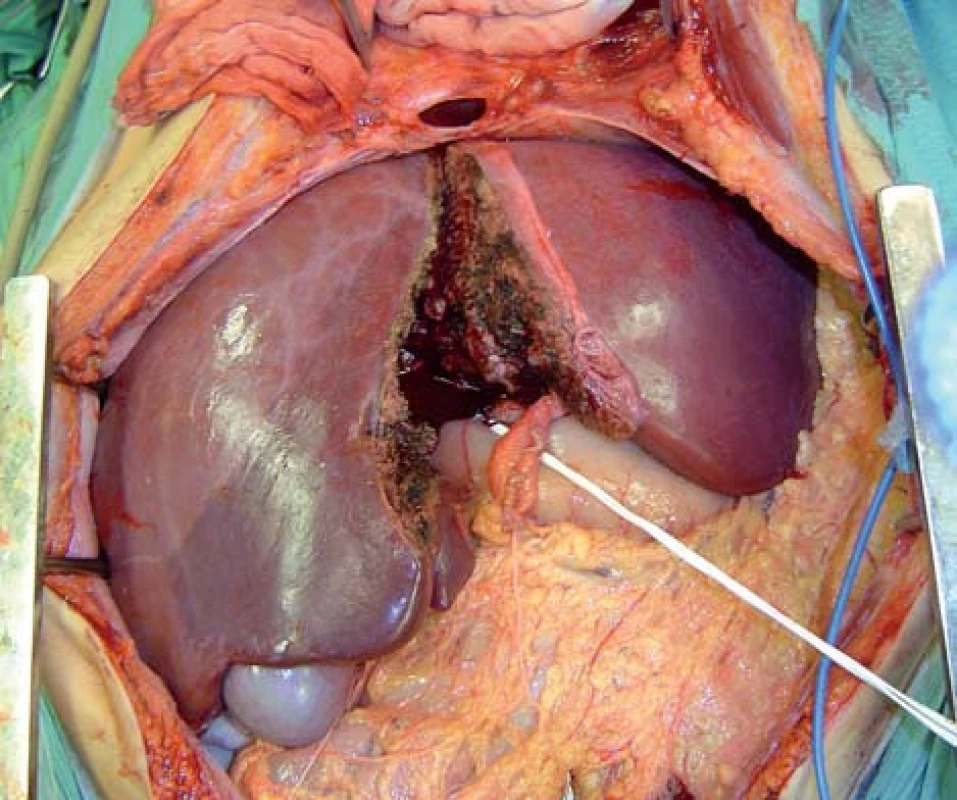
Příbuzenská transplantace jater
Redukce a split jsou techniky využívající mrtvého dárce. Odebrání části jater z živého dárce a jejich transplantace, tzv. „living donor liver transplantation“ (LDLTx), je dalším způsobem, jak rozšířit počet transplantací. Tato metoda byla prvně úspěšně provedena na konci 90. let 20. století [14]. Vzhledem k absolutnímu nedostatku kadaverózních dárců se plně rozvinula a dodnes používá převážně v asijských zemích. V Evropě a na americkém kontinentě se začala prosazovat koncem milénia, nicméně mediálně silně akcentovaná ojedinělá úmrtí dárců významně snížila její expanzi. V Čechách provedli první příbuzenskou transplantaci u dítěte Ryska et al v roce 1998. Dítě bylo následně pro komplikace retransplantováno a zemřelo na sepsi. Nespornou výhodou LDLTx je výborná kvalita štěpu, velmi krátký čas studené ischemie. Jde o zákrok, který je elektivní a lze jej naplánovat a nabídnout pacientům, kteří jsou např. v nebezpečí z časového prodlení (nádory jater a jejich progrese v době čekání, velmi malé děti apod.). Na druhou stranu je zde sice velmi malé, ale existující riziko pro dárce. Nelze zapomenout na velkou technickou náročnost výkonu pro celý tým, jak z hlediska logistiky, tak z hlediska provedení výkonu.
Duální transplantace
Výše popsané metody, které slouží k zvýšení počtu transplantovaných nemocných jsou převážně zaměřeny na skupiny dětí a pacientů nízkých váhových kategorií. Dospělí nemocní zejména v zemích s nízkým počtem kadaverózních dárců, kteří jsou odkázáni pouze na příbuzenské štěpy, zůstávají ve velkém riziku, že se transplantace nikdy nedožijí. Proto byla vyvinuta nová technika tzv. „duální transplantace”, která spočívá v tom, že se 1 příjemci našijí 2 upravené jaterní štěpy (z 2 žijících dárců, z 1 žijícího a 1 kadaverózního nebo i 2 kadaverózních dárců). Pro svoji vysokou náročnost je širší uplatnění velmi limitované. Největší zkušenosti jsou z ASAM Medical Center v Soulu, Jižní Korea [15,16].
Transplantace od dárce s nebijícím srdcem
S výjimkou Asie dominantní podíl dárců orgánů představují zemřelí pacienti. Od svého počátku byl transplantační program založen převážně na dárcích s prokázanou smrtí mozku a bijícím srdcem (donation after brain death – DBD). Přesná definice vznikla na Harvardské univerzitě koncem 70. let20. století [17]. Nicméně snaha o rozšíření spektra dárců vedla k používání orgánů z dárců po srdeční zástavě (non‑heart beating donation – NHBD nebo donation after cardiac death – DCD). Jejich přesná definice vznikla v Maastrichtu v roce 1995 [18]. V současné době jsou tyto programy plně rozvinuté zejména ve Velké Británii a Nizozemsku. Štěpy získané z DCD dárců jsou pochopitelně zatíženy vyšším počtem komplikací a v porovnání s jinými mají i horší prognózu. V České republice jsou tito dárci využíváni pouze v programu transplantací ledvin.
Domino transplantace
Játra jsou centrálním orgánem metabolizmu. Existuje skupina dědičných onemocnění, kdy jinak zdravá játra produkují patologické látky hromadící se v organizmu a po delší době působení způsobují závažné klinické příznaky. Nejtypičtějším příkladem je familiární amyloidová polyneuropatie, autozomálně dominantně dědičné metabolické onemocnění, způsobené mutací genu pro transtyretin v játrech. V jeho důsledku dochází k vzniku patologické nerozpustné bílkoviny – amyloidu, který se predilekčně ukládá v tkáních, kde způsobuje klinické příznaky onemocnění. Tato játra jsou ale funkčně jinak úplně zdravá a lze je využít jako další zdroj orgánů pro nemocné na WL s očekávanou krátkou dobou přežívání nebo vysokým rizikem z progrese (pacienti s nádory). První domino transplantace v Čechách byla provedena v roce 2006 a o 5 let později ve spolupráci se Slovenskou republikou [19].
Transplantace auxiliární
K úplnému výčtu metod používaných v transplantologii jater patří i tzv. „auxiliární transplantace“. Tato metoda spočívá v našití části jater příjemci, jehož játra jsou dočasně nefunkční nejčastěji v důsledku jaterního selhání. Použitý štěp, který by byl pro svůj malý objem v případě klasické TxJ důvodem pro „small for size syndrom“, tak poslouží k překlenutí doby nutné pro reparaci vlastních jater. Následně je odstraněn. Pacient nevyžaduje celoživotní imunosupresi. Takový štěp lze našít heterotopicky, např. do malé pánve nebo ortotopicky po částečné resekci jater nemocných [20].
Diskuze
Transplantace jater je život zachraňující léčebná metoda pro nemocné v ESLD a některé pacienty s nádory jater. Vzhledem k velmi omezenému počtu štěpů v poměru k nemocným na WL je při rozhodování o alokaci štěpu a zavádění nových metod nezbytné vzít v úvahu několik faktorů. Nejdůležitějším z nich je poměr mezi počtem úmrtí na WL a počtem nemocných vyřazených pro progresi z čekací listiny pro progresi onemocnění a výsledky transplantace z hlediska přežívání nemocných a přežívání štěpů. Tuto situaci významně ovlivňuje stav dárcovského programu, t.j. počet dárců na milion obyvatel, které je předmětem jiného sdělení. Zvláštní skupinu pacientů pak představují děti a nemocní s nízkou hmotností, jejichž doba čekání na celý kadaverózní štěp je vždy delší v porovnání s ostatními. Zejména pro tyto nemocné představuje řešení split nebo transplantace příbuzenská. Obě tyto metody přinášejí v porovnání s použitím celých kadaverózních štěpů stejné výsledky z hlediska přežívání. Odlišná je situace po zavedení programu DCD do transplantologie. Nejen, že výsledky jsou horší, ale vývoj nepotvrdil významný očekávaný nárůst dárců, nýbrž změnu poměru DBD vůči DCD [21]. Současné výsledky transplantačního programu v České republice jsou srovnatelné a v některých oblastech lepší než je evropský průměr s relativně krátkou dobou čekání a minimální úmrtností na WL.
Závěr
Od 1. transplantace jater v bývalém Československu provedené v Brně týmem prof. Kořístka uplynulo letos 30 let. Od té doby došlo k významnému rozvoji celého programu, který dnes patří mezi nejlepší v Evropě. Díky dobré organizaci a spolupráci náš kadaverózní program z větší části pokrývá potřeby čekací listiny. Díky zavedení nových chirurgických technik (redukce, split, domino transplantace), které jsou zaměřeny na zvýšení počtu dárců, je Česká republika z velké části schopna pokrýt i potřeby nejmenších příjemců a nemocných nižších váhových kategorií. S očekávaným narůstajícím počtem nemocných indikovaných k transplantaci je nezbytné rozvíjet i méně používané techniky (příbuzenské transplantace, transplantace od dárců s nebijícím srdcem), které pokryjí potřeby všech pacientů a minimalizují úmrtnost a „drop out“ na čekací listině.
Seznam použitých zkratek
TxJ transplantace jater
ESLD end stage liver disease (konečné stadium jaterního selhání)
LDT living donor (transplantace od žijícího dárce)
NHB non heart beating (dárce s nebijícím srdcem)
WL waiting list (čekací listina na transplantaci)
doc. MUDr. Martin Oliverius, Ph.D., FEBS
www.ikem.cz
e‑mail: maol@medicon.cz
Doručeno do redakce: 30. 3. 2013
Sources
1. Starzl TE, Marchioro TL, Vonkaulla KN et al. Homotransplantation of the Liver in Humans. Surg Gynecol Obstet 1963; 117 : 659 – 676.
2. Koristek V, Perestý S, Cerný J et al. Clinical transplantation of the liver. Rozhl Chir 1983; 62 : 372 – 374.
3. Bismuth H, Houssin D. Reduced ‑ sized orthotopic liver graft in hepatic transplantation in children. Surgery 1984; 95 : 367 – 370.
4. Otte JB, de Ville de Goyet J, Sokal E et al. Size reduction of the donor liver is a safe way to alleviate the shortage of size ‑ matched organs in pediatric liver transplantation. Ann Surg 1990; 211 : 146 – 157.
5. Soubrane O, Dousset B, Ozier Y et al. The choice of the reduction technique for orthotopic liver transplantation (OLT) in children using a reduced ‑ size graft. Transplant Proc 1990; 22 : 1487 – 1488.
6. Ong TH, Lynch SV, Pillay SP et al. Reduced ‑ size orthotopic liver transplantation in child-ren: an experience with seven cases. Transplant Proc 1989; 21 : 2443 – 2444.
7. de Ville de Goyet J, Hausleithner V, Reding R et al. Impact of innovative techniques on the waiting list and results in pediatric liver transplantation. Transplantation 1993; 56 : 1130 – 1136.
8. Oliverius M, Janousek L, Adamec M et al. Liver transplantations in children using reduced grafts. Rozhl Chir 2010; 89 : 411 – 416.
9. Yagi S, Uemoto S. Small‑for ‑ size syndrome in living donor liver transplantation. Hepatobiliary Pancreat Dis Int 2012; 11 : 570 – 576.
10. Pichlmayr R, Ringe B, Gubernatis G et al. Transplantation of a donor liver to 2 recipients (splitting transplantation) – a new method in the further development of segmental liver transplantation. Langenbeck’s Arch Chir 1988; 373 : 127 – 130.
11. Goss JA, Yersiz H, Shackleton CR et al. In situ splitting of the cadaveric liver for transplantation. Transplantation 1997; 64 : 871 – 877.
12. Azoulay D, Castaing D, Adam R et al. Split‑liver transplantation for two adult recipients: feasibility and long‑term outcomes. Ann Surg 2001; 233 : 565 – 574.
13. Busuttil RW, Goss JA. Split liver transplantation. Ann Surg 1999; 229 : 313 – 321.
14. Strong RW, Lynch SV, Ong TH et al. Successful liver transplantation from a living donor to her son. N Engl J Med 1990; 322 : 1505 – 1507.
15. Lee SG, Hwang S, Park KM et al. Seventeen adult ‑ to ‑ adult living donor liver transplantations using dual grafts. Transplant Proc 2001; 33 : 3461 – 3463.
16. Ahn CS, Hwang S, Moon DB et al. Right gastroepiploic artery is the first alternative inflow source for hepatic arterial reconstruction in living donor liver transplantation. Transplant Proc 2012; 44 : 451 – 453.
17. A definition of irreversible coma. Report of the Ad Hoc Committee of the Harvard Medical School to Examine the Definition of Brain Death. JAMA 1968; 205 : 337 – 340.
18. Kootstra G, Daemen JH, Oomen AP. Categories of non‑heart ‑ beating donors. Transplant Proc 1995; 27 : 2893 – 2894.
19. Oliverius M, Hampl F, Adamec M et al. First Czech and Slovak domino liver transplantation. Rozhl Chir 2011; 90 : 122 – 126.
20. Belghiti J, Sommacale D, Dondero F et al. Auxiliary liver transplantation for acute liver failure. HPB (Oxford) 2004; 6 : 83 – 87.
21. Monbaliu D, Pirenne J, Talbot D. Liver transplantation using Donation after Cardiac Death donors. J Hepatol 2012; 56 : 474 – 485.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2013 Issue 8-
All articles in this issue
- 30 let transplantace jater v Brně
- Indikace k transplantaci jater a zařazování na čekací listinu
- Výsledky transplantací jater v Brně
- Vývoj imunosupresivní léčby po transplantaci jater
- Imunosuprese po transplantaci jater, současnost a budoucnost
- Zemřelí dárci orgánů, právní normy diagnostiky smrti mozku. Přehled dárců a transplantací jater v České republice
- Chirurgické techniky v době nedostatku dárců
- Možnosti intervenční radiologie při řešení některých komplikací ortotopické transplantace jater
- Biliární (cholestatické) komplikace v biopsiích jater časně po transplantaci
- Transplantace jater u virových hepatitid
- Transplantace jater u tumorů a alkoholických cirhóz
- Kardiorenální syndrom u srdečního selhání
- Nové léky v terapii diabetes mellitus 2. typu
- Kam směřuje léčba hypertenze?
- Renální denervace 2013
- Strategie České onkologické společnosti České lékařské společnosti J. E. Purkyně při organizaci onkologické péče v ČR
- Metformin: na pomezí diabetologie a onkologie
- Kolitida vyvolaná Clostridium difficile – závažný problém současnosti
- Současné možnosti léčby nezvratného selhání ledvin
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Transplantace jater u tumorů a alkoholických cirhóz
- Imunosuprese po transplantaci jater, současnost a budoucnost
- Nové léky v terapii diabetes mellitus 2. typu
- Indikace k transplantaci jater a zařazování na čekací listinu
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career



