-
Medical journals
- Career
Současné možnosti léčby nezvratného selhání ledvin
Authors: O. Viklický; S. Rajnochová‑ bloudíčková
Authors‘ workplace: Klinika nefrologie, Transplantační centrum IKEM Praha, přednosta prof. MU Dr. Ondřej Viklický, CSc.
Published in: Vnitř Lék 2013; 59(8): 747-751
Category:
Overview
Chronické selhání ledvin představuje významný medicínský a ekonomický problém. Základem úspěchu dlouhodobé léčby nezvratného selhání ledvin je adekvátní nefrologická péče. Metodou volby léčby nezvratného selhání ledvin je transplantace ledviny od žijícího dárce a pro ty, co nemají tuto možnost pak transplantace ledviny od zemřelého dárce. V současnosti se počty transplantací ledvin od žijícího dárce zvýšily v Evropě i v USA, především kvůli velké osvětové kampani a využívání inkompatibilních dvojic. V roce 2012 bylo v České republice provedeno 361 transplantací ledvin od zemřelých dárců (34,3 pmp) a 71 transplantací ledvin od žijících dárců (6,7 pmp) a výhodu z funkční transplantované ledviny mělo celkem 4 050 nemocných. Hemodialyzační léčbu k 31. 12. 2012 podstupovalo 5 772 nemocných (550 pmp) zatímco peritoneální dialýzu 489 (47 pmp) nemocných.
Klíčová slova:
chronické onemocnění ledvin – dialýza – transplantace ledviny – peritoneální dialýza – CKD – Česká republikaChronická onemocnění ledvin
Chronické onemocnění ledvin (CKD) je definováno jako abnormality ledvinné struktury nebo funkce přítomné po více než 3 měsíce a ovlivňující zdraví (tab. 1). Tato současná definice CKD zdůrazňuje stav, kdy abnormality ve struktuře a funkci jsou klinicky významné [13]. Z klinické praxe dobře víme, že existuje mnoho situací, kdy nemocní mají omezenou renální funkci, nicméně toto omezení je nijak neohrožuje, protože není progresivní a rovněž není spojeno s dalšími abnormalitami. Většina onemocnění ledvin nemá symptomy až do pozdějších stadií a jsou detekovatelné jako chronická onemocnění. Glomerulární filtrace je všeobecně akceptována jako nejlepší marker funkce ledvin. Snížení GFR pod 60 ml/ min/ 1,73 m2 je považováno za sníženou a GFR < 15 ml/ min/ 1,73 m2 pak za renální selhání. Je dobře známo, že se s věkem GFR snižuje a že jeho normální hodnota u devadesátníků je poloviční než u čtyřicátníků. Při poklesu GFR pod 60 ml/ min/ 1,73 m2 se riziko komplikací významně zvyšuje. Mezi tyto komplikace patří především toxicita léků vyplývající z jejich odlišné farmakokinetiky a farmakodynamiky, metabolické a endokrinní komplikace a zvýšené riziko kardiovaskulárních komplikací.
Table 1. Kritéria pro diagnózu chronického onemocnění ledvin. 
Hlavní příčinou chronických renálních onemocnění je ischemická nefropatie a diabetická nefropatie. Chronické glomerulonefritidy a vrozená onemocnění představují další významné příčiny progresivních nefropatií.
Progrese chronických onemocnění ledvin
Existuje velká variabilita rizika progrese CKD. Samotné jedno kontrolní vyšetření eGFR nemusí znamenat progresi, protože běžně dochází ke kolísání glomerulární filtrace. Jako rychlá progrese CKD se označuje stav, kdy eGFR klesne o více než 5 ml/ min/ 1,73 m2 za rok (0,08 ml/ s). U všech nemocných s progresí by měl být pečlivě zhodnocen stávající postup, měli by být častěji sledováni a rovněž by měli být nadále sledováni nefrology, pokud se tak již nestalo. Mezi známé rizikové faktory progrese patří příčina CKD, hodnota GFR, albuminurie, věk, pohlaví, rasa, hypertenze, hyperglykemie, dyslipidemie, kouření, obezita, anamnéza kardiovaskulárních onemocnění, expozice nefrotoxickými léky (tab. 2) [13].
Table 2. Rizikové faktory progrese CKD. 
Sledování nemocných
Významným faktorem umožňující zpomalit progresi CKD a zabezpečit optimální léčebnou strategii je správné a včasné předání nemocného nefrologovi [11,12]. Pokud víme, že 40 % nemocných přichází do dialyzační léčby tzv. z ulice, je možno soudit, že v této oblasti stále existují v naší zemi závažné nedostatky v předávání nemocných do nefrologické péče včas. Rolí nefrologů je správně edukovat své kolegy v regionu o významu včasného předání nemocných do péče. V některých zemích existují tzv. „low clearance clinic“, ve kterých je multioborovým týmem věnována náležitá péče nemocným v pokročilých stadiích CKD. Někdy se tato pracoviště označují jako predialysis nebo pretransplant clinic, podle toho, kdo má v organizaci programu hlavní slovo [3]. V principu je ale péče stejná. U nás zatím reálně tato pracoviště nemáme a naší hlavní snahou by vedle snahy o jejich rychlé zavedení mělo být zajištění snadného převedení nemocných do péče nefrologů. U nemocných musí být zahájeno sledování v nefrologické ambulanci v těchto případech:
- AKI nebo rychlý pokles GFR.
- GFR < 30 ml/ min/ 1,73 m2 (kategorie GFR G4 – G5).
- Přetrvávající nález signifikantní albuminurie [ACR > 300 mg/ g (> 30 mg/ mmol), albuminurie > 300 mg/ den nebo proteinurie 0,5 g/ den].
- Progresivní forma CKD.
- Jinak nevysvětlitelná erytrocyturie.
- Hypertenze u nemocného s CKD vyžadující 4 a více preparátů.
- Rekurující nebo velká nefrolitiáza.
- Hereditární onemocnění ledvin.
Nemocný musí být rovněž předán nefrologovi dostatečně včas před zahájením léčby náhrady funkce ledvin. Jakkoliv je pojem včas vágní, je jasné, že to není méně než 1 rok před zahájením příslušné léčby. Během roku je dostatečný čas na správnou edukaci, vyhledání žijícího dárce a jeho vyšetření, rozhodnutí o volbě metody v případě, kdy preemptivní transplantace není možná, dietní intervenci, úpravu medikace atd.
Nemocní starší 75 let, polymorbidní nemocní a dále ti s nižším vzděláním a socioekonomickým stavem jsou často předáváni nefrologům pozdě. Tato skupina nemocných má pochopitelně daleko větší výskyt komplikací vyplývající z CKD a jejich léčba je následně také nejvíce nákladná. Studie ukazují, že zhruba 1/ 3 všech nemocných s CKD je předávána do péče nefrologů pozdě. Včasné předání do péče znamená již i v naší zemi většinou preemptivní transplantaci ledviny anebo ambulantní zahájení léčby nezvratného selhání ledvin příslušnou dialyzační metodou, případně kratší úvodní hospitalizaci.
Péče o nemocného s progresivní formou CKD, volba metody další léčby
Důležitým předpokladem úspěšné léčby nemocného s progresivní formou CKD je týmová práce. Není možné si představit, že jeden jediný lékař je schopen dobře postihnout celou problematiku. Zapojení sester, event. koordinátorek do edukace nemocných se v poslední době ukazuje jako zcela nezbytný krok. Pacient s progredující CKD vyžaduje mnohem více času v ambulanci a rovněž častější sledování, než může kapacita ambulance dovolit. Proto je třeba zvolit jiný přístup. Nemocný má mít možnost seznámit se s tištěnými materiály, webovými stránkami obsahujícími informace, které hledá. Kromě nefrologa a nefrologické sestry se v této době na péči podílí i dietolog/ dietní sestra, se kterou má pacient mít možnost konzultovat své stravovací návyky a která mu pomůže upravit jídelníček tak, aby snížil příjem bílkovin na požadovaných 0,8 g/ kg/ den.
Hlavní náplní práce edukační sestry by mělo být vyvážené poučení o možnostech léčby nezvratného selhání ledvin. V prvé řadě je nutné ověřit, zdali je pacient vhodným kandidátem transplantace ledviny, a pokud ano, mělo by být prvním úkolem diskutovat o výhodách transplantací od žijícího dárce. Pokud ano, je třeba zahájit jeho vyšetřování. To se provede buď v režii ošetřujícího nefrologa, nebo nefrologa z transplantačního centra. V současnosti existují v transplantačních centrech určení profesionálové, kteří se transplantacemi od žijících dárců zabývají a je vhodné v určité chvíli vyšetřování konzultovat stav příprav, resp. předat nemocného do péče transplantačního centra před vlastní transplantací. Cílem by měla být preemptivní transplantace ledviny, protože ta poskytuje nejlepší výsledky, a pro ni je vhodné předání do péče transplantačního centra v době, kdy do zahájení léčby nezvratného selhání ledvin zbývá nejméně 6 měsíců (obr. 1).
Image 1. Načasování edukace a léčby náhrady funkce ledvin. 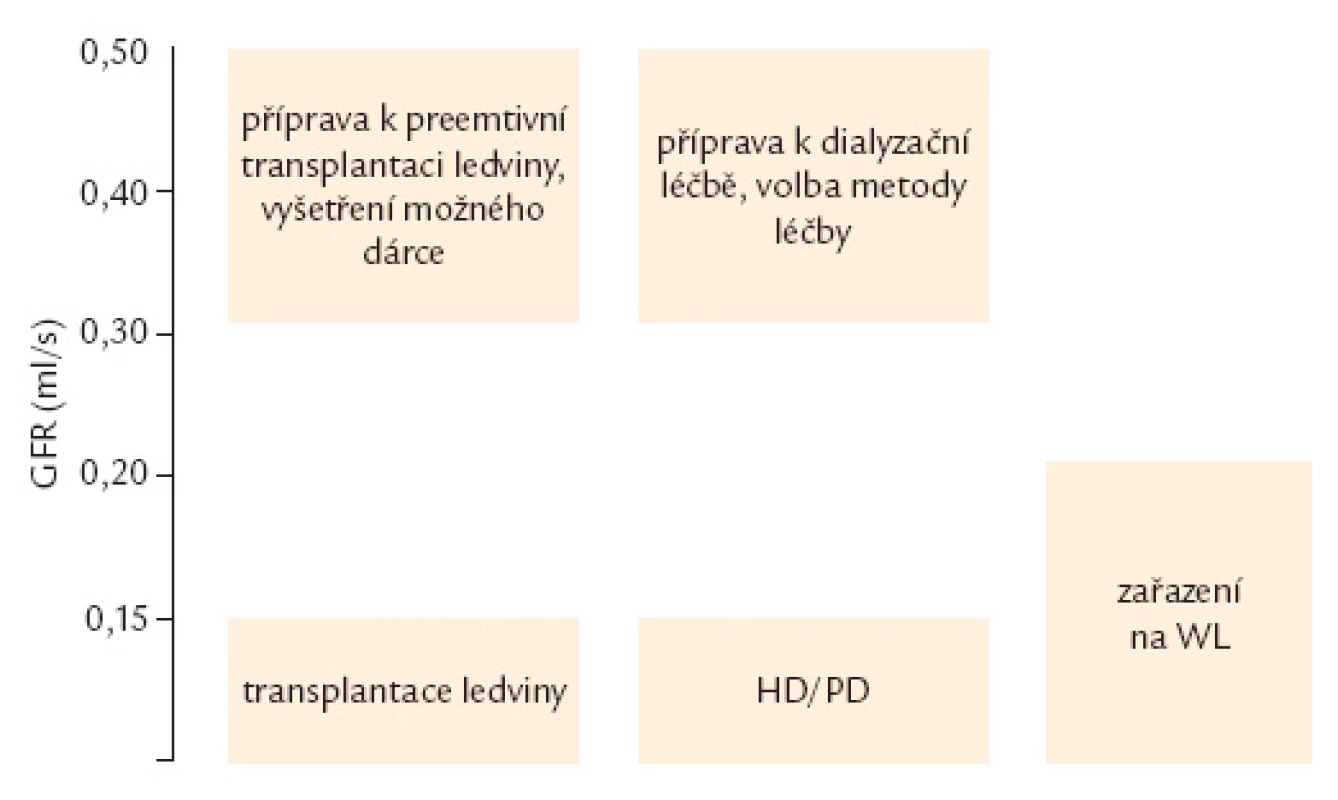
Pokud nebyl dárce nalezen a pokud je nemocný vhodným kandidátem transplantace, je třeba nemocného vyšetřit tak, aby bylo možné jej zařadit do čekací listiny těsně před tím, než bude zahájena léčba nezvratného selhání ledvin. Je ovšem také nutné diskutovat zvolenou metodu, kterou bude nemocný léčen do doby, než bude provedena transplantace od zemřelého dárce. V případech, kdy je na nemocného nahlíženo jako na vhodného kandidáta transplantace, se jedná o soběstačného pacienta, který by mohl profitovat z metod peritoneální dialýzy. Na tu lze v těchto případech nahlížet jako na most k transplantaci. Pokud si pacient vybere tuto možnost, není třeba zakládat cévní spojku.
V případech, kdy nemocný není vhodným kandidátem transplantace ledviny (t.j. existují kontraindikace transplantace – viz kapitola o transplantaci ledviny), je nutné poskytnout vyvážené informace o metodách hemodialýzy a peritoneální dialýzy. Pokud si zvolí jednu nebo druhou možnost, je vždy zásadní, aby s nimi hovořili odborníci, kteří zvládají obě metody a aby bylo vyloučeno zaujetí nebo nátlak. V principu většina nemocných může být léčena oběma metodami. To, že u nás je léčeno metodami peritoneální dialýzy pouze 8 % nemocných, není nadále akceptovatelné [14].
Pokud bude nemocný léčen hemodialýzou, je nutné zajistit včasné vyšetření u cévního chirurga, který by měl zhotovit cévní spojku k dialýze v dostatečném předstihu. Odhadnout tuto dobu nebývá snadné a často se stává, že je cévní spojka zhotovena léta před vlastním zahájením dialyzační léčby.
Kromě poučení o metodě léčby nezvratného selhání ledvin je rovněž nezbytné mít vytvořené protokoly na léčbu nemocných v tzv. predialýze. Tyto protokoly by měly obsahovat seznamy nutných vyšetření, konzilií, očkovací kalendář (pokud nebylo očkování provedeno – viz výše), léčbu anémie, léčby poruch metabolizmu kalcia a fosforu, seznamy diet apod. Často se také zapomíná, že nemocní s progredujícím CKD mají deprese a ty by měly být adekvátně léčeny. Péče o děti s progredující CKD je mnohem složitější a kromě zapojení rodiny je péče psychologa nezbytná.
Transplantace ledviny od žijícího dárce
Jak bylo již řečeno, tento typ transplantace ledviny je spojen s nesporně lepšími výsledky v porovnání s transplantací ledviny od zemřelého dárce. Proto je transplantace ledviny od žijícího dárce nejvýhodnější metodou volby léčby nemocných s ESRD. Klíčovým faktorem je možnost preemptivního provedení, které je spojeno s lepšími dlouhodobými výsledky (až 2krát delší přežívání ledvinného štěpu ve srovnání s transplantací od zemřelého dárce). V případě preemptivní transplantace je příjemce obvykle v dobrém klinickém stavu, bez uremických symptomů a není vystaven riziku vzniku komplikací doprovázejících dialyzační léčbu. Zároveň odpadá i nutnost založení dialyzačního přístupu.
Díky zlepšující se spolupráci ošetřujících nefrologů a transplantologů (za přispění kampaně „Láska prochází ledvinou“ či díky loňskému Světovému dni ledvin věnovanému programu transplantací od žijících dárců) se významně zvýšila informovanost pacientů. Zásadní úlohou ošetřujícího nefrologa je včasné a srozumitelné seznámení každého nemocného s chronickým renálním selháním (včetně jeho blízkých) o možnosti transplantace ledviny od žijícího dárce, včetně jejích rizik a výhod. V případě souhlasu nemocného s transplantací ledviny od žijícího dárce, po provedení základních standardních vyšetření, je nejvhodnější potencionální dvojici odeslat co nejrychleji do transplantačního centra [4]. Transplantace od žijícího dárce by neměla být automaticky kontraindikována v případě inkompatibility krevních skupin či z důvodu „věku“ potenciálního dárce. V případě, kdy příjemce má inkompatibilního dárce (kvůli neshodě v krevní skupině anebo při přítomnosti HLA protilátek), existují tyto možnosti [7–9]:
AB0 inkompatibilní transplantace ledviny od žijícího dárce
Překonání bariéry hemaglutininů umožňuje specifická příprava příjemce ledviny [5,6], kterou v našem centru zahajujeme měsíc před vlastním operačním výkonem. Tento režim zahrnuje užívání imunosupresivních léků a imunoadsorpčních procedur, jejichž cílem je odstranění hemaglutininů a blokáda funkce hemaglutininů v plazmě příjemce. AB0 inkompatibilní transplantaci ledviny lze provést u příjemce podstupujícího svou první transplantaci ledviny, při příznivém titru protilátek příjemce proti hemaglutininům krevní skupiny dárce (≤ 1 : 128) a současné negativitě křížové zkoušky mezi dárcem a příjemcem. Dosud bylo v IKEM provedeno 6 těchto transplantací, první v lednu roku 2011. Přežívání AB0 inkompatibilních ledvinných štěpů je obdobné v porovnání se štěpy od kadaverózních dárců, a to bez ohledu na typ krevní skupiny.
Párová výměna
Pro inkompatibilní dvojice je nutno vytvořit jejich registr. Mezi registrovanými dvojicemi pak v pravidelných intervalech (à 3 měsíce) provádíme imunologické zkoušky ve snaze uskutečnit maximální počet transplantací z evidovaných párů. Bez počítačového programu není možné sestavit větší počet párů. V případě, že se takovéto transplantace účastní 2 páry, mluvíme o párové výměně či zkřížené transplantaci ledviny (v IKEM poprvé provedena v roce 2001). V listopadu roku 2012 byla v IKEM provedena první řetězová transplantace ledviny (obr. 2), při které si vyměnilo ledviny celkem 6 párů, druhá řetězová transplantace byla provedena v IKEM v únoru roku 2013 a tehdy si vyměnilo ledviny celkem 5 párů. V obou případech byl řetěz iniciován altruistickým dárcem a poslední dárce věnoval svou ledvinu příjemci z čekací listiny.
Image 2. Schéma řetězové transplantace. 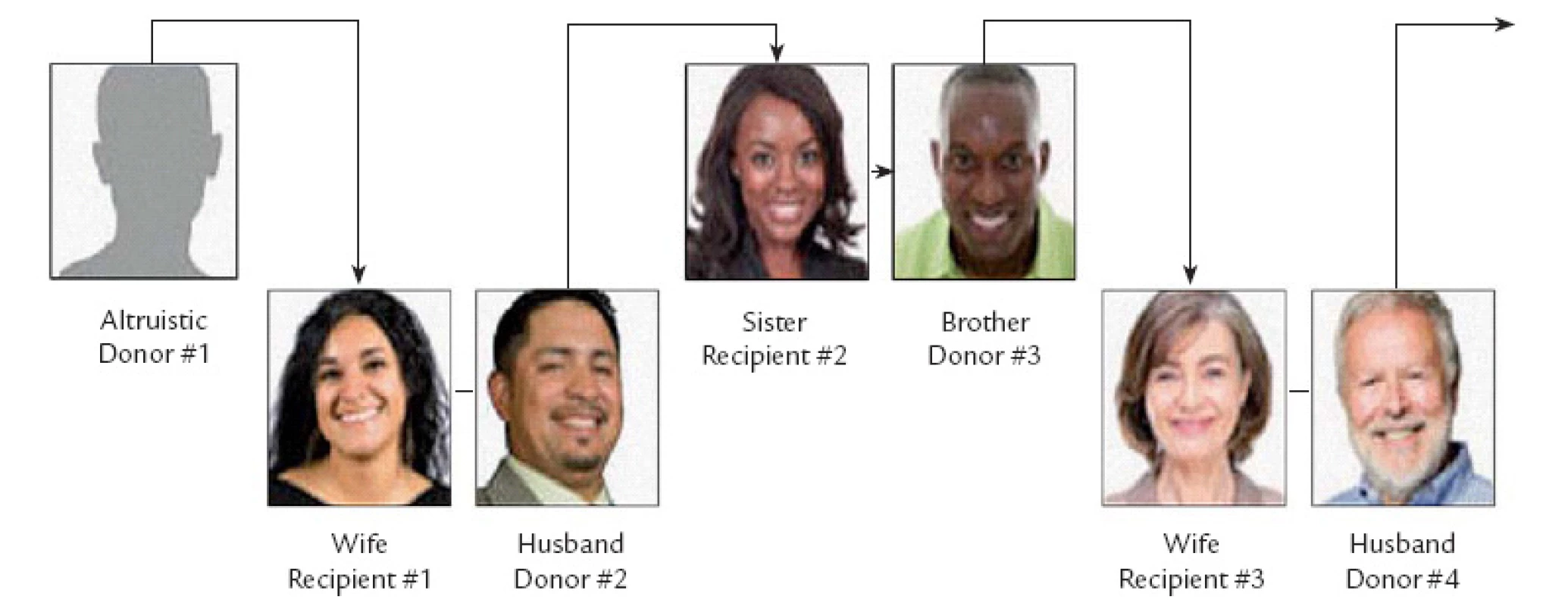
Transplantace ledviny od zemřelého dárce
Pokud není možnost provést transplantaci od žijícího dárce, je možno nemocného zařadit do čekací listiny k transplantaci ledviny. Zařazení do čekací listiny se řídí základním vyšetřovacím schématem s cílem minimalizovat rizika závažných peritransplantačních a potransplantačních (zejména kardiovaskulárních) komplikací. I zde využíváme maximální součinnosti s ošetřujícími nefrology (obvykle lékaři dialyzačních středisek), kteří pacienta s podrobnou lékařskou zprávou obsahující anamnézu, laboratorní nálezy a vyšetření referují transplantačnímu centru. Každý z těchto pacientů je následně vyšetřen v „předtransplantační ambulanci“, na jejímž základě je pacient zařazen či nezařazen do čekací listiny k transplantaci ledviny od zemřelého dárce. Doporučený algoritmus při zařazování nemocných do čekací listiny k transplantaci ledvin vychází z publikovaných doporučení ERA/ EDTA a Americké transplantační společnosti [10]. U řady komorbidit je nezbytné postupovat individuálně, neboť názory na jejich řešení nejsou jednotné a neustále se vyvíjejí. Principiálně by měl být do čekací listiny zařazen každý pacient (bez ohledu na kalendářní věk), který nesplňuje absolutní kontraindikaci. Pacient bez absolutní kontraindikace by měl být co nejdříve referován a vyšetřen v předtransplantační ambulanci. Cílem je zařadit nemocného do čekací listiny k transplantaci ledviny preemptivně, neboť je známo, že doba strávená na dialýze je nezávislým negativně prognostickým faktorem mortality nemocných i přežívání ledvinného štěpu [1,2]. Pacienta s nezvratným selháním ledvin lze zařadit do čekací listiny při poklesu glomerulární filtrace pod 0,17 ml/ s či při předpokládaném zahájení pravidelné dialyzační léčby během 3 měsíců. Ačkoli čekací doba na transplantaci ledviny od zemřelého dárce je v České republice v porovnání s ostatními zeměmi velmi krátká (průměrně 1 rok), je nezbytné pacienty i po zařazení do čekací listiny pravidelně sledovat a vyšetřovat, neboť se jejich stav vyvíjí a mění.
Rozvoj transplantační léčby v posledních 20 letech vedl k podstatnému zvýšení počtu nemocných žijících s funkční transplantovanou ledvinou, v ČR jich žije 4 000 a každým rokem přibývají další. Transplantace ledviny se provádí v IKEM Praha, v Plzni, Hradci Králové, Brně, Olomouci a Ostravě, dětští příjemci jsou léčeni v Praze ‑ Motole. Průměrné přežití transplantovaných ledvin od zemřelého dárce je 9 let, v případě transplantace od žijícího dárce je to až 2krát déle.
Dialyzační léčba
Pravidelná dialyzační péče je v ekonomicky rozvinutých zemích dostupná všem pacientům. V porovnání s transplantací ledviny, léčebný efekt dialyzačních metod je limitován parciální a intermitentní eliminací toxických látek, neboť neobnoví komplexní renální funkci (exkreční, metabolickou, regulační, endokrinní). Jednoznačná kritéria k zahájení dialyzační léčby nelze stanovit, vždy je nezbytné přístup ke každému pacientu s ESRD individualizovat. Bylo prokázáno, že pacienti, kteří nebyli sledováni u nefrologů před zahájením dialyzační léčby (tzv. „z ulice“), mají horší dlouhodobou prognózu. Na druhou stranu nebyla prokázána žádná výhoda z příliš časného zahájení dialyzační léčby. Je tudíž zřejmé, že úroveň reziduální GFR je jen pomocným kritériem k zahájení PDL. Obecně je přijímáno, že při poklesu GFR pod 0,1 ml/ s/ 1,73 m2 by již měla být zahájena dialyzační léčba bez ohledu na nepřítomnost uremických projevů.
Hemodialyzační metody
Hemodialýza využívá principu difuze nahromaděných dusíkatých katabolitů přes semipermeabilní membránu a v případě hemodiafiltrace se tento princip kombinuje s konvekcí. Hlavní podmínkou hemodialyzačních metod je zabezpečení kvalitního cévního přístupu umožňujícího vysoké průtoky krve, který je nezbytný k dosažení požadované dialyzační dávky. Optimální cévní přístup zajistí přívod krve o objemu 200 – 500 ml/ min do dialyzátoru, t.j. 50 – 150 l krve během standardní dialyzační procedury trvající 4 – 5 hod. Účinnost dialyzační procedury je závislá na propustnosti dialyzační membrány („low ‑ flux“ a „high‑flux“), ploše dialyzátoru, délce (času), který je rozhodující pro odstranění látek s větší molekulovou hmotností a nadbytečné vody, a kvalitě cévního přístupu. K tomu je nutné prováděn hemodialyzační metody 3krát týdně po dobu minimálně 4 hod, v řadě případů je nutné léčbu prodloužit. Pacient v chronické dialyzační léčbě může žít kvalitně i mnoho let, obvykle se však i přes adekvátní dialyzační péči vyvíjejí komplikace (akutní i chronické) a jeho očekávaná délka života je ve srovnání se zdravou populací významně zkrácena. Průměrná mortalita v dialyzační léčbě kolísá v ČR kolem 18 %, což předpokládá přežití kolem 5 let [14]. Nejčastějšími komplikacemi, které zároveň bývají i nejčastějšími příčinami úmrtí, jsou komplikace kardiovaskulární (50 %), infekční (20 %) a onkologické. Nefrologicko‑dialyzační péče proto musí být komplexní, tzn. zahrnovat kromě jednotlivých dialyzačních procedur i pravidelné klinické a laboratorní sledování nemocného, včetně onkologického screeningu. K 31. 12. 2012 bylo v ČR léčeno 5 772 nemocných léčených hemodialyzačními metodami [14].
Peritoneální dialýza
Peritoneální dialýza využívá dialyzační schopnosti peritonea. Její podmínkou je bezproblémové založení speciálního katetru do dutiny břišní. Po zahojení rány (obvykle 3 týdny) je možno zahájit léčbu. Nemocný si provádí buď výměny peritoneálního roztoku (2 000 ml) většinou 4krát denně a v noci vynechá, anebo používá přístroj, který provádí výměny automatizovaně sám přes noc a přes den se výměny neprovádějí. Hlavními výhodami této metody jsou hemodynamická stabilita, vyrovnaný stav vnitřního prostředí, méně vyjádřená renální anémie a delší udržení reziduální diurézy vlastních ledvin. Neopomenutelnou výhodou je samostatnost nemocného, neboť si dialyzační procedury provádí sám v domácím prostředí a do dialyzačního střediska dochází na kontroly pouze jednou za 4 – 6 týdnů. Hlavním rizikem je peritonitida. Pokud se peritonitidy opakují, bývá nutné u nemocného někdy změnit metodu za hemodialýzu. Metodami peritoneální dialýzy se k 31. 12. 2012 léčilo v ČR 489 nemocných [14], což je vzhledem k využití této metody v ostatních státech podstatně méně.
prof. MU Dr. Ondřej Viklický, CSc.
www.ikem.cz
e‑mail: onvi@medicon.cz
Doručeno do redakce: 6. 4. 2013
Sources
1. Meier ‑ Kriesche HU, Schold JD. The impact of pretransplant dialysis on outcomes in renal transplantation. Semin Dial 2005; 18 : 499 – 504.
2. Meier ‑ Kriesche HU, Port FK, Ojo AO et al. Effect of waiting time on renal transplant outcome. Kidney Int 2000; 58 : 1311 – 1317.
3. Gill JS, Rose C, Pereira BJ et al. The importance of transitions between dialysis and transplantation in the care of end‑stage renal disease patients. Kidney Int 2007; 71 : 442 – 447.
4. Delmonico F. A report of the Amsterdam forum on the care of the live kidney donor: data and medical guidelines. Transplantation 2005; 79 (Suppl 6): S53 – S66.
5. Genberg H, Kumlien G, Wennberg L et al. Isoagglutinin adsorption in ABO ‑ incompatible transplantation. Transfus Apher Sci 2010; 43 : 231 – 235.
6. Segev DL, Simpkins CE, Warren DS et al. AB0 incompatible high‑titer renal transplantation with-out splenectomy or anti‑CD20 treatment. Am J Transplant 2005; 5 : 2570 – 2575.
7. Montgomery RA. Renal transplantation across HLA and AB0 antibody barriers: integrating paired donation into desensitization protocols. Am J Transplant 2010; 10 : 449 – 457.
8. Wadström J. Hand ‑ assisted retroperitoneoscopic live donor nephrectomy: experience from first 75 consecutive cases. Transplantation 2005; 80 : 1060 – 1066.
9. Foley RN, Ibrahim HN. Long‑term outcome of kidney donors. Curr Opin Nephrol Hypertens 2010; 19 : 129 – 133.
10. Danovitch GM, Hariharan S, Pirsch JD et al. Clinical Practice Guidelines Committee of the American Society of Transplantation. Management of the waiting list for cadaveric kidney transplants: report of a survey and recommendations by the Clinical Practice Guidelines Committee of the American Society of Transplantation. J Am Soc Nephrol 2002; 13 : 528 – 535.
11. Wauters JP, Lameire N, Davison A et al. Why patients with progressing kidney disease are referred late to the nephrologist: on causes and proposals for improvement. Nephrol Dial Transplant 2005; 20 : 490 – 496.
12. Chow KM, Szeto CC, Law MC et al. Impact of early nephrology referral on mortality and hospitalization in peritoneal dialysis patients. Perit Dial Int 2008; 28 : 371 – 376.
13. KDIGO 2013. Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease. Kidney Int Supplement 2013; 3 : 19 – 62.
14. Česká nefrologická společnost. Dostupné na: www.nefrol.cz.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2013 Issue 8-
All articles in this issue
- 30 let transplantace jater v Brně
- Indikace k transplantaci jater a zařazování na čekací listinu
- Výsledky transplantací jater v Brně
- Vývoj imunosupresivní léčby po transplantaci jater
- Imunosuprese po transplantaci jater, současnost a budoucnost
- Zemřelí dárci orgánů, právní normy diagnostiky smrti mozku. Přehled dárců a transplantací jater v České republice
- Chirurgické techniky v době nedostatku dárců
- Možnosti intervenční radiologie při řešení některých komplikací ortotopické transplantace jater
- Biliární (cholestatické) komplikace v biopsiích jater časně po transplantaci
- Transplantace jater u virových hepatitid
- Transplantace jater u tumorů a alkoholických cirhóz
- Kardiorenální syndrom u srdečního selhání
- Nové léky v terapii diabetes mellitus 2. typu
- Kam směřuje léčba hypertenze?
- Renální denervace 2013
- Strategie České onkologické společnosti České lékařské společnosti J. E. Purkyně při organizaci onkologické péče v ČR
- Metformin: na pomezí diabetologie a onkologie
- Kolitida vyvolaná Clostridium difficile – závažný problém současnosti
- Současné možnosti léčby nezvratného selhání ledvin
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Transplantace jater u tumorů a alkoholických cirhóz
- Imunosuprese po transplantaci jater, současnost a budoucnost
- Nové léky v terapii diabetes mellitus 2. typu
- Indikace k transplantaci jater a zařazování na čekací listinu
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

