-
Medical journals
- Career
Význam hodnotenia EKG v diagnostike pľúcnej embólie
: S. Daruľová; M. Stančík; P. Galajda; M. Belicová; M. Mokáň
: I. interná klinika Jesseniovej lekárskej fakulty UK a UN Martin, Slovenská republika, prednosta prof. MU Dr. Marián Mokáň, DrSc., FRCP Edin.
: Vnitř Lék 2013; 59(11): 1017-1021
: Case Report
Akútna pľúcna embólia patrí v súčasnosti medzi jedno z najčastejších a najrizikovejších kardiovaskulárnych ochorení. Napriek dostupnosti rozmanitých vyšetrovacích metód a bohatým klinickým skúsenostiam ide o ochorenie náročné na diagnostiku. Dôvodom je aj nie vždy typický klinický obraz, pod ktorým môže pľúcna embólia prebiehať a zvádzať k výberu nesprávnych diagnostických metód, ktoré stanovenie ochorenia oddialia. Dôsledné vyhodnotenie každého symptómu a bazálnych, resp. doplnkových vyšetrení je preto dôležitým krokom k promptnému a správnemu stanoveniu tejto diagnózy.
Kľúčové slová:
akútna pľúcna embólia – EKG krivkaÚvod
Pľúcna embólia je po artériovej hypertenzii a ischemickej chorobe srdca 3. najčastejším kardiovaskulárnym ochorením. Je významnou príčinou morbidity a mortality celosvetovej populácie a tiež jednou z najčastejších akútnych kardiovaskulárnych príhod vo všetkých vekových skupinách. Jej výskyt vo svete nie je presne známy. Podľa údajov Európskej kardiologickej spoločnosti z roku 2000 je jej incidencia v európskej populácii 6,0/ 1 000 obyvateľov ročne [1]. Novšie údaje sú predovšetkým lokálne. V Európe, štúdie v západnom Francúzku a Švédsku (EPI ‑ GETBO study, Study of Malmö), uvádzajú incidenciu tohto ochorenia 160 – 180/ 100 000 obyvateľov ročne [2]. Vo Veľkej Británii je jej výskyt o niečo vyšší, a to 18,3/ 10 000 obyvateľov. Podľa údajov z roku 2004 je incidencia pľúcnej embólie v Európe 95/ 100 000 obyvateľov za rok, pričom úmrtnosť predstavuje až 34 % [2].
Pľúcna embólia je ochorenie, ktoré nemá vždy jednoznačný klinický obraz, preto napriek širokým diagnostickým možnostiam predstavuje aj v súčasnosti závažný medicínsky problém. Je známe, že aj dnes sa pľúcna embólia klinicky spozná len u 30 % pacientov [1]. Ide teda o ťažkú diagnózu, pri ktorej často dochádza k jej oneskorenému stanoveniu, na čo chceme upozorniť práve touto kazuistikou.
Opis prípadu
Pacientka vo veku 51 rokov, nefajčiarka, po cholecystektómii v roku 2006, liečená na hypotyreózu, bola vyšetrená internistom na urgentnom príjme v šokovom stave.
Dva týždne pred vyšetrením na oddelení pohotovostného príjmu začínajú u pacientky ťažkosti s dýchaním sprevádzané kašľom, ktoré sú ambulantne zhodnotené ako infekt horných dýchacích ciest a ďalej riešené nasadením antibiotickej liečby (ciprofloxacín). Dva dni pred vyšetrením sa u pacientky objavujú hnačky a vracanie a o 48 hod dochádza k vzniku dušnosti a bolestí na hrudníku a v epigastriu. Následne pacientka synkopuje.
Rýchlou zdravotníckou pomocou je privezená na oddelenie pohotovostného príjmu už v šokovom stave – cyanotická, s krvným tlakom 90/ 50 mm Hg, tachykardiou 120/ min a tachypnoe. Pri fyzikálnom vyšetrení dominuje nález na bruchu s palpačnou bolestivosťou epigastria s propagáciou do sakrálnej oblasti, pohmatom zisťujeme i hepatomegáliu. Okrem uvedeného nálezu je abdomen bez príznakov peritoneálneho dráždenia.
Laboratórne zisťujeme normocytovú normochrómnu anémiu ľahkého stupňa (hemoglobín 116 g/ l), eleváciu zápalových parametrov s leukocytózou (C ‑ reaktívny proteín 21 mg/ l, leukocyty 11,4 × 109/ l), stresovú hyperglykémiu (sérová koncentrácia glukózy 23,9 mmol/ l), hepatopatiu (aspartátaminotransferáza 8,16 µkat/ l, alanínaminotransferáza 8,13 µkat/ l, gamaglutamyltransferáza 4,27 µkat/ l). Prítomná je aj porucha acidobázickej rovnováhy v zmysle parciálnej respiračnej insuficiencie a metabolickej acidózy (parciálny tlak kyslíka v kapilárnej krvi 2,8 kPa, pH krvi 7,118, hydrogénuhličitany 11,3 mmol/ l, deficit báz 17,2). Vyšetrenie základnej koagulácie je v norme, D ‑ diméry vzhľadom k šokovému stavu vstupne neboli vyšetrené.
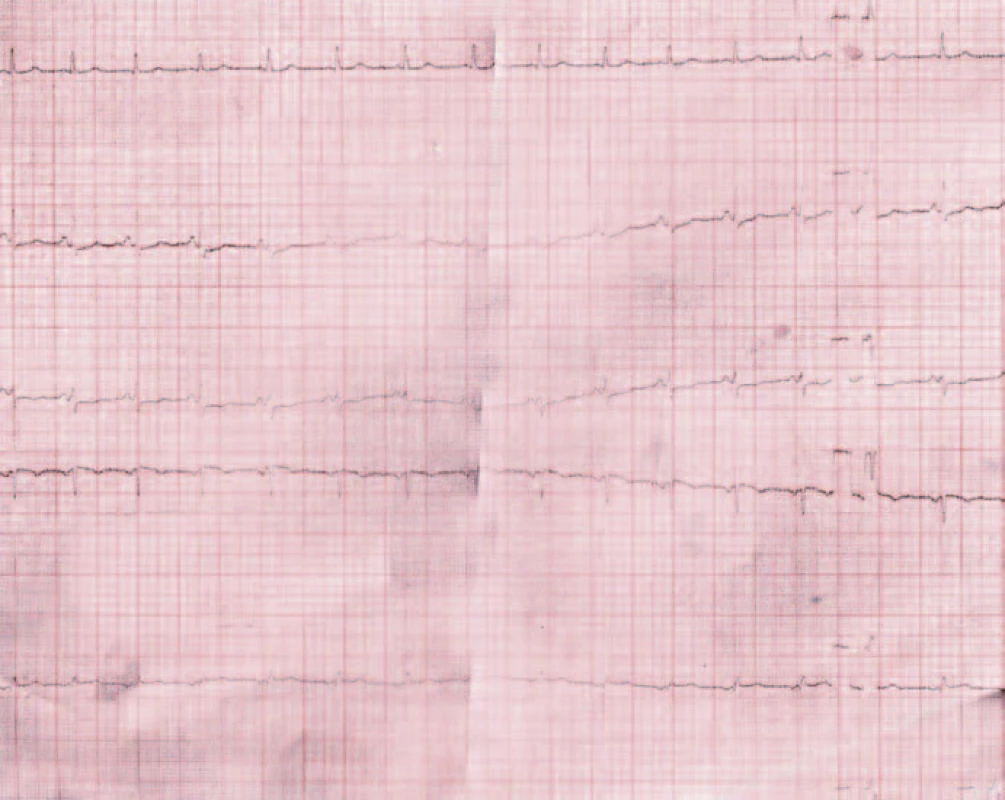
Z pomocných vyšetrení vstupne realizujeme aj klasické 12-zvodové EKG, na ktorom v porovnaní so starším EKG záznamom z dokumentácie verifikujeme nové zmeny (obr. 1, 2).
2. EKG záznam pri urgentnom vyšetrení v porovnaní so záznamom z dokumentácie – sínusová tachykardia, kmit S v I, Q v III, inkompletný blok pravého Tawarovho ramienka. 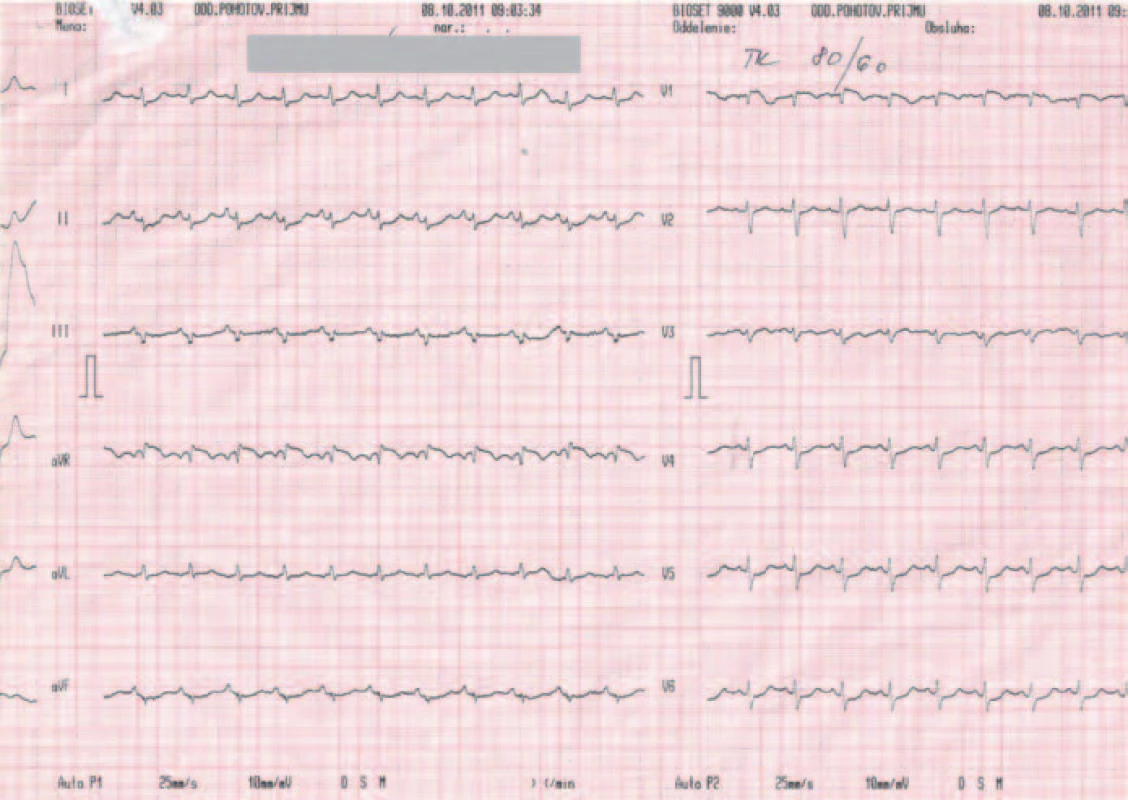
Klinický obraz však pre dominujúci nález na bruchu a anamnézu vracania a hnačiek imponuje ako náhla brušná príhoda v zmysle akútnej pankreatitídy alebo viscerálnej ischémie. Indikované je preto CT vyšetrenie abdomenu, ktoré je v zmysle predpokladaného nálezu negatívne, avšak je jednoznačne viditeľná hepatomegália a dilatácia hepatálnych vén – príznak akútneho pravostranného srdcového zlyhania pri pľúcnej embólii [1,3]. Okamžite dopĺňame CT ‑ pulmoangiografické vyšetrenie s potvrdením embolizácie do oboch vetiev a. pulmonalis (obr. 3).
3. CT-pulmoangiografické vyšetrenie. 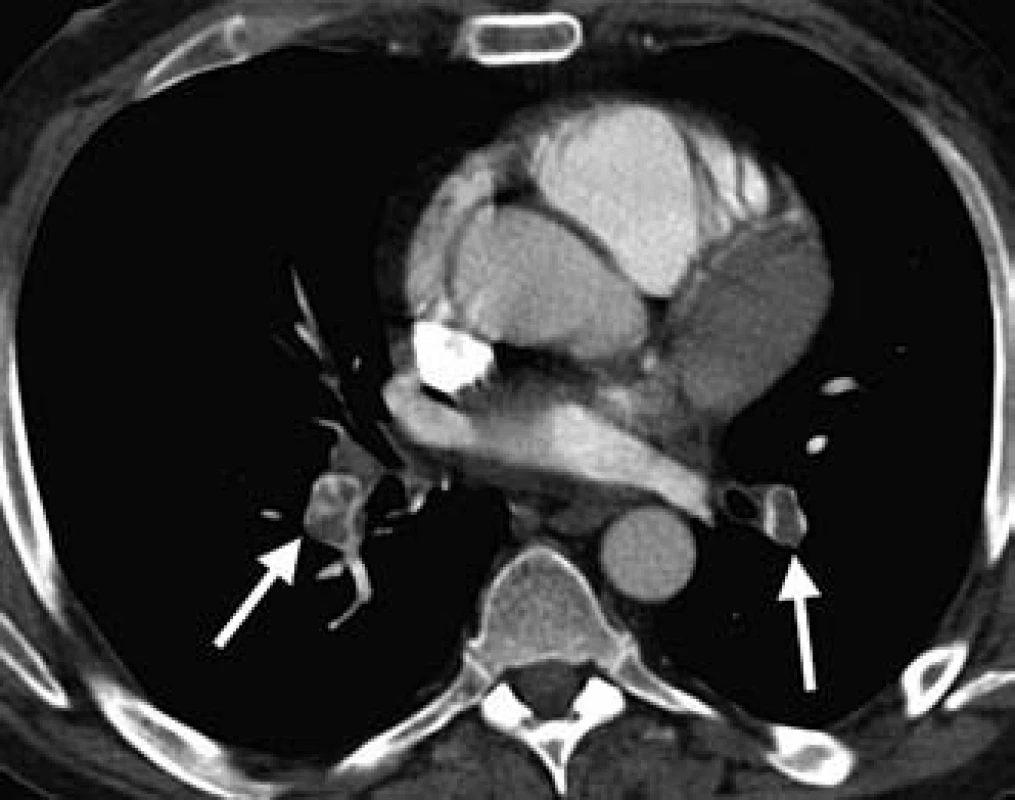
Transtorakálnym echokardiografickým vyšetrením nachádzame znaky typické pre pľúcnu embóliu s vysokým rizikom, a to dilatovanú pravú komoru na 42 mm s útlakom ľavej komory, trikuspidálnu regurgitáciu 3. stupňa s transtrikuspidálnym gradientom 40 mm Hg (obr. 4).
4. Transtorakálne echokardiografické vyšetrenie – dilatácia dutín pravého srdca. 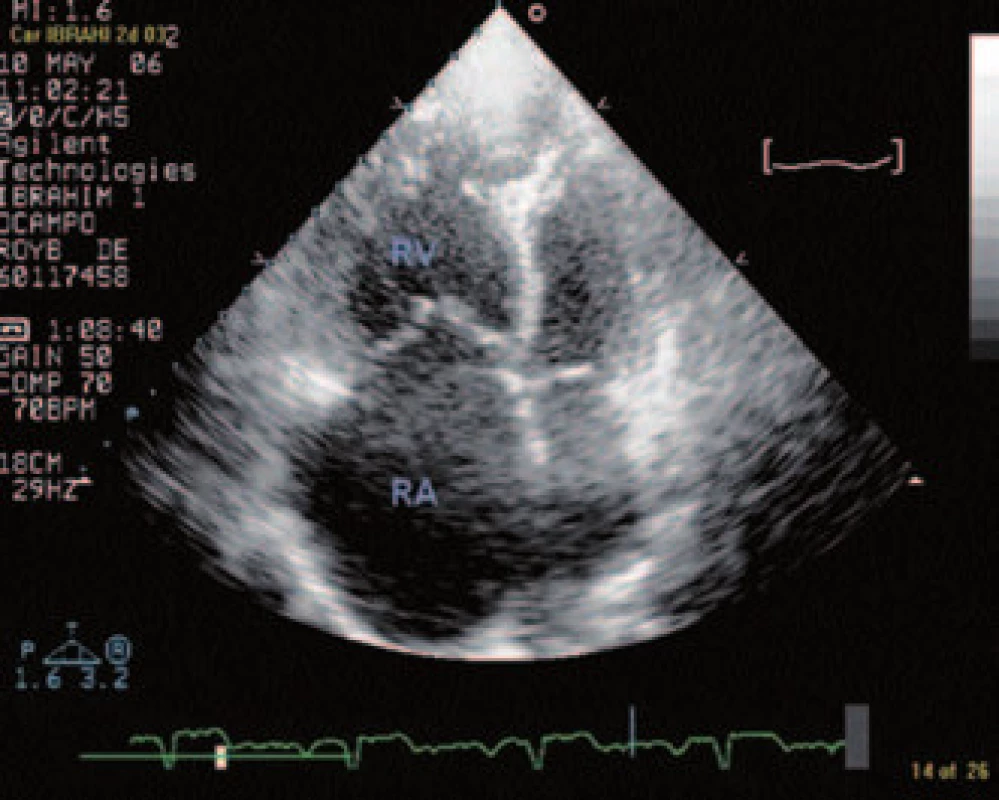
Po prvotnej vazoaktívnej liečbe šokového stavu noradrenalínom a opatrnej volumovej liečbe je zahájená trombolytická terapia podľa platných odporúčaní pre manažment akútnej pľúcnej embólie s vysokým rizikom – pacientke podávame 10 mg alteplázy ako bolus a následne 40 mg za 1. hodinu a 50 mg za 2. hodinu intravenózne [4]. Okrem trombolýzy je aplikovaná aj doplnková antikoagulačná terapia heparínom – pacientke podávame 10 000 j. ako bolus a následne 1 000 j. za hod s úpravou podľa aktuálnych hodnôt aktivovaného parciálneho tromboplastínového času, ktorý udržiavame medzi 1,5 – 2,5-násobkom referenčnej hodnoty [1,4].
Štyridsať osem hod po terapeutickej intervencii realizujeme kontrolné transtorakálne ECHO so signifikantným zlepšením nálezu v porovnaní s vyšetrením pri príjme. Evidentné je zmenšenie pravej komory o 10 mm sprevádzané znížením transtrikuspidálneho gradientu o 10 mm Hg a zlepšením funkcie trikuspidálnej chlopne (trikuspidálna regurgitácia 1. – 2. stupňa pri kontrolnom vyšetrení).
Zmeny vidíme rovnako i na EKG zázname 2 dni po trombolýze, a to v zmysle vymiznutia kmitu S vo zvode I a kmitu Q vo zvode III, signifikantných pre pľúcnu embóliu. Okrem toho vidíme i typický vývoj nových ischemických zmien – inverzných vĺn T vo zvodoch V1 – V4, ktoré imitujú a často sa mýlia s EKG zmenami pri akútnom koronárnom syndróme [5,6] (obr. 5). Postupne dochádza k vymiznutiu aj týchto zmien, a to 5. deň po podaní trombolytickej liečby (obr. 6).
5. EKG záznam 48 hod po liečbe. 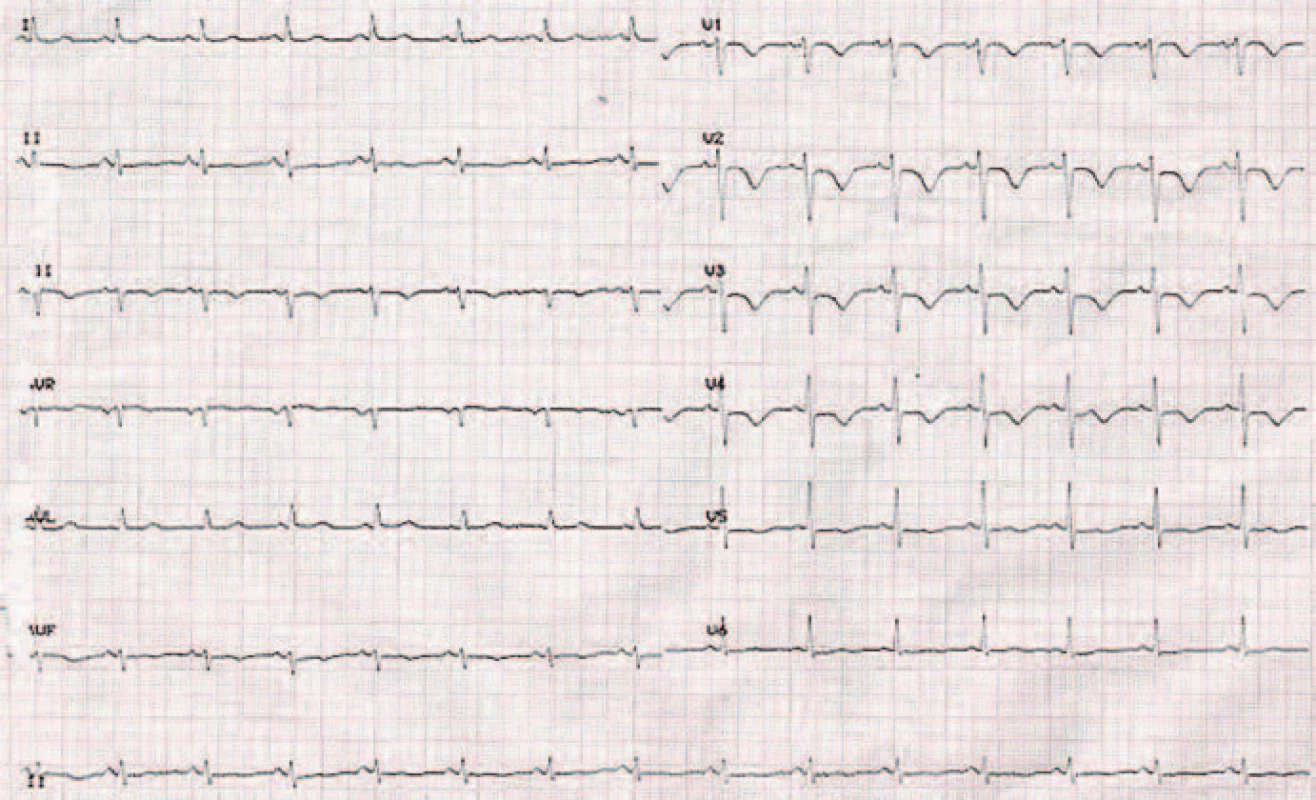
6. EKG záznam 5 dní po liečbe. 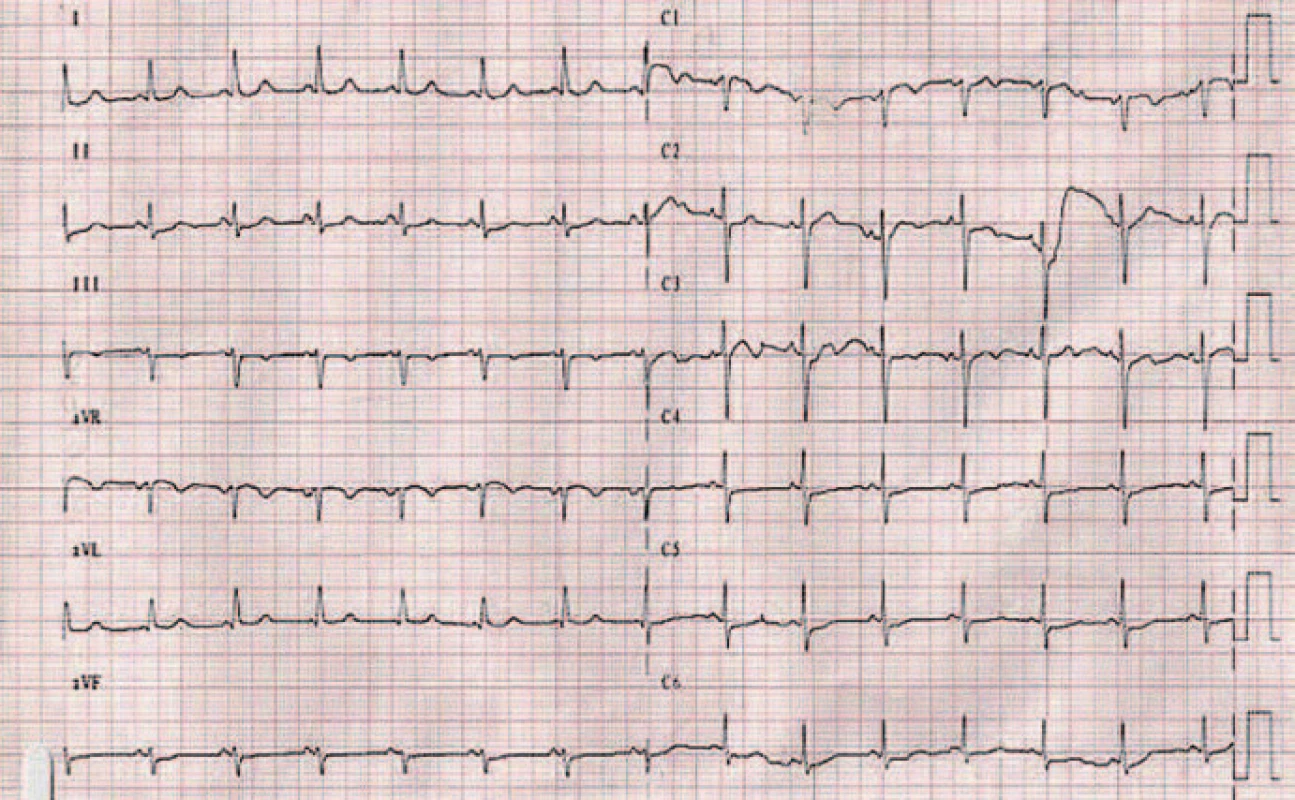
Tri mesiace po ataku akútnej pľúcnej embólie pri kontrolnom EKG vyšetrení konštatujeme, že okrem difúznych porúch v repolarizácii je EKG záznam bez vážnejšej patológie (obr. 7).
7. EKG záznam 3 mesiace po liečbe. 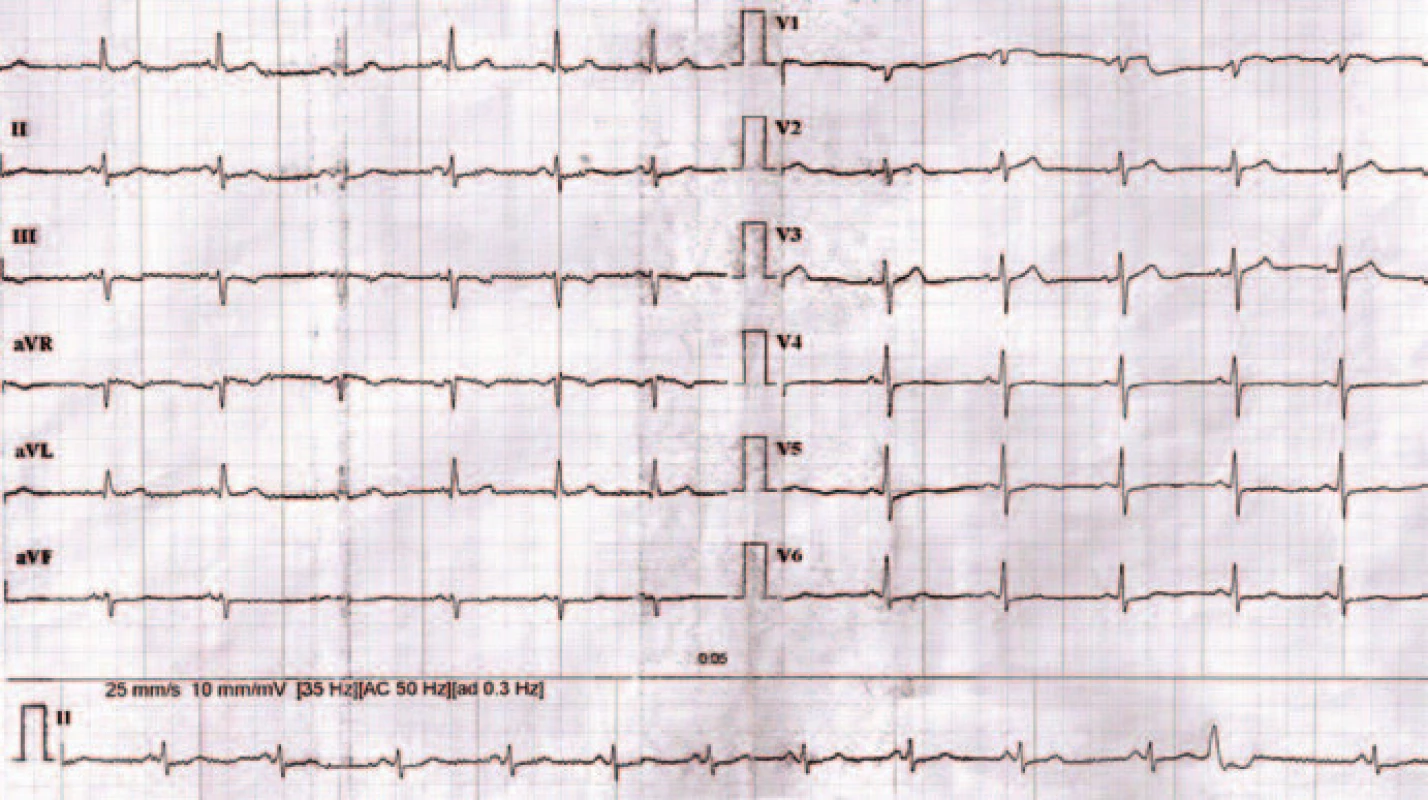
Ešte počas hospitalizácie, po stabilizácii stavu pacientky zahajujeme pátranie po etiológii ochorenia. V anamnéze nenachádzame žiadnu príčinu, ktorá by mohla viesť k vývoju pľúcnej embólie. Pacientka je normostenička s BMI 23, nefajčiarka, bez užívania hormonálnej liečby, bez anamnézy traumy či operácie v posledných 3 mesiacoch, bez vážnejšieho interného predchorobia. V rámci diferenciálnej diagnostiky realizujeme sonografické vyšetrenie hlbokého venózneho systému dolných končatín, avšak bez nálezu trombózy. Za účelom vylúčenia zápalových fokusov realizujeme kultivačné vyšetrenie nosa a hrdla, otorinolaryngologické, stomatologické a gastrofibroskopické vyšetrenie, všetky s normálnym nálezom. V rámci onkologického sceeningu odoberáme onkomarkery (CA 19 – 9, 125, 15 – 3, CEA, α ‑ fetoproteín) a dopĺňame gynekologické vyšetrenie a vyšetrenie stolice na okultné krvácanie (CT hrudníka a abdomenu bolo realizované pri prijatí, bez nálezu neoplastického ochorenia) s negatívnym nálezom. U pacientky je preto indikované hematologické vyšetrenie na trombofilný stav, v rámci ktorého zisťujeme syndróm lepivých doštičiek typ I ako pravdepodobnú príčinu akútnej pľúcnej embólie. Po konzultácii s hematológom preto pacientku nastavujeme okrem perorálnej antikoagulačnej liečby kumarínmi aj na antiagregačnú liečbu acetylsalicylovou kyselinou.
Diskusia
Pľúcna embólia je jedným z najčastejšie sa vyskytujúcich ochorení súčasnosti a tiež jednou z najčastejších akútnych kardiovaskulárnych príhod vo všetkých vekových skupinách, ktorá má významný vplyv nielen na morbiditu, ale aj na mortalitu populácie. Stanovenie diagnózy je neraz náročné, a aj napriek širokým vedomostiam o patofyziológii, intenzívnym profylaktickým opatreniam a adekvátnej liečbe, mortalita na pľúcnu embóliu za posledné desaťročia neklesla.
Krátkodobá prognóza pľúcnej embólie je daná závažnosťou klinického stavu, preto najviac ohrození sú pacienti v kardiogénnom šoku alebo s hypotenziou a akútnym cor pulmonale [3]. Podľa klasifikácie Európskej kardiologickej spoločnosti z roku 2008 ide o pacientov s pľúcnou embóliou s vysokým rizikom mortality, u ktorých je riziko úmrtia vyššie ako 15 % [4]. Títo pacienti majú okrem klinických znakov hemodynamickej instability aj známky dysfunkcie pravej komory verifikovaných echokardiograficky (dilatácia, hypokinéza alebo tlakové preťaženie) alebo laboratórne (elevácia sérových koncentrácií brain‑nátriuretického peptidu a N‑terminálneho pro‑brain‑nátriuretického peptidu). Prítomné sú u nich aj známky poškodenia myokardu, a to pozitivita kardiomarkerov troponínu I alebo T [1,4]. Cenným vyšetrením sa javí aj stanovenie vysoko senzitívneho troponínu T (hsTnT), podľa ktorého je možné, na rozdiel od bežných troponínov, diferencovať medzi zvýšeným a normálnym rizikom mortality [7].
Pri suspekcii na pľúcnu embóliu s vysokým rizikom je nevyhnutné okamžité CT ‑ pulmoangiografické vyšetrenie alebo pri jeho nedostupnosti transtorakálne echokardiografické vyšetrenie a pri ich pozitívnom náleze okamžité zahájenie špecifického terapeutického postupu (trombolýza, resp. embolektómia) [1,3,4]. U pacientov s nejasným alebo negatívnym CT ‑ pulmoangiografickým nálezom napriek vysokej klinickej pravdepodobnosti akútnej pľúcnej embólie je možné využiť na diagnostiku ventilačno?perfúzny scan alebo pľúcnu arteriografiu [7,8]. Výhodnou sa v diagnostike pľúcnej embólie javí i kombinácia CT‑angiografie a CT ‑ venografie pre možnosť pátrania po hlbokej venóznej trombóze ako jednej z možných príčin pľúcnej embólie už v úvode vyšetrovacieho procesu [7,8].
Klinický obraz pľúcnej embólie nie je vždy jednoznačný, a preto aj pri klinicky nestabilných pacientoch je možné váhať alebo predpokladať inú príčinu akútneho stavu. Dôsledkom je, že aj pri dostupnosti všetkých potrebných vyšetrení je primárne zvolená iná vyšetrovacia metóda, čím dochádza k oddialeniu diagnostiky a liečby pľúcnej embólie a tým k zvýšeniu pravdepodobnosti úmrtia. V takýchto prípadoch je preto dôležité správne vyhodnotiť každý symptóm, každý bod anamnézy a každé realizované vyšetrenie.
Klinický obraz pri vstupnom vyšetrení našej pacientky takisto na prvý pohľad neimponoval ako pľúcna embólia, avšak v tomto prípade bolo nutné zamyslieť sa už nad prvými symptómami ochorenia. Dva týždne pred hospitalizáciou pacientka udávala prvé ťažkosti s dýchaním a vznik suchého kašľa, ktoré mohli byť prvými príznakmi pľúcnej embólie. Ambulantne však boli vyhodnotené a liečené ako infekt dýchacích ciest. Pre dominujúci nález na bruchu a anamnézu vomitu a hnačiek pri urgentnom vyšetrení stav imponoval skôr ako náhla brušná príhoda. Z anamnézy je však známa liečba ciprofloxacínom, pri ktorej je výskyt hnačiek častým nežiadúcim účinkom. Palpačná bolesť epigastria bola dôsledkom venostatickej hepatomegálie (verifikovanej už pri fyzikálnom vyšetrení a popisovanej aj pri CT vyšetrení brucha) pri akútnom pravostrannom srdcovom zlyhaní, ktoré bolo dôsledkom tlakového preťaženia pri akútnej pľúcnej embólii.
Dôležitú úlohu v diagnostike pľúcnej embólie zohráva aj EKG záznam. Prvé EKG zmeny charakteristické pre toto ochorenie boli popísané už v roku 1935, kedy McGinn a White na niekoľkých prípadoch opísali známy model S1Q3T3 – kmit S vo zvode I, kmit Q vo zvode III, negatívna vlna T vo zvode III [9]. Dnes vieme, že diagnostika pľúcnej embólie pomocou EKG nie je úplne jednoznačná a okrem uvedených zmien sa môže prejaviť aj vývojom iných patológií, alebo sa na EKG nemusí prejaviť vôbec. V roku 1975, 40 rokov od tejto významnej publikácie, Stein et al vo svojej „Urokinase ‑ Pulmonary Embolism Trial National Cooperative Study“ potvrdili normálny elektrokardiogram u 6 % pacientov s masívnou a u 23 % pacientov so submasívnou pľúcnou embóliou [10]. Typické znaky pľúcnej embólie (blok pravého Tawarovho ramienka, P pulmonale, deviácia srdcovej osi doprava) malo len 26 % zo sledovaných pacientov [10]. Najčastejšie elektrokardiografické abnormality boli nešpecifické zmeny vlny T a ST segmentu (v zmysle elevácie alebo depresie), deviácia srdcovej osi doľava a nízka voltáž komplexu QRS [10,11]. Mnoho ďalších štúdií realizovaných po Steinovej práci potvrdilo výskyt týchto a ďalších nešpecifických elektrokardiografických zmien pri pľúcnej embólii (fibrilácia a flutter predsiení, sínusová tachykardia, posun prechodovej zóny doľava) [12 – 14]. Je teda evidentné, že EKG abnormality pri pľúcnej embólii majú vysokú variabilitu a niektoré z nich nie sú špecifické len pre túto diagnózu. Elektrokardiografia je preto podľa súčasných odporúčaní len doplnkovým vyšetrením, ktoré samo o sebe na diagnostiku pľúcnej embólie nestačí [1,4]. Nie je to však vyšetrenie obsoletné, práve naopak, v prípadoch nejasnej symptomatiky môže byť významnou pomocou pri rozhodovaní o ďalšom diagnostickom postupe.
Na EKG zázname našej pacientky natočenom hneď po príchode na urgentný príjem jednoznačne dominovali zmeny charakteristické pre pľúcnu embóliu – sínusová tachykardia, inkompletný blok pravého Tawarovho ramienka, S1Q3T3. Vzhľadom k atypickému klinickému obrazu však bola diagnostika šokového stavu prvotne vedená úplne iným smerom – pre suspekciu na akútnu brušnú príhodu sa ako prvé realizovalo CT vyšetrenie abdomenu, čo stanovenie správnej diagnózy a teda aj správny manažment pacientky oddialilo.
Záver
Pľúcna embólia je jednou z najčastejších príčin úmrtia v celosvetovej populácii. 2 – 8 % prípadov s rozpoznanou a liečenou pľúcnou embóliou končí fatálne, v prípadoch neliečených táto hodnota dosahuje až 30 % [2]. Napriek širokým diagnostickým možnostiam je však pri nie vždy jednoznačnom klinickom obraze stanovenie tejto diagnózy veľmi náročné. Je známe, že len u 30 % pacientov sa pľúcna embólia rozpozná klinicky [1,2].
Dôsledné vyhodnotenie každého klinického príznaku a využívanie všetkých základných aj doplnkových vyšetrovacích metód, vrátane EKG, preto môže významne napomôcť k zvýšeniu percenta úspešne diagnostikovaných prípadov a tým znížiť mortalitu pacientov s pľúcnou embóliou.
MU Dr. Stanislava Daruľová
www.unm.sk
e‑mail: darulovastanislava@gmail.com
Doručeno do redakce: 15. 5. 2013
Přijato po recenzi: 25. 6. 2013
Sources
1. Vojáček J, Kettner J. Klinická kardiologie. Praha: Nucleus HK 2012.
2. Cohen TA, Agnelli G, Anderson AF et al. Venous thormbembolism (VTE) in Europe. The number of VTE events and associated morbidity and mortality. Thromb Haemost 2007; 98 : 756 – 764.
3. Stein DP. Pulmonary embolism. Massachusetts: Blackwell Publishing 2007.
4. Torbicki A, Perrier A, Konstantinides S et al. Guidelines on the diagnosis and management of acute pulmonary embolism: the Task Force for the Diagnosis and Management of Acute Pulmonary Embolism of the European Society of Cardiology (ESC). Eur Heart J 2008; 29 : 2276 – 2315.
5. Kosuge M, Kimura K, Ishikawa T et al. Electrocardiographic differentiation between acute pulmonary embolism and acute coronary syndromes on the basis of negative T waves. Am J Cardiol 2007; 99 : 817 – 821.
6. Goslar T. Podbregar M. Acute ECG ST – segment elevation mimicking myocardial infarction in a patient with pulmonary embolism. Cardiovasc Ultrasound 2010; 8 : 50.
7. Widimský J. Diagnostika a léčba akutní plicní embolie v roce 2010. Vnitř Lék 2011; 57 : 5 – 21.
8. Widimský J, Malý J, Eliáš P et al. Doporučení diagnostiky, léčby a prevence plicní embolie – verze 2007. Doporučení České kardiologické společnosti. Vnitř Lék 2008; 54 : 25 – 72.
9. McGinn S, White PD et al. Acute cor pulmonale resulting from pulmonary embolism. JAMA 1935; 104 : 1473 – 1480.
10. Stein DP, Dalen JE, McIntyre KM et al. The electrocardiogram in acute pulmonary embolism. Prog Cardiovasc Dis 1975; 17 : 247 – 257.
11. Sinha N, Yalamanchili K, Sukhija R et al. Role of the 12 - lead electrocardiogram in diagnosing pulmonary embolism. Cardiol Rev 2005; 13 : 46 – 49.
12. Daniel RK, Courtney DM, Kline AJ. Assessment of cardiac stress from massive pulmonary embolism with 12 - lead ECG. Chest 2001; 120 : 474 – 481.
13. Todd K, Simpson SC, Redfearn PD et al. ECG for the diagnosis of pulmonary embolism when conventional imaging cannot be utilized: A case report and review of the literature. Indian Pacing Electrophysiol J 2009; 9 : 268 – 275.
14. Brown G, Hogg K. Diagnostic utility of electrocardiogram for diagnosing pulmonary embolism. Emerg Med J 2005; 22 : 729 – 730.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2013 Issue 11-
All articles in this issue
- Prevalence of diabetic retinopathy and distal symmetrical diabetic polyneuropathy, and glomerular filtration screening upon the diagnosis of type 2 diabetes mellitus – a cohort study
- Serious sepsis treatment in intensive care departments in the Czech Republic – EPOSS Project pilot results
- The new blood test biomarker SEPT9 and colorectal carcinoma screening
- Possibilities of genetic diagnostics of intestine tumour and inflammatory diseases in Slovakia
- SAVOR‑ TIMI 53 – Saxagliptin and cardiovascular outcomes in patients with type 2 diabetes mellitus
- Management of superficialis thrombophlebitis. Guidelines of the Angiologiy Section of the Slovak Medical Chamber (2013)
- The value of ECG assessment in pulmonary embolism diagnostics
- Atypical fracture of metatarsal bone in a patient with multiple myeloma who was treated long-term with bisphosphonates
- Inflammatory response and C‑ reactive protein value in patient with acute coronary syndrome
- Thyrostatic treatment and its adverse effects
- Role of cardiac biomarkers in monitoring of cardiotoxicity after hematopoietic stem cell transplantation
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Thyrostatic treatment and its adverse effects
- Inflammatory response and C‑ reactive protein value in patient with acute coronary syndrome
- The value of ECG assessment in pulmonary embolism diagnostics
- Management of superficialis thrombophlebitis. Guidelines of the Angiologiy Section of the Slovak Medical Chamber (2013)
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career