-
Medical journals
- Career
Vénová tromboembólia u onkologického pacienta
: A. Uhrinová; P. Gavornik; I. Vacula
: II. interná klinika Lekárskej fakulty UK a FNsP Bratislava, Slovenská republika, prednosta prof. MUDr. Andrej Dukát, CSc., FESC
: Vnitř Lék 2009; 55(6): 599-603
: Case Reports
Vénová tromboembólia je častou komplikáciou u pacientov s rôznymi nádorovými ochoreniami. V našej kazuistike opisujeme prípad onkologického pacienta v remisii, ktorého stav bol komplikovaný pľúcnou embóliou.
Kľúčové slová:
pľúcna embólia – malignitaÚvod
Asociáciu medzi vénovou tromboembóliou (VTE) a malignitou prvý krát už pred takmer 150 rokmi opísal Armand Trousseau [1]. Pacienti s malígnym nádorovým ochorením predstavujú osobitnú skupinu so zvýšeným rizikom vénovej tromboembólie. Možnosť trombózy u individuálneho pacienta je závislá od viacerých faktorov (typ nádoru, jeho klinické štádium a liečba, pridružené ochorenia atď.). Riziko tromboembolizmu je obzvlášť vysoké pri malígnych mozgových nádoroch, adenokarcinómoch ovária, pankreasu, žalúdka, hrubého čreva, pľúc, prostaty a obličiek. Operácia u pacienta s malígnym nádorom je rizikovejšia v porovnaní s pacientom bez malignity a taktiež použitie niektorých chemoterapeutík zvyšuje riziko tromboembolizmu.
Kazuistika
Pacientom bol 60-ročný muž po subtotálnej kolektómii pre adenokarcinóm sigmy. Operácia sa realizovala 5 mesiacov pred aktuálnou hospitalizáciou a bola nasledovaná chemoterapiou. Aktuálne bol pacient v sledovaní onkológom, v remisii. Na našu kliniku bol pacient prijatý pre neznesiteľnú bolesť ľavej polovice hrudníka a sťažené dýchanie pretrvávajúce 2 dni, len s prechodným ústupom. Bolesť ho obmedzovala v dýchaní a pri pohybe, vystreľovala do ľavej lopatky a ramena. Doma si nameral zvýšenú teplotu (do 38 °C), mal redšiu stolicu a pociťoval zníženú chuť do jedla. Dolné končatiny mu v minulosti neopúchali. Chemoterapia Xelodou® (capecatibinum) sa ukončila 2 týždne pred aktuálnou hospitalizáciou a odvtedy neužíval žiadne lieky.
Počas fyzikálneho vyšetrenia pri prijatí bol pacient v ortopnoickej polohe, mal periférnu cyanózu, tachykardiu (104/min), tlak krvi bol 140/85 mm Hg. Namerali sme zvýšenú telesnú teplotu (38 °C), auskultačne nad bázami pľúc boli počuteľné prízvučné krepitácie s plným jasným poklopom. V krvnom obraze bola prítomná leukocytóza s neutrofíliou (leu 12,9 × 109/l, Neu 92,5 %), v biochemickom vyšetrení boli zvýšené hepatálne testy (bil. celk. 65,5 μmol/l, bil. konjug. 13,7 μmol/l, AST 1,05 μkat/l, ALT 1,13 μkat/l, GMT 1,44 μkat/l, ALP 2,04 μkat/l), pozitívny C‑reaktívny proteín (CRP 158 mg/l) a hyperglykémia (9,6 mmol/l). Hemokoagulačné vyšetrenie ukázalo na aktiváciu intravaskulárnej koagulácie (D-dimér 788 μg/l). Ostatné koagulačné (INR, aPTT-R) a renálne (urea, kreatinín) parametre, ionogram, albumín, markery myokardiálnej nekrózy a vyšetrenie artériových krvných plynov s acidobázickou rovnováhou boli v medziach normy. EKG bolo bez znakov ischémie, prítomná bola sínusová tachykardia. Vzhľadom na výsledky laboratórnych vyšetrení a klinického nálezu sme doplnili RTG vyšetrenie hrudníka, kde bol prítomný nález homogénneho zatienenia vľavo bazálne a pruhovité mäkké splývajúce zatienenia vpravo bazálne. Uvedený nález bol röntgenológom hodnotený ako obojstranná pneumónia (obr. 1). Pre klinické podozrenie na pľúcnu embóliu, ktoré podporoval aj nález významne zvýšeného D-diméru a anamnéza onkologického ochorenia, sme urgentne doplnili CT pulmoangiografické vyšetrenie. Toto vyšetrenie potvrdilo embolizáciu do riečiska pľúcnice, a to do prakticky všetkých segmentálnych artérií pre dolný lalok vpravo, súčasne s kondenzáciami a atelektázami pľúcneho parenchýmu a s podobným nálezom v oblasti linguly vľavo. Prítomná bola tiež atelektáza v oblasti dolného laloka vľavo a ľavostranný fluidothorax do hrúbky 11 mm (obr. 2, 3). Duplexným sonografickým vyšetrením sme nepotvrdili hlbokú vénovú trombózu na žilovom systéme dolných končatín. Echokardiografickým vyšetrením sme zistili len stopovú pulmonálnu a trikuspidálnu regurgitáciu so znakmi ľahkej pulmonálnej hypertenzie.
1. RTG hrudníka – homogénne zatienenie vľavo bazálne a pruhovité mäkké splývajúce zatienenia vpravo bazálne. 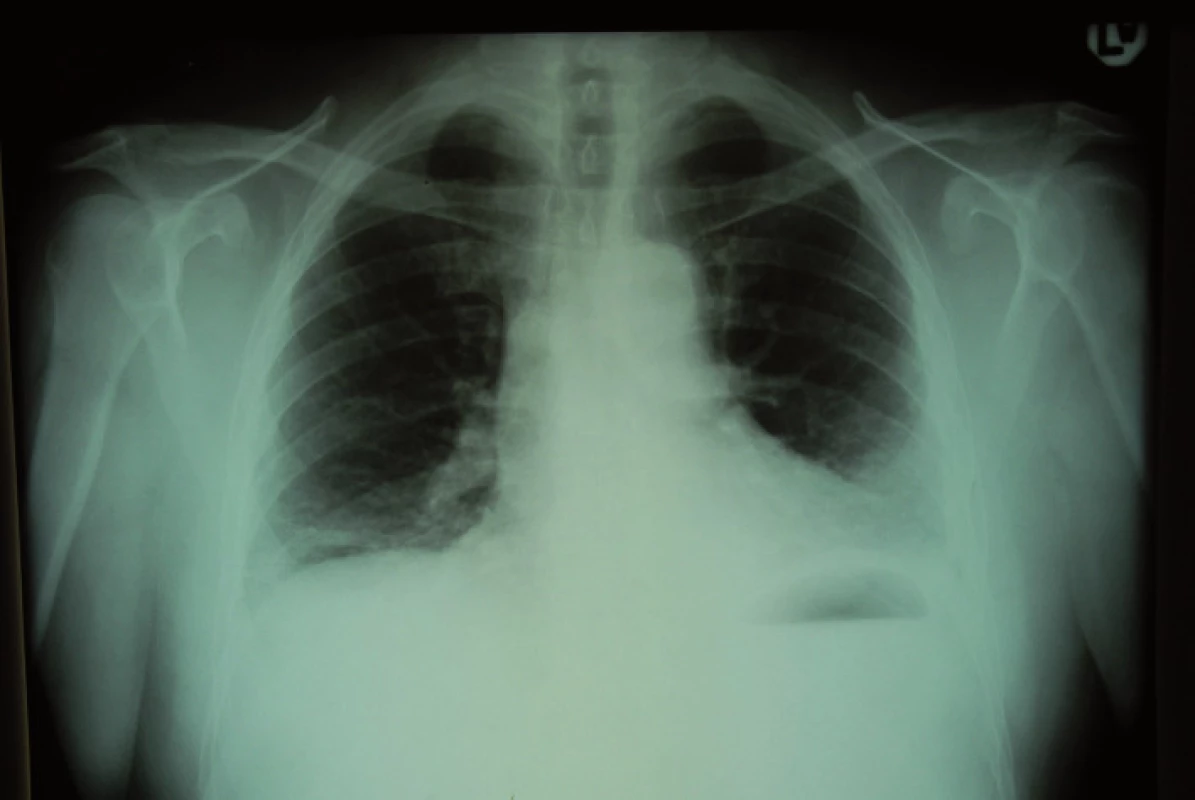
2. CT pulmangiografia – embolizácia do segmentálnych artérií a. pulmonalis pre dolný lalok vpravo a v oblasti linguly vľavo. 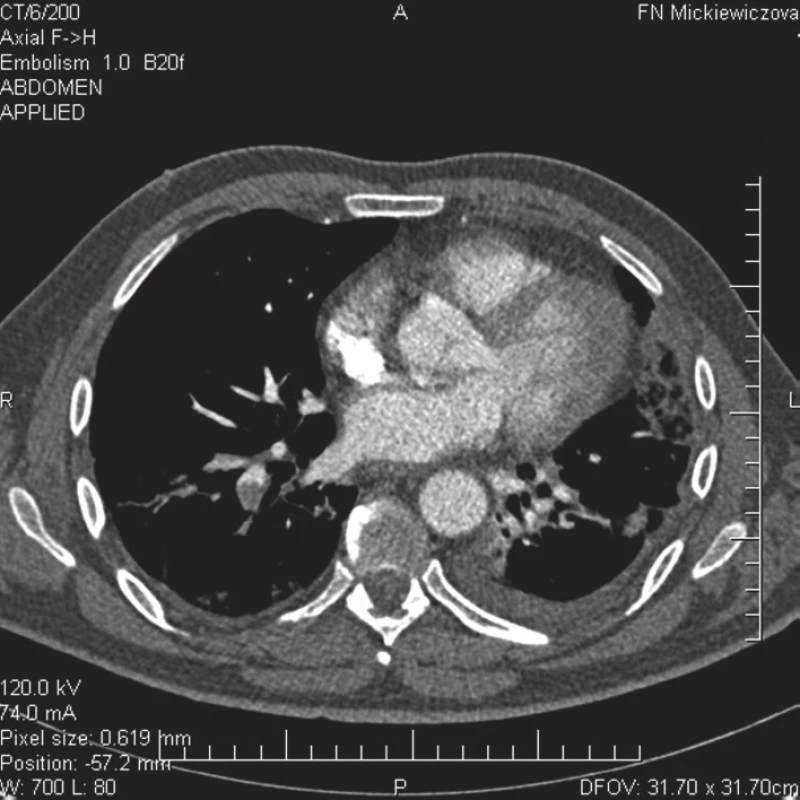
3. CT pulmangiografia – embolizácia do segmentálnych artérií a. pulmonalis pre dolný lalok vpravo spolu s kondenzáciami a atelektázami pľúcneho parenchýmu, atelektáza v oblasti dolného laloka vľavo. 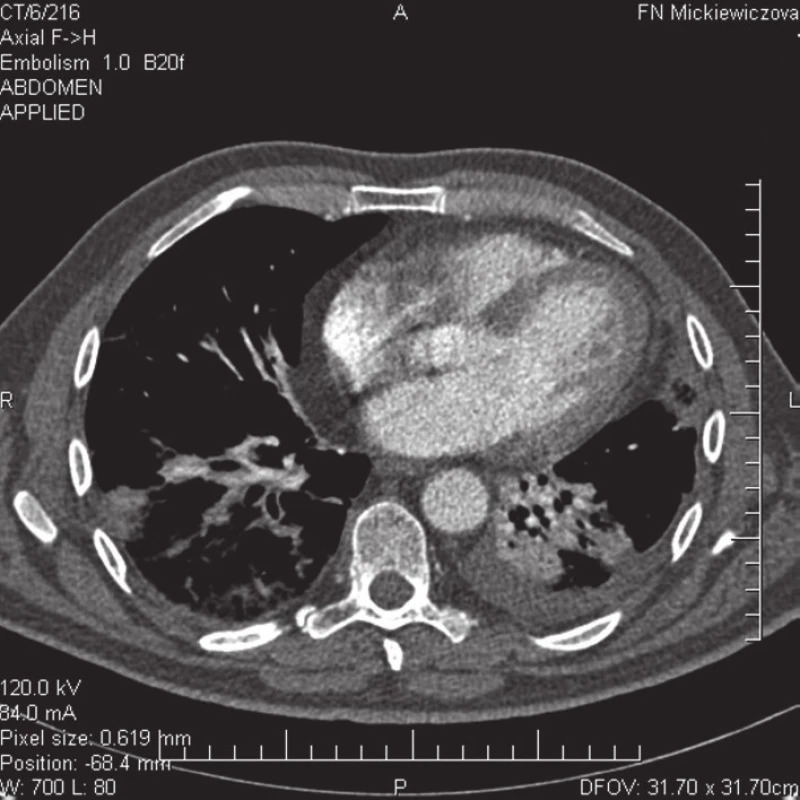
U pacienta sme pri prijatí začali antikoagulačnú liečbu nízkomolekulovým heparínom (LMWH) – dalteparínom v plnej antikoagulačnej dávke (podľa telesnej hmotnosti) a oxygenoterapiu. Pre vysokú pozitivitu zápalových parametrov sme podávali aj empirickú antibiotickú liečbu (klaritromycín). Pacient bol v pokojovom režime, bolesti sme tlmili analgetikami, bandážovali sme dolné končatiny. V priebehu hospitalizácie na 4. deň začal pacient pociťovať tlak na hrudnej kosti so šírením pod pravú lopatku, na EKG sme zachytili supraventrikulárnu tachykardiu s frekvenciou 210/min (obr. 4). V liečbe poruchy rytmu bol zvolený parenterálne podaný metoprolol s dobrým efektom a verziou na sinusový rytmus, ktorý pretrvával. Postupne došlo u pacienta k ústupu dýchavice a bolestí na hrudníku, zlepšeniu objektívneho nálezu a k poklesu D-diméru (788 μg/l ... 236 μg/l), bilirubínu (65,5 μmol/l ... 13,9 μmol/l) a hepatálnych enzýmov (AST 1,05 μkat/l ... 0,36 μkat/l, ALT 1,13 μkat/l ... 0,38 μkat/l), tiež zápalových markerov (leu 12,6 × 109/l ... 8,69 × 109/l, CRP 158 mg/l ... 13,9 mg/l). Po 17 dňoch hospitalizácie sme ho v stabilizovanom stave prepustili do domáceho ošetrenia, v antikoagulačnej liečbe sme ponechali LMWH (dalteparín).
4. EKG – supraventrikulárna tachykardia s frekvenciou 210/min. 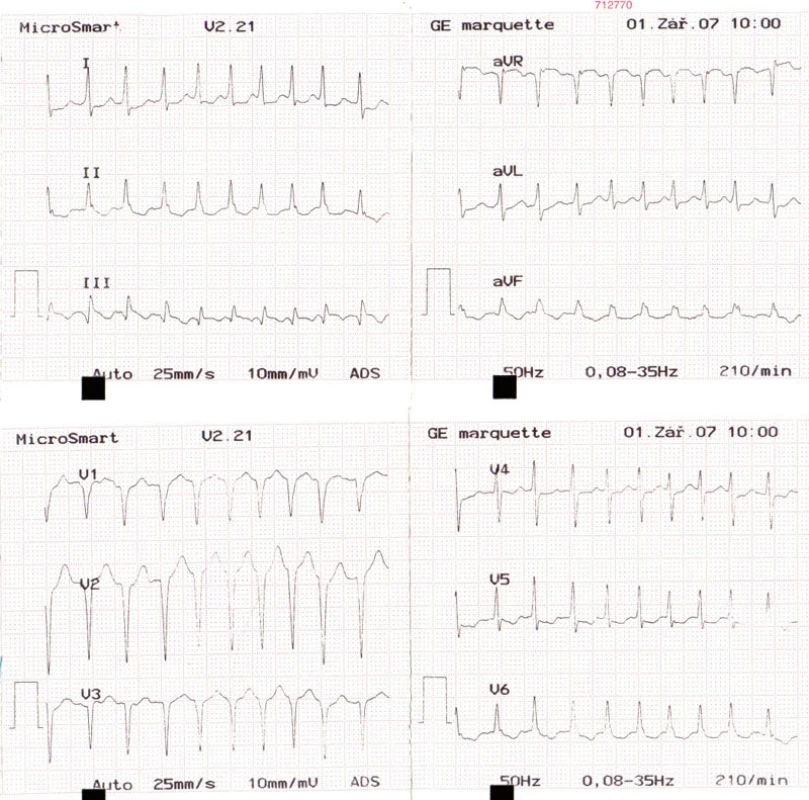
Po prepustení do ambulantnej starostlivosti sme u pacienta pokračovali v antikoagulačnej liečbe nízkomolekulovým heparínom v trvaní viac ako 1/2 roka, pri opakovaných kontrolách bol bez ťažkostí. Za účelom zistenia pôvodu vzniknutej pľúcnej embólie sme po ukončení hospitalizácie realizovali scintigrafické vyšetrenie – tromboscint, ktoré ukázalo na malé ložisko vysoko suspektné z trombózy v dolnej časti v. femoralis vľavo. Kontrolným CT vyšetrením hrudníka, brucha a panvy po 4 mesiacoch sme zistili len nevýrazné reziduá po pľúcnych infarktoch, bez zrejmej recidívy základného onkologického ochorenia, bez metastáz (obr. 5).
5. Kontrolná CT pulmangiografia po 4 mesiacoch. 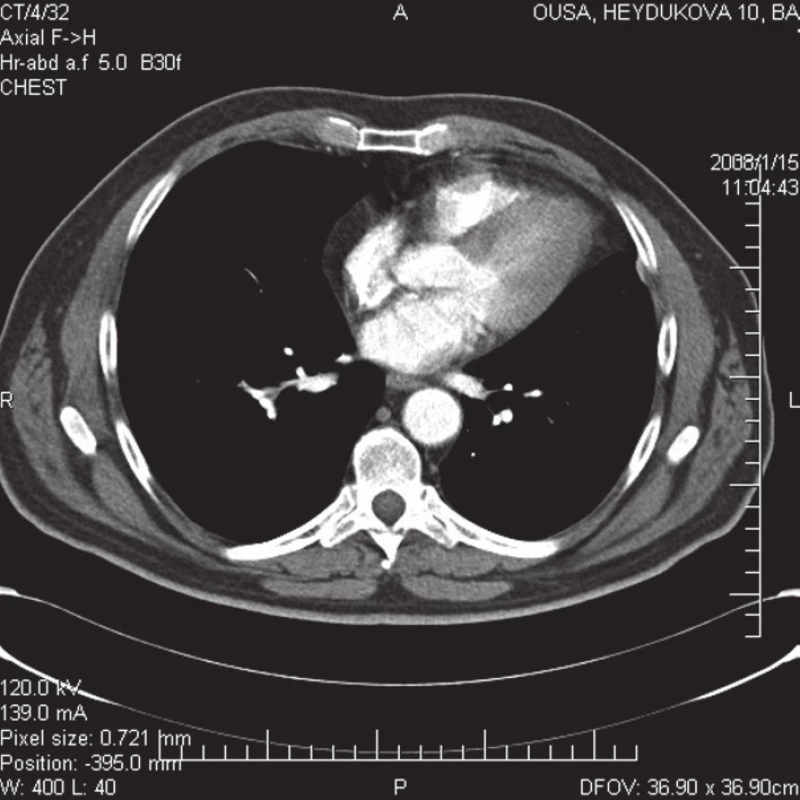
Diskusia
VTE je multifaktoriálne ochorenie s epizodickou klinickou manifestáciou, ku ktorej dochádza vtedy, ak protrombotický potenciál, ktorý je závislý od veku, získaných a genetických rizikových faktorov, presiahne určitú hranicu. Výskyt VTE u pacientov s nádorom je častý a môže komplikovať liečbu nádoru, ako aj skracovať prežívanie onkologických pacientov. Vénová trombóza môže dokonca predchádzať objavenie sa nádorového ochorenia, alebo naň poukázať. VTE je druhou najčastejšou príčinou mortality pacientov s nádorom, pričom onkologickí pacienti predstavujú asi 20 % všetkých pacientov s VTE [2]. Relatívne riziko trombózy pri malígnych ochoreniach 7-násobné v porovnaní so všeobecnou populáciou [3]. Výskyt VTE u pacientov s nádorom závisí najmä od typu nádoru, od štádia nádorového ochorenia, od prítomnosti vzdialených metastáz a od toho, či bola v liečbe použitá chemoterapia, terapia inhibítormi angiogenézy alebo hormonálna terapia [4]. V našom prípade išlo o pacienta s adenokarcinóm sigmy po subtotálnej kolektómii pred 5 mesiacmi, ktorý bol následne liečený adjuvantnou chemoterapiou – Xelodou®. Incidencia VTE u pacientov s kolorektálnym karcinómom je najvyššia v prvých 6 mesiacoch po diagnóze a potom rapídne klesá [5]. K nežiadúcim reakciám Xelody® patrí aj pľúcna embólia, avšak riziko je popisované ako menej časté (t.j. ≥ 1/1 000, < 1/100).
Včasná diagnostika a liečba, ale najmä profylaxia sú predpokladmi zníženia mortality na pľúcnu embóliu. Pľúcna embólia je ochorenie charakterizované často nešpecifickými symptómami a znakmi [6]. U nášho pacienta sa subjektívne prejavila ostrou – pleurálnou bolesťou a dýchavicou, prítomná však bola aj zvýšená telesná teplota. V diferenciálnej diagnostike týchto symptómov na prvom mieste myslíme na pleuropneumóniu. Fyzikálne vyšetrenie, najmä auskultačný nález prízvučných inspiračných krepitácií, podporovalo práve diagnózuzápalového ochorenia pohrudnice a pľúc. RTG hrudníka bol röntgenológom hodnotený ako obojstranná pneumónia a zápalovú etiológiu ťažkostí podporovala aj pozitivita zápalových ukazovateľov (zvýšené CRP a leukocytóza s neutrofíliou).
Zvýšený D-dimér má nízku špecificitu, ale vysokú senzitivitu pre diagnózu VTE [7]. Zvýšený býva tiež pri ochoreniach pečene, zápale, malignitách, traume, u tehotných ženách, po chirurgickom zákroku ako aj u pacientov v pokročilom veku. Prítomnosť zvýšeného D-diméru mohla teda aj u nášho pacienta svedčiť pre pneumóniu, mohla však odrážať aj relaps základného onkologického ochorenia, ale aj naznačovať pľúcnu embóliu. D-dimér sa pre svoju vysokú negatívnu prediktívnu hodnotu a súčasne nízku špecificitu má používať predovšetkým pre vylúčenie prítomnosti VTE u pacientov s nízkou klinickou pravdepodobnosťou VTE. Pre posúdenie klinickej pravdepodobnosti sa využívajú viaceré skórovacie systémy, k najznámejším patrí Wellsov (tab. 1) a genevský skórovací systém. U nášho pacienta bola celková pravdepodobnosť na podklade výpočtu Wellsovho skóre stredne zvýšená. Preto sme doplnili CT pulmoangiografické vyšetrenie, ktoré diagnózu pľúcnej embólie potvrdilo. V našom prípade boli markery myokardiálnej nekrózy v medziach normy. Pozitivita týchto markerov a znaky preťaženia a dilatácia pravostranných oddielov pri echokardiografii ukazujú na prítomnosť mikroinfarktov pri tlakovom preťažení pravej komory a horšiu prognózu ochorenia, kedy sa má uvažovať o trombolýze aj pri hemodynamicky stabilnom pacientovi.
Liečba pľúcnej embólie v závislosti od závažnosti zahŕňa antikoagulačnú, trombolytickú liečbu a trombektómiu. Vzhľadom na to, že náš pacient bol hemodynamicky stabilný a bol bez dysfunkcie pravej komory, sme sa rozhodli pre antikoagulačnú liečbu. Zvolili sme LMWH, ktorý môže byť podávaný bezpečne u ambulantných pacientov bez nutnosti laboratórneho monitorovania a s nízkym rizikom vzniku heparínom indukovanej trombocytopénie. Onkologickí pacienti majú vyššie riziko recidívy VTE, ako aj vyššie riziko krvácania spôsobeného antikoagulačnou liečbou v porovnaní s pacientmi bez nádorového ochorenia. LMWH sú v porovnaní s nefrakciovaným heparínom (UFH) a kumarínmi účinnou, bezpečnou a pohodlnou alternatívou a stali sa metódou voľby v liečbe VTE u onkologických pacientov [8]. Tieto skutočnosti potvrdila aj štúdia CLOT, ktorá dokázala vysokú účinnosť dlhodobej liečby LMWH (dalteparín) v zabránení recidív VTE spolu s nižším rizikom krvácania v porovnaní s kumarínmi. Preto je u pacientov s VTE a malígnym ochorením odporúčaná liečba LMWH v trvaní najmenej 3–6 mesiacov [9]. Na základe tejto štúdie jedine dalteparín a tinzaparín (nie je registrovaný na Slovensku) majú odporúčanie pre liečbu akútnej hlbokej vénovej trombózy a embólie do pľúc a predlženú tromboprofylaxiu (6-mesačnú) u pacientov s nadorovým ochorením – 1A [10]. V liečbe u nášho pacienta sme zvolili dalteparín, počas liečby bol bez krvácavých komplikácií, dobre ju toleroval. Liečba bola úspešná, došlo k ústupu subjektívnych ťažkostí, zlepšeniu laboratórneho nálezu ako i výraznému zlepšeniu nálezu na kontrolnom CT vyšetrení. V ďalšom priebehu sa sledovanie dynamiky D-diméru, aj napriek jeho nízkej špecificite v diagnostike VTE, ukázalo ako užitočné k monitorovaniu účinnosti antikoagulačnej liečby a súčasne má toto vyšetrenie istú hodnotu aj pri hodnotení možnej recidívy onkologického ochorenia.
Záver
Naša kazuistika dokumentuje rozmanitosť prejavov pľúcnej embólie a možné problémy v diferenciálnej diagnostike najmä v prípade zápalom komplikovaného priebehu. Pacienti s malígnym nádorovým ochorením predstavujú osobitnú skupinu so zvýšeným rizikom vénovej tromboembólie. Napriek tomu, v bežnej praxi stále pretrvávajú často neodôvodnené obavy z krvácavých komplikácií a tie prevládajú nad presvedčením o benefite z tromboprofylaxie. Aj naše skúsenosti podporujú úvahy o rozšírení použitia farmakologickej tromboprofylaxie a jej predĺženého podávania a rovnako dokumentuje úspešné a účinné použitie nízkomolekulových heparínov v dlhodobejšej liečbe a sekundárnej prevencii VTE u onkologických pacientov ako bezpečnej a účinnej alternatívy ku perorálnym antikoagulanciám.
Prednesené na XVI. slovenskom angiologickom kongrese v Tatranskej Lomnici dňa 8. 10. 2008
Doručeno do redakce: 16. 1. 2009
Přijato po recenzi: 25. 2. 2009
MUDr. Alena Uhrinová
www.fnspba.sk
e‑mail: alenauhrin@inmail.sk
Sources
1. Trousseau A. Phlegmasia alba dolens. Clinique medicinale de l’Hotel Dieu de Paris. Paris: J-B Baillière § Fils 1865 : 645–712.
2. Lee AY. Management of thrombosis in cancer: primary prevention and secondary prophylaxis. Br J Haematol 2005; 128 : 291–302.
3. Prandoni P. Acquired risk factors for venous thromboembolism in medical patients. Pathophysiol Haemost Thromb 2006; 35 : 128–132.
4. Büller HR, van Doormaal FF, van Sluis GL et al. Cancer and thrombosis: from molecular mechanisms to clinical presentations. J Thromb Haemost 2007; 5 (Suppl 1): 246–254.
5. Alcalay A, Wun T, Khatri V et al. Venous thromboembolism in patients with colorectal cancer: incidence and effect on survival. J Clin Oncol 2006; 24 : 1112–1118.
6. American College of Emergency Physicians Clinical Policies Committee. Clinical policy: critical issues in the evaluation and management of adult patients presenting with suspected pulmonary embolism. Ann Emerg Med 2003; 41 : 257–270.
7. Righini M, Perrier A, De Moerloose P et al. D-Dimer for venous thromboembolism diagnosis: 20 years later. J Thromb Haemost 2008; 6 : 1059–1071.
8. Lee AY. Venous thromboembolism and cancer: prevention and therapy. Vnitř Lék 2006; 52 (Suppl 1): 127–131.
9. Hirmerová J. Optimální délka antikoagulační léčby po žilní tromboembolické příhodě: obecný či individualizovaný přístup? Vnitř Lék 2007; 53 : 662–668.
10. Lee AY, Levine MN, Baker RI et al. Low-molecular-weight heparin versus a coumarin for the prevention of recurrent venous thromboembolism in patients with cancer. N Engl J Med 2003; 349 : 146–153.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2009 Issue 6-
All articles in this issue
- Twenty years of care for cystic fibrosis adults in Czech Republic
- Alemtuzumab in chronic lymphocytic leukemia treatment: retrospective analysis of outcome according to cytogenetics
- Is confirmation of an adrenal adenoma in patients with primary aldosteronism sufficient for indication of adrenalectomy?
- Relationships of hormones of adipose tissue and ghrelin to bone metabolism
- Application of warfarin pharmacogenetics
- The treatment of renal failure in multiple myeloma
- From the diagnosis of celiac disease to the prospect of legislative changes
- The case of familial adenomatous polyposis and a proposal for the system of dispensarisation
- Localized tracheobronchial amyloidosis, type AA, and its differentiation from the systemic form of amyloidosis in clinical practice
- Venous thromboembolism in an oncology patient
- Ascites in Mulibrey syndrome
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- The treatment of renal failure in multiple myeloma
- Is confirmation of an adrenal adenoma in patients with primary aldosteronism sufficient for indication of adrenalectomy?
- Application of warfarin pharmacogenetics
- The case of familial adenomatous polyposis and a proposal for the system of dispensarisation
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career


