-
Medical journals
- Career
Systémový lupus erytematózus
: J. Lukáč; J. Rovenský; O. Lukáčová; D. Kozáková
: Národný ústav reumatických chorôb, Piešťany, Slovenská republika, riaditeľ prof. MUDr. Jozef Rovenský, DrSc., FRCP
: Vnitř Lék 2006; 52(7-8): 702-711
: 130th Internal Medicine Day - Rheumatology in clinical practice
Systémový lupus erytematózus (SLE) je chronické celkové autoimunitné ochorenie charakterizované produkciou autoprotilátkok k rôznym autoantigénom. Jeho etiopatogenéza nie je presne stanovená, ale predpokladajú sa faktory genetické, imunologické, hormonálne a vplyvy vonkajšieho prostredia. Prejavuje sa rozmanitými symptómami a môže postihnúť ktorýkoľvek orgán alebo systém v tele. Klinické prejavy sú dôsledkom chronického zápalu v tkanivách, ktorý je zapríčinený predovšetkým ukladaním imunokomplexov a cytotoxickým poškodením. V ostatných desaťročiach sa výrazne znížila mortalita pacientov so SLE a predĺžil sa ich život. Napriek tomu je diagnostika, sledovanie a liečba tejto choroby zložitá a vyžaduje si interdisciplinárnu spoluprácu.
Kľúčové slová:
systémový lupus erytematózus - diagnostika - klinické prejavy - priebeh - liečbÚvod
Systémový lupus erytematózus (SLE) sa zaraďuje medzi systémové choroby spojiva (SCHS). Prejavuje sa postihnutím kĺbov, šliach, kože, obličiek, pľúc, kardiovaskulárneho, nervového, hematopoetického systému a iných orgánov a systémov. Klinický obraz SLE i jeho priebeh je veľmi rozmanitý: u každého pacienta sa vyskytujú iné kombinácie klinických, laboratórnych a imunologických prejavov. Podľa prevažujúcich príznakov a priebehu sa rozlišuje niekoľko foriem SLE. Okrem toho môže SLE vytvárať prekryté syndrómy s ostatnými SCHS.
Etiopatogenéza SLE
Príčina vzniku SLE nie je známa. Predpokladá sa, že pre jeho rozvoj je dôležitá kombinácia endogénnych a enviromentálnych faktorov. Výskyt SLE je asociovaný s haplotypom HLA A1,B8 a HLA-DR-2, DR-3 a DQ-2 [1]. Okrem genetickej predispozície sú to abnormality imunitného systému, hormonálne vplyvy a vek. Za exogénne spúšťacie faktory sa považujú vírusové infekcie, UV-žiarenie, chemické látky, lieky a prípadne ďalšie, dosiaľ neznáme vplyvy. Ich dôsledkom je vystupňovaná imunitná odpoveď a porucha regulačných mechanizmov, ktoré sa prejavujú hyperaktivitou T - a B-lymfocytov. Aktivované B-lymfocyty produkujú veľké množstvo nešpecifických autoprotilátok proti intracelulárnym antigénom, pričom zlyháva odstraňovanie autoreaktívnych klonov T-lymfocytov v organizme. Určitú úlohu pravdepodobne zohráva aj porucha komplementového systému a fagocytózy, pretože fragmenty apoptotických buniek, ktoré nie sú dostatočne rýchlo eliminované z tkanív, rozoznávajú bunky imunitného systému ako cudzorodé [2]. Vytvárajú proti nim autoprotilátky a vznikajú antigén-protilátkové komplexy (imunokomplexy), ktoré sa deponujú predovšetkým v cievach.
Epidemiológia
Prevalencia SLE kolíše podľa rôznych zdrojov medzi 20 až 50 prípadov na 100 000 obyvateľov. V USA je výskyt SLE 2-3krát častejší u amerických černochov ako u kaukazoidnej rasy. Ženy sú postihnuté 8krát častejšie ako muži. Po 50 rokov veku je pomer žien k mužom 5 : 1 [3].
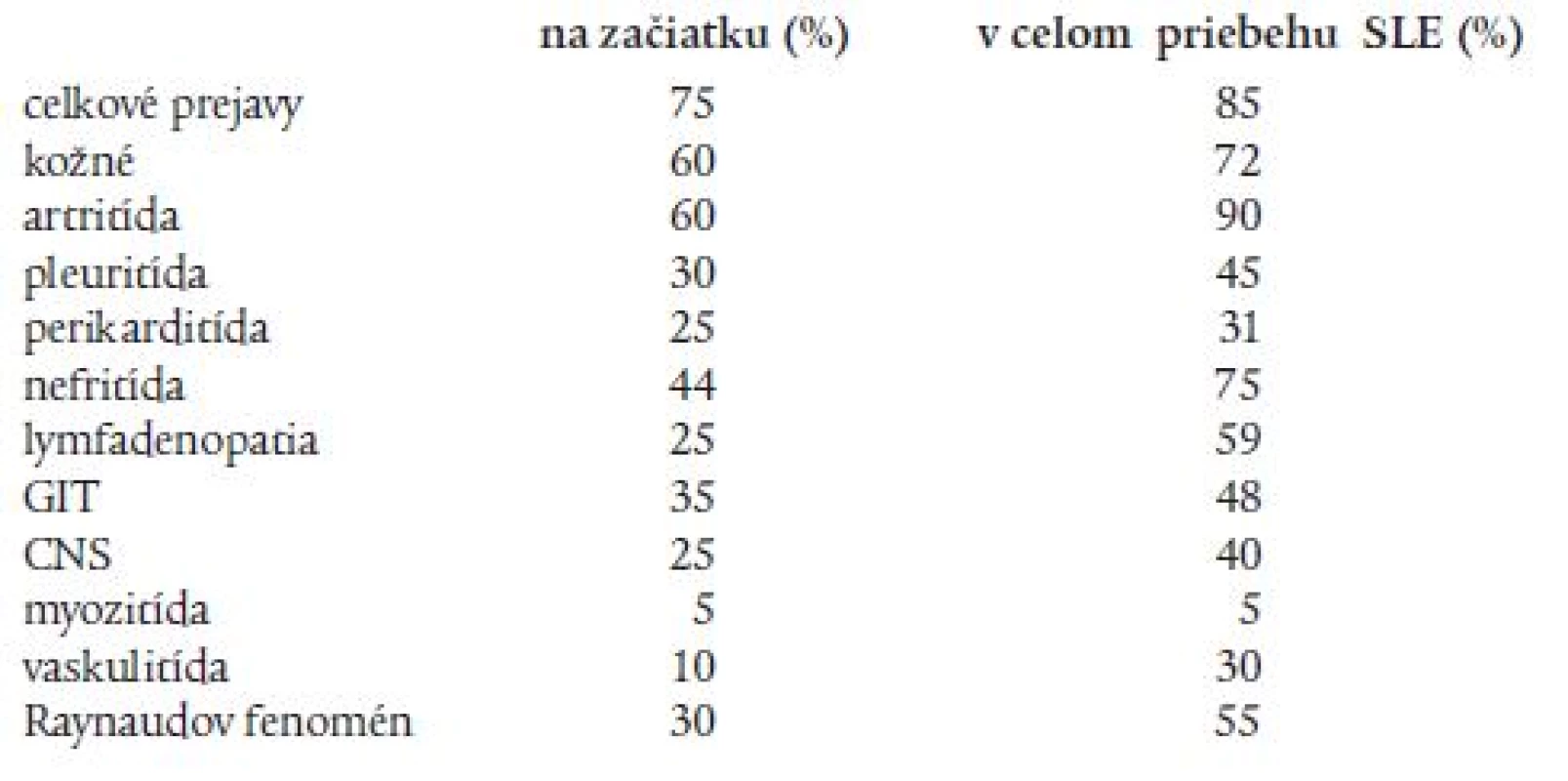
Klinický obraz
Klinický obraz SLE je polysymptómový, môže sa vyskytnúť postihnutie rôznych orgánov a systémov - najčastejšie kĺbov, kože, obličiek, kardiovaskulárneho, respiračného, nervového a hemopoetického systému (tab. 1) [4]. U pacientov so SLE sa pred prepuknutím choroby často vyskytuje leukopénia, fotosenzitivita, Raynaudov fenomén či epizodická artritída. Pri vzplanutí sa zjavujú celkové príznaky - subfebrility, slabosť a chudnutie [5].
Kĺbové a svalové prejavy
Artralgie, artritídy a tendosynovitídy má až 90 % chorých. Artritída je spravidla epizodická, migrujúca, neerozívna, u časti pacientov môže prejsť do polyartritídy pripomínajúcej reumatoidnú artritídu (obr. 1). Zriedkavejšie sa vyskytujú i šľachové deformity. Najčastejšie sú postihnuté drobné kĺby rúk a zápästia. Šľachové deformity sa prejavujú subluxáciami, flekčnými kontraktúrami a ulnárnymi deviáciami. Neerozívna artritída so šľachovými deformitami sa označuje ako Jaccoudova artritída (obr. 2). Rentgenologicky sa zisťuje osteoporóza, erózie sú ojedinelé, u časti pacientov sa vyskytuje avaskulárna nekróza, najčastejšie v hlave femoru. Časté sú myalgie a svalová slabosť, niekedy s elektromyografickým dôkazom myogénnej lézie, ale rozvinutý obraz myozitídy je zriedkavý [6].
1. Šľachové deformity u pacienta s SLE (Jaccoudova artropatia). 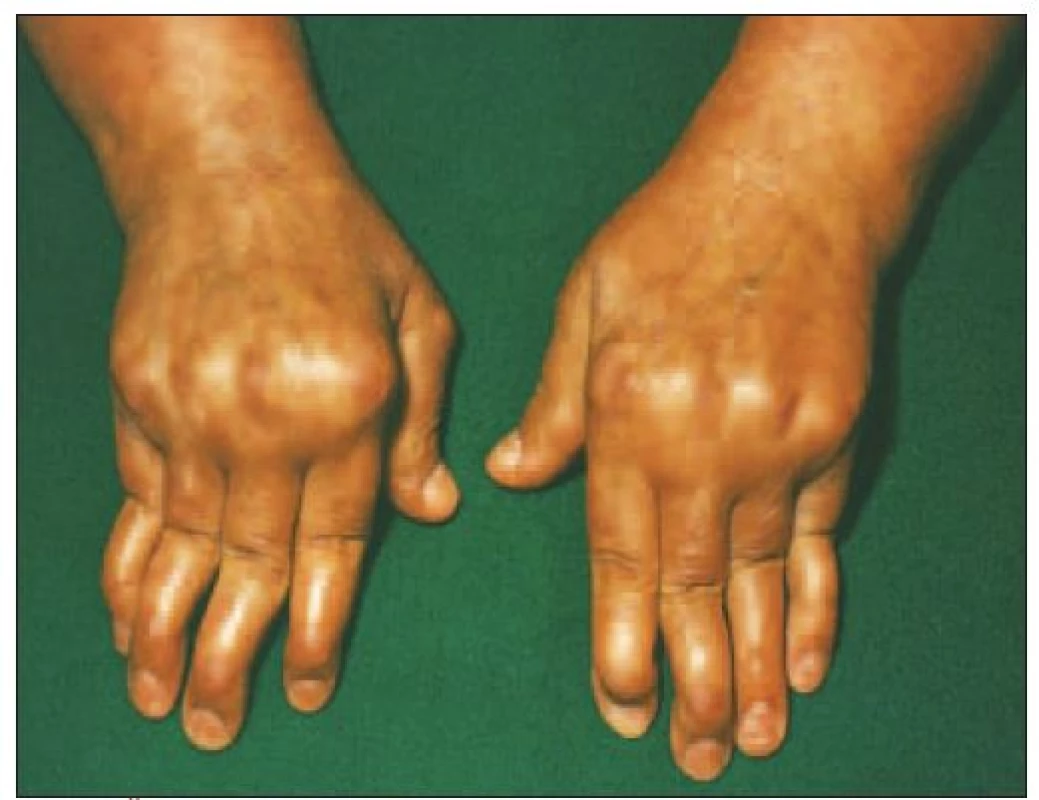
2. Rentgenologický obraz deformít u rovnakej pacientky s SLE – bez erozívnych zmien. 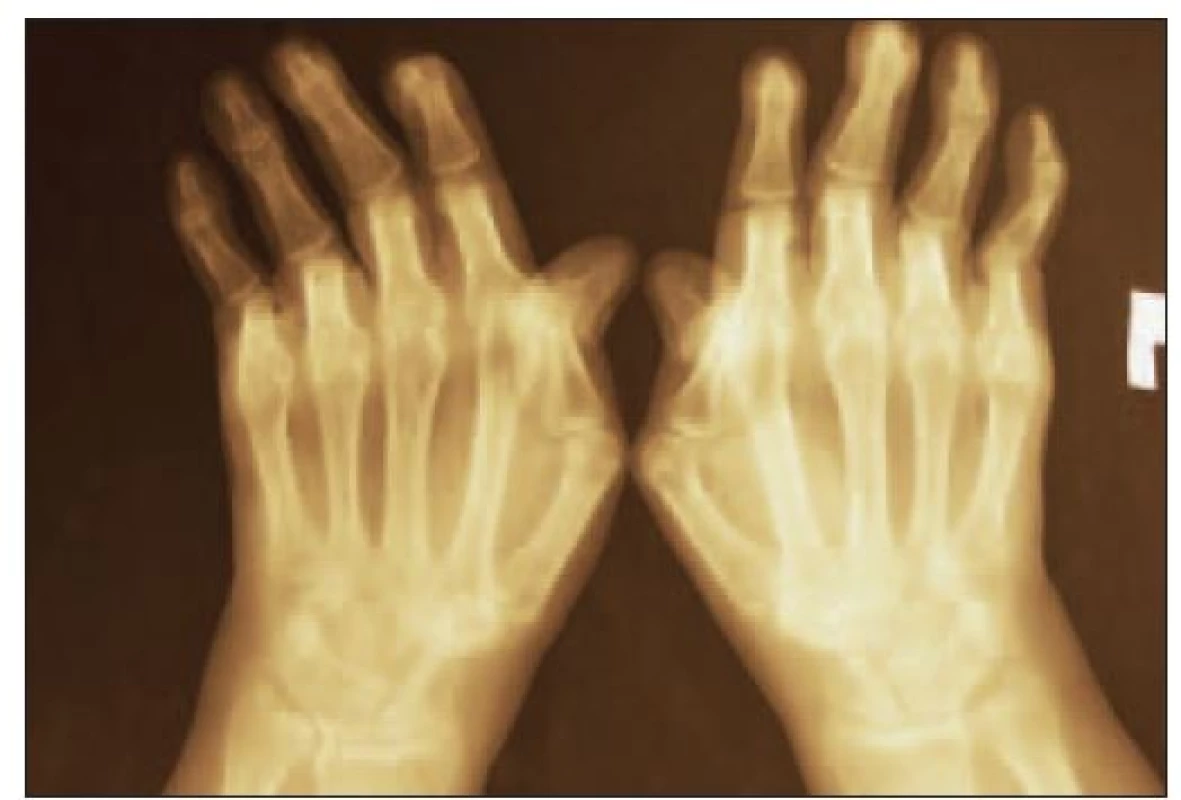
Kožné prejavy
Vyskytujú sa až u 80 % pacientov (tab. 2). Rozoznávajú sa 3 typy kožných morf špecifických pre SLE:
- Akútny kožný lupus erytematózus sa prejavuje typickým motýľovitým erytémom na lícach a prechádzajúcim cez chrbát nosa, alebo generalizovaným erytémom (obr. 3). Erytém je indurovaný, spontánne citlivý alebo pálivý. Najčastejšie je vyvolaný slnečným žiarením. Histologicky sa v bioptických vzorkách erytému zisťujú špecifické zápalové zmeny, imunofluorescenčne aj depozity imunokomplexov. Akútnou formou je i generalizovaný makulopapulózný erytém na trupe a končatinách - niekedy i s bulóznymi prejavmi.
- Subakútny kožný lupus erytematózus sa prejavuje erytémom na tvári, hrudi a pleckách a miestach vystavených slnečnému žiareniu. Má charakter makulopapulóznych erytémov alebo plakov, miestami ošupujúcich sa, miestami až s exulcerácimi (obr. 4). Niekedy má anulárny tvar. Až 70 % týchto pacientov má protilátky anti-Ro.
- Chronický kožný lupus erytematózus. Pre túto formu lupusu sú charakteristické diskoidné morfy prejavujúce sa erytémami, podobnými ako pri subakútnom LE, hypertrofickými alebo verukóznymi, často jazviacimi léziami. Neskôr sa vyvíjajú hyper - a depimentácie. Ložiská sa najčastejšie vyskytujú na tvári alebo v kapilíciu s ložiskovou alopéciou [7].
3. Motýľovitý erytém u pacientky s SLE. 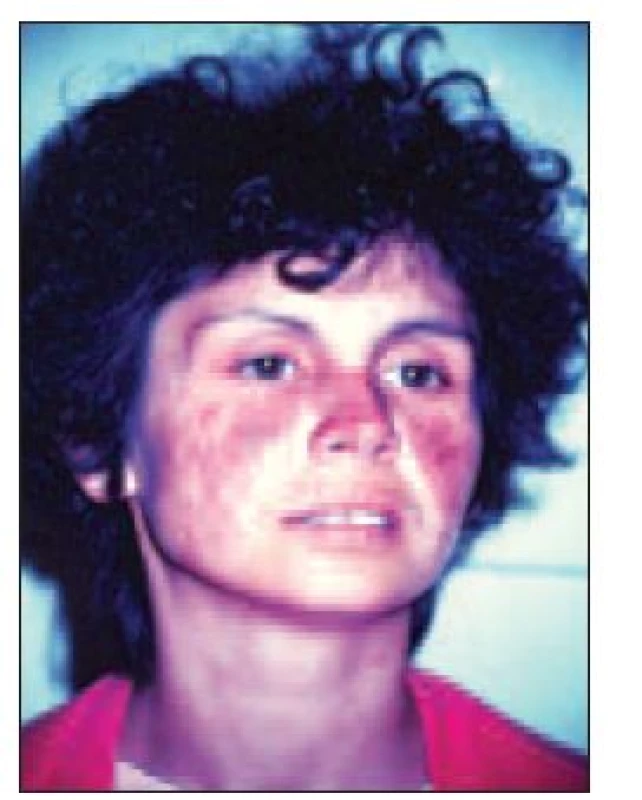
4. Subakútny kožný lupus erytematózus. 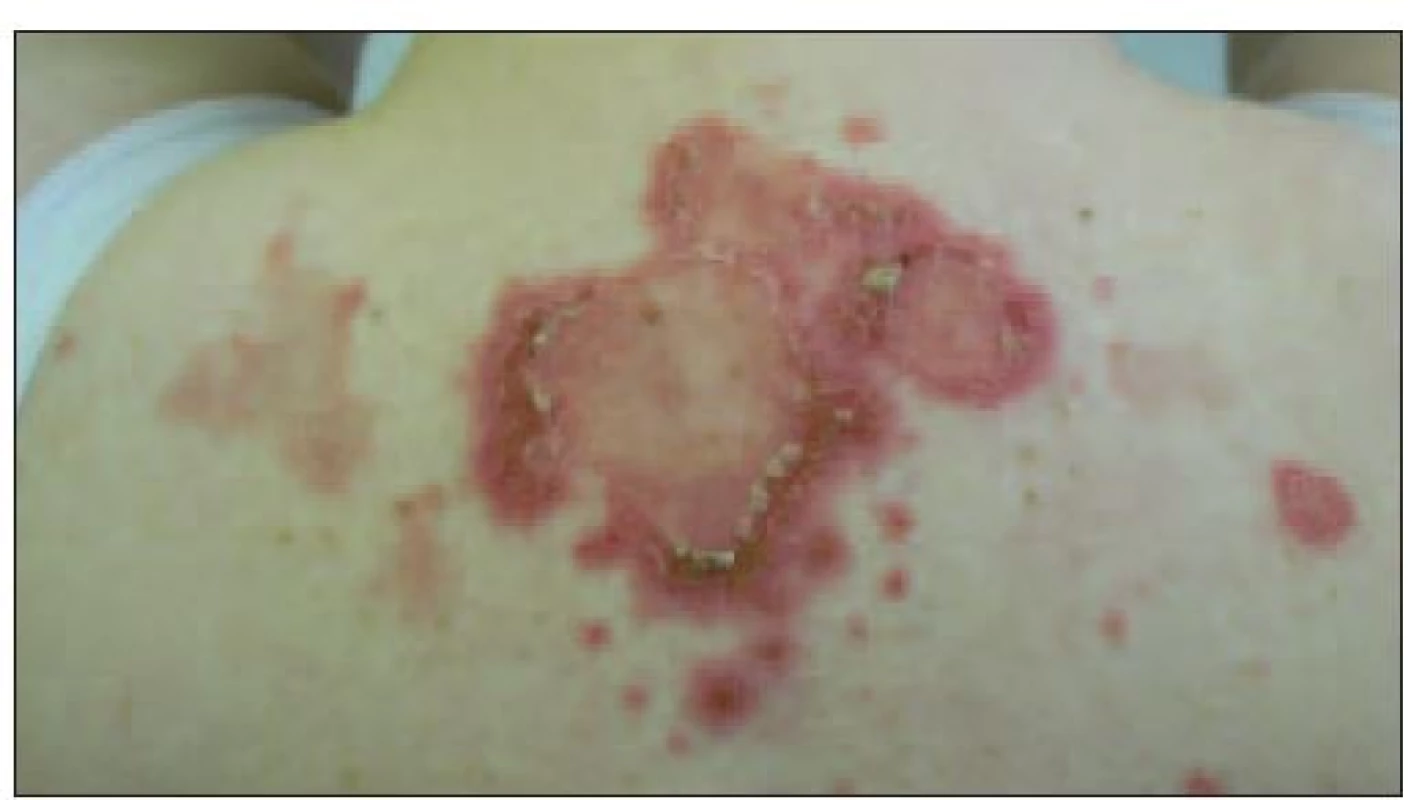
Nešpecifické kožné zmeny pri SLE
Do tejto skupiny príznakov patrí: alopécia, enantém alebo ulcerácie v dutine ústnej, panikulitída a urtikária (vyskytuje sa u 5-10 % chorých). Alopécia môže byť ložisková (obr. 5), alopetické sú aj zjazvené diskoidné morfy v kapilíciu. Panikulitída je pri SLE pomerne zriedkavá, prejavuje sa podkožnými uzlíkmi, histologicky ide o perivaskulárne infiltrácie a nekrózy v podkožnom tukovom tkanive. Pri SLE sa tento príznak označuje ako lupus profundus. Vaskulitída pri SLE môže prebiehať pod obrazom kožných ulcerácií, livedo reticularis, gangrén na prstoch rúk alebo nôh. Za nešpecifické kožné (cievne) zmeny sa považujú aj teleangiektázie a Raynaudov fenomén.
5. Ložisková alopécia u pacientky s SLE. 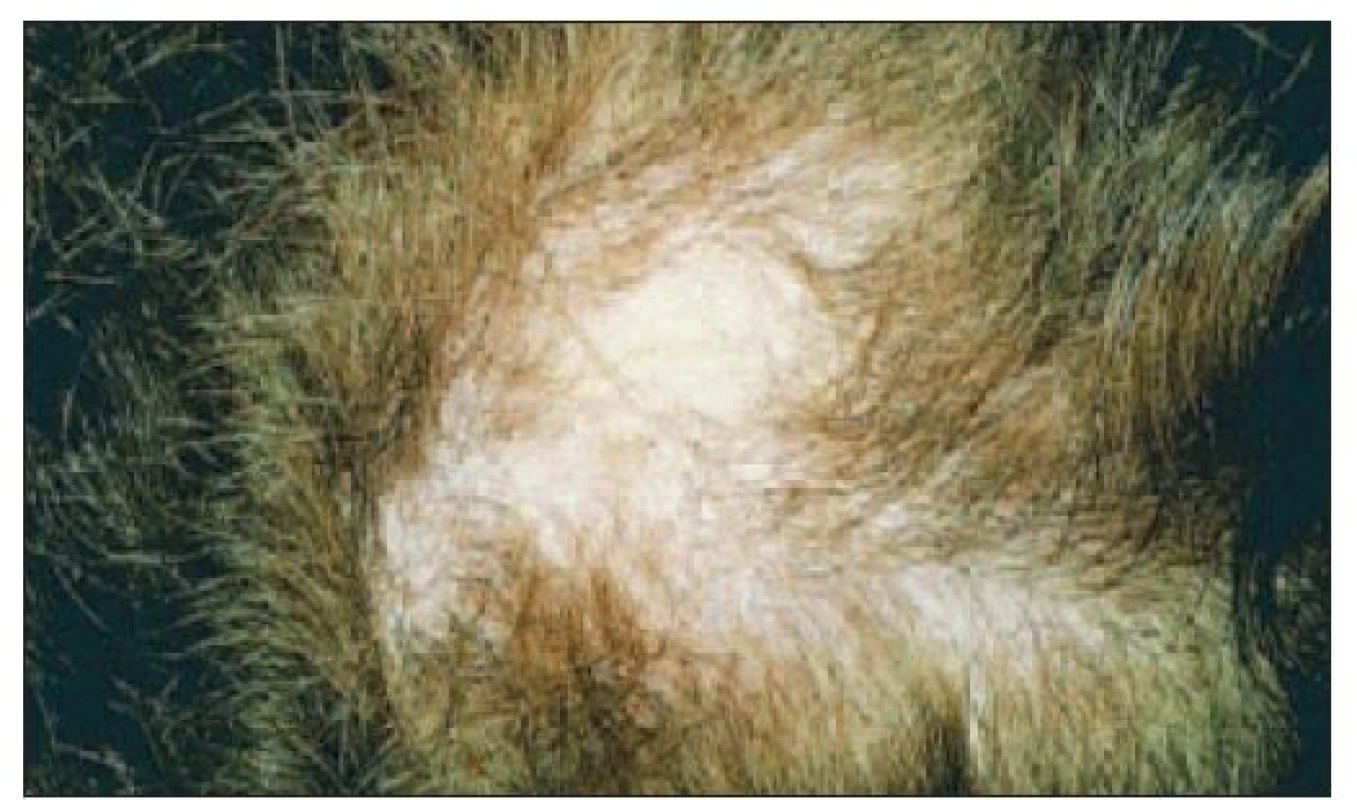
Lupusová nefritída
Klinicky manifestné postihnutie obličiek (lupus-nefritída) s proteinúriou vyššou ako 0,5 g/24 hod, erytrocytúriou a cylindrúriou má asi polovica chorých s SLE, ale podľa výsledkov histologického vyšetrenia bioptických vzoriek obličiek má každý pacient určité glomerulárne abnormality [8]. Vyšetrenie bioptickej vzorky obličiek by sa malo realizovať u všetkých pacientov s lupus-nefritídou. Cieľom biopsie je určiť typ glomerulonefritídy (GN) a tým jej závažnosť. Rozlišuje sa 6 tried glomerulonefritíd pri SLE (tab. 3). Prognosticky najzávažnejšia je difúzna proliferatívna a fokálna proliferatívna GN (s mezangiálnymi zmenami). Asi u 10 % pacientov je lupus-nefritída prvým príznakom choroby a asi u 40 % chorých je lupus-nefritída sprevádzaná nefrotickým syndrómom. Pri závažných formách, prípadne nedostatočne liečených pacientov, sa môže vyvinúť renálna insuficiencia. Prognosticky nepriaznivé znaky pre priebeh lupus-nefritídy je mladší vek pacientov, mužské pohlavie a zvýšený sérový kreatinín na začiatku nefritídy. Priaznivejšiu prognózu má nefritída s izolovanými mezangiálnymi zmenami a membránová GN.
3. Klasifikácia lupusovej nefritídy podľa komisie WHO. 
Sérozitídy
Pleuritída sa vyskytuje u 30 až 60 % chorých, často prebieha subklinicky, niekedy sa prejavuje iba pleurálnou bolesťou pri dýchaní. V autoptických nálezoch sú známky pleuritídy omnoho častejšie ako klinická a rentgenologická diagnostika. Pleuritída sa častejšie vyskytuje u starších osôb so SLE. V pleurálnom výpotku sú častým nálezom LE bunky a pozitivita ANA. Počet leukocytov v pleurálnej tekutine je stredne zvýšený.
Perikarditída sa diagnostikuje u 20-30 % pacientov so SLE. V autoptických študiích sa udáva až 60% výskyt. Echokardiograficky však možno diagnostikovať aj asymptomaticky prebiehajúcu perikarditídu.
Zriedkavejšie sa vyskytuje difúzna peritonitída, niekedy s malým ascitom. Okrem priebehu s typickými bolesťami brucha existuje aj subklinická forma peritonitídy.
Postihnutie pľúc pri SLE
Akútna lupusová pneumonitída a hemoragická alveolitída sú pomerne zriedkavé, prejavujú sa vzostupom teplôt, kašľom a hypoxémiou. Na RTG-snímke sa zisťujú škvrnité alveolárne infiltráty. Syndróm alveolárneho krvácania má podobné klinické príznaky, býva však sprevádzaný akútne vzniknutým anemickým syndrómom, ktorý je vyvolaný krvácaním do pľúc [9].
Chronická difúzna intersticiálna pneumopatia sa najčastejšie prejavuje suchým kašľom a dýchavičnosťou. Počítačovou tomografiou s vysokým rozlíšením sa zisťujú infiltáry - tzv. matnicové - ground glass. V prípade vývoja pľúcnej fibrózy sa zisťuje retikulácia - najčastejšie v dolných a stredných pľúcnych poliach. Zriedkavým a závažným nálezom je pľúcna hypertenzia, ktorá vzniká v dôsledku postihnutia ciev (pľúcna vaskulitída, trombóza, embolizácia).
Postihnutie srdca
Myokarditída sa prejavuje arytmiou, tachykardiou, kardiomegáliou a následne srdcovým zlyhaním. Väčšinou býva sprevádzaná perikarditídou. Pri endokarditíde sa zisťuje zhrubnutie chlopní a chlopňové chyby. Libman-Sachsova endokarditída (abakteriálna verukózna endokarditída) môže byť klinicky nemá, taktiež býva sprevádzaná nedomykavosťou alebo stenózou chlopní. Na postihnutí chlopní sa môže podielať zápal, fibrinoidná degenerácia, zjazvovatenie, vaskulitída alebo ruptúra šlašiniek. Koronárne artérie bývajú postihnuté akcelerovanou aterosklerózou, koronaritída je zriedkavá. U pacientov s antifosfolipidovým syndrómom pri SLE je výskyt valvulopatií vyšší ako u ostatných chorých so SLE. Pacienti s antifosfolipidovým syndrómom majú väčšie riziko koronárnej príhody. Akcelerovaná ateroskleróza je častou neskorou komplikáciou SLE, úmrtnosť na koronárnu chorobu je 9krát vyššia ako predpokladaná úmrtnosť v populácii. Vzniká v dôsledku kortikoterapie, hypertenzie, hyperlipidémie, trombembolických komplikácií a vaskulitídy.
Postihnutie tráviaceho ústrojenstva
U pacientov s vysokou aktivitou SLE sa vyskytujú difúzne bolesti brucha, nechutenstvo a nauzea. Väčšinou ide o funkčné poruchy bez organického podkladu. Môžu však byť dôsledkom peritonitídy, pankreatitídy, enteritídy alebo vaskulitídy mezenteriálnych ciev.
Postihnutie pečene
Asi u tretiny pacientov sa môže vyskytnúť hepatomegália a zvýšenie aminotransferáz. Tento typ hepatopatie pri SLE sa označuje ako nešpecifická reaktívna hepatitída. Pomenovanie lupoidná hepatitída sa nahradilo označením autoimúnna chronická hepatitída. Autoimúnna hepatitída sa môže vyskytovať ako samostatná chorobná jednotka - autoimúnne ochorenie s orgánovošpecifickými protilátkami.
Postihnutie nervového systému
Neurologické a psychiatrické prejavy SLE môžu byť rozmanité a prechodné, preto je ich diagnostika zložitá (tab. 4). Skutočný výskyt neuropsychiatrických prejavov závisí aj od použitých kritérií hodnotenia. Odhaduje sa, že až 2/3 pacientov so SLE majú príznaky postihnutia nervového systému [10]. Najčastejšou príčinou postihnutia CNS je nezápalová vaskulopatia alebo trombózy cerebrálnych ciev. Vaskulitída cerebrálnych ciev je zriedkavá. Možným patogenetickým mechanizmom môže byť aj poškodenie nervových buniek autoprotilátkami. Poškodenie CNS môže byť difúzne alebo ložiskové. Medzi neurologické prejavy CNS sa zaraďujú: bolesti hlavy migrenózneho typu, pohybové poruchy typu chorey, cerebelárnej ataxie a epileptiformné kŕče. Cievne mozgové príhody môžu postihnúť ktorúkoľvek oblasť CNS, preto môžu mať rozmanitý klinický obraz (hemiparézy, afázie, poruchy zraku, cerebelárne poruchy).
4. Postihnutie nervového systému pri SLE. 
Postihnutie hlavových kraniálnych nervov sa môže manifestovať nystagmom, ptózou viečka, vertigom, neuralgiou trigeminu.
Psychiatrické prejavy
Psychóza môže byť prvým prejavom SLE. Do obrazu postihnutia CNS sa zaraďuje aj depresia. Organický psychosyndróm CNS sa manifestuje poruchou pamäti, kognitívnych funkcií a poruchou mentálnych funkcií.
Periférna neuropatia môže byť motorická alebo senzitívna, závažná je transverzálna myelitída alebo mononeuritis multiplex [10].
Laboratórne nálezy
Nešpecifickým nálezom je zvýšená sedimentácia erytrocytov - prítomná takmer u všetkých pacientov s SLE. Hodnoty CRP bývajú na rozdiel od bakteriálnych infekcií zvýšené iba mierne. Preto sa hladina CRP používa ako pomocný ukazovateľ pri odlíšení medzi aktivitou choroby a bakteriálnou infekciou. Anémia sa vyskytuje asi u 2/3 pacientov. Vo väčšine prípadov ide o miernu alebo strednú anémiu, zriedkavejší je výskyt akútnej hemolytickej anémie a pozitivita Coombsovho testu. Leukopénia a lymfopénia je prítomná až u 80 % pacientov, trombocytopéniu má až 1/4 chorých.
Častým nálezom je zníženie hodnôt celkového hemolytického komplementu (CH50) alebo jeho zložiek (C3,C4). Sú jedným z ukazovateľov aktivity SLE. Zníženie komplementu je zapríčinené jeho spotrebovávaním pri tvorbe imunitných komplexov. Pri SLE sa spravidla zisťuje zvýšená hladina imunoglobulínov, najmä imunoglobulínu G a cirkulujúcich imunokomplexov.
Autoprotilátky pri SLE
Pri SLE sú obligátnym nálezom autoprotilátky proti jadrovým, cytoplazmatickým a membránový antigénom. Antinukleárne protilátky (ANA) sa vyskytujú takmer u všetkých pacientov s SLE, sú však málo špecifické, pretože sú pozitívne nielen pri iných SCHS, ale izolovaná pozitivita sa môže vyskytovať aj u zdravých osôb. Pri SLE sa spravidla vyskytuje viac druhov autoprotilátok súčasne. Pre SLE majú vysokú špecificitu najmä protilátky proti dvojšpirálovej deoxyribonukleovej kyseline (anti-dsDNA), proti antigénu Sm (anti-Sm) a proti deoxyribonukleoproteínu (anti-DNP) (tab. 5). Antihistónové protilátky sa zisťujú asi u 2/3 chorých v aktívnom štádiu choroby a pri lupuse indukovanom liekmi. Protilátky anti-Sm patria medzi malé jadrové ribonukleové častice (snRNP). Sú špecifické pre SLE, majú však nízku senzitivitu, sú prítomné iba u 10-30 % chorých. U pacientov s protilátkami anti-U1-RNP sa môžu vyskytovať príznaky iných SCHS (myozitída, artritída, Raynaudov fenomén, intersticiálna pneumopatia). Okrem toho sú anti-U1-RNP pravidelným nálezom u chorých so zmiešanou chorobou spojiva (MCTD - mixed connective tissue disease, Sharpov syndróm). Protilátky anti-Ro (anti-SSA), anti-La (anti-SSB) sú asociované so subakútnym kožným lupusom, neonatálnym lupusom a pri vrodenom deficite zložiek komplementu C2 a C4. Anti-Ro protilátky sú častým nálezom u pacientov s fotosenzitivitou, pneumonitídou a nefritídou. Protilátky proti ribozomálnemu RNP sa vyskytujú u 20-30 % chorých. Majú vysokú špecificitu pre SLE a bývajú asociované s postihnutím CNS. Reumatoidné faktory sa vyskytujú u 20-50 % pacientov so SLE. Ukazovateľmi aktivity choroby sú anti-DNP a anti-dsDNA. Pri prognosticky závažných formách SLE sa zisťujú anti-dsDNA, anti-Sm a anti-rRNP [11,12]. Časť pacientov s SLE ale i inými SCHS má aj orgánovo-špecifické protilátky: proti tyreoglobulínu, erytrocytom, trombocytom, leukocytom.
5. Autoprotilátky pri systémovom lupus erytematózus. 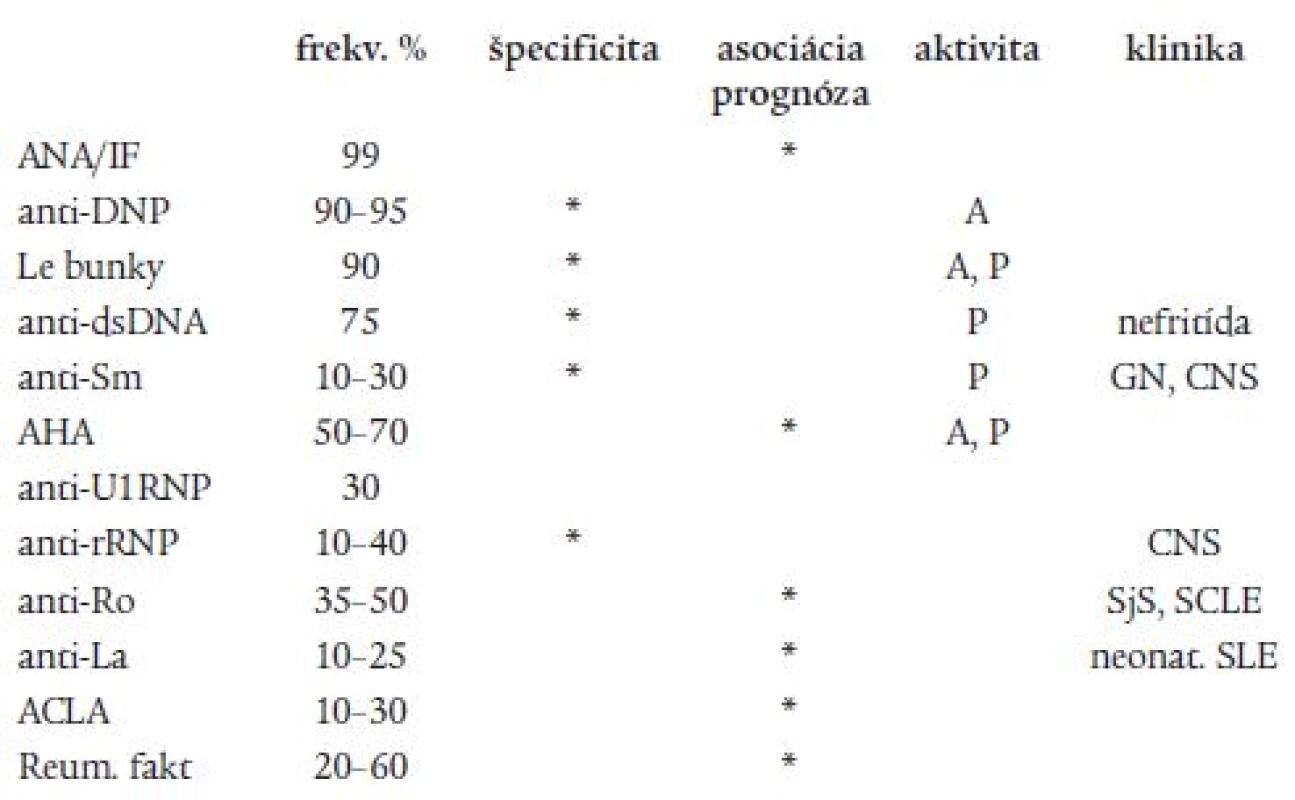
Antifosfolipidové autoprotilátky
Stanovujú sa ako lupus-antikoagulanciá alebo metódou ELISA ako antikardiolipínové protilátky alebo protilátky proti β-2-glykoproteínu I. Antifosfolipidové protilátky sa vyskytujú u 10-30 % pacientov s SLE, ale iba u časti z nich sa vyskytnú klinické príznaky antifosfolipodového syndrómu.
Klinické formy SLE
Priebeh SLE je rozmanitý, niekedy pomerne benígny - bez postihnutia životne dôležitých orgánov, zriedkavejšie je priebeh SLE závažný a môže skončiť fatálne. U časti pacientov prevažuje postihnutie kože. Variabilný klinický obraz viedol k rozčleneniu SLE na viacero subtypov (schéma 1).
Schéma 1. Subtypy systémového lupus erytematózus. 
SLE starších osôb začína vo veku nad 60 rokov a tvorí asi 10-15 % všetkých pacientov s lupusom. Vyznačuje sa pozvoľným začiatkom, častejším postihnutím pľúc, zriedkavým postihnutím obličiek a CNS a významne nižším výskytom protilátok anti-dsDNA [13], benígnejším priebehom a nižším výskytom reaktivácie. Zaznamenaná vyššia mortalita nebola v príčinnej súvislosti s SLE.
SLE pri deficite komplementového systému (najčastejšie C4 a C3 zložky) sa spája s familiárnym výskytom, častý je lupusový erytém a anti-Ro protilátky. Výskyt glomerulonefritídy a anti-dsDNA protilátok je zriedkavý, ANA protilátky môžu byť negatívne [14].
Vyskytujú sa i benígne formy SLE, bez postihnutia životne dôležitých orgánov. V popredí sú kĺbové a kožné prejavy, Raynaudov fenomén. Výskyt anti-dsDNA protilátok je zriedkavý.
Liekmi indukovaný lupus. Obraz SLE sa môže vyvinúť i po niektorých liekoch (hydralazín, prokainamid, izoniazid, metyldopa, penicilamín, chlorpromazín) (tab. 7). Pre takúto formu lupusu sú charakteristické tieto znaky [15]:
- Liečba niektorým z uvedených liekov trvajúca najmenej 1 mesiac.
- Časté artralgie, teploty, artritídy, pleuritída, zriedkavý výskyt orgánového a kožného postihnutia.
- Pozitivita ANA, LE buniek, leukopénia a humorálna aktivita. Zriedkavý je výskyt anti-Sm, anti-dsDNA, anti-Ro a anti-La protilátok.
- Klinické prejavy lupusu ustupujú po niekoľkých dňoch až týždňoch po vysadení príslušného lieku.
6. Lieky najčastejšie vyvolávajúce lupus. 
* Tučne uvedené lieky majú častejší výskyt liekmi indukovaného lupusu. SLE v detskom veku. Až 20 % prípadov SLE vzniká pred 18. rokom veku. Lupusová nefritída je u detí častejšia ako u dospelých, ale artritída a kardiopulmonálne postihnutie sa vyskytujú zriedkavejšie. Lupus neonatorum je autoimunitná choroba vyvolaná prenesením anti-Ro a anti-La protilátok z matky na plod. Má dve klinické formy: prechodný typ je charakterizovaný kožnými prejavmi a útlmom krvotvorby, trvalé postihnutie sa prejavuje poruchami prevodového systému srdca (atrioventrikulárne blokády).
SLE a tehotenstvo. SLE neovplyvňuje výraznejšie fertilitu pacientok. Tehotenstvo môže vyvolať exacerbáciu SLE - najmä v jeho ostatnom trimestri alebo po pôrode. Udáva sa asi 20% fetálna morbidita u tehotných pacientok s SLE. Najčastejšia príčina spontánnych abortov sú antifosfolipidové protilátky. Pacientky s SLE a antifosfolipidovými protilátkami by mali byť počas celej gravidity liečené nízkomolekulárnym heparínom. Tehotenstvo sa neodporúča u pacientok na imunosupresívnej liečbe, chorých s aktívnymi formami SLE či závažným postihnutím vnútorných orgánov.
Diagnostika SLE
Pri diagnostike sa používajú diagnostické kritériá z roku 1982 a doplnené v roku 1997 (tab. 6) [16]. V prípade kožných prejavov je vhodné vyšetrenie bioptickej vzorky kože, pri pozitívnom močovom náleze je indikovaná renálna biopsia. Pri postihnutí CNS je dôležité vyšetrenie EEG, NMR a psychologické testy na organické postihnutie CNS. Pri serozitíde, teplotách, pneumónii, humorálnej aktivite je potrebné vylúčiť i ostatné choroby, ktoré môžu imitovať SLE. Pri diagnostika SLE sa musí stanoviť celé spektrum autoprotilátok, iba stanovenie ANA nie je postačujúce. Pravidelné monitorovanie autoprotilátok je dôležité pri hodnotení supresie a aktivity SLE.
7. Diagnostické kritéria SLE (Tan et al 1982) [16]. ![Diagnostické kritéria SLE (Tan et al 1982) [16].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/f27b63f728b1b91cf5bcd57c37c58fb8.jpg)
Prežívanie pacientov s SLE sa v ostatných desaťročiach výrazne predĺžilo, v súčasnosti prežíva 10 rokov až 90 % pacientov so SLE [17]. Súčasťou liečby je aj monitorovanie aktivity choroby, nežiaducich účinkov liečby a prevencia relapsov. Aj po dosiahnutí primeranej supresie pretrvávajú celkové prejavy, artralgie, myalgie. Choroba si spravidla vyžaduje podávanie udržiavacích dávok glukokortikoidov a antimalarík pre možné riziko relapsov.
Infekcie a SLE
U pacientov so SLE sa vo zvýšenej miere vyskytujú infekčné komplikácie. Dôvodom je primárna porucha imunitných obranných mechanizmov pri SLE a súčasná liečba glukokortikoidmi a imunosupresívami. Môžu sa vyskytovať bakteriálne aj vírusové infekcie - najčastejšie herpes zoster, salmonelózy, infekcie gramnegatívnymi baktériami, ale i špecifické infekcie [18,19]. Infekcie sú na prvom mieste v príčinách mortality pri SLE pred kardiovaskulárnymi komplikáciami a aktivitou základnej choroby [5]. Pri aktívnom SLE a relapsoch SLE je riziko infekcií najvyššie. V prípade febrilií je potrebné pátrať po interkurentnej infekcii, zvážiť antibiotickú liečbu a sledovať parametre celulárnej imunity so zameraním na imunodeficit.
Prekryté syndrómy
Prekryté syndrómy (PS) spĺňajú súčasne diagnostické kritériá dvoch alebo viacerých SCHS, najčastejšie sú súčasťou PS polymyozitída (PM), dermatomyozitída (DM), systémová skleróza a SLE (schéma 2), najčastejšie PS sú: systémová skleróza/SLE, systémová skleróza /polymyozitída, SLE/polymyozitída. Pri SLE sa môže vyskytovať Sjögrenov syndróm alebo antifosfolipidový syndróm, vtedy hovoríme o sekundárnom Sjögrenovom syndróme alebo sekundárnom antifosfolipidovom syndróme.
Schéma 2. SLE a príbuzné choroby. 
Antifosfolipidový syndróm (AFS) sa vyznačuje prítomnosťou antifosfolipidových protilátok so žilnými a/alebo arteriálnymi trombózami, výskytom tromboembolických komplikácií, trombocytopéniou a opakovanými spontánnymi abortami. Antifosfolipidovým syndróm môže byť primárny alebo sekundárny. Sekundárny AFS sa vyskytuje pri SCHS, ale aj iných chorobách (malignity, infekčné choroby, lieky). Pre stanovenie diagnózy AFS a je potrebná prítomnosť antifosfolipidových protilátok (AFP) a aspoň jedného z nasledujúcich klinických prejavov: spontánny potrat, trombocytopénia alebo flebotrombóza. Katastrofický antifosfolipidový syndróm je akútny stav spojený s trombocytopéniou, trombotickými príhodami s postihnutím vnútorných orgánov. Pacienti s AFS si vyžadujú antikoagulačnú liečbu a následne dlhodobé podávanie antiagregancií.
Sjögrenov syndróm (SjS) je SCHS, ktorá postihuje predovšetkým exokrinné žľazy zápalom a poškodením ich štruktúry a funkcie. Vyskytuje sa ako samostatná chorobná jednotka (primárny SjS) alebo sprevádza ďalšie SCHS (sekundárny SjS).
Zmiešaná choroba spojiva (mixed connective tissue disease - MCTD) je syndróm patriaci medzi SCHS [20]. Pre diagnózu MCTD je podmienkou prítomnosť Raynaudovho fenoménu, difúznych (párkovitých) opuchov prstov rúk alebo sklerodaktýlie a vysokých titrov protilátok anti-U1RNP. Pri MCTD sa môžu vyskytovať aj iné klinické a laboratórne príznaky: artritída, myozitída, leukopénia, serozitída, intersticiálna pneumopatia, protilátky ANA, hypergamaglobulinémia, leukopénia, anémia. Celkove pri MCTD klinický obraz nespĺňa kritériá SLE, SSc alebo DM, ale asi u 1/3 pacientov sa MCTD vyvíja do inej SCHS - najčastejšie SSc, SLE, PM [21].
Nediferencovaná difúzna choroba spojiva (undifferentiaded connective tissue disease - UCTD). Okrem chorobných jednotiek spĺňajúcich diagnostické kritériá niektorej SCHS sa vyskytujú aj nediferencované syndrómy. Takýto syndróm sa môže klinicky prejavovať artralgiami, artritídou, myalgiami, fotosenzitivitou, Raynaudovým fenoménom, subfebriliami, laboratórne zvýšenou humorálnou aktivitou, antinukleárnoun pozitivitou, reumatoidným faktorom, leukopéniou a pod.
Syndróm podobný lupusu (lupus-like syndrome) je označenie pre klinický obraz , ktorý má klinické znaky SLE, nespĺňa však jeho diagnostické kritériá. UCTD sa taktiež môže vyvinúť do niektorej chorobnej jednotky SCHS.
Liečba a prognóza SLE
Liečba musí byť komplexná, základom je stanovenie správnej diagnózy a formy SLE. Všeobecné zásady - informácia pacienta a rodinných príslušníkov, úprava denného režimu s vylúčením fyzickej a psychickej záťaže, vyhýbanie sa vplyvu chladu, priamemu slnečnému žiareniu, riziku infekcií. U žien vo fertilnom veku je dôležité poučenie o rizikách tehotenstva [22]. Medikamentózna liečba pozostáva z podávania nesteroidových antiflogistík, glukokortikoidov, antimalarík a imunosupresív (schéma 3).
Dávka glukokortikoidov per os závisí od aktivity a závažnosti SLE. Iniciálne iba zriedka presahuje 60 mg prednizónu denne. Po dosiahnutí supresie sa dávka znižuje zvyčajne o 10 % dávky každých 14 až 21 dní. Na rýchle a účinné dosiahnutie supresie sa využíva pulzná liečba (PL) metylprednizolónom v dávke 500 mg až 1 g 3 dni za sebou alebo ob deň. Pulznú liečbu možno podávať opakovane. Udržovacie dávky glukokortikoidov závisia od aktivity a závažnosti základnej choroby, zvyčajne sa udržujú medzi 5 až 15 mg prednizolónu denne.
Antimalariká (chlorochín, hydroxychlorochín) sú indikované u benígnejších foriem SLE s kožnými a kĺbovými prejavmi. Azatioprín je imunosupresívum, ktoré sa podáva v dávke 1 - 2 mg/kg/deň u pacientov s orgánovým postihnutím.
Cyklofosfamid je v liečbe SLE účinnejší ako azatioprín alebo monoterapia glukokortikoidmi. Miesto perorálnej liečby cyklofosfamidom v dávke priemerne 1 mg/kg/deň sa v súčasnosti uprednostňuje PL cyklofosfamidom i.v. v dávke 0,5-1 g/m2 každý mesiac (pol roka) potom každé 3 mesiace. Účinnosť perorálnej a PL je približne rovnaká. PL cyklofosfamidom má rýchlejší nástup účinku, nižší výskyt leukopénie, hepatopatie, hemoragickej cystitídy [23]. Pulzná liečba cyklofosfamidom sa môže kombinovať s antimalarikami, cyklosporínom A a plazmaferézou.
Cyklosporín A je indikovaný pri SLE rezistentnom na konvenčnú liečbu, s nežiaducimi účinkami alebo kontraindikáciami liečby cytostatikami, je účinný pri liečbe lupusovej nefritídy a trombocytopénie, znižuje klinickú aktivitu SLE. Podáva sa v dávke 2,5-5 mg/kg/deň [24,25].
Metotrexát v dávke 7,5-15 mg týždenne je účinný predovšetkým u pacientov s artritídou, kožnými prejavmi alebo serozitídou.
Pri liečbe SLE sa ako účinný preukázal i mykofenolát mofetil (lupus-nefritída) a niektoré hormóny (danazol, dehydroepiandrosteron).
Plazmaferéza je pri SLE indikovaná v týchto prípadoch: hyperviskozita, kryoglobulinémia, trombocytopenická purpura, vaskulitída CNS, progredujúca GN, katastrofický antifosfolipidový syndróm. Väčšinou sa aplikuje v kombinácii s imunosupresívami.
Vysoké dávky intravenóznych imunoglobulínov (400 mg/kg i.v. 5 dní za sebou) sú indikované pri rezistentných formách lupus-nefritíd, postihnutí CNS, autoimúnnej trombocytopenickej pupure, antifosfolipidovom syndróme a u tehotných pacientiek s SLE.
Rituximab je monoklonová protilátka proti molekule CD20 na povrchu zrelých B-lymfocytov, jeho podanie spôsobuje depléciu B-lymfocytov. Rituximab je účinný v liečbe reumatoidnej artritídy i SLE [26].
Imunomodulanciá sú indikované iba pri SLE so sekundárnym imunodeficitom prejavujúcim sa recidivujúcimi infekciami, poruchami celulárnej imunity, s nízkou autoprotilátkovou aktivitou.
doc. MUDr. Jozef Lukáč, CSc.
www.nurch.sk
e-mail: lukac@nurch.sk
Doručeno do redakce: 30. 5. 2006
Sources
1. Arnett FC. Genetics aspects of human lupus. Clin Immunol Immunopathol 1992; 63 : 4-6.
2. Botto M, Walport MJ. C1q, autoimmunity and apoptosis. Immunobiol 2002; 205 : 395-406.
3. Johnson AE, Gordon C, Palmer R et al. The prevalence and incidence of systemic lupus erythematosus in Birmingam, Englnad. Relationship to ethicity and country of birth. Arthritis Rheum 1995; 38 : 551-558.
4. Dostál c et al. systémový lupus erytematodes. Praha: Mediprint 1997.
5. Wallace DJ, Hahn BH (eds). Dubois´lupus erythematosus. London: William and Wilkins 1997.
6. Cronin ME. Musculoskeletal manifestation of SLE. Rheum Dis Clin North Am 1988; 14 : 99-116.
7. Sontheimer RD, Gilliam JN. SLE and the skin. In: Lahita RG (ed). Systemic lupus erythematosus. New York: Churchill Livingstone 1992 : 657-681.
8. Austin HA III, Boumpas DT, Vaughan EM et al. Predicting renal outcomes in severe lupus nephritis: contributions of clinical and histological data. Kidney 1994; 45 : 544-550.
9. Segal AM, Calabrese LH, Ahmad M et al. The pulmonary manifestation of SLE. Semin Arthritis Rheum 1985; 14 : 202-224.
10. ACR AD HOC commitee on neuropsychiatric lupus nomenclature. The American College of Rheumatology nomenclature and case definitions for neuropsychatric lupus syndromes. Arthritis Rheum 1999; 42 : 599-608.
11. Venclovský J, Kafková J, Štork J. Antinukleární a anticytoplaymatické autoprotilátky u systémových revmatických onemocnení - vyšetření imunoblotingem. Čes Revmatol 1997; 5 : 71-81.
12. Horák P, Heřmanová Y, Faltýnek L et al. Autoprotilátkový profil a aktivita chroby u nemocných se systémovým lupus erythematodes. Vnitř Lék 1997; 43 : 639 - 644.
13. Tuchyňová A, Rovenský J et al. Systémový lupus erythematodes vo vyššom veku: retrospektívna štúdia. Čes Revmatol 1998; 6 : 123-126.
14. Pickering MC, Botto M, Taylor PR et al. Systemic lupus erythematosus, complement deficiency and apoptosis. Advances Immunol 2000; 76 : 227-324.
15. Price EJ, Venables PJW. Drug-induced lupus. Drug safety 1995; 12 : 283-290.
16. Tan EM et al. The 1982 revised criteria for the classification of SLE. Arthritis Rheum 1982; 25 : 1271-1277.
17. Lukáč J, Rovenský J et al. Clinical characteristic of SLE with duration over the 15 years. Reumatologia 1998; 36(Suppl): 179.
18. Pavelka K, Lukáč J, Rovenský J et al. Výskyt salmonelózy u nemocných s generalizovaným lupus erythematodes. Vnitř Lék 1984; 30 : 502-507.
19. Rovenský J, Kovalančík M, Krištúfek P et al. Problém výskytu tuberkulózy u pacientov so systémovým lupus erythematosus. Interná medicína 2002; 10 : 624-629.
20. Sharp GC, Irvin WS et al. Mixed connective tissue disease: an apparently distinct rheumatic disease syndrome associated with a specific antibody to an extractable nuclear antigen. Am J Med 1972; 52 : 148-159.
21. Lukáč J, Rovenský J, Cebecauer L et al. Diagnostika a prognóza zmiešaného syndrómu spojiva (MCTD). Rheumatologia 1995; 9 : 73-80.
22. Rovenský J et al. Klinická reumatológia. Martin: Osveta 2000.
23. Lukáč J, Rovenský J Cebecauer L et al. Intravenous versus oral cyclophosphamide therapy of systemic lupus erythematosus. Annual European Congress of Rheumatology, 12-15 June, 2002, Stockholm (Abstract): 102. Ann Rhem Dis 2002.
24. Lukáč J, Rovenský J, Rauová L et al. Long-term cyclosporin A treatment in systemic lupus erythematosus. Int J Immunoter 1996; 14 : 33-40.
25. Dostál C, Tesař V, Rychlík I et al. Effect of 1 year cyclosporine A treatment on the activity and renal involvement of systemic lupus erythematosus: a pilot study. Lupus 1998; 7 : 39-36.
26. Leandro MJ, Ehrenstein MR, Edwards JCW et al. An open study of B lymphocyte depletion in systemic lupus erythematosus. Arthritis Rheum 2002; 46 : 2673-2677.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2006 Issue 7-8-
All articles in this issue
- Problems of cardiovascular toxicity of coxibs and non-selective NSA
- Nonsteroidal antiinflammatory drugs and the kidney
- Polymyalgia rheumatica and giant cell arteritis – first results of a year-long study
- How can the autoantibody detection help in the diagnostics and evaluation of connective tissue diseases?
- Treatment of early arthritis – recommendations of EULAR
- Gastroduodenal complications associated with non-steroidal anti-inflammatory drugs in Slovak Republic: results of one-year prospective study
- Systemic lupus erythematodes
- New Trends in Diagnosis and Treatment of Systemic Sclerosis
- Antiphospholipid syndrome
- Early diagnostics of ankylosing spondylitis
- Ankylosing spondylitis – the current situation and new therapeutic options
- Pathogenesis, diagnostics and therapy of gout
- Musculoskeletal manifestations of diabetes mellitus
- Present possibilities of diagnostics and therapy of osteoporosis
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Nonsteroidal antiinflammatory drugs and the kidney
- Systemic lupus erythematodes
- Ankylosing spondylitis – the current situation and new therapeutic options
- Antiphospholipid syndrome
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career