-
Medical journals
- Career
Systémová AL−amyloidóza s dominující klinickou manifestací v trávicím traktu
Authors: R. Kroupa 1; M. Dastych 1; M. Šenkyřík 1; J. Lata 1; Petr Dítě 1; S. Hotárková 2; P. Hrobař 3
Authors‘ workplace: Interní gastroenterologická klinika Lékařské fakulty MU a FN Brno, pracoviště Bohunice, přednosta prof. MUDr. P. Dítě, DrSc. 1; Patologicko-anatomický ústav Lékařské fakulty MU a FN Brno, pracoviště Bohunice, přednosta prof. J. Mačák, CSc. 2; Radiologická klinika Lékařské fakulty MU a FN Brno, pracoviště Bohunice, přednosta prof. MUDr. V. A. Válek, CSc. 3
Published in: Vnitř Lék 2005; 51(5): 588-592
Category: Case Reports
Overview
Je popisován případ atypické manifestace systémové AL–amyloidózy sdružené s mnohočetným myelomem u 69leté ženy s dlouhodobými dyspeptickými obtížemi přičítanými chronické vředové chorobě gastroduodena. Opakovaně byla operována pro stenózu duodena. Postupně progredoval váhový úbytek a laboratorní známky těžké malnutrice a malabsorpce. Až z opakovaného odběru biopsie z chronické ulcerace žaludku byla prokázána depozita amyloidu. Stav progredoval, pacientka zemřela na přidružené infekční komplikace. Při pitvě byla prokázána masivní infiltrace amyloidem myokardu, plic, žaludku, střeva a ledvin. V kostní dřeni bylo zmnožení plazmatických buněk odpovídající mnohočetnému myelomu. Případ byl uzavřen jako primární systémová amyloidóza z lehkých řetězců (AL) při mnohočetném myelomu s klinicky dominujícím postižením trávícího traktu a malabsorpcí. Na amyloidózu je nutno pomýšlet v diferenciální diagnostice všech chronických zánětlivých změn a infiltrací žaludku i střeva. K jednoznačnému určení diagnózy je nutný nález amyloidových fibril při histologickém vyšetření.
Klíčová slova:
primární AL-amyloidóza – malabsorpční syndrom – mnohočetný myelomÚvod
Amyloidóza je onemocnění charakterizované ukládáním fibrilárního proteinu – amyloidu do extracelulární matrix různých tkání a orgánů. Dle původu amyloidu rozlišujeme amyloidózu AL (amyloid light chain) – primární, AA (acquired amyloidosis) – sekundární a vzácné familiární formy, u kterých amyloidová vlákna tvoří proteiny produkované v důsledku enzymatické mutace.
U primární AL-amyloidózy je amyloid tvořen z fragmentů v nadbytku produkovaných monoklonálních lehkých řetězců imunoglubulinů. V kostní dřeni jsou zmnoženy monoklonální plazmatické buňky produkující imunoglubuliny, které jsou amyloidogenní. Tato forma může doprovázet mnohočetný myelom. V některých případech nelze tato dvě onemocnění od sebe jednoznačně odlišit [1].
Amyloidóza sekundární vzniká na podkladě jiného primárního onemocnění s vysokou produkcí interleukinu-1, což indukuje tvorbu sérového amyloidového prekurzorového proteinu (SAA). Jeho štěpením ve fagocytech vznikají amyloidové fibrily. K sekundární amyloidóze nejčastěji vedou chronická zánětlivá onemocnění. U chorob trávicího traktu je relativně nejvyšší výskyt sekundární amyloidózy u Crohnovy nemoci, z jiných onemocnění se amyloidóza vyskytuje např. u revmatoidní artritidy, osteomyelitidy a bronchiektazií.
Klinické příznaky vyplývají z perivaskulárního a subendotelového ukládání amyloidu v postižených orgánech, někdy mohou být neúplné a pozdě vyjádřené.
U primární AL-amyloidózy jsou většinou počáteční symptomy nespecifické – únava a váhový úbytek. Další symptomy vyplývají z postižení funkce infiltrovaných orgánů. Nejčastěji bývá postižen myokard s projevy progresivního srdečního selhání, svaly jazyka s makroglosií a ledviny s proteinurií až nefrotickým syndromem. Nebývá vzácná senzitivní a autonomní neuropatie (tab. 1).
Table 1. Postižení orgánů a klinické projevy amyloidózy (dle četnosti). 
U sekundární amyloidózy se amyloid ukládá v játrech, slezině, nadledvinách, ledvinách a ve střevní stěně. Klinickému obrazu obvykle dominují příznaky primárního onemocnění a postižení ledvin. Trávicí trakt může být infiltrován amyloidem v celém průběhu od jazyka až po sliznici rekta [9].
Diagnóza amyloidózy je založena na klinickém obraze a průkazu depozit amyloidu v tkáňové biopsii. U AL-amyloidózy je nutný průkaz monoklonálních protilátek imunoelektroforézou a vyšetření kostní dřeně. V diferenciální diagnostice jednotlivých typů amyloidózy je důležitá spolupráce klinika s patologem.
Průběh nemoci je progresivní a prognóza pacientů s AL-amyloidózou je obecně špatná, medián přežití je 1 až 2 roky. Nejzávažnějším prognostickým faktorem je postižení srdce a ledvin. Masivní postižení trávicího traktu je též limitujícím faktorem, výrazně zkracujícím přežití pacienta. Prognóza nemocných se sekundární AA-amyloidózou je většinou dána průběhem a možností léčby základního onemocnění [1,4,9,10].
V léčbě amyloidózy dominují symptomatická opatření při zhoršení funkce jednotlivých postižených orgánů – např. léčba srdečního selhání, hemodialýza při selhání ledvin, nutriční intervence při malabsorpci apod. Vzácně u lokálních komplikací v oblasti trávícího traktu je možný chirurgický, nejčastěji resekční výkon.
V léčbě AL-amyloidózy bývá podávána chemoterapie kombinací melfalanu s kortikosteroidy, bohužel jen s částečným efektem. Zkušenosti s léčbou kolchicinem, dimetylsulfoxidem a interferonem-α nepřinesly jednoznačně příznivé výsledky. U vybraných pacientů se jeví slibná vysokodávkovaná chemoterapie s autologní transplantací krvetvorných buněk [1,4].
Léčba sekundární AA-amyloidózy je zaměřena na zvládnutí základního onemocnění, případně chirurgickou sanaci zánětlivého ložiska. U nejčastějších forem familiární amyloidózy je indikována transplantace jater umožňující obnovení chybějících enzymů.
Popis případu
Popisujeme případ 69leté ženy s chronickými dyspeptickými obtížemi přičítanými chronické vředové chorobě gastroduodena s komplikacemi. V 43 letech podstoupila pyloroplastiku a vagotomii pro ulceraci duodena, poté byla desítky let bez výraznějších obtíží. V předchorobí byla diagnostikována ischemická choroba srdeční a paroxyzmální fibrilace síní. Dlouhodobě užívala selektivní beta-blokátory. V posledním roce byla vyšetřena pro nechutenství a váhový úbytek v regionální nemocnici. Endoskopicky a RTG vyšetřením byly zjištěny chronické postulcerózní změny a stenóza v oblasti pyloru, a proto pacientka podstoupila další operační zákrok – gastroenteroanastomózu a enteroenteroanastomózu dle Brauna. Histologicky ze vzorků odebraných při operaci byly opakovaně prokázány jen zánětlivé změny, bez známek malignity. Dle dokumentace dostupné z regionálního chirurgického pracoviště nelze nálezy blíže specifikovat.
U pacientky nadále přetrvávaly nespecifické dyspeptické obtíže – bolesti břicha, nechutenství a sklon k průjmovité stolici. Opakovaně byla léčena širokospektrými antibiotiky a antimykotiky pro infekční komplikace. Stav pacientky se příliš nelepšil, postupně převládaly klinické i laboratorní projevy malnutrice. Po 2 měsících obtíží neřešitelných na chirurgickém pracovišti byla pacientka k došetření přeložena na naši kliniku.
Při přijetí v objektivním nálezu dominovala celková anasarka a kožní léze charakteru epidermolýzy. Pacientka se cítila slabá, bolesti neměla. Nebyla schopna dostatečného perorálního příjmu.
Laboratorní vyšetření v průběhu hospitalizace odpovídalo malnutrici – hypalbuminemie, hypoproteinemie, nízké hladiny železa, kalcia, magnézia, fosforu a stopových prvků. Krevní obraz: leu 8,2 × 109 /l, ery 2,57 × 1012/l, Hb 91 g/l, MCV 91 fl, tro 119 × 109/l, diferenciální rozpočet leukocytů byl v normě, sedimentace 40/70 byly vysvětlitelné protrahovanou malnutricí a opakovanými infekcemi. Abnormální byla proteinurie 2,8 g/l. Na EKG byla nižší amplituda kmitů v končetinových svodech, eufrekvenční fibrilace síní a nespecifické ST-T změny nad spodní a přední stěnou levé komory. Na přehledném RTG hrudníku bylo bilaterálně bazálně zastínění odpovídající drobnému fluidotoraxu a hraniční šíře srdečního stínu.
V diferenciální diagnostice bylo pátráno po možné malignitě a příčinách malabsorpce. CT břicha ukázalo nepřehledné kličky tenkého střeva, dilatované a naplněné tekutinou, bez patologického nálezu na játrech a pankreatu (obr. 1). Abdominální sonografie prokázala volnou tekutinu v dutině břišní, bez ložiskového postižení parenchymových orgánů.
Image 1. CT břicha. 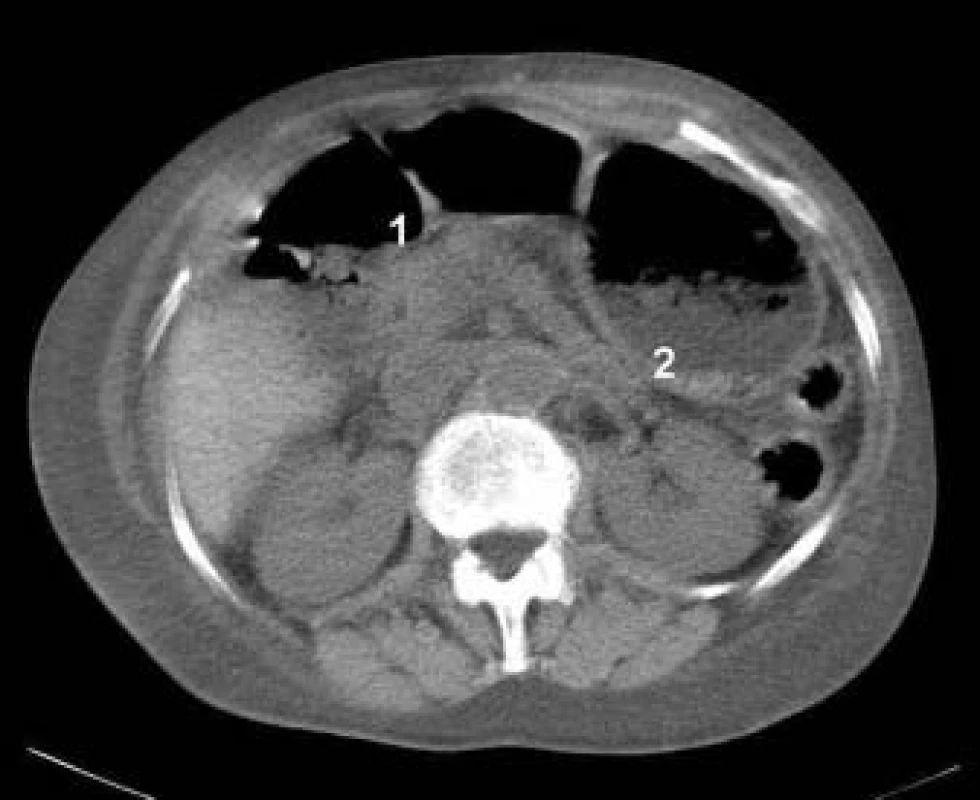
Dilatované střevní kličky naplněné tekutinou (1), špatně přehledné. Lehce zesílená stěna žaludku (2). Vyšetření protilátek proti gliadinu, endomysiu, kravskému mléku a autoprotilátek na systémová onemocnění bylo negativní. Enteroskopické vyšetření s odběry sliznice tenkého střeva k průkazu možné Whippleho choroby či infiltrujícího onemocnění nebylo možno aktuálně provést.
Pacientce byla podávána kombinovaná enterální a parenterální výživa. Navzdory zavedené terapii se její stav horšil, opakovaly se infekční komplikace – bronchopneumonie a uroinfekce. Rozhodujícím vyšetřením pro diferenciální diagnostiku byl až opakovaný odběr sliznice z ulcerace žaludku. Histologicky byla prokázána granulační tkáň s drobnými depozity amyloidu (obr. 2). Stav byl komplikován respirační insuficiencí a dechovou a oběhovou zástavou. Pacientka byla resuscitována, napojena na řízenou ventilaci, nutná byla podpora oběhu katecholaminy. Echokardiografickým vyšetřením byla zjištěna významná srdeční dysfunkce (EF 40 %) s poruchou kinetiky stěn levé komory, významnou mitrální a trikuspidální regurgitací, dilatovaná levá síň. Nebyla prokázána dilatace či ztluštění stěny srdečních komor ani perikardiální výpotek. V dalším období byla podávána opět antibiotika, parenterální výživa, při krvácivých projevech bylo nutné hrazení krevními deriváty. Postupně se vyvinulo multiorgánové selhání a pacientka po několika dnech zemřela.
Image 2. Žaludek – biopsie. 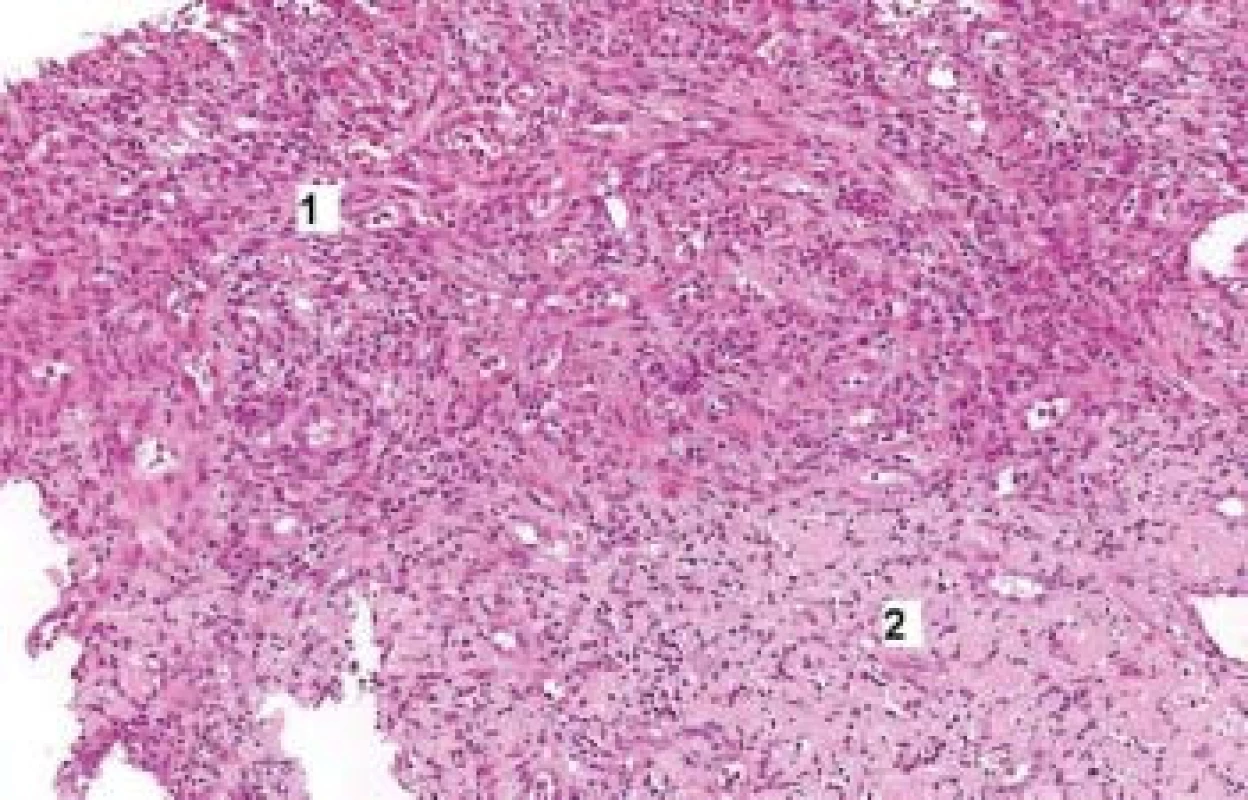
Biopsie ulcerace z oblasti antra: granulační tkáň prostoupená zánětlivými elementy (1). Fokusy nodulárních hmot charakteru amyloidu (2). Barvení hematoxylin-eozin. Zvětšení 40×. Imunoelektroforéza bílkovin séra a moči byla kompletizována až po úmrtí pacientky, s nálezem monoklonálních κ řetězců v séru i moči, hypoproteinemie, hypalbuminemie.
Pitevní nález potvrdil předpokládanou infiltraci amyloidem v mnoha orgánech – plicích, ledvinách, žaludku, střevech a myokardu (obr. 3). V kostní dřeni bylo nalezeno významné zmnožení plazmatických buněk splňující kritéria mnohočetného myelomu (obr. 4). Pacientka podlehla infekčním komplikacím – hnisavé bronchopneumonii a perikarditidě. Dalším nálezem byla arterioskleróza koronárních arterií a difuzní myofibróza myokardu bez větších nekrotických ložisek.
Image 3. Střevo – kolon, autopsie. 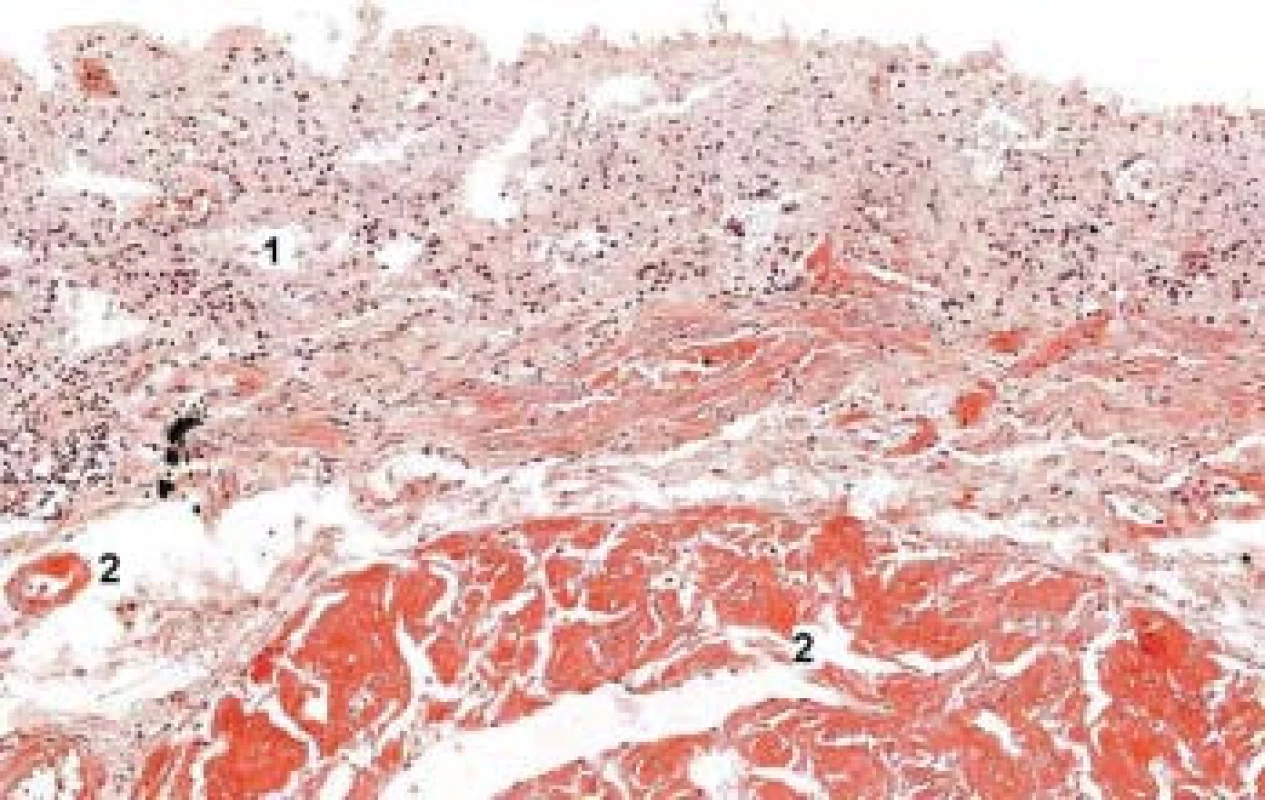
Autolytické změny (1), depozita amyloidu v submukóze, ve stěně cév a v ložiscích mimo ně (2). Barvení kongo–červení, amyloid zvýrazněn. Zvětšení 40×. Image 4. Kostní dřeň – autopsie. 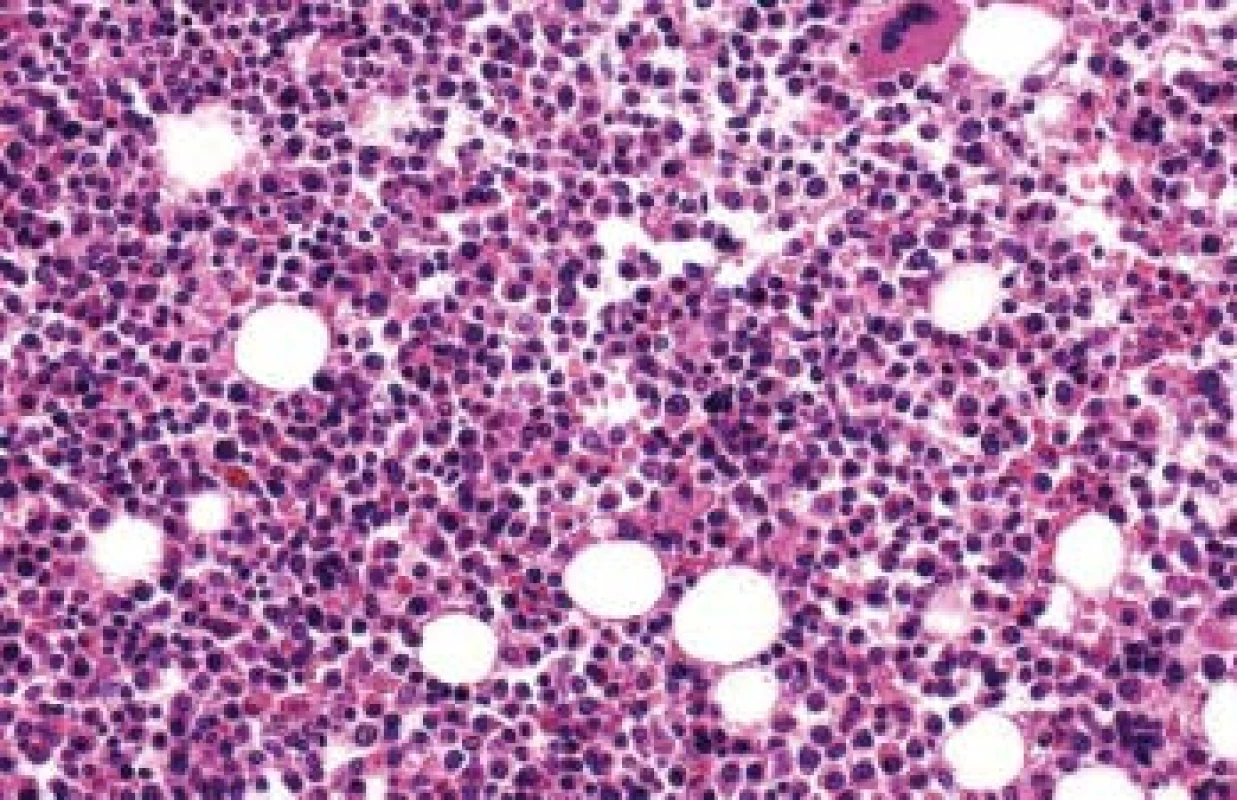
Intersticiální infiltrace cca ze 70 % středně zralými plazmatickými buňkami, mnohočetný myelom. Barvení hematoxylin-eosin. Zvětšení 80×. Diskuse
Amyloidóza patří k méně častým onemocněním – incidence v Evropě je odhadována na 0,7–1 %. AL-amyloidóza převažuje v poměru 2 : 1. Vzhledem k postižení různých orgánů se s ní setkávají mnozí specialisté z oborů vnitřního lékařství – hematologie, onkologie, nefrologie, kardiologie, revmatologie. Dominující klinická manifestace v trávicím traktu přivádějící pacienta primárně na gastroenterologii je snad nejméně častá. Na našem pracovišti zabývajícím se komplexní diagnostikou a léčbou chorob trávícího traktu byly v průběhu posledních 4 let zaznamenány jen 2 případy, u kterých jako primární příčina obtíží byla diagnostikována AL-amyloidóza [7].
Diagnostika amyloidózy je často obtížná a zdlouhavá, k definitivní diagnóze je nutný bioptický průkaz infiltrace amyloidem. Trávící trakt je relativně dostupný pro odběr vzorků, nejčastěji z oblasti rekta. Alternativou je odběr vzorků z podkožní tukové tkáně břicha [1,10]. Přesto v našem případě nebyla infiltrace amyloidem prokázána při opakovaných odběrech z oblasti chronické ulcerace žaludku, a to ani z operačního preparátu. Lze předpokládat rychlou progresi onemocnění při celkovém zhoršování stavu pacientky a nedostatečnou hloubku odebíraných vzorků při nadměrné a rychlé tvorbě granulační tkáně.
Symptomatické postižení trávicího traktu s rozvinutou malabsorpcí u primární systémové amyloidózy je vzácné (5 %), častější je jen asymptomatický nález amyloidu v biopsii z trávicí trubice [10]. Klinicky se projevuje nejčastěji jako průjem, nechutenství a slabost a značný váhový úbytek.
Endoskopický obraz při postižení trávícího traktu amyloidem může být velmi různorodý. Makroskopicky zvlnění sliznice, obraz zánětu, ulcerací a erozí, až k prominujícím masám. V případě jinak nevysvětlitelné malabsorpce je žádoucí odběr histologie nejlépe z duodena či jejuna při enteroskopii [6].
Infiltrace trávicího traktu amyloidem může být zdrojem život ohrožujícího krvácení či střevní obstrukce [7,8].
Kromě endoskopických metod je možno v diagnostice využít i jiné zobrazovací metody – ultrasonografii, enteroklýzu a CT vyšetření střev. Nálezy nejsou specifické, mohou být i zcela normální, z patologických nálezů bývá nejčastější zesílení střevní stěny a/nebo dilatace střevních kliček [2].
Stanovení správné diagnózy trvá obvykle mnoho měsíců. Prognóza pacientů s převládajícím postižením trávícího traktu je špatná, stejně jako u postižení jiných orgánů. Medián přežití není delší než 1 rok [5].
V našem případě klinicky nepřevládalo postižení srdce či ledvin, jak bývá typické u primární AL-amyloidózy [3].
Pro diagnostiku mnohočetného myelomu jsou stanovena přesná arbitrární kritéria [1]. Při retrospektivním hodnocení námi popisovaného případu neměla pacientka během života žádné typické symptomy tohoto onemocnění, které by si vyžádaly časnější cílené vyšetřování. Z laboratorních vyšetření bylo důležité potvrzení přítomnosti monoklonálních imunoglubulinů v séru i moči a abnormity v krevním obraze, na kterých se jistě přítomnost myelomu podílela. Za života pacientky nebyla zjištěna žádná osteolytická ložiska.
Ani časnější záchyt infiltrace trávícího traktu amyloidem by v námi popisovaném případu asi nezlepšil možnosti léčby a další prognózu pacientky.
Závěr
V článku byl popsán případ atypické manifestace primární amyloidózy. Při dominujícím postižení trávícího traktu mohou vzniklé symptomy překrýt ostatní projevy choroby, a tak stanovení správné diagnózy může být obtížné a pozdní. Na amyloidózu je nutno pomýšlet v diferenciální diagnostice všech chronických zánětlivých změn a infiltrací žaludku i střeva amalabsorpčního syndromu. K jednoznačnému určení diagnózy je nutný nález amyloidových fibril při histologickém vyšetření. V případě negativního či nejednoznačného bioptického nálezu je nutno vzorky odebírat opakovaně.
MUDr. Radek Kroupa
www.fnbrno.cz
e-mail: rkroupa@fnbrno.cz
Doručeno do redakce: 12. 7. 2004
Přijato po recenzi: 9. 10. 2004
Sources
1. Adam Z, Vorlíček J et al. Hematologie II. Přehled maligních hematologických nemocí. Praha: Grada Publishing 2001.
2. Araoz PA, Batts KP, Mac Carty RL. Amyloidosis of the alimentary canal: radiologic-pathologic correlation of CT findings. Abdominal Imaging 2000; 25 : 38–44.
3. Brychta T, Pařenica J, Zatočil T et al. Restriktivní kardiomyopatie jako projev primární amyloidózy. Vnitř Lék 2004; 50 : 66–71.
4. Falk RH, Comenzo RL, Skinner M. The systemic amyloidozes, review article. N Eng J Med 1997; 337 : 898–909.
5. Hayman SR, Lacy MQ, Kyle RA et al. Primary systemic amyloidosis: a cause of malabsorption syndrome Am J Med 2001; 111 : 535–540.
6. Hurlstone DP. Iron–deficiency anemia comlicating AL amyloidosis with recurrent small bowel pseudoobstruction and hindgut sparing. J Gastroenterol Hepatol 2002; 17 : 623–624.
7. Husová L, Lata J, Hušek K et al. Primární amyloidóza jako neobvyklá příčina krvácení z trávicího ústrojí. Čes a Slov Gastroent 2000; 54 : 112–116.
8. Chang SS, Lu CL, Tsay SH et al. Amyloidosis–induced gastrointestinal bleeding in a patient with multiple myeloma. J Clin Gastroenterol 2001; 32 : 161–163.
9. Klener P et al. Vnitřní lékařství. Praha: Galén, 2. vydání, 2001.
10. Kyle R, Gertz MA. Primary systemic amyloidosis: clinical and laboratory features in 474 cases. Seminars in Hematology 1995; 32 : 45–59.
11. Peny MO, Debongnie JC, Haot J et al. Localized amyloid tumor in small bowel. Dig Dis Sci 2000; 45 : 1850–1853.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2005 Issue 5-
All articles in this issue
- Prevence žilní trombózy a plicní embolie na interním oddělení
- Příčina klinických projevů chronické žilní nedostatečnosti u pacientů s nadváhou a obezitou
- Urgentní endoskopická papilosfinkterotomie u osob starších 70 let
- Prietok cez portálnu vénu a kongestívne poškodenie pečene u chorých s pokročilým srdcovým zlyhávaním
- Katetrová ablace atrioventrikulární nodální reentry tachykardie (neinvazivní možnosti diagnostiky, okamžité a jednoroční výsledky sledování skupiny 40 nemocných s provedenou radiofrekvenční ablací v roce 2002)
- Vazospastická angina pectoris – patogeneza, diagnostika a léčba
- Prodloužené podávání nízkomolekulárních heparinů v prevenci pooperační trombózy
- Genetické testy v predikcii účinnosti a toxicity chemoterapie u onkologických pacientov
- Pneumologická problematika pacientů s diabetes mellitus
- Obstrukční spánková apnoe, hypertenze a erektilní dysfunkce
- Lokalizace zdroje recidivujícího krvácení v tenkém střevě u hemoragické hereditární teleangiektazie pomocí scintigrafie s in vivo označenými erytrocyty pomocí 99mTc−pertechnetátu
- Systémová AL−amyloidóza s dominující klinickou manifestací v trávicím traktu
- Naše zkušenosti s léčbou membranózní nefropatie cyklosporinem
- Akútna myokarditída, výskyt, diagnostika a liečba v spádovej nemocnici
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Akútna myokarditída, výskyt, diagnostika a liečba v spádovej nemocnici
- Vazospastická angina pectoris – patogeneza, diagnostika a léčba
- Naše zkušenosti s léčbou membranózní nefropatie cyklosporinem
- Pneumologická problematika pacientů s diabetes mellitus
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

