-
Medical journals
- Career
Chronická kritická končetinová ischemie: distální revaskularizace vs distální revaskularizace s volným svalovým přenosem
Authors: B. Zálešák 1; P. Tošenovský 2; I. Čižmář 3; J. Zapletalová 4; M. Šimek 5
Authors‘ workplace: Klinika popálenin a rekonstrukční chirurgie Lékařské fakulty MU a FN Brno, pracoviště Bohunice, přednosta prof. MUDr. Pavel Brychta, CSc. a oddělení plastické a estetické chirurgie FN, Olomouc, přednosta MUDr. Pavel Hartl 1; Klinika transplantační chirurgie IKEM, Praha, přednosta doc. MUDr. Miroslav Ryska, CSc. 2; Oddělení úrazové chirurgie, FN Brno, pracoviště Bohunice, přednosta doc. MUDr. Michal Mašek CSc. 3; Ústav biofyziky a biometrie Lékařské fakulty UP, Olomouc, přednosta prof. Ing. Jan Hálek, CSc. 4; Kardiochirurgická klinika Lékařské fakulty UP a FN, Olomouc, přednosta doc. MUDr. Petr Němec, CSc. 5
Published in: Vnitř Lék 2005; 51(3): 292-298
Category: Original Contributions
Overview
Studie srovnává 3leté výsledky léčby u 2 skupin pacientů s kritickou končetinovou ischemií:
skupinu A – 21 pacientů léčených pouze pedálním bypassem se skupinou B – 17 pacientů léčených pedálním bypassem a volným mikrochirurgickým svalovým přenosem krytým dermoepidermálním štěpem. Primární/sekundární jednoletá průchodnost byla v první skupině 64,7/82,4 % a 54,5/81,8 % ve druhé skupině. Zhodnocením průchodnosti ke konci studie pomocí analýzy přežití spolu s konstrukcí Kaplan-Meierových křivek přežití a long-rank-testem nebyl prokázán signifikantně významný rozdíl mezi oběma skupinami (p = 0,14). Statisticky významné rozdíly nebyly zjištěny ani v počtu recidiv, amputací a úmrtí. Přestože kombinovaný výkon klade nesrovnatelně vyšší nároky na chirurgický tým, pro pacienta představuje podstatně vyšší zátěž a je prováděn v podmínkách rozsáhlejšího periferního postižení končetiny než pouhý pedální bypass, není spojen s vyšším počtem recidiv, amputací ani mortalitou. Je neospravedlnitelné odepírat tento výkon pacientům v pokročilém věku s přidruženými chorobami a zdůvodňovat to možnými riziky takto náročného výkonu. Pedální bypass a přenos svalu je pro tyto pacienty poslední možností záchrany končetiny a zachování bipedální chůze.Klíčová slova:
kritická ischemie – pedální bypass – volný svalový lalok – záchrana končetinyProblematika
Ateroskleróza je chronický progredující proces, který postupně zhoršuje prokrvení cílových tkání. Jak postupně dochází k progresi onemocnění a narůstání plátů, vyčerpávají se kompenzační možnosti kolaterální cirkulace a rozvíjí se tkáňová ischemie a onemocnění se klinicky manifestuje. Nejzávažnější stupeň arteriosklerotického postižení končetinové cirkulace je označován jako chronická kritická končetinová ischemie (ChKKI). Jedná se o stav, kdy periferní tkáně nejsou dostatečně oxygenovány a dochází k rozvoji nehojících se defektů a gangrény. Kriticky ischemická končetina je vždy bezprostředně ohrožena amputací. Vzhledem k tomu, že po jednostranné vysoké amputaci je riziko vzniku kritické ischemie na druhé končetině do dvou let až 50 % [5,6], je nutné usilovat o záchranu každé končetiny ohrožené amputací. Jedinou efektivní léčbou vedoucí k záchraně končetiny je účinná revaskularizace – pedální bypass samotný nebo v kombinaci s volným svalovým přenosem. Zjistit, zda jeden nebo druhý způsob léčby zaručuje superiorní výsledky nebo větší procento komplikací, bylo cílem naší tříleté studie.
Cíl studie
Během 3letého období 2001–2003 bylo cílem porovnat výsledky interdisciplinární léčby 2 skupin pacientů s kritickou končetinovou ischemií léčených rozdílným způsobem. Skupinu léčenou distální revaskularizací a malým amputačním výkonem (nízkou amputací) se skupinou léčenou distální revaskularizací a volným svalovým přenosem krytým dermoepidermálním štěpem. Léčba probíhala na Klinice popálenin a rekonstrukční chirurgie LF MU a FN Brno, pracoviště Bohunice, a na Klinice transplantační chirurgie IKEM.
Úvod
V roce 1991 bylo v ČR provedeno více než 4 000 vysokých amputací u diabetiků [1]. Toto číslo je neakceptovatelně vysoké. Hlavní příčinou amputací těchto pacientů je těžké postižení tepen dolních končetin obliterující aterosklerózou. Ateroskleróza je dlouhodobý progredující proces, který postupně zhoršuje prokrvení cílových tkání. Tento proces predilekčně postihuje oblast Hunterova kanálu, tj. stehenní řečiště [2].
U diabetiků je obraz postižení odlišný a nejvýrazněji bývá postiženo bércové řečiště. Postižení bércového řečiště a vyšších etáží ovšem nutně neznamená i postižení pedálních tepen. Tyto bývají velmi často ušetřeny aterosklerotického procesu [3]. Nejzávažnější stupeň arteriosklerotického postižení končetinové cirkulace je označován jako chronická kritická končetinová ischemie (ChKKI).
Podle Evropské klasifikace (European Consensus) můžeme o kriticky ischemické končetině hovořit v případě, kdy je přítomna klidová bolest nebo nekróza trvající déle než 2 týdny a kdy zároveň systolický tlak na tepnách v úrovni kotníku je nižší (nebo roven) 50 mm Hg, systolický tlak na palci je 30 mm Hg a nižší [12]. Ve své podstatě jde o stav, kdy i v klidovém stavu nedostačuje arteriální zásobení postižené končetiny k pokrytí metabolických potřeb tkání. Arteriograficky tomuto stavu odpovídá rozsáhlé postižení tepenného řečiště s kritickými stenózami v některé z etáží s rozsáhlou fragmentací tepenného řečiště bez zřetelné kolaterální cirkulace.
Defekt nebo gangréna je v této situaci vždy velmi závažný stav bezprostředně ohrožující zachování končetiny [4,5,6,7,8,9,10]. Defekt nebo gangréna prakticky nemá šanci na spontánní zhojení. Veškeré lokální chirurgické pokusy končí neúspěchem a vedou ke zhoršení lokálního nálezu. Progrese lokálního nálezu si vynutí vysokou amputaci. Po jednostranné vysoké amputaci je riziko vzniku kritické ischemie a následné amputace druhé končetiny do 2 let až 50 % [5,6].
Jedinou racionální léčbou vedoucí k záchraně končetiny je efektivní revaskularizace. Někdy je možné dosáhnout revaskularizace pomocí technik intervenční radiologie. V těch případech, kdy nelze situaci řešit pomocí perkutánního výkonu, je nutné revaskularizovat chirurgicky. Pro úspěšnou revaskularizaci je nutné splnit 3 základní podmínky – dostatečně kvalitní vtok, kvalitní žilní štěp a dostatečný výtokový trakt. Vlastní revaskularizace je prováděna pomocí pedálního bypassu, nebo pedálního bypassu kombinovaného s volným svalovým lalokem Pedální bypass je chirurgický výkon, při němž je přemostěna postižená část tepenného řečiště a oxygenovaná krev je přivedena do některé pedální arterie, čímž je obnoven pulzatilní tok. U kombinovaného výkonu je pomocí bypassu revaskularizována ischemická periferie nohy a bypass současně zajišťuje vtok pro lalok.
Volný svalový lalok hraje významnou roli – kryje rozsáhlé tkáňové defekty a obnažené struktury, limituje radikalitu amputačního výkonu a jako dobře prokrvená tkáň pomáhá eradikovat přítomnou infekci. Expanduje redukovaný výtokový trakt, a tak zvyšuje průtok cévní rekonstrukcí.
Materiál a metody
Rozdělení pacientů do skupin:
Skupina A: pacienti s kritickou končetinovou ischemií, léčení pouze distální revaskularizací a drobným amputačním výkonem, s primárním uzávěrem nebo hojením per secundam.
Skupina B: pacienti s kritickou končetinovou ischemií s nedostatečným výtokovým traktem, a/nebo rozsáhlým defektem tkání, léčeni distální revaskularizací a volným svalovým lalokem, krytým dermoepidermálním štěpem.
V obou skupinách byla sledována a porovnávána: primární a sekundární průchodnost, zachování končetiny, délka hospitalizace a doba potřebná pro zahojení defektu, procento primárních zhojení (bez další intervence), recidiva a sekundární komplikace, peroperační a pooperační mortalita a délka přežívání. Z hlediska dlouhodobých perspektiv navrhnout optimální intervenční algoritmus pro záchranu končetiny u ChKKI.
Ve skupině léčené pouze pedálním bypassem bylo celkem 21 pacientů. Průměrný věk v době operace byl 69,4 (52–83) let. Průměrná doba sledování byla 13,9 (2–30) měsíců.
Ve skupině léčené pedálním bypassem a volným svalovým lalokem bylo celkem 17 pacientů. Průměrný věk v době operace byl 60,8 (49–75) let. Průměrná doba sledování byla 16,0 (1–31) měsíců.
K léčbě byli indikováni pacienti splňující kritéria ChKKI s angiografickým (DSA) nálezem fragmentovaného bércového řečiště, bez zřetelných bércových tepen nebo s nálezem jediné, těžce sklerotické tepny s kritickými stenózami (obr. 1, 2).
Image 1. Angiografie – fragmentace bércového řečiště, žádná bércová tepna. 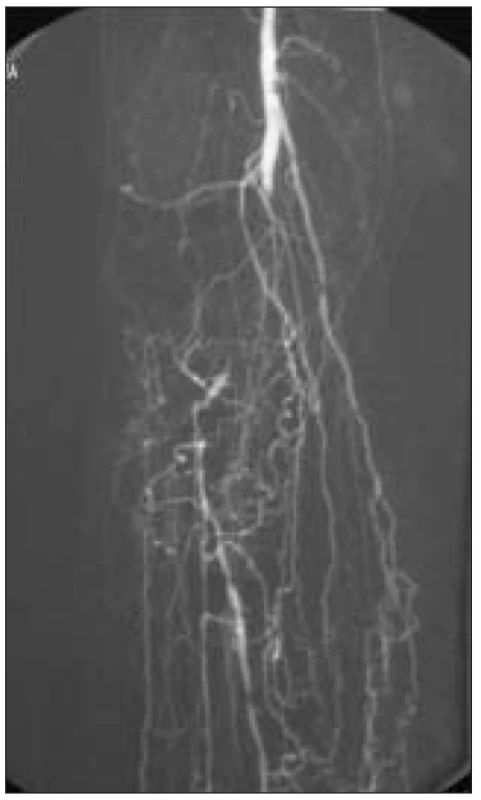
Image 2. Angiografie – fragmentace bércového řečiště, jediná bércová tepna. 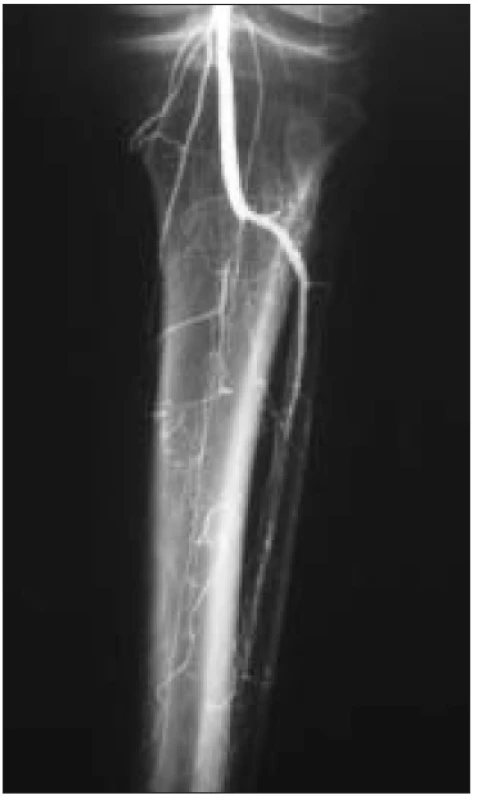
Na začátku výkonu je zrevidována distální céva (ADP, ATP) a zhodnocena vhodnost pro našití anastomózy. Hodnocen je makroskopický vzhled, průsvit tepny a zpětný tok. Je nutno nalézt alespoň 10 mm dlouhý úsek kompresibilní cévy k našití anastomózy. Peroperační revizi pedálních tepen je nutné provádět ve všech případech. Jedině tak je možné zhodnotit kvalitu cévy a ozřejmit skutečný stav v případech, kdy se pedální cévy při angiografii nezobrazují. Nezobrazení pedálních tepen při angiografii nutně neznamená jejich neprůchodnost. Následně je zrevidována popliteální arterie a rovněž zde se snažíme nalézt dostatečně dlouhý úsek tepny k provedení anastomózy, hodnotíme kvalitu přítoku arteriální krve.
Pro bypass je následně odebrána autologní žíla. Nejčastěji homolaterální vena saphena magna (VSM). V případě potřeby je odebírána vena saphena parva (VSP), kontralaterální VSP nebo jiné žíly.
Žílu je možno použít jako reverzní nebo nonreverzní nevaskularizovaný štěp, případně jako štěp in situ, při němž zůstává zachována vaskularita štěpu a žilní větve a spojky jsou podvázány z drobných incizí za pomoci angioskopu. Preferován byl angioskopicky asistovaný pedální bypass in situ. Valvulotomie byla prováděna valvulotomem (Gore Ltd.) s 2 - a 4milimetrovou hlavicí naslepo, nebo pod angioskopickou kontrolou.
Anastomóza na popliteální arterii byla našita standardním způsobem. Před naložením svorek bylo aplikováno 1–2 mg heparinu/kg hmotnosti i.v.
U bypassu samotného byla distální anastomóza našita způsobem end to side na pedální tepnu. Byla provedena nekrektomie defektu nebo limitovaná amputace s primárním uzávěrem. Při nejasné demarkaci bylo definitivní chirurgické ošetření provedeno s několikadenním odstupem.
U jednodobých kombinovaných výkonů byla distální anastomóza našita způsobem end to side a lalok byl potom přímo nebo s pomocí žilních štěpů napojen na bypass (obr. 3). Jindy byla našita side-to-side-anastomóza mezi bypassem a pedální tepnou a žilní štěp bypassu byl protažen až do periferie a zde našit přímo na tepnu laloku (obr. 4, 5). Tento způsob je výhodný zejména tam, kde je místo anastomózy velmi vzdálené od defektu. Není nutné odebírat žilní štěp a dochází ke zkrácení operačního výkonu. U dvoudobých kombinovaných výkonů byla distální anastomóza našita způsobem end to side a lalok byl přenášen s odstupem 10 až 14 dní. Žilní štěpy musely být použity k napojení (obr. 6).
Image 3. Schéma kombinovaného výkonu s end to side anastomózou. 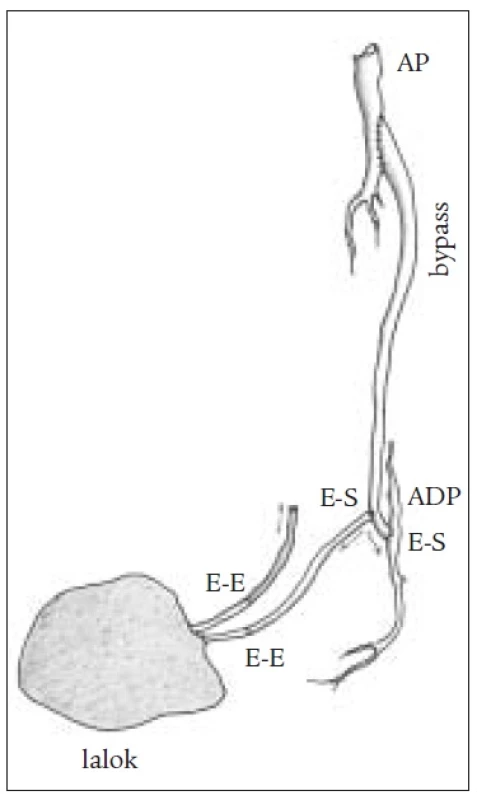
Image 4. Schéma kombinovaného výkonu se side to side anastomózou, štěp pokračuje do laloku. 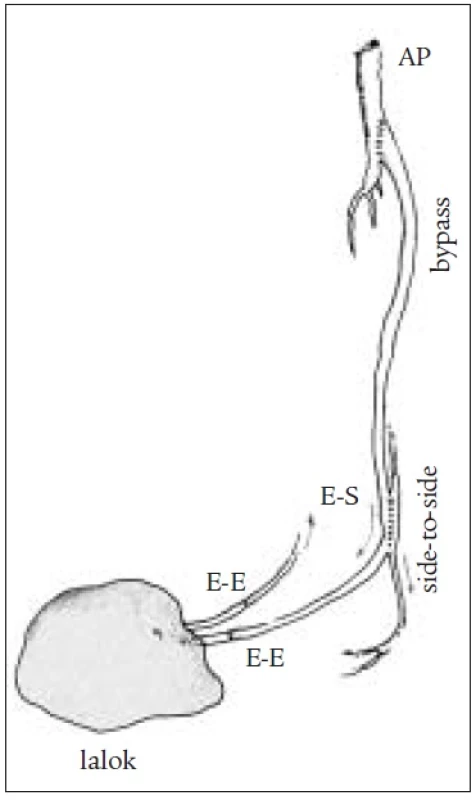
Image 5. Angiografie – pedální bypass a volný svalový lalok – side to side anastomóza. 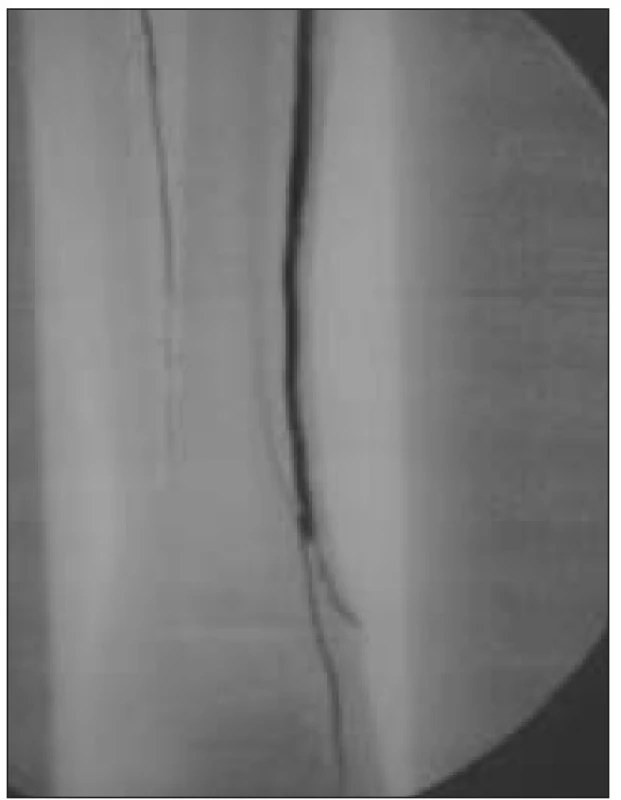
Image 6. Angiografie – pedální bypass a volný lalok přenesen v druhé době, napojení žilním štěpem. 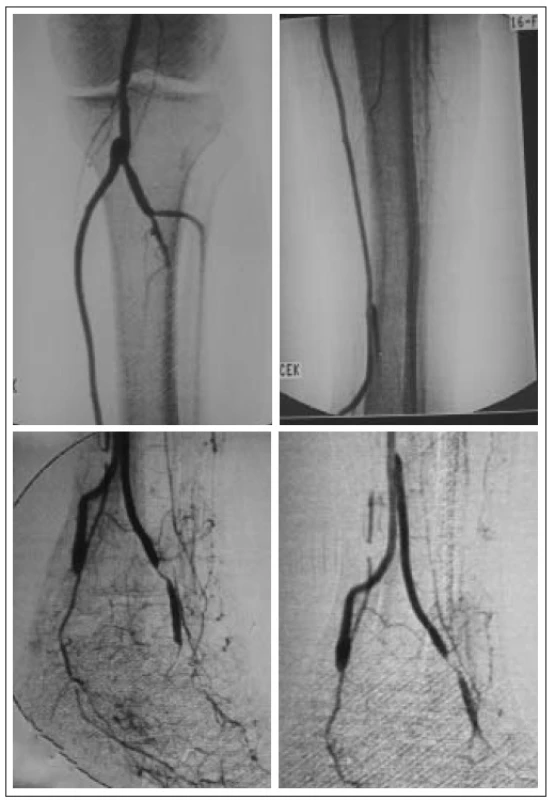
K přenosu byl v našem souboru použit m. rectus abdominis. Sval byl kryt středně silným meschovaným dermoepidermálním štěpem.
Pacienti byli umístěni na JIP nebo na ARO. Byl prováděn standardní mikrochirurgický monitoring klinicky a za pomoci ultrazvuku. Převaz laloku a rány byl proveden 5. pooperační den. Heparin byl podáván v dávce 1 000 j/hodinu kontinuálně i.v. po dobu 7–10 dní a kontrolován protrombinový čas, podle kterého bylo možno dávkování heparinu, eventuálně upravit. Potom byli pacienti převedeni na antiagregační léčbu.
Pacienti byli sledováni v 1 a 3měsíčních intervalech a sami prováděli autoobservaci bypassu a laloku.
Diabetes mellitus byl přítomen u 16 pacientů ve druhé skupině, tj. v 94,1 %. Průměrná délka trvání diabetu byla 14,5 (1–20) roků.
13 výkonů bylo jednodobých a 4 byly dvoudobé. Arteria poplitea sloužila 15krát jako vtoková céva, arteria femoralis superficialis 2krát. Jako vtok sloužila ADP 13krát, ATA 2krát a ATP 2krát. Celkem 16krát byl použit m. rectus abdominis. Jednodobých výkonů bylo provedeno 13, dvoudobé výkony byly provedeny 4. Průměrná doba operace u jednodobého kombinovaného výkonu byla 8,0 (6–12) hodin. Průměrná doba operace přenosu svalu u dvoudobého kombinovaného výkonu byla 8,25 (7–11) hodin. Ke statistickému zpracování dat byl použit statistický software SPSS, v. 10.1. Sledované skupiny pacientů byly porovnány vmetrických ukazatelích (věk v době operace, délka sledování a délka hospitalizace) pomocí Studentova t–testu pro dva výběry. Bylo zjištěno, že obě skupiny se statisticky významně liší ve věku a délce hospitalizace. U skupiny „bypass“ byl zjištěn statisticky významně vyšší věkový průměr oproti skupině „lalok + bypass“: 69,4 ± 9 resp. 60,8 ± 7,7, (průměr ± SD) (p = 0,004). U skupiny „bypass + lalok“ byla zjištěna statisticky významně vyšší délka hospitalizace oproti skupině „bypass“: 36,1 ± 19,7 resp. 17,0 ± 15,1 (průměr ± SD) (p = 0,002). V ostatních kategoriálních parametrech (průchodnost, provedení sekundárních výkonů, recidiva, amputace, exitus) byly sledované skupiny porovnány pomocí testu χ2. Na základě těchto testů bylo zjištěno, že obě skupiny se statisticky významně liší v podílu sekundárních výkonů. Ve skupině „bypass“ byly sekundární výkony provedeny u 71,4 % případů, ve skupině „lalok + bypass“ to bylo u 29,4 % případů. Tento rozdíl je statisticky významný (p = 0,01). Pro porovnání průchodnosti v obou sledovaných skupinách byla použita tzv. analýza přežití pro cenzorovaná data spolu s konstrukcí Kaplan-Meierových křivek přežití a log-rank-testem pro zjištění rozdílu mezi oběma skupinami. Výsledky log-rank testu byly nesignifikantní (p = 0,14), skupiny se v tomto parametru statisticky významně nelišily.
Obr. 7a. 65letý pacient s gangrénou pravé nohy septickou artritidou 4. MTTF-kloubu. 
Obr. 7b. Tentýž pacient, stav 3 měsíce po provedeném nonreverzním popliteo-ADP bypassu. 
Obr. 8a. 58letý pacient po amputaci 2. a 3. prstce, progredující septickou artritidou a hlubokou kavitou v plantárním prostoru. 
Obr. 8b. Tentýž pacient rok po výkonu (jednodobý nonreverzní popliteo-ADP-bypass a m. rectus abdominis). Stabilní monopedální stoj. 
Výsledky
Ve skupině léčené pouze pedálním bypassem byla primární 1letá průchodnost byla 64,7 %. Sekundární 1letá průchodnost byla 82,4 %. V průběhu sledování došlo k uzávěru 5 rekonstrukcí po 13, 18, 22, 24 a 30měsících od operace. Všechny se podařilo pomocí intervenčního radiologického výkonu zprůchodnit. Průchodnost k datu ukončení studie byla 76,2 %. Délka operace nikdy nepřesáhla 3,5 hodiny. Průměrná délka hospitalizace byla 17 (5–50) dní. Jednu končetinu bylo nutno amputovat ve stehně 3 měsíce po revaskularizaci. Důvodem byl septický stav při progresi onemocnění proximálně na bérec, při průchodném bypassu. U 2 pacientů došlo k recidivě. U 1 pacienta byla provedena akrální amputace a u druhého akrální amputace a PTA. To vedlo ke zvládnutí stavu a záchraně končetiny. 4 pacienti zemřeli: 6, 7, 20 a 24 měsíců po revaskularizaci se zachovanou a zhojenou končetinou. Do 30 dnů bylo zhojených 17 pacientů a u zbývajících čtyř došlo ke zhojení později. Jeden se nikdy nezhojil a končetina musela být amputována.
V souboru došlo k uzávěru celkem 5 rekonstrukcí, z nichž všech 5 se podařilo zprůchodnit pomocí PTA.
Ve skupině léčené pedálním bypassem a volným svalovým lalokem byla primární 1letá průchodnost 54,5 %. Sekundární 1letá průchodnost byla 81,8 %.
V průběhu sledování došlo k uzávěru 7 rekonstrukcí po 3, 4, 6, 8, 9, 10 a 12 měsících od operace. Z nich se 4 podařilo zprůchodnit PTA. Průchodnost k datu ukončení studie byla 76,5 %. Průměrná délka hospitalizace byla 36,1 (14–80) dní. Celkem 3 končetiny bylo nutno amputovat ve stehně 1, 2 a 3 měsíce po revaskularizaci. V prvním případě byl důvodem septický stav při nekróze laloku a progresi onemocnění proximálně na bérec, při průchodném bypassu. Příčinou byla infekce stopky laloku. V druhém případě se jednalo o progresi onemocnění proximálně s rozvojem septického stavu při průchodné rekonstrukci. V třetím případě došlo k uzávěru rekonstrukce dekubitu na patě a následné sepsi, která si vyžádala amputaci nad kolenem. Nezávislá chůze a chůze s malou oporou byla zachována u 11 pacientů (64 %). U 3 pacientů došlo k recidivě, z nichž u 1 nemocného musela být provedena amputace. U další došlo ke zhojení po PTA. Poslední se zhojila konzervativně. 2 pacienti zemřeli. Jednou se jednalo o časný exitus na infarkt myokardu do 30 dní od revaskularizace. Průměrná doba ke zhojení byla 93,9 (62–270) dne. V této skupině došlo ke ztrátě pouze jednoho volného laloku v důsledku žilní trombózy následkem poranění stopky. Přežití laloku dosáhlo 94,1% úspěšnosti (tab).
Table 1. Přehledná tabulka výsledků ve skupině léčené pedálním bypassem a skupině léčené pedálním bypassem a volným svalovým přenosem. 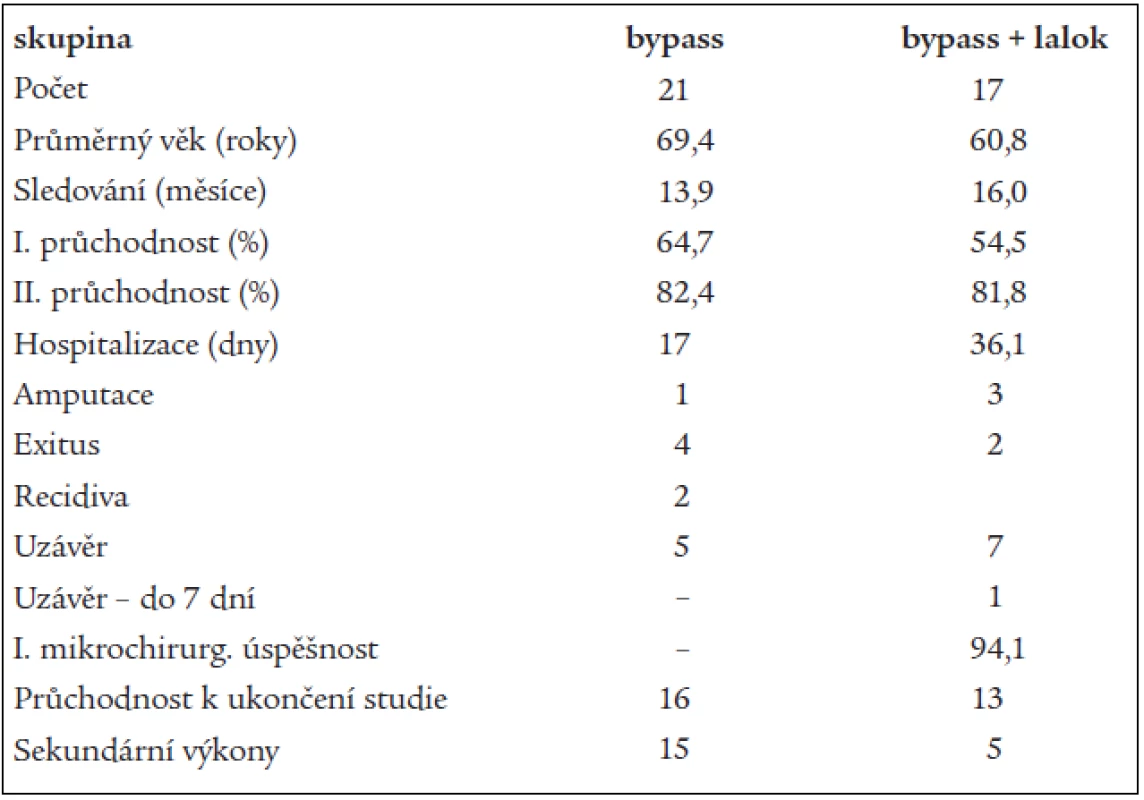
Diskuse
V posledních letech došlo k výraznému posunu v léčbě pacientů s kritickou končetinovou ischemií. Pedální bypass byl již akceptován jako standardní způsob revaskularizace a všeobecně je považován za rutinní metodu [11,12,13,14,17]. Nedůvěra v záchranu končetiny ovšem panuje u zdravotnického personálu v takových případech, v nichž je přítomen rozsáhlý defekt a došlo ke ztrátě části nohy a kde jsou obnaženy důležité struktury – zejména skelet. Rozsah postižení, nemožnost uzávěru a obava z příliš rozsáhlého kombinovaného výkonu odsuzuje tyto pacienty k vysoké amputaci.
V naší studii jsme potvrdili, že obě skupiny se statisticky významně nelišily v průchodnosti, v počtu recidiv, amputací a v procentu úmrtí. Statisticky významný byl rozdíl v délce hospitalizace, v počtu sekundárních výkonů a v průměrném věku v obou skupinách.
Pracovní hypotéza, že volný lalok povede ke zvětšení výtokového traktu, a tím i k lepším výsledkům, se nepotvrdila. Vyšší počet sekundárních výkonů ve skupině pacientů léčených bypassem logicky vyplývá z léčebné strategie: revaskularizace a následná akrální amputace až po demarkaci s odstupem několika dní. Ve skupině bypass a lalok je nutné provést dostatečnou sanaci defektu a lalok je nutno primárně krýt dermoepidermálním štěpem. Tento postup vytváří podmínky pro zhojení bez nutné další intervence.
Pacienti ve skupině bypass a lalok mají delší dobu hospitalizace vzhledem k rozsahu výkonu a náročnosti pooperačního sledování laloku. Nižší věkový průměr ve skupině bypass s lalokem je na první pohled překvapující. Pravděpodobným vysvětlením je věkový faktor ovlivňující předoperační rozhodování. Mladší pacienti jsou rozhodnější, zatímco starší jedinci spíše preferují amputaci před složitým a náročným rekonstrukčním výkonem. To může vést ke snížení věkového průměru ve skupině s lalokem.
Z našich výsledků vyplývá, že přenos svalu v druhé době je časově náročnější než jednodobý kombinovaný výkon. Obtížná preparace ve zjizveném terénu, nutnost používat žilní štěpy činí výkon časově a technicky velmi náročným. Dle našich zkušeností je jednoznačně výhodnější indikovat pacienta k jednodobému výkonu.
Jednodobý výkon umožňuje provedení distální anastomózy bypassu způsobem side to side. Žilní štěp touto anastomózou nekončí, ale je natažen až k laloku, na jehož tepnu je našit způsobem end to end. Je umožněno přímé napojení laloku, aniž by bylo nutné odebírat separátní žilní štěp. Odpadá odběr štěpu a jedna anastomóza. V případě trombózy side to side anastomózy zůstávají zachovány příznivé hemodynamické poměry pro proudění krve do laloku, který přežije a umožní zhojení defektu a neovaskularizaci ischemické periferie [15]. Tato anastomóza může být s jistou modifikací použita i u dvoudobého výkonu. V tomto případě štěp bypassu nekončí na tepně laloku, ale je přiveden do periferie k místu předpokládané stopky laloku, otočen centripetálně a našit na některou z dostupných žil. Vytváříme tak vlastně A-V-shunt/kličku, na niž po jejím rozpojení bude napojen přenesený lalok. Toto vede výraznému zkrácení operačního času.
Vysoká primární úspěšnost – přežití laloku v 94,1 % – dokazuje, že bypass zajišťuje dostatečný vtok do laloku, aniž by docházelo k častějším trombózám anastomózy, na něž by se vzhledem k přítomné ateroskleróze dalo usuzovat. Za zmínku stojí, že během pooperačního období jsme se setkali s povrchní nekrózou svalu tak, jak je v jiných odborných pracích uváděno [16]. Nízká peroperační mortalita je překvapivá vzhledem k výrazné morbiditě diabetiků a aterosklerotiků v 7. decéniu. Obavy z možného peroperačního rizika by neměly být důvodem k odepření těchto výkonů těm pacientům, pro nichž představují poslední možnost záchrany kriticky ischemické končetiny.
Závěr
Přestože integrace pedálního bypassu a volného svalového laloku nepřináší lepší výsledky stran průchodnosti a zachování končetiny, není tento náročný a komplexní výkon zatížen větší peroperační a pooperační mortalitou. Je neospravedlnitelné, aby tento výkon byl z obavy před možnými riziky odpírán pacientům v pokročilém věku, s přidruženými chorobami, pro které je toto řešení poslední možností záchrany končetiny a zachování bipedální chůze. Kombinovaný výkon je plnohodnotnou alternativou k pedálnímu bypassu všude tam, kde je nutné doplnit kožní kryt, zachránit část skeletu nohy před příliš radikální resekcí a tam, kde je nutno sanovat kostní infekci. Jedná se o skutečně poslední možnost, která funguje i tam, kde revaskularizace samotná nemá šanci na úspěch.
Projekt NJ 6855-3 byl realizován za ekonomické podpory IGA MZ ČR.
MUDr. Bohumil Zálešák
www.fnol.cz
e-mail: zalesakb@fnol.cz
Doručeno do redakce: 10. 3. 2004
Přijato po recenzi: 4. 5. 2004
Sources
1. Jirkovská A, Wosková V, Kobilková J et al. Onemocnění nohou u diabetiků a péče o dolní končetiny. Praha: IKEM 1992.
2. Gensler SV, Haimovici H, Hoffer P et al. Study of vascular lesions in diabetics, nondiabetic patients. Arch Surg 1967; 95 : 918.
3. LoGerfto FW, Coffman JD. Vascular and microvascular disease of the foot in diabetes. N Engl J Med 1984; 311(25): 1615–19.
4. Gutman M, Kaplan O, Skornik Y et al. Gangrene of the lower limbs in diabetic patients: A malignant complication. Am J Surg 1987; 154(3): 305–309.
5. Bodily KC, Burgess EM. Contralateral limb and patient survival after leg amputation. Am J Surg 1983; 146(2): 280–282.
6. Kucan JO, Robson MC. Diabetic foot infections: Fate of the contralateral foot. Plast Reconstr Surg 1986; 77(3): 439–41.
7. High RM, McDowell DE, Sawrin RA. A critical review of amputation in vascular patients. J Vasc Surg 1984; 1(5): 653–5.
8. Ouriel K, Fiore WM, Geary JE. Limb threatening ischemia in medically compromised patient: Amputation or revascularization? Surgery 1988; 104(4): 667–72.
9. European Working Group on Critical Leg Ischaemia. Second European consensus document on chronic critical leg ischaemia. Eur J Vasc Surg 1992; 6(Suppl A): 1–32.
10. Tosenovsky P, Zalesak B, Janousek L et al., Pedální bypass v léčbě ischemie diabetické nohy, Rozhl Chir 2002; 81(1): 118–21.
11. Tosenovsky P, Zalesak B, Janousek L et al. Microvascular steal syndrome in the pedal bypass and free muscle transfer? Eur J Vasc Endovasc Surg 2003; 26(5): 562–564.
12. Tošenovský P, Zálešák B, Adamec M et al. Pedální bypass v léčbě ischemie diabetické nohy. Rozhl Chir 2002; 81(1): 18–21.
13. Marusiak J, Strincl J, Rambousek Z et
al. Periferní revaskularizace dolních končetin u pacientů s kritickou končetinovou ischemií. Rozhl Chir 1998; 77(4): 179–184.
14. Zálešák B, Tošenovský P, Trupár E et al. Záchrana končetina ohrožené kritickou končetinovou ischemií kombinovaným výkonem. Bulletin HPB 2003; 11(1): 25–28.
15. Dražan L. Léčení diabetické nohy s pomocí mikrochirurgie: Závěrečná zpráva Grant IGA MZ ČR ND 5219–3.
16. Staffa R, Leypold J, Kříž Z. Význam pedálního bypassu při záchraně končetiny. Role of Pedal Bypass Grafting in Limb Salvage. Rozhl Chir 2004; 83 : 24–30.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2005 Issue 3-
All articles in this issue
- Multikomponentní automatizované odběry – nový trend v dárcovství krve
- Hyperfosfatemie jako závažná komplikace chronické renální insuficience a chronického selhání ledvin: I. Etiopatogeneze, důsledky a diagnostika
- Hyperfosfatemie jako závažná komplikace chronické renální insuficience a chronického selhání ledvin: II. Léčba
- Nové poznatky o metabolizmu železa
- Léčba starších pacientů s koinfekcí virů hepatitidy B a C
- Kuřácké návyky lékařů a lékařek v porovnání s kouřením v populaci ČR. Porovnání se stavem v roce 1991
- Chronická kritická končetinová ischemie: distální revaskularizace vs distální revaskularizace s volným svalovým přenosem
- Příčiny akutních intoxikací v průběhu jednoho roku na jednotce intenzivní metabolické péče
- Předpokládané náklady na terapii diabetes mellitus a jeho pozdních komplikací v ČR – předbě
- Diabetická kardiomyopatia
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Hyperfosfatemie jako závažná komplikace chronické renální insuficience a chronického selhání ledvin: I. Etiopatogeneze, důsledky a diagnostika
- Hyperfosfatemie jako závažná komplikace chronické renální insuficience a chronického selhání ledvin: II. Léčba
- Nové poznatky o metabolizmu železa
- Předpokládané náklady na terapii diabetes mellitus a jeho pozdních komplikací v ČR – předbě
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

