-
Medical journals
- Career
Akutní pankreatitida, obávaná diagnóza i ve starším věku
Authors: M. Berková; Z. Berka; E. Topinková
Authors‘ workplace: Geriatrická klinika 1. LF UK a VFN Praha 1; 2. interní klinika LF UP a FN Olomouc 2
Published in: Geriatrie a Gerontologie 2015, 4, č. 1: 19-25
Category: Review Article
Overview
Akutní pankreatitida je neinfekční zánětlivé onemocnění primárně vznikající v exokrinní části pankreatu. Incidence akutní pankreatitidy mírně stoupá (ve střední Evropě přibližně 20 případů/100 000 obyvatel za rok). Etiologicky se nejčastěji jedná o biliární a alkoholickou pankreatitidu. Patologicko-anatomicky probíhá akutní pankreatitida jako intersticiální edematózní pankreatitis nebo akutní nekrotická pankreatitis. Revidovaná klasifikace z Atlanty z roku 2012 rozděluje akutní pankreatitidu podle klinického průběhu do tří forem: na mírnou, středně závažnou a těžkou. K nejzávažnějším komplikacím patří multiorgánové selhání a infekce pankreatických a extrapankreatických nekróz. Z vyšetřovacích metod je nejpřínosnější ultrasonografie břicha, počítačová tomografie s aplikací kontrastní látky a vyšetření magnetickou rezonancí s cholangiopankreatografií, eventuálně endoskopická ultrasonografie. Endoskopická retrográdní cholangiopan-kreatografie (ERCP) je vymezena pro terapeutické účely při biliární pankreatitidě. Přes významné léčebné pokroky na jednotkách intenzivní péče a anesteziologicko-resuscitačních odděleních je mortalita těžké pankreatitidy s oběhovým selháním, zejména u starších polymorbidních pacientů, vysoká (≥ 50 %).
Klíčová slova:
akutní pankreatitida – systémová zánětlivá odpověď – orgánové selhání – pankreatická nekróza – mortalitaDefinice
Akutní pankreatitida je neinfekční zánětlivé onemocnění vznikající primárně v zevně sekretorické (exokrinní) části pankreatu. Diagnóza akutní pankreatitidy se opírá o klinický obraz a přítomnost alespoň dvou ze tří kritérií:
- pankreatická bolest
- alespoň trojnásobně zvýšená hladina sérových amyláz a/nebo lipáz
- charakteristický nález při zobrazovacích metodách (ultrazvukové vyšetření – UZ, počítačová tomografie s aplikací kontrastní látky – CECT, magnetická rezonance – MRI).
Incidence
V publikovaných studiích se roční incidence akutní pankreatitidy liší podle zeměpisné lokality, zejména v závislosti na konzumaci alkoholu, stravovacích zvyklostech a výskytu onemocnění žlučových cest, a pohybuje se od 5 do 70 případů na 100 000 obyvatel(1,2,3). Ve střední Evropě se objevuje průměrně 20 případů na 100 000 obyvatel za rok(4). Většina akutních pankreatitid má mírný průběh s rychlou úpravou stavu a dobrou prognózou. Avšak až jedna pětina akutních pankreatitid představuje velmi závažné onemocnění s orgánovým selháním a vysokou mortalitou (≥ 50 %)(5,6,7). Ve vyšším věku je onemocnění provázeno vyšší incidencí multiorgánového selhání i úmrtností než u mladších pacientů.
Etiologie
Nejčastější příčinou akutní pankreatitidy jsou nemoci žlučových cest se změnou tlakových poměrů, které se přenášejí do pankreatických vývodných cest s následným rozvojem tzv. akutní biliární pankreatitidy (50–70 %). Vyvolávajícím faktorem bývá choledocholitiáza nebo benigní pozánětlivá stenóza Vaterovy papily. Zatímco u žen jsou nejčastější příčinou akutní pankreatitidy žlučové kaménky, u mužů je to také abúzus alkoholu, který je celkově druhým nejčastějším etiologickým faktorem akutní pankreatitidy (25–35 %). Alkohol vede k intraacinární aktivaci pankreatických enzymů s autodigestivním působením na pankreatickou žlázu. Akutní alkoholická pankreatitida se objevuje ale jen u méně než 5 % konzumentů se spotřebou více než 50 g alkoholu denně, proto se předpokládá i součinnost dalších faktorů, jako např. genetická predispozice či kouření. Alkoholická akutní pankreatitida má charakter od diskrétních epizod až po těžkou nekrotizující pankreatitidu. Přestože maligní nádory jako příčina akutní pankreatitidy byly dříve pokládány vysloveně za diagnózu staršího věku, jejich výskyt se přesouvá do stále mladších věkových kategorií a je na ně nutno pomýšlet již u pacientů ve věku nad 40 let. Akutní pankreatitida může komplikovat také tupé poranění břicha nebo operační či invazivní výkony na žlučových cestách (10–15 %). Post-ERCP pankreatitida se rozvíjí obvykle do 6, méně často do 12 hodin od provedeného výkonu(8). Přísnější indikační kritéria a zlepšení techniky výkonu snížily výskyt této komplikace na 2–4 % všech ERCP(2,8). Relativně řídkou příčinou pankreatitidy jsou hypertriglyceridemie, léky, hyperkalcemie a hyperparathyreoidismus, vrozené anatomické anomálie (např. pancreas divisum – kdy vývodné cesty části pankreatu se nenapojují na hlavní ductus pancreaticus maior Wirsungi, ale inkriminovaná část pankreatu je drénována cestou ductus accessorius Santorini, který ústí na papila duodeni minor nad Vaterovou papilou; drobná papila minor s úzkým průsvitem může být příčinou špatného odtoku pankreatických šťáv a predisponovat ke vzniku pankreatitidy). Funkční poruchy Oddiho svěrače Vaterovy papily bývají příčinou zánětu slinivky břišní výjimečně a jen v přítomnosti dalších vyvolávajících faktorů. S primárně infekční etiologií pankreatitidy se setkáváme velmi zřídka při virové parotitidě, virové hepatitidě, AIDS, coxsackiové či protozoární infekci. Někdy se přesnou příčinu pankreatitidy nepodaří zjistit a pak hovoříme o idiopatické akutní pankreatitidě (10–30 %).
Patofyziologie a patologická anatomie
Akutní pankreatitida probíhá ve dvou fázích(10):
- časná fáze (první týden) – u mírné pankreatitidy dochází k úpravě stavu již během této časné fáze,
- pozdní fáze – u středně závažného a těžkého průběhu pankreatitidy časově navazuje na časnou fázi.
V časné fázi hraje hlavní roli uvolnění pankreatických enzymů do intersticia slinivky. Uvolněné proteolytické enzymy, lipázy a amylázy pronikají do intersticia, způsobují aktivaci cytokinové kaskády a vazoaktivních látek (bradykinin, kallidin) s promptní ztrátou tonu vazomotorů. Dochází k vazodilataci, zvýšené permeabilitě kapilár a úniku tekutiny extravazálně. Vzniká edém a zánětlivá celulizace pankreatické žlázy, peripankreatické tukové tkáně a většinou se vytvoří i peripankreatický výpotek (intersticiální edematózní pankreatitis).
Při těžším poškození pankreatické tkáně účinkem uvolněných pankreatických enzymů dochází k závažné systémové zánětlivé odpovědi. Únik tekutiny z cévního řečiště je masivní a může představovat až 40 % celkového objemu plazmy během prvních 6 hodin. Hypovolemie je potencovaná zvracením, nedostatečným příjmem a zvýšenými ztrátami tekutin perspirací. Vzniká šokový stav s rozvojem orgánového či multiorgánového selhání. Těžký systémový zánět, hypovolemie s orgánovou dysfunkcí a oběhové selhání jsou významným prediktorem mortality v časné fázi těžké pankreatitidy.
Při lehké pankreatitidě (80 % případů), která je reprezentována pouze edémem slinivky bez syndromu těžké systémové zánětlivé odpovědi, se stav upraví většinou již během časné fáze. U těžších forem pankreatitidy je však postižení tak závažné, že úplná restituce během prvního týdne není možná. Pozdní fáze akutní pankreatitidy je charakterizovaná přetrvávajícími známkami systémového zánětu anebo manifestací lokálních či dalších komplikací. V důsledku poklesu krevního tlaku s venostázou a následnou hypoxií ve splanchnické oblasti a současným natrávením pankreatické tkáně proteolytickými enzymy a lipázou dochází ke vzniku žilních trombóz, erozi cév s hemoragiemi do tkáně. Vznikají tukové a hemoragické nekrózy pankreatu. Nekrotické postižení zasahuje většinou i okolní, někdy i vzdálenější tkáně. O akutní nekrotické pankreatitidě (5–20 % případů) hovoříme při okrsku nekrózy větším než 3 cm nebo zaujímajícím více než 30 % pankreatu nebo při vzniku extrapankreatické nekrózy. Při úplné autolýze je nekrotická tkáň slinivky rozbředlá. Postupem času může podle velikosti nekrózy dojít k její vazivové přeměně nebo kolikvaci s fibrotickým ohraničením. Nekróza se začíná vyvíjet většinou během prvního týdne onemocnění a zobrazovacími metodami je zachytitelná po 5–10 dnech od začátku onemocnění. Obávanou komplikací pozdní fáze je infekce nekrotického ložiska, která signifikantně zvyšuje morbiditu a mortalitu pacientů.
Table 1. Léky s rizikem polékové pankreatitidy 
Klinický obraz
Klasifikace akutní pankreatitidy podle klinického průběhu byla revidována v Atlantě v roce 2012. Podle tohoto nového hodnocení dělíme akutní pankreatitidu do tří stupňů (tab. 2).
Table 2. Klinické formy akutní pankreatitidy – revidovaná klasifikace z Atlanty z roku 2012 
Mírná forma akutní pankreatitidy je představována edematózním postižením žlázy. Má lehký průběh bez orgánového selhání a komplikací. Středně závažné a závažné formy nelze v iniciální fázi od sebe rozlišit pro jejich stejně závažný průběh s orgánovým selháním a komplikacemi. Pokud se podaří orgánové selhání zvládnout do 48 hodin, klasifikujeme akutní pankreatitidu jako středně závažnou, pokud orgánové selhání trvá déle než 48 hodin, jedná se o těžkou formu akutní pankreatitidy.
Akutní pankreatitida vzniká náhle, často po požití jídla bohatého na tuky či alkohol. Základním příznakem akutní pankreatitidy je intenzivní bolest břicha, lokalizovaná ve středním horním epigastriu či levém horním kvadrantu, propagující se do páteře, do levého boku, někdy i do hrudníku a levé paže, takže může imitovat akutní infarkt myokardu. Bolest je trvalého charakteru a zhoršuje se polohou na zádech, úleva přichází v předklonu. Na rozdíl od jiných akutních břišních příhod se pacient nesnaží ležet v klidu, ale jeví spíše neklid s opakovanými změnami polohy. Bolest je provázena nauzeou a zvracením. Subikterus nebo ikterus je patrný při obstrukci žlučových cest či útlaku choledochu zvětšenou hlavou pankreatu. Při biliární pankreatitidě můžeme zjistit známky cholecystitidy či cholangitidy. Peritoneální dráždění většinou chybí v prvních hodinách nemoci. Téměř vždy však vzniká alespoň menší ascites, který je klinicky špatně prokazatelný, ale průkazný při zobrazovacích metodách. Při zatékání exsudátu do malé pánve způsobuje bolestivost celého Douglasova prostoru a při iritaci pobřišnice registrujeme peritoneální dráždění. Častá je zástava plynů, někdy i s rozvojem paralytického ileu. Vzácně se na kůži břicha, třísel či zad vybarvuje namodralé zbarvení při břišních hemoragiích (Cullenovo znamení při namodralém zbarvení kolem pupku). V levé polovině hrudníku se může tvořit reaktivní pleurální výpotek nebo bazální atelektáza.
U celkově závažné formy akutní pankreatitidy se již v iniciální fázi vyvíjejí známky systémového zánětu (SIRS – systemic inflammatory response syndrome = syndrom systémové zánětlivé odpovědi), který charakterizuje tachykardie (nad 90/minutu), tachypnoe (nad 20/min), hypotenze až klinický obraz šoku s oligurií a anurií a leukocytózou s posunem doleva. Použití skórovacích systémů umožní zhodnotit rizikovost pacienta (Glasgow skóre, skóre podle Ransona, viz tabulky3, 4)(3) a optimalizovat terapii. Při zvládnutí orgánového selhání do 48 hodin je mortalita pacientů podstatně nižší oproti protrahovanému multiorgánovému selhání(11).
Table 4. Modifikované Ransonovo skóre 
Pokud se stav pacienta nelepší po 7–10 dnech léčby, je nutno pomýšlet na další lokální či jiné komplikace. Souhrn komplikací akutní pankreatitidy uvádí tabulka 5. Obávanou komplikací je infekce nekrotických hmot(10). Téměř polovina případů infekce nekrotické pankreatitidy se objeví již během prvního týdne onemocnění. Příznaky infekce nekrózy však mohou být podobné jako u nekrózy sterilní (horečka, leukocytóza, vysoké CRP, prokalcitonin, orgánové selhání) a nelze je podle klinického stavu rozlišit, proto je důležitý vývoj onemocnění (nelepšení se, zhoršování). Rozvoj lokálních komplikací je indikací k vyšetření (zobrazovací metody, ve vyhrazených případech punkce tenkou jehlou za kontroly CT k získání materiálu ke kultivaci).
Table 5. Komplikace akutní pankreatitidy 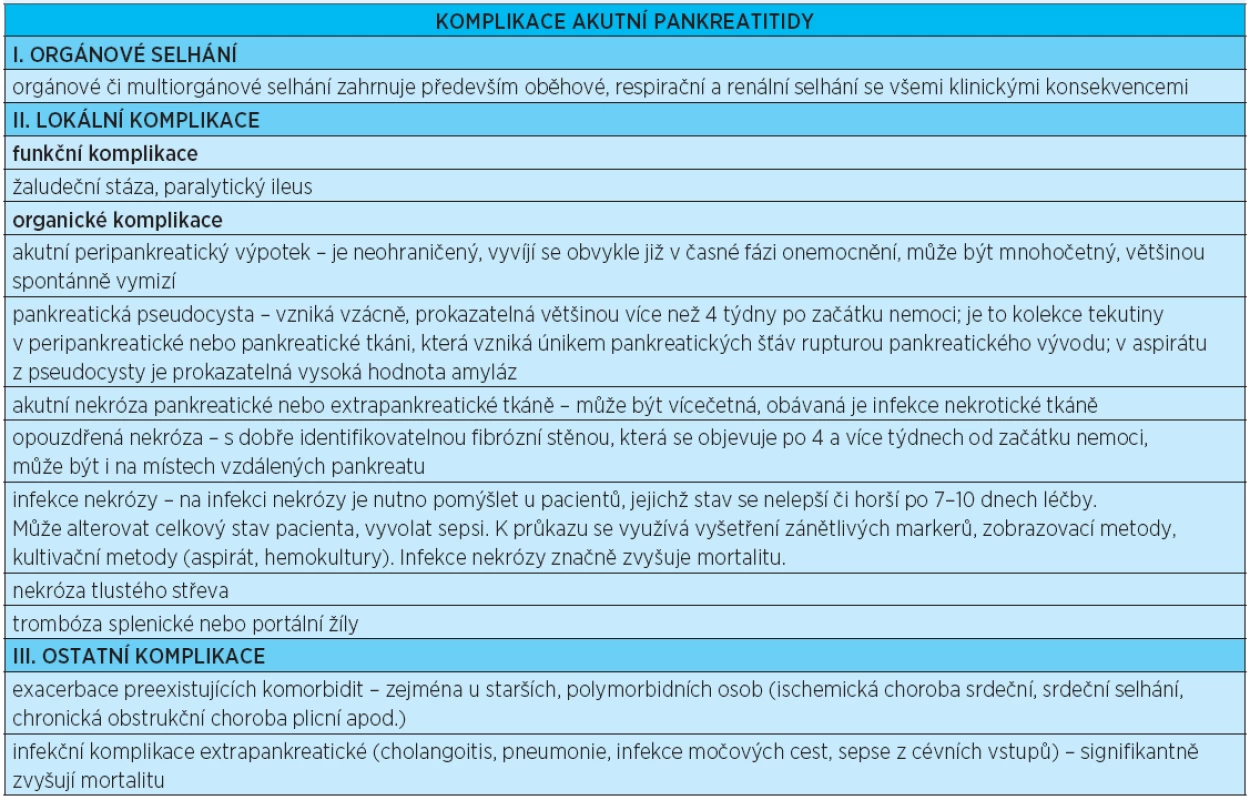
Infekční pankreatické či extrapankreatické komplikace včetně nozokomiálních (pneumonie, infekce močových cest, sepse z cévních vstupů) jsou nejčastější příčinou morbidity a mortality.
Post-ERCP pankreatitida (PEP)
Jde o pankreatitidu vyvolanou endoskopickou retrográdní cholangiopankreatografií. V souvislosti s provedením ERCP dochází u pacientů ke zvýšení amyláz až v 75 % případů, což však nutně neznamená vznik pankreatitidy(12). Hlavním příznakem vzniku post-ERCP pankreatitidy je nově vzniklá či zhoršená charakteristická bolest a alespoň trojnásobné zvýšení amyláz/lipáz nad normu v časovém odstupu nejméně 24 hodin po výkonu. Rizikovými faktory je průnik kontrastní látky do pankreatických cest, balonková dilatace nebo papilosfikterotomie jako součást výkonu, dysfunkce Oddiho svěrače a již dřívější post-ERCP pankreatitida v anamnéze(13).
Laboratorní vyšetření
Amylázy a lipázy. Vzestup amyláz v séru je u akutní pankreatitidy velmi rychlý, dá se prokázat během několika hodin po začátku a přetrvává 3–5 dní. Vzestup amyláz v moči je lehce opožděn, ale přetrvává déle. Sérové lipázy stoupají pomaleji a jejich zvýšení přetrvává déle než u amyláz. Lipáza se do moči nevylučuje. Za diagnosticky signifikantní považujeme 3násobné zvýšení normy jak pro amylázy, tak pro lipázy. Normální hodnoty amyláz (až u 20 % pacientů) nevylučují těžkou, zejména akutní alkoholickou pankreatitidu nebo pankreatitidu při hypertriglyceridemii. Naopak zvýšené amylázy můžeme najít i při onemocnění slinných žláz, snížené glomerulární filtraci, někdy i při jiných břišních zánětech, např. appendicitidě, cholecystitidě, peptickém vředu, obstrukčním nebo ischemickém ileu, gynekologických zánětech, vzácně při makroamylazemii (tvorba velkých molekulárních komplexů imunoglobulinů s amylázami). Proto vzhledem k nižší senzitivitě a specificitě se nedoporučuje vyšetřovat pouze amylázy, ale i lipázy, které mají vyšší specificitu, i když také hladina lipáz může být ovlivněna některými patologickými stavy, jako je renální insuficience či břišní extrapankreatické záněty. Zvýšená hladina lipáz byla prokázána i u diabetiků(14). Zvýšení hladiny amyláz a lipáz déle než týden budí podezření na progresi choroby nebo vznik komplikací. Pokud jsou zvýšené amylázy, ale klinický obraz budí pochybnosti o diagnóze, je vhodné doplnit vyšetření zobrazovacími metodami (CECT)(2).
Triglyceridy. V případě hypertriglyceridemie jako etiologického činitele při vzniku pankreatitidy bývá sérum mléčně bílé a hodnoty triglyceridů přesahují 11 mmol/l (1000 mg/dl). Vyšetření triglyceridemie je nutno opakovat po odeznění zánětu, protože zvýšené triglyceridy u akutní pankreatitidy mohou být, aniž by byly v příčinné souvislosti se vznikem onemocnění.
Minerály. Z minerálů má prvořadý význam stanovení kalia a kalcia. Hypokalcemie a hyperkalemie mají prognostický význam. Uvolněná lipáza štěpí ve tkáních triglyceridy na glycerol a mastné kyseliny. Uvolněné mastné kyseliny reagují s kalciem a vytvářejí se nerozpustná vápenatá mýdla. Vzniká hypokalcemie. Hyperkalemie vzniká v důsledku rozpadu nekrotických buněk nebo při snížení renálních funkcí. V dalším průběhu, jak je kalium vylučováno do moči, jeho hladina klesá.
Jaterní testy (bilirubin, alkalická fosfatáza, gamaglutamyltransferáza, transaminázy) podávají informaci o možnosti současné obstrukce žlučových cest a eventuální cholangoitidě.
Glykemie. Její zvýšené hodnoty svědčí o postižení i vnitřně sekretorické části pankreatu.
Další laboratorní vyšetření. Hladina urey, kreatininu, krevní obraz a diferenciální rozpočet, CRP (jako ukazatel zánětu nemusí být v prvopočátku zvýšen, teprve po 48–74 hodinách se zvyšuje jeho prediktivní hodnota), acidobazická rovnováha, saturace krve O₂, proteinemie, albuminemie, prokalcitonin – při suspekci na infekční komplikaci.
Zobrazovací vyšetřovací metody
Základním zobrazovacím vyšetřením je ultrazvukové vyšetření břicha, které je nejdostupnější, nejlevnější a nemá kontraindikace. CT vyšetření s kontrastní látkou nebo vyšetření magnetickou rezonancí s cholangiopan-kreatografií (MRCP) jsou vyšetření s vysokou senzitivitou a specificitou, ale nemusí být přínosná v prvních hodinách onemocnění, neboť nekrózy pankreatu se vyvíjejí v časovém odstupu. Tato vyšetření jsou důležitá při diagnostice nejasného nebo během 48–72 hodin se nelepšícího stavu. Při klinicky jasném stavu se doporučuje provést CT s aplikací kontrastní látky nebo MRI po 5–7 dnech nemoci k diagnostice možné nekrózy nebo jiných lokálních komplikací (tab. 6). V nekrotické tkáni není krevní cirkulace, proto se při aplikaci kontrastní látky nezobrazí. Na komplikující infekci může upozornit přítomnost extraluminálního plynu. MRCP je schopna odhalit kaménky v choledochu větší než 3 mm v průměru či disrupci pankreatického vývodu. U pacientů s alergií na kontrastní látku nebo se selháváním ledvin je možno zvolit MRI vyšetření bez aplikace kontrastní látky. Provedení endoskopické retrográdní cholan-giopankreatografie (ERCP) je vyhrazeno pro pacienty se známkami obstrukce žlučových cest. U pacientů s akutní pankreatitidou a současnou akutní cholangoitidou by měla být ERCP provedena do 24 hodin od přijetí. U většiny pacientů, kteří mají žlučové kameny, ale bez známek pokračující obstrukce (litiáza může spontánně odejít do střeva), není nutno ERCP provádět. Vhodnější metodou při suspekci na choledocholitiázu je v tomto případě MRCP nebo endoskopická ultrasonografie (EUS).
Table 6. CT morfologická klasifikace nekrózy po aplikaci kontrastní látky podle Balthazara (1990) 
Diferenciální diagnostika
Diferenciálnědiagnosticky je třeba odlišit: akutní cholangoitidu a cholecystitidu, perforovaný duodenální vřed, mezenteriální trombózu, disekující aneurysma aorty, cévní nebo strangulační ileus, appendicitidu, absces jater, infarkt myokardu, embolii plic, spontánní pneumotorax.
Léčba
Lehká forma akutní pankreatitidy umožňuje léčbu na standardním oddělení za sledování fyziologických funkcí a bilance tekutin s adekvátní terapeutickou reakcí podle aktuálního stavu pacienta. Těžší formy pankreatitidy se většinou manifestují již od počátku závažným průběhem. Pokud pacient přichází se známkami systémové zánětlivé reakce, je nutná komplexní terapie na jednotce intenzivní péče nebo na anesteziologicko-resuscitačním oddělení, kde je zajištěna kontinuální monitorace a úprava léčebného postupu podle aktuálně se měnícího klinického stavu pacienta a výsledků laboratorních či zobrazovacích vyšetření. Nejdůležitějším úkolem je zajistit hemodynamickou stabilitu pacienta. Pravidelně se provádí hodnocení závažnosti stavu a rizika orgánového selhání (krevní tlak a jeho reakce na volumovou expanzi, pulz, saturace krve O₂, centrální žilní tlak, nitrobřišní tlak). Hodnotí se stav respirace, renálních funkcí (sérový kreatinin), acidobazická rovnováha a další výše uvedená laboratorní vyšetření. Měří se hodinová diuréza a v případě žaludeční atonie se zavádí nazogastrická sonda k odvádění stagnační tekutiny.
Nejdůležitější léčebné přístupy:
- Intenzivní hydratace. Podáváme 250–500 ml izotonického roztoku/hodinu, v případě hypovolemie z úniku velkého množství tekutin extravazálně je nejefektivnější v prvních 12–24 hodinách. Objem podaných tekutin může představovat 10 i více litrů na den. U starších osob, zejména s renálním či kardiálním onemocněním, jsme si vědomi rizika rychlé rehydratace, proto stav pacienta pečlivě sledujeme, abychom se vyhnuli závažným komplikacím, především srdečnímu selhání. K volumexpanzi používáme koloidní roztoky, z krystalických roztoků se jako nejvhodnější ukazuje v některých studiích Ringer laktát(15). Albumin podáváme při závažném úniku albuminu z krevního řečiště, krevní převody při poklesu červené krevní řady v krevním obrazu.
- Orgánová podpora. Rozvoj komplikujícího orgánového, především oběhového selhání si může vynutit inotropní podporu sympatomimetiky (dobutamin, noradrenalin), oxygenoterapii, umělou plicní ventilaci a hemodialýzu.
- Úprava minerálového rozvratu. Důležitá je zejména úprava hypokalcemie, hyperkalemie či hypokalemie.
- Prevence atonie žaludku a střev. Platí zákaz perorálního příjmu potravy po dobu bolestí, pozitivního zánětlivého fyzikálního nálezu na břiše a vzrůstajících pankreatických enzymech v séru; při atonii a dilataci žaludku odčerpávání stagnační tekutiny
- Analgetika se podávají v injekční formě k tlumení bolesti (metamizol, tramadol, fentanyl, piritramid, pentazocin); při krutých bolestech se někdy volí analgetika podávaná kontinuálním epidurálním katétrem; nepodávat spasmolytika – zhoršují střevní peristaltiku.
- ERCP se provádí jako terapeutický výkon u biliární pankreatitidy s obstrukcí žlučových cest. Umožňuje odstranění kamene zaklíněného ve žlučových cestách pomocí košíčku, provedení papilosfinkterotomie nebo zavedení duodenobiliárního stentu k drenáži žlučových cest. Neprovádí se jako pouhá diagnostická metoda, neboť toto vyšetření samo o sobě nese riziko vzniku akutní pankreatitidy.
- Antibiotická terapie. Preventivní podávání antibiotik ani antimykotik se u sterilní pankreatitidy nedoporučuje, neboť se neprokázal jejich benefit(16,17). Léčba antibiotiky je rezervována pro pacienty s infekčními komplikacemi. Zpočátku empiricky nasazená antibiotika mohou být zaměněna podle výsledků kultivačních vyšetření (hemokultury, aspirace tenkou jehlou pod CT kontrolou). K nejúčinnějším antibiotikům pronikajícím pankreatickou nekrózou patří carbapenem, chinolony, metronidazol a vysoké dávky cefalosporinů(18). Stejně tak jsou antibiotika indikována u extrapankreatických infekcí. Včasné nasazení antibiotik snižuje nutnost intervence, morbidity i mortality.
- Chirurgické řešení. Asymptomatické pankreatické a/nebo extrapankreatické nekrózy nebo pseudocysty nevyžadují chirurgické řešení, bez ohledu na velikost či lokalizaci. U pacientů s infikovanou nekrózou začínáme antibiotickou terapií, která někdy sama stačí zvládnout infekční komplikaci. Pokud je indikovaná u stabilních pacientů s infikovanou nekrózou chirurgická nebo endoskopická drenáž či drenáž pod rtg kontrolou, je doporučeno ji odložit pokud možno na dobu alespoň 4 týdnů, aby mohla nekrotická tkáň zkolikvovat a fibroticky se ohraničit(2). U nestabilních pacientů se symptomatickou infikovanou nekrózou volíme pokud možno minimálně invazivní metodu nekrektomie s laparoskopickým, video-asistovaným či endoskopickým přístupem nebo jejich kombinací. Provádí se také perkutánní drenáž s katétrem zavedeným pod radiologickou kontrolou, která je preferována před operací s otevřením dutiny břišní (chirurgický débridement)(2).
V případě akutní pankreatitidy biliární etiologie je také třeba následně řešit cholecystolitiázu. Cholecystektomie se doporučuje jako prevence recidivy zánětu slinivky. U křehkých pacientů seniorského věku s četnými komorbiditami, pro které by byl operační výkon rizikový, lze jako efektivní preventivní řešení recidivy biliární pankreatitidy zvolit papilosfinkterotomii. U těžké nekrotizující biliární pankreatitidy se cholecystektomie doporučuje po odeznění akutního zánětu, aby se zabránilo infekční komplikaci. - Nutrice. U mírné pankreatitidy můžeme podávat perorální nízkotučnou pankreatickou dietu po ústupu bolestí, odeznění nauzey, zvracení a obnově pasáže. U těžké pankreatitidy podáváme enterální výživu nazojejunální sondou (zavádí se pod rtg kontrolou nebo endoskopicky). Enterální výživa je preferována před parenterální. Preference enterální výživy vychází z pozorování, že sliznice střeva, do kterého nepřichází strava, atrofuje a zvyšuje se riziko průniku infekce ze střeva do nekrotických tkání(19,20). Nedoporučuje se podávání probiotik, v klinických studiích byla prokázána zvýšená mortalita(21).
Prognóza a prevence
Prognóza závisí na vyvolávající příčině a závažnosti onemocnění. Zatímco mortalita lehké pankreatitidy nepřesahuje 1–2 %, u sterilní nekrotické pankreatitidy dosahuje 12 %(7).
Rizikovými faktory mortality jsou věk nad 55 let, četné komorbidity, body mass index > 30, známky hypovolemie a renálního selhání, známky těžkého zánětu, pleurální výpotky a alterace psychického stavu. Mortalita těžké pankreatitidy s orgánovým selháním přesahuje 50 %(5,6,7,).
Nejlepší prevencí vzniku pankreatitidy je správná životospráva, vyvarování se abúzu alkoholu, včasné řešení patologie žlučových cest. Prevence post-ERCP pankreatitidy (PEP) spočívá v aplikaci přísnějších indikačních kritérií, kdy ERCP představuje především terapeutickou metodu, zatímco v diagnostice se snažíme využívat neinvazivní metody (ultrazvukové vyšetření CT, MRI nebo endoskopickou ultrasonografii). Stratifikace pacientů podle rizika, zlepšení techniky výkonu a využití zavaděčů při kanylaci žlučových cest, aby nedošlo k nechtěnému nástřiku pankreatických vývodů, snížily výskyt PEP. K poklesu incidence PEP přispělo také dočasné zavádění pankreatických duktálních stentů při komplikovaných výkonech s obtížnou kanylací žlučových cest nebo s manipulací zavaděčem v pankreatických vývodech, po provedené sfinkterotomii či po odběru pankreatické brush cytologie(22,23,24). Neúspěšný pokus o zavedení stentu s neopatrnou manipulací ve vývodných cestách však může PEP vyvolat(18). Některé studie prokázaly snížení incidence PEP podáním nesteroidních antirevmatik v čípcích těsně před výkonem nebo po výkonu (indomethacin nebo diclofenac sodný) u vysoce rizikových pacientů(25,26 ,27), jiné však tento benefit nepotvrdily(28). Metaanalýzy neprokázaly ani efekt kortikoidů(29,30). Určité pozitivní výsledky přinesla aplikace somatostatinu či octreotidu. Při metaanalýze studií však nebyly dostatečně signifikantní(31–35).
Autoři prohlašují, že v souvislosti s publikací článku nejsou ve střetu zájmů a vznik ani publikace článku nebyly podpořeny farmaceutickou firmou.
MUDr. Marie Berková, Ph.D.1
MUDr. Zdeněk Berka2
prof. MUDr. Eva Topinková, CSc.1
1Geriatrická klinika 1. LF UK a VFN Praha
22. interní klinika LF UP a FN Olomouc
MUDr. Marie Berková, Ph.D.
e-mail: Marie.berkova@lf1.cuni.cz
Pracuje na Geriatrické klinice 1. LF UK a VFN v Praze.
Sources
1. Fagenholz PJ, Castillo CF, Harris NS, et al. Increasing United States hospital admissions for acute pancreatitis, 1988-2003. Ann Epidemiol 2007; 17(7): 491–7.
2. Tenner S, Baillie J, DeWitt J, et al. Management of Acute Pancreatitis. Am J Gastroenterol 2013; 108 : 1400–1415.
3. Zazula R, Wohl P. Akutní pankreatitida. Medicína pro praxi 2005; 4 : 147–151.
4. Dítě P, Lukáš M, Lata J. Akutní pankreatitida. In: Češka R, Ťulc T, Tesař V. Vnitřní lékařství. Praha: Triton 2010. 415–418.
5. Špičák J. Léčba akutní pankreatitidy. Lékařské listy 2010; 11(59): 23.
6. Besselink MG, Berwer TJ, Shoenmaeckers EJ, et al. Timing of surgical intervention in necrotizing pancreatitis. Arch Surg 2007; 142 : 1194–1201.
7. Banks PA, Freeman ML. Practice Parameters Committee of the American College of Gastroenterology. Practice guidelines in acute pancreatitis. Am J Gastroenterol 2006; 101 : 2379–2400.
8. Badalov N, Tenner S, Baillie J. The Prevention, Recognition and Treatment of Post-ERCP Pancreatitis. JOP 2009; 10(2): 88–97.
9. Špičák J. Etiologie akutní pankreatitidy. In: Akutní pankreatitida. Praha: Grada Publishing 2005. 87–101.
10. Banks PA, Bollen TL, Dervenis C, et al. Classification of acute pancreatitis—2012: revision of the Atlanta classification and definitions by interna-tional consensus. Gut 2013; 62 : 102–111.
11. Tenner S. Initial Management of Acute Pancreatitis: Critical issues during the first 72 hours initial management of acute pancreatitis. Am J of Gastroenterol 2004; 99 : 2489–2494.
12. Zheng MH, Xia HH, Chen YP. Rectal administration of NSAIDs in the prevention of post-ERCP pancreatitis: a complementary meta-analysis. Gut 2008; 57 : 1632–3.
13. Freeman ML. Adverse outcomes of ERCP. Gastrointest Endosc 2002; 56(6 Suppl): S273–82.
14. Steinberg W, DeVries JH, Wadden TA, et al. Tu1502 Longitudinal Monitoring of Lipase and Amylase in Adults With Type 2 Diabetes and Obesity: Evidence From Two Phase 3 Randomized Clinical Trials With the Once-Daily GLP-1 Analog Liraglutide. Gastroenterology 2012; 142 (5): Suppl 1, S 850–851.
15. Wu BU, Hwang JQ, Gardner TH et al. Lactated Ringer‘s solution reduces systemic inflammation compared with saline in patients with acute pancreatitis. Clin Gastroenterol Hepatol 2011; 9(8): 710–717.
16. Dellinger EP, Tellado JM, Soto NE, et al. Early antibiotic treatment for severe acute necrotizing pancreatitis: a randomized, double blind, placebo controlled study. Ann Surg 2007; 245 : 674–683.
17. Isenmann R, Runzi M, Kron M, et al. Prophylactic antibiotic treatment in patients with predicted severe acute pancreatitis: a placebo-controlled, double-blind trial. Gastroenterology 2004; 126 : 997–1004
18. De Vries A, Besselink MG, Buskens E, et al. Randomized controlled trials of antibiotic prophylaxis in severe acute pancreatitis: relationship between methodologic quality and outcome. Pancreatology 2007; 7 : 531–538.
19. Gupta R, Patel K, Calder PC, et al. A randomised clinical trial to assess the effect of total enteral and total parenteral nutritional support on metabolic, inflammatory and oxidative markers in patients with predicted severe acute pancreatitis II (APACHE ≥6). Pancreatology 2003; 3 : 406–413.
20. Yi F, Ge L, Zhao J, et al. Meta-analysis: total parenteral nutrition versus total enteral nutrition in predicted severe acute pancreatitis. Intern Med 2012; 51 : 523–530.
21. Besselink MG, van Santvoort HC, Buskens E, et al. Probiotic prophylaxis in predicted severe acute pancreatitis: a randomised, double-blind, placebo-controlled trial. Lancet 2008; 371 : 651–659.
22. ASGE Standards of Practice Committee. Complications of ERCP. Gastrointestinal Endoscopy 2012; 75(3): 467–473.
23. Freeman ML. Pancreatic stents for prevention of post-endoscopic retrograde cholangiopancreatography pancreatitis. Clin Gastroenterol Hepatol 2007; 5 : 1354–1365.
24. Ito K, Fujita N, Noda Y, et al. Can pancreatic duct stenting prevent postERCP pancreatitis in patients who undergo pancreatic duct guidewire placement for achieving selective biliary cannulation? A prospective randomized controlled trial. J Gastroenterol 2010; 45 : 1183–1191.
25. Elmunzer BJ, Waljee AK, Elta GH, et al. A meta-analysis of rectal NSAIDs in the prevention of post-ERCP pancreatitis. Gut 2008; 57 : 1262–1267.
26. Zheng MH, Xia HH, Chen YP. Rectal administration of NSAIDs in the prevention of post-ERCP pancreatitis: a complementary meta-analysis. Gut 2008; 57 : 1632–1623.
27. Dai HF, Wang XW, Zhao K. Role of nonsteroidal anti-inflammatory drugs in the prevention of post-ERCP pancreatitis: a meta-analysis. Hepatobiliary Pancreat Dis Int 2009; 8 : 11-16.
28. Cheon YK, Cho KB, Watkins JL, et al. Efficacy of diclofenac in the prevention of post-ERCP pancreatitis in predominantly high-risk patients: a randomized double-blind prospective trial. Gastrointest Endosc 2007; 66 : 1126–1132.
29. Zheng M, Bai J, Yuan B, et al. Meta-analysis of prophylactic corticosteroid use in post-ERCP pancreatitis. BMC Gastroenterol 2008; 8 : 6.
30. Bai Y, Gao J, Shi X, et al. Prophylactic corticosteroids do not prevent post-ERCP pancreatitis: a meta-analysis of randomized controlled trials. Pancreatology 2008; 8 : 504–509.
31. Dumonceau JM, Andriulli A, Deviere J, et al. European Society of Gastrointestinal Endoscopy (ESGE) Guideline: prophylaxis of post-ERCP pancreatitis. Endoscopy 2010; 42 : 503–515.
32. Concepción-Martín M, Gómez-Oliva C, Juanes A, et al. Somatostatin for prevention of post-ERCP pancreatitis: a randomized, double-blind trial. Endoscopy 2014; 46(10): 851–856.
33. Chen C-C. Somatostatin for Prevention of Post-endoscopic Retrograde Cholangiopancreatography Pancreatitis: A Never-ending Story? J Chin Med Assoc 2009; 72(2): 57–59.
34. Manolakopoulos S, Avgerinos A, Vlachogiannakos J et al. Octreotide versus hydrocortisone versus placebo in the prevention of post-ERCP pancreatitis: a multicenter randomized controlled trial. Gastrointest Endosc 2002; 55(4): 470–475.
35. Špičák J. Prevence pankreatitidy po ERCP. Gastroent Hepatol 2013; 67(2): 162–164.
Labels
Geriatrics General practitioner for adults Orthopaedic prosthetics
Article was published inGeriatrics and Gerontology

2015 Issue 1-
All articles in this issue
- Srdeční selhání u seniorů v podmínkách oddělení následné péče
- Kvalita života obyvateľov v zariadeniach pre seniorov
- Akutní pankreatitida, obávaná diagnóza i ve starším věku
- Tuberkulóza v seniorském věku
- Věnujeme dost pozornosti orální hygieně seniorů?
- Tinnitus – často opomíjený problém
- Inkluzivní mobilita – o dopravě a stárnutí populace měst
- Geriatrics and Gerontology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Akutní pankreatitida, obávaná diagnóza i ve starším věku
- Tinnitus – často opomíjený problém
- Kvalita života obyvateľov v zariadeniach pre seniorov
- Tuberkulóza v seniorském věku
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career



