-
Medical journals
- Career
Dysfágia po prednej krčnej diskektómii a intersomatickej fúzii
Authors: R. Opšenák; B. Kolarovszki; M. Benčo; J. Šutovský; R. Richterová; P. Snopko
Authors‘ workplace: Neurochirurgická klinika JLF UK a UN Martin, Slovenská republika
Published in: Gastroent Hepatol 2017; 71(2): 150-155
Category: Clinical and Experimental Gastroenterology: Original Article
doi: https://doi.org/10.14735/amgh2016csgh.info17Overview
Úvod:
Dysfágia je častým nálezom po prednej krčnej diskektómii. Incidencia a závažnosť porúch prehĺtania po operačnom výkone sú variabilné a závisia od mnohých faktorov.Pacienti a metódy:
Prospektívna otvorená monocentrická štúdia, sledovanie 6 mesiacov. Do štúdie bolo zaradených 66 pacientov po jedno - alebo dvojsegmentovej prednej krčnej diskektómii a fúzii (ACDF – anterior cervical discectomy and fusion) klietkou Zero-P VA® alebo ROI-C® v období od mája 2012 do augusta 2014. Stupeň závažnosti porúch prehĺtania bol hodnotený pomocou Bazaz-Yoo dysfagického skóre pred operačným výkonom, 6 týždňov, 3 a 6 mesiacov po operačnom výkone. Bol sledovaný vplyv faktorov ako preexistujúca dysfágia, pohlavie, počet operovaných segmentov, fajčenie a trvanie operačného výkonu na výskyt pooperačnej dysfágie. Bola tiež hodnotená korelácia medzi trvaním operačného výkonu a závažnosťou pooperačnej dysfágie.Výsledky:
V celom súbore pacientov bola dysfágia prítomná predoperačne u 15 % pacientov, 6 týždňov pooperačne udávalo poruchu prehĺtania 56 % pacientov, 3 mesiace pooperačne 32 % a 6 mesiacov pooperačne 18 % pacientov. Žiadny pacient v súbore neudával v celom období sledovania ťažký stupeň dysfágie. Pooperačne nebol zistený signifikantný vzťah medzi incidenciou preexistujúcej a pooperačnej dysfágie. Preexistujúcu poruchu prehĺtania udávalo 3 % fajčiarov a 24 % nefajčiarov, tento rozdiel bol signifikantný (p < 0,05). V celom období sledovania nebol zistený signifikantný vzťah medzi pohlavím, fajčením, počtom operovaných segmentov, trvaním operačného výkonu a incidenciou pooperačnej dysfágie. V celom období sledovania nebola zistená korelácia medzi trvaním operačného výkonu a závažnosťou pooperačnej dysfágie.Záver:
Väčšina pacientov udávala 6 týždňov po ACDF poruchu prehĺtania mierneho stupňa, v ďalšom období bola už väčšina pacientov bez porúch prehĺtania. Preexistujúca dysfágia, pohlavie, fajčenie, počet operovaných segmentov a trvanie operačného výkonu nemajú vplyv na incidenciu dysfágie po ACDF. Trvanie operačného výkonu nekorelovalo so závažnosťou pooperačnej dysfágie.Kľúčové slová:
krčná chrbtica – diskektómia – dysfágia – rizikové faktoryÚvod
Predná krčná diskektómia je najčastejší operačný výkon v rámci operačnej liečby degeneratívneho ochorenia krčnej chrbtice. Podobne ako u iných operačných výkonov, aj pri prednej krčnej diskektómii sa môžu vyskytnúť peroperačné a pooperačné komplikácie. Pooperačná dysfágia je častý nález a dobre známa komplikácia po prednej krčnej diskektómii. Patofyziológia pooperačnej dysfágie je však nejasná a liečba perzistujúcej dysfágie problematická.
Prehĺtanie sa delí do troch neuroanatomických fáz:
- Orálna fáza – začína vstupom jedla do ústnej dutiny, kde je rozdrobené pomocou žuvacích svalov a jazyka. Svalstvo jazyka, ktoré inervuje podjazykový nerv, manipuluje s bolusom jedla. Komplexná koordinácia mäkkého podnebia, pohybov jazyka, slinných žliaz a žuvacieho svalstva vrátane vedenia informácií z chemoreceptorov a mechanoreceptorov v ústach je zabezpečená lícnym, jazykohltanovým a podjazykovým nervom.
- Faryngeálna fáza – charakterizuje ju už mimovôľová koordinácia svalovej kontrakcie, ktorá posúva bolus jedla. Kritickým aspektom tejto fázy je elevácia laryngu, epiglotická inverzia zabraňujúca vniknutiu jedla do dýchacích ciest a kontrakcia konstriktorov faryngu. Inerváciu faryngeálnej fázy prehĺtania zabezpečujú nervus laryngeus superior a nervus laryngeus recurrens.
- Ezofageálna fáza – začína pasážou bolusu jedla cez horný ezofageálny sfinkter a končí pasážou cez dolný ezofageálny sfinkter. Táto fáza je kompletne mimovôľová a realizovaná koordinovanou peristaltikou ezofageálnej muskulatúry. Koordináciu tejto fázy zabezpečuje autonómna činnosť plexus myentericus Auerbachi, ktorý je pod kontrolou blúdivého nervu. Jazykohltanový a podjazykový nerv môžu byť poškodené pri prístupe v segmente C3 a vyššie, nervus laryngeus superior pri prístupe k intervertebrálnemu disku C3–C4 a nervus laryngeus recurrens pri prístupe v segmente C6 a nižšie. Blúdivý nerv, prirodzene chránený v karotickom púzdre, môže byť poškodený excesívnou retrakciou v celej oblasti subaxiálnej krčnej chrbtice.
Nezodpovedanou otázkou zostáva vplyv rôznych faktorov na incidenciu a závažnosť pooperačných porúch prehĺtania. V publikáciach sa skúmajú rôzne rizikové faktory v súvislosti s pooperačnou dysfágiou po prednej krčnej diskektómii. Ich výsledky sa však v rámci jednotlivých rizikových faktorov líšia a nemožno ich považovať za jednoznačne smerodajné.
Súbor pacientov a metodika
Do prospektívnej monocentrickej štú - die sme zaradili 66 pacientov s degeneratívnym ochorením krčnej chrbtice, u ktorých bola realizovaná predná krčná diskektómia prístupom podľa Smith-Robinsona a intersomatická fúzia v jednom alebo dvoch pohybových segmentoch. Intersomatická fúzia bola indukovaná implantáciou klietok Zero-P VA® (DePuy Synthes, Švajčiarsko) (obr. 1) alebo ROI-C® (LDR Medical, Francúzsko) (obr. 2). Dizajn uvedených klietok s integrovanou dlahou v tele implantátu podmieňuje ich nulový profil a predpokladá redukciu výskytu a závažnosti pooperačných porúch prehĺtania. Súbor pacientov z hľadiska pohlavia tvorilo 47 žien a 19 mužov. Medzi exklúzne kritériá patrili graficky verifikovaná myelopatia (magnetická rezonancia), gravidita, kontraindikácia elektívneho výkonu, nádorové a infekčné ochorenia chrbtice. Všetky operačné výkony boli realizované na Neurochirurgickej klinike JLF UK a UN Martin v období od mája 2012 do augusta 2014. Závažnosť pooperačnej dysfágie bola hodnotená pomocou Bazaz-Yoo dysfagického skóre, ktoré je uvedené v tab. 1 [1]. Závažnosť pooperačných porúch prehĺtania bola sledovaná pred operačným výkonom a v pooperačnom období (6 týždňov, 3 mesiace a 6 mesiacov). Následne bola hodnotená korelácia medzi trvaním operačného výkonu v minútach u pacientov rozdelených podľa závažnosti dysfágie v uvedených pooperačných obdobiach pomocou Kruskalov-Wallisovho testu. Osobitne bol sledovaný výskyt dysfágie pred vlastným operačným výkonom a v pooperačnom období (6 týždňov, 3 mesiace, 6 mesiacov). Súbor pacientov sme rozdelili podľa trvania operačného výkonu do dvoch skupín – operačný výkon s trvaním ≤ 90 min a > 90 min, podľa anamnézy fajčenia na fajčiarov a nefajčiarov, podľa pohlavia na mužov a ženy, podľa počtu operovaných segmentov na pacientov po jednoúrovňovej a dvojúrovňovej prednej krčnej diskektómii. Podobne sme rozdelili súbor pacientov na dve skupiny podľa prítomnosti alebo absencie porúch prehĺtania pred vlastným operačným výkonom. Následne bol hodnotený vplyv faktorov ako preexistujúca dysfágia, pohlavie, fajčenie, počet operovaných segmentov a trvanie operačného výkonu na incidenciu pooperačnej dysfágie pomocou Fischerovho testu. Rovnako pomocou Fischerovho testu bol hodnotený vzťah medzi fajčením a incidenciou preexistujúcej dysfágie a vzťah medzi pohlavím a počtom operovaných segmentov.
Image 1. Pooperačný laterogram po implantácii klietky Zero-P VA<sup>®</sup> v segmentoch C5–C6 a C6–C7 (archív autora). Fig. 1. Lateral X-ray image after Zero-P VA<sup>®</sup> cage implantation in segments C5–C6 and C6–C7 (author’s archive). 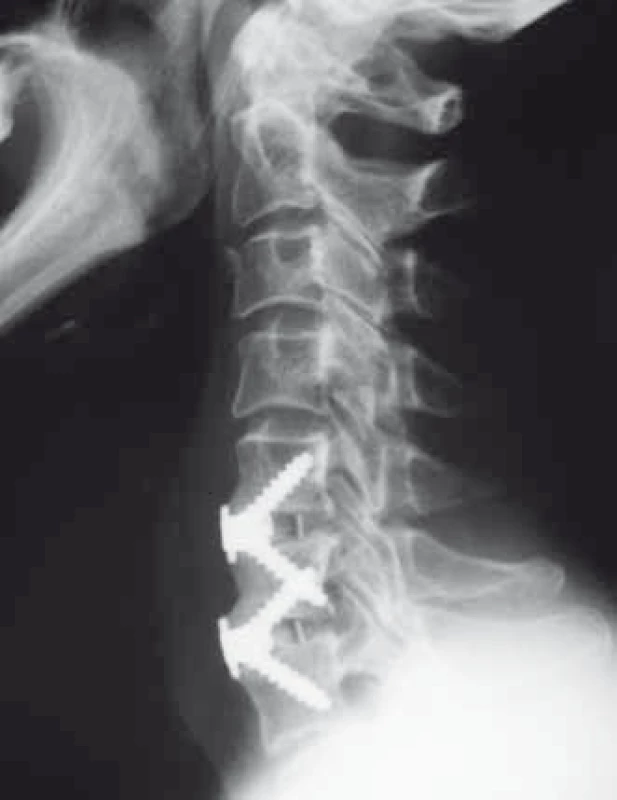
Image 2. Pooperačný laterogram po implantácii klietky ROI-C<sup>®</sup> v segmente C5–C6 (archív autora). Fig. 2. Lateral X-ray image after ROI-C<sup>®</sup> cage implantation in segment C5–C6 (author’s archive). 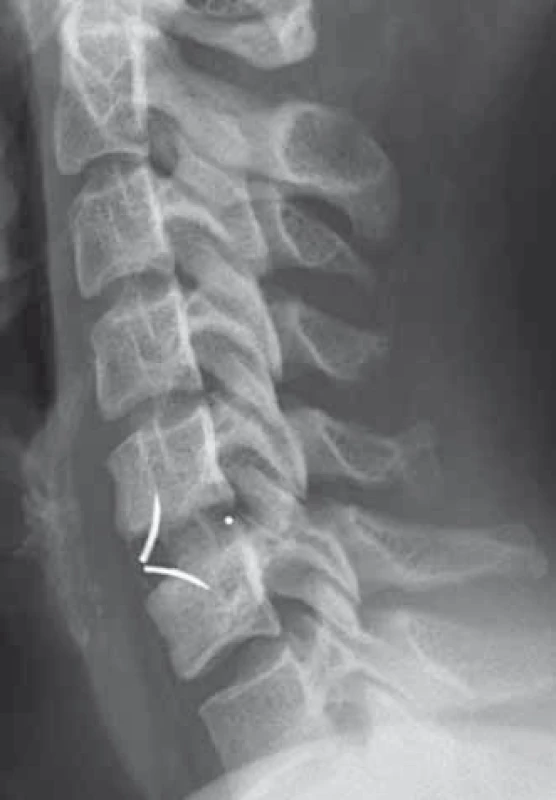
Table 1. Bazaz-Yoo dysfagické skóre. Upravené podľa [1]. Tab. 1. Bazaz-Yoo dysphagia score. Adapted from [1]. ![Bazaz-Yoo dysfagické skóre. Upravené podľa [1].
Tab. 1. Bazaz-Yoo dysphagia score. Adapted from [1].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/46e4f589b4d5d13e223d27fc3b46fb69.png)
Výsledky
Žiadny pacient v celom období sledovania neudával poruchu prehĺtania ťažkého stupňa podľa Bazaz-Yoo dysfagického skóre. V celom sledovanom súbore bola predoperačne prítomná dysfágia u 15 % pacientov, z toho v 9 % prípadov mierneho stupňa a v 6 % prípadov stredne ťažkého stupňa podľa Bazaz-Yoo dysfagického skóre. Šesť týždňov po prednej krčnej diskektómii a implantácii klietky s nulovým profilom udávalo poruchu prehĺtania 56 % pacientov, pričom u 50 % pacientov bola prítomná dysfágia mierneho stupňa a v 6 % prípadov stredne ťažkého stupňa. Tri mesiace po operácii bola incidencia dysfágie v celom súbore pacientov 32 %, v 27 % prípadov mierneho a v 5 % prípadov stredne ťažkého stupňa. Šesť mesiacov po operácii udávalo poruchu prehĺtania celkovo 18 % pacientov, u všetkých pacientov bola mierneho stupňa.
Počas celého obdobia sledovania nebol zistený signifikantný vzťah medzi incidenciou preexistujúcej a pooperačnej dysfágie, bol však zaznamenaný uvedený vzťah na hranici významnosti 6 mesiacov po prednej krčnej diskektómii (Fischerov test; p = 0,07). Sledovaný súbor pacientov tvorí 71 % žien a 29 % mužov. Nebol zistený signifikantný vzťah medzi pohlavím a počtom operovaných segmentov. Pohlavie pacientov teda neovplyvnilo v uvedenom súbore rozsah operačnej intervencie. V súbore pacientov v celom období sledovania nebol zistený signifikantný vzťah medzi pohlavím a incidenciou pooperačnej dysfágie. V sledovanom súbore udávali fajčenie 44 % pacientov. Preexistujúcu poruchu prehĺtania udávalo 3 % fajčiarov a 24 % nefajčiarov, tento rozdiel bol štatisticky významný (Fischerov test; p < 0,05). Uvedený rozdiel je možné považovať za charakteristiku tohto súboru pacientov. V celom sledovanom pooperačnom období nebol zistený signifikantný rozdiel medzi fajčením a výskytom pooperačnej dysfágie.
Predná krčná diskektómia a fúzia (ACDF – anterior cervical discectomy and fusion) v jednom pohybovom segmente bola vykonaná u 45 % pacientov z celého súboru, u 55 % pacientov bola vykonaná intervencia v dvoch pohybových segmentoch. V celom pooperačnom sledovaní nebol zistený signi - fikantný vzťah medzi počtom operovaných segmentov a incidenciou dysfágie. Priemerné trvanie operačného výkonu v celom súbore pacientov bolo 101 min. Priemerné trvanie jednosegmentovej ACDF bolo 84 min, dvojsegmentovej ACDF 115 min. Nebola zistená korelácia medzi trvaním operačného výkonu a závažnosťou dysfágie podľa Bazaz-Yoo dysfagického skóre v celom období sledovania. Rovnako nebol počas celého obdobia sledovania zistený signifikantný vzťah medzi trvaním operačného výkonu a incidenciou pooperačnej dysfágie, bol však zaznamenaný uvedený vzťah na hranici významnosti 3 mesiace po operačnom výkone (Fischerov test; p = 0,06).
Diskusia
Publikovaná incidencia dysfágie po prednej krčnej diskektómii kolíše v širokom rozmedzí 0–89 % a klesá s narastajúcim odstupom od vlastného operačného výkonu (tab. 2). Frempong-Bodau et al udávajú celkovú incidenciu dysfágie 1 mesiac po operačnom výkone v 48 %. Vek, diabetes mellitus, artériová hypertenzia, fajčenie a stav výživy neboli spájané s pooperačnými abnormalitami prehĺtania. Pooperačné zdurenie faryngu a prevertebrálnych mäkkých tkanív referovali u 61 % pacientov, pričom 86 % z týchto pacientov malo abnormálne testy prehĺtania pri vyšetrení pasáže báriom [2].
Table 2. Klinické štúdie zamerané na hodnotenie incidencie dysfágie po prednej krčnej diskektómii. Tab. 2. Clinical studies conducted to evaluate the incidence of dysphagia after anterior cervical discectomy. 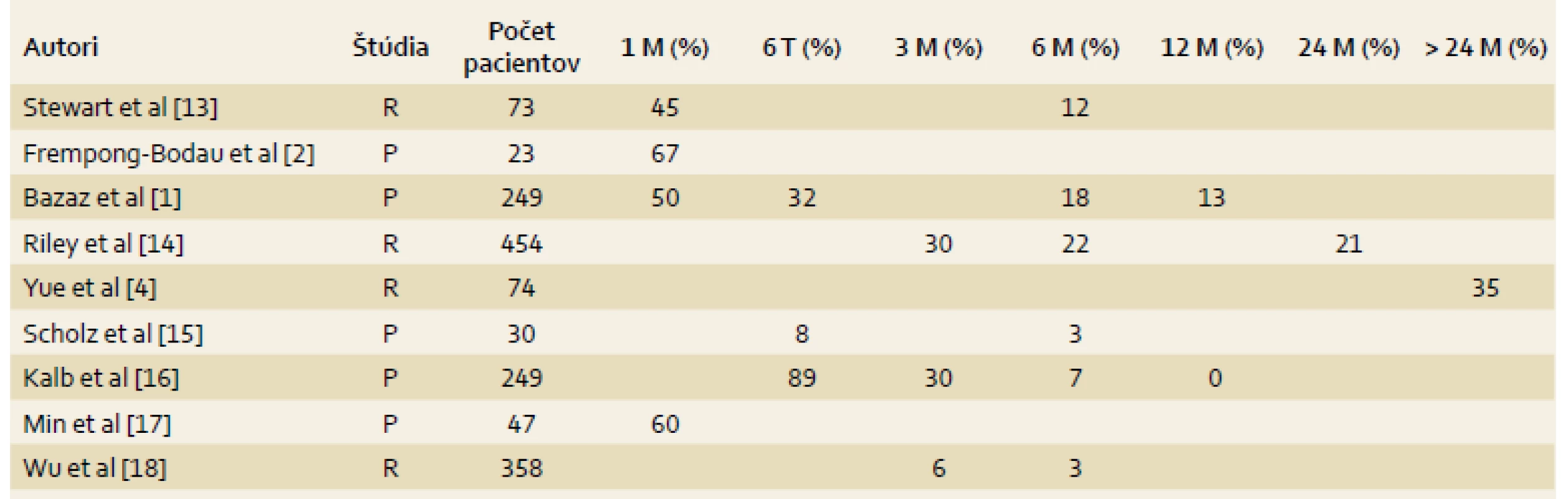
R – retrospektívna, P – prospektívna, M – mesiac, T – týždeň Bazaz et al prospektívne analyzovali 249 pacientov po prednej krčnej diskektómii alebo somatektómii a pooperačne hodnotili závažnosť dysfágie pomocou vlastného skórovacieho systému (Bazaz-Yoo dysphagia score), ktorý je uvedený v tab. 1. Tento skórovací systém sa používa vo väčšine súčasných štúdií na hodnotenie stupňa závažnosti pooperačných porúch prehĺ - tania a bol použitý aj pri hodnotení našeho súboru pacientov. Jeden mesiac po operácii bola dysfágia prítomná v tejto štúdii u 50,3 % pacientov, z toho v 5,6 % prípadov bola ťažkého stupňa. Šesť mesiacov po operácii boli prítomné poruchy prehĺtania u 17,7 % pacientov a 12 mesiacov pooperačne u 12,5 % pacientov. Ženské pohlavie bolo rizikovým faktorom 6 mesiacov po operácii, multisegmentový operačný výkon bol rizikovým faktorom 1 mesiac po operácii, ale v období 6 mesiacov pooperačne už v porovnaní s monosegmentovými výkonmi nebol rozdiel štatisticky významný. Vek, primárny vs. revízny výkon, somatektómia vs. diskektómia a použité inštrumentárium neboli rizikovými faktormi v celom období sledovania [1].
Smith-Hammond et al v trojročnej prospektívnej štúdii sledovali incidenciu dysfágie po predných krčných výkonoch. V kontrolných skupinách sledovali tiež pacientov po zadných výkonoch na krčnej a driekovej chrbtici. Dysfágia bola zisťovaná pred výkonom a pooperačne cestou subjektívnych otázok a verifikovaná videofluoroskopicky alebo endoskopicky fibroskopom. Incidencia dysfágie u pacientov po prednom krčnom prístupe bola 50 %, pričom u 70 % týchto pacientov regredovala v priebehu 2 mesiacov. Zaujímavé bolo zistenie, že až 20 % pacientov po zadných výkonoch na krčnej chrbtici malo poruchy prehĺtania, pričom endotracheálna intubácia nefigurovala ako rizikový faktor v tejto štúdii [3].
Štúdia publikovaná autormi Yue et al potvrdzuje, že pooperačná dysfágia môže pretrvávať aj v dlhšom časovom intervale ako 12 mesiacov. Autori sledovali 74 pacientov priemerne 7 rokov po prednom výkone na krčnej chrbtici. Celková incidencia dysfágie bola 35 %, pričom v 16,2 % prípadov bola stredne ťažkého a u jedného pacienta ťažkého stupňa podľa Bazaz-Yoo dysfagického skóre [4].
Martin et al hodnotili u 13 pacientov pooperačnú dysfágiu videofluoroskopicky a nachádzali abnormality v rôznych fázach prehĺtania. U troch pacientov dokázali poruchu faryngeálnej fázy v dôsledku poranenia nervus laryngeus superior, u štyroch pacientov poruchu orálnej fázy v dôsledku poranenia nervus hypoglossus. Dvaja pacienti mali pooperačnú dysfágiu v dôsledku edému prevertebrálnych mäkkých tkanív, ktorý obmedzuje pohyb steny faryngu a ezofágu. U ďalších pacientov bola prítomná inkompletná epiglotická deflekcia [5].
Uvedené štúdie teda potvrdzujú prítomnosť dysfágie po predných prístupoch ku krčnej chrbtici vo včasnom pooperačnom období na úrovni okolo 50 %. U väčšiny pacientov dochádza do 6 mesiacov pooperačne k úprave, pričom 12 mesiacov pooperačne je incidencia dysfágie už len okolo 13 %. V našom súbore bola incidencia pooperačnej dysfágie 6 týždňov po ACDF na úrovni 56 %, 3 mesiace po operácii na úrovni 32 % a 6 mesiacov pooperačne klesla na 18 %. Incidencia pooperačnej dysfágie v našej štúdii je porovnateľná s výsledkami ostatných štúdií skúmajúcich problematiku pooperačnej dysfágie po prednej krčnej diskektómii (tab. 2).
Niektoré štúdie referujú prítomnosť poruchy prehĺtania už pred vlastnou prednou krčnou diskektómiou. V našej štúdii bola incidencia predoperačnej dysfágie 15 %, pričom preexistujúca dysfágia bola prítomná signifikantne častejšie u nefajčiarov v porovnaní s fajčiarmi. Frempong-Bodau et al referujú u 66 % pacientov s myelopatiou predoperačne abnormality prehĺtania, ktoré boli verifikované pomocou pasáže bária. Predpokladali preto, že príčinou prehĺtania u týchto pacientov je porucha lokálnych reflexných mechanizmov na pregangliovej, sympatickej úrovni, v dôsledku kompresie miechy. Táto skupina pacientov bola náchylná pooperačne k výskytu významnej pretrvávajúcej dysfágie [2]. V našej štúdii bola myelopatia exklúznym kritériom.
Lee et al skúmali v prospektívnej štúdii význam dizajnu prednej krčnej dlahy ako rizikového faktoru. Vo svojej prospektívnej štúdii zistili, že použitie krčnej dlahy Zephir™ (Medtronic, Sofamor Danek, USA) je spojené s nižšou incidenciou pooperačnej dysfágie ako použitie dlahy Atlantis® od rovnakého výrobcu. Autori vysvetľujú uvedené zistenie hladším povrchom a nižším profilom krčnej dlahy Zephir™ [6]. Táto štúdia predikuje nižšiu incidenciu pooperačnej dysfágie pri použití implantátov s nulovým profilom. Zástupcom týchto implantátov sú aj klietky s integrovanou dlahou v tele implantátu (Zero-P VA®, DePuy Synthes, Švajčiarsko (obr. 1); ROI-C®, LDR Medical, Francúzsko (obr. 2)), ktoré boli použité pre nastolenie fúzie po prednej krčnej diskektómii u pacientov v našom súbore. Segebarth et al udávajú incidenciu dysfágie po monosegmentovej krčnej artroplastike 15,8 % v porovnaní s monosegmentovou intersomatickou fúziou s použitím dlahy 42,1 %. Tento nález rovnako vysvetľuje nulový profil arteficiálneho disku v porovnaní s nálezom po implantácii konvenčnej prednej krčnej dlahy [7]. Fogel et al referujú v retrospektívnej analýze 44 pacientov s perzistujúcou poruchou prehĺtania po ACDF regresiu dysfágie po odstránení konvenčnej prednej krčnej dlahy a adheziolýze pri revíznom výkone v 55 % prípadov. Peroperačne nachádzali rozsiahle adhézie medzi pažerákom a dlahou, prípadne prevertebrálnou fasciou [8]. Použitie klietok s integrovanou dlahou teda predpokladá elimináciu vzniku rozsiahlych fibroadhezívnych zmien.
Medzi faktory, ktoré sú väčšinou spájané so zvýšeným rizikom pooperačnej dysfágie, patria počet operovaných segmentov, ženské pohlavie, dlhý operačný čas a vek nad 60 rokov. Faktory, u ktorých prevažne nebol zaznamenaný súvis s pooperačnou dysfágiou, sú bolesti hlavy, typ incízie (transverzálna, oblúkovitá, longitudinálna), veľkosť predných osteofytov, pseudoartróza, zanorenie implantátu, uvoľnenie alebo rozlomenie implantátu, intubácia, závažnosť myelopatie, retrakcia ezofágu, osteoartritída, užívanie alkoholu a obezita [9]. V našej štúdii nebol zistený signifikantný vzťah medzi incidenciou pred - a pooperačnej dysfágie. Pohlavie, počet operovaných segmentov a trvanie operačného výkonu rovnako nemali signifikantný vplyv na incidenciu pooperačnej dysfágie.
Medzi preventívne opatrenia redukujúce výskyt pooperačnej dysfágie patria šetrná operačná technika, dôsledná hemostáza počas operačného výkonu a aplikácia drénu na konci operačného výkonu pre elimináciu hematómu. Niektoré štúdie skúmali špecifické možnosti prevencie pooperačnej dysfágie. Pedram et al v prospektívnej štúdii aplikovali 78 pacientom bez anamnézy ochorenia horného gastroin - testinálneho traktu metylprednizolón v dávke 1 mg/kg na konci operácie, po 12 a 24 hod po operácii. V porovnaní s kontrolnou skupinou podanie kortikoidu neredukovalo incidenciu dysfágie [10]. Apfelbaum et al v štúdii na kadaveroch skúmali hodnoty tlaku v manžete endotracheálnej kanyly po aplikácii retraktoru pre predný krčný prístup. Manžetu kanyly insuflovali na hodnotu 15 mm Hg, následne po naložení retraktoru tlak elevoval nad úroveň 52 mm Hg. Počas výkonu realizovali jednoduchý manéver, a to desufláciu a následnú insufláciu manžety endotracheálnej kanyly po naložení retraktoru, ktorý umožní centrálne umiestnenie kanyly v endolarynxe. Následne autori použili túto procedúru počas 650 predných krčných prístupov a zistili, že tento jednoduchý manéver znížil incidenciu poranenia nervus laryngeus reccurens z úrovne 6,8 na 2,0 % [11]. Ratnaraj et al realizovali štúdiu, v ktorej intraoperačne monitorovali a regulovali tlak manžety endotracheálnej kanyly v priebehu predných prístupov ku krčnej chrbtici. V experimentálnej skupine pacientov bol tlak monitorovaný a upravovaný tak, aby nepresiahol hranicu 20 mm Hg. V kontrolnej skupine pacientov nebol tlak monitorovaný ani korigovaný. Po 24 hod udávali pacienti v experimentálnej skupine signifikantne menšie bolesti hrdla v porovnaní s kontrolnou skupinou (51 vs. 74 %). Podobne, 24 hod po operácii, dlhší čas retrakcie koreloval s vývojom dysfágie. Záverom konštatovali, že udržiavanie nízkeho tlaku v endotracheálnej kanyle (do 20 mm Hg) a minimalizácia retrakčného času znižujú výskyt pooperačnej dysfágie a bolesti hrdla [12].
Záver
Vo včasnom pooperačnom období je incidencia pooperačnej dysfágie okolo 50 %, v ďalšom období dochádza ku významnej redukcii výskytu dysfágie. Väčšina pacientov 3 a 6 mesiacov po ACDF je už bez porúch prehĺtania. Zistené výsledky potvrdzujú výsledky doteraz publikovaných štúdii, ktoré sa zaoberali výskytom porúch prehĺtania po prednej krčnej diskektómii. Ťažká porucha prehĺtania sa v celom období sledovania našeho súboru pacientov nevyskytla. Preexistujúca dysfágia sa v našom súbore pacientov vyskytla signifikantne častejšie u nefajčiarov v porovnaní s fajčiarmi. Tento výsledok však možno hodnotiť ako charakteristiku súboru pacientov, ktorá bola predmetom štúdie. Nebol zistený vplyv faktorov ako preexistujúca dysfágia, fajčenie, počet operovaných segmentov a trvanie operačného výkonu na incidenciu pooperačnej dysfágie. Tento výsledok je v rozpore s výsledkom väčšiny publikovaných štúdií, v ktorých ženské pohlavie, počet operovaných segmentov a trvanie operačného výkonu boli rizikovým faktorom pooperačnej dysfágie [1,2,9]. Rovnako nebol zistený signifikantný vzťah medzi pohlavím a počtom operovaných segmentov. V celom období pooperačného sledovania nebola zistená korelácia medzi trvaním operačného výkonu a incidenciou pooperačnej dysfágie. Pre získanie validnejších výsledkov je nutné dlhšie sledovanie väčšieho súboru pacientov so zameraním sa na širšie spektrum rizikových faktorov.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Doručeno: 17. 1. 2016
Přijato: 5. 7. 2016
MUDr. René Opšenák
Neurochirurgická klinika
JLF UK a UN Martin
Kollárova 2
036 59 Martin
Slovenská republika
opsenak@gmail.com
Sources
1. Bazaz R, Lee MJ, Yoo JU. Incidence of dysphagia after anterior cervical spine surgery: a prospective study. Spine (Phila Pa 1976) 2002; 27 (22): 2453–2458.
2. Frempong-Bodau A, Houten JK, Osborn B et al. Swallowing and speech dysfunction in patients undergoing anterior cervical discectomy and fusion: a prospective, objective preoperative and postperative assesment. J Spinal Disord Tech 2002; 15 (5): 362–368.
3. Smith-Hammond CA, New KC, Pietrobon R et al. Prospective analysis of incidence and risk factors of dysphagia in spine surgery patients: comparison of anterior cervical, posterior cervical, and lumbar procedures. Spine (Phila Pa 1976) 2004; 29 (13): 1441–1446.
4. Yue WM, Brodner W, Highland TR. Persistent swallowing and voice problems after anterior cervical discectomy anf fusion with allograft and plating: a 5 - to 11-year follow-up study. Eur Spine J 2005; 14 (7): 677–682.
5. Martin RE, Neary MA, Diamant NE. Dysphagia following anterior cervical spine surgery. Dysphagia 1997; 12 : 2–8.
6. Lee MJ, Bazaz R, Furey C et al. Influence of anterior cervical plate design on dysphagia: a 2-year prospective longitudinal follow-up study. J Spinal Disord Tech 2005; 18 (5): 406–409.
7. Segebarth B, Datta JC, Darden B et al. Incidence of dysphagia comparing cervical arthroplasty and ACDF. SAS Journal 2010; 4 (1): 3–8. doi: 10.1016/j.esas.2009.12.001.
8. Fogel GR and McDonnell MF. Surgical treatment of dysphagia after anterior cervical interbody fusion. Spine J 2005; 5 (2): 140–144.
9. Anderson KK, Arnold PM. Oropharyngeal dysphagia after anterior cervical spine surgery: a review. Global Spine J 2013; 3 (4): 273–286. doi: 10.1055/s-0033-1354253.
10. Pedram M, Castagnera L, Carat X et al. Pharyngolaryngeal lesions in patients undergoing cervical spine surgery trough the anterior approach: contribution of methylprednisolon. Spine J 2003; 12 (1): 84–90.
11. Apfelbaum RI, Kriskovich MD, Haller JR. On the incidence, cause, and prevention od recurent laryngeal nerve palsies during anterior cervical spine surgery. Spine (Phila Pa 1976) 2000; 25 (22): 2906–2912.
12. Ratnaraj J, Todorov A, McHugh T et al. Effects of decreasing endotracheal tube cuff pressures during neck retraction for anterior cervical spine surgery. J Neurosurg 2002; 97 (2 Suppl 1): 176–179.
13. Stewart M, Johnston RA, Stewart I et al. Swallowing performance following anterior cervical spine surgery. Br J Neurosurg 1995; 9 (5): 605–609.
14. Riley LH 3rd, Skolasky RL, Albert TJ et al. Dysphagia after anterior cervical decompression and fusion: prevalence and risk factors from a longitudinal cohort study. Spine 2005; 30 (22): 2564–2569.
15. Scholz M, Schnake KJ, Pingel A et al. A new Zero-profile implant for stan-alone anterior cervical interbody fusion. Clin Orthop Relat Res 2011; 469 (3): 666–673. doi: 10.1007/s11999-010-1597-9.
16. Kalb S, Reis MT, Cowperthwaite MC et al. Dysphagia after cervical spine surgery: incidence and risk factors. World Neurosurg 2012; 77 (1): 183–187. doi: 10.1016/j.wneu.2011.07.004.
17. Min Y, Kim WS, Kang SS et al. Incidence of dysphagia and serial videofluoroscopic swallow study findings after anterior cervical discectomy and fusion: a prospective study. Clin Spine Surg 2016; 29 (4): E177–E181. doi: 10.1097/BSD.0000000 000000060.
18. Wu B, Song F, Zhu S. Reasons of dysphagia after operation of anterior cervical decompression and fusion. Clin Spine Surg 2016. In press.
Labels
Paediatric gastroenterology Gastroenterology and hepatology Surgery
Article was published inGastroenterology and Hepatology
2017 Issue 2-
All articles in this issue
- Hepatologie
- Doporučený postup České hepatologické společnosti ČLS JEP pro diagnostiku a léčbu akutních porfyrií
- Léčba krvácení v důsledku portální hypertenze při jaterní cirhóze – aktualizace doporučených postupů ČHS ČLS JEP
- Standardní diagnostický a terapeutický postup chronické infekce virem hepatitidy C
- Přímo působící antivirotika v léčbě HCV asociovaných maligních lymfomů
- Dysfágia po prednej krčnej diskektómii a intersomatickej fúzii
- První případ elektrické stimulační terapie dolního jícnového svěrače indikovaný v České republice k implantaci
- Výběr z mezinárodních časopisů
- Picoprep® – očistný prostředek s novým dávkovacím schématem
- Ustekinumab – nová biologická léčba pro pacienty s Crohnovou chorobou
- Mechanizmy vzniku motorických a evakuačních poruch při gastroezofageální refluxní chorobě se souběžnou obezitou
-
Developments in digestive endoscopy
Andrea May, Marco Bruno and Bjorn Rembacken Lectures – Gastro Update Europe 2016, Prague
- Gastroenterology and Hepatology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Ustekinumab – nová biologická léčba pro pacienty s Crohnovou chorobou
- Doporučený postup České hepatologické společnosti ČLS JEP pro diagnostiku a léčbu akutních porfyrií
- Picoprep® – očistný prostředek s novým dávkovacím schématem
- Léčba krvácení v důsledku portální hypertenze při jaterní cirhóze – aktualizace doporučených postupů ČHS ČLS JEP
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

