-
Medical journals
- Career
Variabilita testů na okultní krvácení používaných praktickými lékaři ve screeningu kolorektálního karcinomu v České republice
Authors: N. Král; B. Seifert; M. Korcová
Authors‘ workplace: Ústav všeobecného lékařství, 1. LF UK v Praze
Published in: Gastroent Hepatol 2015; 69(3): 255-258
Category: Gastrointestinal Oncology: Original Article
doi: https://doi.org/10.14735/amgh2015255Overview
V roce 2009 došlo k inovaci screeningu kolorektálního karcinomu s cílem dosažení lepších výsledků. Vedle testů guajakových se začaly používat testy imunochemické s vyšší senzitivitou i specificitou. Při zvýšení adherence české populace však došlo i k výraznému zvýšení pozitivity imunochemických testů s následnou obavou z vyšší falešné pozitivity. Doposud v ČR neexistoval přehled o typech jednotlivých imunochemických testů a jejich nastavení (cut-off).
Klíčová slova:
screening – kolorektální karcinom – imunochemický test – praktický lékařÚvod
Uvedení imunochemického testu na okultní krvácení (iTOKS) do programu screeningu kolorektálního karcinomu (KRK) v ČR v roce 2009 bylo jedním z opatření, které navrhla Komise Ministerstva zdravotnictví pro screening KRK (Věstník MZ) s cílem zvýšit účast ve screeningu a jeho efektivitu. Podkladem pro rozhodnutí o zařazení imunochemických testů do screeningu byla dobrá dostupnost imunochemických testů na českém trhu a výstupy zahraničních studií [1–3] ukazující na výhody imunochemického testu oproti tradičnímu testu guajakovému (gTOKS). Uvedení imunochemického testu provázel také předpoklad zapojení gynekologů do screeningu [4,5]. ČR se tak stala první evropskou zemí, která do organizovaného národního programu uvedla imunochemické cesty.
Imunochemické testy jsou založeny na principu stanovení lidského hemoglobinu ve stolici reakcí s protilátkou v testu. Imunochemické testy mají několik výhod oproti guajakovým testům: nevyžadují dietní omezení, stačí odběr jen z jedné stolice prováděný jednodušším a přijatelnějším způsobem. Imunochemické testy vykazují vyšší senzitivitu a stejnou specificitu při jednorázovém vyšetření ve srovnání s guajakovým testem prováděným na šesti vzorcích ze tří odběrů stolice. Imunochemické testy jsou selektivní na KRK tím, že jsou málo senzitivní na krvácení z proximální části gastrointestinálního traktu. Imunochemické testy pomáhají zvyšovat adherenci ke screeningu [6–9].
V ČR jsou v současné době dostupné tři typy imunochemických testů. K dispozici jsou jednorázové kvalitativní (kazetové) imunochemické testy od několika výrobců s nejnižší cenou odpovídající ceně guajakového testu. Kvalitativní imunochemické testy pracují na bázi plošné imunochromatografie. Analytický limit pozitivity (cut-off) je nastaven výrobcem. Výsledek ve tvaru pozitivní/ negativní se odečítá na testovacím proužku jako barevná linie testu. Testy umožňují jednoduchý odběr stolice a jednoduché vyhodnocení přímo v místě poskytování péče.
V praxi jsou rozšířené POCT (point of care testing) analyzátory, původně využívané zejména ke stanovování C - reaktivního proteinu. Tyto přístroje umožňují automatické vyhodnocení TOKS turbidimetrickou metodou. Mají výrobcem nastavitelný cut-off pro TOKS. Výsledek se objeví na displeji ve tvaru pozitivní/ negativní nebo v modernější verzi přístroje umožňující kvantitativní měření od 75, resp. 100 – 1 000 ng/ ml jako číselný údaj. Kromě nákladů na přístroj je třeba kalkulovat cenu jednoho vyšetřovacího kitu, která činí zhruba 75 Kč [10].
Konečně některé laboratoře disponují multianalyzátory, které provádějí kvantitativní vyhodnocení testů turbidimetrickou metodou. Cena odběrové kazety a vyšetření odpovídá nákladům na jedno vyšetření u POCT analyzátoru.
Věstník MZ z roku 2009 nespecifikuje typ imunochemického testu, jen poskytovatele, kteří screening provádějí. Úhrada testů je jednotná. Test prováděný v laboratoři nemá v rámci screeningu úhradu pojišťoven, je proplácen pouze jako test diagnostický.
Z opatření uvedených do screeningu v roce 2009 mělo zavedení imunochemických testů pravděpodobně nejvyšší význam pro zvýšení účasti cílové populace ve screeningu. Podíl gynekologů na screeningu přesáhl jen těsně 8 %. Podíl screeningové kolonoskopie zvolené jako alternativa TOKS byl zanedbatelný a znamenal méně než 1 % screeningových výkonů. Přitom v letech 2009 – 2012 stouplo pokrytí z 19 % na 25 % a ve věkové kategorii 60 – 69 let až na 30 % [11].
Ve stejném období však vzrostla nejen účast ve screeningu, ale i míra pozitivity testů, a to v průměru téměř dvojnásobně z 3,9 % v roce 2008, na 6,7 % v roce 2011. Navíc jsme zaznamenali významnou variabilitu v pozitivitě v závislosti na regionech České republiky; 3,9 – 13,9 %. Do výsledků se promítla i skutečnost, že na sklonku roku 2009 výbory Gastroenterologické společnosti a Společnosti všeobecného lékařství (SVL) ČLS JEP doporučily ukončit používání guajakových testů s nižší senzitivitou [12].
Zvýšení zájmu o screening, navíc umocněné zavedením adresného zvaní od 1. ledna 2014 spolu se zvýšenou pozitivitou testů, znamená logicky zvýšení nároků na kolonoskopické kapacity a vede k prodlužování čekací doby. Vyšší pozitivita testů a jejich variabilita vybízí k zamyšlení nad falešnou pozitivitou, která je nejčastěji kritizovanou charakteristikou testů na okultní krvácení ve screeningu KRK.
Vzhledem k tomu, že TOKS je všeobecnými praktickými lékaři (VPL) a gynekology vykazován jednotným kódem bez ohledu na typ testu, nemáme k dispozici data o tom, jaké testy se aktuálně v praxi používají a s jakým nastavením citlivosti. Proto jsme připravili a uskutečnili průzkum mezi všeobecnými praktickými lékaři s cílem tyto skutečnosti zjistit.
Metodika
Průzkum mezi VPL obsahoval jedinou otázku: Jaký test používáte při screeningu KRK ve Vaší praxi?
Jednalo se o průřezový průzkum s cílem oslovit alespoň 10 % VPL během měsíce února v roce 2014. Paralelně byly použity tři cesty: 1. telefonický průzkum náhodně vybraných deseti ordinací v každém ze 14 regionů ČR, 2. průzkum s využitím náhodně vybraných mailů praxí a 3. průzkum na regionálních edukačních seminářích SVL ČLS JEP, které probíhají pravidelně každý měsíc ve všech krajích.
Výsledky
Celkem bylo osloveno 778 VPL a získáno 522 odpovědí, což představuje 67% výtěžnost průzkumu a informace od 10,2 % lékařů z celkového počtu 5 117 VPL v ČR. Telefonický průzkum vykázal 100% návratnost u 140 oslovených lékařů. Na 314 zaslaných mailů odpovědělo 207 lékařů (návratnost 66 %) a 175 odpovědí bylo získáno na seminářích SVL ČLS JEP (návratnost 54 %) (tab. 1).
Table 1. Návratnost odpovědí podle zvolené metodiky oslovení. Tab. 1. Response rate by the chosen method. 
V telefonické části bylo zjištěno, že 66 % VPL používá ve své praxi imunochemický test kazetový, 20 % VPL vyhodnocuje testy na POCT analyzátorech, 5 % VPL zůstává u gTOKS a 9 % dotázaných odesílá test k vyhodnocení do laboratoře (tab. 2).
Table 2. Zastoupení využívaných metod zjištěných na základě telefonického dotazování. Tab. 2. Representation of the methods identified using telephone interviews. 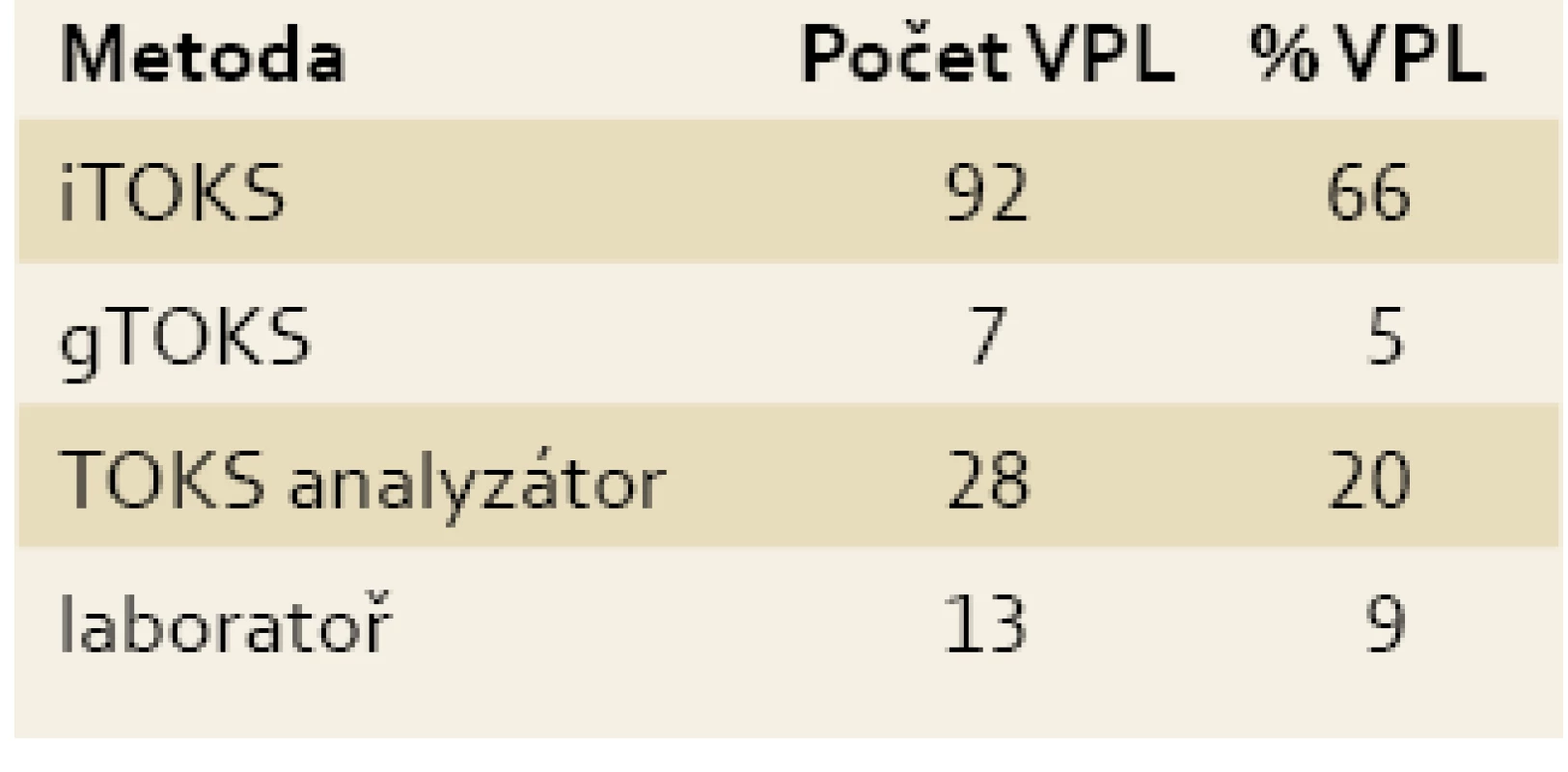
Na základě dotazníkové akce v rámci seminářů pro VPL bylo zjištěno, že 63,5 % VPL používá ve své praxi imunochemický test kazetový, 22 % VPL vyhodnocuje testy na POCT analyzátorech, 2,5 % VPL zůstává u gTOKS a 12 % dotázaných odesílá test k vyhodnocení do laboratoře (tab. 3).
Table 3. Zastoupení využívaných metod zjištěních ná základě dotazování v rámci seminářů. Tab. 3. Representation of the methods identified using CME sessions. 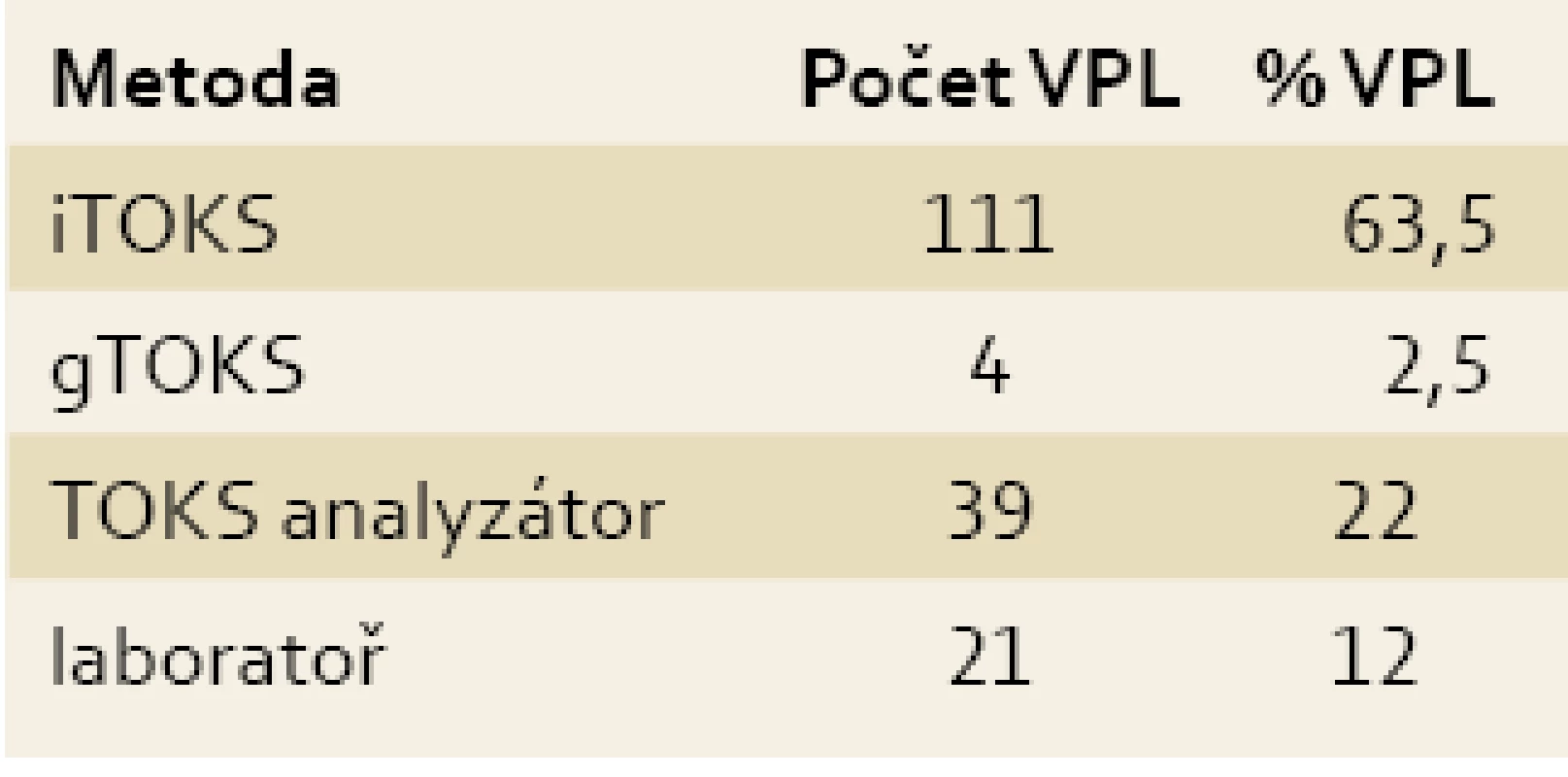
Z e-mailové části vyplývá, že 68,5 % VPL používá ve své praxi imunochemický test kazetový, 27 % VPL vyhodnocuje testy na POCT analyzátorech, 1,5 % VPL zůstává u gTOKS a 3 % dotázaných odesílají test k vyhodnocení do laboratoře (tab. 4).
Table 4. Zastoupení využívaných metod zjištěních ná základě dotazování v rámci emailové komunikace. Tab. 4. Representation of the methods identified using email communication. 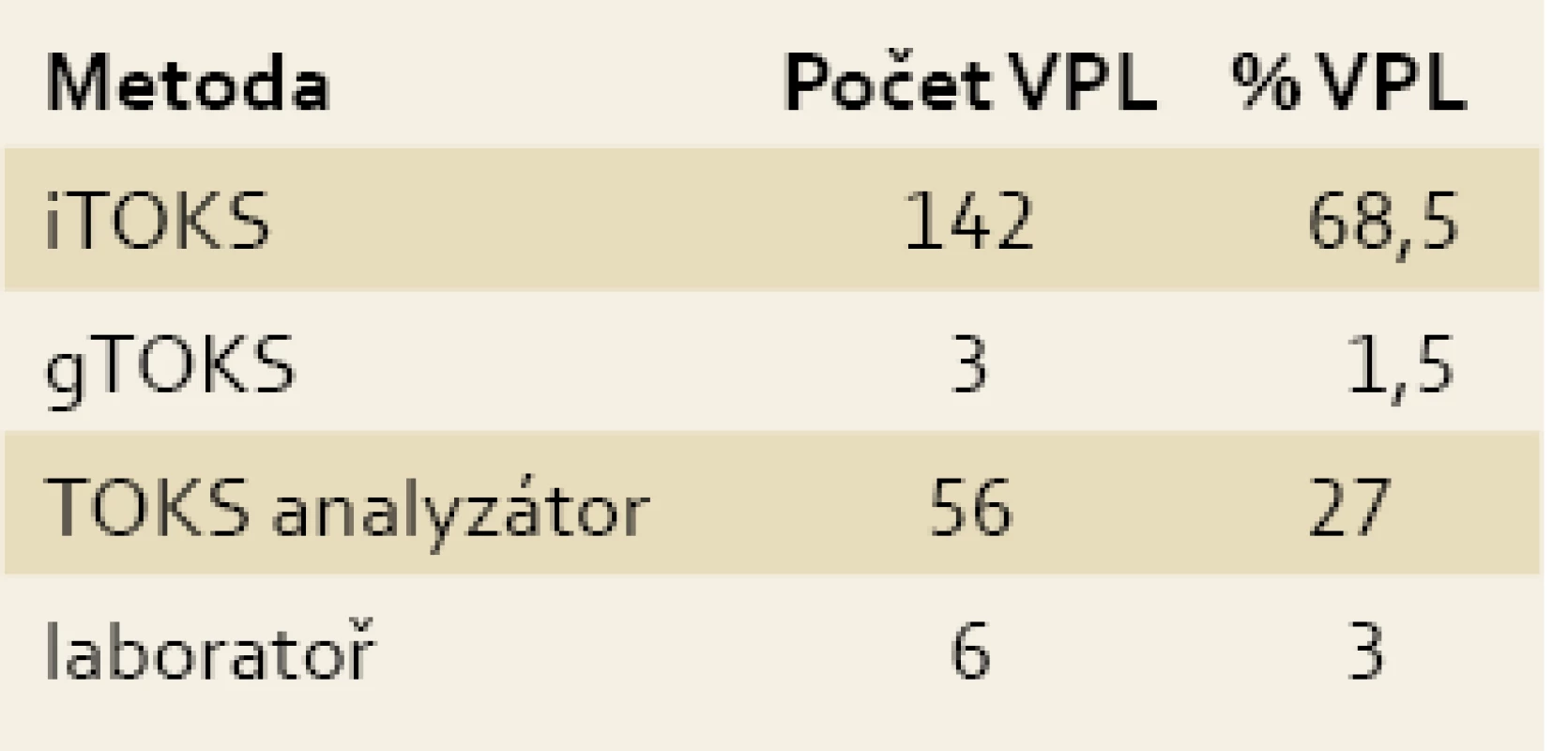
Přestože byly zvoleny tři různé metody sběru dat, výsledky zjištěné jednotlivými metodami nevykazovaly významné rozdíly. Při shrnutí všech tří částí je zastoupení následovné: 1. kazetové testy iTOKS 66 %, iTOKS analyzátor 23,5 %, gTOKS 3 % a laboratorní vyhodnocení 7,5 % (tab. 5). Nebyly zjištěny statisticky významné rozdíly mezi lékaři v závislosti na regionu.
Table 5. Celkové výsledky na základě shrnutí všech předchozích metod (telefon, emailová komunikace, semináře). Tab. 5. Overall results on the basis of a summary of all previous methods (phone, e-mail communication, CME sessions). 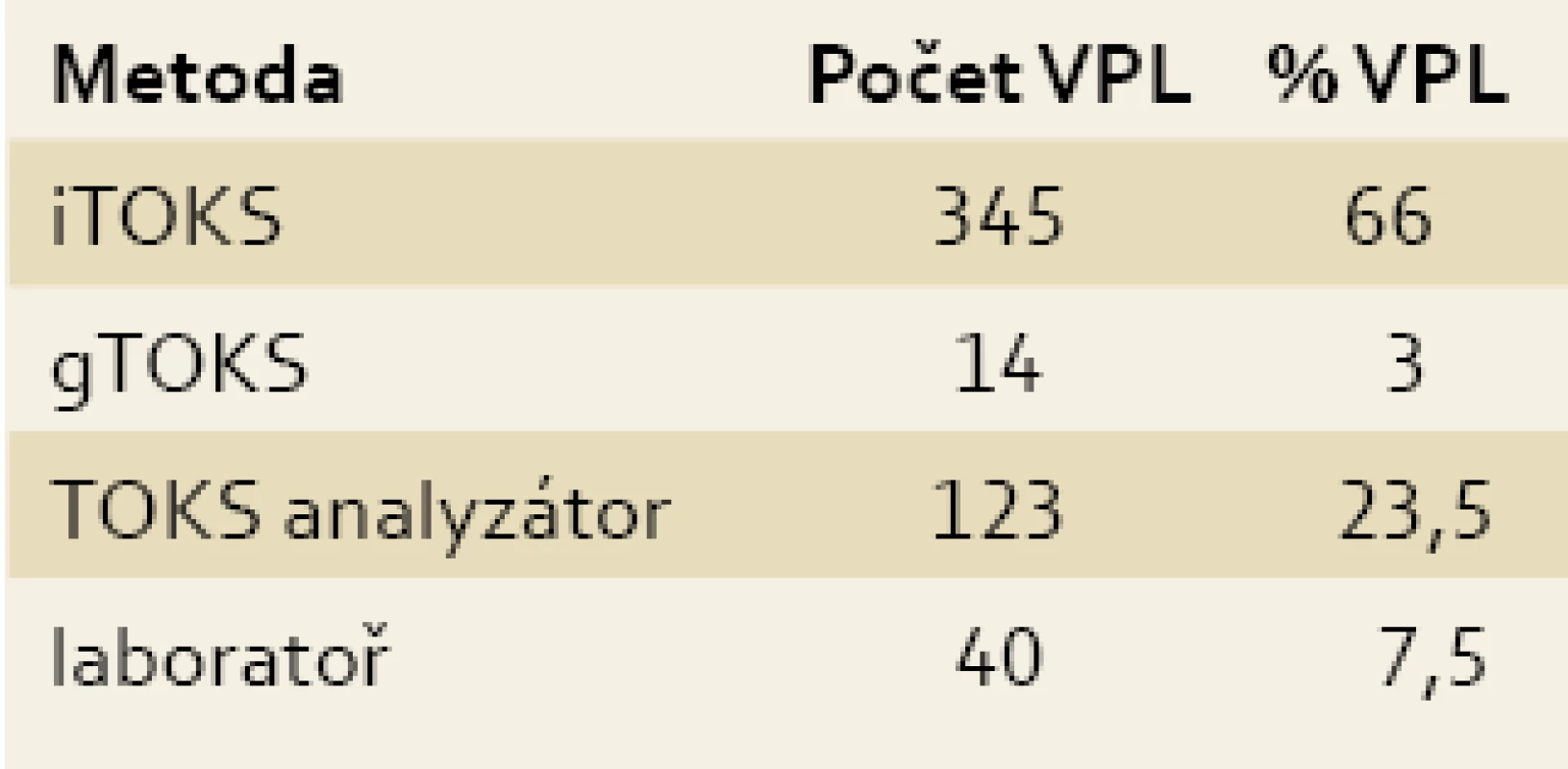
VPL uvedli osm různých typů kazetových iTOKS a tři typy POCT analyzátorů. Zjištěná nastavení cut-off u kazetových iTOKS byla v rozmezí od 10 ng/ ml do 200 ng/ ml. Ceny testů kolísaly od 28 Kč do 168 Kč.
Diskuze
Výstupy průzkumu vysvětlují vyšší pozitivitu TOKS a také její vysokou variabilitu. 97 % lékařů používá v praxi imunochemické testy, guajakové testy jsou prakticky odbourány. Nejvyšší podíl připadá na jednoduché, levné, uživatelsky příjemné kvalitativní kazetové testy. Tyto testy jsou nejspíše zodpovědné za zvýšení pozitivity a její vysokou variabilitu.
Podíl testů vyhodnocovaných na POCT analyzátorech odpovídá očekávání. Po roce 2010 došlo paradoxně k poklesu úhrady TOKS na základě přepočítání materiálových nákladů na nejlevnější guajakový test. Test na POCT analyzátorech je tak hraničeně rentabilní.
Překvapivým zjištěním v průzkumu je 8 % testů odesílaných VPL k vyhodnocení v laboratoři. Z průzkumu nevyplývá, zda jsou tyto kódy lékařem vykazovány či nikoli. Jak bylo výše uvedeno, laboratoř screeningový TOKS vykazovat nemůže, a tak se může jednat o šedý screening, který nemůže být datově zpracováván. Může to souviset se skutečností, kterou udávají pojišťovny, že zhruba 5 – 10 % VPL screeningové kódy nevykazuje.
Autoři studie vnímají zjištění z průzkumu jako závažná. Český pacient může získat od deseti různých praktických lékařů deset různých testů, každý s jiným nastavením citlivosti. Zatímco u jednoho lékaře má pravděpodobnost pozitivního výsledku TOKS 1 : 25, u druhého může jít o pravděpodobnost 1 : 8. To je eticky nepřijatelná variabilita, která ovlivňuje kvalitu a bezpečnost národního screeningového programu KRK.
V ČR probíhá intenzivní kampaň ke zvýšení účasti ke screeningu, která není vyvážena dostatečným vysvětlením všech souvislostí screeningu k informovanému rozhodování osob o účasti ve screeningu. Informované rozhodování občanů je dnes vnímáno jako zásadní ve Velké Británii, Nizozemsku, Francii a ve Skandinávii [13–15]. Právě informace o limitech TOKS, o možném překrývání normálních a abnormálních výsledků, falešné negatitivě a pozitivitě, je považována za zásadně důležitou. Aktuální variabilitu testů v ČR nelze pacientům vysvětlit.
Evropská doporučení pro zajištění kvality ve screeningu a diagnostice KRK doporučují pro národní programy pouze laboratorní kvantitativní imunochemické testy [16,17], a to především z důvodu zajištění externí kontroly kvality, standardizace a možnosti nastavení a případné změny cut-off podle potřeb programu [18,19]. Kvalitativní kazetové TOKS jsou používané i v zahraničí, ale nemají úhradu v systematických programech kolorektálního screeningu v Evropě. Na druhou stranu, většina evropských zemí, včetně Velké Británie, používá ve svých národních programech ještě testy guajakové [20].
Závěr
ČR zavedením imunochemických testů zvýšila výkonnost i efektivitu screeningu KRK a do jisté míry předstihla Evropu. Ovšem za cenu toho, že jsou v programu používány testy s nejrůznějším nastavením citlivosti, které nemohou zaručit standardní testování pro občany v různých ordinacích, stejnou míru citlivosti, a tím i stejný přístup k prevenci. Navíc ve spojitosti se zavedením adresného zvaní od 1. ledna 2014 narůstají čekací doby a zhoršuje se dostupnost kolonoskopie. Situaci si uvědomují jak organizátoři screeningu, tak zástupci poskytovatelů. Komise MZ pro KRK spolu se SVL ČLS JEP a Sdružením praktických lékařů ČR připravila opatření, která by měla zajistit v blízké době používání jen imunochemických testů s nastavením limitu citlivosti na 75 ng/ ml, event. 100 ng/ ml podle potřeb programu.
Lze předpokládat, že navržená opatření představují přechodné řešení a že i ČR, pod tlakem evropských kritérií kvality screeningu KRK, postupně přejde k používání iTOKS s nastavitelným cut-off a zajištěnou externí kontrolou kvality.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Doručeno: 6. 2. 2015
Přijato: 17. 5. 2015
MUDr. Norbert Král
Ústav všeobecného lékařství
1. LF UK v Praze
Albertov 7, 120 00 Praha 2
norbert.kral@seznam.cz
Sources
1. Brenner H, Tao S. Superior diagnostic performance of faceal immunochemical tests for haemoglobin ina head - to - head comparison with guiac based faecal occult blood tests among 2235 participants of screening colonoscopy. Eur J Cancer 2013; 49 : 3049 – 3054. doi: 10.1016/ j.ejca.2013.04.023.
2. Guittet L, Guillaume E, Levillain G et al. Analytical comparison of three quantitative immunochemical fecal occult blood tests for colorectal cancer screening. Cancer Epidemiol Biomarkers Prev 2011; 20 : 1492–1501. doi: 10.1158/1055-9965.EPI-10-0594.
3. Denters M, Deutekom M, Fockens Pet al. Implementation of population screen-ing for colorectal cancer by repeated fecal occult blood test in the Netherlands. BMC Gastroenterol 2009; 9 : 28. doi: 10.1186/ 1471 - 230X - 9 - 28.
4. American College of Obstetricians and gynecologists. Committee Opinion No 482.Colonoscopy and colorectal cancer screening strategies. Obstet Gynecol 2011; 117(3): 766 – 771. doi: 10.1097/ AOG.0b013e3182147930.
5. Menees SB, Inadomi J, Elta G et al. Colorectal cancer screening compliance and contemplation in gynecology patients. J Women Health 2010; 19(5): 911 – 916.
6. Hol L, Wilschut JA, van Ballegooijen Met al. Screening for colorectal cancer: random comparison of guaiac and immunochemical faecal occult blood testing at different cut-off levels. Br J Cancer 2009; 100(7): 1103–1110. doi: 10.1038/sj.bjc.6604961.
7. Faivre J, Dancourt V, Lejeune C. Screening for colorectal cancer with immunochemical faecal occult blood tests. Dig Liver Dis 2012; 44(12): 967 – 973. doi: 10.1016/ j.dld.2012.07.004.
8. Berchi C, Guittet L, Bouvier V et al. Cost-effectiveness analysis of the optimal threshold of an automated immunochemical test for colorectal cancer screening: performances of immunochemical colorectal cancer screening. Int J Technol Assess Health Care 2010; 26(1): 48 – 53. doi: 10.1017/ S0266462309990808.
9. Kuipers EJ, Rösch T, Bretthauer M et al. Colorectal cancer screening - optimizing current strategies and new directions. Nat Rev Clin Oncol 2013; 10(3): 130 – 142. doi: 10.1038/ nrclinonc.2013.12.
10. Kral N, Seifert B, Dušek L et al. Změny ve screeningu kolorektálního karcinomu – krok správným směrem? Onkologie 2010; 4(4): 251 – 255.
11. Dusek L et al. Epidemiology, prevention and treatment of colorectal cancer based on available studies and data. Prague: University Hospital Motol 2012.
12. Zavoral M, Fric P, Suchanek S et al. Národní program screeningu sporadického kolorektálního karcinomu (KR-CA): vývoj, současnost, perspek. Lékařské listy 2013 : 16–18.
13. von Wagner C, Semler C, Good A et al. Health literacy and self - efficacy for participating in colorectal cancer screening: the role of information processing. Patient Educ Couns 2009; 75(3): 352 – 357. doi: 10.1016/ j.pec.2009.03.015.
14. Jepson RG, Hewison J, Thompson A et al. Patient perspective on information and choice in cancer screening: a qualitative study in UK. Soc Sci Med 2007; 65(5): 890 – 899.
15. Weller DP, Patnick J, McIntosh H et al. Uptake in cancer Screening programmes. Lancet Oncol 2009; 10(7): 693 – 699. doi: 10.1016/ S1470 - 2045(09)70145 - 7.
16. von Karsa L, Patnick J Segnan N et al. European Colorectal Cancer Screening Guidelines Working Group. European guidelines for quality assurance in colorectal cancer screening and diagnosis: overview and introduction to the full supplement publication. Endoscopy 2013; 45(1): 51 – 59. doi: 10.1055/ s - 0032 - 1325997.
17. Segnan N, Patnick J, von Karsa L. European guidelines for quality assurance in colorectal cancer screening and diagnosis. 1st ed. Luxembourg: Publications Office of the European Union 2010.
18. Sakata N, Sakata Y, Shimoda R et al. Repeated screening with fecal immunochemical tests reduced the incidence of colorectal cancers in Saga, Japan. Hepatogastroenterology 2014; 61(133): 1224 – 1228.
19. Stock C, Ihle P, Schubert I et al. Colonoscopy and fecal occult blood test use in Germany: results from a large insurance-based cohort. Endoscopy 2011; 43(9): 771 – 781. doi: 10.1055/ s - 0030 - 1256504.
20. Weller D, Coleman D, Robertson Ret al. The UK colorectal cancer screening pilot: results of the second round of screening in England. Br J Cancer 2007; 97(12): 1601 – 1605.
Labels
Paediatric gastroenterology Gastroenterology and hepatology Surgery
Article was published inGastroenterology and Hepatology
2015 Issue 3-
All articles in this issue
- Digestivní endoskopie
- Kvíz
- Torpidní průběh herpetické ezofagitidy u imunokompetentní pacientky – videokazuistika
- Biliární papilomatóza – raritní příčina obstrukčního ikteru
- Doporučené postupy chirurgické léčby pacientů s idiopatickými střevními záněty – 2. část: Crohnova nemoc
- Budd-Chiariho syndrom u těhotné pacientky s Crohnovou chorobou
- Dysfunkce dolní části gastrointestinálního traktu u kriticky nemocných – současný pohled
- Těžký průběh kortikodependentní ulcerózní kolitidy u malého dítěte před érou biologické terapie
- Variabilita testů na okultní krvácení používaných praktickými lékaři ve screeningu kolorektálního karcinomu v České republice
- Správná odpověď na kvíz
- Trombotická mikroangiopatie z pohledu nefrologa
- Saccharomyces boulardii – probiotická kvasinka z Indočíny
- Autodidaktický test: digestivní endoskopie
- Žliabková (paraduodenálna) pankreatitída – séria šiestich pacientov
- Gastroenterology and Hepatology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Saccharomyces boulardii – probiotická kvasinka z Indočíny
- Žliabková (paraduodenálna) pankreatitída – séria šiestich pacientov
- Doporučené postupy chirurgické léčby pacientů s idiopatickými střevními záněty – 2. část: Crohnova nemoc
- Trombotická mikroangiopatie z pohledu nefrologa
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

