-
Medical journals
- Career
Súčasné možnosti diagnostiky a liečby diabetickej retinopatie a diabetického edému makuly
Authors: Mária Molnárová
Authors‘ workplace: VIKOM, s. r. o., 1. žilinské očné centrum, Žilina 1; Očná klinika JLF UK, Martin 2
Published in: Forum Diab 2019; 8(2): 106-110
Category: Review Article
Overview
V nastávajúcom desaťročí sa predpokladá prudký nárast DM, a tým aj diabetickej retinopatie. Zlepšenie diagnostických a terapeutických možností podstatnou mierou zlepšuje a urýchľuje klinickú a sociálnoekonomickú efektívnosť terapeutických procesov. V liečbe PDR dominuje stále laserkoagulačná liečba. V liečbe diabetického edému makuly laserovú liečbu vystriedala intravitreálna farmakoterapia s antirastovými faktormi. Steroidy intravitreálne ostávajú rezervované pre chroniocký edém makuly. Chirurgická liečba – pars plana vitrektómia – je indikovaná pre rozvinutú proliferatívnu diabetickú retinopatiu a chronický pretrvávajúci diabetický edém makuly nereagujúci na intravitreálnu antiVEGF ani na steroidnú liečbu.
Klíčová slova:
A OCT – antiVEGF – diabetická retinopatia – diabetický edém makuly – FAG – chirurgická liečba – intravitreálna liečba – laserová liečba – OCT
Úvod
Prevalencia diabetickej retinopatie (DR) a diabetického edému makuly (DEM) v celom svete narastá. Vo vyspelých krajinách sveta je DR najčastejšou príčinou nových prípadov slepoty u pacientov v produktívnom veku (20–65 rokov). Hlavnými rizikovými faktormi pre vznik DR, resp. progresiu preexistujúcej diabetickej retinopatie podľa štúdií ETDRS, DCCT, UKPDS a FIELD, sú: trvanie DM, metabolická kontrola DM (HbA1c > 7,0 %), nedostatočná kompenzácia arteriálnej hypertenzie, nedostatočná kontrola metabolizmu tukov, anémia a gravidita [1–4].
Diabetická retinopatia je termín pre prítomné mikrovaskulárne abnormality na sietnici pacienta s diabetes mellitus (DM) pozorované oftalmoskopickým vyšetrením sietnice alebo zobrazením na farebnej fotogtafii fundu (sietnice) [5].
Príznaky a diagnostika
Hlavné príznaky neproliferatívnej DR sú mikroaneuryzmy (MA), intraretinálne hemorágie, tvrdé exsudáty, mäkké vatovité ložiská, intraretinálne mikrovaskulárne abnormality (IRMA), flebopatia a nonperfúzne zóny. Pre proliferatívnu diabetickú retinopatiu sú tyické preretinálne alebo sklovcové plošné hemorágie, fibrovaskulárne proliferatívne pruhy a membrány bez alebo s trakčným odlúpením sietnice.
Diabetický edém makuly môže byť prítomný pri oboch formách diabetickej retinopatie (obr. 1).
Image 1. Klinické parametre a štandardná zobrazovacia vyšetrovacia metóda – fluoresceínová angiografia – sú stále základom diagnostiky diabetickej retinopatie. Obr. 1a | Závažná neproliferatívna diabetická retinopatia Obr. 1b | Fluoresceínová angiografia závažnej neproliferatívnej diabetickej retinopatie, artério-venózna fáza. Archív autorky 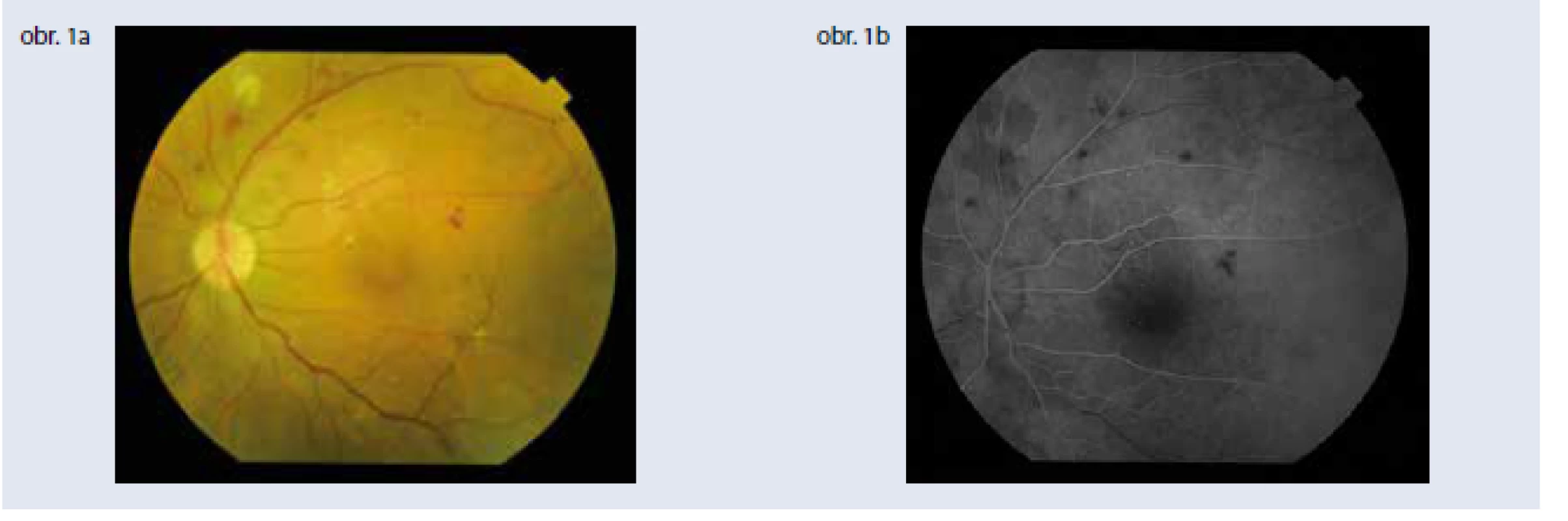
Fluoresceínová angiografia (FAG) posudzuje závažnosť patológie a zobrazuje presakujúce lézie vhodné na uzavretie cielenou fokálnou laserovou liečbou a neperfundované arey v periférii sietnice, ktoré ak sú plošné, sú indikáciou na laserovú liečbu sietnice s cieľom znížiť produkciu rastových faktorov, tzv. panretinálnu laserkoaguláciu [6].
FAG predstavuje v diagnostike diabetického edému stále zlatý štandard. Dokáže rozlíšiť a zobraziť dôležité znaky DR a DEM, ako sú mikroaneuryzmy, proliferácie, ischemické oblasti a diabetický edém makuly, ktorý je výsledkom presakovania pri cievnom ochorení sietnicových kapilár [7].
Optická koherentná tomografia (OCT) je neinvazívna zobrazovacia vyšetrovacia metóda, ktorá zobrazuje sietnicu v reze in vivo v rozlíšení 3 až 5 μm. OCT meria hrúbku sietnice, umožňuje rozlíšenie presakujúcich mikroaneuryziem od nepresakujúcich, zobrazuje voľnú tekutinu (edém) v jednotlivých vrstvách sietnice, vykazuje morfologické znaky a charakteristiky a diagnostikuje typy DEM. Táto neinvazívna zobrazovacia vyšetrovacia metóda sa využíva na skríning DR a DEM, klasifikáciu DR a DEM, na monitorovanie vývoja ochorenia a hodnotenie liečby DEM (obr. 2) [8,9].
Image 2. Optická koherentná tomografia. Obr. 2a | Optická koherentná tomografia normálnej makuly Obr. 2b | Optická koherentná tomografia diabetického cystoidného edému makuly. Archív autorky 
Angio-OCT (A-OCT) je nová neinvazívna zobrazovacia vyšetrovacia metóda, ktorá bez použitia kontrastu intravenózne zobrazuje separátne povrchovú a hlbokú kapilárnu sieť sietnice, vonkajšie vrstvy – komplex pigmentový epitel sietnice s fotoreceptormi a extra cievovku. Ako kontrast táto metóda využíva prúdenie erytrocytov v krvi. Princíp A-OCT umožňuje presné vyhodnotenie lokalizácie a veľkosti patologickej lézie v jednotlivých vrstvách sietnice. Nezobrazuje niektoré stredné mikroaneuryzmy, ktoré detekujeme oftalmoskopicky, pretože spomalený krvný prúd v takýchto mikroaneuryzmách je nedostatočný na vytvorenie dekorelačného signálu potrebného na jej zobrazenie. Má však schopnosť zobraziť veľmi malé suboftalmoskopické mikroaneuryzmy, ktoré nie sú detekovateľné oftalmoskopicky, ani pomocou FAG (malé mikroaneuryzmy – majú pomerne rýchly prietok krvi dostatočný na vytvorenie dekorelačného signálu A-OCT). Preto môžeme diagnostikovať už suboftalmoskopické štádiá neproliferatívnej diabetickej retinopatie (NPDR). A-OCT zobrazuje abnormality sietnicovej vaskulatúry alebo abnormality v choriocapillaris, ako sú mikroaneuryzmy, remodelácia ciev v blízkosti fyziologickej avaskulárnej zóny fovey (FAZ), rozšírenie FAZ, rozšírenie interkapilárnych priestorov, ktoré pomocou FAG nie je možné zobraziť, kapilárna tortuozita a dilatácia (intraretinálne mikrovaskulárne abnormality) a nonperfúzne zóny (obr. 3) [10,11].
Image 3. Angio-OCT: závažná NPDR s fokálnym diabetickým edémom makuly. Archív autorky 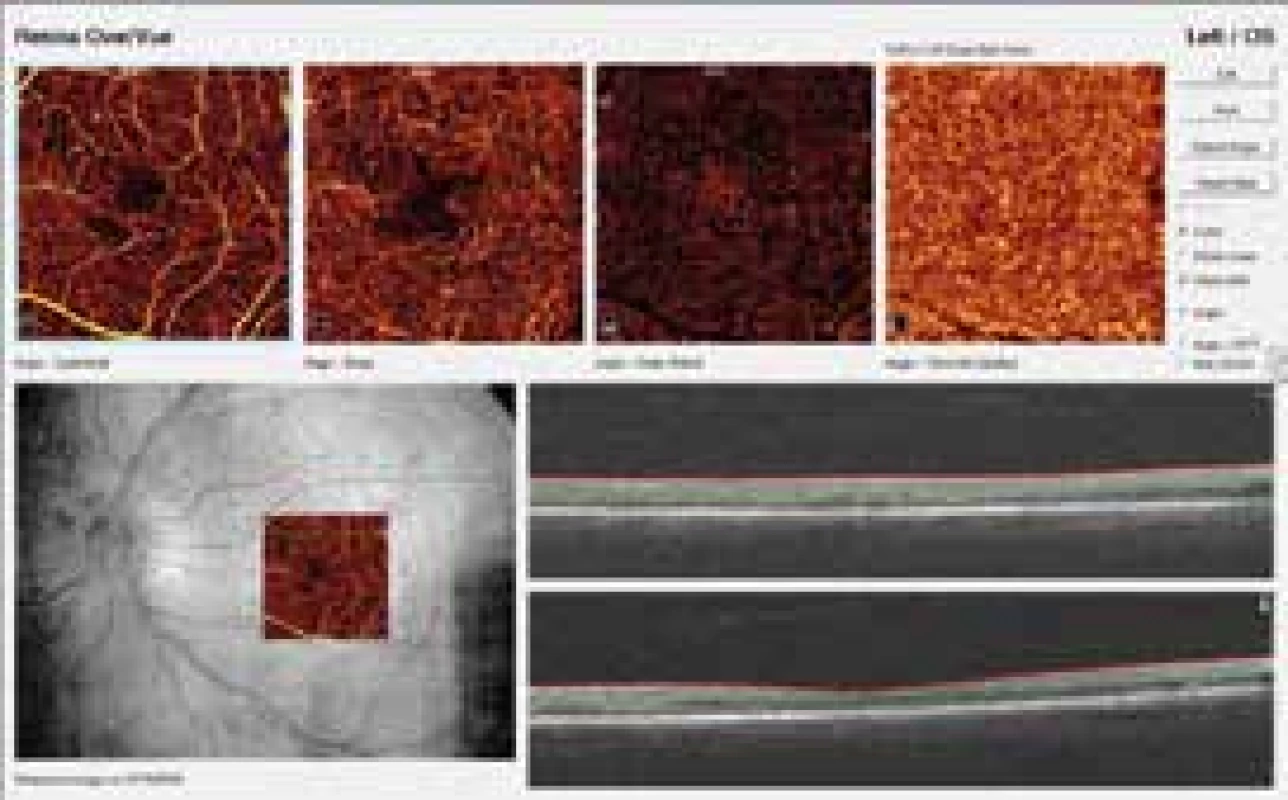
Liečba
V minulosti neexistoval žiaden spôsob liečby diabetickej retinopatie.
Prvým a zásadným prepodkladom akejkoľvek liečby DR a DEM je dobrá kontrola glykémií, čo potvrdili výsledky veľkých štúdií DCCT, UKPDS a FIELD [2–4].
V roku 1956 Mayer Schwickerat ako prvý na svete použil na liečbu diabetickej retinopatie xenónovú výbojku a Maiman v roku 1980 argónový laser. Využitie laserového lúča v liečbe diabetickej retinopatie predstavoval prvý zásadný prelom a pre 50 % pacientov s diabetickou retinopatiou znamenal laser záchranu zraku. Na základe klinických štúdií DRS, ETDRS, DRCR.net a T-protokol sa laserová liečba dodnes používa pri:
- proliferatívnej diabetickej retinopatii (DRS) [12]
- fokálnom diabetickom edéme makuly [7,13]
Pri proliferatívnej diabetickej retinopatii sa robí tzv. panretinálna laserkoagulácia (obr. 4). Je to „deštrukčná“ liečebná metóda, pri ktorej sa po funde rovnomerne aplikuje 2 000 až 3 000 laserových zásahov veľkosti 200 až 300 μm s vynechaním centrálnej krajiny a okolia terča zrakového nervu. Podstatou tejto liečby je deštrukcia 30 až 40 % hypoxickej sietnice, čím sa dosiahne presun nespotrebovaného kyslíka do susedných nekoagulovaných okrskov sietnice a jej vnútorných vrstiev a na zadný pól fundu (TZN a makula). V dôsledku zlepšenia oxygenácie sietnice nastane zníženie až zastavenie tvorby rastových faktorov pôvodne ischemickým tkanivom sietnice, následne dochádza k uzatváraniu a involúcii neovaskularizácií a k zníženiu patologickej permeability sietnicových kapilár. Pri fokálnom diabetickom edéme makuly sa presakujúce lézie detekujú pomocou FAG a cielene sa laserom uzavrú. Existujúci edém sa vstrebe a nový nevznikne [5]. V posledných rokoch sa odporúča používať na laserovú liečbu DEM a DR podprahové lasery [14].
Image 4. Stav po panretinálnej laserkoagulácii sietnice. Archív autorky 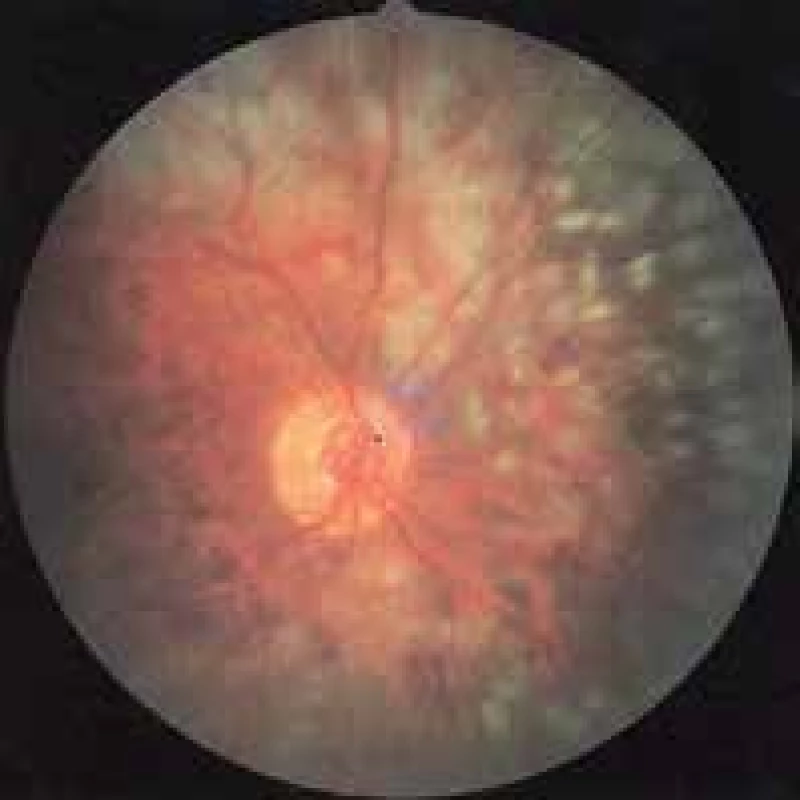
Objavením antiVEGF začala nová éra liečby diabetického edému makuly. V roku 2012 sa začalo s intravitreálnou farmakologickou liečbou injekciami antirastových faktorov a neskôr aj steroidov (obr. 5). Veľké klinické štúdie RIDE/RISE [15], RESTORE [13], VIVID, VISTA [16], DRCR.net a T-protokol [17] vykázali vysokú účinnosť a bezpečnosť liečby DEM antirastovými faktormi. Zo záverov klinických štúdií vyplýva viac liečebných režimov vedúcich k zlepšeniu a stabilizácii anatomického aj funkčného nálezu pri DEM a DR.
Image 5. Intravitreálna liečba DEM intravitreálnou injekciou antiVEGF a steroidov 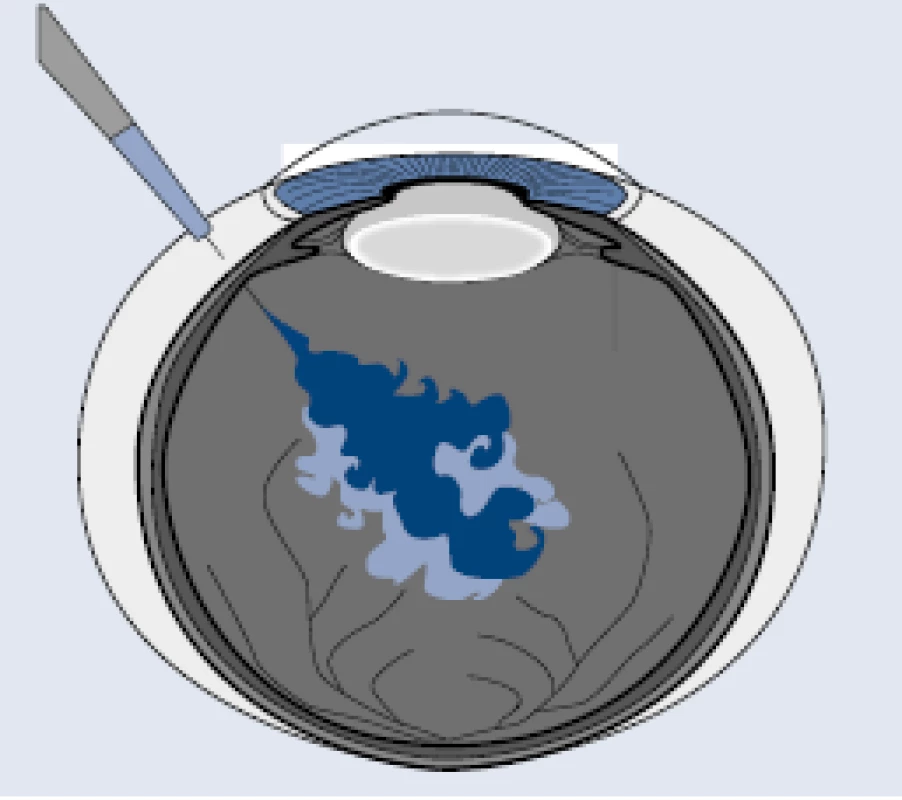
Fixný režim aplikácií predstavuje 3 až 5 nasycovacích dávok = intravitreálne injekcie 1-krát mesačne a potom podľa použitej molekuly antiVEGF pokračovanie buď raz za 1, alebo raz za 2 mesiace až do štádia, kedy sa dosiahnuté zlepšenie nezastabilizuje [13,15].
Pri liečebnom režime „pro re nata“ (PRN) po 3 nasycovacích intravitreálnych injekciách v 1-mesačných intervaloch každá ďalšia injekcia sa indikuje a aplikuje pri pretrvávaní alebo objavení sa aktivity (edému). Pri tomto režime je určité riziko podliečenia [5].
Pri liečebnom režime Treat & Extend (TE) sa po 3–5 nasycovacích intravitreálnych injekciách v 1-mesačných intervaloch postupne predlžuje interval medzi injekciami vždy o 2 týždne a pomocou OCT sa sleduje najdlhší interval medzi injekciami, ktorý stačí na udržanie dosiahnutej stabilizácie nálezu. Výhodnosť tohto liečebného režimu potvrdili klinické štúdie RETAIN a DRCR.net. T-protokol [18,19]. V praxi sa rutinne používajú ranibizumab a aflibercept, off-label aj bevacizumab.
V liečbe diabetickej retinopatie a hlavne diabetického edému makuly majú svoje opodstatnenie aj steroidy aplikované intravitreálne na nosičoch. Steroidy v etiopatogenéze DR a DEM znižujú hladinu zápalových mediátorov, hlavne prostaglandínov, interleukínov IL6 a IL8, znižujú transkripciu a tvorbu rastových faktorov: TNF, PDFG a VEGF a znižujú cez ovplyvnenie ICAM1 leukostázu a cievnu permeabilitu [20]. Účinnosť a bezpečnosť liečby potvrdili klinické štúdie DRCR net. B a I-protokol , štúdie PLACID, MEAD, CHROME a FAME [21,22].
Steroidy intravitreálne sú odporúčané ako druhá voľba, ak DEM nereguje na intravitreálnu liečbu s antiVEGF.
PDR s možnými komplikáciami je najstaršou a stále platnou indikáciou na chirurgickú liečbu – pars plana vitrektómiu s vnútornou tamponádou vzduchom, expanzným plynom, prípadne silikónovým olejom (obr. 6).
Image 6. Pars plana vitrektómia, membranektómia fibrovaskulárnej membrány a endolaserkoagulácia. Upravené podľa [25] ![Pars plana vitrektómia, membranektómia fibrovaskulárnej membrány a endolaserkoagulácia.
Upravené podľa [25]](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image_pdf/87767652a3f1c9b06a9eaa0b2763aa31.png)
Chirurgická liečba má opodstatnenie aj pri DEM refraktérnom na intravitreálnu farmakoterapiu s antiVEGF a steroidmi. Vlastnosti zmeneného sklovca u diabetikov môžu súvisieť s vývojom DEM. Vitreomakulárna trakcia môže byť významnou mierou zodpovedná za vznik a udržanie DEM. Pracovná teória vysvetľuje opodstatnenosť chirurgickej liečby aj refraktérneho DEM bez evidentnej trakcie: odstránenie patologického sklovca a subklinickej trakcie, eliminácia zápalových častíc, zlepšenie permeability sietnicových ciev, zlepšenie koncentrácie kyslíka môžu viesť k normalizácii krvného prietoku v makule, k zníženiu permeability, a tým k redukcii edému makuly [23,24].
Záver
Liečba DEM sa v poslednom desaťročí výrazne zmenila v súvislosti s vývojom antiVEGF a vývojom a možnosťou ich intravitreálnej aplikácie formou intravitreálnych injekcií. Druhá línia liečby DEM súvisí s vývojom dexametazónových sklovcových implantátov. Chirurgická liečba sa odporúča pri DEM refraktérnom na intravitreálnu antiVEGF a steroidnú liečbu a pri prítomnom vitreomakulárnom trakčnom syndrome.
MUDr. Mária Molnárová, PhD.
Doručené do redakcie 10. 4. 2019
Prijaté po recenzii 3. 5. 2019
Sources
- Davis MD, Fisher MR, Gangnon RE. Risk factors for high-risk proliferative diabetic retinopathy and severe visual loss: Early Treatment Diabetic Retinopathy Study Report #18. Invest Ophthalmol Vis Sci 1998; 39(2): 233–252.
- Progression of retinopathy with intensive versus conventional treatment in the Diabetes Control and Complications Trial. Diabetes Control and Complications Trial Research Group. Ophthalmology 1995; 102(4): 647–661.
- Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKP - DS 33). UK Prospective Diabetes Study (UKPDS) Group. Lancet 1998; 352(9131): 837–853.
- Keech AC, Mitchell P, Summanen PA et al. Effect of fenofibrate on the need for laser treatment for diabetic retinopathy (FIELD study): a randomised controlled trial. Lancet 2007; 370(9600): 1687–1697.
- Schmidt-Erfurth U, Garcia-Arumi J, Bandello F et al. Guidelines for the Management of Diabetic Macular Edema by the European Society of Retina Specialists (EURETINA). Ophthalmologica 2017; 237(4): 185–222. Dostupné z DOI: <http://doi: 10,1159/000458539>.
- Bresnick GH. Diabetic macular edema. A review. Ophthalmology 1986; 93(7): 989–997.
- Early Treatment Diabetic Retinopathy Study Research Group. Treatment techniques and clinical guidelines for photocoagulation of diabetic macular edema. Early Treatment Diabetic Retinopathy Study Report Number 2. Ophthalmology 1987; 94(7): 761–774.
- Wang H, Chhablani J, Freeman WR et al. Characterization of diabetic microaneurysms by simultaneous fluorescein angiography and spectraldomain optical coherence tomography. Am J Ophthalmol 2012; 153(5): 861–867. Dostupné z DOI: <http://doi: 10.1016/j.ajo.2011.10.005>.
- Schmidt-Erfurth U, Chong V, Loewenstein A et al. Guidelines for the management of neovascular age-related macular degeneration by the European Society of Retina Specialists (EURETINA). Br J Ophthalmol 2014; 98(9): 1144–1167. Dostupné z DOI: <http://doi: 10.1136/bjophthalmol-2014–305702>.
- Hwang TS, Gao SS, Liu L et al. Automated Quantification of Capillary Nonperfusion Using Optical Coherence Tomography Angiography in Diabetic Retinopathy. JAMA Ophthalmol 2016; 134(4): 367–373. Dostupné z DOI: <http://doi: 10.1001/jamaophthalmol.2015.5658>.
- Couturier A, Mane V, Bonnin S et al. Capillary plexus anomalies in diabetic retinopathy on optical coherence tomography angiography. Retina 2015; 35(11): 2384–2391. Dostupné z DOI: <http://doi: 10.1097/IAE.0000000000000859>.
- [The Diabetic Retinopathy Study research Group]. Photocoagulation treatment of proliferative diabetic retinopathy. Clinical application of Diabetic Retinopathy Study (DRS) findings, DRS Report Number 8. Opohthalmology 1981; 88(7): 583–600.
- Mitchell P, Bandello F, Schmidt-Erfurth U et al. The RESTORE study: ranibizumab monotherapy or combined with laser versus laser monotherapy for diabetic macular edema. Ophthalmology 2011; 118(4): 615–625. Dostupné z DOI: <http://doi: 10.1016/j.ophtha.2011.01.031>.
- Lavinsky D, Cardillo JA, Melo LA jr et al. Randomized clinical trial evaluating mETDRS versus normal or high-density micropulse photocoagulation for diabetic macular edema. Invest Ophthalmol Vis Sci 2011; 52(7): 4314–4323. Dostupné z DOI: <http://doi: 10.1167/iovs.10–6828>.
- Nguyen QD, Brown DM, Marcus DM et al. Ranibizumab for diabetic macular edema: results from 2 phase III randomized trials: RISE and RIDE. Ophthalmology 2012; 119(4): 789–801. Dostupné z DOI: <http://doi: 10.1016/j.ophtha.2011.12.039>.
- Korobelnik JF, Do DV, Schmidt-Erfurth U et al. Intravitreal aflibercept for diabetic macular edema. Ophthalmology 2014; 121(11): 2247–2254. Dostupné z DOI: <http://doi: 10.1016/j.ophtha.2014.05.006>.
- Wells JA, Glassman AR, Ayala AR et al. Aflibercept, bevacizumab, or ranibizumab for diabetic macular edema. N Engl J Med 2015; 372(13): 1193–1203. Dostupné z DOI: <http://doi: 10.1056/NEJMoa1414264>.
- Prunte C, Fajnkuchen F, Mahmood S et al. Ranibizumab 0.5 mg treat-and-extend regimen for diabetic macular oedema: the RETAIN study. Br J Ophthalmol 2016; 100(6): 787–795. Dostupné z DOI: <http://doi: 10.1136/bjophthalmol-2015–307249>.
- Wells JA, Glassman AR, Ayala AR et al. Aflibercept, Bevacizumab, or Ranibizumab for Diabetic Macular Edema: Two-Year Results from a Comparative Effectiveness Randomized Clinical Trial. Ophthalmology 2016; 123(6): 1351–1359. Dostupné z DOI: <http://doi: 10.1016/j.ophtha.2016.02.022>.
- Zhang X, Zeng H, Bao S t al. Diabetic macular edema: new concepts in patho-physiology and treatment. Cell Biosci 2014; 4 : 27. Dostupné z DOI: <http://doi: 10.1186/2045–3701–4–27>.
- Boyer DS, Yoon YH, Belfort R jr et al. Three-year, randomized, sham-controlled trial of dexamethasone intravitreal implant in patients with diabetic macular edema. Ophthalmology 2014; 121(10): 1904–1914. Dostupné z DOI: <http://doi: 10.1016/j.ophtha.2014.04.024>.
- Cunha-Vaz J, Ashton P, Iezzi R et al. Sustained delivery fluocinolone acetonide vitreous implants: long-term benefit in patients with chronic diabetic macular edema. Ophthalmology 2014; 121(10): 1892–1903. Dostupné z DOI: <http://doi: 10.1016/j.ophtha.2014.04.019>.
- Bhagat N, Grigorian RA, Tutela A et al. Diabetic macular edema: pathogenesis and treatment. Surv Ophthalmol 2009; 54(1): 1–32. Dostupné z DOI: <http://doi: 10.1016/j.survophthal.2008.10.001>.
- Haller JA, Qin H, Apte RS et al. Vitrectomy outcomes in eyes with diabetic macular edema and vit - reomacular traction. Ophthalmology 2010; 117(6): 1087–1093. e1083. Dostupné z DOI: <http://doi: 10.1016/j.ophtha.2009.10.040>.
- Kanski JJ. Clinical Ophthalmology. 8rd ed. Saunders 2015. ISBN-13 : 978–0702055720. ISBN-10 : 0702055727.
Labels
Diabetology Endocrinology Internal medicine
Article was published inForum Diabetologicum

2019 Issue 2-
All articles in this issue
- Moderné trendy v liečbe diabetu 2. typu a jeho komplikácií v roku 2019
- Implementujeme aktuálne odporúčania ADA/EASD do liečby pacientov s diabetes mellitus 2. typu dostatočne?
- Novinky vo farmakoterapii obezity
- Perspektívy v liečbe dyslipoproteinémií pri diabete
- Moderné trendy v liečbe hypertenzie
- Moderné trendy v lokálnej liečbe diabetickej nohy
- Diabetes mellitus a srdcové zlyhávanie – osudová príťažlivosť
- Súčasné možnosti diagnostiky a liečby diabetickej retinopatie a diabetického edému makuly
- Moderné trendy v liečbe diabetickej nefropatie
- Výber liečby do dvojkombinácie pri nedostatočnej liečbe metformínom samotným: výsledky štúdie DiaSTATUS-2
- Moderné trendy v antiagregačnej liečbe pacientov s diabetes mellitus
- Moderné trendy v liečbe diabetes mellitus u pacientov s hepatopatiami
- Liečba diabetes mellitus 1. typu pomocou inzulínovej pumpy – komu a prečo?
- Odborné odporúčanie k preskripcii diabetes špecifickej roborujúcej výživy s vysokou kalorickou hodnotou pre pacientov s diabetes mellitus a malnutríciou
- Možnosti využitia genetických poznatkov pri diabete 2. typu v klinickej praxi
- Pleiotropné (antiaterogénne) účinky inhibície PCSK9. Áno, či nie?
- Forum Diabetologicum
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Moderné trendy v liečbe hypertenzie
- Novinky vo farmakoterapii obezity
- Moderné trendy v lokálnej liečbe diabetickej nohy
- Liečba diabetes mellitus 1. typu pomocou inzulínovej pumpy – komu a prečo?
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

