-
Medical journals
- Career
Rizikové faktory vzniku tromboembolické nemoci u mladistvých uživatelek hormonální antikoncepce
Authors: M. Havlín; D. Ondrová
Authors‘ workplace: Česká společnost gynekologie dětí a dospívajících
Published in: Čes-slov Pediat 2020; 75 (3): 142-145.
Category:
Overview
Článek se zabývá etiopatogenezí tromboembolické nemoci a analyzuje hlavní rizikové mechanismy jejího vzniku. Text především zdůrazňuje multifaktoriálnost vzniku tromboembolických stavů. Probírá vztah trombofilních mutací k hormonálním léčbám a kvantifikuje jejich rizika. Velký důraz je kladen na prevenci trombofilních podnětů, tj. především na racionální životní styl. Přes všechna rizika je hormonální antikoncepce (při dodržení postupu lege artis) nejspolehlivější antikoncepční metodou a její benefity výrazně převažují nad negativy.
Klíčová slova:
dospívající dívka – hormonální antikoncepce – rizikové faktory trombózy – trombofilní mutace – preskripční doporučení
ÚVOD
V posledních zhruba sto letech se stále více rozevírají nůžky mezi biologickou vyspělostí a společenskou zralostí. V současné době je průměrný věk menarche u českých dívek 12,3 roku (fyziologické rozmezí 10–15 let) a zdá se, že dále se již výrazně nemění. Cca 1–1, 5 roku po menarche převažují anovulační cykly, poté ale nastane převaha cyklů ovulačních a dívka se stává plodnou. Podle dlouhodobých sledování věk koitarche klesal do poloviny 90. let a poté se stabilizoval okolo 17. roku života. Sexuálně aktivních je 70–80 % mladistvých.
Těhotenství mladistvé dívky je nejen medicínsky rizikovější, ale je hlavně společenským problémem spojeným s mnoha negativními sociálně patologickými jevy u matky i dítěte. Antikoncepce je řešením, jak překlenout období mezi biologickou a sociální zralostí a hormonální antikoncepce (HA) je nejúčinnějším nástrojem této snahy.
HORMONÁLNÍ ANTIKONCEPCE
Hormonální antikoncepce (za dodržení postupů lege artis) je dominantní antikoncepční metodou v ČR. HA v současnosti užívá téměř milion žen a ve skupině mladistvých ji najdeme u cca 40 % dívek.
Rozlišujeme dva základní typy HA:
- kombinovanou (obsahuje estrogenní a gestagenní složku),
- gestagenní (obsahuje pouze gestagen) – tato má minimální vliv na riziko trombózy.
Dominantním estrogenem užívaným v kombinované HA je ethinylestradiol (EE). V posledních letech přišly na trh kontraceptiva s dalšími estrogeny velmi blízkými přirozenému estradiolu – estradiol valerátem a estradiol hemihydrátem. Podle dávky EE dělíme kombinovanou HA na:
- vysokodávkovanou (40–50 µg EE) – v současnosti se již nepoužívá,
- nízkodávkovanou (30–35 µg EE),
- velmi nízkodávkovanou (15–20 µg EE).
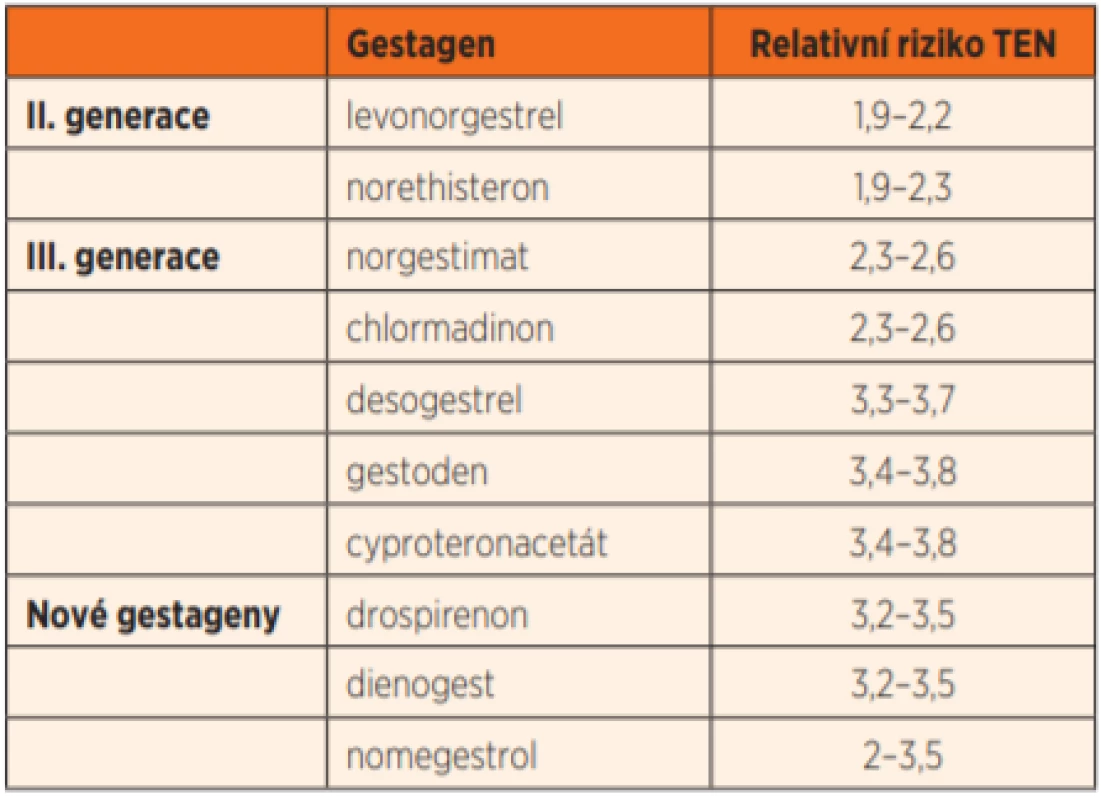
Na rozdíl od estrogenní složky nemá gestagenní komponenta dominantní látku. V historii bylo užito zhruba 50 druhů gestagenů, v současné době je využíváno cca 10. Dělení gestagenů je možné podle chemického složení (od kterého steroidu je molekula odvozena), ale v praxi je užívanější dělení na generace.
Gestageny I. generace se již neužívají, gestageny tzv. II. generace mají reziduální androgenní efekt, ale menší protrombotickou aktivitu. Nejvíce homogenní skupinou jsou gestageny III. generace, které mají minimální androgenní aktivitu a pozitivní vliv na metabolismus lipidů, ale jsou mírně rizikovější v etiologii trombóz – nárůst relativního rizika je udáván na 1,7–3. Skupina nových gestagenů (termín IV. generace se neujal) se svými vlastnostmi podobá gestagenům III. generace. Řada autorů ale členění na generace zpochybňuje a doporučuje hodnotit každý zvlášť.
Přehled základních gestagenů a jejich vztah k riziku TEN ukazuje tabulka 1. Uváděná rizikovost platí při použití v kombinaci s estrogenem.
TROMBOEMBOLICKÁ NEMOC (TEN)
TEN je v současné době nejdiskutovanějším problémem HA. Ten je navíc umocněný značnými mediálními kampaněmi, obvykle velmi pochybné objektivity. Je třeba si uvědomit, že problematika TEN se netýká jen antikoncepce, ale hormonálních terapií obecně:
- HA je u mladistvých nejrozšířenější hormonální léčbou;
- gestagenní či kombinovaná estrogen-gestagenní léčba je užívána ke korekci nepravidelného cyklu;
- HRT (hormonal replacement therapy) se užívá v dorostové gynekologii vzácně, především při těžších formách hormonálních deficitů (dysgeneze gonád, předčasné selhání ovariální funkce apod.);
- metodiky asistované reprodukce se této věkové skupiny netýkají.
V posledních dvou dekádách problematika TEN byla bohužel redukována pouze na vztah HA k trombofilním mutacím, byť se při vzniku trombózy jedná o komplexní multifaktoriální onemocnění (Virchowova trias).
Frekvence TEN je výrazně vázána na věk – u žen do 45 let je incidence idiopatické TEN 1/10 000 žen, ve vyšším věku 10/10 000. Specifická data pro adolescentky nejsou k dispozici. V roce 2012 užívalo HA cca 1,1 milionu uživatelek, což je téměř 45 % žen ve fertilním věku. Ve věkovém pásmu 15–49 let je výskyt trombóz cca 30/100 000 žen, tj. cca 350 trombotických příhod za rok. Z nich je přibližně 90 % vázáno na hormonální terapie – čili jde o zhruba o 310–320 případů ročně TEN spojených s HA. Riziko plicní embolie při hluboké žilní trombóze je 1–2%, což znamená 3–6 případů ročně. Mladistvých uživatelek HA je 6–7 %. Jde o prvouživatelky s rizikem neodhalených trombofilních mutací, což je ale vyváženo lepším zdravotním stavem oproti dospělým ženám a nižší pravděpodobností TEN v tomto věkovém pásmu.
Užívání hormonální léčby vede k mírnému vychýlení hemostázy k většímu trombotickému potenciálu a k nepřiměřeně zvýšené reakci na drobný trombotický podnět. Tyto změny jsou velmi individuální a podílí se na nich estrogenní i gestagenní složka HA. Klesající dávky EE vedly ke klesajícímu výskytu TEN, pokles na 50 µg EE vedl k signifikantnímu poklesu TEN, další pokles byl již méně výrazný. Dávka 30–35 µg EE snížila riziko TEN na polovinu. V současné době nejsou jednoznačné důkazy o poklesu výskytu TEN vázaném na snížení estrogenní dávky na 15–20 µg EE. Shoda je na faktu, že gestageny III. generace zvyšují riziko TEN 1,7 až 3krát oproti II. generaci. Na druhou stranu gestageny III. generace svým pozitivním efektem na aterogenní index více chrání cévní stěnu.
Rozvoj molekulárně genetických vyšetření v posledních dvou dekádách přinesl zvýšený zájem o vrozené vady ovlivňující hemokoagulační poměry – tzv. trombofilní mutace. Jejich výskyt je udáván u 3–8 % bílé populace, u ostatních ras je významně nižší. Trombofilní mutace se vyskytují v heterozygotní a rizikovější homozygotní formě. Tabulka 2 ukazuje nejčastější trombofilní mutace, jejich výskyt v populaci a míru rizikovosti. Izolovaná mutace genu pro enzym MTHFR (methylentetrahydrofolát reduktáza) bez zvýšené hladiny homocysteinu není rizikovým faktorem pro vznik TEN.
Table 2. Nejčastější trombofilní mutace. 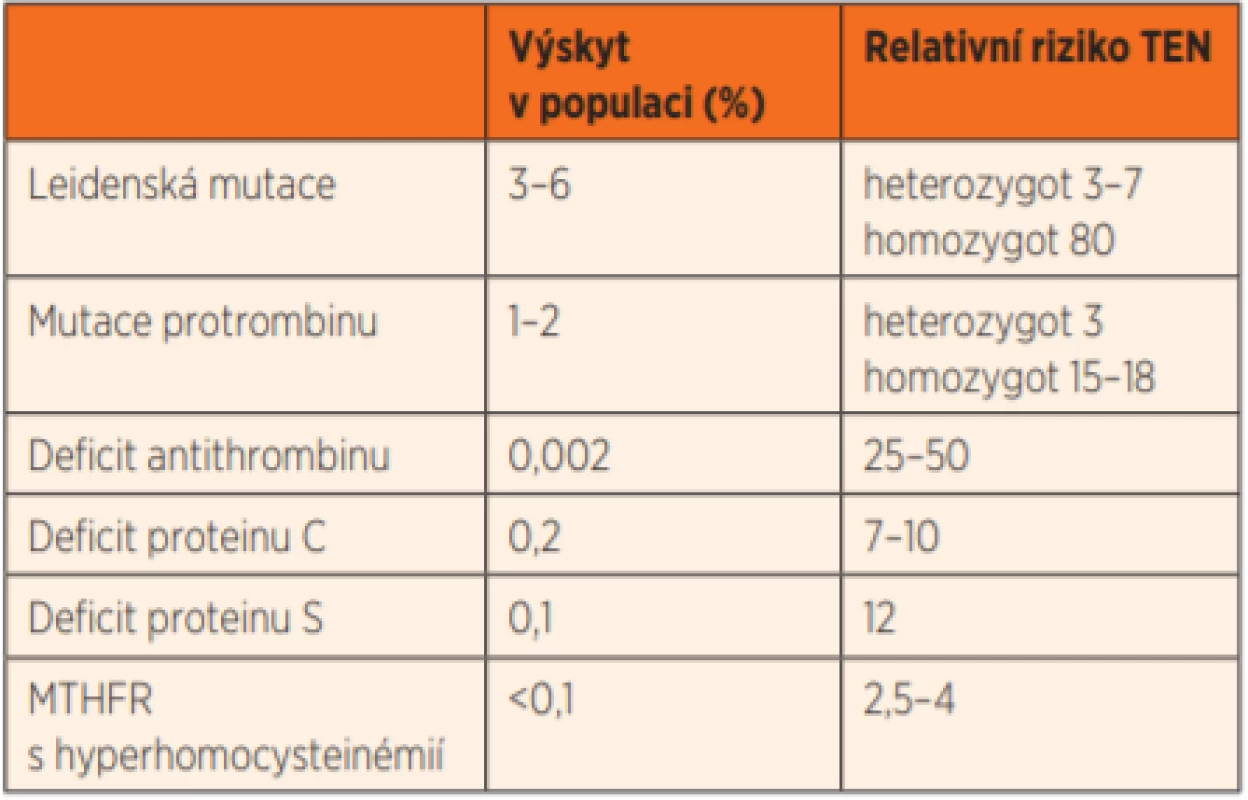
Pro hormonální léčbu jsou významné především Leidenská mutace (faktor V) a mutace protrombinu (faktor II). Heterozygotní mutace jsou 20–30krát častější než klinicky závažnější formy homozygotní. Trombofilní mutace jsou dobře vystopovatelné v pečlivě odebrané rodinné (až rodové) anamnéze, kde nacházíme zvýšený výskyt samotné TEN či stavů spojených s hyperkoagulací (infarkt myokardu, cévní mozkové příhody apod.). Varovnou známkou jsou tato onemocnění v mladším věku (pod 50 let). V literatuře odborné i laické se píše především o Leidenské mutaci, byť mutace protrombinu je daleko závažnější – naštěstí méně častá.
Pro vznik idiopatických tromboembolických stavů je charakteristický vznik krátce po nasazení HA – vyskytují se obvykle v prvních 3 až 6 měsících užívání. Poté se hemostáza vrací do zhruba výchozích poloh. Pro vznik TEN při dlouhodobějším užívání je třeba masivnější trombogenní podnět (např. úraz dolní končetiny).
Ženy užívají HA především proto, aby neotěhotněly. Od tohoto banálního faktu se ale odvíjejí častá nedorozumění mezi gynekology a lékaři jiných oborů, kteří s gravidními ženami přichází do kontaktu podstatně méně či vůbec. Nezapomínejme, že přes všechny pokroky moderní medicíny období gravidity, porodu a šestinedělí představuje pro ženu zdravotně rizikovější životní etapu. Proto v tabulce 3 porovnáváme hlavní rizikové faktory vzniku TEN s riziky gravidity a porodu.
Table 3. Rizikové faktory tromboembolické nemoci (TEN). 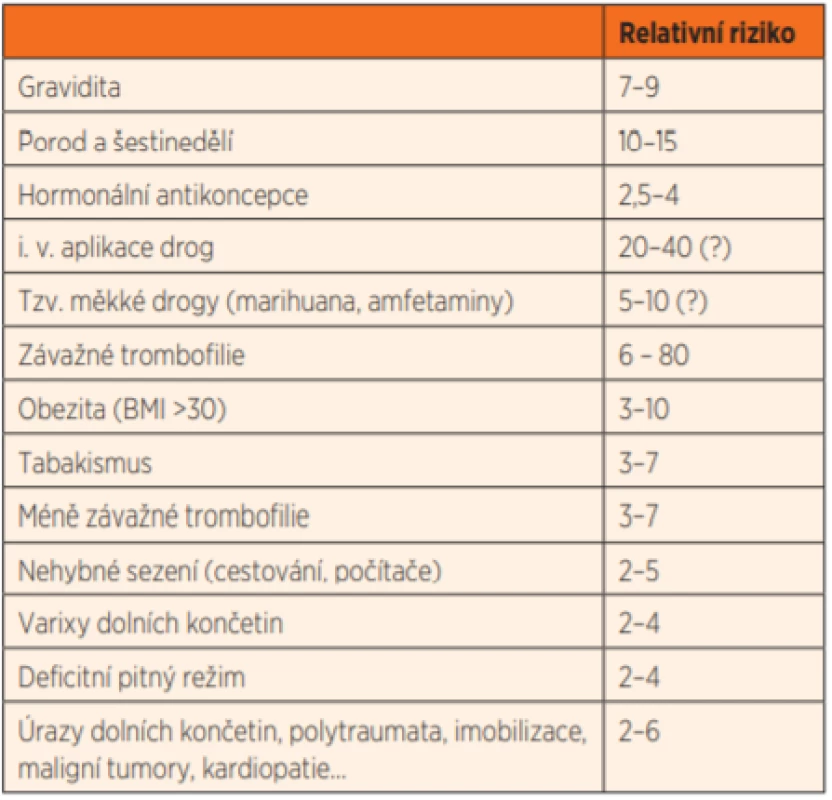
Z uvedeného jasně vyplývá, že s výjimkou závažných trombofilních mutací a zřejmě i drogového abúzu jsou všechny rizikové faktory (včetně HA) méně rizikové než těhotenství, porod a šestinedělí. Zásadní roli hraje racionální životní styl.
Drogová scéna mladistvých v ČR patří mezi nejaktivnější v Evropě a v konzumaci marihuany máme evropský primát. Téma ale není u nás ani ve světě významněji studováno a máme proto k dispozici nedostatečné množství relevantních dat. Nicméně i z nečetných sdělení se zdá, že drogy mají významný protrombotický efekt. U nitrožilních drog hraje významnou roli i znečištění a nedokonalá sterilizace aplikovaného roztoku.
Z klinické praxe bych zdůraznil některé rizikové faktory rozšířené mezi mládeží (a nejen mezi ní). Literárně bývá zdůrazňován syndrom turistické třídy – ale jak často létáme přes Atlantik? Podobný efekt mají každodenní hodiny nehybného sezení ve školách, zaměstnání či u počítačů, obvykle bez dostatečného pitného a pohybového režimu. Není žádným tajemstvím, že značná část mládeže v těchto „disciplínách“ vyniká. Dalším problémem je dlouhé sezení při autokarových zájezdech. Riziko TEN též výrazně narůstá s BMI a naše mládež jistě nepatří mezi nejštíhlejší. Pro mladší generaci je též typická vyšší míra sportovních aktivit přinášejících úrazy dolních končetin.
Co tedy učinit pro redukci rizika TEN u ženy s hormonální léčbou? Především začít již zmiňovanou podrobnou anamnézou – během studií medicíny jsme se dozajista setkali s výrokem „anamnéza je polovina diagnózy“. Vhodnou pomůckou mohou být různé dotazníky s výčtem rizikových faktorů, které buď pacientka vyplní sama, či lékař během odebírání anamnézy. Tímto postupem se snižuje pravděpodobnost opomenutí některé z důležitých informací.
V případě pozitivní rodinné či osobní anamnézy je indikováno molekulárně genetické vyšetření. Přehledné je doporučení Molekulárně genetická vyšetření u trombofilních stavů spojených s žilním tromboembolismem a jeho komplikacemi – konsensus České společnosti pro trombózu a hemostázu ČLS JEP a Společnosti pro lékařskou genetiku ČLS JEP z roku 2010.
1. Tromboembolická nemoc je multifaktoriální onemocnění, a proto nelze vycházet jen z určení molekulárně genetických znaků.
2. Z molekulárně genetických vyšetření mají při pátrání po trombofilním stavu spojeného s TEN zásadní klinický význam pouze určení mutace FV Leiden a mutace genu pro protrombin.
3. Vyšetření těchto dvou genetických vyšetření doporučujeme zdravotnickým zařízením indikovat pouze selektivně:
a) před zahájením kombinované perorální hormonální u žen s pozitivní osobní anamnézou prodělané TEN, nebo s pozitivní rodinnou anamnézou výskytu TEN;
b) u osob se stavem po prodělané idiopatické TEN;
c) u žen po opakovaných 3 potratech v 1. trimestru gravidity;
d) u těhotných žen s pozitivní osobní nebo rodinnou anamnézou prodělané TEN nebo při některých těhotenských komplikacích.
4. Mimo vyšetření FV Leiden a mutace genu pro protrombin jsou vyšetření jiných polymorfismů, spojovaných s TEN indikována ve vybraných případech pouze trombotickými centry.
5. Molekulárně genetická vyšetření spojovaná s TEN provádějí pouze laboratoře s ověřenou kontrolou kvality.
6. Při pozitivním záchytu uvedených mutací je vhodné provést tato vyšetření i u jejich blízkých příbuzných, pokud se u nich vyskytují další rizika spojená s trombofilií. U dětí až po 12.roce jejich věku, pokud k tomu nejsou jiné důvody.
Pochopení multifaktoriální etiologie TEN vede k závěru, že prodělaná TEN či trombofilní mutace nejsou jednoznačnou absolutní kontraindikací HA či jiné hormonální léčby, nýbrž důvodem k přísně individuálnímu posouzení stavu pacientky. Je nutno zohlednit následující kritéria:
1. Anamnéza a celkový zdravotní stav.
2. Trombofilie (pokud je prokázána)
- typ,
- homo - či heterozygotní forma.
3. Prodělaná TEN
- vazba na hormonálně změněné situace,
- obecné vlivy zvyšující riziko TEN.
Za absolutní kontraindikaci je považována TEN vázaná na hormonálně změněnou situaci (gravidita, HA či jiná hormonální léčba) bez výrazného trombotického podnětu a dále při homozygotní formě Leidenské mutace a mutace protrombinu. Diskutabilní je zákaz kombinované HA u dlouhodobé, nerizikové uživatelky, která prodělala TEN ve vazbě na výrazný zevní podnět (např. úraz dolní končetiny). Podobně je sporná i anamnestická TEN bez vazby na hormonální léčbu či graviditu při negativitě trombofilních mutací. Heterozygotní formy uvedených mutací jsou dnes řadou autorů chápány jako relativní kontraindikace HA. V těchto situacích je na místě důkladné hematologické vyšetření a vysoce individuální rozvaha.
Nasazení HA – a především u mladých prvouživatelek – je vhodné spojit se zdravotní osvětou, především s poučením o nevhodnosti tabakismu a dalších abúzů a propagací zdravého životního stylu (boj proti obezitě, pohybové aktivity, pitný režim apod.). Osvědčilo se také krátké poučení o příznacích TEN. U rizikových dívek je potřeba poučení podstatně důkladnější.
ZÁVĚR
Každá medikace má klady i zápory a obě stránky je třeba hodnotit ve světle medicíny založené na důkazech. Respektování indikací a kontraindikací, důsledně odebraná rodová anamnéza případně doplněná dotazníkem rizikových faktorů významně snižuje riziko preskripční chyby. Při dodržení těchto pravidel klady hormonální antikoncepce výrazně převyšují nad jejími riziky.
Adolescentkám dává moderní hormonální antikoncepce účinný nástroj ochrany před nežádoucím početím, což ve svém důsledku vede k redukci umělých přerušení těhotenství a tím i ke zlepšení budoucího reprodukčního zdraví. Celospolečensky přínosný je též pokles porodů mladistvých matek.
Korespondenční autor:
MUDr. Dana Ondrová Ph.D., MBA, IFEPAG
předsedkyně České společnosti gynekologie dětí
a dospívajících ČLS JEP
vedoucí lékařka ambulance GDD
Ústav pro péči o matku a dítě
Podolské nábřeží 157
147 00 Praha 4
e - mail: danyondra3@centrum.cz
Sources
1. Bailly C, Merceron O, Hammoudi N, et al. Cannabis induced acute coronary syndrome in a young female. Int J Cardiol 2010 Aug 6; 143 (1): e4–6.
2. Botzenhardt S, Toni I, Rascher W, Neubert A. Venous thromboembolism in adolescents associated with fourth generation oral contraceptives. Klin Padiatr 2013 Sep; 225 (5): 268–276.
3. Dinger J, Assman A, Mohner S, et al. Risk of venous thromboembolism and the use of dienogest - and drospirenone-containing oral contraceptives: results from a German case-control study. J Fam Plann Reprod Health 2010, 36 (3): 123–129.
4. Duchene C, Olindo S, Chausson N, et al. Cannabis-inducedcerebral and myocardial infarction in a young woman. Rev Neurol (Paris) 2010 Apr; 166 (4): 438–442.
5. Dulíček P. Riziko venózního tromboembolismu. Moderní gynekologie, Supplementum B. 2010; 19 (1): 86 – 92
6. Elikowski W, Małek M, Kurosz J, et al. Severe pulmonary embolism in a young marijuana smoker. Kardiol Pol 2011; 69 (11): 1168–70
7. Hadačová I. Trombóza a hormonální antikoncepce u mladistvých dívek. Pediatr praxi 2012; 13(4): 225–226
8. Havlín M. Antikoncepce mladistvých. In: Hořejší J, a kol.: Dětská gynekologie. Praha: Mladá fronta, 2017.
9. Křepelka P. Hormonální antikoncepce a kardiovaskulární systém. Postgrad Med 2012; 3 : 255–260.
10. Kessler P. Trombofilní stavy. Interní Med 2006; 9 : 374–379.
11. Kvasnička J. Doporučený postup pro indikaci molekulárně genetických vyšetření v rámci diagnostiky trombofilních stavů v žilním systému. Vnitř Lék 2010; 56 (12): 1251.
12. Lidegaard O. Hormonal contraception and risk of venous thromboembo-lism: national follow-up study. BMJ 2009 Aug 13, p. 339.
13. Martínez F, Avecilla A. Combined hormonal contraception and venous thromboembolism. Eur J Contracept Reprod Health Care 2007 Jun; 12 (2): 97–106.
14. Rott H. Contraception, venous thrombosis and biological plausability. Minerva Med 2013 Apr; 104 (2): 161–167.
15. Pillai P, Bonny AE, O‘Brien SH. Contraception-related venous thromboembolism in a pediatric institution. J Pediatr Adolesc Gynecol 2013 Jun; 26 (3): 186–188.
16. Rott H. Hormonal contraception in thrombophilic adolescents: risk of thrombosis and recommendations. Hamostaseologie 2012; 32 (1): 15–21.
17. Roztočil A. Moderní gynekologie. Praha: Grada Publishing, 2011.
18. Schramm G, Schrah B. The efficacy and safety of an oral contraceptive containing chlormadiononacetate: reset of pooled analysis of non interventional trials in adult and adolescent women. Contraception 2011; 84 : 390–401.
19. Sidney S, Cheetham TC, Connell FA, et al. Recent combined hormonal contraceptives (CHCs) and the risk of thromboembolism and other cardiovascul arevents in new users. Contraception 2013 Jan; 87 (1): 93–100.
20. Sultan C. Pediatric and Adolescent Gynecology. Basel: Karger, 2012.
21. Unzeitig V, Čepický P, Dvořák V, et al. Doporučení k předpisu kombinované hormonální antikoncepce. Čes Gynekol 2012; 77 (6): 597–599.
22. van Vlijmen EF, Veeger NJ, Middeldorp S, et al. Thrombotic risk during oral contraceptive use and pregnancy in women with factor V Leiden or protrombin mutation: a rational approach to contraception. Blood 2011 Aug 25; 118 (8): 2055–2061.
23. Verhaeghe J. Clinical practice: Contraception in adolescents. Eur J Pediatr 2012 Jun; 171 (6): 895–899.
Labels
Neonatology Paediatrics General practitioner for children and adolescents
Article was published inCzech-Slovak Pediatrics

2020 Issue 3-
All articles in this issue
- Problematika oboru Gynekologie dětí a dospívajících – editorial
- Bolesti břicha u dívek v dětském a pubertálním období
- Krvácení z rodidel v dětském věku z pohledu dětského gynekologa
- Vrozené vývojové vady dělohy a pochvy – poruchy vývoje Müllerových vývodů a jejich derivátů – ultrazvuková diagnostika u dětí a dospívajících
- Rizikové faktory vzniku tromboembolické nemoci u mladistvých uživatelek hormonální antikoncepce
- Časná a pozdní morbidita a mortalita u dvojčat narozených mezi 24. a 36. gestačním týdnem v perinatologickém centru a mimo něj
- Hematopoietic stem cell transplantation in patients with chronic granulomatous disease in the Czech Republic and Slovakia (2007–2019)
- Vzťahová väzba a chronické ochorenie u detí
- Alkohol v rukách detí a mladistvých čoraz častejšie končí pobytom v nemocnici – skúsenosti z Bratislavy a okolia
- Eisenmengerův syndrom a jeho komplikace v dětském věku
- Význam a zloženie oligosacharidov materského mlieka
- Kontinuální monitorace glykémie (CGM) „ve velkém“ na letním dětském diatáboře
- Tomáš Garrigue Masaryk, prof. MUDr. Josef Švejcar, DrSc., a Martin
- MUDr. Petr Pešák – 70 let
- Profesor MUDr. Milan Šamánek, DrSc., FESC (*9. 5. 1931 – † 29. 4. 2020) – odchod legendy
- Zemřel prof. MUDr. Jaroslav Stejskal, DrSc.
- Czech-Slovak Pediatrics
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Krvácení z rodidel v dětském věku z pohledu dětského gynekologa
- Bolesti břicha u dívek v dětském a pubertálním období
- Vrozené vývojové vady dělohy a pochvy – poruchy vývoje Müllerových vývodů a jejich derivátů – ultrazvuková diagnostika u dětí a dospívajících
- Eisenmengerův syndrom a jeho komplikace v dětském věku
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career