-
Medical journals
- Career
Kontaktní dermatitidy – část I.
: G. Janoušková 1; A. Machovcová 1,2
: Dermatovenerologické oddělení FN Motol, Praha primářka MUDr. Alena Machovcová, Ph. D., MBA 1; Klinika nemocí z povolání 1. LF UK a VFN, Praha přednostka prof. MUDr. Daniela Pelclová, CSc. 2
: Čes-slov Derm, 91, 2016, No. 3, p. 102-112
: Reviews (Continuing Medical Education)
Kontaktní dermatitidy (KD) jsou exogenně vyvolané dermatózy, které se vyskytují u dětské i dospělé populace. Vznikají působením látek iritační a/nebo alergické povahy na kůži za spolupůsobení dalších vlivů. Klinický obraz je pestrý. Kromě typických ekzémových projevů se objevují projevy neekzémového charakteru (kopřivkovité, lichenoidní, granulomatózní, poruchy pigmentace a další). Konečná diagnóza je syntézou podrobné anamnézy (včetně pracovních i mimopracovních návyků), klinického obrazu, provedených vyšetření (epikutánní testy, prick testy a další) a vyhodnocení klinické relevance. KD se léčí zevními externy, většinou topickými kortikosteroidy, ve vhodném vehikulu podle klinického stadia nemocnění. Prevence KD spočívá v důsledném vyloučení všech provokujících vlivů, a to zejména zjištěných kontaktních alergenů, ochrana kůže při a po práci, vhodná volba zaměstnání s ohledem na anamnézu a přítomnost jiných dermatóz (např. atopického ekzému).
Klíčová slova:
kontaktní dermatitidy (iritační, alergická, proteinová, airborne, systémová) – příčiny vzniku – léčbaÚVOD
Kontaktní dermatitidy (KD) patří mezi kožní onemocnění vyvolané kontaktem kůže s látkami vyskytujícími se v zevním prostředí. Mohou způsobit iritační nebo alergickou odpověď kůže. Podezření na tuto diagnózu vzniká na základě typického klinického obrazu kožních lézí, jejich distribuce, ale současně absence ostatních možných příčin, včetně kožních projevů systémového onemocnění. Akutní projevy KD charakterizuje erytém, otok, papuly a/nebo vezikuly. Recidivující nebo perzistující projevy KD vedou ke ztluštění a zhrubění kůže (lichenifikace), k tvorbě ragád a šupení. Pro všechny formy KD jsou typické svědění, méně pálení, různě dlouhá doba trvání a časté recidivy. Klinicky je obtížné oba typy reakcí od sebe odlišit, protože mají podobné projevy [6, 9, 10, 14, 44, 51, 69].
DERMATITIS CONTACTA IRRITATIVA
(IRITAČNÍ KONTAKTNÍ DERMATITIDA)Definice
Iritační kontaktní dermatitida (IKD) je charakterizována jako nespecifická, uniformní zánětlivá reakce kůže vznikající na exogenní podněty bez předchozí senzibilizace kůže. Vyvolávají ji látky, které poškozují kožní struktury přímým kontaktem. Klinický obraz je velmi variabilní, zahrnuje senzorickou iritaci, akutní dermatitidu, chronickou (kumulativní) dermatitidu, poleptání a další reakce [6, 9, 14, 44, 51, 69].
Epidemiologie
IKD je nejčastějším typem kontaktních dermatitid. V zahraničí představuje přibližně 80 % profesionálních kontaktních dermatitid a je považována za nejčastější příčinu ekzémových projevů na rukou [13, 57]. Prevalence IKD obecně a zejména na rukou je vyšší u žen než u mužů, pravděpodobně v souvislosti s vyšší expozicí detergentům a „mokré práci“ doma a v zaměstnání [57]. Riziko IKD profesionální etiologie je vyšší mezi pracovníky tzv. „vlhkých profesí“, kterými jsou např. zdravotníci, zaměstnanci úklidových firem, kadeřníci apod. [13, 16].
Patogeneze
Mechanismus vzniku IKD stále není plně objasněn. Za primární faktory při vzniku IKD je považována porucha epidermální bariéry chemickými nebo fyzikálními noxami, která vede ke zvýšené kožní permeabilitě a zvýšeným transepidermálním ztrátám vody (TEWL). Poškození buněčné membrány, cytotoxický efekt na keratinocyty, uvolnění cytokinů z keratinocytů a aktivace vrozené imunity představují další mechanismy uplatňující se při vzniku IKD. Za genetický faktor zapojený do vzniku chronické IKD je považován polymorfismus cytokinů a chemokinů (TNFA-308 a IL1A-889) [26]. Experimentálně (např. s laurylsulfátem sodným) vyvolaná akutní porucha epidermální bariéry na zvířecích nebo lidských modelech vede k uvolnění cytokinů z keratinocytů (interleukin IL-1 alfa, IL-1 beta, IL-6 a TNF alfa), přičemž IL-1 alfa a TNF-alfa působí jako primární signál vedoucí k uvolnění dalších prozánětlivých chemokinů (CCL20, CCL21, CXCL8), které přitahují mononukleáry a polynukleáry na postižené místo [18, 52, 71]. TNF-alfa současně indukuje expresi intercelulárních adhezivních molekul 1 (ICAM-1) na keratinocytech, které podporují infiltraci leukocytů do epidermis [52]. Dlouhodobé působení mírných iritancií může vést ke zmírnění zánětlivé odpovědi a stimulaci buněčné proliferace a diferenciace za vzniku chronické IKD [66].
Faktory ovlivňující vznik IKD jsou kombinací vlivu individuálních faktorů konkrétního pacienta a zevního prostředí, které modifikují odpověď kůže na podráždění. Uplatňují se fyzikální (viz dále) i chemické vlivy. Mezi obvyklé chemické látky s iritačním účinkem patří voda, detergenty a surfaktanty, rozpouštědla, oxidační činidla, kyseliny a zásady. Síla iritačního účinku jednotlivých látek je závislá na jejich chemické povaze (např. na molekulární hmotnosti, rozpustnosti v tucích, disociační konstantě kyselin, ionizaci, polarizaci) a délce kontaktu s kůží [13]. Vysoké koncentrace většiny chemikálií vedou k iritaci téměř u všech osob, zatímco nízké koncentrace těchto látek vedou k zánětlivé odpovědi jen u citlivých jedinců, nebo po opakovaném nebo dlouhodobém působení na kůži [7]. Citlivost kůže vůči iritačním látkám je nejvyšší v dětství, s přibývajícím věkem klesá [53]. Účinek iritačních látek je nejnižší na dlaních, ploskách a zádech, nejvyšší na obličeji, hřbetech rukou a bříškách prstů, v závislosti na tloušťce stratum corneum [13] nebo vlivem poškozené kožní bariéry (např. atopická dermatitida) [25].
Klinický obraz
Klinický obraz IKD je variabilní, spektrum kožních projevů, jako reakce na podráždění, je široké. Od subjektivních pocitů bez viditelných klinických projevů přes akutní reakce až k typickému obrazu IKD. Někdy krátkodobý kontakt s určitou látkou vyvolá rozsáhlé poškození [14, 69].
Typy IKD
1. Senzorická iritace – zahrnuje dysestezie různé povahy (píchání, pálení, mravenčení, bodání) bez viditelného poškození kůže. Objevuje se po kontaktu s určitými látkami (např. propylenglykolem, etanolem, kyselinou mléčnou, kyselinou azelaovou a benzoovou, benzoylperoxidem, retinoidy atp.) v kosmetických, dermatologických nebo hygienických přípravcích. U predisponovaných osob se potíže objevují po potravinách s obsahem kyseliny sorbové nebo disiřičitanu sodného [14, 69].
2. Iritační reakce – na kůži zjišťujeme mírné známky zánětu (suchost, diskrétní olupování, zarudnutí). První projevy se objevují v meziprstí rukou (obr. 1) nebo pod šperky (obr. 2).
1. Iritační reakce v meziprstí rukou („mokrá práce“, saponáty) 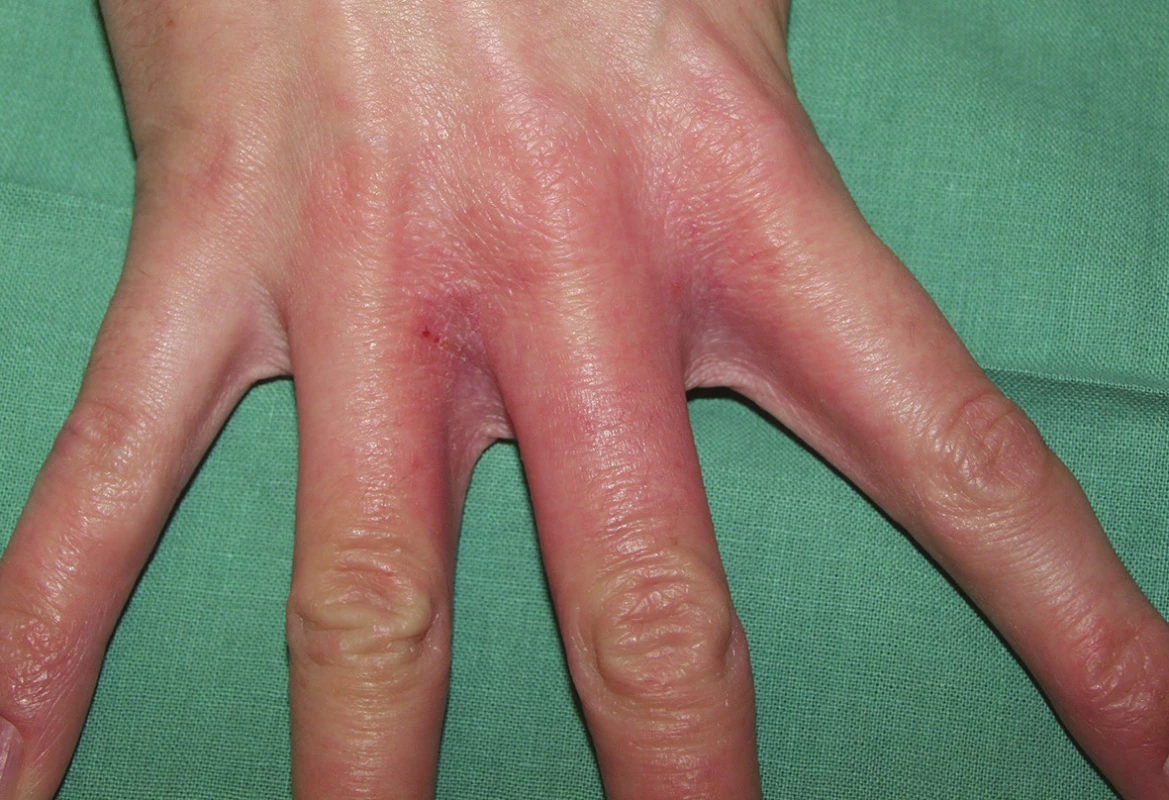
2. Iritační reakce pod šperkem 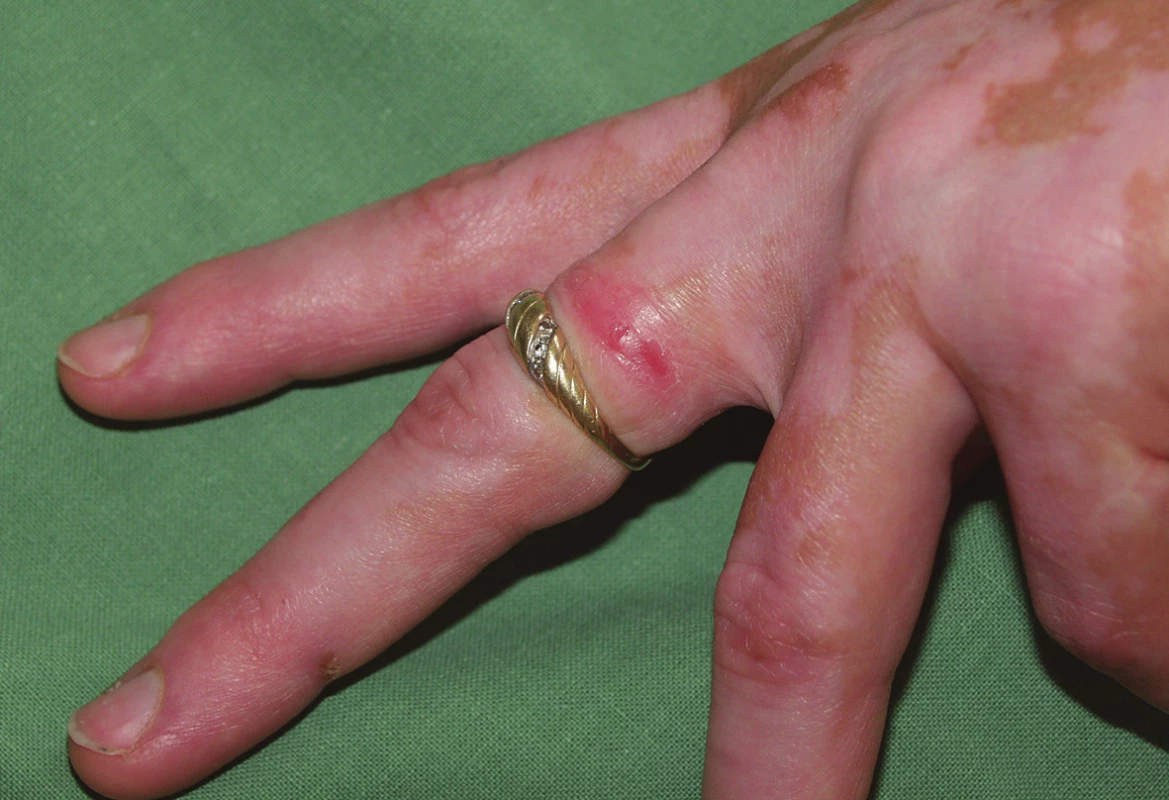
Na prezentovaných fotografiích jsou dokumentovány konkrétní případy, kde byla diagnóza ověřena. Klinický obraz ale není sám zpravidla určující pro konkrétní noxu.
Vyvolavatelem bývá intenzivní kontakt s vodou, šampony, detergenty (např. u kadeřníků) nebo s chladicími kapalinami (u obráběčů) [14, 69].
3. Akutní iritační kontaktní dermatitida – vzniká během několika minut až hodin po expozici (většinou náhodné profesionální) látkám s vysokým iritačním potenciálem. Klinicky se objevuje intenzivní erytém, edém, buly (obr. 3), subjektivně jí doprovázejí pálení, algezie, ve stadiu hojení svědění. Těžké tkáňové poškození s nekrózou a escharami (cauterisatio) vyvolávají anorganické kyseliny, silné zásady, soli kovů (chromáty), rozpouštědla nebo plyny (etylenoxid). Způsobí hlubokou tkáňovou destrukci (obr. 4), jejíž hojení je obvykle spojeno s jizvením [14, 27, 30, 69].
3. Akutní iritační kontaktní dermatitida s hemoragickými bulami po opakovaném umytí rukou v pracím prášku Colon 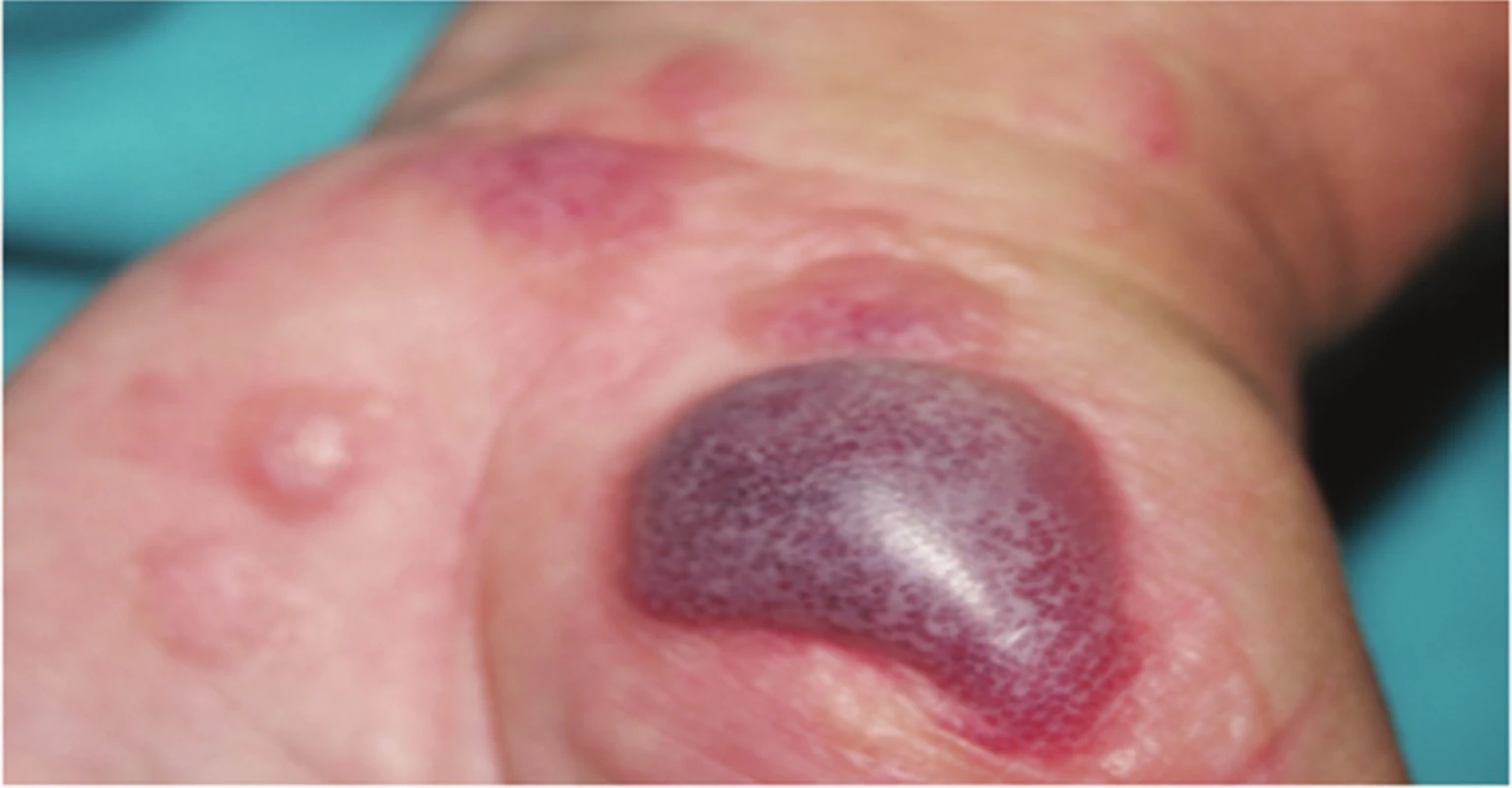
4. Akutní iritační dermatitida po solích chrómu (cauterisatio) 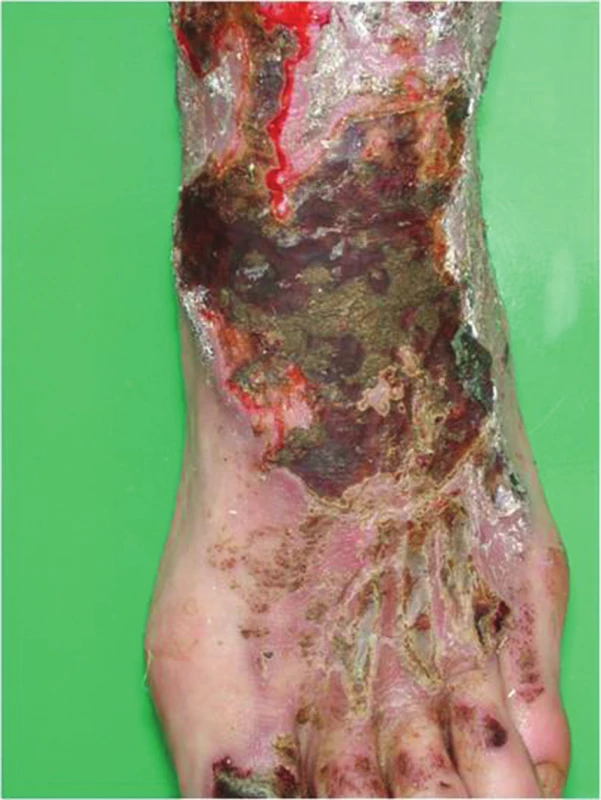
4. Opožděná akutní IKD – má podobné symptomy jako akutní IKD, klinicky viditelný erytém se objevuje po expozici opožděně (po 8–24 hodinách) a může imitovat alergickou kontaktní dermatitidu. Typickými vyvolavateli jsou bezalkonium chlorid, ditranol, etylenoxid. Tento typ reakce vídáme i během epikutánních testů, reakce nemají typický „crescendo“ vývoj, během odečítání zeslabují nebo kompletně vymizí [14, 69].
5. Kumulativní iritační kontaktní dermatitida se vyskytuje často. Objevuje po opakovaném podráždění kůže bez dostatečného času k obnově kožních bariérových funkcí. Způsobují ji kombinace látek nebo jeden často se opakující prostředek (např. opakované mytí rukou – více než 10krát za den, mýdla, dezinfekční prostředky, saponáty, čisticí prostředky, minerální oleje apod.). V klinickém obraze dominuje suchost kůže, červenohnědý erytém, lichenifikace, hyperkeratózy a ragády (obr. 5) [14, 27, 28, 44, 51, 66, 69].
5. Chronická iritační kontaktní dermatitida na dlaních po pracovních rukavicích 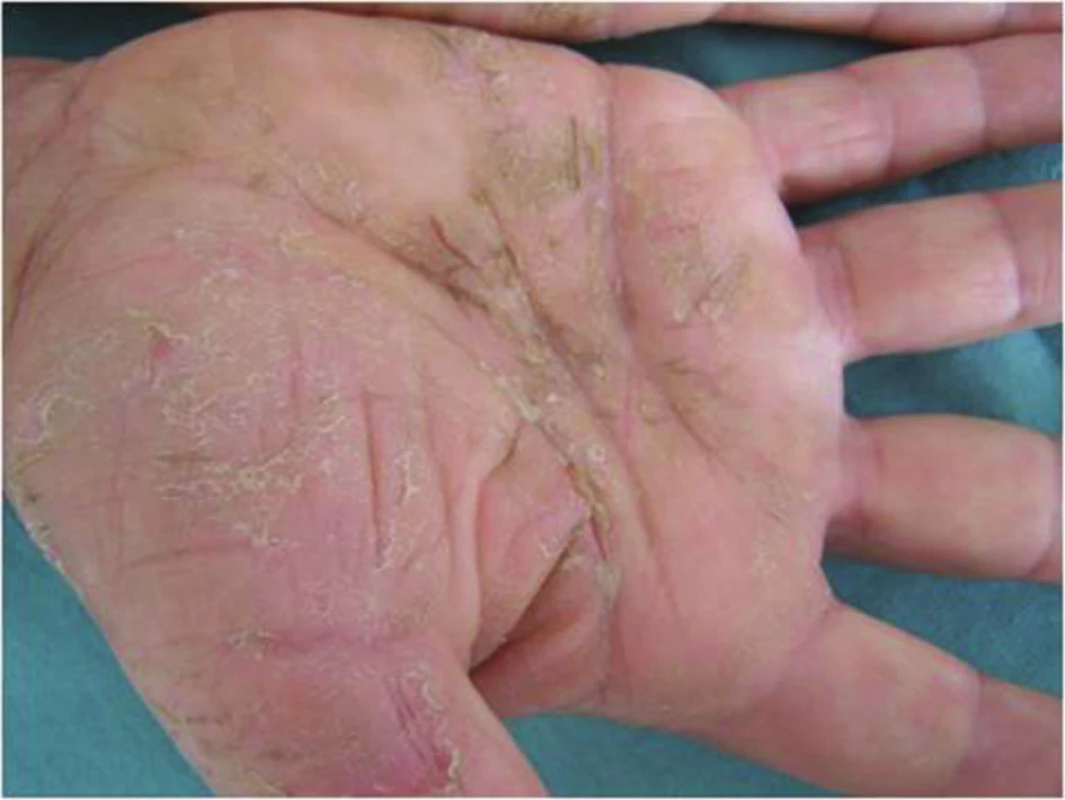
6. Asteatotická (senilní) iritační kontaktní dermatitida je zvláštním typem KD. Pro svou vazbu na zimní měsíce se nazývá „zimní ekzém“. Postihuje osoby vyššího věku s častým koupáním nebo sprchováním v horké vodě bez pravidelného promašťování. Klinicky dominuje intenzivní pruritus, suchá kůže, ichtyoziformní šupení a charakteristicky popraskaná kůže („eczema craquelé“) [14, 45, 69].
7. Airborne iritační kontaktní dermatitida vzniká drážděním výpary a solidními mikročásticemi obsaženými ve vzduchu. Postihuje odkryté partie, ale i místa, kde se látky zadržují v oděvu. Často jsou projevy generalizované. Postiženy jsou nejčastěji horní víčka, tváře (obr. 6), krajiny retroaurikulární a submentální, dále partie záhybů a styčných ploch. Příčinami bývají formaldehyd, syntetické pryskyřice, amoniak, terpentýn, dezinfekční prostředky, éterické oleje, agrochemikálie, vlákna azbestová, skelná, různé prachové částice [11, 14, 44, 69].
6. Airborne iritační kontaktní dermatitida po persterilu 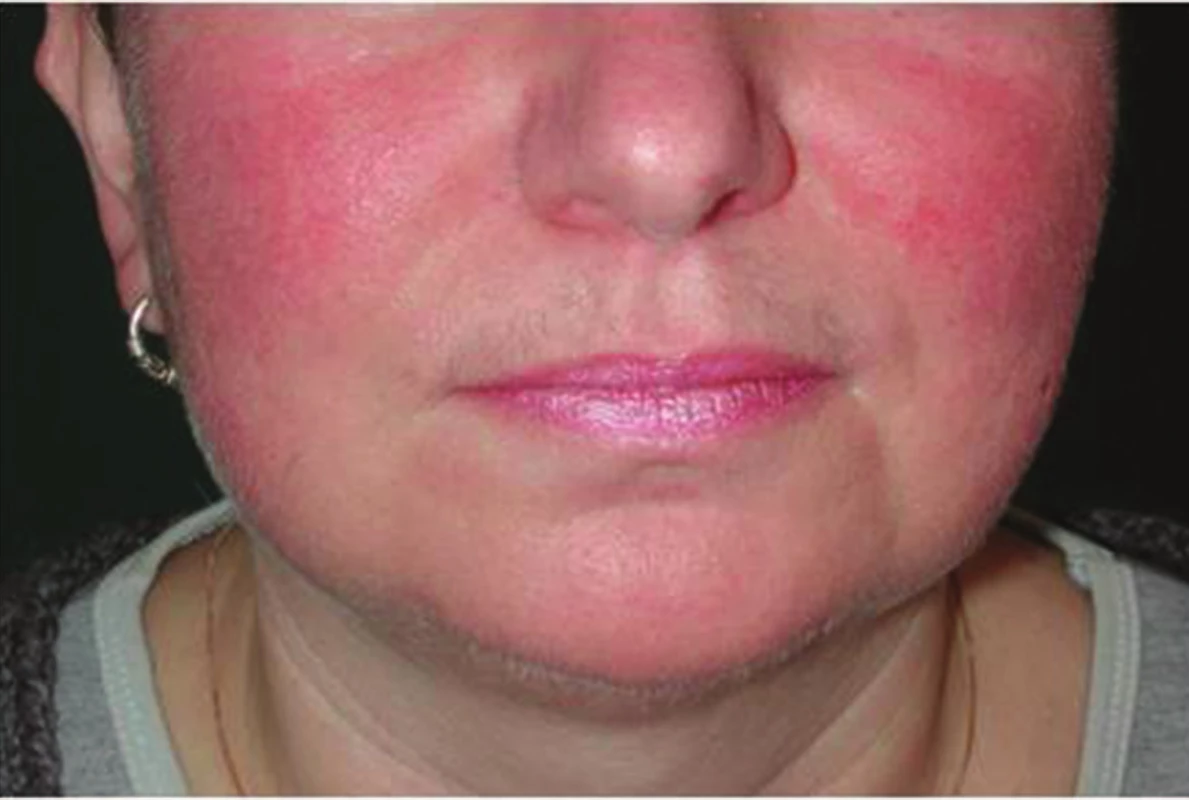
8. Traumatická/mechanická iritační kontaktní dermatitida vzniká nešetrným mytím rukou s použitím abrazivních past, často spolu s používáním koncentrovaných čisticích prostředků a rozpouštědel nebo kontaktem s minerálními vlákny (např. izolační materiály, sklolaminát apod.). Klinicky se vyskytují erytém, infiltrace, šupení a tvorba fisur, lokalizace je často na hřbetech rukou a/nebo na předloktí. Občas dochází k otužení kůže [14, 66, 69].
9. Pustulózní a akneiformní iritační kontaktní dermatitida vzniká po expozici určitým látkám (např. kovy, minerální oleje, chladicí kapaliny, dehet nebo asfalt, minerální vlákna, chlorované uhlovodíky apod.) [14].
Nejčastější vyvolavatelé
- Fyzikální faktory – působení vysokých teplot, větru vede k narušení funkce kožní bariéry a k její vyšší prostupnosti pro látky iritační povahy. Chlad a nízká vlhkost okolního vzduchu zvyšují transepidermální ztráty vody s následnou vyšší citlivostí kůže k působení iritačních látek. Chronická mikrotraumata kůže vyvolaná třením pevnými látkami (např. části kovů, dřevo, skelná vlákna, části rostlin, papír, prach nebo zemina) vedou k IKD z fyzikálních příčin [3, 4, 13]. Nově byla popsána IKD po dlouhodobém tlaku, tření a pocení (5 hodin denně a více) při práci s myší počítačů [20].
- Voda jako univerzální rozpouštědlo má iritační vlastnosti. Z hlediska koncentrace iontů jde o hypotonický roztok a na erodovanou kůži působí cytotoxicky. Dlouhodobým kontaktem s intaktní kůží dochází k bobtnání stratum corneum, narušení intercelulárních lipidů, zvýšení kožní permeability a citlivosti k působení dalších iritačních látek [64]. Některé další vlastnosti vody (tvrdost, teplota, osmolarita, pH) se spolupodílí na iritačních vlastnostech vody, které ještě zvyšuje okluze v neprodyšných ochranných pracovních rukavicích [3, 18, 33, 44, 69].
- Detergenty a čisticí prostředky obsahují povrchově aktivní látky (surfaktanty), které mají odmašťující a emulgační schopnosti. Způsobují odstranění lipidů a hygroskopických látek ve stratum corneum, vedou k denaturaci proteinů a poškození buněčných membrán. Při běžném používání vyvolávají IKD vzácně. Anionické detergenty (mýdla) dráždí více než non-ionické a amfoterické skupiny. Jako referenční látka k vyvolání iritace se používá roztok laurylsulfátu sodného [3, 18, 33, 44, 69].
- Rozpouštědla se v kontaktu s kůží chovají podobně jako detergenty. Vymývají lipidy z epidermis, zvyšují perkutánní penetraci látek. Déletrvající kontakt může vyvolat těžké popáleniny nebo celkové příznaky. Používají se v řadě průmyslových oborů. Jejich iritační potenciál je závislý na chemické struktuře, klesá v pořadí: aromatické (benzen, toluen) > alifatické > chlorované > terpentýn > alkoholy > estery > ketony [18, 33, 44, 69].
- Tělesné sekrety (moč, stolice, sliny apod.) způsobují IKD u malých dětí v oblasti plen. Plenková dermatitida má multifaktoriální etiologii (vlhkost kůže, fekální enzymy, okluze, pH kůže, tření a další vlivy). Fekální enzymy (lipázy a protézy) zvyšují pH do alkalických hodnot a kůži dráždí. Přítomné mikroorganismy (kvasinkové, stafylokokové, peptostreptokokové a další) jsou dalšími negativní faktory [1, 3, 14, 46, 69].
- Kyseliny (anorganické, organické) mají korozivní účinky na kůži a poškozují epidermis denaturací bílkovin a cytotoxickými účinky. Anorganické kyseliny způsobují poškození ve větší rozsahu než organické kyseliny. Ty mají mírný iritační potenciál, který se využívá léčebně [3, 14, 44, 69].
- Alkálie vyvolávají zmýdelnění lipidů, vedou k narušení keratinových můstků a k otoku. Ve srovnání s kyselinami poškozují ve větším rozsahu. Mokrý cement je schopen vyvolat hlubokou nekrózu kůže svým alkalickým pH a uvolněním hydroxidu vápenatého. Nekrózy se objevují 8–12 hodin po kontaktu [3, 14, 30, 44, 69].
- Potraviny a potravinová aditiva obsahují látky, které kůži dráždí, někdy i senzibilizují. Mezi typické potraviny patří česnek (obsahuje alicin, diallyldisulfit), ananas (bromelain), hořčice, křen, zelí, brokolice apod. [14].
Histopatologie
Histopatologický obraz IKD je variabilní, v epidermis se vyskytuje mírná spongióza, nekróza keratinocytů a zánětlivý infiltrát. V horní dermis je přítomný lymfocytární perivaskulární infiltrát. Dalšími známkami jsou akantóza s mírnou hypergranulózou a hyperkeratózou. Změny nejsou specifické pro IKD a histologicky nelze odlišit alergickou kontaktní dermatitidu nebo jiné chronicky probíhající dermatitidy [14, 69].
Vyšetřovací metody
Epikutánní testy musí být v případě IKD negativní. Jako referenční látka k vyvolání iritační reakce se v epikutánním testu používá 0,25% vodný roztok laurylsulfátu sodného [18, 63]. Iritační reakce v epikutánních testech často vyvolává formaldehyd nebo nesprávně testované hygienické nebo kosmetické přípravky.
Diferenciální diagnóza
Diferenciálně diagnosticky musíme odlišit alergickou kontaktní dermatitidu, jiné dermatitidy (atopickou, seboroickou), lékové exantémy, urtikárii, psoriázu, mykózy a další dermatózy. Diagnóza IKD zůstává vylučovací, tzv. zbytková, kdy je třeba vyloučit jiné typy dermatitid, zejména alergickou kontaktní dermatitidu a atopickou dermatitidu. Forenzní význam má vyloučení jiných typů dermatitid v případě podezření na vliv profese [14, 44, 69].
Léčení
Cílem léčby je obnovení funkcí kožní bariéry. Časté je používání topických kortikosteroidů, jejich účinek je kontroverzní. Systémové kortikosteroidy pomáhají zklidnit akutně probíhající zánět, nejsou účinné u chronicky probíhající IKD, u které mohou být efektivní fototerapie UVB 311 nm nebo PUVA terapie. Hyperkeratotická palmoplantární dermatitida nebo chronická IKD na rukou příznivě reaguje na léčbu celkovými retinoly (acitretin nebo alitretinoin) nebo na systémovou imunosupresivní léčbu (metotrexát, cyklosporin) a pravděpodobně i na biologickou léčbu [14, 69].
Primárním preventivním opatřením je vyloučení, popř. přerušení expozice, příčinným iritačním látkám v domácím i pracovním prostředí do zhojení kožních projevů. Dalším opatřením je úprava péče o kůži. Mezi opatření individuální povahy patří minimalizace kontaktu s dráždivými látkami, důsledné používání osobních ochranných pracovních pomůcek, pravidelné promašťování kůže. Z pracovního hlediska se tato opatření doplňují vhodnými režimovými opatřeními systémové povahy (např. změna technologie, automatizace výroby) [33, 70].
Prognóza
U některých osob IKD ustupuje spontánně i přesto, že kontakt se škodlivinou trvá. Je to výsledek adaptačního procesu kůže na škodlivinu, tzv. hardening (otužení) [66]. U IKD hrozí vždy riziko sekundární senzibilizace na různé alergeny, které se vyskytují v pracovním i mimopracovním prostředí [33, 70].
DERMATITIS CONTACTA ALLERGICA
(ALERGICKÁ KONTAKTNÍ DERMATITIDA)Definice
Alergická kontaktní dermatitida (AKD) je projevem IV. typu přecitlivělosti zprostředkované T lymfocyty a významnou roli při vzniku hraje individuální dispozice. Alergenů schopných vyvolat kontaktní senzibilizaci (KS) je velké množství (soli kovů, složky kosmetických výrobků, barviva apod.). V klinickém obraze převažují projevy ekzémového charakteru, méně často se vyskytují projevy neekzémové (např. lichenoidní, granulomatózní apod.). Epikutánními testy potvrzujeme diagnózu. KS je častou příčinou choroby z povolání [33, 59, 70].
Epidemiologie
Prevalence senzibilizace na jednotlivé alergeny se různě liší podle vzorku testovaných pacientů. Výskyt KD se v Německu se odhaduje na 15–20 %. Incidence AKD v Nizozemí dosahovala 28 na 1000 osob/rok u běžně testované populace, ve Velké Británii byla spočítána na 1,6 na 1000 osob/rok. Podle modelů se odhaduje incidence AKD na 3/1000 osob/rok [10, 47]. AKD se vyskytuje 2krát častěji u žen než u mužů, postihuje všechny věkové skupiny, prevalence ve skupině 12–16letých se pohybuje kolem 15 % [10, 47, 56].
Rizikové a predispoziční faktory pro vznik kontaktní senzibilizace
Rozvoj KS závisí na řadě faktorů, zejména na individuální dispozici organismu. Potvrzují to studie epidemiologické, mezi příbuznými členy rodiny a studie na dvojčatech [12]. Neméně významnou roli hrají chemické vlastnosti látky [44].
Rizikové faktory pro vznik KS rozdělujeme na vrozené a získané. Mezi vrozené faktory patří genetická výbava, věk, pohlaví a rasová příslušnost. Geneticky podmíněné rizikové faktory (např. genový polymorfismus) jsou zapojeny do příslušných kroků pro rozvoj KS. Ovlivňují vychytávání antigenu při průchodu kožní bariérou, antigen-specifickou reakci imunitních buněk nebo metabolismus antigenů ovlivněný kožními enzymy [12, 49]. Příkladem posledně jmenovaného je metabolismus a aktivace antigenů epidermálními N-acetyltransferázami (NATs), jehož vyšší enzymatická aktivita byla prokázána ve studiích u pacientů s kontaktní dermatitidou [68].
Počet senzibilizovaných jedinců v populaci závisí na míře expozice jednotlivým alergenům [3]. Pohlaví může ovlivňovat procento KS na jednotlivé alergeny. Vyšší výskyt AKD u žen je spíše dán vyšší expozicí jednotlivým kontaktním alergenům a vyšším počtem testovaných žen než rozdílnými vlastnostmi kůže mezi pohlavími [37]. V případě KS na soli niklu, na složky kosmetických přípravků a vlasových barev se jedná o důsledek vyšší expozice alergenu než o vliv pohlaví [3, 9]. Vztah mezi rasou, jako jedním z vrozených rizikových faktorů, vznikem KS a AKD dosud nebyl prokázán. Podle dostupných publikací se jedná spíše o vliv vyšší bariérové funkce kůže a tím nižší riziko vzniku KS [22, 67]. U osob s vyššími fototypy (III a výše) se udává snížená schopnost vyvolat senzibilizaci bez ohledu na senzibilizační potenciál alergenu. Při odečítání epikutánních testů je současně možné slabší reakce přehlédnout [22].
Mezi získané rizikové faktory patří zánětlivá kožní onemocnění (např. IKD, stasis dermatitis). Zvažována je i atopická dermatitida, ale vztah atopické dermatitidy a KS není stále vyjasněn a je předmětem dosud neuzavřených diskusí [48]. Vyšší prevalence KS u pacientů s atopickou dermatitidou se vysvětluje poruchou epidermální bariéry a vyšší permeabilitou atopické kůže [43, 48 62].
Patogeneze
AKD je projevem IV. typu přecitlivělosti podle Coombse a Gella, tedy T-lymfocyty zprostředkovanou reakcí u dříve senzibilizovaného jedince. Při reakcích v kůži se uplatňují i mechanismy alergické reakce I. typu. Rozvoj kontaktní alergické reakce probíhá dvoufázově. V indukční fázi dochází k průniku alergenu, který ve formě haptenu penetruje kožní bariérou přes stratum corneum. Kontaktní alergeny jsou většinou látky s molekulovou hmotností menší než 500 D. Tato velikost jim umožňuje průchod přes stratum corneum, ale k vyvolání alergické reakce je nutná jejich vazba s autologními proteiny v kůži za vzniku antigenu s molekulovou hmotností větší než 5000 D. Ke konjugaci dochází s proteiny MHC I. nebo II. třídy (major histocompatibility komplex). MHC I. třídy exprimují všechny jaderné buňky, MHC II. třídy exprimují především antigen prezentující buňky, mezi které patří dendritické buňky, makrofágy a B lymfocyty [34, 36, 50]. K vazbě dochází s proteiny buněčné membrány antigen prezentujících Langerhansových buněk (LB) s následným předkládáním antigenu T lymfocytům v kůži, aferentních lymfatických cévách a regionálních lymfatických uzlinách. Vazba komplexu hapten-MHC na povrchu LB s antigen specifickým receptorem T buňky (TCR) je prvním signálem pro aktivaci a proliferaci klonu antigen specifických T lymfocytů. Vlastní vazba LB s T-lymfocyty se uskutečňuje pomocí adhezivních molekul, po které dochází k produkci interleukinů (IL) IL-1, IL-10, IL-12 a tumor nekrotizujícího faktoru α (TNF-α), které tvoří nezbytný druhý signál k aktivaci T lymfocytů. Teprve poté nastává klonální expanze antigen specifických T lymfocytů a jejich diferenciace na efektorové a paměťové T lymfocyty, které jsou specifické pro daný alergen [(CD4+ (pomocné - Th) nebo CD8+ (cytotoxické-Tc)] [34, 40, 50]. Bez uvedených dvou kostimulačních signálů nedojde k senzibilizaci, dochází k anergii nebo apoptóze buňky. Antigen specifické efektorové T lymfocyty jsou uvolňovány z regionálních lymfatických uzlin a vstupují do krevního oběhu. Indukční fáze trvá nejméně 4 dny, ale může trvat mnoho týdnů i měsíců bez zjevných projevů na kůži [34, 39, 40].
Po opětovném kontaktu kůže s alergenem u dříve senzibilizovaných osob nastává efektorová fáze, která dosahuje vrcholu do 48 hodin. Stejně jako v indukční fázi jsou potřebné antigen prezentující buňky k aktivaci specifických paměťových T lymfocytů. Po kontaktu kůže s alergenem dochází nejprve ke spuštění nespecifické zánětlivé odpovědi. Uvolnění zánětlivých a vazoaktivních mediátorů z mastocytů (C5a, serotonin), cytokinů a chemokinů (TNF-α, IL-1α, GM-CSF – granulocyte macrophage colony-stimulatin factor, IL-18) z keratinocytů, později z monocytů a dendritických buněk, je následováno aktivací endoteliálních buněk a expresí adhezivních molekul. Akumulace specifických paměťových T lymfocytů a makrofágů je následována uvolněním cytokinů (IFN-γ, TNF-α, TNF-b, GM-CSF, IL-1). Hlavním cytokinem je IFN-γ, který společně s TNF-b zvyšuje expresi ICAM-1 – intercellular adhesion molekule-1 [34, 50, 65]. IL-12 přispívá k aktivaci cytotoxických lymfocytů a jeho účast je důležitá jak v indukční tak efektorové fázi [34, 50, 73]. Cytokiny stimulují keratinocyty k produkci IP-10 (IFN-indukovaný protein 10 kDa), Mig (monokiny indukované INF gama) a I-TAC (INF-inducibilní T buněčný alfa-chemoatraktant). Všechny tyto chemokiny přednostně míří na paměťové T buňky prostřednictvím jediného a sdíleného receptoru CXCR3 [5]. Imunohistochemicky v kůži postižené projevy AKD se nachází 70 % CXCR3 + buněk, zatímco u IKD vykazuje CXCR3 expresi jen 20 % buněk [6]. Zánětlivou reakci prohlubují aktivované mastocyty a trombocyty. Posledním krokem elicitační fáze jsou opět nespecifické zánětlivé procesy [34, 50].
Kontaktní alergeny
Počet chemických látek schopných vyvolat kontaktní senzibilizaci (KS) se odhaduje na 4 000 [40, 59]. Kontaktní alergeny jsou většinou jednoduché nízkomolekulární organické nebo anorganické sloučeniny (obvykle menší než 1 kDa) a mají různý senzibilizační potenciál. Silné, agresivní alergeny senzibilizují častěji a rychleji, dinitrochlorbenzen nebo primin jsou schopny senzibilizovat každého jedince [9, 44, 56, 59].
Přetrvávání KS
Studie potvrdily přetrvávání KS na soli niklu v 79 % po 8 letech od zjištění. U dalších alergenů se udávala průměrně v 60 %, u lanolinu přetrvávala KS po 5 letech u 41 % testovaných [19].
KS u dětí
KS stoupá se zvyšujícím se věkem, je možné jí diagnostikovat i u dětí včetně novorozenců a kojenců [15, 17, 19, 23, 32, 38, 62], u kterých se v důsledku nezralého imunitního systému předpokládala nižší schopnost vyvolat KS [9]. Publikovány byly případy s prokázanou alergickou reakcí v epikutánních testech (ET) na epoxidovou pryskyřici (z nemocničního náramku), na nikl z patentů oblečení [17], na kalafunu z EKG elektrod při dlouhodobém opakovaném monitorování srdeční akce [29, 31, 41].
Klinický obraz
Projevy ekzémového charakteru
Projevy AKD korespondují s místem kontaktu alergenu s kůží (primární lokalizace), bývají nejčastěji na rukou, předloktích (obr. 7), na obličeji, ve výstřihu a na krku. Při přetrvávajícím kontaktu se alergen přenáší prsty, oděvem na místa vzdálenější (sekundární lokalizace). Projevy akutní dermatitidy zahrnují živě červené makuly, papuly či makulopapulky velikosti špendlíkové hlavičky, uspořádané do trsů či skupinek. Při vystupňované zánětlivé reakci se objevují vezikuly, buly, mokvání, tvorba krust nebo šupin (obr. 8). Pro chronickou dermatitidu jsou typické červenohnědý erytém s/bez papulovezikul, deskvamace, hyperkeratózy, tvorba ragád a lichenifikace [27, 28, 39, 44, 59].
7. Alergická kontaktní dermatitida na soli niklu 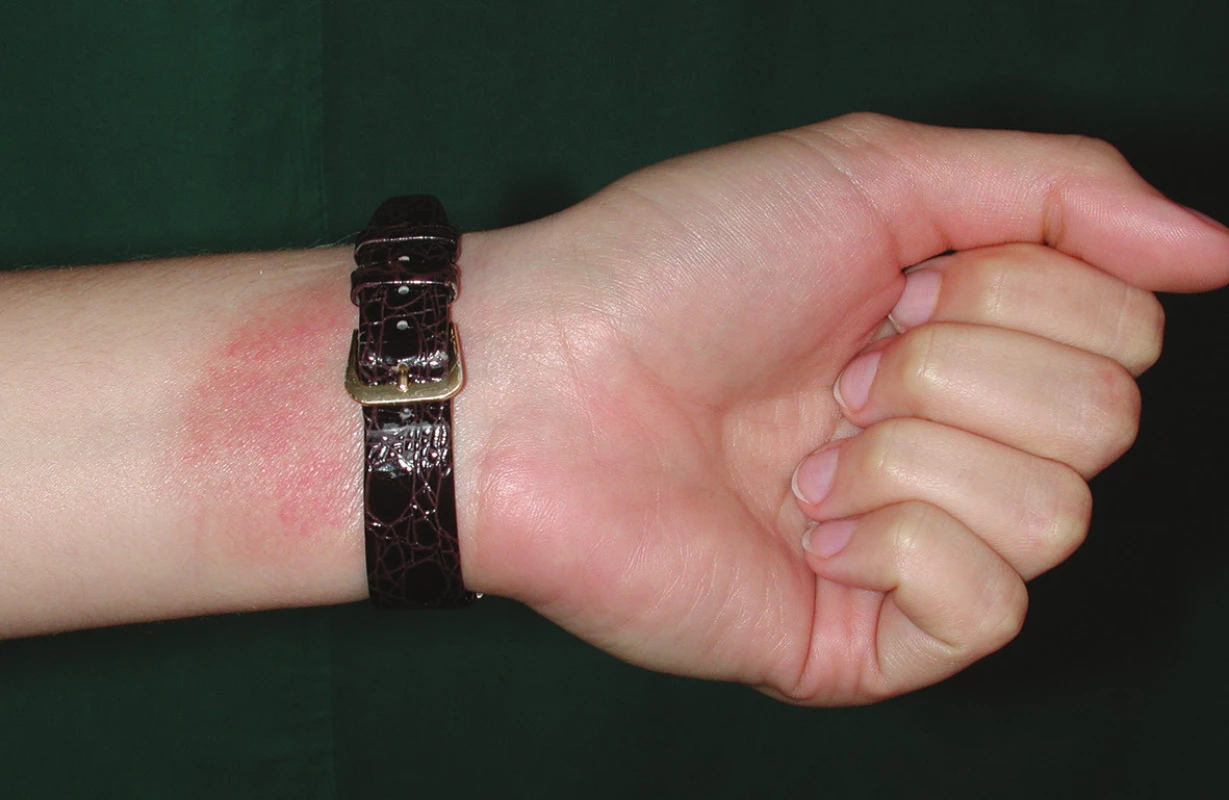
8. Alergická kontaktní dermatitida po ketoprofenu 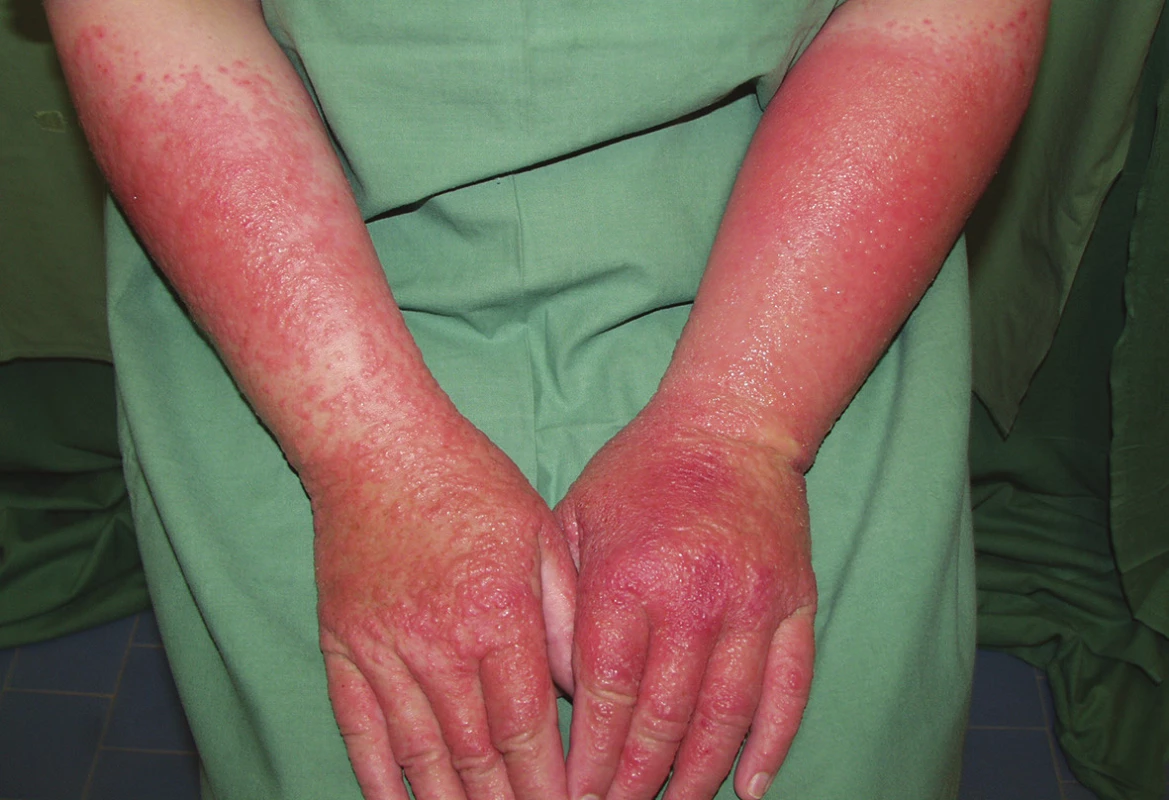
Projevy neekzémového charakteru
Některé alergeny (nikl, zlato, rtuť, paladium) vyvolávají projevy lichenoidní (obr. 9), granulomatózní (obr. 10), bulózní, papulo-nodulární nebo pustulózní projevy. Projevy typu purpury byly popsány po chemikáliích pryže, parafenylendiaminu (PPD) [8] nebo bílkovinách latexu [9, 44]. Erythema exsudativum multiforme-like reakce vyvolávají lokální léky (nesteroidní antiflogistika, antibiotika apod.) [9, 10, 27, 44, 58, 60, 70].
9. Alergická kontaktní stomatitida lichenoidního typu v dutině ústní po amalgámu 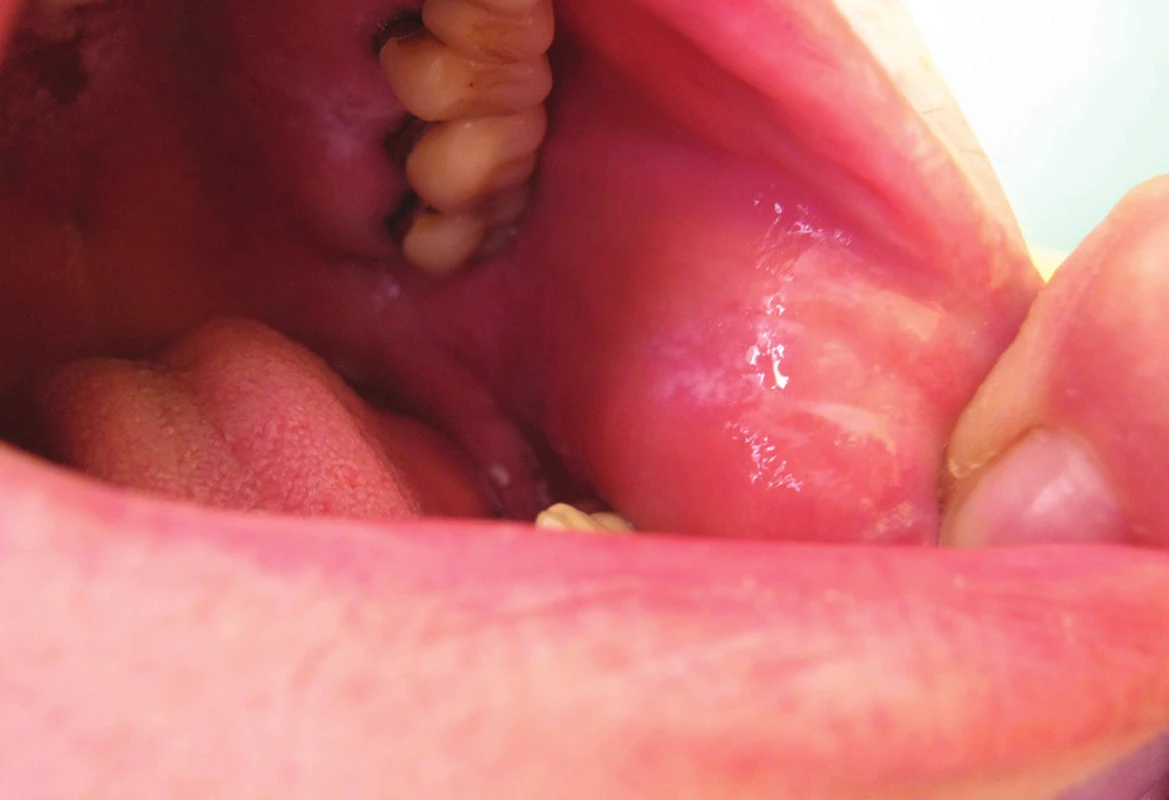
10. Alergická kontaktní cheilitida granulomatózního typu po solích rtuti v amalgámu 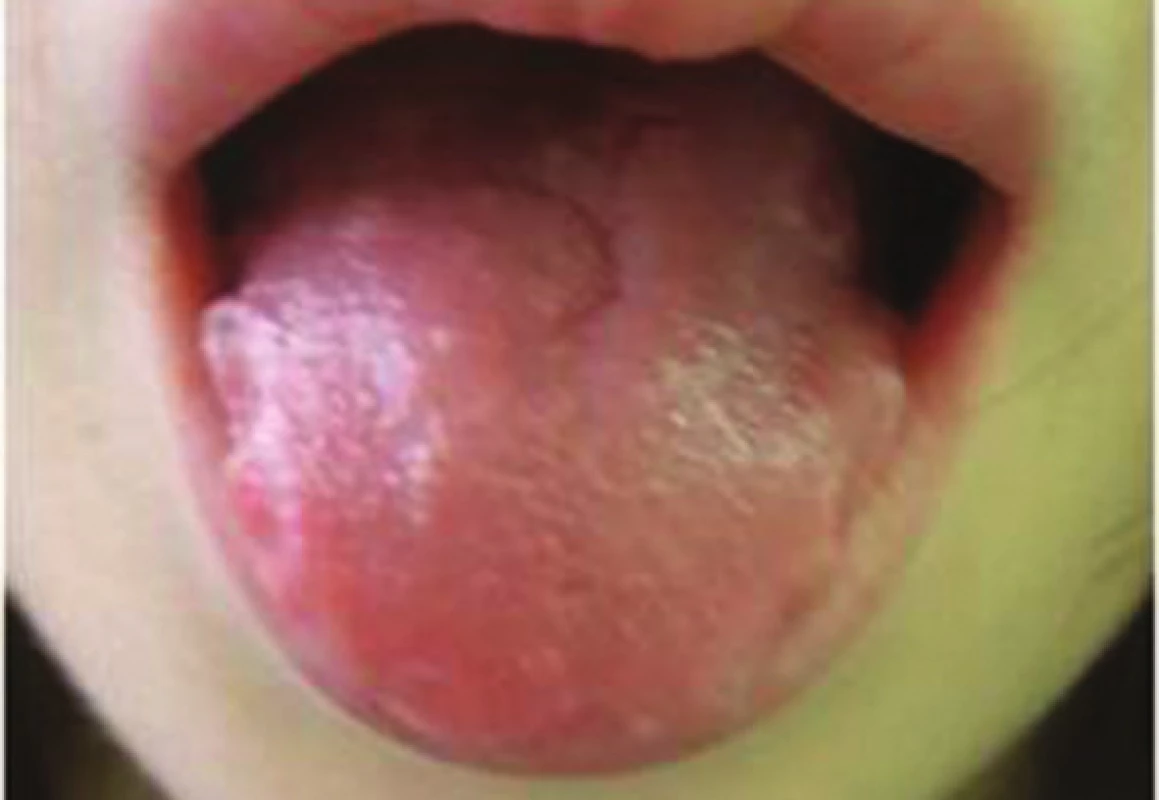
„Airborne“ alergická kontaktní dermatitida
Prevalence výskytu airborne AKD se udává od 0,6 % do 3,2 % v závislosti na studované populaci [11, 54]. Výpary alergenu nebo jeho solidní mikročástice se přenášejí vzduchem, na pylových nebo prachových částečkách. Výskyt projevů je na odhalených partiích těla (např. obličej, krk, dekolt, horní polovina hrudníku ruce, zápěstí a předloktí) a na místech s tenkou kůží (zejména na horních víčkách). Projevy se mohou vyskytovat i na místech krytých oděvem, kde dochází k hromadění látek (např. v záhybech oděvu, v podpaží apod.). Provokační faktory bývají často součástí profese nemocného. Z vyvolavatelů se uplatňují metylisothiazolinon a další konzervační prostředky (např. benzalkonium chlorid, formaldehyd, kyselina benzoová), kovy (kobalt, zlato, rtuť, paladium, apod.) syntetické a přírodní pryskyřice (obr. 11), jejich tvrdidla, izokyanáty, rostliny, dřeva, dřevný prach (zejména exotických dřevin), léky (tetrazepam, statiny, antibiotika, apod.). Pokud se na možnost kontaktní senzibilizace nemyslí, bývá pacient zpravidla léčen pod diagnózami seboroické dermatitidy nebo atopické dermatitidy apod. [2, 11, 35, 39, 54, 55, 61, 70].
11. Airborne alergická kontaktní dermatitida po kalafuně 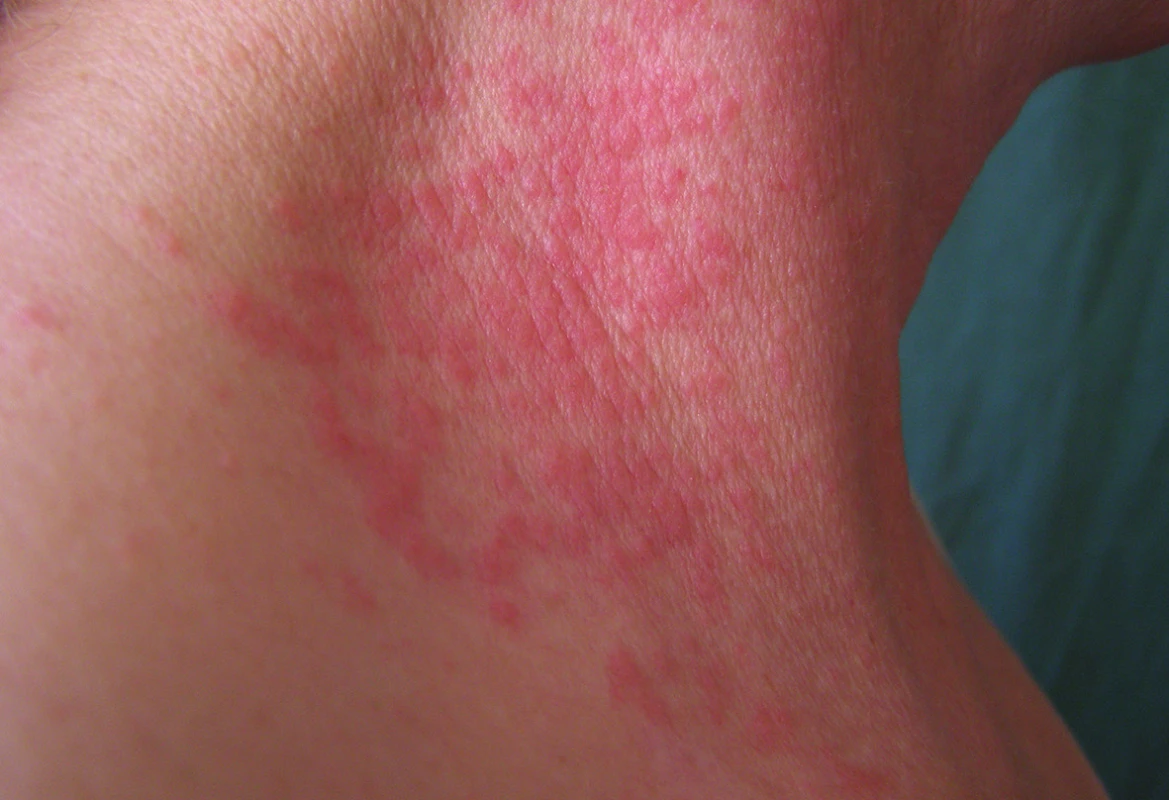
Proteinová kontaktní dermatitida
Vyvolavatelem je alergen většinou bílkovinné povahy. Přesný patofyziologický mechanismus vzniku této dermatitidy není objasněn. Předpokládají se dva mechanismy senzibilizace – pozdní (IV. typ) přecitlivělosti a/nebo časný (I. typ) typ, u kterého hrají roli IgE a/nebo IgG receptory na žírných buňkách nebo IgE receptor na Langerhansových buňkách, ale i jiné mechanismy [21, 24, 39, 44].
Projevy jsou povahy urtikariální (kontaktní kopřivka) nebo ekzémové, objevují se do půl hodiny od kontaktu s alergenem (okamžitá reakce) a přetrvávají hodiny až jeden den. Během 1–2 dnů se mohou vytvořit projevy ekzémového charakteru. V dlaních mívají charakter dysidrotické dermatitidy (obr. 12). Nejčastějším místem výskytu jsou ruce a předloktí (obr. 13). Atopická predispozice, současné ekzémové onemocnění jiné etiologie, poškození nebo oslabení kožní bariéry hrají významnou roli. Vyvolavateli jsou většinou alergeny živočišné nebo rostlinné povahy, často se jedná o profesionální senzibilizaci. Diagnóza se stanovuje pomocí epikutánních testů (bez/s předchozí lehké skarifikace), prick testů (pokud je k dispozici standardizovaný alergen, např. bílkovina latexu) nebo tzv. prick-prick testů (u nestandardizovaných alergenů) nebo testu vetřením. Prick-prick test se používá k testování čerstvých potravin, kdy se kousek potraviny propíchne lancetkou k prick testům a stejná lancetka se použije k narušení rohové vrstvy (jako u klasického prick testu). Odečítá se časná reakce (po 30 minutách), ale i pozdní typ (po 48 hodinách) [21, 24, 27, 28, 33, 39, 59, 63].
12. Proteinová kontaktní dermatitida dysidrotického typu po bílkovině latexu 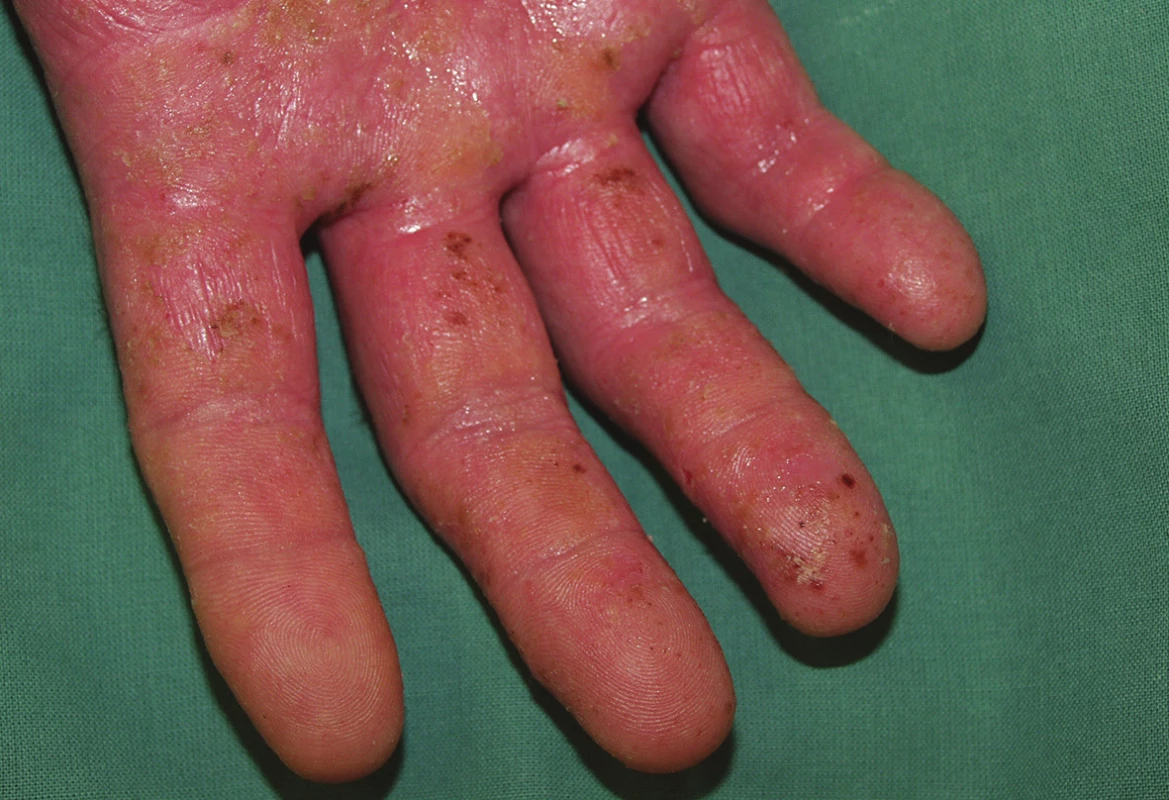
13. Proteinová kontaktní dermatitida na hřbetech rukou po mase a koření u kuchaře 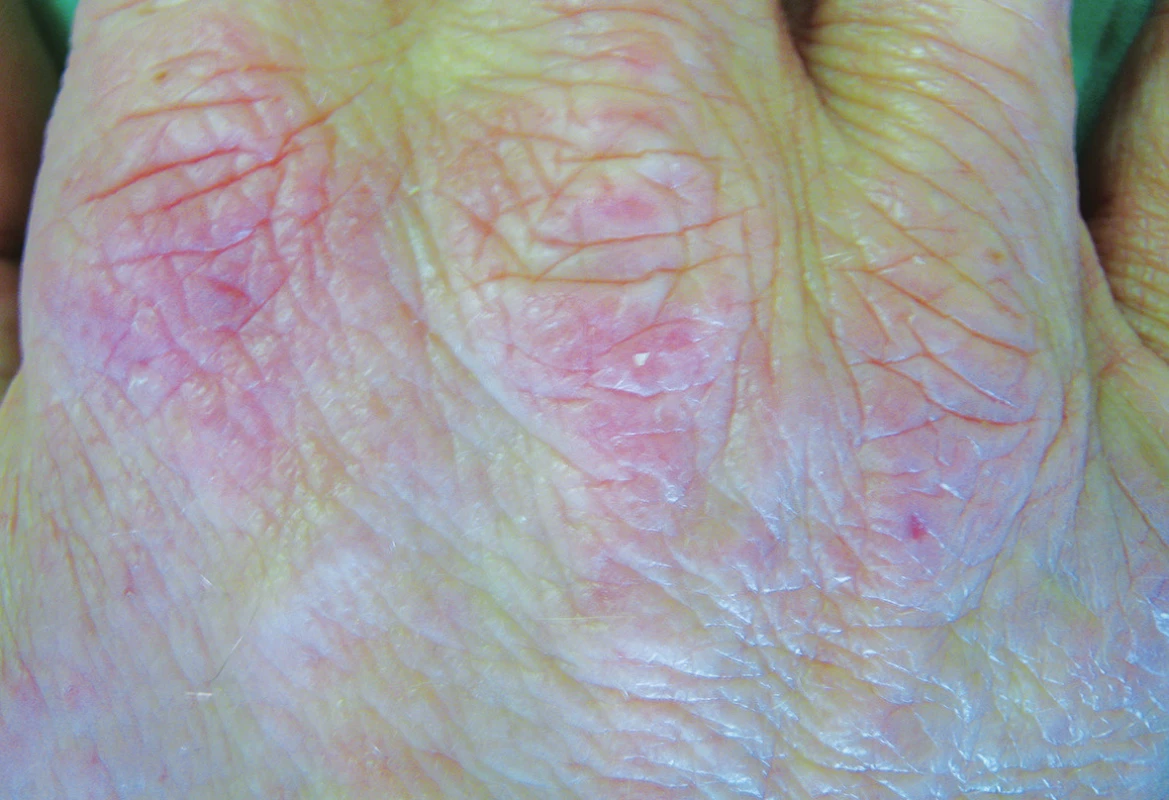
Fototoxická a fotoalergická kontaktní dermatitida
Jsou analogií iritační a alergické kontaktní dermatitidy, kde se kromě vyvolavatele (iritans, alergen) spolupodílí ultrafialové (UV) záření. Expozice noxám s fotodynamickými účinky vede k reakcím fototoxickým. U reakcí fotoalergických je podkladem KS, jejíž nezbytnou součástí je expozice kůže UV záření. Nevyskytují se příliš často.
Dermatitis fototoxica je způsobena látkami s fototoxickým (fotodynamickým) účinkem. Fotodynamicky aktivní vlastnosti (imunologicky nepodmíněné zvýšená citlivost kůže na UV záření) mají dehty a smoly, přírodní živice, deriváty ropy, chlorované naftaleny, éterické oleje, složky parfémů (tzv. berloque dermatitis) a furokumariny v některých rostlinách (viz dále) [27, 35]. Hematogenně zvyšují citlivost kůže na UV záření porfyriny, některé léky (sulfonamidy, fenothiazinové deriváty, tetracyklinová antibiotika, diuretika, chlorpromazin, perorální antidiabetika, halogenované salicylanilidy, eosin, rivanol a další). Dermatitis striata pratensis je fytofotodermatóza vyvolaná furokumariny v rostlinách (např. v bolševníku, pastináku a karotce, petrželi, kopru, pakmínu, fenyklu, citrusech a v dalších rostlinách). Většinou se uplatňuje profesionálně u zahradníků, při zpracování pastináku, mrkve apod., neprofesionální se často vyskytuje po kontaktu kůže s bolševníkem, kdy následné oslunění vyvolává vezikuly nebo buly s následnými hyperpigmentacemi [27, 28, 33, 35, 39, 42, 59, 69, 70].
U fotoalergické kontaktní dermatitidy se kromě alergenu, který funguje jako hapten, uplatňuje UV záření, jehož přítomnost je nezbytná v obou fázích (senzibilizační i elicitační) reakce. Akční spektrum UV záření leží obvykle v UVA části spektra, může se kombinovat UVA s UVB typem záření. Klinický obraz fotokontaktní alergické dermatitidy se od běžné AKD liší tím, že projevy se vyskytují výhradně na kůži vystavené UV záření (tzv. solární lokalizace – obličej, krk, dekolt, hřbety rukou, nárty apod.). K typickým fotoalergenům patří ketoprofen, fenothiazinové deriváty, kyseliny paraaminobenzoová a paraaminosalicylová, sulfonamidy, parfemace v kosmetických přípravcích, složky pracích prostředků nebo saponátů apod. [27, 28, 35, 42, 44, 59, 69, 70].
Systémová kontaktní dermatitida
Systémová (hematogenní, inhalační, intravenózní apod.) expozice chemikáliím může vyvolat generalizované projevy. Tato reakce vzniká na látky, na které byl v minulosti pacient již senzibilizovaný. Následná další systémová expozice (perorální, parenterální, intranazální, inhalační) alergenu nebo zkříženě reagujícímu alergenu vyvolá generalizované projevy. Předpokládá se mechanismus opožděné T lymfocyty zprostředkované reakce. Systémová kontaktní dermatitida byla popsána po ethylendiaminu (obsažený v infuzi s aminofylinem), po antibiotikách, rostlinách nebo rostlinných produktech, po propylenglykolu, kyselině sorbové a kovech. U některých potvrzených alergenů (např. u peruánského balzámu), které se vyskytuji v koření nebo potravinách, se doporučují dietní opatření. Dietní opatření s omezením těchto potravin mohou vést u některých pacientů ke zlepšení aktuální dermatitidy a mají sloužit jako prevence systémové kontaktní dermatitidy. Na dietní opatření při senzibilizaci na soli niklu (tzv. nízkoniklová dieta) jsou stále kontroverzní názory. Popsáno bylo zhojení klinických projevů po vyloučení potravinového doplňku obsahující chróm u pacienta s pozitivním ET na soli chrómu [9, 35, 39, 44, 72].
Diagnóza
Diagnóza AKD se stanovuje na základě anamnézy, klinického obrazu, pozitivních výsledků ET a zjištění KR. AKD může sekundárně nasedat na již existující onemocnění, což může stanovení přesné diagnózy komplikovat [9, 10, 39, 44, 59, 63].
Diferenciální diagnostika
Diferenciální diagnostika AKD zahrnuje většinu ostatní forem dermatitid, jako je IKD, atopická dermatitida, stasis dermatitis, seboroická dermatitida stejně jako erytematózní forma růžovky. AKD na dlaních a ploskách může napodobovat tineu, psoriázu apod. U generalizovaných projevů je třeba vždy na diagnózu AKD nebo na KS u jiné probíhající dermatózy (např. atopická dermatitida) myslet a vyloučit jí ET [9, 39].
Léčba
Léčbou volby jsou lokální kortikosteroidy, jejich výběr musí být podřízen klinickému obrazu a lokalizaci projevů. Je možné léčbu kombinovat s topickými imunomodulátory. K preventivnímu ošetřování vysušené, drsné a popraskané kůže jsou vhodné mastné krémy typu v/o. Celkově se podávají antihistaminika, krátkodobě je možné nasadit systémové kortikosteroidy [9, 10, 33, 39, 44].
Prevence recidiv
Ve zcela ojedinělých případech dojde k vyhasnutí alergie, u většiny pacientů přetrvává jednou vzniklá alergie celoživotně. Prevencí recidiv AKD je vyvarování se kontaktu s alergenem. Nemocného je nutné vybavit alergologickým průkazem obsahujícím jednoduše vysvětlené principy kontaktní alergie. Důležitý je podrobný informační leták o možných zdrojích zjištěného alergenu. Pro zmírnění a kompletní vyléčení projevů je nezbytné důsledné vyloučení kontaktu se zjištěným alergenem. Řada alergenů se vyskytuje současně v pracovním i v mimopracovním prostředí, v řadě případů v maskované podobě. Úplné přerušení kontaktu s určitými alergeny není vždy jednoduché, reálné a podílí se na chronickém průběhu potíží senzibilizovaných pacientů. Pacienti obdrží písemné informační letáky o výskytu zjištěných pozitivních kontaktních alergenech v běžném prostředí [9, 10, 28, 33, 39, 70].
Do redakce došlo dne 9. 5. 2016.
Adresa pro korespondenci:
Prim. MUDr. Alena Machovcová, Ph.D., MBA
Dermatovenerologické oddělení FN Motol
150 00 Praha 5
e-mail: alena.machovcova@fnmotol.cz
Sources
1. Adam, R. Skin Care of the Diaper Area. Pediatric Dermatology, 2008, 25, p. 427–433.
2. Aerts, O., Cattaert, N., Lambert, J., Goossens, A. Airborne and systemic dermatitis, mimicking atopic dermatitis, caused by methylisothiazolinone in a young child. Contact Dermatitis, 2013, 68, p. 250–251.
3. Agner, T., Menné, T. Individual Predisposition to Irritant and Allergic Contact Dermatitis. In Frosch, P. J., Menne, T., Lepoittevin, J.-P., (Eds). Contact Dermatitis. 4th ed., Berlin: Springer-Verlag, 2006, p. 127–134.
4. Agner, T., Serup, J. Seasonal variation in the skin resistance to irritants. Br. J. Dermatol., 1989, 121, p. 323–328.
5. Albanesi, C., Scarponi, C., Sebastiani, S. et al. IL-4 Enhances Keratinocytes Expression of CXCR3 Agonistic Chemokines. J. Immunol., 2000, 165, 3, p. 1395–1402.
6. Ale, S. I., Maibach, H. I. Irritant Contact Dermatitis Versus Allergic Contact Dermatitis. In CHEW, A. L., MAIBACH, H. I. Irritant Dermatitis. Berlin: Springer Verlag, 2006, p. 11–18.
7. Aramaki, J., Loffler, C., Kawana, S. et al. Irritatnt patch testing with sodium lauryl sulphate: interrelation between concentration and exposure time. Br. J. Dermatol., 2001, 145, 5, p. 704–708.
8. Batschvarov, B., Minkov, D. M. Dermatitis and purpura from rubber in clothing. Trans. St. John’s Hospital Dermatol. Soc., 1968, 54, p. 178–182.
9. Beck, M. H., Wilkinson, S. M. Contact Dermatitis: Allergic. In Burns, T., Breathnach, S., Cox, N., Griffiths, C. Rook‘s Textbook of Dermatology. 7th ed., Vol. 1, Oxford: Blackwell Science, 2004, p. 20.1–20.124.
10. Brasch, J., Becker, D., Aberer, W. et al. Guideline contact dermatitis: S1-Guidelines of the German Contact Allergy Group (DKG) of the German Dermatology Society (DDG), the Information Network of Dermatological Clinics (IVDK), the German Society for Allergology and Clinical Immunology (DGAKI), the Working Group for Occupational and Environmental Dermatology (ABD) of the DDG, the Medical Association of German Allergologists (AeDA), the Professional Association of German Dermatologists (BVDD) and the DDG. Allergo J. Int., 2014, 23, 4, p. 126–138.
11. Breuer, K., Uter, W., Geier, J. Epidemiological data on airborne contact dermatitis – results of the IVDK. Contact Dermatitis, 2015, 73, p. 239–247.
12. Bryld, L. E., Hindsberger, C., Kyvik KO et al. Genetic factors in nickel allergy evaluated in a population-based female twin sample. J. Invest. Dermatol., 2004, 123, p. 1025–1029.
13. CLARK, S. C., ZIRWAS, M. J. Management of occupational dermatitis. Dermatol. Clin., 2009, 27, 3, p. 365–383.
14. Cohen, D. E., de Souza, A. Irritant Contact Dermatitis. In Bolognia, J. L., Jorizzo, J. L., Schaffer, J. V. Dermatology. 3rd ed., Vol. I, USA: Elsevier Saunders, 2012, p. 249–259.
15. De Waard-van der Spek, F. B., Oranje, A. P. Patch Test in Children with Suspected Allergic Contact Dermatitis: A Prospective Study and Review of the Literature. Dermatology, 2009, 218, p. 119–125.
16. Dickel, H., Kuss, O., Schmidt, A. et al. Importance of irritant contact dermatitis in occupational skin disease. Am. J. Clin. Dermatol., 2002, 3, 4, 283–289.
17. Fisher, A. A. Allergic contact dermatitis in early infancy. Cutis, 1994, 54, p. 300–302.
18. Fluhr, J. W., Darlenski, R., Angelova-Fischer, I. et al. Skin irritation and sensitization: mechanisms and new approaches for risk assessment. 1. Skin Irritation. Skin Pharmacol. Physiol., 2008, 21, 3, p. 124–135.
19. GARG, S., McDONAGH, A. J. G., GAWKRODER, D. J. Age - and sex-related variations in allergic contact dermatitis to common allergens. Contact Dermatitis, 2009, 61, p. 46–47.
20. GHASRI, P., FELDMAN, S. R. Frictional lichenified dermatosis from prolonged use of a computer mouse: Case report and review of the literature of computer-related dermatoses. Dermatology Online Journal, 2010, 16, 12.
21. GIMENEZ-ARNAU, A., MAURER, M., DE LA CUADRA, J. et al. Immediate Contact Skin Reactions, an Update of Contact Urticaria, Contact Urticaria Syndrome and Protein Contact Dermatitis – „A Never Ending Story“. Eur. J. Dermatol., 2010, 20, 5, p. 552–562.
22. GOH, C. L. Prevalence of contact allergy by sex, race and age. Contact Dermatitis, 1986, 14, p. 237–240.
23. GOOSSENS, A., MORREN, M. Contact Allergy in Children. In FROSCH, PJ., MENNE, T., LEPOITTEVIN, J-P., (Eds). Contact Dermatitis. 4th ed., Berlin: Springer-Verlag, 2006, p. 811–830.
24. HANNUKSELA, M. Protein Contact Dermatitis. In FROSCH, P. J., MENNÉ, T., LEPOITTEVIN, J.-P., (Eds). Contact Dermatitis. 4th ed., Berlin: Springer-Verlag, 2006, p. 345–348.
25. JAKASA, I., VERBERK, M. M., ESPOSITO, M. et al. Altered penetration of polyethylene glycols into uninvolved skin of atopic dermatitis pacients. J. Invest. Dermatol., 2007, 127, 1, p. 129–134.
26. JOHANSEN, J. D., FROSCH, P. J., LEPOITTEVIN, J.-P. Mechanisms of Irritant and Allergic Contact Dermatitis. Contact Dermatitis, 2011, 5, p. 43–75.
27. KALENSKÝ, J. Profesionální poškození kůže v zemědělství. Praha: Avicenum, 1985, 332 s. ISBN 08-051-85.
28. KANERVA, L., ESLNER, P., WAHLBERG, J. E. et al. Condensed Handbook of Occupational Dermatology. Berlin: Springer - Verlag, 2004, 528 s. ISBN 3-540-44348-7.
29. LEE, P. W., ELSAIE, M. L., JACOB, S. E. Allergic contact dermatitis in children: common allergens and treatment: a review. Curr. Opin. Pediatr., 2009, 21, p. 491–498.
30. MACHOVCOVÁ, A. Caustic ulcers caused by cement aqua: report of a case. Ind. Health, 2010, 48, 2, p. 215–216.
31. MACHOVCOVÁ, A. Colophony, a Hidden Allergen on ECG Electrodes in a Boy After Cardiovascular Surgery. Pediatr. Dermatol., 2011, 28, 3, p. 345–347.
32. MACHOVCOVÁ, A. Contact Dermatitis in Children. In YOUNG SUCK, R. O., (Ed). Contact Dermatitis. Rijeka: InTech, 2011, p. 141–156.
33. MACHOVCOVÁ, A. Profesionální kožní nemoci z povolání. In PELCLOVÁ, D. a kol. Nemoci z povolání a intoxikace. Praha: Karolinum, 2014, p. 41–48.
34. MARTIN, S. F. New concepts in cutaneous allergy. Contact Dermatitis, 2015, 72, 1, p. 2–10.
35. McGOVERN, T. W. Dermatoses Due to Plants. In BOLOGNIA, J. L., JORIZZO, J. L., SCHAFFER, J. V. Dermatology. 3rd ed., Vol. I, USA: Elsevier Saunders, 2012, p. 273–289.
36. MICHALÍKOVÁ, H. Kontaktní alergie v dětství a dospívání. Dermatol. Prax., 2015, 9, 4, p. 167–169.
37. MODJTAHEDI, B. S., MODJTAHEDI, S. P., MAIBACH, H. I. The sex of the individual as a factor in allergic contact dermatitis. Contact Dermatis, 2004, 50, 2, p. 53–59.
38. MOUSTAFA, M., HOLDEN, C. R., ATHAVALE, P. et al. Patch testing is a useful investigation in children with eczema. Contact Dermatitis, 2011, 65, p. 208–212.
39. MOWAD, C. M., MARKS, J. G. Jr. Allergic Contact Dermatitis. In BOLOGNIA, J. L., JORIZZO, J. L., SCHAFFER, J. V. Dermatology. 3rd ed., Vol. I, USA: Elsevier Saunders: 2012, p. 233–248.
40. NEMŠOVSKÁ, J., ŠVECOVÁ, D. Súčasný pohl‘ad na patogenézu, diagnostiku, kliniku a liečbu kontaktního ekzému. Dermatol. Prax, 2014, 8, 2, p. 55–58.
41. OESTMANN, E., PHILIPP, S., ZUBERBIER, T. et al. Colophony-induced contact dermatitis due to ECG electrodes in an infant. Contact Dermatitis, 2007, 56, p. 177–178.
42. PALMER, R. A., WHITE, I. R. Phototoxic and Photoallergic Reactions. In FROSCH, P. J., MENNÉ, T., LEPOITTEVIN, J.-P. Contact Dermatitis. 4th ed., Berlin: Springer-Verlag, 2006, p. 309–317.
43. PEISER, M., TRALAU, T., HEIDLER, J. et al. Allergic contact dermatitis: epidemiology, molecular mechanisms, in vitro methods and regulatory aspects. Cell Mol. Life Sci., 2012, 69, 5, p. 763–781.
44. RIETSCHEL, R. L., FOWLER, J. F. Jr. Fisher’s Contact Dermatitis. 6th ed., Hamilton: BC Decker Inc, 2008, 862 s. ISBN 978-1-55009-378-0.
45. SEYFARTH, F., SCHLIEMANN, S., ANTONOV, D. Dry skin, barrier function, and irritant contact dermatitis in the elderly. Clin. Dermatol., 2011, 29, p. 31–36.
46. SCHEINFELD, N. Diaper dermatitis: a review and brief survey of eruptions of the diaper area. Am. J. Clin. Dermatol., 2005, 6, 5, p. 273–281.
47. SCHNUCH, A., UTER, W., GEIER, J. et al. Epidemiology of contact allergy: an estimation of morbidity employing the clinical epidemiology and drug-utilization research (CE-DUR) approach. Contact Dermatitis, 2002, 47, p. 32–39.
48. SCHNUCH, A., UTER, W., REICH, K. Allergic contact dermatitis and atopic eczema. In RING, J., PRZYBILLA, B., RUZICKA, T., (Eds.). Handbook of Atopic Eczema. 2nd ed., Berlin: Springer-Verlag, 2006, p. 178–201.
49. SCHNUCH, A., WESTPHAL, G., MOSSNER, R. et al. Genetic factors in contact allergy-review and future goals. Contact Dermatitis, 2011, 64, 1, p. 2–23.
50. SCHWARZ, T. Immunology. In BOLOGNIA, J. L., JORIZZO, J. L., SCHAFFER, J. V. Dermatology. 3rd ed., Vol. I, USA: Elsevier Saunders, 2012, p. 81–98.
51. SLODOWNIK, D., LEE, A., NIXON, R. Irritant contact dermatitis: a review. Australas J. Dermatol., 2008, 49, 1, p. 1–9.
52. SPIEKSTRA, S. W., TOEBAK, M. J., SAMPAT-SARDJOEPERSAD, S. et al. Induction of cytokine (interleukin-1alfa and tumor necrosis factor-alfa) and chemokine (CCL20, CCL27, and CXCL8) alarm signals after allergen and irritatnt exposure. Exp. Dermatol., 2005, 14, 2, p. 109–116.
53. SCHWINDT, D. A., WILHELM, K. P., MILLER, D. L. et al. Cumulative irritation in older and younger skin: a comparsion. Acta Derm. Venereol., 1998, 78, 4, p. 279–283.
54. SWINNEN, I., GOOSSENS, A. An update on airborne contact dermatitis: 2007–2011. Contact Dermatitis, 2013, 68, p. 232–238.
55. SWINNEN, I., GHYS, K., KERRE, S. et al. Occupational airborne contact dermatitis from benzodiazepines and other drugs. Contact Dermatitis, 2014, 70, p. 227–232.
56. THYSSEN, J. P., JOHANSEN, J. D., MENNÉ, T. Contact allergy epidemics and their controls. Contact Dermatitis, 2007, 56, p. 185–195.
57. THYSSEN, J. P., JOHANSEN, J. D., LINNEBERG, A. et al. The epidemiology of hand eczema in the general population – prevalence and main findings. Contact Dermatitis, 2010, 62, 75–87.
58. TOMKA, M., MACHOVCOVÁ, A., PELCLOVÁ, D. et al. Orofacial granulomatosis associated with hypersensitivity to dental amalgam. Oral Surg. Oral Med. Oral Pathol. Oral Radiol. Endod., 2011, 112, 3, p. 335–341.
59. URBANČEK, S., DASTYCHOVÁ, E., BUCHVALD, D. et al. Kontaktné alergeny v pracovnom a životnom prostředí. 2. upravené vydání, Banská Bystrica: Press Group, 2013, 304 s. ISBN 80-969307-5-3.
60. VALLADARES-NARGANES, L. M., SANCHEZ-SAMBUCETY, P., RUIZ-GONZALEZ, I. et. al. Lymphomatoid dermatitis caused by contact with textile dyes. Contact Dermatitis, 2013, 68, p. 62–64.
61. VAN STEENKISTE, E., GOOSSENS, A., MEERT, H. et al. Airborne-induced lymphomatoid contact dermatitis caused by methylisothiazolinone. Contact Dermatitis, 2015, 72, p. 237–240.
62. VOZMEDIANO, F., HITA, A. Allergic contact dermatitis in children. J. Eur. Acad. Dermatol. Venereol., 2005, 19, p. 42–46.
63. WAHLBERG, J. E., LINDGERG, M. Patch testing. In FROSCH, P. J., MENNÉ, T., LEPOITTEVIN, J.-P., (Eds.). Contact Dermatitis, 4th ed., Berlin: Springer-Verlag, 2006, p. 366–390.
64. WARNER, R. R., BOISSY, Y. L., LILLY, N. A. et al. Water disrupts stratum corneum lipid lamellae: damage is similar to surfactants. J. Invest. Dermatol., 1999, 113, 6, p. 960–966.
65. WATANABE, H., UNGER, M., TUVEL, B. et al. Contact hypersensitivity: the mechanism of immune responses and T cell balance. J. Interferon Cytokine Res., 2002, 22, p. 407–412.
66. WATKINS, S. A., MAIBACH, H. I. The hardening phenomenon in irritant contact dermatitis: an interpretative update. Contact Dermatitis, 2009, 60, p. 123–130.
67. WEDIG, J. H., MAIBACH, H. I. Percutaneous penetration of dipyrithione in man: effect of skin color (race). J. Am. Acad. Dermatos, 1981, 5, 4, p. 433–438.
68. WESTPHAL, G. A., REICH, K., SCHULZ, T. G. et al. N-acetyltransferase 1 and 2 polymorphisms in para - substituted arylamine-induced contact allergy. Br. J. Dermatol., 2000, 142, 6, p. 1121–1127.
69. WILKINSON, S. M., BECK, M. H. Contact Dermatitits: Irritant. In BURNS, T., BREATHNACH, S., COX, N., GRIFFITHS, C. Rook‘s Texbook of Dermatology. 7th ed., Vol. 1, Oxford: Blackwell Science, 2004, p. 19.1–19.30.
70. WILKINSON, S. M. Occupational Dermatoses. In BOLOGNIA, J. L., JORIZZO, J. L., SCHAFFER, J. V. Dermatology. 3rd ed. Vol. I, USA: Elservier Saunders, 2012, p. 261–272.
71. WOOD, L. C., ELIAS, P. M., CALHOUN, C. et al. Barrier disruption stimulates interleukin-1 alpha expression and release from a pre-formed pool in murine epidermis. J. Invest. Dermatol., 1996, 106, 3, p. 397–403.
72. WONG, C. C., NIXON, R. L. Systemic allergic dermatitis caused by cobalt and cobalt toxicity from a metal on a metal hip replacement. Contact Dermatitis, 2014, 71, p. 113–114.
73. YAWALKER, N., EGLI, F., BRAND, C. U. et al. Antigen-presenting cells and keratinocytes express interleukin 12 in allergic contact dermatitis. Contact Dermatitis, 2000, 42, 1, p. 18–22.
Labels
Dermatology & STDs Paediatric dermatology & STDs
Article was published inCzech-Slovak Dermatology

2016 Issue 3-
All articles in this issue
- „Airborne Dermatitis“ Caused by Disinfectants
- Trichophytia Profunda as an Occupational Disease in an Immunosuppressed Patient
- Professional Chronic Radiodermatitis
- Measles as an Occupational Disease
- Contact Dermatitis – Part I.
- Contact Allergy to Epoxy Resins
- Allergy to Titanium Proven by Patch Tests
-
Profesionální proteinová kontaktní dermatitida
– popis dvou případů
- Czech-Slovak Dermatology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Allergy to Titanium Proven by Patch Tests
- Contact Dermatitis – Part I.
- Contact Allergy to Epoxy Resins
- Trichophytia Profunda as an Occupational Disease in an Immunosuppressed Patient
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

