-
Medical journals
- Career
Koinfekce syfilis a HIV
: Z. Rozehnalová 1; J. Hercogová 1; D. Jilich 2; L. Machala 2; H. Rozsypal 2
: Dermatovenerologická klinika UK 2. LF a FN Na Bulovce, Praha přednostka prof. MUDr. Jana Hercogová, CSc. 1; Infekční klinika UK 2. LF a FN Na Bulovce, Praha Přednostka doc. MUDr. Vilma Marešová, CSc. 2
: Čes-slov Derm, 84, 2009, No. 5, p. 278-283
: Venereology
U většiny HIV pozitivních pacientů se syfilis projevuje shodně jako u HIV negativních, přesto kombinace může měnit průběh obou nákaz. HIV infekce může urychlit průběh syfilidy, a naopak syfilis může způsobit progresi chronické nákazy HIV. Článek sleduje odchylky klinického průběhu syfilidy u HIV pozitivních, upozorňuje na úskalí sérologické diagnostiky a hodnotí účinnost léčebných režimů.
Klíčová slova:
syfilis – HIV infekce – koinfekce syfilis/HIV – sérologie – terapieÚVOD
Syfilis a HIV patří mezi pohlavně přenosná onemocnění, postihují podobné skupiny osob, a koinfekce je proto běžná. Ve světě i u nás se značné množství případů vyskytuje mezi homosexuálními muži. Všem pacientům se syfilidou by mělo být doporučeno vyšetření na HIV i ostatní pohlavně přenosné infekce (STI), a naopak.
KOINFEKCE SYFILIDY A HIV
Všechna běžně popisovaná stadia syfilidy se vyskytují i u pacientů s HIV infekcí a ve většině případů se u nich projevují shodně jako u HIV negativních pacientů (14).
Kombinace infekcí HIV a syfilidy však může měnit průběh obou nákaz (9).
HIV infekce může urychlit průběh syfilidy, a naopak tato nákaza může způsobit progresi chronické HIV infekce a vyústit v přechod do vyššího stadia onemocnění (27). Diagnosticky může dojít k nálezu falešné negativity (20) stejně jako falešné pozitivity (10).
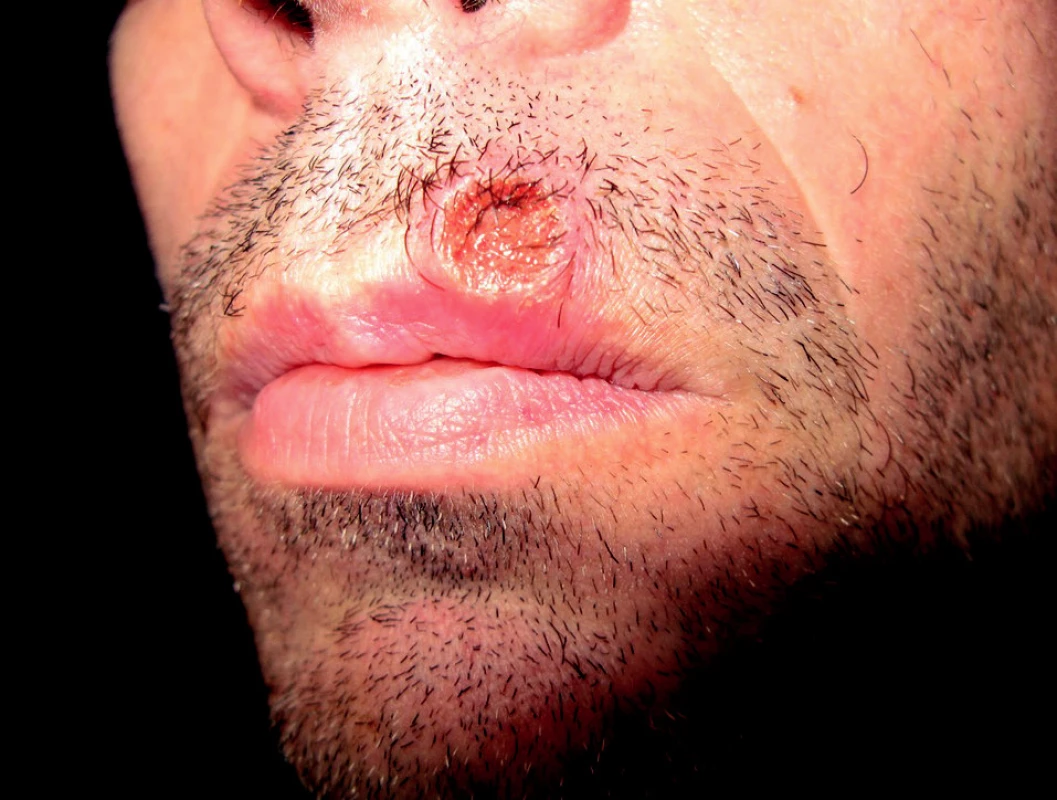
Většina HIV pozitivních pacientů s infekcí T. pallidum vyvine zcela typické projevy primárního a sekundárního stadia syfilidy, jako je tvrdý vřed a difúzní makulopapulózní exantém (5). Některé studie však ukazují na vyšší výskyt symptomatické primární syfilidy (20), rozsáhlejší či mnohočetné tvrdé vředy (14, 10), jejich prodloužené hojení (14, 10, 17) a přetrvávání těchto lézí i v sekundárním stadiu (14).
Udávána je i větší incidence klinicky manifestních sekundárních forem onemocnění (20, 17) jako i nodulární či ulcerativní exantémy, často s nekrotickými centry, tzv. lues maligna (30, 34, 12, 15). Kožní projevy druhého stadia se i přes léčbu mohou hojit pomaleji (26). Na začátku léčby se častěji setkáváme s Jarischovou-Herxheimerovou reakcí a častější bývají také klinické i sérologické exacerbace sekundární syfilidy (14). Sekundární forma může být v porovnání s imunokompetentními osobami více agresivní (20) s časným postižením centrálního nervového systému (CNS) (20, 27). Většina případů HIV – pozitivních pacientů s referovanou neurosyfilidou představují jedinci s akutní syfilitickou meningitidou, postižením hlavových nervů či jejich kombinacemi (26). Zánět mening, indukovaný samotným virem HIV, může usnadňovat průnik spirochét do CNS a podílet se tak na vzniku symptomatické neurosyfilidy (24).
Oftalmologické (20, 14, 10) i otologické (31) manifestace syfilidy jsou u HIV – pozitivních popisovány častěji ve srovnání se zbytkem populace (14).
Popsána byla i kratší doba latence do vzniku časné neurosyfilidy a její častější výskyt (6). Ve studii prováděné v San Francisku mezi lety 1985–1992 však nebyla prokázána větší incidence neurosyfilidy u HIV – pozitivních pacientů (8). Data z jednotlivých publikací se velmi často významně liší. Některé práce uvádějí například relativně rychlou progresi syfilidy do gummat, destruujících kůži, kosti a orgány (10).
Laboratorní diagnostika syfilidy u HIV – pozitivních
Ačkoli jsou v důsledku HIV infekce častější biologicky falešně pozitivní i negativní sérologické výsledky (14, 10), řídí se diagnostika syfilidy u HIV – pozitivních pacientů standardními kritérii: netreponemovými a treponemovými testy (33). Specifita a senzitivita netreponemových testů může být u HIV – pozitivních nižší (14). Jejich negativita může být způsobena selháním tvorby protilátek proti T. pallidum. Biologicky falešně pozitivní výsledky mnohdy souvisejí s polyklonální aktivaci B-lymfocytů (14) a jejich falešnou pozitivitu verifikuje negativní fluorescenční test. Jestliže mají pacienti pozitivní netreponemový test a negativní konfirmační treponemové testy, je diagnóza aktivní syfilidy velmi nepravděpodobná. Z toho vyplývá nezbytnost zhodnocení dostatku dat pečlivě zjišťovaných v rámci anamnézy s cílenými venerologickými dotazy, klinickým vyšetřením zahrnujícím venerologické vyšetření, srovnání předchozích sérologických testů a ostatní laboratorní vyšetření event. biopsie podezřelých lézí (14).
Při podezření na primární syfilidu je nutné udělat vyšetření v zástinovém mikroskopu, protože sérologické testy mohou být v té době ještě negativní. U běžně používaných netreponemových testů (RPR, VDRL) jsou někdy titry protilátek u HIV+ pacientů naopak vyšší, než je tomu ve zbytku populace (14, 11). Oproti HIV – negativním pacientům s průměrnými titry netreponemových testů ve studii se sekundární syfilidou 1 : 32 byly titry HIV – pozitivních 1 : 128 (11). Taktéž jejich pokles, jakožto odpověď na léčbu penicilinem, může být mnohem pomalejší (10, 26). Častější je i tzv. zonální fenomén, tedy stav, kdy jsou netreponemové testy interpretovány jako negativní, neboť vzorek nebyl dostatečně naředěn a vysoká koncentrace antigenů nedovolí odečíst komplexy antigen–protilátek (14). Zonální fenomén může způsobit falešně negativní netreponemové testy, hlavně ve II. stadiu syfilidy, kdy je vysoká koncentrace treponemových antigenů (14). Jestliže je pozitivní mikroskopické vyšetření primárních či sekundárních lézí v zástinu a sérologické testy jsou negativní, je třeba vyloučit zonální fenomén kvantitativním stanovením netreponemových testů a jejich naředěním.
V praxi se u pacientů s HIV infekcí setkáváme s častějšími sérologickými exacerbacemi po léčbě syfilidy (14, 10). Ačkoliv klinické zkušenosti předpokládají negativizaci netreponemových testů po léčbě, studie 857 pacientů ukázala, že 28 % pacientů s primární syfilidou a 44 % se sekundární syfilidou mělo perzistující netreponemové testy ještě 36 měsíců po léčbě (10). V jiné studii mělo přibližně 80 % HIV – pozitivních pacientů adekvátní sérologickou odpověď za šest měsíců po terapii syfilidy. V menším procentu byl zjištěn méně než čtyřnásobný pokles netreponemových testů (2).
Je třeba uvést, že ačkoliv se sérologická odpověď HIV – pozitivních po léčbě časné syfilidy někdy liší od HIV – negativních pacientů, ve většině případů není tento rozdíl klinicky významný. Přesto jsou následné klinické a sérologické kontroly nutností k vyloučení přetrvávající infekce (20, 14). Důležité je také odlišení reinfekce, neboť protilátky proti Treponema pallidum nejsou protektivní, a reinfekce je tak možná při každé další rizikové expozici.
Postižení CNS je při nákaze syfilidou možné v jakémkoli stadiu syfilidy. U HIV – pozitivních osob k tomu dochází relativně častěji (14). CNS je běžně asymptomaticky postižen při časné syfilidě, standardní dávky penicilinu a adekvátní imunitní odpověď jsou však pro tyto případy terapeuticky dostatečné (26). Popisována je ale i vyšší frekvence symptomatické neurosyfilidy a očního postižení, proto by mělo být u imunodeficitních pacientů na tuto formu onemocnění pomýšleno (14, 10). Neurosyfilis se, kromě neurologického vyšetření zkušeným specialistou na tuto problematiku a sérologickými testy, stanovuje především vyšetřením mozkomíšního moku (cerebrospinal fluid, CSF). Kromě shodných treponemových i netreponemových testů používaných při vyšetření séra se navíc určuje hladina glukózy, bílkovin a leukocytů v likvoru.
Kritéria CDC pro provedení lumbální punkce u pacientů se syfilidou jsou následující: neurologické a/nebo oční symptomy; pozdní latentní syfilis nebo syfilis nejasné délky trvání u HIV – pozitivních; aktivní terciární syfilis; selhání léčby syfilidy (10). Někteří odborníci doporučují lumbální punkci u všech pacientů s koinfekcí HIV/lues. Některé práce uvádějí vysoké riziko asymptomatické neurosyfilidy u osob s netreponemovými testy vyššími než 1 : 32 a počty CD4+ < 350/μl (10).
Lumbální punkce je nyní u HIV – pozitivních pacientů bez neurologických obtíží doporučována jen při latentní syfilidě pozdního či nejasného data (10). Abnormity v likvoru jsou časté u HIV – pozitivních i negativních pacientů v době primární, sekundární či časné latentní syfilidy. Takovéto nálezy však mají neznámou prognostickou hodnotu a většinou mizí po standardní terapii penicilinem (29). Vyšetření likvoru před zahájením léčby proto není v těchto stadiích indikované ani u HIV – pozitivních. Samozřejmostí je také vyšetření mozkomíšního moku ve všech stadiích při jakýchkoli neurologických příznacích, včetně abnormálního chování, psychických změnách, očních, ušních či neurologických symptomech. Vyšetření likvoru je nutné také po selhání terapie časných stadií syfilidy (10).
Diagnostika neurosyfilidy u HIV infikovaných je založena na vyhodnocení vzorku likvoru, ve kterém nacházíme zvýšený počet leukocytů, zvýšenou hladinu bílkovin a pozitivitu VDRL testu (6). Senzitivita CSF-VDRL je však poměrně nízká, pohybuje se mezi 30 – 70 % (10).
Jestliže je VDRL test v likvoru negativní, je stanovení diagnózy neurosyfilidy obtížné. Samotná HIV infekce totiž stejně jako syfilis nervového systému mírně zvyšuje hladinu lymfocytů v CSF (23). Proto při negativitě CSF-VDRL může diagnózu neurosyfilidy potvrdit či vyloučit reaktivní fluorescenční test CSF-FTA (CSF-FTA-ABS) a procento CSF B-lymfocytární pleocytózy (23).
Oproti netreponemovému CSF-VDRL testu má CSF-FTA-ABS poměrně vysokou senzitivitu, avšak nízkou specifitu (10). Samotný likvorový FTA-ABS test tak může pomoci vyloučit neurosyfilis, je-li negativní, ale pozitivní výsledky nejsou specifické (6, 23).
1. Exantémy syfilis II bývají u HIV+ častější. 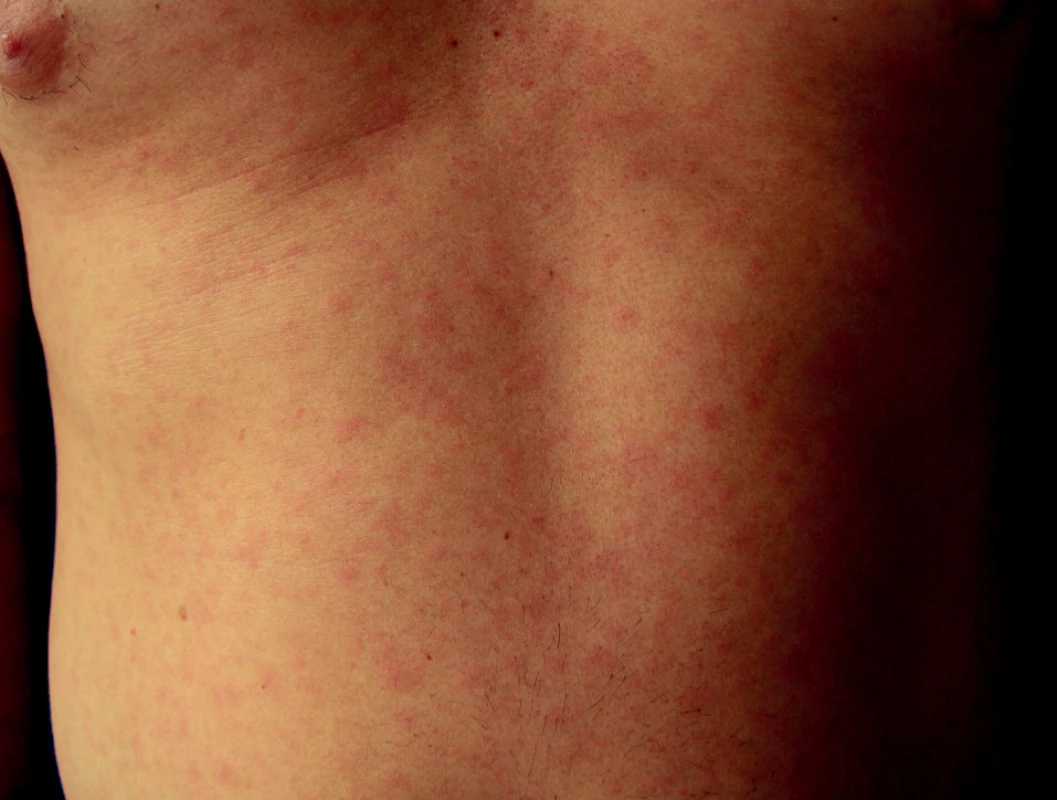
Terapie syfilidy u HIV – pozitivních
Terapie syfilidy u HIV – pozitivních osob se řídí podobnými pravidly jako u ostatních pacientů. Základním lékem stále zůstává penicilin podávaný parenterálně. U pacientů s anamnézou alergie na penicilin je vhodné provést kožní testy k jejímu ověření, po kterém se doporučuje desenzibilizace.
V naší zemi se tradičně používají spíše větší dávky a delší doba léčby.
Některé publikace poukazují u imunodeficitních pacientů na menší úspěšnost standardní terapie časné syfilidy i častější selhání terapie obecně (10). Proto je nezbytné provádět po ukončení terapie pečlivé kontroly, s klinickým vyšetřením za 1–2 týdny a dále klinické a sérologické kontroly za 3, 6, 9, 12 a v případě pozdní latentní syfilidy a neurosyfilidy i 24 měsíců po léčbě (14). Lékaři by též měli sledovat pacienty častěji a delší dobu, než je obvyklé, jestliže existuje jakákoliv pochybnost o správnosti jejich klinické či sérologické odpovědi. Při kontrolách je důležité používat stejné netreponemové testy, protože RPR a VDRL testy nejsou svými titry srovnatelné.
Všichni HIV – pozitivní pacienti by měli být v případě nákazy syfilidou léčeni penicilinem (20). Doxycyklin a cefalosporiny nejsou léky volby, protože nebyly provedeny studie k určení přesných dávek a doby léčby. Ze stejných důvodů není např. CDC (Centers for Diseases Control and Prevention) doporučován erytromycin a azitromycin. Ačkoliv se azitromycin zdál být nadějným lékem pro perorální léčbu v inkubační době a u časné syfilidy (16, 28), nedávno publikovaná data ukázala vysokou míru rezistence (více než 56 % v San Francisku, 2004) a je tedy jasné, že toto antibiotikum nemůže být pro všeobecné použití doporučováno (21, 25). Jediný amoxicilin má určitý teoretický benefit díky zvýšené penetraci do CNS, která dosahuje treponemocidních hodnot. Studie srovnávající léčbu samotným benzylpenicilinem a jeho kombinaci s amoxicilinem však neukázala významnější rozdíly (29).
Před zahájením léčby všech stadií syfilidy musí být pacient pečlivě vyšetřen k vyloučení neurologického postižení.
U primární, sekundární a časné latentní syfilidy je léčba shodná jako u HIV – negativních pacientů – benzathin benzylpenicilin G 2,4 MIU i. m. jednorázově (14). Někteří odborníci však u HIV – pozitivních s časnou syfilidou předpokládají větší riziko neurologických komplikací a vyšší riziko selhání léčby standardními režimy. Míra rizika však není přesně definována a lze pouze spekulovat. V zahraničních publikacích se mnohdy setkáváme s přídavnou terapií, nejčastěji ve formě více dávek benzathin benzylpenicilinu G (jako u latentní syfilidy). V České republice se rutinně používá 10–14denní kúra prokain penicilinu 1,5 mil. IU i. m. podávána 1 krát denně, zakončená 2,4 mil. IU benzathin benzylpenicilinu G i. m. (19) či přidáním jiných antibiotik. Vzhledem k nedostupnosti balení 2,4 mil. IU v ČR je toto balení nyní nahrazováno 2 x 1,5 mil. IU benzathin benzylpenicilinu i. m. jednorázově. Alternativní režimy (makrolidy apod.) nejsou vzhledem k nedostatku studií a možnosti rezistence doporučovány (14). U pacientů s anamnézou penicilinové alergie je doporučováno tuto skutečnost ověřit. U dobře spolupracujících pacientů, u kterých není možná desenzibilizace, je CDC doporučována (s výjimkou neurosyfilidy) léčba doxycyklinem (16, 28). V praxi se používá doxycyklin 100 mg p.o. à 12 h po dobu 14 dní. Terapeutický účinek tohoto schématu není jednoznačně ověřen u HIV infikovaných pacientů. Ceftriaxon může být též zvažován jako alternativa, ačkoli přesné schéma léčby není stanoveno. Někteří odborníci doporučují 1 g i.m. či i.v. po dobu 8 až 10 dní (1, 7, 32).
V případě pozdní latentní infekce nebo syfilidy neznámého stáří je před léčbou doporučována lumbální punkce k vyloučení postižení CNS (14). Jsou-li parametry mozkomíšního moku normální, léčíme benzathin benzylpenicilinem G v celkové dávce 7,2 MIU rozdělené do tří i. m. dávek po týdnu (14) (v ČR nyní 1,5 MIU benzathin benzylpenicilinu do levého a pravého hýžďového svalu 3 krát à týden). Ostatní léčebné režimy (tetracykliny, ceftriaxon apod.) nejsou u HIV pacientů podrobně prostudovány (14). Není-li jiná možnost, používá se v praxi doxycyklin 100 mg p.o. 2 krát denně po 28 dní. Jestliže není možné likvor vyšetřit, je vhodné léčit schématy pro neurosyfilis.
Intravenózní krystalický penicilin zůstává stále lékem volby u všech forem neurosyfilidy a očních postižení (18). Základní denní dávka i. v. benzylpenicilinu (penicilinu G draselné soli) je 18–24 MU, rozdělená na 6 dávek à 4 h po dobu 10–14 dní (6). Není-li intravenózní aplikace možná, doporučuje se prokain penicilin 1,5 mil. IU i. m. 1 krát denně plus probenecid (t. č. není v ČR registrován) 500 mg p. o. à 6 h po dobu 14 dní; injekční aplikace jsou však často bolestivé a vyžadují dobrou compliance pacienta (6). Většina odborníků doporučuje oba tyto léčebné režimy zakončit benzathin benzylpenicilinem G 2,4 MIU i. m. 3–4 krát v týdenních intervalech.
Ostatní léčebné režimy (tetracykliny, makrolidy), jež byly použity u neurosyfilitických pacientů s normální imunitou, nejsou vzhledem k neznámé účinnosti u HIV – pozitivních doporučovány. U pacientů s neurosyfilidou lze označit jako jedinou účinnou alternativu vzhledem ke své dobré CSF penetraci a delšímu poločasu ceftriaxon v denní dávce 2 g při parenterálním podání po dobu 14 dní (22).
Vyšetření likvoru po této terapii je doporučováno za 6, 12 a 24 měsíců ke sledování normalizace mozkomíšních parametrů (2). Pleocytóza by se měla upravit do šesti měsíců a celkově by měl být mozkomíšní mok bez odchylek do dvou let (2).
Doporučení pro léčbu latentní syfilidy a neurosyfilidy jsou dány spíše klinickými zkušenostmi než kontrolovanými studiemi (10). Z obav z neurologické exacerbace a přetrvávání živých treponemat v mozkomíšním moku u HIV – pozitivních pacientů léčených benzathin benzylpenicilinem, doporučují někteří odborníci prodloužit celkovou dobu léčby, zvýšit dávky a tím zlepšit CSF penetraci. Předpoklady k těmto doporučením jsou však pouze teoretické.
U nás se většinou doporučuje pro léčbu syfilidy u HIV – pozitivních zavést léčebný režim jako u non HIV+ pacientů s neurosyfilidou. Tedy větší dávky po delší dobu. Například benzylpenicillin (draselná sůl penicilin G) 24 mil. j. denně i. v. v 6 dávkách po 4 mil. j. po dobu 2 týdnů s následným benzathin benzylpenicillinem 2 x 1,5 mil. j. i. m. v týdenních intervalech po 3 týdny, ev. prokain penicilin.
U novorozenců a dětí s podezřením na koinfekci syfilis a HIV je preferována intravenózní léčba benzylpenicilinem (35), léčebné schéma u dětí závisí na řadě faktorů a je konsenzem odborníků z oboru venerologie, infektologie, pediatrie a mikrobiologie (NRL pro dg. syfilis).
Pro možnost časné klinické exacerbace po terapii syfilidy u HIV pacientů jsou nutné následné časté kontroly. Dispenzární péče by měla být zaměřena především na klinické příznaky, neurologické obtíže a stoupající sérologické titry. Opakovaná léčba je podávána hlavně v souvislosti s nedostatečným poklesem netreponemových testů (10).
Určení úplného vyléčení není jednoduché, neboť neexistuje jednoznačné kritérium. Přetrvávající pozitivita RPR či VDRL testu nemusí znamenat aktivní infekci, ale spíše nepatologickou přetrvávající vyšší sérologickou hladinu. Je třeba také vzít v potaz, že kritéria pro selhání léčby byla stanovena podle sérologických odpovědí pacientů s normální imunitní odpovědí. Tato kritéria jsou následující: přetrvávání, rekurence či vznik klinických příznaků syfilidy; přetrvávající (déle než dva týdny) čtyřnásobný vzestup titrů netreponemových testů; nepřítomnost čtyřnásobného poklesu netreponemových testů za 6–12 měsíců po léčbě primární, sekundární a časné latentní syfilidy a za 12–24 měsíců po léčbě syfilidy pozdní a nejasného stáří (3, 13).
Všichni pacienti s primární, sekundární či časnou latentní syfilidou, u kterých selhala terapie, by měli mít vyšetřen mozkomíšní mok a být znovu léčeni benzathin benzylpenicilinem 2 x 1,5 MIU i. m. 1 krát týdně po dobu 3 týdnů (pokud je výsledek vyšetření mozkomíšního moku normální). Dále by měli být vyšetřováni každých 6 a 12 měsíců.
Pro pacienty po první léčbě neurosyfilidy jsou nutná vyšetření likvoru v šesti měsíčních intervalech do normalizace nálezu. Abnormality CSF v počtu bílých krvinek a hladiny bílkovin by se měly normalizovat do 6 měsíců po léčbě (není-li současně přítomna jiná infekce CNS), ale CSF – VDRL test se nemusí normalizovat ještě po dobu minimálně dvou let. Jestliže však jsou tyto CSF parametry abnormální ještě po dvou letech, měli by být pacienti schématy pro neurosyfilidu opakovaně léčeni.
Koinfekce syfilis a HIV v Praze
Oficiální počty koinfekce syfilis a HIV nejsou běžně sledovány v České republice ani ve světě. Praha je tradičně krajem se suverénně nejvyšším výskytem HIV infekce, 520 osob k 31. 12. 2007 (36). AIDS centrum FN Na Bulovce má v ČR registrovaný největší počet HIV pozitivních pacientů, přibližně 80 %, ke konci roku 2007 tedy něco přes 800 registrovaných HIV – pozitivních. Proto lze podobnou situaci očekávat v celé republice. Počet námi zjištěných pacientů pražského AIDS centra s koinfekcí HIV/syfilis (včetně již nežijících) k 31. 12. 2007 byl 94, nejstarší nákaza virem HIV v našem souboru pacientů pocházela z roku 1986. Z 96 případů koinfekce HIV/syfilis bylo 86 mužů a 8 žen. Žádné dítě (0–18 let) nemělo tuto koinfekci. Z ostatních STI byla nejčastější nákaza kapavkou (19 pacientů), a to mnohdy i opakovaně. Dále hepatitidou B (14 krát) , hepatitidou C (3 krát), akuminátními kondylomaty (3 krát) a svrabem (1 krát).
Českou národnost mělo 78 mužů (z toho 1 současně i francouzské občanství), 3 muži pocházeli z Ruska, 1 ze Slovenska, 1 z Ukrajiny, 1 z Velké Británie, 1 z Libanonu a 1 z Pobřeží Slonoviny. Hodně českých mužů přiznalo pohlavní styky v cizině nebo s cizinci. Z žen byly 4 Ukrajinky, 2 Češky, 1 Ruska a 1 pocházela z Litvy. Převážná většina mužů s touto koinfekcí uvedla jako způsob přenosu homosexuální (72 mužů, z toho 1 krát navíc i. v. aplikace drog) či bisexuální (9 mužů) pohlavní styk. U mužů heterosexuálně orientovaných byl dále přítomen ještě aspoň jeden rizikový faktor: jiná národnost (1 krát Rusko, 1 krát Ukrajina, 1 krát Pobřeží Slonoviny), pohlavní styk se ženou jiné národnosti (1 krát s Ukrajinkou), transfúze (1 krát), jiná národnost + abúzus drog (1 krát Rus + i. v. drogy).
Všechny ženy (8) v našem souboru byly heterosexuálně orientované, též s alespoň jedním rizikovým faktorem: prostituce (1 krát), i. v. drogy (1 krát), jiná národnost (Ukrajina 2 krát), jiná národnost + prostituce (1 krát Ukrajina, 1 krát Litva), jiná národnost + i. v. drogy (Rusko 1 krát), jiná národnost + i. v. drogy + prostituce (1 krát Ukrajina).
Nákaza samotným virem HIV námi sledovaných pacientů byla největší ve věkové kategorii 30–34 let (18 mužů), následováno věkovou kategorií 40–44 let (15 mužů) a 25–29 let (14 mužů) . Mezi ženami byla nákaza virem HIV, až na jediný případ (44 let, Litva), zjištěna ve věku 20–29 let. U čtyř žen byly obě infekce (HIV a syfilis) zjištěny v graviditě, v jednom případě byla v graviditě zjištěna nákaza samotným virem HIV. Z pěti těhotenství se v AIDS centru FN Na Bulovce narodilo celkem šest dětí (1 krát dvojčata), vzhledem k zajišťovací terapii a celému systému preventivních opatření byly všechny děti zdrávy (HIV a syfilis po 24 měsících negativní).
Dalším sledovaným parametrem byl časový vztah mezi nákazou syfilis a nákazou virem HIV. Syfilis jako svou první nákazu mělo 31 mužů, ale z nich měli dále 3 muži recidivu syfilidy již v době, kdy věděli o své nákaze HIV. U 22 mužů byly obě infekce zjištěny současně. Nejprve zjištěnou nákazu virem HIV mělo 33 mužů, kteří se až poté nakazili syfilidou, navíc jeden muž se syfilidou nakazil opakovaně (1 krát reinfekce) během své HIV pozitivity. Oproti mužům byla u žen zjištěna syfilis buď současně (5 krát), nebo před (3 krát) zjištěním nákazy HIV.
Terapie syfilidy byla nejčastěji kombinací prokain penicilinu a benzathin benzylpenicilinu (39 krát), kúrou prokain penicilinu (24 krát), benzathin benzylpenicilinu (8 krát), doxycyklinu – při alergii na penicilin – (8 krát), počátečními injekcemi prokain penicilinu, zaměněnými za p.o. doxycyklin pro alergii (2 krát), kombinací krystalického penicilinu s dokončením léčby prokain penicilinem (1 krát), v ojedinělých případech i jinými p.o. antibiotiky, většinou v cizině: azitromycinem (1 krát), erytromycinem (1 krát), klaritromycinem (1 krát).
ZÁVĚR
V článku jsme uvedli data, která jsme zjistili u pacientů registrovaných v AIDS centru FN Na Bulovce s koinfekcí HIV/syfilis. Šlo převážně o homo/bisexuálně orientované muže. Do budoucna očekáváme vyšší incidenci této koinfekce, a proto by dermatovenerologové měli být seznámeni s možnými odchylkami v klinickém průběhu, diagnostice a terapeutickém přístupu k této nákaze.
Došlo do redakce: 15. 5. 2009
MUDr. Zuzana Rozehnalová
Dermatovenerologická klinika
2 LF UK a FN Na Bulovce
Budínova 2
180 81 Praha 8
E-mail: fiedlerova@post.cz
Sources
1. Augenbraun, M. Workowski, K. Ceftriaxone therapy for syphilis: report from the emerging infections network. Clin Infect Dis, 1999, 29, p. 1337-8.
2. BOLAN, G. Syphilis and HIV. HIV In Site Knowledge Base Chapter, 1998, May, p. 1-20.
3. Brown, ST. Zaidi, A. Larsen, SA. Serological response to syphilis treatment. A new analysis of old data. JAMA, 1985, 253, p. 1296-9.
4. BUCHACZ, K. GREENBERG, A. ONORATO, I. Syphilis epidemics and human immunodeficiency virus (HIV) incidence among men who have sex with men in United States: implications for HIV prevention. Sex Transm Dis, 2005, 32 (10), p. 73-9.
5. BUTT, M. NANDWANI, R. Sexually transmitted diseases in HIV-1-infected patiens. Lancet, 2001, 357, p. 1533.
6. CARMO, AR. MOURA, SA. CHRISTO, P. Syphilitic meningitis in HIV-patients with meningeal syndrome. Braz j. Infect Dis, 2001, 5 (5), p. 280-287.
7. Centers for Disease Control and Prevention. Sexually transmitted diseases treatment guidelines 2002. MMWR Recomm Rep, 2002, 51, p. 1-78.
8. FLOOD, JM. WEINSTOCK, HS. GUROY, ME. Neurosyphilis during the AIDS epidemic, San Francisco, 1985-1992. J Infect Dis 1998, 177, p. 931-40.
9. FUNNYE, AS. AKHTAR, AJ. Syphilis and human immunodeficiency virus co-infection. J Natl med Assoc, 2003, 95 (5), p. 363-82.
10. GOLDEN, R. MARRA, Ch. HOLMES, K. Update on syphilis: resurgence of an old problem. JAMA, 2003, 290 (11), p. 1510-1514.
11. GOUREVITCH, MN. SELWYN, PA. DAVENNY, K. Effects of HIV infection on the serologic manifestations and response to treatment of syfilis in intravenous drug users. Ann Intern Med, 1993, 118 (5), p. 350-5.
12. Gregory, N. Sanchez, M. Buchness, MR. The spectrum of syphilis in patients with human immunodeficiency virus infection. J Am Acad Dermatol, 1990, 22, p. 1061-7.
13. Guinan, ME. Treatment of primary and secondary syphilis: defining failure at three - and six - month follow-up. JAMA, 1987, 257, p. 359-60.
14. HALL, S. Ch., KLAUSNER, D. J., BOLAN, A. G. Managing syphilis in the HIV-infected patient. Curr Infect Dis Rep, 2004, 6, p. 72-82.
15. Hicks, CB. Benson, PM. Lupton, GP. Seronegative secondary syphilis in a patient infected with the human immunodeficiency virus (HIV) with Kaposi sarcoma. A diagnostic dilemma. Ann Intern Med, 1987, 107, p. 492-5.
16. Hook, EW. Martin, DH. Stephens, J. A randomized, comparative pilot study of azithromycin versus benzathine penicillin G for treatment of early syphilis. Sex Transm Dis, 2002, 29, p. 486-90.
17. HUTCHINSON, CM. HOOK, EW. SHEPHERD, M. HIV and the presentation of early syphilis. Ann Intern Med, 1994, 121, p. 94-99.
18. JAY, CA. Treatment of neurosyphilis. Curr Treat Options Neurol, 2006, 8 (3), p. 185-92.
19. Kuklová, I. Kojanová, M. Velčevský, P. Současný stav problematiky sexuálně přenosných onemocnění, Čes-slov Derm, 2008, 83 (3), p. 115-121.
20. KURUMUDI, UR. AUGENBRAUN, M. Syphilis and HIV: a dangerous duo. Expert Rev Anti Infect Ther, 2005, 3 (5), p. 825-31.
21. Lukehart, SA. Godornes, C. Molini, BJ. Macrolide resistance in Treponema pallidum in the United States and Ireland. N Engl J Med, 2004, 351, p. 154-8.
22. Marra, CM. Boutin, P. McArthur, JC. A pilot study evaluating ceftriaxone and penicillin G as treatment agents for neurosyphilis in human immunodeficiency virus-infected individuals. Clin Infect Dis, 2000, 30, p. 540-4.
23. MARRA, CM. TANTALO, LC. MAXWELL, CL. Alternative cerebrospinal fluid tests to diagnose neurosyphilis in HIV-infected individuals. Neurology, 2004, 63 (1), p. 85-8.
24. MARRA, Ch. Syphilis, Human immunodeficiency virus, and the nervous system. AIDS and the Nervous System, 1997, Philadelphia, p. 677-690.
25. Mitchel, SJ. Engelman, J. Kent, CK. Azithromycin-resistant syphilis infection: San Francisco, California, 2000-2004. Clin Infect Dis, 2006.
26. MUSHER, DM. HAMILL, RJ. BAUGHN, RE. Effect of human immunodeficiency virus (HIV) infection on the course of syphilis and on the response to treatment. Ann Intern Med, 1990, 113 (11), p. 872-81.
27. PODWINSKA, J. Syphilis and AIDS. Arch immunol Ther Exp, 1996, 44 (5-6), p. 329-33.
28. Riedner, G. Rusizoka, M. Todd, J. Single-dose azithromycin versus penicillin G benzathine for the treatment of early syphilis. N Engl J Med, 2005, 353, p. 1236-44.
29. Rolfs, RT. Joesoef, MR. Hendershot, EF. A randomized trial of enhanced therapy for early syphilis in patients with and without human immunodeficiency virus infection. The Syphilis and HIV Study Group. N Engl J Med, 1997, 337, p. 307-14.
30. Schofer, H. Imhof, M. Thoma-Greber, E. Active syphilis in HIV infection: a multicentre retrospective survey. The German AIDS Study Group (GASG). Genitourin Med, 1996, 72, p. 176-81.
31. Smith, ME. Canalis, RF. Otologic manifestations of AIDS: the otosyphilis connection. Laryngoscope, 1989, 99, p. 365-72.
32. Smith, NH. Musher, DM. Huang, DB. Response of HIV-infected patients with asymptomatic syphilis to intensive intramuscular therapy with ceftriaxone or procaine penicillin. Int J STD AIDS, 2004, 15, p. 328-32.
33. TAYLOR, M. HAWKINS, K. GONZALEZ, A. Use of the serologic testing algorithm for recent HIV seroconversion (STARHS) to identify recently acquired HIV infections in men with early syphilis in Los Angeles county. J Acquir Immune Defic Syndr, 2005, 38 (5), p. 505-508.
34. Tucker, SC. Yates, VM. Thambar, IV. Unusual skin ulceration in an HIV-positive patient who had cutaneous syphilis and neurosyphilis. Br J Dermatol, 1997, 136, p. 946-8
35. Velčevský, P. Kuklová, I. Léčba sexuálně přenosných onemocnění, Čes-slov Derm, 2008, 83 (3), p. 123-135.
36. STÁTNÍ ZDRAVOTNÍ ÚSTAV ČESKÉ REPUBLIKY NRL pro AIDS HIV/AIDS v ČR 2007. Praha, 2008.
Labels
Dermatology & STDs Paediatric dermatology & STDs
Article was published inCzech-Slovak Dermatology

2009 Issue 5-
All articles in this issue
- Diabetic Foot Syndrome – a Diabetologist’s View
- Significance of Atopic Patch Tests and Other Diagnostic Methods in the Diagnostics of Food Allergy to Cow’s Milk and Wheat Flour in Patients with Atopic Eczema Older Than 14 Years
- Primary Cutaneous Actinomycosis in Two Patients Treated with Clindamycin
- Cutaneons Metastasis as a Primary Manifestation of a Renal Cell Carcinoma
- Syphilis and HIV Coinfection
- Czech-Slovak Dermatology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Syphilis and HIV Coinfection
- Primary Cutaneous Actinomycosis in Two Patients Treated with Clindamycin
- Cutaneons Metastasis as a Primary Manifestation of a Renal Cell Carcinoma
- Diabetic Foot Syndrome – a Diabetologist’s View
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career