-
Medical journals
- Career
Validace české verze dotazníků hodnotících funkční omezení pacientů se systémovou sklerodermií
Authors: S. Heřmánková B.oreská * 1,* 2,3; H. Šmucrová 2; M. Mikulášová 2; M. Špiritović 1,2; H. Štorkánová 2,3; R. Bečvář 2,3; J. Vencovský 2,3; H. Mann 2,3; M. Tomčík 2,3
Authors‘ workplace: autorky přispěly stejnou mírou *; Fakulta tělesné výchovy a sportu, Katedra fyzioterapie, Univerzita Karlova, Praha 1; Revmatologický ústav Praha 2; Revmatologická klinika 1. lékařské fakulty, Univerzita Karlova, Praha 3
Published in: Čes. Revmatol., 28, 2020, No. 4, p. 216-230.
Category: Original article
Overview
Systémová sklerodermie (SSc) jako chronické multisystémové onemocnění je spojeno se závažným funkčním postižením a významným dopadem na kvalitu života pacientů. K hodnocení dopadu tohoto onemocnění na funkční omezení pacientů v běžném životě bylo vyvinuto několik specifických nástrojů, včetně Scleroderma Health Assessment Questionaire (SHAQ), Cochin Hand Functional Scale (CHFS), Mouth Handicap in Systemic Sclerosis (MHISS) a UCLA Scleroderma Clinical Trial Consortium Gastrointestinal Tract 2.0 (UCLA SCTC GIT 2.0).
Cílem této práce bylo vytvoření českých verzí těchto nástrojů a jejich lingvistická validace. Originální verze dotazníků byly přeloženy třemi nezávislými bilingválními revmatology a tyto překlady byly konsenzuálně diskutovány a sjednoceny autorskou skupinou. Poté se šest bilingválních nelékařů vyjádřilo k lingvistické a obsahové stránce dotazníků a jejich připomínky byly expertním panelem zapracovány. Tato verze byla postoupena dvěma nezávislým zaslepeným překladatelům k přeložení zpět do anglického jazyka. Konsenzuálně pak byly vytvořeny prefinální české verze dotazníků, které vyplnilo 55 pacientů se SSc.
K hodnocení srozumitelnosti a výstižnosti jednotlivých otázek dotazníků byl použit dotazník zpětné vazby. Všichni pacienti se SSc označili dotazníky jako zcela jasné a srozumitelné. Výsledkem této práce jsou české verze dotazníků SHAQ, CHFS, MHISS a UCLA SCTC GIT 2.0. Hodnoty dosažených skóre pacientů se SSc se numericky blížily výsledkům jiných publikací. Tyto dotazníky mohou být vhodnými nástroji používanými v klinickém výzkumu i v rutinní klinické praxi.
Klíčová slova:
systémová sklerodermie – Scleroderma Health Assessment Questionaire – Cochin Hand Functional Scale – Mouth Handicap in Systemic Sclerosis – Scleroderma Clinical Trial Consortium Gastrointestinal Tract (UCLA GIT 2.0) – lingvistická validace
ÚVOD
Systémová sklerodermie (SSc) je relativně vzácné chronické zánětlivé onemocnění pojiva s incidencí jeden až 20 případů na milion obyvatel. Ženy bývají postiženy 3–7krát častěji než muži (1). Pro onemocnění jsou charakteristické tři patologické procesy: aktivace imunitního systému, mikrovaskulopatie, fibrotizace kůže a vnitřních orgánů (2). Podle rozsahu postižení kůže se SSc klasifikuje na dva hlavní podtypy: kožně difuzní forma (diffuse cutaneous SSc – dcSSc) spojená s častějším orgánovým postižením a horší prognózou a kožně limitovaná forma (limited cutaneous SSc – lcSSc). Vzácnějšími podtypy lcSSc jsou pak SSc sine scleroderma (ssSSc, tedy SSc bez charakteristické fibrózy kůže) a CREST syndrom (kalcifikace, Raynaudův fenomén, dysmotilita jícnu, sklerodaktylie a teleangiektázie) (3).
SSc má jako chronické multisystémové onemocnění významný dopad na kvalitu života pacientů (4). V důsledku postižení kůže, muskuloskeletálního systému, cévního systému a orgánového postižení jsou pacienti se SSc výrazně omezení v běžném životě a sebeobsluze a mají sníženou celkovou kvalitou života (health related quality of life – HRQoL) v porovnání s běžnou populací (5).
K hodnocení dopadu chronických onemocnění na stav a funkční omezení pacientů v každodenním životě bylo vyvinuto mnoho nástrojů. Mezi ně můžeme zařadit i dotazníky specifické pro pacienty se SSc: Scleroderma Health Assessment Questionaire (SHAQ), Cochin Hand Functional Scale (CHFS), Mouth Handicap in Systemic Sclerosis (MHISS) a UCLA Scleroderma Clinical Trial Consortium Gastrointestinal Tract 2.0 (UCLA SCTC GIT 2.0) (6, 7).
Scleroderma Health Assessment Questionaire (SHAQ)
Kvalita života u pacientů s chronickým onemocněním včetně SSc je důležitým aspektem, jež bereme v úvahu při rozhodování o terapii. Fyzikální nález, ač významný pro ošetřujícího lékaře, nemusí vždy korelovat s kvalitou života, přičemž pro pacienta mají význam obě tyto složky (8). Pro hodnocení kvality života je nutný spolehlivý, validní nástroj, který zároveň odpovídá změnám v průběhu sledování pacienta (9). K tomuto účelu byl v roce 1980 vytvořen a publikován Health Assessment Questionaire – disability index (HAQ-DI), který byl primárně určený pro pacienty s revmatoidní artritidou (RA) a v roce 1991 poprvé použit u pacientů se SSc (10).
HAQ byl později upraven pro pacienty se SSc s ohledem na charakter postižení. K původnímu dotazníku byla přidána standardní vizuální analogová škála (VAS) hodnotící bolest (I) a pět dalších VAS škál (tzv. orgánově specifické škály), které hodnotí: (II) postižení gastrointestinálního traktu (GIT), (III) plicní postižení, (IV) Raynaudův fenomén, (V) digitální ulcerace a (VI) celkovou závažnost onemocnění. Vznikl tak specifický dotazník pro SSc – Scleroderma HAQ (SHAQ), který má přidanou hodnotu v hodnocení vaskulárních a orgánových postižení typických pro tuto chorobu (11, 12). Psychometrické vlastnosti dotazníku SHAQ byly ověřeny v několika studiích, jež prokázaly dostatečnou validitu a reliabilitu. V původní studii byla testovaná test-retest reliabilita u 50 pacientů se SSc, kteří vyplnili SHAQ na začátku studie a po měsíci. Korelační koeficienty obou skóre byly 0,78–0,87 pro VAS hodnotící Raynaudův fenomén, digitální ulcerace a plicní postižení. Méně korelovaly VAS pro bolest a GIT postižení s koeficienty 0,69 a 0,68, což odpovídá větší variabilitě těchto symptomů v rámci 1 měsíce (12). Souběžná validita byla hodnocena porovnáním SHAQ s výsledky dotazníku United Kingdom Scleroderma Functional Score (UKFS). Studie prokázala střední korelaci VAS škál dotazníku SHAQ s UKFS (r = 0,45–0,72) (13). Ukázalo se, že SHAQ je taktéž senzitivní na detekci změn v čase. Pacienti, kteří uváděli zhoršení na vaskulární VAS, vyvinuli digitální ulcerace. Podobně došlo u pacientů, kteří uvedli vyšší hodnoty na škále GIT obtíží, k progresi GIT symptomatologie. U pacientů, u kterých bylo naměřeno snížení vitální kapacity plic o více než 15 %, bylo nalezeno zvýšení na VAS plicního postižení o 1,1 bodu, kdežto při zvýšení vitální plicní kapacity o 15 % se prokazatelně snížilo VAS skóre o 0,62 bodu (11).
Výpočet skóre u SHAQ je z části shodný se systémem výpočtu u HAQ. První část se týká samotného standardního dotazníku HAQ, a proto obsahuje shodně s HAQ celkem 20 otázek rozdělených do osmi oblastí (domén): oblékání, péče o vlasy, vstávání, stravování, chůze, hygiena, rozsah pohybu, úchop a běžné denní aktivity (14). Odpovědi na otázky jsou bodovány 0 (bez problému) až 3 (neschopen provést). Pro každou oblast se počítá průměrné skóre a celkové kompozitní skóre pro HAQ se získá jako součet hodnot získaných v jednotlivých oblastech vydělený počtem zodpovězených oblastí. Výsledná hodnota 0 znamená bez omezení, naopak 3 značí maximální funkční postižení. Ve druhé části se u každé z pěti tzv. orgánových VAS škál (II až VI) určují hodnoty samostatně a navzájem se nesčítají ani nepřičítají k celkovému skóre HAQ. Škály VAS představují úsečky o délce 15 cm s rozsahem 0 až 3 body, u nichž každý 1 cm odpovídá 0,2 bodu. Hodnota 0 značí minimální a hodnota 3 maximální postižení (11). V odborných pracích je však zvykem uvádět i celkové skóre SHAQ jako průměr těchto pěti tzv. orgánových škál (II až VI), a to opět s rozsahem 0 až 3 body. Později bylo navrženo kompozitní skóre nazvané „SSc HAQ skóre“, které představuje vážený průměr osmi domén standardního dotazníku HAQ a pěti tzv. orgánových VAS škál (II až VI) z dotazníku SHAQ. Formule pro výpočet tohoto kompozitního skóre je tedy následující: SSc HAQ skóre = (součet skóre 8 HAQ domén + součet skóre 5 tzv. orgánových VAS škál) děleno 13. Globální skóre nabývá taktéž hodnot od 0 (minimální omezení) do 3 (maximální funkční postižení) (15).
Cochin Hand Functional Scale (CHFS)
Postižení rukou u pacientů se SSc je způsobeno fibrotizací kůže, šlach, artritidou, akroosteolýzou, tvorbou kalcifikací měkkých tkání a vaskulopatií, která se manifestuje digitálními ulceracemi (16, 17). Vzhledem k významu dopadu tohoto postižení na celkový stav a funkci pacientů vyvstala potřeba vytvořit specifický nástroj k hodnocení omezení funkce ruky (18). Mezi prvními dostupnými nástroji byly testy Hand Mobility in Scleroderma index (HAMIS) (19) a Arthritis Hand Functional Test (AHFT) (20). Oba testy jsou založené na klinickém měření funkce ruky a vyžadují relativně hodně času, speciální pomůcky nebo technické vybavení a zkušenosti vyšetřujícího. To komplikuje jejich využití v běžné praxi i v klinických studiích (21). Navíc nehodnotí disabilitu danou omezením funkce rukou v běžném životě (22). S cílem vytvořit spolehlivý nástroj pro vyšetření a monitoraci funkce rukou během terapeutické intervence byl sestaven dotazník Duruöz Hand Index (DHI), jinak zvaný Hand Functional Disability Scale anebo Cochin Scale, neboli Cochin Hand Functional Scale (CHFS) (23). Původně byl určený pro pacienty s RA a osteoartrózou rukou (24, 25), později byl testován také u pacientů se SSc (21).
CHFS sestává z celkem 18 otázek, rozdělených do pěti okruhů, hodnotících funkci rukou při běžných činnostech v kuchyni, oblékání, osobní hygieně, kancelářských úkonech a dalších běžných činnostech. Odpovědi jsou bodované na škále od 0 (bez potíží) do 5 (neschopný provést). Celkové maximální skóre je 90 (21). U pacientů se SSc prokázal CHFS vysokou spolehlivost a zároveň dobrou korelaci s jinými indexy (HAMIS, Keital Functional Test – KFT, AHFT, HAQ) (21). Variabilita skóre CHFS je schopna vysvětlit až 75 % variability skóre HAQ u SSc, což poukazuje na význam postižení rukou a důležitost jeho hodnocení u SSc (18). Vyšší skóre CHFS může souviset se zhoršenou schopností práce, častější nutností invalidního důchodu a se zhoršením socioekonomického statusu (26).
Mouth Handicap in Systemic Sclerosis (MHISS)
Kožní postižení u SSc často zahrnuje obličej a zejména ústa. Důsledkem je nejen omezení funkce úst, ale také estetické následky. Postižení úst se podílí na celkové disabilitě pacientů se SSc z více než jedné třetiny. Omezené otevírání úst ztěžuje udržování ústní hygieny a stomatologické ošetření (27). S výraznějším zmenšením ústní apertury se častěji objevuje sklon ke xerostomii a pacienti udávají závažnější estetické problémy. Suchostí v ústech trpí až 49 % pacientů se SSc, z toho kolem 10 % splňuje kritéria pro Sjögrenův syndrom (28, 29). Svou roli zde může hrát také gastroezofageální reflux a abnormity dásní. Estetické následky postižení u SSc jsou dané zejména vznikem teleangiektázií v obličeji (častěji u lcSSc) a retrakcí kůže obličeje při fibróze (přítomné jak u lcSSc, tak u dcSSc) (27).
Do roku 2007 neexistoval specifický nástroj pro kvantitativní hodnocení postižení obličeje v rámci SSc. Skupina francouzských autorů ve spolupráci s pacienty se SSc vytvořila seznam potíží, které v běžném životě nejvíce omezují pacienty v souvislosti s postižením obličeje a úst u SSc. Na jeho základě vytvořili dotazník Mouth Handicap in Systemic Sclerosis (MHISS) obsahující celkem 12 otázek rozdělených do tří oblastí: omezení otevírání úst, suchost v ústech a estetické problémy. Odpovědi na každou otázku jsou bodované v celých číslech od 0 (bez potíží) do 4 (významné omezení) s rozsahem celkového skóre 0 až 48, přičemž maximální skóre znamená nejhorší stav (27).
MHISS prokázal dobrou validitu a schopnost hodnotit vliv postižení na funkční schopnost pacientů se SSc i mimo rámec dostupných dotazníků (HAQ, CHFS, Hospital Anxiety and Depression Scale, McMaster-Toronto Arthritis questionnaire) a objektivního měření ústní apertury (distance mezi řezáky při maximálním otevření úst). Zároveň dokázal vysvětlit 36,5 % variability celkového skóre dotazníku HAQ (27). Vnitřní konzistence (Cronbachova α = 0,863) a test-retest reliabilita byla hodnocena jako vynikající (r = 0,88) (30). Vyšší skóre MHISS koreluje se zhoršenou pracovní schopností a častější pracovní neschopností zejména v zaměstnáních, které vyžadují sociální kontakt. Důvodem je pravděpodobně estetická otázka a zhoršená schopnost mluvit (26).
University of California, Los Angeles Scleroderma Clinical Trial Consortium Gastrointestinal Tract 2.0 (UCLA SCTC GIT 2.0)
Postižení GIT se vyskytuje až u 90 % pacientů se SSc (31, 32) a patří k hlavním faktorům negativně ovlivňujícím kvalitu života (33, 34). K hodnocení závažnosti a progrese postižení GIT byl v roce 2009 vytvořen dotazník UCLA Scleroderma Clinical Trial Consortium Gastrointestinal Tract 2.0 (UCLA SCTC GIT 2.0), který vznikl úpravou předchozího validovaného dotazníku Scleroderma Gastrointestinal Tract Involvement 1.0 (SSC-GIT 1.0) (35, 36). Původní dotazník SSC-GIT 1.0 byl sice spolehlivý a validní, avšak poměrně rozsáhlý a časově náročný. Účelem revize původního dotazníku bylo jeho zestručnění a zároveň zachování spolehlivosti a upřesnění některých problematických otázek, zejména odlišení symptomů refluxní choroby a nadýmání. Navíc byla přidána škála hodnotící fekální inkontinenci vzhledem k její vysoké prevalenci u pacientů se SSc (37). Cílem bylo vytvořit kompozitní skóre, které by celkově posoudilo zátěž postižením GIT u pacientů se SSc (36).
Dotazník UCLA SCTC GIT 2.0 obsahuje 34 otázek, 33 původních a jednu nově přidanou otázku týkající se úniku stolice (fekální inkontinence). Otázky jsou rozdělené do sedmi okruhů: (I) reflux, (II) nadýmání, (III) inkontinence, (IV) průjem, (V) fungování ve společnosti, (VI) emoční pohoda a (VII) zácpa. Odpovědi na každou otázku jsou bodované od 0 (bez postižení) do 3 (těžké postižení). Souhrnné skóre pro každý ze sedmi okruhů se vypočte jako průměr skóre jednotlivých otázek obsažených v daném okruhu a pro zjednodušení je uvedeno vždy na pravé straně daného okruhu. Celkové skóre celého dotazníku se určí vypočtením průměru bodů z prvních šesti okruhů (I až VI), přičemž body z domény zácpa (VII) se do celkového skóre nezahrnují, ale uvádějí se zvlášť. Celkové skóre tedy dosahuje hodnoty od 0 do 3, přičemž nižší skóre indikuje postižení s menším dopadem na kvalitu života (HRQoL) (36). Nová verze dotazníku se ukázala jako spolehlivá a přesnější oproti SSC-GIT 1.0 při hodnocení postižení GIT u pacientů se SSc (36). Není však známá korelace celkového skóre UCLA SCTC GIT 2.0 s objektivním vyšetřením postižení GIT (38).
Cílem této práce byl překlad a lingvistická validace dotazníků SHAQ, CHFS, MHISS, UCLA SCTC GIT 2.0 a tvorba českých verzí těchto dotazníků pro použití v klinické a výzkumné praxi u pacientů se SSc.
SOUBOR A METODIKA
Překlad a lingvistická validace
Překlad dotazníků a jejich lingvistická validace probíhala v Revmatologickém ústavu v roce 2014. Překlad originálních verzí dotazníků byl proveden nezávisle třemi českými revmatology, kteří splňovali kritérium plynné znalosti mluvené i psané angličtiny (JV, RB, MT). Z překladů (T1, T2, T3) byla konsenzuálně vytvořena syntéza a vznikly první české verze dotazníků (T-123). Verze T-123 byly následně předloženy šesti bilingválním nelékařům, kteří se vyjádřili k lingvistické a obsahové stránce dotazníků a jejich připomínky byly posléze zhodnoceny a zapracovány expertním panelem sestaveným ze zkušených revmatologů (JV, RB, MT, SO) a zdravotníků nelékařů (HŠt, HŠm, MŠ, BH). Tato verze byla postoupena dvěma nezávislým zaslepeným překladatelům (lékař, nelékař) s plynnou znalostí mluvené i psané angličtiny (HM, MM) k přeložení zpět do anglického jazyka. Oba anglické překlady (BT1 a BT2) byly zpětně porovnány s originálními dotazníky a diskutovány expertním panelem, který se vyjádřil k sémantické, lingvistické, koncepční a terminologické stránce dotazníků. Konsenzuálně byly vytvořeny prefinální české verze dotazníků (39).
Testování dotazníků
Do validační studie bylo zařazeno celkem 55 pacientů se SSc z ambulantního nebo lůžkového oddělení Revmatologického ústavu v Praze. Všichni pacienti se SSc splnili klasifikační kritéria ACR/EULAR 2013 (40). Demografická a klinická charakteristika skupiny je uvedena v tabulce 1. V rámci testování dotazníků byli pacienti požádáni o vyplnění demografických údajů, prefinální verze dotazníků SHAQ, CHFS, MHISS, UCLA SCTC GIT 2.0 a dotazníku zpětné vazby.
Table 1. Demografická a klinická charakteristika testované skupiny pacientů se systémovou sklerodermií 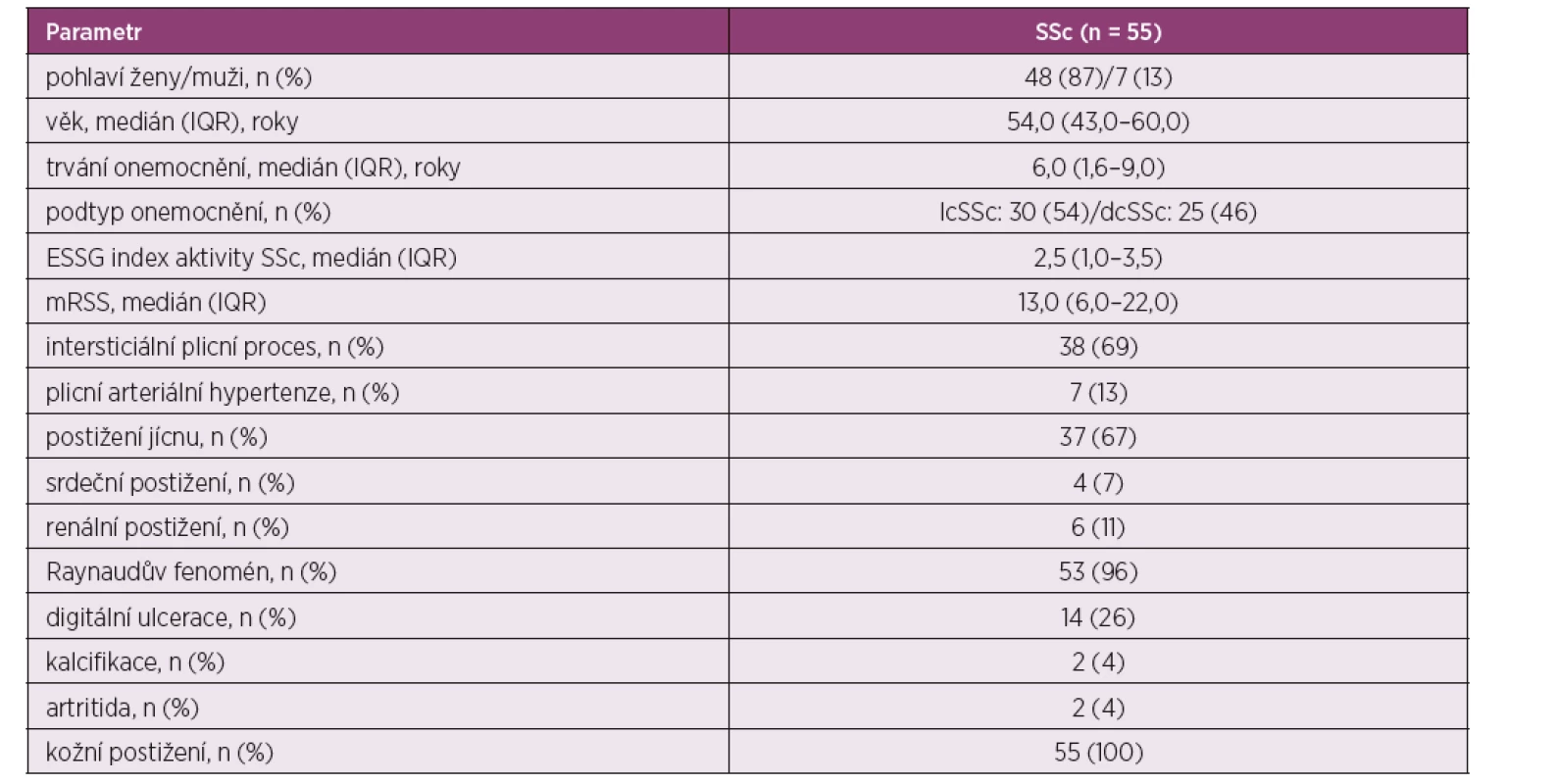
SSc – systémová sklerodermie, lcSSc – kožně limitovaná forma SSc, dcSSc – kožně difuzní forma SSc, IQR – mezikvartilové rozpětí, ESSG – European Scleroderma Study Group, mRSS – modifikované Rodnanovo kožní skóre Dotazník zpětné vazby jsme vytvořili na základě mezinárodních doporučení (39) k hodnocení srozumitelnosti a jednoznačnosti jednotlivých otázek v dotaznících SHAQ, CHFS, MHISS, UCLA SCTC GIT 2.0. V něm jsme požádali respondenty, aby po vyplnění výše zmíněných dotazníků uvedli, jestli informace v nich uvedené byly srozumitelné a jednoznačné, a pokud ne, aby vypsali konkrétní otázku nebo bod a vysvětlili, v čem vidí problém. Připomínky pacientů byly expertním panelem zohledněny v tvorbě definitivních českých verzí dotazníků.
VÝSLEDKY
Výsledkem této validační studie jsou české verze dotazníků SHAQ, CHFS, MHISS a UCLA SCTC GIT 2.0, které jsou součástí příloh 1 až 4. Celkem dotazníky vyplnilo 55 pacientů se SSc. Dosažená skóre všech dotazníků pro obě skupiny jsou uvedena v tabulce 2.
Table 2. Výsledky hodnocení dopadu systémové sklerodermie na funkční omezení v běžném životě pomocí dotazníků SHAQ, MHISS, CHFS a UCLA SCTC GIT 2.0. Data jsou prezentována jako průměrné hodnoty ± směrodatná odchylka. 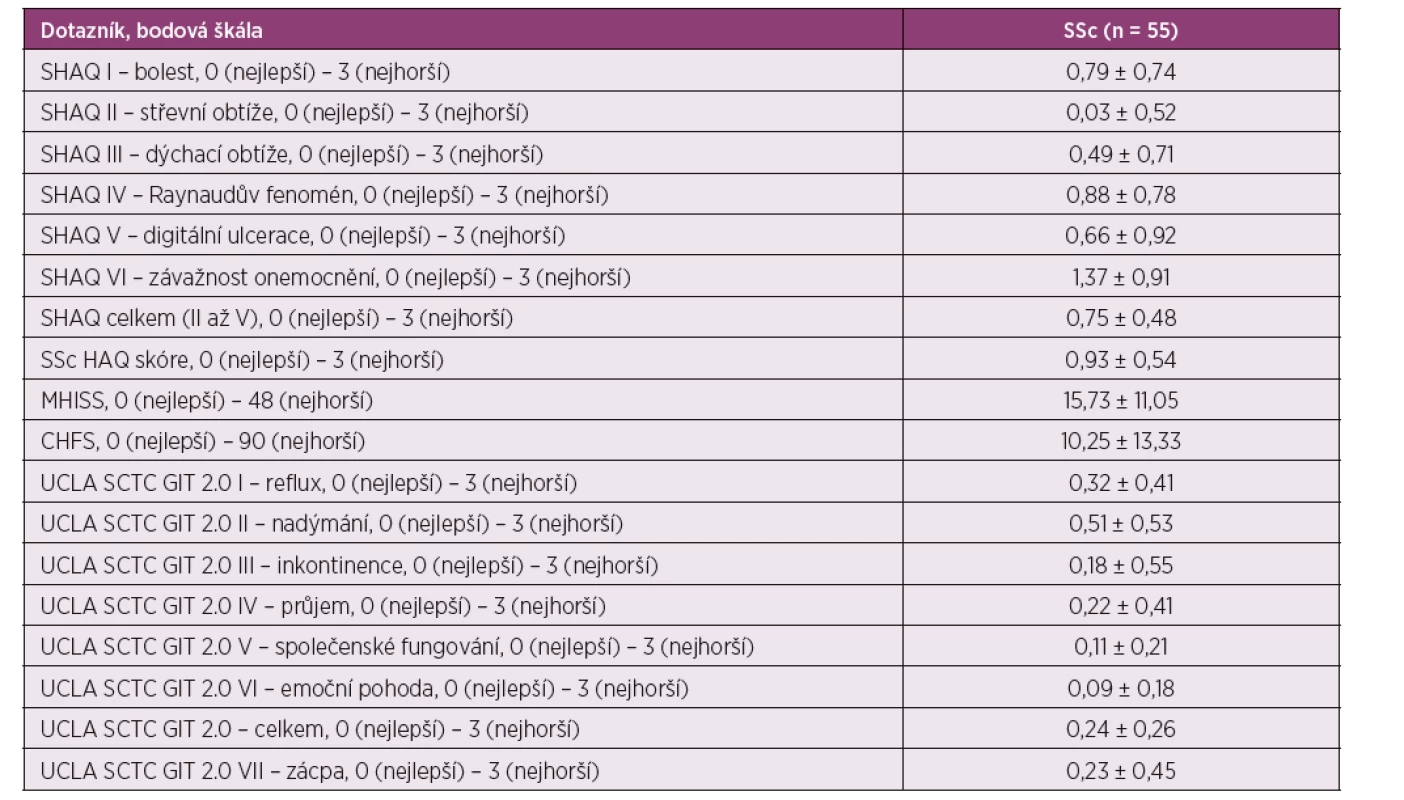
SSc – systémová sklerodermie, SHAQ – Scleroderma Health Assessment Questionaire, MHISS – Mouth Handicap in Systemic Sclerosis, CHFS – Cochin Hand Functional Scale, UCLA SCTC GIT 2.0 – University of California, Los Angeles Scleroderma Clinical Trial Consortium Gastrointestinal Tract 2.0 Během překladu narazili autoři na kulturní odlišnost, kterou bylo třeba adaptovat pro české podmínky. V dotazníku CHFS v otázce č. 15, která v originální verzi zní: „Can you turn a round door knob?“ bylo třeba upravit znění otázky: „Dokážete zmáčknout kliku u dveří?“, protože systém klik a otevírání dveří se v českých a anglosaských podmínkách liší. Tato úprava však znamená, že otázka v českém dotazníku hodnotí odlišný typ úchopu. Při otevírání dveří kulovou klikou zpravidla využíváme úchop kulový a pohyb předloktí do supinace, kdežto v případě klasické kliky mluvíme o úchopu válcovém s pozicí předloktí v pronaci (41). Při zhodnocení funkční schopnosti ruky bychom si měli být této odlišnosti vědomi. Při překladu dotazníků SHAQ, MHISS a UCLA SCTC GIT 2.0 se překladatelé s kulturními nesrovnalostmi nesetkali.
Při zaslepeném zpětném překladu českých verzí do angličtiny nebyla nalezena žádná obsahová změna ve srovnání s anglickým originálem, vyjma výše zmíněných předem konsenzuálně odsouhlasených úprav v rámci kulturních odlišností. K hodnocení srozumitelnosti a výstižnosti jednotlivých otázek jsme použili dotazník zpětné vazby. Všichni pacienti se SSc označili dotazníky jako zcela jasné a srozumitelné.
DISKUZE
Cílem této práce byl překlad a lingvistická validace dotazníků SHAQ, CHFS, MHISS, UCLA SCTC GIT 2.0 a tvorba českých verzí těchto dotazníků. Dotazníky založené na výsledcích hodnocených pacientem včetně měření kvality života související se zdravím se v posledních letech jeví jako důležité výstupy měření. Kromě hodnocení HRQoL mohou být tyto nástroje použity v klinických studiích k hodnocení účinnosti léčby, k analýze individuálních potřeb pacienta a k pomoci lékařům při rozhodování o volbě terapie. Dosavadní evidence poskytuje spolehlivé důkazy o tom, že u pacientů se SSc je HRQoL značně narušena a potřeba jejího hodnocení v rámci klinického výzkumu i rutinní klinické praxe je vysoká (42). Za účelem zkvalitnění hodnocení HRQoL u pacientů se SSc jsme přeložili a vytvořili české verze anglických dotazníků SHAQ, CHFS, MHISS a UCLA SCTC GIT 2.0.
České překlady byly validovány na kohortě 55 pacientů se SSc. Srovnáme-li průměrná skóre naší kohorty s výsledky předchozích studií, dostáváme v jednotlivých škálách numericky podobné hodnoty. V práci Meijs et al. (2014), jejímž cílem bylo zhodnotit validitu dotazníku UCLA SCTC GIT 2.0 u 89 pacientů se SSc, bylo průměrné celkové skóre 0,31 ± 0,39 (43). V jiné studii dosahovali pacienti se SSc (n = 220) průměrných celkových skóre 0,29 ± 0,37 (44). Podrobnější srovnání výsledků v celkových i dílčích skóre tohoto nástroje s jinými studiemi (43–45) je uvedeno v tabulce 3. V dotazníku MHISS se dvě studie shodly na hodnotě celkového skóre 17 bodů, konkrétně (průměr ± směrodatná odchylka) 17,7 ± 5,2 (46) a 17,5 ± 10,0 (47). Skupina pacientů v naší práci dosáhla průměrného celkového skóre 15,7 ± 11,1. Ačkoliv jsou uvedené hodnoty téměř numericky shodné, vliv na průměrné hodnoty skóre tohoto nástroje může mít poměr pacientů s kožně limitovanou a difuzní formou SSc v testovaném vzorku, protože pacienti s dcSSc dosahují signifikantně horších výsledků ve srovnání s pacienty s lcSSc (46). Obdobně je tomu tak i u hodnocení funkce rukou pomocí dotazníku CHFS, kde rovněž skupina pacientů s dcSSc uvedla signifikantně závažnější postižení rukou oproti skupině s lcSSc (18). Ve studii Rannou et al. (2007) dosahovaly hodnoty pacientů se SSc (n = 50) v dotazníku CHFS 16,6 ± 16,4 (18), v jiné studii byly publikovány hodnoty u 60 pacientů se SSc 18,2 ± 13,5 (48) a v naší práci 10,3 ± 13,3. U dotazníku SHAQ byly publikovány hodnoty SSc HAQ skóre 0,72 ± 0,53 pro dcSSc a 0,90 ± 0,64 pro lcSSc (49), zatímco v naší studii dosáhla celá kohorta průměrného skóre 0,93 ± 0,54.
Table 3. Srovnání výsledků naší kohorty v dotazníku UCLA SCTC GIT 2.0. u pacientů se systémovou sklerodermií s výsledky jiných studií. Data jsou prezentována jako průměrné hodnoty ± směrodatná odchylka. 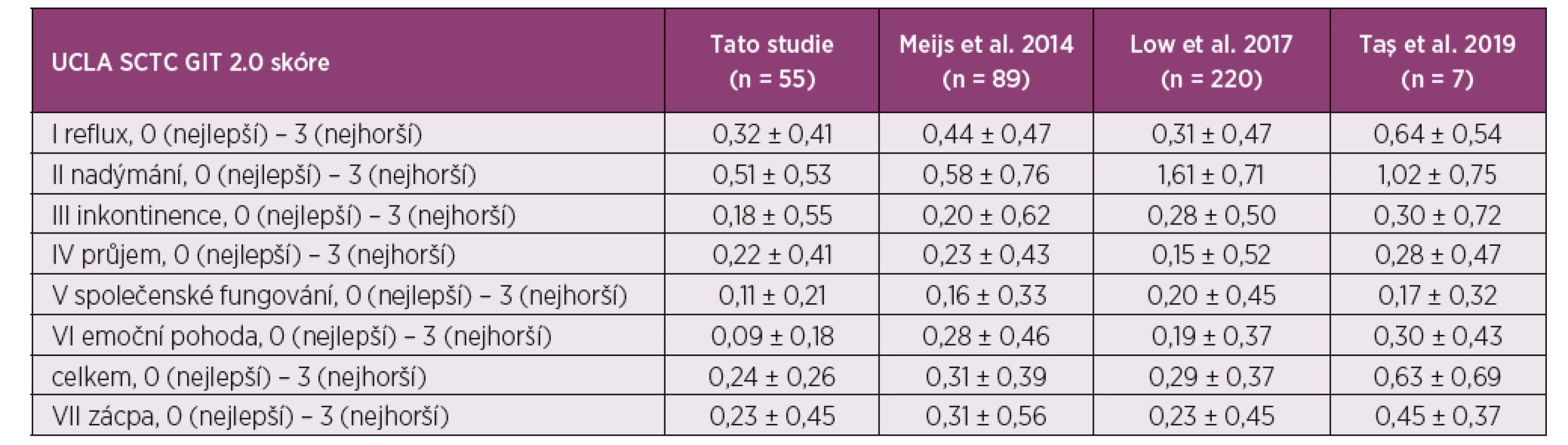
UCLA SCTC GIT 2.0 – University of California, Los Angeles Scleroderma Clinical Trial Consortium Gastrointestinal Tract 2.0 Obecnou limitací dotazníkových šetření může být absence jednoduchého souhrnného skóre. Na tento nedostatek narážel i dotazník SHAQ, ve kterém se původně uvádělo skóre pro každou VAS samostatně (11). Srovnání výsledků mezi pacienty či různými kohortami tak vyžadovalo srovnání každé stupnice individuálně. Jak již bylo zmíněno, francouzští autoři navrhli výpočet kompozitního „SSc HAQ skóre“, které je kombinací výsledků osmi domén standardního dotazníku HAQ a pěti tzv. orgánových VAS škál dotazníku SHAQ (15). Zdá se, že použití tohoto kompozitního skóre bylo akceptováno a rozšířeno, čímž se zjednodušila interpretace a porovnatelnost dotazníku SHAQ. Ostatní dotazníky (CHFS, MHISS a UCLA SCTC GIT 2.0) však souhrnná skóre nabízejí již od samotného vytvoření.
ZÁVĚR
Použití dotazníků založených na výsledcích hodnocených pacientem představuje jednoduchý a finančně nenáročný způsob jak zhodnotit rozsah a závažnost funkčního postižení u pacientů se SSc a reflektovat jejich prognózu. Dotazníky vybrané pro validační proces v této studii jsou specifické pro diagnózu SSc a jejich psychometrické vlastnosti byly na této populaci v předešlých studiích ověřeny. Pevně věříme, že výsledné české překlady anglických originálů těchto dotazníků budou využívány jako užitečné nástroje klinického výzkumu i v rutinní klinické praxi. Předmětem budoucího výzkumu by mělo být zhodnocení validity, reliability a senzitivity českých verzí dotazníků na četnější populaci pacientů se SSc.
Práce vznikla za podpory grantů AZV 16-33542A, 16-33574A, 16-33746A, NV18-01-00161A, GA UK 1578119, 312218, SVV 260373 a institucionální podpory Ministerstva zdravotnictví ČR pro Revmatologický ústav č. 023728.
Konflikt zájmů: žádný
adresa pro korespondenci:
doc. MUDr. Michal Tomčík, Ph.D.
Revmatologický ústav
Na Slupi 4, 128 00 Praha 2
e-mail: tomcik@revma.cz
Příloha 1 Dotazník Scleroderma Health Assessment Questionnaire
Příloha 2 Dotazník Cochin Hand Function Scale
Příloha 3 Dotazník Mouth Handicap in Systemic Sclerosis
Příloha 4 Dotazník UCLA Scleroderma Clinical Trial Consortium Gastrointestinal Tract 2.0
Sources
1. Firestein GS, Budd RC, Gabriel SE, McInnes IB, O’Dell JR. Kelley’s Textbook of Rheumatology E-Book: Elsevier Health Sciences 2012.
2. Allcock RJ, Forrest I, Corris PA, Crook PR, Griffiths ID. A study of the prevalence of systemic sclerosis in northeast England. Rheumatology (Oxford) 2004; 43(5): 596–602.
3. Brady SM, Shapiro L, Mousa SA. Current and future direction in the management of scleroderma. Arch Dermatol Res 2016; 308(7): 461–471.
4. Khanna D, Furst DE, Clements PJ, Park GS, Hays RD, Yoon J, et al. Responsiveness of the SF-36 and the Health Assessment Questionnaire Disability Index in a systemic sclerosis clinical trial. J Rheumatol 2005; 32(5): 832–840.
5. Hudson M, Thombs BD, Steele R, Panopalis P, Newton E, Baron M, et al. Quality of life in patients with systemic sclerosis compared to the general population and patients with other chronic conditions. J Rheumatol 2009; 36(4): 768–772.
6. Mouthon L, Rannou F, Berezne A, Pagnoux C, Guilpain P, Goldwasser F, et al. Patient preference disability questionnaire in systemic sclerosis: a cross-sectional survey. Arthritis Rheum 2008; 59(7): 968–973.
7. Pope J. Measures of systemic sclerosis (scleroderma): Health Assessment Questionnaire (HAQ) and Scleroderma HAQ (SHAQ), physician - and patient-rated global assessments, Symptom Burden Index (SBI), University of California, Los Angeles, Scleroderma Clinical Trials Consortium Gastrointestinal Scale (UCLA SCTC GIT) 2.0, Baseline Dyspnea Index (BDI) and Transition Dyspnea Index (TDI) (Mahler’s Index), Cambridge Pulmonary Hypertension Outcome Review (CAMPHOR), and Raynaud’s Condition Score (RCS). Arthritis Care Res (Hoboken) 2011; 63(Suppl 11): S98–111.
8. Guyatt GH, Feeny DH, Patrick DL. Measuring health-related quality of life. Ann Intern Med 1993; 118(8): 622–629.
9. Hays RD, Hadorn D. Responsiveness to change: an aspect of validity, not a separate dimension. Qual Life Res 1992; 1(1): 73–75.
10. Poole JL, Steen VD. The use of the Health Assessment Questionnaire (HAQ) to determine physical disability in systemic sclerosis. Arthritis Care Res 1991; 4(1): 27–31.
11. Johnson SR, Hawker GA, Davis AM. The health assessment questionnaire disability index and scleroderma health assessment questionnaire in scleroderma trials: an evaluation of their measurement properties. Arthritis Rheum 2005; 53(2): 256–262.
12. Steen VD, Medsger TA, Jr. The value of the Health Assessment Questionnaire and special patient-generated scales to demonstrate change in systemic sclerosis patients over time. Arthritis Rheum 1997; 40(11): 1984–1991.
13. Smyth A, MacGregor A, Mukerjee D, Brough G, Black C, Denton C. A cross-sectional comparison of three self-reported functional indices in scleroderma. Rheumatology 2003; 42(6): 732–738.
14. Bruce B, Fries JF. The Stanford Health Assessment Questionnaire: dimensions and practical applications. Health Qual Life Outcomes 2003; 1 : 20.
15. Georges C, Chassany O, Mouthon L, Tiev K, Toledano C, Meyer O, et al. Validation of French version of the Scleroderma Health Assessment Questionnaire (SSc HAQ). Clin Rheumatol 2005; 24(1): 3–10.
16. Entin MA, Wilkinson RD. Scleroderma hand: a reappraisal. Orthop Clin North Am 1973; 4(4): 1031–1038.
17. Palmer DG, Hale GM, Grennan DM, Pollock M. Bowed fingers. A helpful sign in the early diagnosis of systemic sclerosis. J Rheumatol 1981; 8(2): 266–272.
18. Rannou F, Poiraudeau S, Berezne A, Baubet T, Le-Guern V, Cabane J, et al. Assessing disability and quality of life in systemic sclerosis: construct validities of the Cochin Hand Function Scale, Health Assessment Questionnaire (HAQ), Systemic Sclerosis HAQ, and Medical Outcomes Study 36-Item Short Form Health Survey. Arthritis Rheum 2007; 57(1): 94–102.
19. Sandqvist G, Eklund M. Hand Mobility in Scleroderma (HAMIS) test: the reliability of a novel hand function test. Arthritis Care Res 2000; 13(6): 369–374.
20. Poole JL, Gallegos M, O’Linc S. Reliability and validity of the Arthritis Hand Function Test in adults with systemic sclerosis (scleroderma). Arthritis Care Res 2000; 13(2): 69–73.
21. Brower LM, Poole JL. Reliability and validity of the Duruoz Hand Index in persons with systemic sclerosis (scleroderma). Arthritis Rheum 2004; 51(5): 805–809.
22. Sandqvist G, Eklund M. Validity of HAMIS: a test of hand mobility in scleroderma. Arthritis Care Res 2000; 13(6): 382–387.
23. Duruoz MT, Poiraudeau S, Fermanian J, Menkes CJ, Amor B, Dougados M, et al. Development and validation of a rheumatoid hand functional disability scale that assesses functional handicap. J Rheumatol 1996; 23(7): 1167–1172.
24. Poiraudeau S, Lefevre-Colau MM, Fermanian J, Revel M. The ability of the Cochin rheumatoid arthritis hand functional scale to detect change during the course of disease. Arthritis Care Res 2000; 13(5): 296–303.
25. Poiraudeau S, Chevalier X, Conrozier T, Flippo RM, Liote F, Noel E, et al. Reliability, validity, and sensitivity to change of the Cochin hand functional disability scale in hand osteoarthritis. Osteoarthritis Cartilage 2001; 9(6): 570–577.
26. Nguyen C, Poiraudeau S, Mestre-Stanislas C, Rannou F, Berezne A, Papelard A, et al. Employment status and socio-economic burden in systemic sclerosis: a cross-sectional survey. Rheumatology (Oxford) 2010; 49(5): 982–989.
27. Mouthon L, Rannou F, Berezne A, Pagnoux C, Arene JP, Fois E, et al. Development and validation of a scale for mouth handicap in systemic sclerosis: the Mouth Handicap in Systemic Sclerosis scale. Ann Rheum Dis 2007; 66(12): 1651–1655.
28. Avouac J, Sordet C, Depinay C, Ardizonne M, Vacher-Lavenu MC, Sibilia J, et al. Systemic sclerosis-associated Sjogren’s syndrome and relationship to the limited cutaneous subtype: results of a prospective study of sicca syndrome in 133 consecutive patients. Arthritis Rheum 2006; 54(7): 2243–2249.
29. Salliot C, Mouthon L, Ardizzone M, Sibilia J, Guillevin L, Gottenberg JE, et al. Sjögren’s syndrome is associated with and not secondary to systemic sclerosis. Rheumatology (Oxford) 2007; 46(2): 321–326.
30. Tore NG, Sarì F, Tunà Z, Kucuk H, Haznedaroglu S, Oskay D. Translation, validation and cross-cultural adaptation of the mouth handicap in systemic sclerosis questionnaire into the Turkish language. Int J Rheum Dis 2020; 23(5): 669–673.
31. Sjögren RW. Gastrointestinal motility disorders in scleroderma. Arthritis Rheum 1994; 37(9): 1265–1282.
32. Lock G, Holstege A, Lang B, Scholmerich J. Gastrointestinal manifestations of progressive systemic sclerosis. Am J Gastroenterol 1997; 92(5): 763–771.
33. Nietert PJ, Mitchell HC, Bolster MB, Curran MY, Tilley BC, Silver RM. Correlates of depression, including overall and gastrointestinal functional status, among patients with systemic sclerosis. J Rheumatol 2005; 32(1): 51–57.
34. Gliddon AE, Dore CJ, Maddison PJ, Quins Trial Study G. Influence of clinical features on the health status of patients with limited cutaneous systemic sclerosis. Arthritis Rheum 2006; 55(3): 473–479.
35. Khanna D, Hays RD, Park GS, Braun-Moscovici Y, Mayes MD, McNearney TA, et al. Development of a preliminary scleroderma gastrointestinal tract 1.0 quality of life instrument. Arthritis Rheum 2007; 57(7): 1280–1286.
36. Khanna D, Hays RD, Maranian P, Seibold JR, Impens A, Mayes MD, et al. Reliability and validity of the University of California, Los Angeles Scleroderma Clinical Trial Consortium Gastrointestinal Tract Instrument. Arthritis Rheum 2009; 61(9): 1257–1263.
37. Trezza M, Krogh K, Egekvist H, Bjerring P, Laurberg S. Bowel problems in patients with systemic sclerosis. Scand J Gastroenterol 1999; 34(4): 409–413.
38. Tay T, Ferdowsi N, Baron M, Stevens W, Hudson M, Proudman SM, et al. Measures of disease status in systemic sclerosis: A systematic review. Semin Arthritis Rheum 2017; 46(4): 473–487.
39. Beaton DE, Bombardier C, Guillemin F, Ferraz MB. Guidelines for the process of cross-cultural adaptation of self-report measures. Spine 2000; 25(24): 3186–3191.
40. van Den Hoogen F, Khanna D, Fransen J, Johnson SR, Baron M, Tyndall A, et al. 2013 classification criteria for systemic sclerosis: an American College of Rheumatology/European League against Rheumatism collaborative initiative. Arthritis Rheum 2013; 65(11): 2737–2747.
41. Klusoňová E. Ergoterapie v praxi: Národní centrum ošetřovatelství a nelékařských zdravotnických oborů 2011.
42. Danieli E, Airo P, Bettoni L, Cinquini M, Antonioli CM, Cavazzana I, et al. Health-related quality of life measured by the Short Form 36 (SF-36) in systemic sclerosis: correlations with indexes of disease activity and severity, disability, and depressive symptoms. Clin Rheumatol 2005; 24(1): 48–54.
43. Meijs J, Pors D, Vliet Vlieland T, Huizinga T, Schouffoer A. Translation, cross-cultural adaptation, and validation of the UCLA Scleroderma Clinical Trial Consortium Gastrointestinal Tract Instrument (SCTC GIT) 2.0 into Dutch. Clin Exp Rheumatol 2014; 32(6 Suppl 86): S41–48.
44. Low AHL, Xin X, Law WG, Teng GG, Santosa A, Lim A, et al. Validation of the UCLA Scleroderma Clinical Trial Consortium Gastrointestinal Tract Instrument 2.0 in English-and Chinese-speaking patients in a multi-ethnic Singapore systemic sclerosis cohort. Clin Rheumatol 2017; 36(7): 1643–1648.
45. Taş YM, Hakim GD, Keskinoğlu P, Kenar G, Yarkan H, Zengin B, et al. The validity and reliability study of the University of California, Los Angeles Scleroderma Clinical Trial Consortium Gastrointestinal Tract (UCLA SCTC GIT) 2.0 questionnaire for the Turkish society. Turk J Gastroenterol 2019; 30(3): 234.
46. Maddali Bongi S, Del Rosso A, Miniati I, Galluccio F, Landi G, Tai G, et al. The Italian version of the Mouth Handicap in Systemic Sclerosis scale (MHISS) is valid, reliable and useful in assessing oral health-related quality of life (OHRQoL) in systemic sclerosis (SSc) patients. Rheumatol Int 2012; 32(9): 2785–2790.
47. Schouffoer AA, Strijbos E, Schuerwegh AJ, Mouthon L, Vliet Vlieland TP. Translation, cross-cultural adaptation, and validation of the Mouth Handicap in Systemic Sclerosis questionnaire (MHISS) into the Dutch language. Clin Rheumatol 2013; 32(11): 1649–1655.
48. Chiari A, Sardim CCdS, Natour J. Translation, cultural adaptation and reproducibility of the Cochin Hand Functional Scale questionnaire for Brazil. Clinics 2011; 66(5): 731–736.
49. Karadag DT, Karakas F, Tekeoglu S, Yazici A, Isik OO, Cefle A. Validation of Turkish version of the Scleroderma Health Assessment Questionnaire. Clin Rheumatol 2019; 38(7): 1917–1923.
Labels
Dermatology & STDs Paediatric rheumatology Rheumatology
Article was published inCzech Rheumatology

2020 Issue 4-
All articles in this issue
-
Něco staré končí,
něco nové začíná…. - The opinion of the Czech Society of Rheumatology on the treatment of rheumatic diseases and vaccination in the context of SARS-CoV-2 infection
- Clinical experience in the long-term treatment of axial spondyloarthritis with secukinumab
- Validation of Czech versions of questionnaires assessing functional impairment in patients with systemic sclerosis: Scleroderma Health Assessment Questionnaire (SHAQ), Cochin Hand Functional Scale (CHFS), Mouth Handicap in Systemic Sclerosis (MHISS), UCLA Scleroderma Clinical Trial Consortium Gastrointestinal Tract 2.0 (UCLA SCTC GIT 2.0)
-
Low-dose computed tomography with tin filtration for the diagnosis of sacroiliitis –
our first experience - Cardiotoxicity of cyclophosphamide in the treatment of microscopic polyangiitis – case report
- L. Pitfalls of diagnosis of ANCA-associated vasculitis – case report
-
Něco staré končí,
- Czech Rheumatology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- L. Pitfalls of diagnosis of ANCA-associated vasculitis – case report
- Validation of Czech versions of questionnaires assessing functional impairment in patients with systemic sclerosis: Scleroderma Health Assessment Questionnaire (SHAQ), Cochin Hand Functional Scale (CHFS), Mouth Handicap in Systemic Sclerosis (MHISS), UCLA Scleroderma Clinical Trial Consortium Gastrointestinal Tract 2.0 (UCLA SCTC GIT 2.0)
- The opinion of the Czech Society of Rheumatology on the treatment of rheumatic diseases and vaccination in the context of SARS-CoV-2 infection
- Clinical experience in the long-term treatment of axial spondyloarthritis with secukinumab
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career







