-
Medical journals
- Career
Embolie plodovou vodou – přehledový článek
: A. Černý; A. Pařízek; Patrik Šimják
: Gynekologicko-porodnická klinika 1. LF UK a VFN, Praha, přednosta prof. MUDr. A. Martan, DrSc.
: Ceska Gynekol 2014; 79(4): 255-259
Embolie plodovou vodou je sice vzácná, ale smrtelná komplikace v těhotenství. Příznaky můžou být od lehkých až po náhlou srdeční zástavu až smrt. Embolie plodovou vodou patří v rozvinutém světě mezi nejčastější příčiny mateřské úmrtnosti. Základem je průnik plodové vody nebo částic v ní rozpuštěných do krevního oběhu matky. Předpokládá se, že tady částice působí zejména na mechanismu imunitní reakce. Výsledkem plně rozvinutého syndromu je široké spektrum klinických projevů, ze kterých vynikají zejména komplikace kardiovaskulární, respirační a hematologické. Léčba těchto stavů vyžaduje akutní mezioborovou spolupráci. Mortalita na tuto těhotenskou patologii v posledních letech klesá. Stává se tak v důsledku zvyšování kvality intenzivní péče a zařazováním lehkých případů do registrů perinatologických patologií.
Klíčová slova:
embolie plodovou vodou, anafylaktický šok, sepseÚVOD
Embolie plodovou vodou (dále AFE – amniotic fluid embolism) je vzácná těhotenská komplikace s častými smrtelnými následky. Proti AFE neexistuje žádný způsob prevence a její výskyt nemůžeme obvykle nijak předvídat. Proto AFE patří mezi nejzávažnější a nejčastější příčiny morbidity a mortality v perinatologii ve vyspělých zemích [1, 6].
PATOFYZIOLOGIE, PATOGENEZE
Základním předpokladem vzniku AFE je průnik plodové vody anebo částic z ní do krevního oběhu matky. Částice můžou být tuhé – lanugo, epitelie, mázek, hlen, anebo solubilní – prostaglandiny, aktivátory komplementu, imunologické faktory. Děje se tak nejčastěji skrz mikroskopické lacerace dolního děložního segmentu, otevřenou ránou ve venózních pleteních v okolí dělohy nebo přes oblast placentární inzerce. Předpokladem je tlakový gradient podporující přechod plodové vody do oběhu. Příznaky se objevují až s určitým odstupem po přechodu plodové vody do oběhu [8].
Přesný mechanismus AFE není známý. Předpokládá se, že v oběhu způsobuje plodová voda:
- mechanickou obstrukci cév (embolizaci),
- zánětlivou odpověď organismu,
- imunologickou reakci organismu (aktivace komplementu a koagulační kaskády).
Z klinického hlediska plně rozvinutý AFE spíše připomíná prudkou alergickou reakci, anafylaxi nebo sepsi než embolickou příhodu. Nerozvíjejí se ale kožní příznaky ani se nezvyšuje tělesná teplota. Proto se v současnosti označuje spíše jako „anafylaktoidní těhotenský syndrom“ [2].
Příznaky AFE obvykle nastupují v peripartálním období, nejdéle do 2 až 4 hodin od přechodu plodové vody do oběhu resp. porodu plodu [8].
AFE má dvě fáze.
Akutní fáze – prvních asi 30 minut po přestupu agens do oběhu matky. Plodová voda s částicemi způsobí plicní vazokonstrikci. Některé práce přisuzují reakci přítomnosti endotelinu [8]. Na ni nasedá plicní hypertenze se srdečním selháváním, systémová hypotenze a hypoxémie matky. Akutní hypoxémie může vyústit až v infarkt myokardu. Přítomnost solubilních částic v plodové vodě způsobí prostupnost cévních kapilár, a tedy vznik nekardiálního plicního edému s bronchospazmem. V tomto stadiu umírá většina postižených.
Pozdní fáze – rozvíjí se levostranné srdeční selhání na základě ischemie myokardu [8], vzniká kardiogenní šok. Následná vazodilatace způsobí prohloubení závažné hypotenze. Primární plicní postižení se často rozvíjí do ARDS [14].
V plodové vodě jsou přítomny kromě jiných také srážecí faktory II, VII a X a tkáňový faktor, které můžou spustit koagulační kaskádu s intravaskulární konzumpcí koagulačních faktorů. Koagulopatie může vyústit v plně rozvinutý časný DIC a život ohrožující krvácení s následným hemoragickým šokem [8].
Z důvodu hypoxie u matky a plodu může dojít ke vzniku neurologických dysfunkcí. Ty jsou jedny z nejčastějších dlouhotrvajících následků AFE.
Plodová voda a látky v ní rozpuštěné jsou běžně v oběhu i u fyziologických těhotných a rodiček. Proč se u nich AFE nerozvíjí, není známo. Některé práce uvádějí, že se příznaky syndromu AFE nerozvinuly ani u pokusných zvířat, kterým bylo aplikováno větší množství plodové vody nitrožilně [2].
INCIDENCE
Neexistuje přesný údaj o incidenci AFE. Nejpřesnější údaje jsou z národních registrů AFE (viz kapitolu Záchyt). Plně klinicky vyjádřená AFE se odhadem objevuje v 1 : 8000 až 1 : 80 000 těhotenství [2].
Velký rozptyl je dán širokým spektrem symptomů a nejednoznačnou diagnostikou u žen, které přežijí.
Incidence se liší podle zvolené metody sběru dat. U prospektivních studií je popsán výskyt AFE 1,9 až 6,1 na 100 000 těhotných, u retrospektivních 5,5 až 6,1 na 100 000 těhotných [7].
Ve Spojeném království je incidence 1,9/100 000 porodů, v Nizozemsku 2,5/100 000 porodů, v USA 5,5/100 000 porodů, v Kanadě 6,0/100 000 porodů, v Austrálii průměrně 6,1/100 000 porodů [7].
MORTALITA A MORBIDITA
Mateřská mortalita kolísá mezi hodnotami 0,5 až 1,7 úmrtí na 100 000 porodů ve vyspělých zemích (0,5 ve Švédsku a ve Spojeném království, 0,7 v Kanadě, 1,5 v Austrálii a 1,0–1,7 v USA). V rozvojových zemích je mateřská úmrtnost mezi 1,8 až 5,9 na 100 000 porodů [9].
Ve Velké Británii jde o pátou nejčastější příčinu úmrtí těhotných. Ve Francii 13 % těhotných umírá na AFE, je to třetí nejčastější příčina úmrtí těhotných žen. V Singapuru AFE způsobuje až 30% mortalitu, zároveň je to nejčastější příčina úmrtí těhotných žen [11].
V porovnání se staršími studiemi mateřská mortalita v dnešní době klesá – je to výsledek pokroku v léčbě a přesnější diagnostiky stavů připomínajících AFE [9].
PREDIKCE A RIZIKOVÉ FAKTORY
Přesná predikce výskytu AFE není dosud možná. Na základě hodnocení registrů perinatologických patologií (Austrálie, Kanada, Nizozemsko, UK, USA) byly zjištěny některé faktory zvyšující relativní riziko (RR) vzniku AFE [7]. Rozdíly v hodnotách jsou způsobeny rozdílnou metodikou sbírání dat do „registrů“ (viz kapitolu Záchyt).
Faktory způsobující zvýšení RR pro vznik AFE můžeme rozdělit do 4 skupin:
- Anamnestické faktory.
- Těhotenské faktory.
- Indukce porodu.
- Porodní faktory (poznámka – menší plod, např. IUGR nebo předčasný porod, vykazuje relativní riziko nižší [13]).
Podrobnější rozdělení včetně některých hodnot relativního rizika obsahuje tabulka 1.
1. Přehled rizikových faktorů a relativních rizik pro vznik AFE 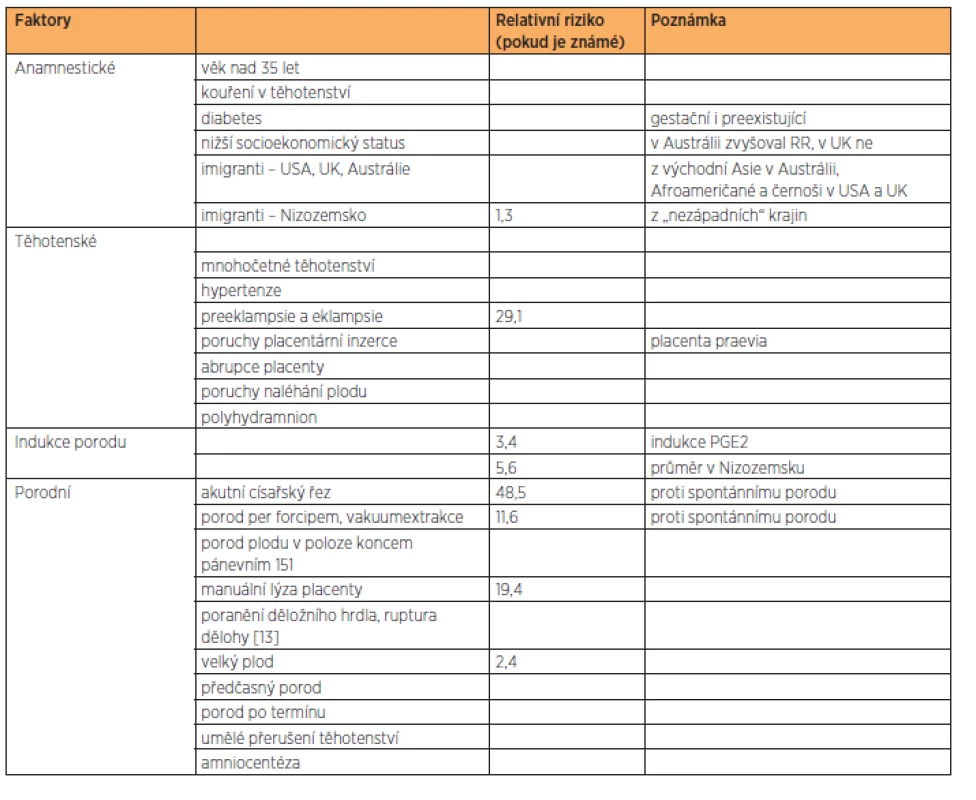
Je popsán i vznik AFE po extrakci cerclage stehu nebo po skrytém abdominálním traumatu [14]. Vyšší výskyt je také vázán na mužské pohlaví plodu a Rh izoimunizaci [2].
S mortalitou jsou spojeny faktory: vyšší věk rodičky (nad 35 let), multiparita, kouření v těhotenství, nižší socioekonomický status, černošská rasa nebo obecně etnická menšina v dané společnosti, indukce porodu, celková anestezie nebo epidurální analgezie a způsob porodu (operační ukončení zvyšuje relativní riziko) [7].
ZÁCHYT
Na světě jsou zavedeny jen dva samostatné registry AFE – The United Kingdom Amniotic Fluid Embolism Register ve Velké Británii (součást The United Kingdom Obstetric Surveillance System) [12] a National Registry for Amniotic Fluid Embolism v USA [2].
Údaje z jiných krajin se opírají o retrospektivní studie z obecných registrů porodů (např. Australasian Maternity Outcomes Surveillance Syste – AMOSS, Canadian Perinatal Surveillance System atd.).
Do registrů se v USA a v UK zadávají údaje o pacientkách majících následující příznaky:
- akutní hypotenze nebo srdeční zástava, arytmie,
- akutní hypoxie (dyspnoe, cyanóza) nebo zástava dechu,
- nevysvětlitelná koagulopatie (DIC, fibrinolýza, hemoragie),
- ztráta vědomí, křeče, excitace, otupění, dušnost,
- fetální distress,
- výskyt v průběhu porodu, císařského řezu, dilatace nebo evakuace dutiny děložní nebo v časném šestinedělí (asi do 30 minut po porodu),
- a současně absence jiného možného vysvětlení vzniklého stavu, nebo pacientky, u kterých byla diagnostikována AFE post mortem nálezem fetálních buněk nebo lanuga v plicích [2, 6].
DIAGNOSTIKA
Diagnostika je možná jen na základě příznaků po vyloučení jiných stavů (per exclusionem!), které mají podobné příznaky. Jednoznačnou diagnózu vyslovujeme jen při pitvě po nálezu částic plodové vody v plicních kapilárách (epitelie, lanugo, mekonium, mázek) [1].
Mezi příznaky AFE jsou (v závorce procentuální výskyt):
- hypotenze a fetální distress (100 % případů),
- plicní edém nebo ARDS (93 %),
- kardiopulmonální zástava (87 %),
- cyanóza (83 %),
- koagulopatie (83 %),
- dyspnoe (49 %),
- poruchy vědomí nebo záchvaty (třes, křeče, připomínající epileptický záchvat atd. 48 %),
- atonie dělohy (23 %),
- bronchospazmus (15 %),
- tranzitorní hypertenze (11 %),
- kašel (7 %),
- bolesti hlavy (7 %),
- bolesti na hrudníku (2 %) [8].
Všechny tyto příznaky musíme odlišit zejména od stavů, jako je alergie/anafylaxe, kardiopulmonální selhání, sepse, plicní embolie (jiná než AFE), aspirace žaludečního obsahu, eklamptický záchvat, ischemická choroba srdeční, hemoragie, transfuzní reakce, toxicita anestetik apod.
U přeživších dosud neexistuje přesný laboratorní test na AFE. Materiálem pro laboratorní diagnostiku je periferní krev matky, bronchiální sekret nebo krev z centrálního venózního katétru.
Mezi běžné laboratorní markery, které můžeme zjišťovat u přeživších žen, patří zejména součásti komplementu C3 a C4, u kterých dochází k poklesu hladin po konzumpci při vzniku koagulopatií, zejména pak u žen s nějakou alergickou anamnézou.
Dále můžeme zjišťovat hladinu sérové tryptázy – uvolňuje se z mastocytů společně s histaminem (ten je v malé míře detekovatelný v moči) při anafylaktické reakci, samotné příznaky ale nevyvolává [15].
Z dalších markerů je to Zn-koproporfyrin (ZnCP-1), obsažený v mekoniu, dále STN (sialosyl Tn) obsažený v hlenu a mekoniu. STN se v poslední době spíše ukazuje jako prognostický faktor mortality po AFE [10].
Z dalších proteinů jsou to zejména látky produkované fetálními buňkami do plodové vody – tumor markery, jako SCC (squamous cell carcinoma), CEA (carcinoembryonic antigen), CA125, hCG beta apod. [10].
Významným novým diagnostickým parametrem se zdá být insulin-like growth factor binding protein-1 (IGFBP-1), jehož výrazně zvýšené hladiny byly prokázány u pacientek po AFE [3].
TERAPIE
Terapie musí být neodkladná, mezioborová a prováděna automaticky.
Při podezření na AFE okamžitě:
- podat kyslík maskou,
- přivolat zkušeného porodníka a anesteziologa, k nim dostatečný počet středního zdravotnického personálu,
- založit záznam pro diagnostiku a léčbu život ohrožujících stavů (TK, pulz, počet dechů, saturace, podané léky, jiné zákroky). Poznámky vede 1 osoba (nejlépe lékař, ale i porodní asistentka nebo anesteziologická sestra) čitelně a srozumitelně, podle přesné časové posloupnosti. Tato osoba se kromě zápisu nevěnuje žádné jiné činnosti.
Ve spolupráci porodník-anesteziolog-sestra dále:
Dýchací cesty:
- zhodnotit stav,
- udržovat průchodnost,
- 100% O2 maskou, 15 l/min, vhodný PEEP,
- použít pulzní oxymetr,
- při známkách kardiopulmonálního stavu zvážit orotracheální intubaci.
Krevní oběh:
- zhodnotit stav oběhu a TK,
- pokud je ještě před porodem, tak uložit rodičku na levý bok (prevence aortokavální komprese),
- zajistit 2 intravenózní (dále jen i.v.) přístupy,
- monitorovat EKG a TK,
- odebrat krev pro zhodnocení krevního obrazu a koagulačních parametrů (očekáván DIC),
- léčba arytmií,
- statim objednat deleukotizovanou erymasu (alespoň 6 IU), dále fibrinogen nebo léky na léčbu DIC.
Další postup:
- okamžité (tj. ideálně do 3–4 minut od vzniku akutního stavu [5]) ukončení těhotenství,
- léčba hypotenze (i.v. koloidy, před porodem efedrin, po porodu noradrenalin),
- zavedení centrálního žilního katétru (pro diagnostiku akutní plicní hypertenze nebo pro řešení hypovolémie, zvážit zavedení arteriálního katétru),
- konzultace léčby DIC s hematologem (podávání krevních derivátů, event. heparinu v hyperkoagulační fázi DIC),
- kontrola krvácení z dělohy (podání uterotonik, kontrola poporodního krvácení, ultrazvukové vyšetření dělohy – při neztišitelném krvácení další postup podle Doporučených postupů ČGPS),
- ke zvážení podání kortikosteroidů, pentoxifylinu, oxidu dusného (NO), nootropik, faktoru VIIa,
- pokus o eliminaci „spouštěčů“ (ECMO, hemofiltrace, plazmatická výměna),
- rentgen srdce a plic, scintigrafie plic,
- diferenciální diagnostika příčin kardiopulmonálního selhání nebo DIC,
- další vyšetření k určení příčiny (komplement C3 a C4 a jiné laboratorní markery – viz kapitolu Diagnostika) [1].
Chirurgická léčba spočívá například v:
- akutní plicní embolektomii,
- mimotělním oběhu,
- kardiopulmonárním bypassu,
- intraoperační rekuperaci krve („cell salvage“),
- intraaortální balonkové kontrapulzaci,
- transezofageálním ECHO,
- využití srdečních pump [4, 5].
ZÁVĚR
AFE je závažná komplikace, která vyžaduje sledování a další studium. Zde je na místě otázka, zda právě nenadešel ten správný čas vytvořit i v našich podmínkách národní registr mapující všechny porody v zemi a patologie vzniklé v průběhu a krátce po porodu.
Zhodnocením dat můžeme také přispět k vysvětlení mechanismu embolizace plodové vody do oběhu matky a vzniku život ohrožujících klinických projevů. Zároveň nám registr poskytne obraz o všech jiných patologiích v české perinatologii.
MUDr. Andrej Černý
Gynekologicko-porodnická klinika
1. LF UK a VFN
Apolinářská 18
128 08 Praha 2
e-mail: andrej.cerny@gmail.com
Sources
1. Benson, MD. Current concepts of immunology and diagnosis in amniotic fluid embolism. Clin Dev Immunol, 2012, 2012 : 946576, 7 p.
2. Clark, SL., Hankins, GDV., Dudley, DA., et al. Amniotic fluid embolism: Analysis of the national registry. Am J Obstet Gynecol, 1995, 172, p. 1158–1169.
3. Conde-Agudelo, A., Romero, R. Amniotic fluid embolism: an evidence based review. Am J Obstet Gynecol, 2009, 201, p. 445.e1–445.13.
4. Dobbenga-Rhodes, YA. Responding to amniotic fluid embolism. AORN J, 2009, 89, p. 1079–1088.
5. Firstenberg, MS., Abel, E., Blais, D., et al. Temporary extracorporeal circulatory support and pulmonary embolectomy for catastrophic amniotic fluid embolism. Heart Surg Forum, 2011, 14, p. 157–159.
6. Knight, M., Berg, C., Brocklehurst, P., et al. Amniotic fluid embolism incidence, risk factors and outcomes: a review and recommendations. BMC Pregnancy and Childbirth. 2012, 12, 11 s. http://www.biomedcentral.com/1471-2393/12/7.
7. Knight, M., Tuffnell, D., Brocklehurst, P., et al. Incidence and risk factors for amniotic-fluid embolism. Obstet Gynecol, 2010, 115, p. 910–917.
8. Kobayashi, H., Naruse, K., Sado, T., et al. Search for amniotic fluid-specific markers: novel biomarker candidates for amniotic fluid embolism. Open Women’s Health J, 2011, 5, p. 7–15.
9. Kramer, MS., Rouleau, J., Liu, S., et al. Amniotic fluid embolism: incidence, risk factors, and impact on perinatal outcome. BJOG, 2012, 119, p. 874–879.
10. Legrand, M., Rossignol, M., Dreux, S., et al. Diagnostic accuracy of insulin-like growth factor binding-protein-1 for amniotic fluid embolism. Crit Care Med, 2012, 40, p. 2059–2063.
11. McDonnell, NJ., Percival, V., Peach, MJ. Amniotic fluid embolism: a leading cause of maternal death yet still a medical conundrum. Int J Obstet Anesth, 2013, 22, p. 329–336.
12. Pařízek, A. Embolie plodovou vodou. In Pařízek, A. Kritické stavy v porodnictví. Kamenice: Mother-Care-Centrum Publishing, 2012, s. 108–110.
13. Thongrong, C., Kasemsin, P., Hofmann, JP., et al. Amniotic fluid embolism. Int J Crit Illn Inj Sci, 2013, 3, p. 51–57.
14. Tuffnell, DJ. Amniotic fluid embolism. Curr Opin Obstet Gynecol, 2003, 15, p. 119–122.
15. Tuffnell, DJ. United Kingdom amniotic fluid embolism register. BJOG, 2005, 112, p. 1625–1629.
Labels
Paediatric gynaecology Gynaecology and obstetrics Reproduction medicine
Article was published inCzech Gynaecology

2014 Issue 4-
All articles in this issue
- Amniotic fluid embolism – review
- Prebioptic methods in the cervical cancer screening
- Prenatal growth curves of the Czech population
- Correlation between the incidence of PIK3CA mutations in breast cancer and histopathological characteristics of the tumor
- Characteristics of sexual maturation in girls in Bratislava region
- Pregnancy and delivery in patients with an implanted shunt for hydrocephalus
- Dysplasia and cervical cancer: current diagnostic possibilities
- Intraindividual variability of uroflowmetry in women
- Principles and limits of clinical methods in the diagnosis of fetal hypoxia
- Shute´s parallel forceps
- The most valuable predictorsof endometrial receptivity
- Effect of six antiretroviral drugs (delavirdine, stavudine, lamivudine, nelfinavir, amprenavir and lopinavir/ritonavir in association) on albino pregnant rats (Rattus norvegicus Albinus, Rodentia, Mammalia): biological assay
- Tuberculosis in pregnancy:a challenging differential diagnosisfor inflammatory bowel disease
- Czech Gynaecology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Amniotic fluid embolism – review
- Prenatal growth curves of the Czech population
- Dysplasia and cervical cancer: current diagnostic possibilities
- Prebioptic methods in the cervical cancer screening
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

