-
Medical journals
- Career
Pars plicata vitrektomie u nedonošených novorozenců pro odchlípení sítnice v důsledku retinopatie nedonošených, naše výsledky
Authors: L. Hejsek; J. Kadlecová; J. Dusová; M. Macháčková; N. Jirásková
Authors‘ workplace: Oční klinika FN, Hradec Králové, přednosta prof. MUDr. Naďa Jirásková, PhD., FEBO
Published in: Čes. a slov. Oftal., 73, 2017, No. 4, p. 140-145
Category: Original Article
Overview
Úvod:
Cílem této práce je zhodnotit naše vlastní výsledky operačního řešení odchlípení sítnice při retinopatii u nezralých novorozenců. Retinopatie nedonošených (ROP) patří mezi nejzávažnější oční postižení, jak ve smyslu diagnostiky, tak i léčby. Jedná se o potenciálně oslepující onemocnění, které vzniká na podkladě nekompletního vývoje krevního řečiště neuroretiny předčasně narozených dětí. Nejefektivnější terapií je v současnosti ablace vaskulární sítnice laserovou fotokoagulací, či kryokoagulací. Navzdory této léčbě může dojít k rozvoji odchlípení nezralé sítnice.Metodika:
Uvádíme kazuistické výsledky retrospektivního sledování 4 očí u 2 pacientů se závažnými očními i celkovými komplikacemi při nedonošenosti. Oční pozadí nedonošených dětí bylo vyšetřováno v arteficiální mydriáze nepřímým oftalmoskopem a v průběhu pozdější sledovací doby i fotografickým přístrojem RetCam. Stadia ROP byla hodnocena podle ICROP klasifikace. Všechny oči byly při dosažení prahového stadia ROP ošetřeny kryo-retinopexí, dále sledovány a pro progresi se vznikem trakční amoce sítnice indikovány k nitrooční operaci. Operační technikou byla 3 portová 25-G PPV (pars plicata vitrektomie) se zavedením portů 1,5 mm od limbu. PPV byla provedena pomocí operační jednotky Constellation (ALCON), kontrolující nitrooční tenzi na 15 torrech. Hodnocení zrakové ostrosti bylo prováděno odhadem dle škály: bez světlocitu (není reakce dítěte na světlo), světlocit (pozitivní, či negativní reakce na osvit), fixační a sledovací pohyby očí.Výsledky:
U všech operovaných očí došlo k přiložení sítnice, více uvádíme v jednotlivých kazuistikách.Závěr:
Současné možnosti vitreoretinální chirurgie umožňují anatomickou úspěšnost operace trakčního odchlípení sítnice při ROP již v novorozeneckém věku.Klíčová slova:
odchlípení sítnice, retinopatie nedonošených, PPV, chirurgieÚVOD
Retinopatie nedonošených (ROP z angl. Retinopathy of prematurity) patří mezi nejvážnější oční postižení, jak ve smyslu diagnostiky, a tak i terapie. Již samotné vyšetření očního pozadí bývá v pokročilejších stavech obtížné (obvykle pro nedostatečnou mydriázu, nebo komplikace celkového stavu pacienta), přičemž jemné detaily nitroočního nálezu ovlivňují správné stanovení diagnózy a načasování případné léčby.
ROP je potencionálně oslepující onemocnění, které vzniká na podkladě nekompletního vývoje krevního řečiště neuroretiny předčasně narozených dětí (11). Patologie postihuje především děti narozené před 31. gestačním týdnem s hmotností 1 250 g a méně. Významným rizikovým faktorem je anémie, respirační obtíže pacienta a jeho celkové (ne-)prospívání.
Navzdory vysoce efektivní terapii zrak ohrožujících forem ROP laserem (studie ETROP 2003) (5), či kryokoagulací (studie CRYO-ROP 2001) (4), se stále setkáváme s trakčním odchlípením sítnice (TOS) při ROP. Výsledky stran zrakových funkcí při TOS nebývají uspokojivé (6). V poslední době se v literatuře objevují povzbuzující zprávy o dobrých anatomických i funkčních výsledcích vitrektomie, provedené v časných stadiích odchlípení sítnice při ROP (3, 9, 10).
Empiricky potvrzeným předpokladem úspěchu pars-plicata vitrektomie (PPV) při odchlípení sítnice při ROP je načasování zákroku do doby vyhasínání neovaskulární aktivity ROP (a regrese známek tzv. „plus disease“). Pokud „plus disease“ přetrvává, bývá prediktorem komplikací: krvácení, zvýšená exsudace a pokračující proliferace, které indukují pozdější kontrakci neuroretiny po provedení PPV možný neúspěch chirurgického zákroku (3, 7). V některých případech však může dojít k velmi rychlé progresi amoce ještě předtím, než „plus disease“ a neovaskulární aktivita dostatečně zregredují. Vyčkávání s indikací k PPV pak vede k horší prognóze pooperačního stavu. Čím je stav pokročilejší, tím je pooperační prognóza horší a snižuje se šance na přiložení (zejména při totálním odchlípení sítnice) (8).
Existuje i možnost anti-VEGF terapie před provedením PPV (anti-VEGF pretretment), jejíž efekt již byl také předmětem několika publikací. Smyslem anti-VEGF intravitreální terapie je „příprava“ před vlastní PPV, která má zajistit pokles vaskulární aktivity onemocnění před zákrokem (15).
Cílem této práce je zhodnotit naše vlastní výsledky operačního řešení odchlípení sítnice při ROP u nezralých novorozenců a poukázat na aspekty a úskalí léčby tohoto onemocnění.
METODIKA
Uvádíme naše kazuistické výsledky retrospektivního sledování 4 očí u 2 pacientů se závažnými očními i celkovými komplikacemi při nedonošenosti. Během celé doby intenzivního očního sledování byli pacienti hospitalizováni na Dětské klinice FN Hradec Králové. Oční pozadí nedonošených dětí bylo 1x týdně vyšetřováno v arteficiální mydriáze (Unitropic 1% gtt. a Neosynephrine 10% gtt.) nepřímým oftalmoskopem a v průběhu pozdější sledovací doby i fotografickým přístrojem RetCam (Clarity Medical Systeme, Pleasanton, CA). Stadia ROP byla hodnocena podle ICROP klasifikace (International Classification of Retinopathy of Prematurity) (13).
Všechny oči byly při dosažení prahového stadia ROP ošetřeny kryo-retinopexí, dále sledovány a pro progresi se vznikem trakčního odchlípení sítnice indikovány k nitrooční operaci amoce.
Operační technika v celkové anestezii byla obecně stejná ve všech případech. Všechny operace prováděl jeden chirurg (L.H.). Byla provedena tříportová 25-G PPV (pars plicata vitrektomie) se zavedením portů v obvyklých lokalizacích 1,5 mm od limbu. Pozice infuzní kanyly byla měněna během operace s ohledem na možnosti ošetření celé periferie sítnice. Jako infuze byl použit Ringerův roztok 500 ml s 5 ml 10% glukózy a 0,4 ml adrenalinu. Vitrektomie byla provedena pomocí operační jednotky Constellation (ALCON), kontrolující nitrooční tenzi na 15 torrech, s rychlostí sekání 1000–5000 za minutu. K vizualizaci byl použit operační mikroskop ZEISS OPMI Lumera 700 (s bezkontaktním systémem Resight pro zobrazení zadního segmentu). Hlavním cílem operace bylo vystříhání změněného sklivce a přetětí všech trakčních sil spojujících pars plicata a nitrooční čočku a pars plicata a sítnici se zrakovým nervem. Bohužel v prvním případě (kazuistika č. 1) nebylo možné pro tíži nálezu v daleké periferii sítnice ponechat pacienta fakického. Současně v tomto případě bylo nutné použít i tamponádu decalinem a silikonovým olejem. V druhém případě (kazuistika č. 2) nebyla použita žádná nitrooční tamponáda. Všechny operační vstupy byly na konci zákroku ošetřeny transkonjunktivální suturou vstřebatelným stehem (8-0 Vicryl). Poslední součástí operace byla parabulbární aplikace 3 ml směsi Diprophos a Gentamicin (v poměru 1 : 1).
Hodnocení zrakové ostrosti bylo prováděno odhadem dle škály: bez světlocitu (není reakce dítěte na světlo), světlocit (pozitivní, či negativní reakce na osvit), fixační a sledovací pohyby očí.
VÝSLEDKY
V této práci retrospektivně hodnotíme dva případy našich nejkomplikovanějších nedonošených pacientů, které bylo nutné pro rozvoj trakční amoce při ROP již v novorozeneckém období operovat.
Kazuistika č. 1
Jednalo se o chlapce narozeného v 27. gestačním týdnu (GT) s porodní váhou 700 g. Porodu předcházela parciální hemorhagická abrupce placenty v 25. GT s hypotrofizací plodu. Po narození vznikl syndrom dechové tísně s nutností podání surfaktantu a třetí den života spontánní perforace ilea při jeho vrozené vývojové vadě. Stav byl řešen dvěma resekcemi postižených úseků střeva a anastomózami end-to-end. V prvním měsíci života bylo pak nutné provést ještě jednu resekci ilea. Až poté pacient začal tolerovat enterální příjem. Distenze břicha zhoršovala dýchací obtíže a pacient střídavě vyžadoval plnou plicní ventilaci. V krátkosti uvádíme ještě základní souhrn dalších diagnóz: syndrom krátkého střeva s anémií (nutnost transfuzí) a hypovitaminózou, bronchopulmonální dysplázie, mírná hydronefróza, tříselná kýla oboustranně a stav po respiračním selhání ve 4. týdnu života (31. GT).
Plný enterální příjem toleroval až od 33. GT, ve 35. GT ukončena dechová podpora s oxygenoterapií.
Pro ROP byl tento rizikový pacient sledován v týdenních intervalech od 31. GT. Ve 36. GT jsme zaznamenali ROP 2. stupně v zóně 2 a tento klidný stav se neměnil až do 41. GT. V tomto týdnu byla zjištěna na obou očích výrazná tortuozita cév v periferii, cirkulární progrese výšky valu, na kterém byly hemorhagie a živé cévní proliferace do sklivcového prostoru. Retina byla přiložená, trakční projevy ve sklivci nebyly patrné, stav hodnotíme jako stadium 3 s „plus disease“ a indikujeme provedení kryo-retinopexe. Ošetření bylo provedeno hned následující den. Při zákroku (detailní vyšetření v celkové anestezii s indentací periferie sítnice) vznášíme podezření na suspektní plošnou amoci v horních kvadrantech obou očí. Po kryoretinopexi sítnice vznikají nové dechové obtíže pacienta, který znovu vyžaduje dvoudenní úplnou plicní ventilaci. Pacient je dále sledován v týdenních intervalech, postupně ustupují projevy „plus disease“, mizí hemorhagie a neovaskularizace, cévní složka se klidní. Ve 45. GT ale potvrzujeme odchlípení sítnice na pravém oku s ležící makulou (ROP ve stadiu 4A). Zrakové funkce odhadujeme na úrověň světlocitu. Za čočkou je patrný trakční hřebínek, který vazivovým můstkem komunikuje v amovanou periferií sítnice. Nález na levém oku zůstává stabilní, zde je odchlípení sítnice pouze suspektní (oftalmoskopicky), s negativním nálezem při ultrasonografickém vyšetření očního pozadí. Vzhledem k progresi nálezu a zklidnění cévní složky retinopatie přistupujeme k provedení operačního řešení na pravém oku.
Před zákrokem na OP byla provedena (již v celkové anestezii) kontrola pozadí OL nepřímým oftalmoskopem: nález bez známek plus onemocnění, sítnice leží, vaskularizace velkých cév je prakticky kompletní, v temporální periferii (v zóně 3) je suspektní plošná amoce, trakční projevy nebyly nalezeny. Levé oko v této době k operaci neindikujeme. Dále provedena PPV pravého oka: těsně za čočkou je v její periferii cirkulárně vysoký hřeben, který je vazivovými membránami již napojen na zadní pouzdro čočky, proto provedena pars plana lensektomie, pokračujeme v PPV, amoce je totální (v makule plošná), vystříhání těžce vazivově změněného sklivce, odloučení hutných membrán před papilou a kolem papily, které zde vytvářejí zkrácený pohárek z odchlípené neuroretiny, odloučení velmi pevně lnoucí zadní sklivcové membrány až po sklivcovou basi, peeling mnohočetných membrán na zadním pólu po obarvení ředěným Triamem a modří, rozepnutí zadního pólu dekalinem, segmentace a delaminace velmi hustých trakčních membrán v oblasti ciliárního tělesa. Ani po kompletním uvolnění všech vazivových změn se sítnice kompletně nepřikládá. Výměna za vzduch, Miostat do PK, bazální kolobom v č. VI vitrektomem, následně výměna za silikonovou tamponádu (Oxane 1300, Bauch and Lomb).
Při peroperačním nálezu byla patrná velice řídce vaskularizovaná makula, neuroretina obsahuje prakticky jen velké cévy, temporální část makuly a zevní střední periferie je degenerativně až cysticky změněná, ROP je ve stadiu 5 (obr. 1).
Image 1. Peroperační nález OP: chabá vaskularizace, vazivové změny na povrchu sítnice, v dolní periferii (horní část obrázku) vysoký hřeben s membránami na povrchu 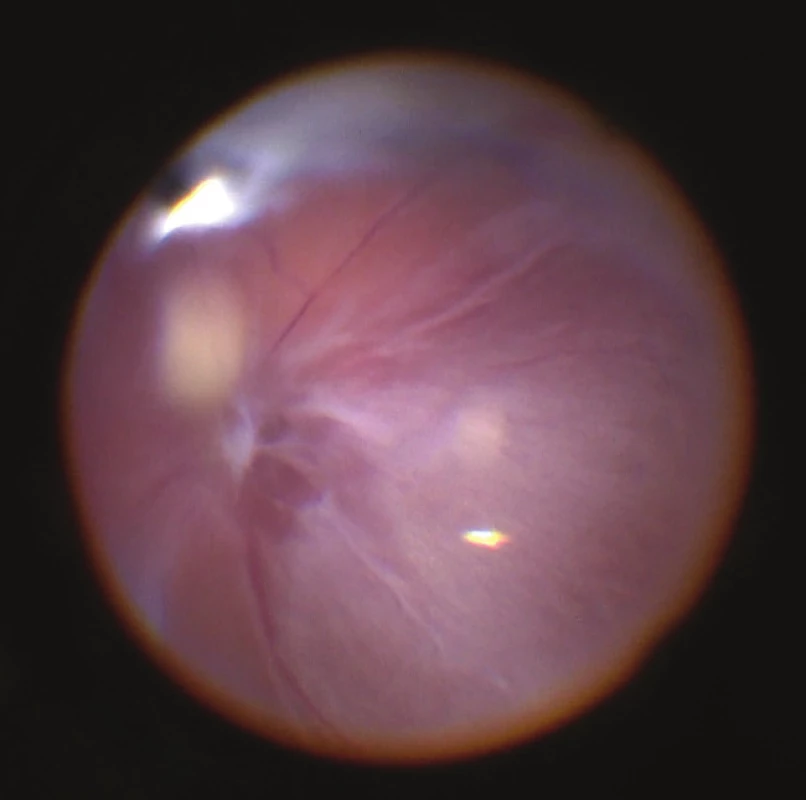
Pokračujeme v týdenních kontrolách – nitrooční nález na levém oku se zhoršil ve 48. GT, kdy amoce sítnice oftalmoskopicky progreduje v nasálních kvadrantech (ROP 4A). Také na tomto oku indikujeme operační zákrok. Bylo provedeno: vystříhání retrolentálního vazivově změněného sklivce, za zadní plochu čočky jsou napjaté membrány, které napínají (cirkulárně) hřeben amoce vysoko v periferii sítnice (obr. 2), proto také provedena lensektomie vitrektomem. Sklivec obarven ředěným triamcinolonem, peeling mnohočetných membrán na zadním pólu, decaline pro oploštění makuly. Postupné odstřihávání a odlučování četných membrán cirkulárně. Provedeny relaxační radiální nástřihy ve vazivu na vrcholu cirkulárně uloženého hřebene v periferii. Pinzetou postupně odlučujeme vazivový prstenec, který cirkulárně retrahuje sítnici. Miostat do PK, bazální iridektomie vitrektomem v č. VI., výměna za vzduch a následně za silikonovou tamponádu (Oxane 1300, Bauch and Lomb).
Image 2. Peroperační nález OL: po provedení lensektomie, shave vazivových membrán na povrchu elevovaného trakčního hřebenu v periferii 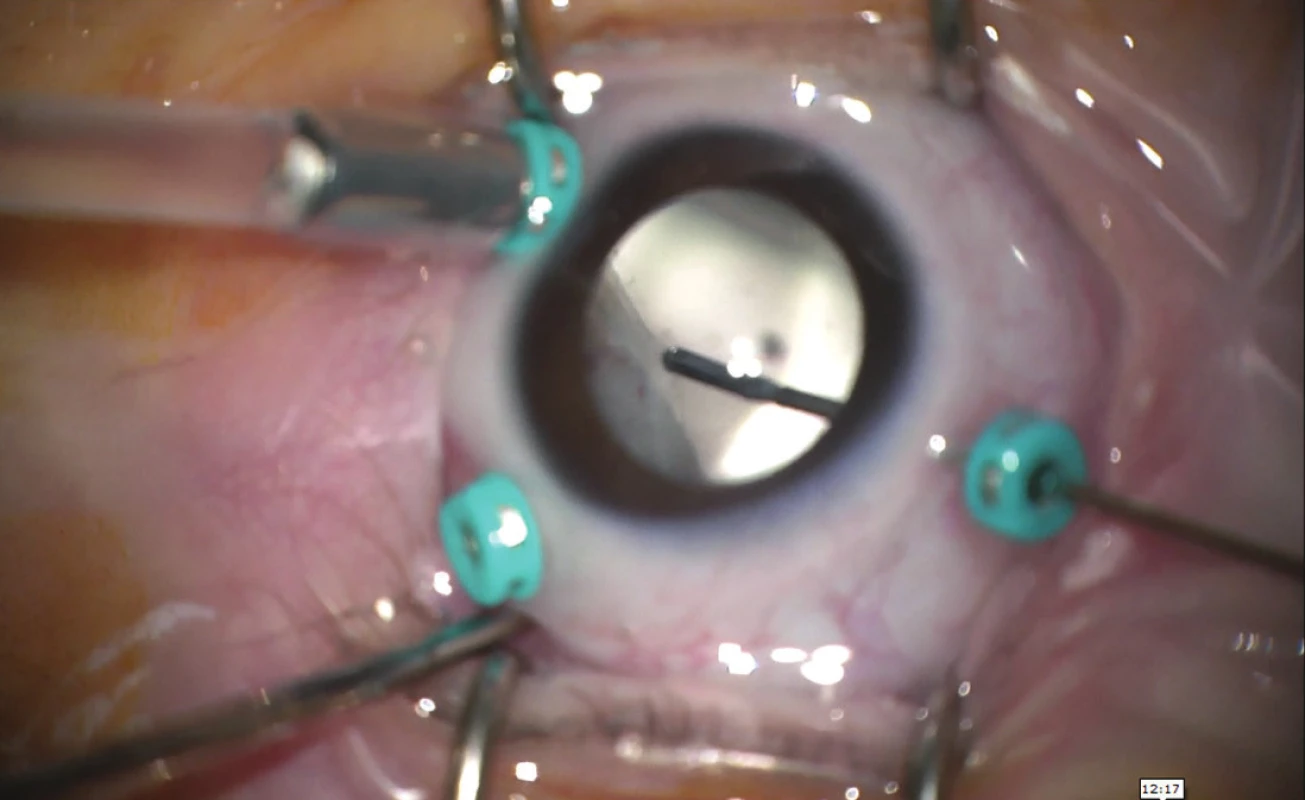
V pooperačním období se nález na očním pozadí pozvolna zlepšuje, amoce sítnice klesá a zbytkové plošné odchlípení spolehlivě ustupuje na levém oku 2,5 měsíce a vpravo až 4 měsíce po provedené PPV. Silikonová tamponáda neproniká do přední komory, rohovka je transparentní, nitrooční tenze normální (měřeno přístrojem TonoPen) a kolobomy průchodné.
Na konci sledovací doby (1,5 roku po narození) je dítě fyzicky vitální, celkový stav bez alterace, somatický nález odpovídá retardaci růstu (hmotnost 6 580 g). Nosí brýlovou korekci +15,0 vpravo a +18,0 vlevo, zraková ostrost je oboustranně na úrovni spolehlivé fixace. Nejsou přítomné nystagmoidní pohyby. Přední segment na obou očích je bez komplikací, silikonová tamponáda ve sklivcovém prostoru, retina leží. Papily jsou oboustranně bledší. Na sítnici jsou patrné zejména velké cévní kmeny, jinak je cévní kresba chudá, vpravo nalézáme perivaskulární bledé exsudace podél hlavních cévních kmenů a od střední periferie výrazné pigmentové přesuny až atrofie (obr. 3). Vlevo je porucha vývoje cévního řečiště méně výrazná než vpravo, nejsou exsudace, makula a střední periferie jeví také známky výrazných pigmentových přesunů, zevně od centra jsou atrofické změny RPE.
Image 3. Barevné foto pravého oka v pooperačním období 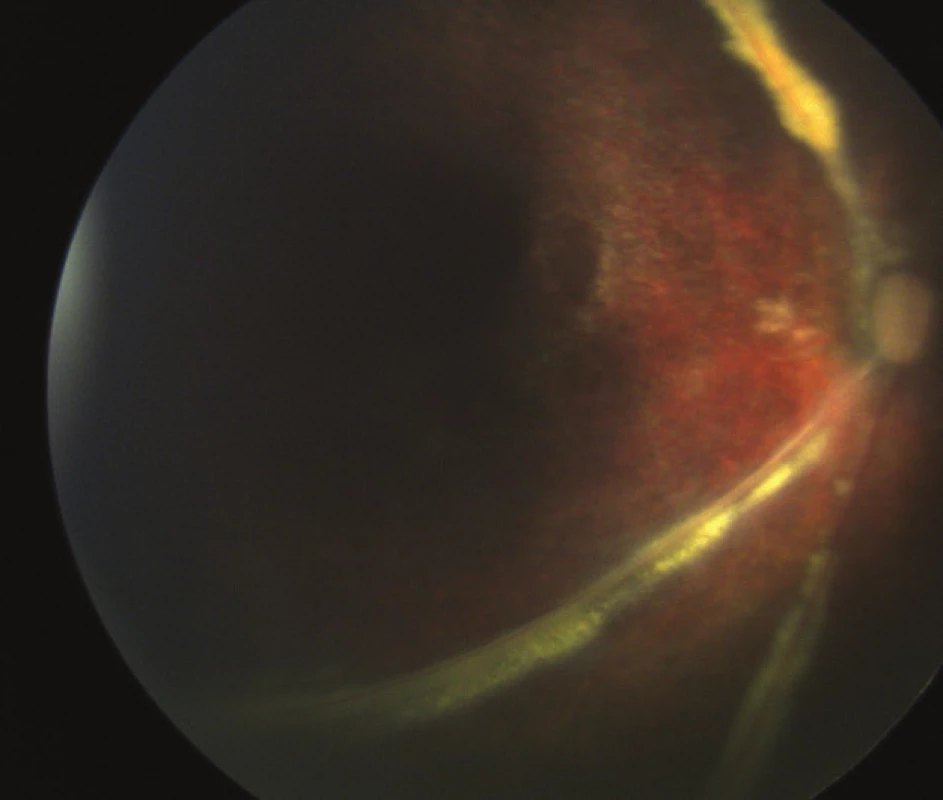
Kazuistika č. 2
Jedná se o děvče (narozené jako dvojče „B“, společně s bratrem – „A“) v 24. gestačním týdnu s porodní váhou 500 g. Také u jejího bratra se vyvinula ROP, která byla v prahovém stadiu oboustranně ošetřena kryo-retinopexí. V tomto případě došlo po zákroku k regresi nálezu bez následného rozvoje trakční amoce.
Porodu těchto dvojčat předcházela chorio-amniitida v průběhu 24. GT. U holčičky se krátce postnatálně rozvíjí syndrom dechové tísně a perzistující plicní hypertenze. Byly podány 2 dávky surfaktantu, napojení na úplnou plicní ventilaci a celková kortikoterapie pro bronchopulmonální dysplazii. Plicní ventilace byla ukončena v 31. GT, ale dechová podpora s oxygenoterapií je nutná až do 39. GT. Poporodní průběh je dále komplikován opakovanými infekcemi: stafylokoková sepse, kandidová sepse a následně pneumonie. V 45. GT se rozvíjí nekrotizující enterokolitis, řešená operační revizí a resekcí části tenkého střeva. Z dalších patologií vyjímáme: přechodná hyperglykémie s nutností inzulinoterapie pumpou (trvající dva měsíce), anémie smíšené etiologie, periventrikulární leukomalácie s atrofií corpus callosum (38. GT), cytomegalovirová hepatitis.
Pro ROP je tato riziková pacientka sledována v týdenních intervalech od 29. GT. Od 31. GT pozorujeme počínající stadia – ROP 1 v zóně 2. Progrese retinopatie nastupuje v 33. GT, ROP 2 až 3 v zóně 2, vaskularizace velkých cév pozvolna dorůstá, ale cévy začínají být tortuózní. V 37. GT se zvýrazňují známky „plus disease“ na pravém oku (zde ROP 2 až 3 v zóně 2) a zejména na levém oku (zde ROP 3 v celé temporální periferii, elevace sítnice na valu a fokální hemorrhagie ve sklivci). Následující den provedena kryo-retinopexe oboustranně, kdy na pravém oku jsou již také aktivní neovaskulární proliferace v celé temporální periferii a lehký hemoftalmus. Během dalšího sledování se zklidňuje cévní patologie, mizí neovaskularizace a oplošťuje se prominentní val v periferii obou očí. Za zcela klidného stavu v periferii sítnice na konci 39. GT nastupuje plošná amoce na fundu pravého oka (ROP 5) a dolní periferie vlevo (ROP 4A). Zrakové funkce jsou na úrovni světlocitu. Indikujeme operační řešení na obou očích současně (sekvenční provedení PPV).
Při PPV na OP bylo provedeno vystříhání sklivce, přetětí trakčních pruhů před sítnicí, šetrný shave cirkulární membrány, která vytváří hřeben při okraji sklivcové base a indukuje totální odchlípení sítnice (obr. 4).
Image 4. Peroperační nález OP: hemoftalmus, trychtýřovitá totální amoce 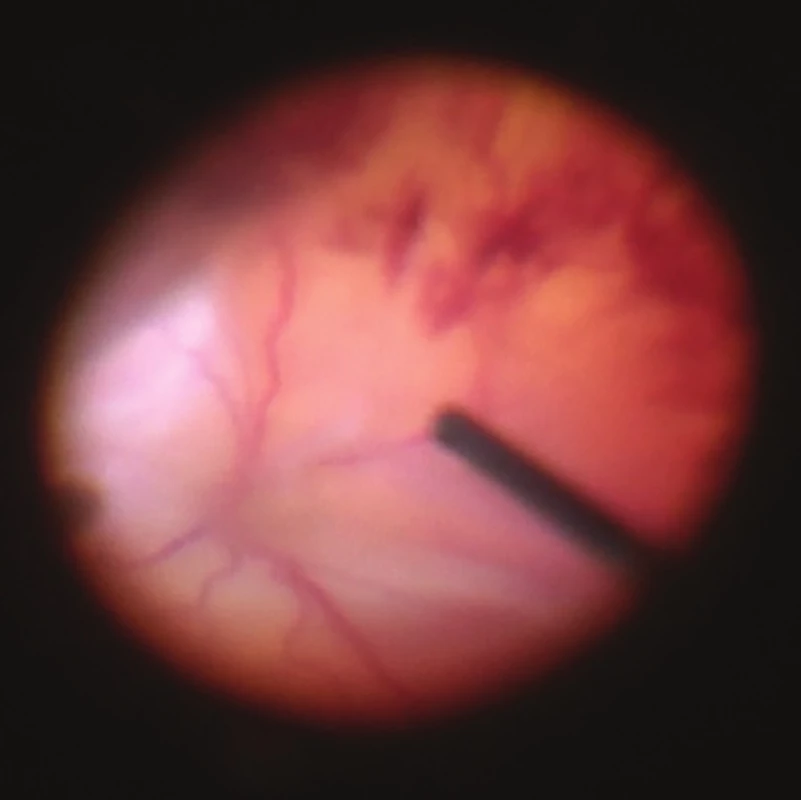
Na OL byl nejprve vystříhán jemný hemoftalmus, poté přetnuty mnohočetné membrány, které cirkulárně odlučují sítnici. Segmentace a delaminace trakčních membrán před papilou a v makulární krajině, uvolnění předpokládané zadní sklivcové membrány až do periferie, vystříhání base sklivce a její shave (obr. 5).
Image 5. Peroperační nález OL: krevní koagula a vazivové proliferace v makule, totální amoce 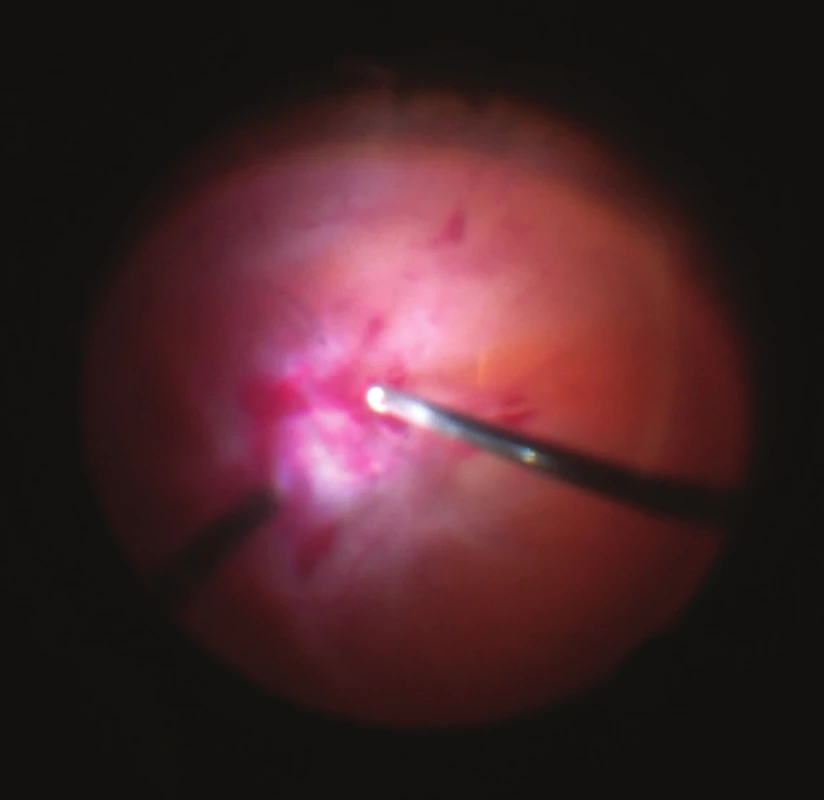
Pacientka ponechána oboustranně fakická a bez nitrooční tamponády. Peroperačně diagnostikujeme stadium ROP 5 oboustranně. Retina se po zákroku opět pozvolna přikládá, vpravo kompletně leží za 35 dní po zákroku a vlevo až za 45 dní.
Při poslední kontrole (v 7. měsíci věku) je dítě zdravé, vitální, má hmotnost 3 680 g. Zraková ostrost je na úrovni spolehlivé fixace. Nejsou přítomné projevy strabismu ani nystagmu. Nález na předním segmentu obou očí je fyziologický, sklivcový prostor čistý, retina leží. Vpravo je papila s normálním nálezem, vlevo překryta plošnou gliózou. Centrální krajina levého oka vykazuje změny pigmentace a vazivové projevy, cévní síť obou očí je chabá (obr. 6 a 7).
Image 6. Barevné foto pravého oka v pooperačním období 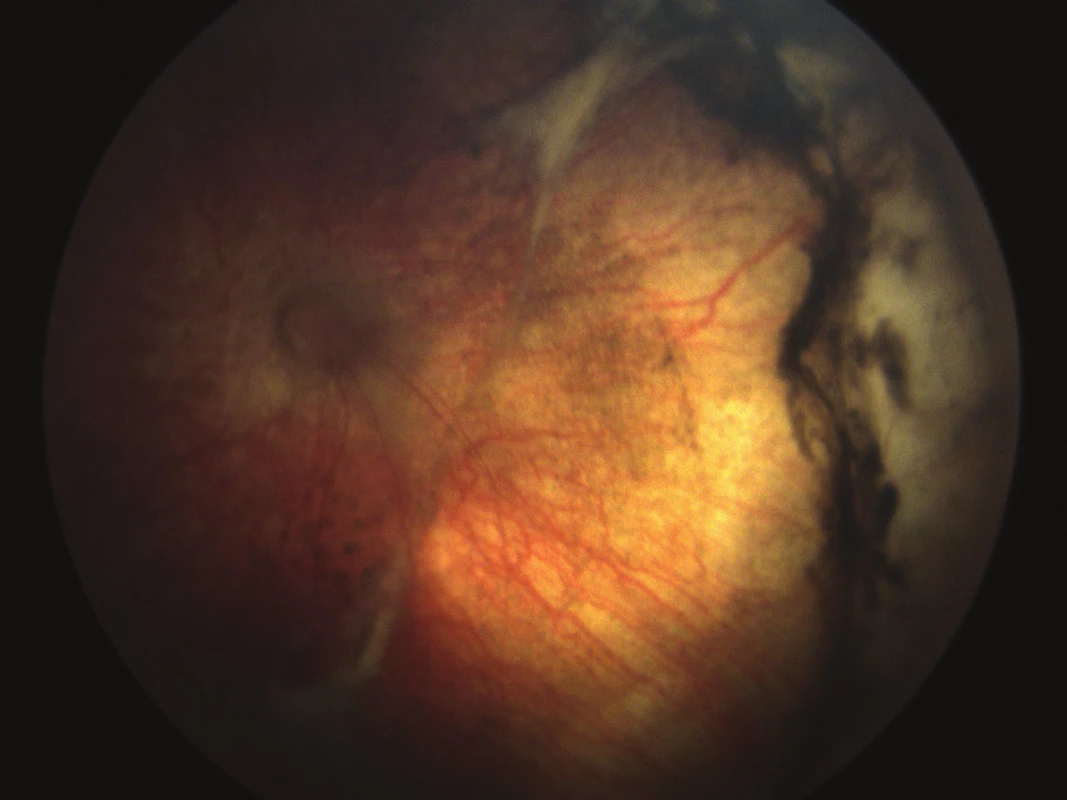
Image 7. Barevné foto levého oka v pooperačním období 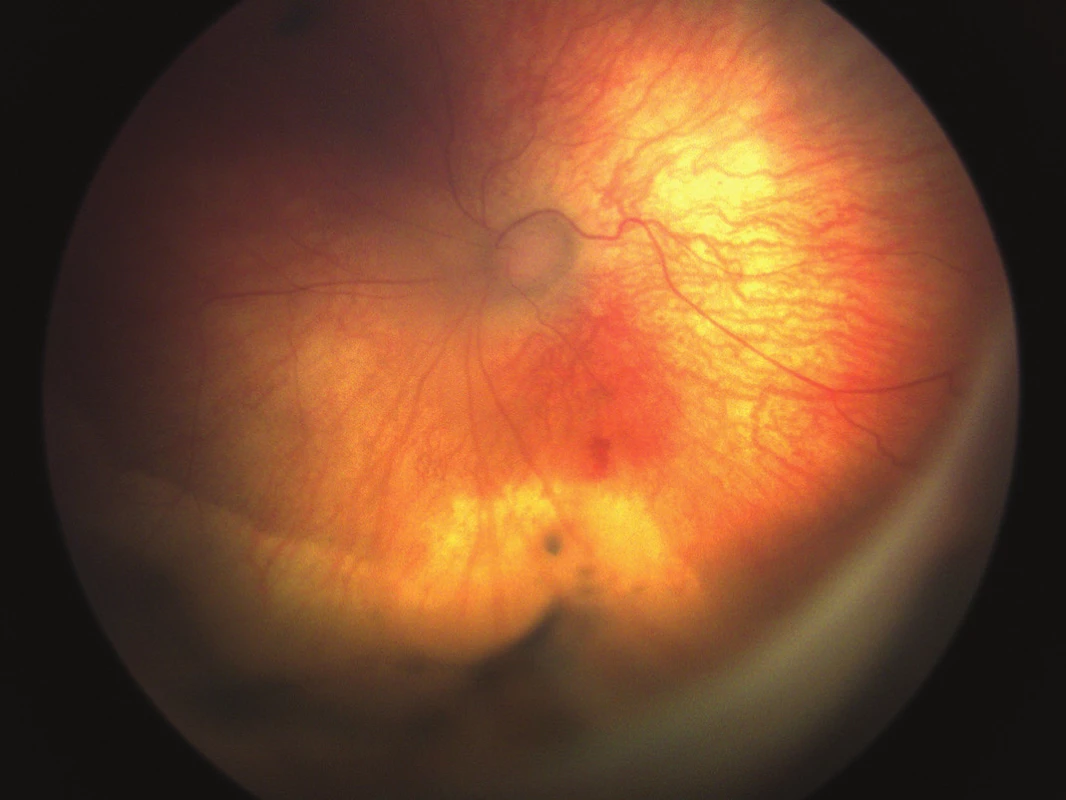
DISKUSE
Retinopatie nedonošených je potenciálně oslepující onemocnění, zejména pro riziko trakčního odchlípení sítnice. Současně je také rizikovým faktorem pro další možné oční komplikace: těžká krátkozrakost, amblyopie, glaukom atd. Nejefektivnější terapií je v současnosti ablace vaskulární sítnice laserovou fotokoagulací či kryokoagulací (1). Tyto techniky jsou ale méně či více destruktivní pro oční pozadí. Příslibem pro některé typy ROP se zdá být anti-VEGF terapie, která je v současné době předmětem klinického výzkumu.
Pokud výše uvedená terapie ROP selhává, dochází k rozvoji amoce postižené sítnice. Obvykle postihuje odchlípení zpočátku jen část sítnice (stadium 4). Základní typy amocí, které mohou vzniknout při ROP jsou: serózní a trakční (a jejich kombinace), výjimečně rhegmatogenní. Serózní amoce je způsobena průsakem tekutiny abnormálními cévními strukturami do sítnice a subretinálního prostoru. Tvar takové amoce bývá konvexní, obvykle je amoce za hřebínkem a rozšiřuje se k makule i za čočku. Serózní amoce se může přiložit spontánně, i bez operačního řešení. Převážně trakční amoce je provázena přítomností fibrovaskulární tkáně, která může vytvářet záhyby, nebo stanovitá vyvýšení neuroretiny. Možnost spontánní úpravy nálezu je při trakčním odchlípení nepravděpodobná. Některé amoce se tedy mohou i samy upravit, nebo alespoň zůstat stacionární v čase. Pak může být náročné rozhodnout a správně načasovat indikaci k provedení PPV, jejíž hlavním smyslem je zabránit rozvoji slepoty.
Postižení amocí není bohužel příliš vzácné: ve studii ETROP (5) mělo amoci alespoň na 1 oku 16 % nedonošených s rizikovou formou retinopatie. Rizikové faktory predisponující k amoci, která nebude mít snahu spontánní úpravy, hledala retrospektivní studie kontrolovaných případů. Mezi tyto faktory patří: 1. přetrvávající, či rekurentní „plus disease“ ve 2 kvadrantech oka, 2. elevace hřebenu v rozsahu 6 nebo více kontinuálních hodin a 3. organizace sklivce na rozhraní vaskulární a vaskulární neuroretiny, nebo u zrakového nervu a 4. krvácení nebo fibrovaskulární kontrakce na hřebenu (12).
Spolehlivé rozlišení těchto detailů však může být obtížné: závisí na zkušenostech vyšetřujícího, velikosti zornice, vyšetřitelnosti pacienta atd. Nedostatečné zhodnocení nálezu může ohrozit pacienta ve smyslu pozdně provedeného zákroku, kdy aktuální nitrooční stav může být natolik těžký, že bude vyžadovat provedení lensektomie a použití nitrooční tamponády. Taková situace nastala v našem případě – Kazuistika č. 1. Velmi prospěšnou pomocnou zobrazovací technikou se nám jeví současně provedená fotografie (například přístroj RetCam) a ultrasonografie.
Na základě našich chirurgických zkušeností a operačních výsledků se přikláníme k doporučením Americké akademie (AAO): PPV se zachováním čočky doporučujeme při diagnostice ROP ve stadiu 4 s cílem předejít progresi do stadia 5 a zachovat makulární funkce a vývoj zraku. Hlavním cílem operace je uvolnit veškeré trakční síly a umožnit tak sítnici její spontánní přiložení bez nitrooční tamponády. Pokud bude TOS operována ve stadiu 5, můžeme očekávat úspěch pouze asi v 1/3 případů (4). Časnější provedení PPV omezuje riziko kontaktu fibrovaskulární tkáně se zadní plochou čočky a sklivcové base. Taková operace je potom i technicky snažší (jak bylo patrné v naší druhé kazuistice) a umožňuje ponechat vlastní čočku pacienta in situ (15).
Obávanými komplikacemi zákroku jsou 1. pooperační afakie – pro velmi obtížnou zrakovou rehabilitaci a vysokému riziku težké amblyopie a 2. jatrogenní díry neuroretiny, které indukují rychlý rozvoj inoperabilní amoce s proliferativní vitreoretinopatií a vedou tak ke slepotě. Dalšími známými riziky jsou: rozvoj katarakty (5–15 % případů), endoftalmitidy a závažné zhoršení zdravotního stavu pacienta po zákroku v celkové anestezii. (12) Uchování vlastní čočky u nedonošených pacientů je důležité významně předchází rozvoji deprivační amblyopie a podporuje vývoj zraku (14).
Dále je třeba znovu připomenout, že operační řešení má nejlepší výsledky při vyhaslé cévní aktivitě ROP. Přetrvávání aktivity ve smyslu „plus disease“ zhoršuje operační výsledky. Taková PPV je spojena s rizikem komplikujícího peroperačního krvácení, výraznější exsudativní aktivity a pokračující proliferace, která je společně s retrakcí následně vytvořených membrán hlavní příčinou selhání PPV (3).
ZÁVĚR
Současné možnosti oční chirurgie umožňují anatomickou úspěšnost operace trakčního odchlípení sítnice při retinopatii nedonošených v novorozeneckém věku. Podle našich zkušeností a literárních údajů je operace technicky jednodušší v časnějších stadiích odchlípení. Načasování zákroku (dle vývoje amoce a aktivity cévní složky retinopatie) je klíčové pro jeho jeho konečnou úspěšnost. Nezbytným předpokladem pro diagnostiku a terapii je důkladně provedené vyšetření a využitím pomocných zobrazovacích metod (fotografie a echografie).
Autoři práce prohlašují, že vznik i téma odborného sdělení a jeho zveřejnění není ve střetu zájmu a není podpořeno žádnou farmaceutickou firmou.
Poděkování:
Děkujeme za konzultaci prim. MUDr. Milanu Odehnalovi, MBA a za spolupráci s MUDr. Annou Zobanovou.
Do redakce doručeno dne 4. 9. 2017
Do tisku přijato dne 20. 10. 2017
MUDr. Libor Hejsek, PhD., FEBO
Oční klinika FN Hradec Králové
Sokolská 581
500 05 Hradec Králové
Sources
1. Autrata, R., Holousova, M., Rehurek, J.: Cryotherapy and photocoagulation in the treatment of retinopathy of prematurity. Cesk Slov Oftalmol. 2002 Jan;58(1):30-5.
2. Azuma, N., Ishikawa, K., Hama, Y. et al.: Early vitreous surgery for aggressive posterior retinopathy of prematurity. Am J Ophthalmol, 142; 2006 : 636–643.
3. Capone, A. Jr., Trese, M. T.: Lens-sparing vitreous surgery for tractional stage 4A retinopathy of prematurity retinal detachments. Ophthalmology, 108; 2001 : 2068–2070.
4. Cryotherapy for Retinopathy of Prematurity Cooperative Group.: Multicenter trial of cryotherapy for retinopathy of prematurity: ophthalmological outcomes at 10 years. Arch Opthalmol., 119; 2001 : 1110–1118.
5. Early Treatment for Retinopathy of Prematurity Cooperative Group: Revised indication for the treatment of retinopathy of prematurity: results of early treatment for ROP randomized trial. Arch Ophthalmol, 121; 2003 : 1684–1696.
6. Gilbert, W.S., Quinn, G.E., Dobson, V. et al.: Partial retinal detachment at 3 months after threshold retinopathy of prematurity. Long-term structural and functional outcome. Arch Opthalmol, 114; 1996 : 1085–1091.
7. Hartnett, M.E.: Features associated with surgical outcome in patients with stages 4 and 5 retinopathy of prematurity. Retina, 23; 2003 : 322–329.
8. Mintz-Hittner, H.A., O’Malley, R.E., Kretzer, F.L.: Long-term form identification vision after early, closed, lensectomy-vitrectomy for stage 5 retinopathy of prematurity. Ophthalmology, 104; 1997 : 454–459.
9. Moshfeghi, A.A., Banach, M.J., Salam, G.A. et al.: Lens-sparing vitrectomy for progressive tractional retinal detachments associated with stage 4A retinopathy of prematurity. Arch Ophthalmol, 122; 2004 : 1816–1818.
10. Prenner, J.L., Capone, A., Jr., Trese, M.T.: Visual outcomes after lens-sparing vitrectomy for stage 4A retinopathy of prematurity. Ophthalmology, 111; 2004 : 2271–2273.
11. Steinkuller, P.G., Du, L., Gilbert, C. et al.: Childhood blindness. J AAPOS, 3; 1999 : 26–32.
12. Shulman, J.P., Hobbs, R., Hartnett, M.E.: Retinopathy of Prematurity: Evolving Concepts in Diagnosis and Management. FocalPoints AAO, Vol. XXXIII, N. 7, Jul 2015.
13. The Committee for the Classification of Retinopathy of Prematurity. An international classification of retinopathy of prematurity. Arch Ophthalmol., 102; 1984 : 1130-4.
14. Taylor, D., Hoyt, C.S.: Pediatric ophthalmology and strabismus, 3rd edn. Edinburgh, Scotland: Elsevier Saunders, 2005.
15. Yu, X., Qi, Z., Xiaoli, K. et al.: Early vitreoretinal surgery on vascularly active stage 4 retinopathy of prematurity through the preoperative intravitreal bevacizumab injection. Acta Ophthalmol., 91; 2013 : 304–310.
Labels
Maxillofacial surgery Ophthalmology
Article was published inCzech and Slovak Ophthalmology

2017 Issue 4-
All articles in this issue
- Nekorigovaná zraková ostrost do blízka po implantaci monofokální IOL
- Léčba keratokonu metodou akcelerovaného cross-linkingu
- Pars plicata vitrektomie u nedonošených novorozenců pro odchlípení sítnice v důsledku retinopatie nedonošených, naše výsledky
- Brownův syndrom: jednotlivé formy a jejich léčba (včetně expanderu vlastní konstrukce)
- In vivo konfokální mikroskopie rohovky: princip metody a současné možnosti
- MOŽNOSTI IN VIVO KONFOKÁLNÍ MIKROSKOPIE NERVOVÝCH VLÁKEN ROHOVKY U DIABETIKŮ
- Czech and Slovak Ophthalmology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Brownův syndrom: jednotlivé formy a jejich léčba (včetně expanderu vlastní konstrukce)
- Léčba keratokonu metodou akcelerovaného cross-linkingu
- Nekorigovaná zraková ostrost do blízka po implantaci monofokální IOL
- In vivo konfokální mikroskopie rohovky: princip metody a současné možnosti
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career


