Verteporfin s ranibizumabem u neovaskulární makulární degenerace
:
P. Souček; I. Součková
:
Oftalmologická klinika FNKV, Praha, přednosta prof. MUDr. Pavel Kuchynka, CSc.
:
Čes. a slov. Oftal., 64, 2008, No. 4, p. 135-140
Cíl:
Cílem práce je zhodnotit bezpečnost a účinnost ranibizumabu intravitreálně (RIV) a fotodynamické terapie s verteporfinem (FTV) u neovaskulární makulární degenerace.
Metodika:
Soubor tvoří 10 očí 10 pacientů, z nichž ve 2 případech (20 %) se jednalo o nově diagnostikovanou idiopatickou choroidální neovaskularizací a 8 jedinců (80 %), již podstoupilo minimálně jedno sezení FTV pro věkem podmíněnou makulární degeneraci. FTV byla provedena standardním způsobem. Druhý až čtvrtý den poté byl aplikován RIV v dávce 0,5 mg. Před léčbou a každý další měsíc bylo provedeno komplexní celkové a oční vyšetření včetně vizu na ETDRS (Early Treatment Diabetic Retinopathy Study) optotypech, biomikroskopie a OCT („Optical Coherence Tomography“). Fluorescenční angiografie (FAG) byla provedena před léčbou a 3 měsíce poté (k vyloučení prosakování léze, které by bylo indikací k následnému sezení FTV). Kritérii k rozhodnutí o dalšímu postupu (týkající se event. nutnosti opakování RIV) byl vizus, který nesměl klesnout více než o 1 řádek optotypů, centrální tloušťka sítnice (CTS) dle OCT, jejíž hodnota se nesměla zvýšit o více než 100 μm a vyloučení nálezu nových hemoragií na fundu. Tato metodika je nazývána PRN („pro re nata“, tj. podle potřeby). Průměrné hodnoty před léčbou u vizu byly 0,3, u CTS 228 μm a u objemu makuly 6,79 mm³. Průměrná sledovací doba byla 3,5 měsíce.
Výsledky:
Během žádné z kontrolních návštěv (n = 35) nedošlo k poklesu vizu či nárůstu CTS nad povolené rozdíly hodnot. Nezaznamenali jsme ani vznik nových hemoragií na fundu či prosakování ani na jedné z kontrolních FAG (n = 10). U všech nemocných (100 %) tak bylo provedeno pouze jedno sezení FTV/RIV. Při poslední kontrole se vizus nezměnil nebo zlepšil až o 7 řádků ETDRS optotypů průměrně na 0,5 (zlepšení o 13,5 písmene). Hodnota CTS při poslední kontrole klesla průměrně na 198 μm a makulárního objemu na 6,33 mm³. U žádného pacienta (0 %) jsme nezaznamenali závažné oční či celkové komplikace.
Závěr:
Velmi nadějné první výsledky metody FTV/RIV podložené zlepšením vizu o 13,5 písmene po jednom sezení a nulovým množstvím závažných komplikací při současném snížení organizační a finanční zátěže bychom v budoucnu chtěli potvrdit rozšířením našeho souboru a prodloužením sledovací doby pacientů. Teprve poté bude možné určit zda se FTV/RIV stane v léčbě neovaskulární makulární degenerace metodou volby.
Klíčová slova:
verteporfin, ranibizumab, neovaskulární makulární degenerace, choroidální neovaskularizace, optická koherentní tomografie, fluorescenční angiografie
Úvod
Fotodynamická terapie s verteporfinem (FTV) (Visudyne, Novartis Europharm Limited, Velká Británie) statisticky významně zpomaluje pokles vizu u pacientů se subfoveolárně uloženou převážně klasickou choroidální neovaskularizací (CHNV) u různých forem makulární degenerace. Její efekt je založen na selektivním vazookluzivním účinku. Dlouhodobé výsledky FTV byly publikovány i v domácí literatuře (15).
Podávání ranibizumabu (fragmentu humanizované monoklonální protilátky vaskulárního endoteliálního růstového faktoru – VEGF) (Lucentis, Novartis Europharm Limited, Velká Británie) ve studii ANCHOR zajistilo stabilizaci nebo zlepšení vizu u 78 % jedinců, kdy byl tento anti-angiogenní preparát aplikován intravitreálně v měsíčních intervalech po dobu dvou let (2). Studie se účastnilo i Specializované centrum pro léčbu věkem podmíněné makulární degenerace (VPMD) Fakultní nemocnice Královské Vinohrady v Praze. Jak se po odtajnění druhu terapie ukázalo, byl jeden pacient léčen pomocí ranibizumabu intravitreálně (RIV) v dávce 0,5 mg. Tento pacient má vizus 4/20, nález v makule je stabilizovaný bez nutnosti doplňkové léčby po dobu dalších 18 měsíců od ukončení studie (obr. 1, 2 a 3).
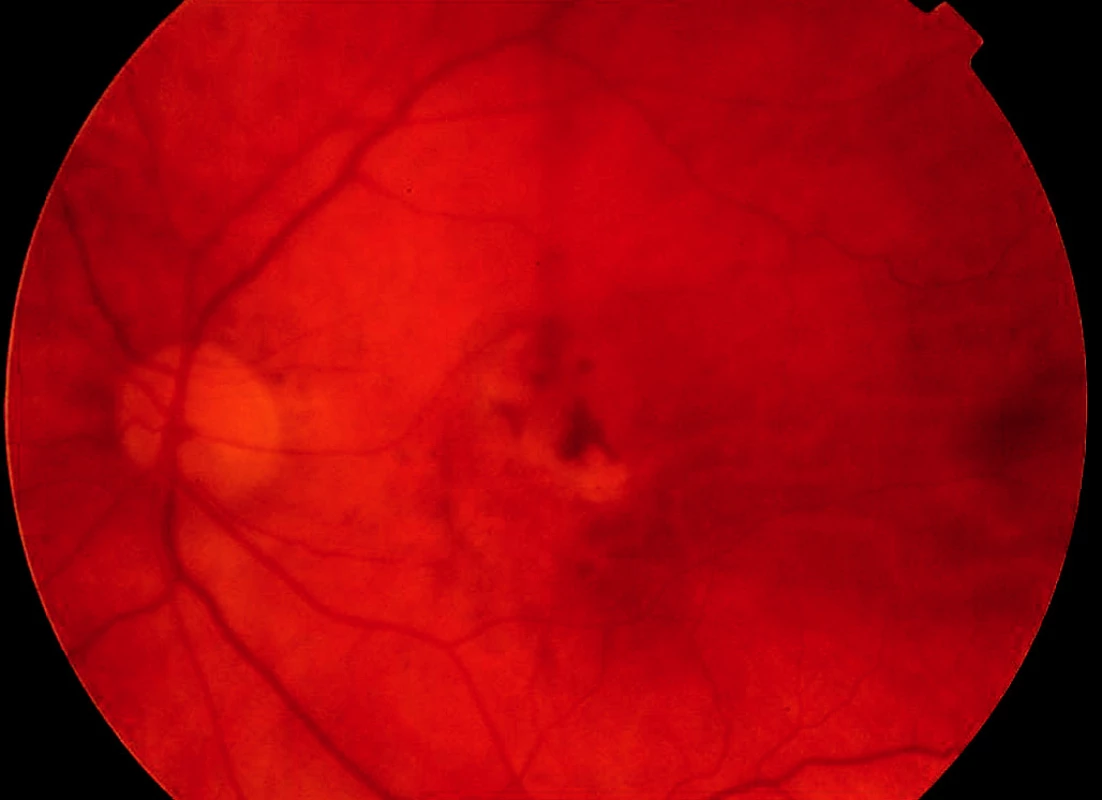
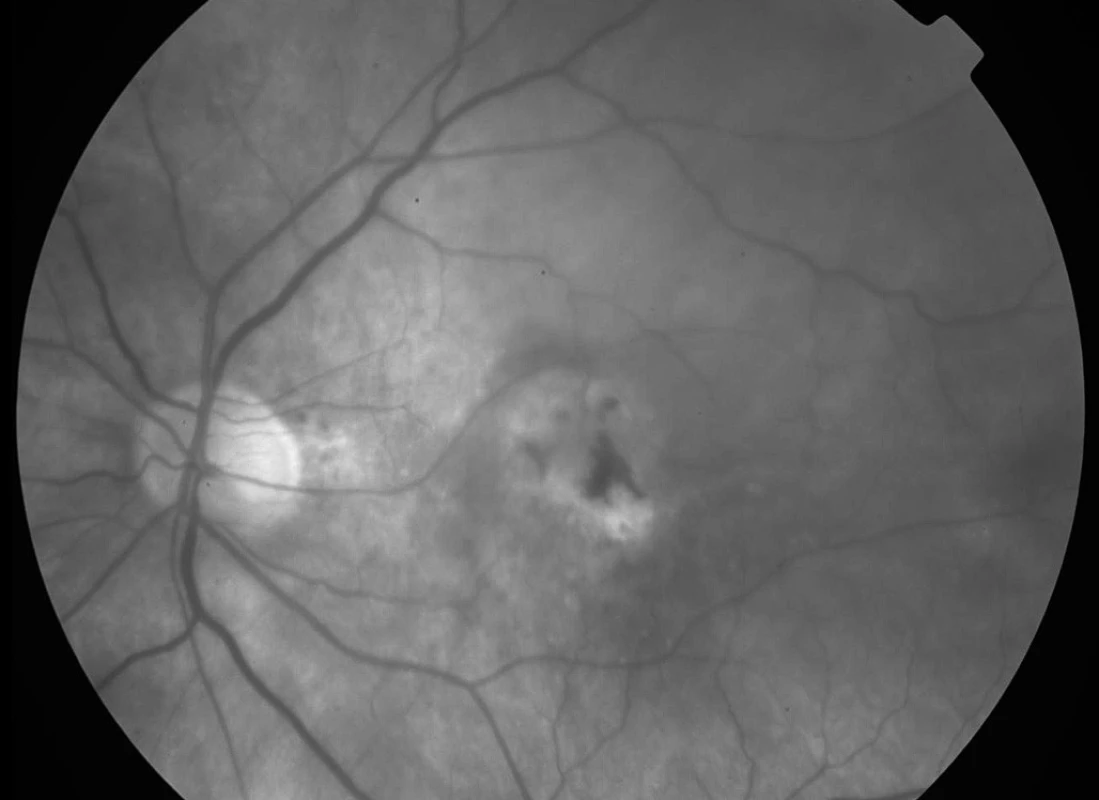
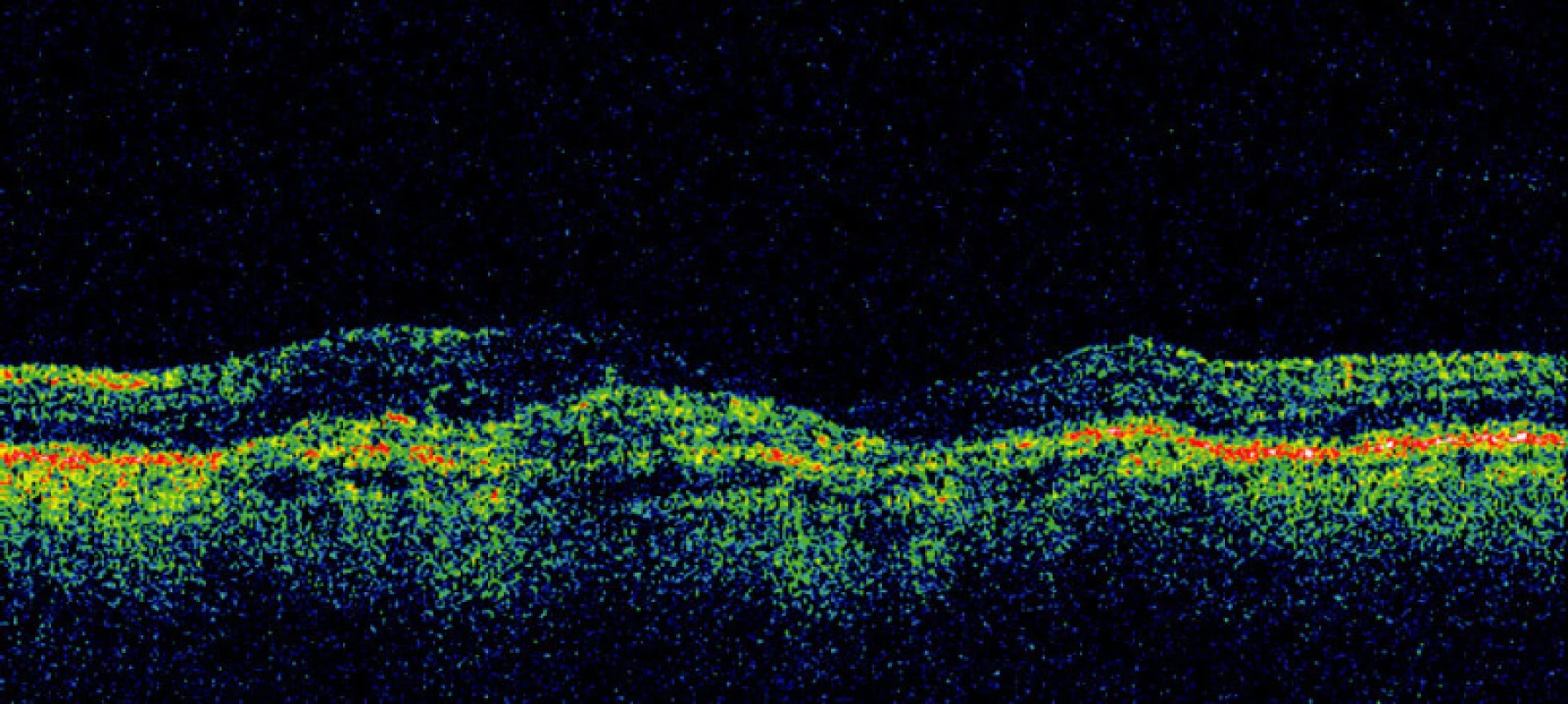
Účinnost a bezpečnost FTV i RIV byla ověřena na nejvyšší úrovni medicíny založené na důkazech, tj. pomocí řady randomizovaných kontrolovaných dvojitě maskovaných klinických studií fáze III (19, 21).
Z výše uvedeného se jeví v léčbě neovaskulární makulární degenerace jako vhodné synergické spojení mechanismů účinků obou léčiv. Navíc by se tímto způsobem mohla snížit frekvence léčebných sezení (v ideálním případě na jedno) při zachování funkčních výsledků monoterapie RIV (4).
Do února 2008 si ranibizumab pořídilo 15 našich nemocných indikovaných k FTV.
Výsledky FTV/RIV u pilotní skupiny prvních 10 z nich prezentujeme v této práci.
Metodika
Soubor tvoří 10 očí 10 nemocných s neovaskulární makulární degenerací ve věku od 35 do 80 let (průměr 62 roky). Pět z nich bylo žen (50 %) a pět mužů (50 %). U všech byla prosakující subfoveolárně lokalizovaná CHNV potvrzena na fluorescenční angiografii (FAG). Ve dvou případech se jednalo o nově diagnostikovanou idiopatickou klasickou CHNV (20 %), 8 jedinců již podstoupilo 3 měsíce předtím minimálně jedno sezení FTV pro VPMD (80 %). Interní vyšetření neprokázalo u žádného pacienta dekompenzovanou arteriální hypertenzi, nestabilní anginu pectoris či jiné závažné akutní onemocnění. Léčba byla provedena do jednoho týdne od FAG a nemocní byli vyšetřeni dříve popsaným způsobem na OCT (Stratus OCT, Zeiss) („Optical Coherence Tomography“) (3), kdy byl zároveň vydán recept na lokální terapii ofloxacinem 5krát denně.
Po zjištění nejlépe korigovatelného vizu a nálezu na předním segmentu byl změřen nitrooční tlak, pulz (v rozmezí 50–120/min), tlak (systolický v rozmezí 90–180 mm Hg, diastolický v rozmezí 50–105 mm Hg), váha a výška. Poté, co nemocní podepsali informovaný souhlas, byli vyšetřeni v arteficiální mydriáze na štěrbinové lampě a biomikroskopicky. FTV byla provedena standardním způsobem (16, 17). Jeden až tři dny (průměr 2 dny) poté byl za aseptických podmínek na operačním sále aplikován RIV 0,5 mg v 0,05 ml roztoku transkonjunktiválně pomocí jehly 30G. K dezinfekci operačního pole byl použit běžným způsobem jód povidon, k lokální anestezii oxybuprocain, dále byl aplikován ofloxacin a subkonjunktivální injekce 2% lidocainu. Na konci zákroku jsme nález verifikovali pomocí indirektní oftalmoskopie, opět byl použit ofloxacin a sterilní krytí.
Operace proběhla ambulantně za monitorování vitálních funkcí. Antibiotika pacient používal po dobu následujících 3 dnů a byl poučen o příznacích komplikací, které měl možnost v případě potřeby kdykoliv konzultovat telefonicky. Další kontroly proběhly po 1 a 2 měsících stejným způsobem kromě FAG. Kritériem k rozhodnutí o dalšímu postupu (týkající event. nutnosti dalšího sezení) byl vizus, který nesměl klesnout více než o 1 řádek ETDRS (Early Treatment Diabetic Retinopathy Study) optotypů, centrální tloušťka sítnice (CTS) dle OCT, jejíž hodnota se nesměla zvýšit o více než 100 μm a vyloučení nálezu nových hemoragií na fundu. Kontrolní FAG byla provedena 3. měsíc po operaci a dále byli nemocní zváni opět v měsíčních intervalech. Tolerance maximální odchylky pro pulz byla 15/min, pro systolický tlak 20, pro diastolický tlak 15 mm Hg a pro hmotnost 7 %.
Vstupní vizus byl 0,05 až 0,78 (průměrně 0,31) (graf 1), vizus 4/8 a lepší měli čtyři pacienti (40 %), vizus 4/40 a horší také čtyři nemocní (40 %). Hodnoty CTS byly 135 až 366 μm (průměrně 228 μm) (graf 2) a objem makuly dle OCT 5,96 až 7,93 mm3 (průměrně 6,79 mm3) (graf 3). Sledovací doba činila u pěti pacientů (50 %) 4 měsíce, u ostatních pěti (50 %) tři měsíce (průměr 3,5 měsíce).



Výsledky
Během žádné z kontrolních návštěv (n = 35) nedošlo k poklesu vizu či nárůstu CTS nad povolené rozdíly hodnot (Obr. 4, 5, 6 a 7). Nezaznamenali jsme ani vznik nových hemoragií na fundu či prosakování na kontrolní FAG (n = 10) (obr. 8, 9, 10, 11, 12 a 13). U všech nemocných (100 %) tak bylo provedeno pouze jedno sezení FTV/RIV.
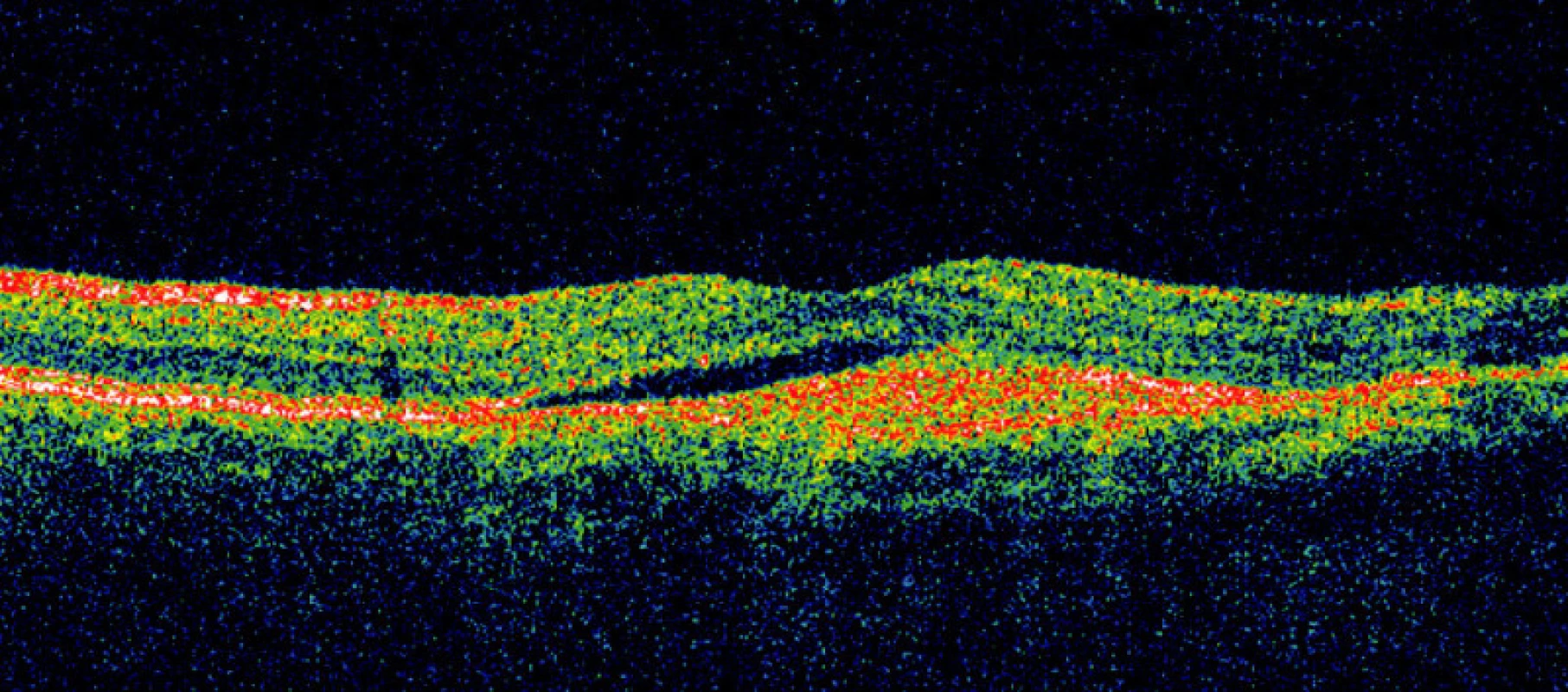
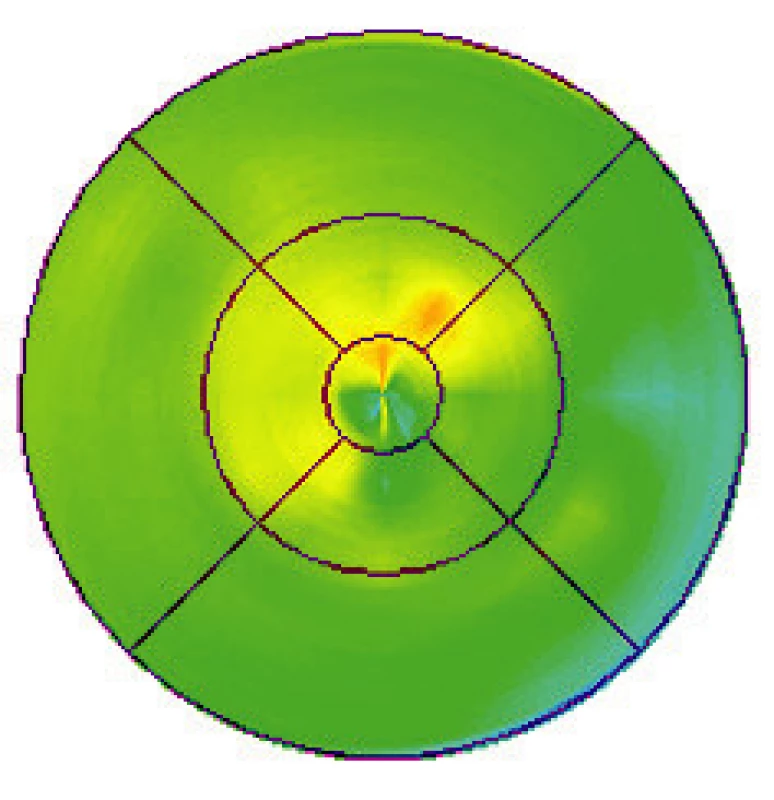
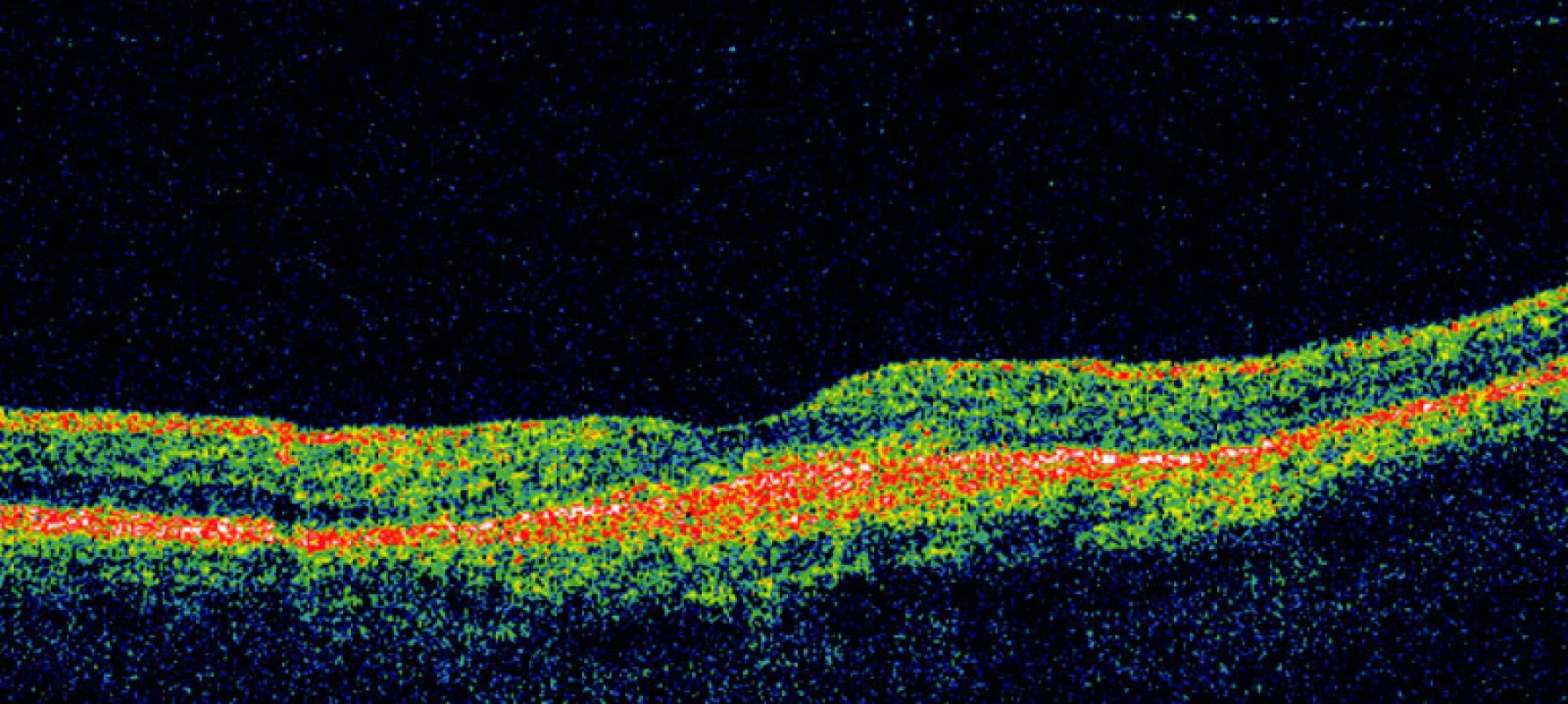
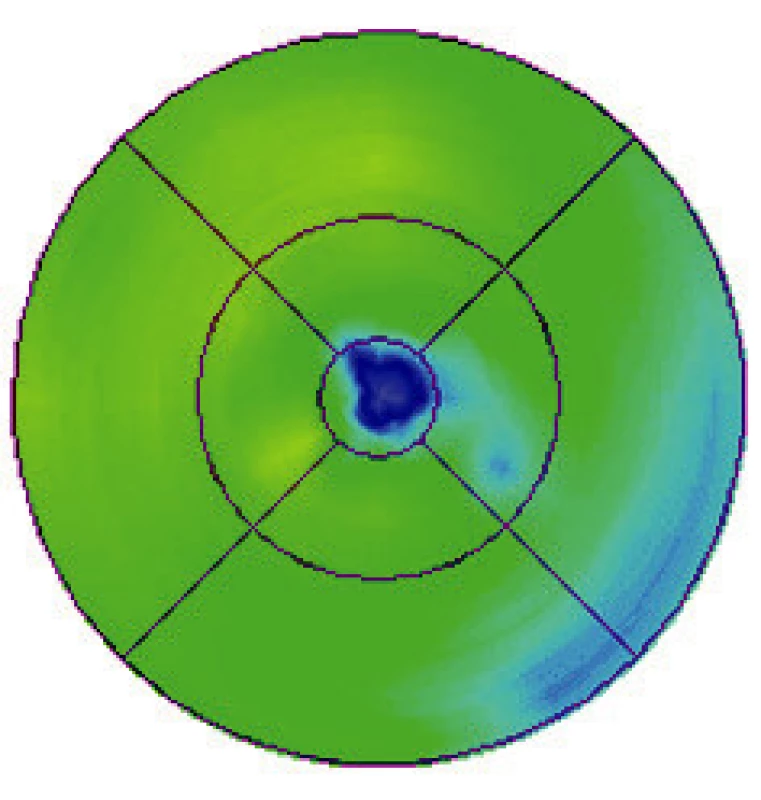
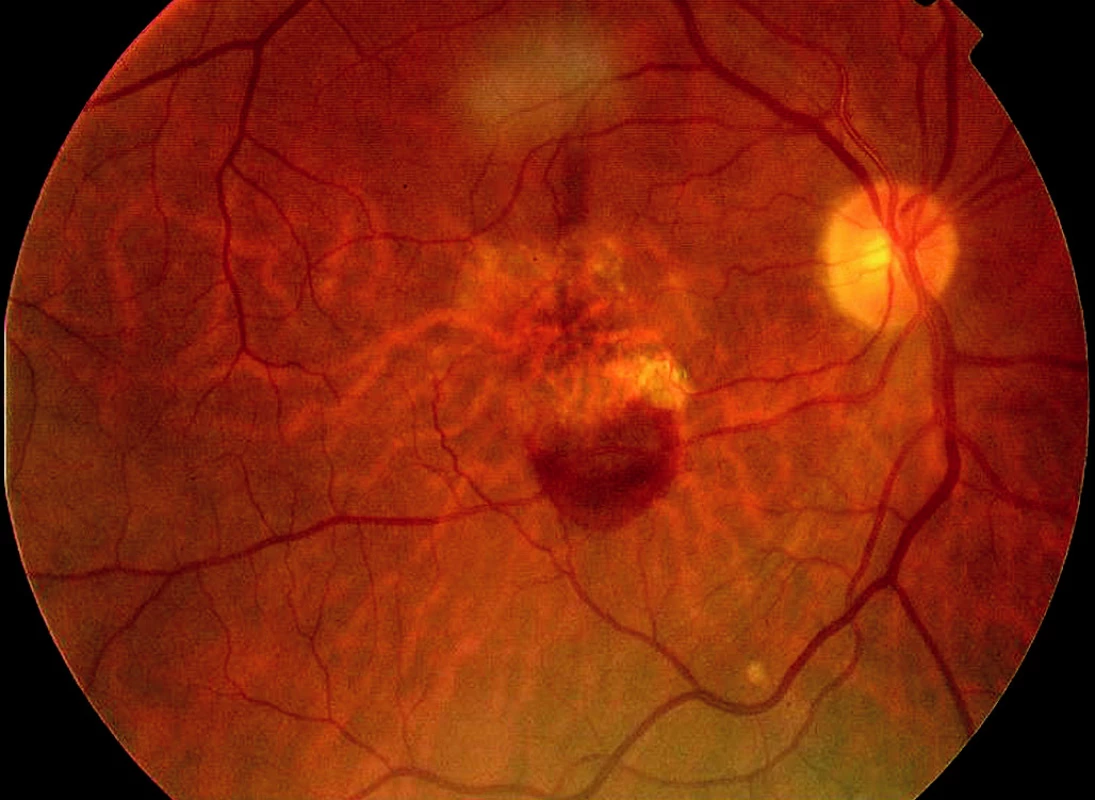
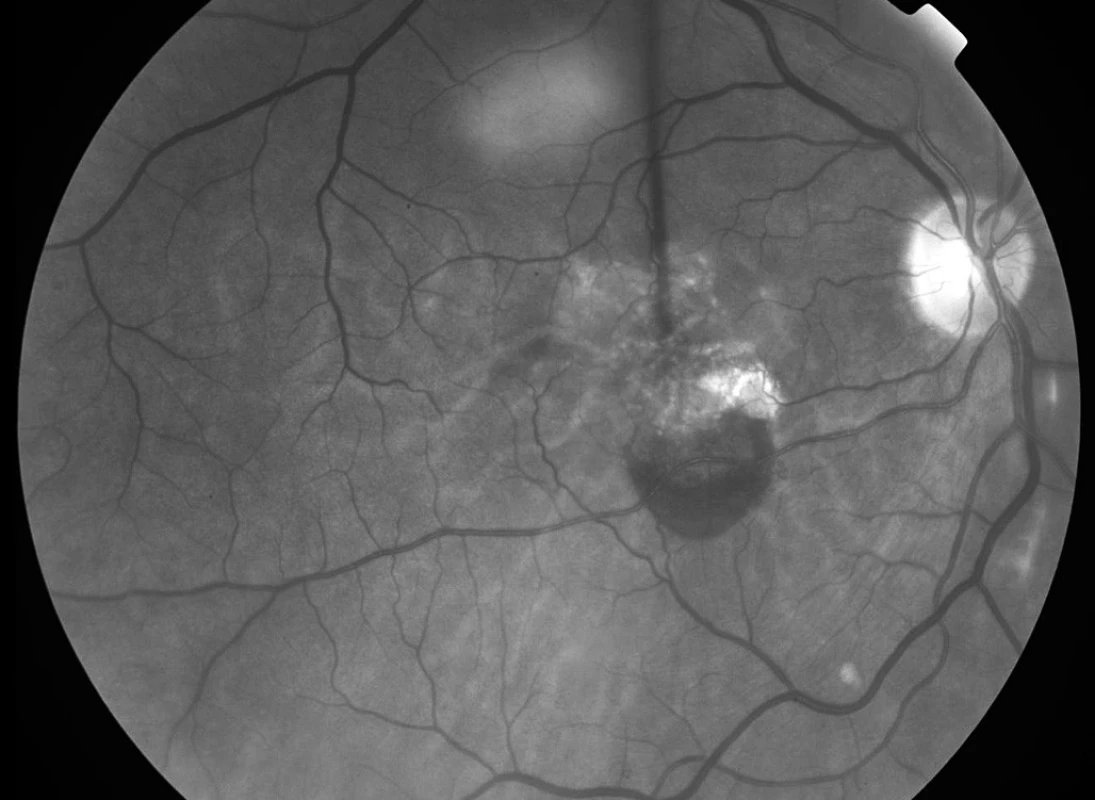
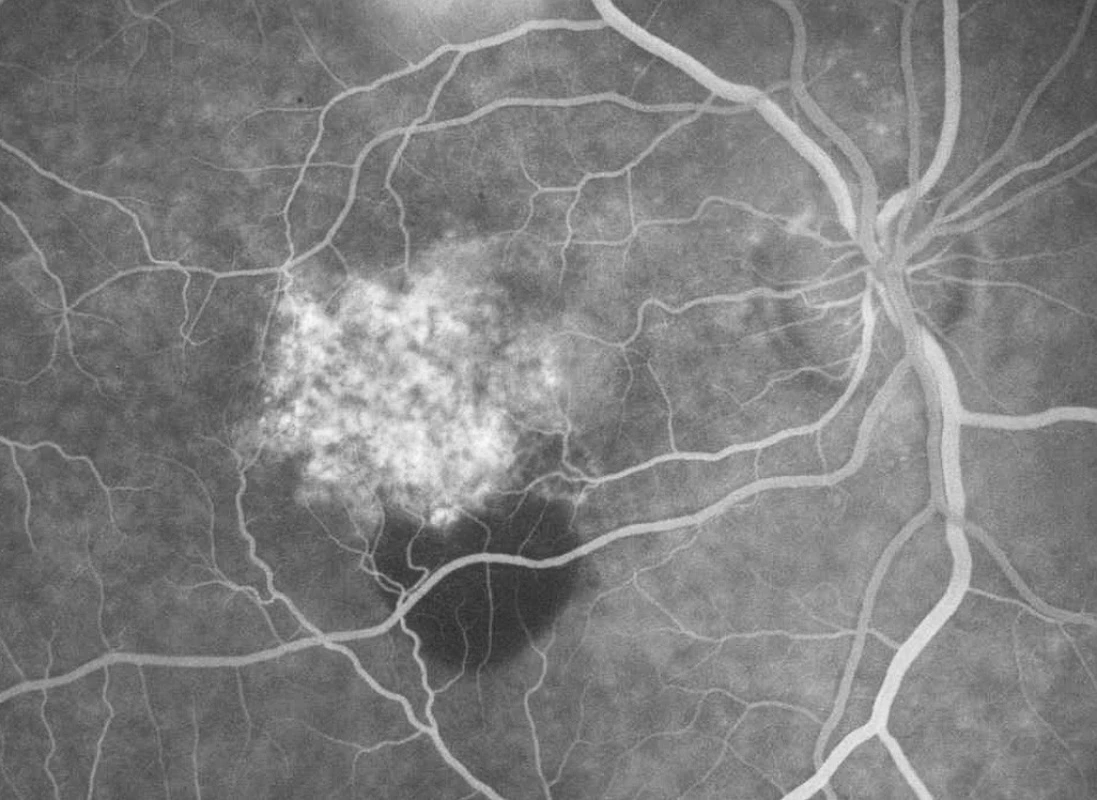
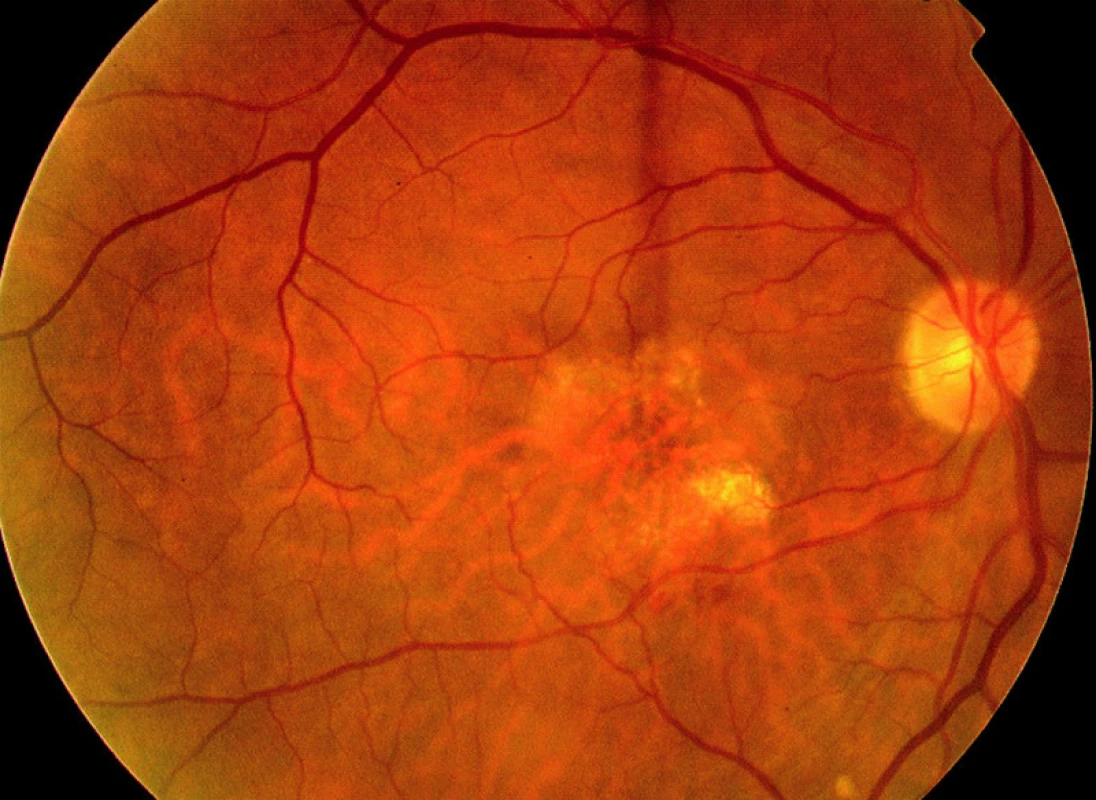
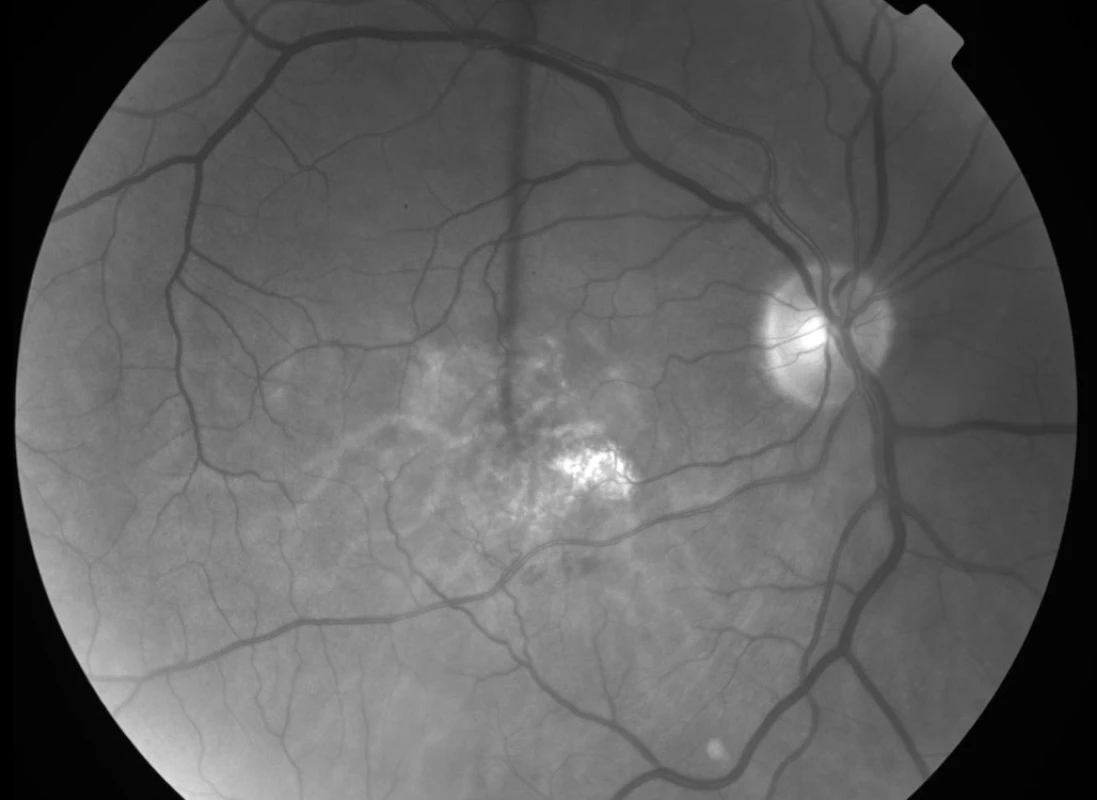
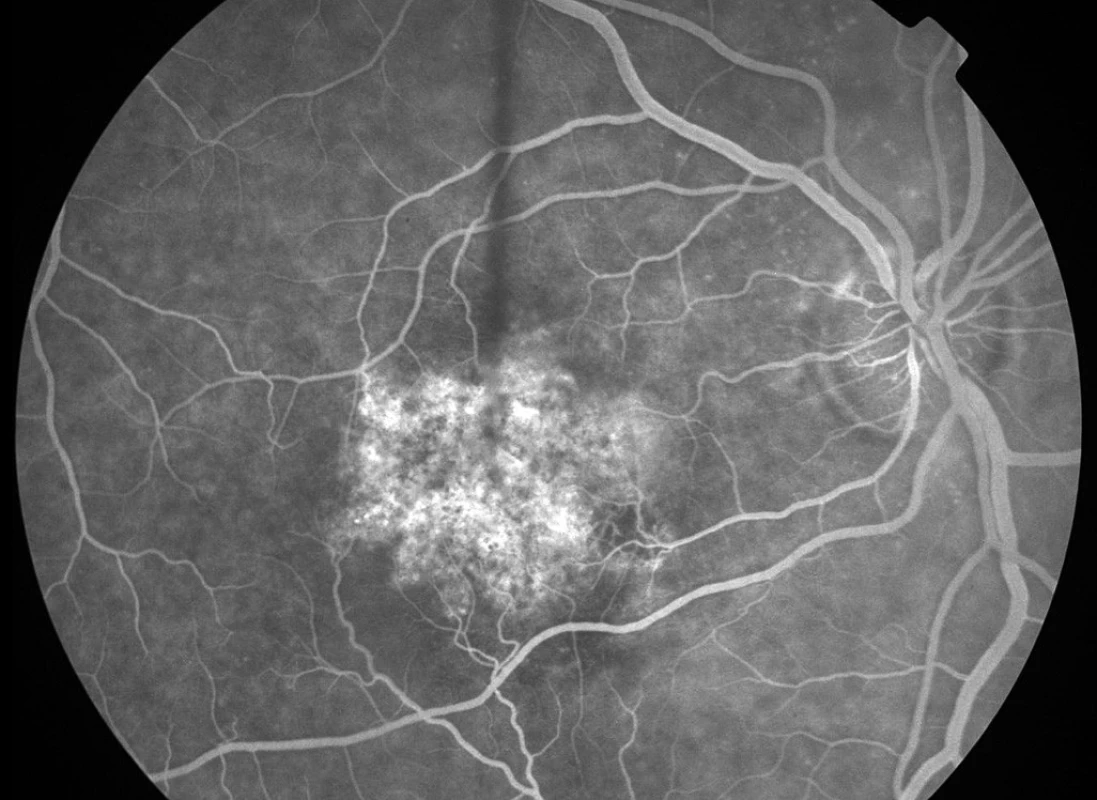
Při poslední kontrole se vizus nezměnil nebo zlepšil až o sedm řádků ETDRS optotypů (průměrné zlepšení o 13,5 písmene) na 0,1 až 1,33 (průměrně na 0,50, viz graf 1). Ke zlepšení o tři a více řádků došlo u pěti (50 %) jedinců. Ke zhoršení vizu nedošlo u žádného pacienta (0 %). Vizus 4/8 a lepší mělo šest (60 %) nemocných a vizus 4/40 jeden pacient (10 %). CTS při poslední kontrole byla od 130 do 301 μm (průměrně 198 μm, viz graf 2). U 9 očí (90 %) došlo k poklesu CTS o 5 až 128 μm, v 1 případě (10 %) k nárůstu o 25 μm (průměrně došlo k poklesu o 30 μm). Makulární objem při poslední kontrole byl 5,25 až 7,23 mm3 (průměrně 6,33 mm3, viz graf 3). U všech očí (100 %) došlo k poklesu objemu makuly, a to od 0,07 do 1,37 mm3 (průměrně o 0,46 mm3).
U žádného pacienta (0 %) jsme nezaznamenali závažné oční či celkové komplikace (včetně změn vitálních funkcí nad povolenou mez).
Diskuse
V současné literatuře najdeme úvahy varující před vysokými náklady na léčbu a upozorňující na nedostatečné kapacity ošetřujících oftalmologů, což vede k diskuzi o použití metod, jejichž bezpečnost není dostatečně prověřena klinickými studiemi (9, 13).
V našem souboru se vizus po jednom sezení FTV/RIV zlepšil průměrně z 0,3 na 0,5 (průměrně o 13,5 písmene ETDRS optotypů). Ke zlepšení o 3 a více řádků došlo u 50 % jedinců. Počet pacientů s vizem 4/8 a lepším se během sledovací doby 3,5 měsíců zvýšil o 20 % a těch, kteří měli vizus 4/40 a horší, klesl o 30 %. Ke zhoršení vizu nedošlo u žádného pacienta (0 %), stejně tak jsme nezaznamenali závažné oční či celkové komplikace (0 %).
Ve studii ANCHOR se průměrný vizus u stejné terapeutické dávky ranibizumabu zlepšil o 11,3 písmene ETDRS optotypů po jednom roce při opakovaných aplikacích v měsíčních intervalech. O tři a více řádků se zlepšil u 40 % pacientů. Vizus 4/40 nebo horší mělo při poslední kontrole 16 % ve srovnání s 23 % jedinců před léčbou. Závažné oční komplikace (tj. odchlípení sítnice, uveitida nebo hemoftalmus) byly pozorovány u méně než 1,5 % případů. Riziko endoftalmitidy bylo menší než 0,1 % na 1 injekci. Celkové cévní komplikace nebyly častější než u srovnatelné populace (2).
Studie Univerzitní oční kliniky Západní Virginie v USA na 18 očích s identickou metodikou jako v našem souboru prokázala průměrný celkový počet FTV 1x/RIV 3,1x na pacienta ročně s průměrným intervalem mezi nimi 25 týdnů. Vizus lepší než 4/8 mělo při 6měsíční kontrole 44 % nemocných (7).
Průměrné hodnoty v našem souboru byly při poslední kontrole u CTS 198 μm s poklesem o 30 μm a u makulárního objemu 6,33 mm3 s poklesem o 0,46 mm3.
Odpovídající hodnoty v literatuře jsou: 204–232 μm pro CTS (po 3 měsících ve studii PrONTO, resp. po 9 měsících ve studii PROTECT, viz dále) (6, 22) a 6,69 mm3 pro makulární objem (30 ± 14 dní po RIV) (14).
Je známo, že průměrný počet sezení monoterapie FTV během 5 let je 7,5 (20).
Ještě častější (měsíční) aplikace RIV, jejíž funkční výsledky jsou však lepší, je pro pacienty nepřijatelná a v praxi z mnoha důvodů nerealizovatelná.
Retrospektivní analýza výsledků studie ANCHOR ukázala, že největšího zlepšení vizu je dosaženo po prvních 3 dávkách RIV (8,7 + 1,3 + 0,2 písmena) (8). Tento bifázický efekt vedl ke změně designu ve studii PIER, kdy po úvodních 3 dávkách následovaly aplikace fixně ve 3měsíčních intervalech (12).
K další úpravě došlo poté, co investigátoři zjistili, že odpověď na terapii není u všech pacientů stejná, a proto ve studii SUSTAIN byla terapie od 3. měsíce indikována pouze při poklesu vizu či změně nálezu na OCT (11). Využitím tohoto individualizovaného dávkování podle potřeby, nazývaném též „pro re nata“ (PRN), studie PrONTO prokázala, že k udržení funkčního efektu srovnatelným s dřívějšími výsledky postačí průměrně 5,5 dávek ranibizumabu na pacienta ročně (6).
Na zvířecím modelu bylo prokázáno, že anti-VEGF léčba provedená společně s fotodynamickou terapií vede ke zpomalení reperfuze uzavřených cév, a to ve větším měřítku než u obou metod samostatně (23), bezpečnost FTV/RIV byla ověřena na primátech (10) a dlouhodobé výsledky zkoumá studie SUMMIT, kde je aplikace uvedených preparátů nahrazena metodikou PRN (5).
Závěry studie PROTECT již synergické spojení mechanismů účinků obou léčiv potvrdily. Po úvodní sérii (FTV 1x/RIV 3x) se snížila frekvence FTV na 0,5 na pacienta ročně (22). RIV totiž navíc kompenzuje nadprodukci VEGF indukovanou stabilním proteinovým komplexem HiF-1 při navozené tkáňové hypoxii jako vedlejšího účinku FTV. Podobný efekt jsme pozorovali u FTV/intravitreálně triamcinolon acetát (IVTA) (18). Vzhledem k možným komplikacím (glaukom, katarakta, neinfekční endoftalmitida) a relativní dostupnosti ranibizumabu od této metody dnes ustupujeme. Aplikaci IVTA rezervujeme jako doplněk pro potlačení zánětlivé složky v rámci komplexní léčby VPMD (1).
Naše výsledky odpovídají údajům publikovaným v zahraničí.
Závěr
Velmi nadějné první výsledky metody FTV/RIV podložené zlepšením o 13,5 písmene po jednom sezení a nulovým množstvím závažných komplikací při současném snížení organizační a finanční zátěže bychom v budoucnu chtěli potvrdit rozšířením našeho souboru a prodloužením sledovací doby pacientů. Teprve poté bude možné určit, zda se FTV/RIV stane v léčbě neovaskulární makulární degenerace metodou volby.
Doc. MUDr. Petr Souček, Ph.D.
Počernická 40
108 00 Praha
www.petrsoucek.eu
e-mail: info@petrsoucek.eu
Sources
1. Augustin, AJ., Offerman, I.: Combination therapy for choroidal neovascularization, Drugs Aging, 24, 2007: 979–990
2. Brown, DM., Kaiser, PK., Michels, M. et al.: Ranibizumab versus verteporfin for neovascular age-related macular degeneration, N Engl J Med, 355, 2006: 1432-1444
3. Cihelková, I., Souček, P.: Nálezy na optické koherentní tomografii u pacientů s makulární degenerací léčených pomocí fotodynamické terapie s preparátem Visudyne. Čes. a slov. Oftal, 59, 2003: 250–256
4. Cihelková, I., Souček, P.: Atlas makulárních chorob/Atlas of macular diseases, Praha, Galén/Karolinum, 2005, 521 s.
5. DENALI Study Group: SUMMIT: Combination Therapy With Verteporfin PDT and Ranibizumab for Subfoveal Choroidal Neovascularization Due to AMD, Invest Ophthalmol Vis Sci, 48, 2007: ARVO E-Abstract 1817
6. Fung, AE., Lalwani, GA., Rosenfeld, PJ. et al.: An Optical Coherence Tomography-Guided, Variable Dosing Regiment with Intravitreal Ranibizumab (Lucentis) for Neovascular Age-related Macular Degeneration, Am J Ophthalmol, 143, 2007: 566–583
7. Jabbour, NM., Odom, JV.: Comparison of Treatment Using Intravitreal Ranibizumab Alone With Combination Treatment Using Intravitreal Ranibizumab and Verteporfin Photodynamic Therapy in Neovascular Age-Related Macular Degeneration, , 2008: poster 560/A528
8. Kaiser, PK., Brown, DM., Zhang, K. et al.: Ranibizumab for Predominantly Classic Neovascular Age-related Macular Degeneration: Subgroup Analysis of First-year ANCHOR Results, Am J Ophthalmol, 144, 2007: 850–857
9. Karel I.: Možnosti a ekonomické ukazatele léčby exsudativní věkem podmíněné makulární degenerace s choroidální neovaskulární membranous, Čes. a slov. Oftal, 63, 2007: 311‑319
10. Kim, IK., Husain, D., Michaud, N.: Effect of Intravitreal Injection of Ranibizumab in Combination with Verteporfin PDT on Normal Primate Retina and Choroid, Invest Ophthalmol Vis Sci, 47, 2006: 357-363
11. Meyer, CH., Eter, N., Holz, FG.: Ranibizumab in Patients With Subfoveal Choroidal Neovascularization Secondary to Age-Related Macular Degeneration. Interim Results From the SUSTAIN Trial, , 2008: poster 273/A582
12. Regillo, CD., Brown, DM., Abraham, P. et al.: Randomized, Double Maskér, Sham-Controlled Trial of Ranibizumab for Neovascular Age-related Macular Degeneration: PIER Study Year 1, Am J Ophthalmol, 145, 2008: 239-248
13. Schmidt-Erfurth, UM., Richard, G., Augustin, A. et al.: Guidance for the treatment of neovacular age-related macular degeneration, Acta Ophthalmol Scand, 85, 2007: 486-494
14. Shah, AR., Del Priore, LV.: Duration of Action of Intravitreal Ranibizumab and Bevacizumab in Exudative AMD Based on Macular Volume Measurements, , 2008: poster 305/D626
15. Souček, P., Boguzsaková, J., Cihelková, I.: Fotodynamická terapie s preparátem Visudyne u makulární degenerace se subfoveolárně uloženou převážně klasickou choroidální neovaskularizací, Čes a Slov Oftal, 58, 2002: 89-97
16. Souček, P., Cihelková, I.: Treatment of macular degeneration, a controlled case, Neuroendocrinol Lett, 23, 2002: 370-372
17. Souček, P., Cihelková, I.: Photodynamic therapy with verteporfin in predominantly classic subfoveal CNV in age-related and myopic macular degeneration. In Ioseliani (Ed.), Focus on Macular Degeneration Research, New York, Nova Publishers, 2004, p. 241-252
18. Souček, P., Cihelková, I.: Fotodynamická terapie s verteporfinem u převážně klasické subfoveolární choroidální neovaskularizace – řešení akutních forem makulární degenerace. In Rozsíval, P. (Ed.), Trendy soudobé oftalmologie, III. svazek, Praha, Galén, 2006, s. 197-217
19. Souček, P., Cihelková I.: Fotodynamická terapie v éře anti-VEGF, Farmakoterapie, 3, 2007: 523-527
20. Treatment of Age-related Macular Degeneration with Photodynamic Therapy (TAP) Study Group: Verteporfin therapy of subfoveal choroidal neovascularization in age-related macular degeneration: 5-year results of two randomized clnical trials with an open-label extension – TAP Report No. 8, Graefes Arch Clin Exp Ophthalmol, 244, 2006: 1132-1142
21. Virgili, G., Do, DV., Bressler, NM. et al.: New therapies for neovascular age-related macular degeneration: critical appraisal of the current evidence, Acta Ophthalmol Scand, 85, 2007: 6-20
22. Wolf, S.: Nine Month Exploratory Endpoint Results From an Open-Label, Multicenter, Phase II Study of Same-Day Verteporfin and Ranibizumab 0.5mg (PROTECT Study), as Measured Using Optical Coherence Tomography, Fundus Photography and Fluorescein Angiography, Invest Ophthalmol Vis Sci, 48, 2007: ARVO E-Abstract 2871
23. Zuluaga, MF., Mailhos, C., Robinson, G. et al.: Synergies of VEGF Inhibition and Photodynamic Therapy in the Treatment of Age-Related Macular degeneration, Invest Ophthalmol Vis Sci, 48, 2007: 1767-1772
Labels
OphthalmologyArticle was published in
Czech and Slovak Ophthalmology

2008 Issue 4
Most read in this issue
- Anterior Transposition or Myectomy of the Inferior Oblique Muscle in Vertical Deviation – Long Term Results
- Immunohistochemical Detection of the Gene p53 and p21 Expression in Cells of the Malignant Melanoma of the Uvea
- Intravitreal Ranibizumab in Combination with Verteporfin Photodynamic Therapy in Neovascular Macular Degeneration
- Visual Functions in Premature Children after Posthemorrhagic Hydrocephalus Surgery
