-
Medical journals
- Career
Cervikální vertigo – fikce či realita?
: Z. Kadaňka Jr.; J. Bednařík
: Neurologická klinika LF MU a FN Brno
: Cesk Slov Neurol N 2018; 81(5): 521-527
: Review Article
prolekare.web.journal.doi_sk: https://doi.org/10.14735/amcsnn2018521Cervikální vertigo je již řadu let značně kontroverzní jednotka, která je však v praxi široce akceptována odbornou veřejností. Podáváme souhrn o současných poznatcích týkající se možné etiologie, diagnostiky a léčby této nozologické jednotky. Cervikální vertigo je značně přediagnostikované, stále neexistuje žádný laboratorní nebo klinický test specifický pro tuto diagnózu a žádná z možných teorií nevysvětluje plně etiologii možných potíží. Léčba je obtížná a spíše empirická.
Klíčová slova:
vertigo – cervikální vertigo – vertebrobazilární insuficience – cervikookulární reflex – vestibulookulární reflex – závratěÚvod
Pocity vertiga a nevolnosti patří mezi 20 nejčastějších příčin návštěv u lékaře v celosvětovém měřítku [1]. Celková prevalence v populaci bývá odhadována na 5 – 10 %, u pacientů nad 50 let na více než 50 % a bývá příčinou až 25 % pádů u pacientů starších 65 let [1]. Zprávy z pracovišť urgentního příjmu v USA z let 1995 – 2004 uvádějí, že vertigo a pocity nevolnosti bývají cca v 2,5 % příčinami akutního vyšetření [2]. Cervikální vertigo je stále považováno za značně kontroverzní a problematickou entitu, která bývá velmi často přediagnostikována, a neurolog musí nezřídka čelit situaci, kdy je nucen odmítnout či potvrdit tuto diagnózu stanovenou jiným lékařem. U většiny pacientů, kteří jsou takto primárně diagnostikováni, se totiž po podrobnějším prošetření nalezne jiná vysvětlující příčina (až v 90 %) [3].
Etiologie vertiga
Pocity nejistoty v prostoru či závratí mají často multifaktoriální a komplikovanou příčinu. V praxi to znamená, že poměrně velké procento závrativých stavů zůstává etiologicky neobjasněno (zejména při absenci detailního vyšetření). Pro udržení správného pocitu tělesné rovnováhy je nezbytná:
- správná prostorová orientace (v klidu i při pohybu),
- neporušená fixace pohledu při pohybech hlavy i celého těla;
- neporušená zpětná vazba mezi svalovým tonem a CNS k udržení správné tělesné postury.
Tyto systémy jsou mezi sebou propojeny velmi složitým způsobem a pocity závratí znamenají dysfunkci ne pouze jednoho, ale celé řady kontrolních mechanizmů současně. Například senzorická dysfunkce u starších lidí – potíže se zrakem (např. katarakta), se sluchem (presbyakuze), ischemické kmenové léze či zhoršená propriocepce (např. polyneuropatie) – se mohou projevovat pocity vertiga či celkové nejistoty. Závrativost též vyvolává silný emoční doprovod – na jedné straně nepříjemné (domnělé či skutečné) pocity nekontrolovaného pádu, na straně druhé pozitivní emoce z pocitů rotací (např. při tanci či turistických a pouťových atrakcích). Vertigo bývá často spojeno s nauzeou a zvracením, což svědčí o těsném vztahu k vegetativním centrům. Pocity vertiga mohou být vyvolány i u jinak zcela zdravého jedince (např. výšková závrať, při rychlé jízdě automobilem apod.). Vertigo bývá často i projevem různých interních onemocnění (arteriální hypotenze a hypertenze, srdeční arytmie, hypoglykemie) nebo psychiatrických onemocnění. Nezřídka se jedná o účinek mnoha užívaných léků [4].
Krční vertigo
Krční páteř jako možný zdroj vertiga byla dlouho v odborné literatuře zcela ignorována. První reference se objevují až v roce 1955 [5]. Již tato pilotní práce s sebou však nese výrazné kontroverze, které jakoby předurčily další osud této nozologické jednotky. Ryan et al totiž popsali kazuistiky pěti pacientů, z nich však čtyři měli velmi pravděpodobně příznaky benigního paroxyzmálního polohového vertiga (BPPV) spolu s radikulární krční symptomatikou (jak bylo zjištěno později), a nazvali je cervikálním vertigem [5]. Někteří autoři tuto jednotku od počátku zcela popírají [3], jiní její existenci hájí [6].
Krční oblast obsahuje několik struktur, které se mohou teoreticky spolupodílet na mechanizmu řízení rovnováhy – krční aferentace ze svalových vřetének, čistě cévní struktury (karotické a vertebrální arterie) a svalové struktury, které se podílejí na udržení správné postury jedince, dále pak karotická tělíska, která se však účastní selektivně v procesu regulace kardiovaskulárního systému.
Pohyby krční páteří jsou za fyziologických podmínek asociovány i s pohybem hlavy, takže pocity vertiga mohou být teoreticky způsobeny porušením vestibulárního, zrakového, cévního či krčního proprioceptivního mechanizmu. Termín cervikální vertigo bývá většinou rezervován pro případy se suspektním porušením proprioceptivní složky [7], někteří však pojem cervikálního vertiga asociují spíše s lézemi nervového systému ve vertebrobazilárním (VB) povodí, což se již jeví poněkud diskutabilní – viz níže. Vestibulární aparát vnitřního ucha detekuje jakýkoli pohyb hlavy v prostoru. Vstupy do vestibulárního systému zahrnují cervikální proprioceptivní aferentaci, zrakové vjemy a informace o korekci plánovaných pohybů z cerebela (do mozečku vstupují tyto motorické povely „jako kopie plánovaných pohybů”, které jsou vysílány z primární motorické kůry) [8]. Všechny tyto vstupy jsou vyhodnocovány vestibulárním nukleárním komplexem, který vydává příkazy k pohybu očí a těla. Tento systém je velmi přesný a je kontrolován a řízen mozečkem – obr. 1.
1. Schéma senzorické integrace.
Fig. 1. Scheme of sensory integration.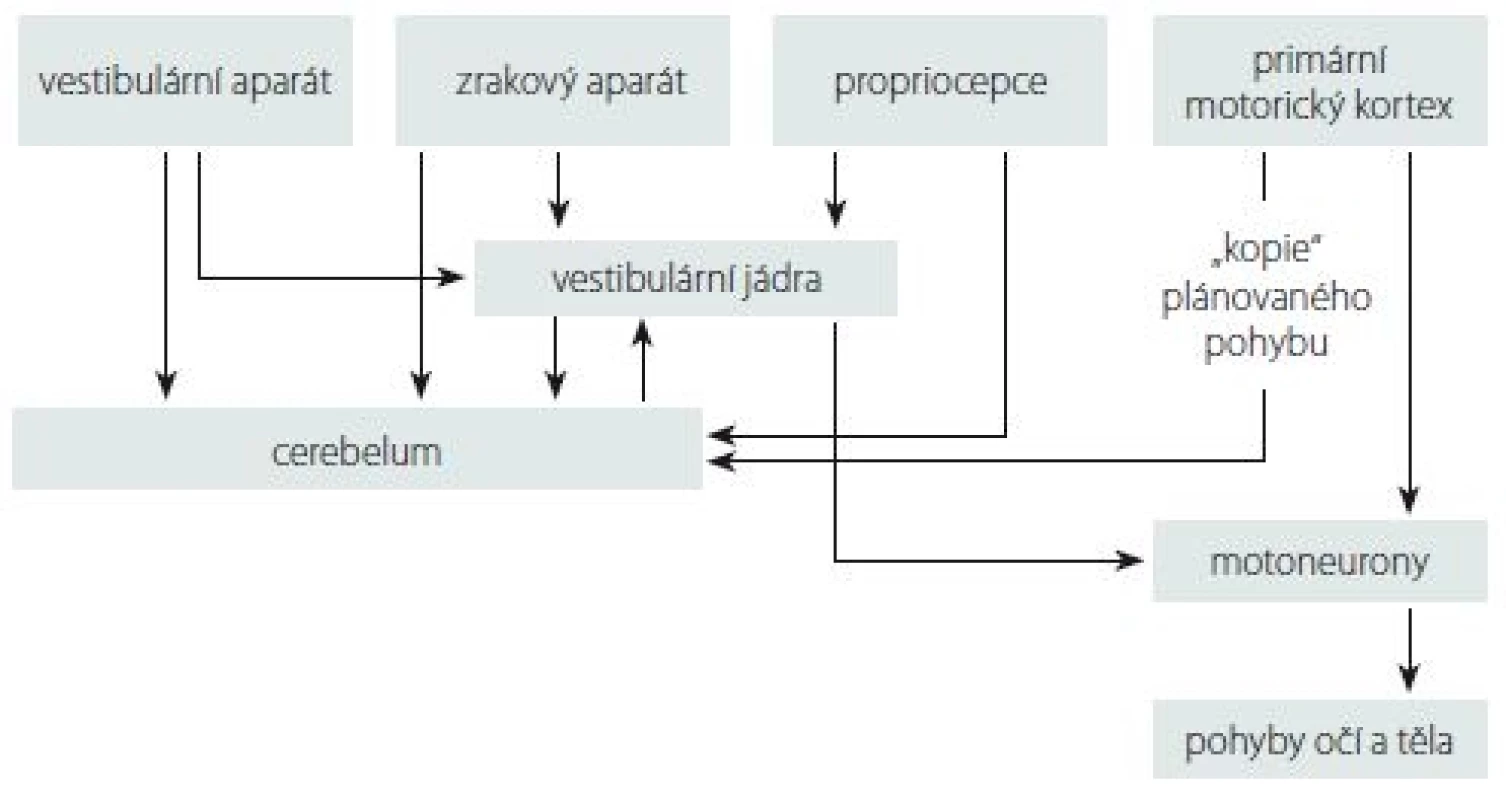
Již prvním problémem je samotná definice cervikálního vertiga. Yahia et al je popisují takto: chronická krční bolest spojená s vertigem po rotaci krční páteře (avšak bez nystagmu) s nálezem krční osteoartritidy a degenerativních změn meziobratlových disků [9]. Furman et al je charakterizují jako neurčitý pocit změny rovnováhy a prostorové orientace, který vzniká abnormální aktivitou krčních aferentních drah [10]. Wristley et al uvádí, že diagnóza cervikálního vertiga závisí na korelujících symptomech nerovnováhy a závratí ve spojitosti s bolestmi krční páteře a při vyloučení jiné vestibulární patologie [11]. Lewit se zmiňuje o tom, že cervikogenní závrať je polymorfní skupina krátce trvajících závratí vyvolaných určitým postavením (pohybem) hlavy proti trupu, při kterém nemocný udává pocit náhlého tahu ke straně, dopředu nebo dozadu s představou, že se musí bránit. Nauzea a zvracení zpravidla chybí [12]. Vidíme tedy, že jednoznačná definice cervikálního vertiga neexistuje, autoři si často pomáhají různými popisnými syndromologickými pojmy a vylučovacími formulacemi, které působí poněkud kostrbatě a komplikovaně.
Teoretické předpoklady možných příčin cervikálního vertiga
V průběhu posledních 60 let se objevila celá řada studií a různých teorií, které měly vysvětlovat možnou příčinu vzniku cervikálního vertiga. U žádné z nich však neexistuje spolehlivý důkaz o její platnosti. Podáváme rozbor těch nejvíce užívaných a citovaných.
Krční aferentace
Cervikální propriocepce je závislá zejména na krátkých hlubokých krčních svalech, které jsou bohatě zásobeny svalovými vřeténky a které hrají důležitou roli v řízení správné tělesné postury [13]. Dle recentně publikovaných údajů se uvažuje i o roli Ruffiniho tělísek, která fungují též jako mechanoreceptory a jejichž zvýšený počet byl nalezen v krčních meziobratlových discích u pacientů s krční spondylózou a vertigem [14]. Krční proprioceptory zprostředkovávají dva typy reflexů – posturální krční reflexy a cervikookulární reflex (COR). Tonické krční reflexy nejvíce studoval Magnus [15]. U lidí jsou výbavné pouze u novorozenců (např. ipsilaterální flexe a kontralaterální extenze končetin spojená s rotací hlavy – tzv. „pozice šermíře“), v průběhu zrání nervového systému však vymizí. COR interferuje s vestibulookulárním reflexem (VOR), jenž se též podílí na stabilizaci hlavy v prostoru [16].
První demonstroval cervikookulární reflex Bárány u králíků [17]. De Jong et al prokázali, že blokováním aferentních cervikálních drah (bez současné vestibulární stimulace) lze vyvolat nystagmus u celé řady zvířat [18]. U lidí je však tento reflex klinicky výbavný pouze u novorozenců [19] či u pacientů s těžkým postižením CNS, event. u pacientů s výrazně porušeným vestibulárním aparátem [20]. Cervikookulární reflex totiž výrazně interferuje s reflexem vestibulookulárním, který jej u zdravého jedince prakticky zcela inhibuje. Abychom vyloučili vliv vestibulárního a zrakového aparátu, musel by být pacient vyšetřen s hlavou fixovanou, v zatemněné místnosti. Byla tak provedena celá řada studií s použitím elektronystagmografie se zaměřením na porovnání výbavnosti COR a VOR. Při těchto experimentálních modelech skutečně došlo u vyšetřovaných jedinců při rotaci trupu k subjektivním pocitům rotace hlavy [21] a i u zdravých (tj. zcela asymptomatických) jedinců se podařilo vybavit COR s nystagmem (reflex byl však velmi potlačen a nystagmus měl pomalou frekvenci) [22]. Pokud však byla hlava fixována pevně či za normálních zrakových podmínek, rotace trupu žádné pocity pohybů hlavy či vertiga nevyvolaly [23]. Dále se zjistilo, že COR je zvýšen u pacientů s nespecifickými bolestmi krční páteře [24], stejně tak u pacientů s omezenými krčními pohyby (blokáda apod.) [25] a u starších jedinců [26] – též ve specifických experimentálních podmínkách odlišných od běžné klinické praxe. Je prokázáno, že COR a VOR fungují jako „spojité nádoby”, že existuje korelace mezi hodnotami VOR a COR, tj. že při útlumu VOR dochází ke zvýšení COR, který tak přebírá jeho funkci [27]. Hluboká stimulace krčních svalů vibrací (tj. aktivace svalových vřetének) způsobuje pocity náklonu hlavy a iluzi pohybujícího se obrazu, přičemž se zjistilo, že ta je zapříčiněna minutovou pomalou fází očních pohybů [23]. De Jong et al dokumentovali, že lokální anestezie hlubokých krčních svalů u člověka vyvolá zvýšený ipsilaterální a snížený kontralaterální tonus extenzorů, což vede k poruchám chůze s tendencí k pádu k umrtvené straně [18]. Nicméně u pacientů, u kterých byla (za fyziologických podmínek) provedena krční blokáda anestetikem v etáži C2, nebyl prokázán žádný nález na elektronystagmografii, statické posturografii, nebyly zaznamenány ani subjektivní pocity pohybu zrakového pole [28]. Brand prokázal, že lze za specifických podmínek (v zatemnělé místnosti) vyvolat nystagmus dokonce i pasivní rotací paže [29], Hinoki et al jej vybavili i prokainizací v lumbální oblasti [30]. Některé studie předpokládají, že za udržení svalového tonu a postury jsou odpovědné zejména proprioceptivní informace z horních tří dorzálních kořenů (C1 – C3) [18]. Hülse zjistil, že 50 % krčních proprioreceptorů se skutečně nachází v kloubních pouzdrech C1 – C3 [31]. Klinicky však bývají nervové kořeny postiženy v drtivé většině ze segmentů kaudálnějších (C5/ 6, C6/ 7), kraniální segmenty bývají postiženy vzácně, což je opět v kontrastu s výše uvedenou hypotézou [32]
Co tedy z výše uvedeného vyplývá? Krční aferentace se zcela prokazatelně podílí na stabilizaci polohy hlavy a trupu, avšak u zdravého jedince (resp. u člověka s nepostiženým periferním vestibulárním aparátem či bez difuzního těžkého postižení CNS) je klinicky výrazně utlumena a v roli „stabilizátora polohy hlavy” dominuje vestibulární ústrojí. Vliv krční aferentace též nelze „separovat” od vlivu vestibulárního či zrakového aparátu a termín cervikální vertigo se nám proto nejeví jako ideální. Vybavení nystagmu ve specifických podmínkách (zatemnělá místnost s fixací hlavy) je fyziologické a jistě není průkazem existence cervikálního vertiga. Propriocepce však nepochází pouze z oblasti krční, ale samozřejmě i z hrudní, bederní a potažmo ze všech končetin. Pokud tedy uznáváme tuto teorii, nebylo by logičtější užívat termín „vertigo proprioceptivní”? Pak se ovšem nabízí otázka, jestli je vertigo proprioceptivní synonymem pro vertigo cervikální. Dle našeho názoru nikoli.
Whiplash injury
Často se v literatuře uvádí, že krční vertigo vzniká následkem úrazu krční páteře: tzv. whiplash injury – jedná se o poranění vzniklé při prudkém a nečekaném pohybu hlavy, zejména vlivem působení velké síly při vnějším nárazu [33]. Nejčastějšími symptomy u těchto pacientů však nejsou závratě, ale bolesti krční páteře, bolesti hlavy, následované zrakovou symptomatikou (rozmazaný vizus), kognitivními a emočními potížemi [34]. Pouze u poloviny pacientů jsou přítomny závratě a poruchy rovnováhy [35]. Nejčastěji zvažovaným mechanizmem, který má vysvětlovat etiologii tohoto posttraumatického vertiga, je porucha koordinace mezi vestibulárním, zrakovým a proprioceptivním vstupem do vestibulárních jader, tedy v podstatě tytéž mechanizmy, které se zvažují v etiologii cervikálního vertiga – viz výše [36]. Významnou roli zde však zcela jistě hrají i psychosociální a forenzní důvody [37] a finanční kompenzace [38]. V případech krčního traumatu je však obtížné odlišit současné postižení vestibulárního labyrintu nebo vestibulárních jader a drah od postižení krční páteře, protože prakticky vždy s traumatem páteře dochází i k traumatu hlavy a možnému postižení rovnovážných center (tj. posttraumatické BPPV, postižení utriculu a sacculu nebo vznik perilymfatické fistuly) [39,40].
Někteří autoři vysvětlují etiologii vertiga u poranění typu whiplash injury VB insuficiencí či posttraumatickou lézí v oblasti mozkového kmene. Endo et al ve své studii (20 pacientů po whiplash injury, 13 zdravých kontrol) prokázali abnormální nález na MRA vertebrálních tepen (okluze, stenóza či redukce průtoku) v 77 % případů v kontrolní (tj. „zdravé“) skupině a v 60 % případů ve skupině pacientů. Zjistili však větší mezistranovou (pravo/ levou) diferenci při měření krevního průtoku ve skupině pacientů (6,1 ± 3,0 cm/ s) v porovnání se skupinou kontrolní (3,5 ± 2,5 cm/ s). Z těchto dat vyvozují postulát, že pacienti s perzistujícím vertigem či nevolností po whiplash injury mají častější příznaky VB insuficience [41].
Co se týče studií funkce mozku, tak ty prokázaly (na funkčním MR a jednofotonové emisní výpočetní tomografii [SPECT]) reflexní hypoperfuzi a hypometabolizmus u pacientů s whiplash injury v různých oblastech (frontální, temporální lalok, inzula, bazální ganglia, talamus) [34,42].
S další možnou etiologií vzniku vertiga přichází japonští autoři, kteří zjistili, že až 80 % pacientů (po poranění typu whiplash) má známky cerebrospinální hypovolémie na radioizotopové cisternografii. Tito pacienti pak byli vyšetřeni elektronystagmograficky a posturograficky s abnormálním nálezem a byla u nich provedena MR, která prokázala pokles mozečkových tonzil a zploštění Varolova mostu, což jsou charakteristické známky cerebrospinální hypovolémie nazývané „brain sagging” (čili mozkový pokles či průvěs). Z toho vyvozují teorii, že vertigo je způsobeno tímto mechanizmem, čili se jedná vlastně o syndrom nitrolební hypotenze [43].
Dalším možným etiologickým faktorem může být i vestibulární migréna, která prokazatelně může být též spuštěna poraněním krční páteře [44].
Z výše uvedeného tedy vyplývá, že whiplash injury vyvolává difuzní postižení v oblasti mozku a krční míchy. Jedná se spíše o sdruženou symptomatologii než o izolované postižení krční páteře s projevy cervikálního vertiga.
Vaskulární teorie (komprese vertebrálních tepen)
Teorie vaskulární komprese vychází z hemodynamických studií, které byly prováděny v 60. letech na kadáverech. Toole et al zjistili, že rotace hlavy je spojena s kompresí vertebrální tepny (AV) na protilehlé straně, a postulovali teorii, že tento mechanizmus může být příčinou cervikálního vertiga [45]. Pokud by tato teorie platila, pak by musela být komprese AV spojena i s další symptomatikou ze zadní cirkulace (diplopie, poruchy zorného pole, dropp attacks, vomitus atd.), a nevysvětluje též příčinu bolestí krční páteře. Epizody symptomatiky z VB povodí bychom též museli definovat spíše jako tranzitorní ischemické ataky (TIA) v zadní cirkulaci (s riziky, etiologií a léčbou s nimi spojenými) a nikoliv jako cervikální vertigo. Navíc novější studie s digitální subtrakční angiografií (DSA) potvrdily, že klinicky významná arteriální komprese (při pouhé rotaci hlavy) není v podmínkách in vivo prakticky vůbec možná [46]. Nicméně výjimku z výše uvedeného přehledu představuje tzv. Bow Hunterův syndrom, což je ovšem velmi vzácná příčina přechodné ischemie v zadní mozkové cirkulaci vzniklá kompresí AV. V literatuře bylo prozatím popsáno cca 200 pacientů s tímto syndromem [47]. Symptomy zahrnují paroxyzmální vertigo, nystagmus, tinnitus, synkopy, rozostření vidění, nauzeu a zvracení [47]. Vzniká při kompresi dominantní AV kostními strukturami při rotaci či náklonu hlavy. Etiologicky se jedná o velké osteofyty nebo atlantookcipitální hypermobilitu. Patologie je často spojena s hypoplazií či stenózou nedominantní AV. Symptomy odezní po návratu hlavy do neutrální polohy [48]. Syndrom musí být potvrzen radiologicky, metodou volby je dynamická DSA, která prokáže uskřinutí AV. Léčba je chirurgická [49].
Je třeba navíc dodat, že Choi et al ve své práci následně potvrdili, že ischemie a pocity vertiga ve VB povodí jsou způsobeny ischemií v oblasti vnitřního ucha, nikoliv v oblasti kmene [50].
Neurovaskulární hypotéza – syndrom zadního krčního sympatiku (Barré-Lieou)
Tuto teorii poprvé publikovali v roce 1926 Jean-Alexander Barré a Young-Choen Lieou [51]. Předpokládali, že plexus sympaticus, který obklopuje vertebrální tepny, může být mechanicky drážděn degenerativními změnami krční páteře, a iritace sympatiku tak způsobí reflexní vazokontrikci ve VB povodí. Experimentální data však prokázala, že sympatická denervace nezpůsobuje vazodilataci ani u zvířat, stejně jako iritace sympatiku nezpůsobuje vazokonstrikci [52]. Syndrom Barré-Lieou je tedy dnes jednoznačně považován za obsolentní jednotku, přesto se s ním občasně i nadále v neurologické literatuře setkáme [53].
Teorie komprese krční míchy
Někteří autoři udávají příčinnou souvislost cervikálního vertiga s kompresí ascendentních a descendentních míšních drah, které jsou ve spojení s vestibulárními jádry nebo vestibulospinálními projekcemi. Podle jejich názoru je diskogenní komprese míchy dokonce nejčastější příčinou cervikálního vertiga [54]. Jako průkaz této hypotézy bývají nezřídka uváděny dobré efekty různých invazivních výkonů na krční páteři, jako např. pozitivní efekt transkutánní laserové dekomprese disku [55] či zlepšení subjektivních potíží po přední krční diskektomii a fúzi obratlů [56]. Mechanizmus účinku a etiopatogeneze tohoto subjektivního zlepšení však i nadále zůstává na úrovni výše diskutovaných teorií – tj. že např. chirurgická dekomprese kořene nebo míchy umožní lepší přenos proprioceptivních signálů do CNS a tím zlepší i řízení postury [56], či zcela opačný postulát – tj., že po odstranění aberantních mechanoreceptorů (po náhradě postiženého intervertebrálního disku) dojde k úpravě abnormální propriocepce, která jinak způsobuje „mismatch” ve vestibulárních jádrech CNS [14]. Musíme si však uvědomit, že efekt chirurgického či jakéhokoliv jiného invazivního zákroku (zejména u pacientů s nespecifickými potížemi) je obecně velmi často výrazný [57]. Nenašli jsme v literatuře studii, která by se zabývala tzv. shame operacemi v oblasti krční páteře, ale zajímavé jsou např. práce, které byly provedeny u pacientů s osteoporotickou frakturou obratlů, kdy v podstatě placebové zákroky (povrchová kožní anestezie) měly srovnatelný efekt v úlevě bolesti jako reálně provedená vertebroplastika [58]. Musíme též vzít do úvahy prozatím nevysvětlitelnou diskrepanci mezi pacienty s těžkou blokádou a bolestí krční páteře (dokonce i s myelopatií) bez vertiga a pacienty s prakticky imobilizujícím vertigem a pouze mírnou bolestí páteře [7]. Dále je třeba si uvědomit, že spojení páteře s vestibulárním systémem je bilaterální – tj., že chronická primárně vestibulární léze vede k asymetrickému napětí šíjových svalů, a tím k sekundárním potížím s krční páteří.
Teorie vestibulární migrény
V roce 2013 Yacovino a Hain „oživili” hypotézu migrénou navozeného cervikálního vertiga. Tímto způsobem se snaží vysvětlovat diskrepanci mezi pacienty, kteří mají bolesti krční páteře s vertigem, a mezi těmi, kteří mají pouze bolesti bez vertiga, a domnívají se, že právě migréna by měla být pojítkem mezi krční bolestí a krčním vertigem [59]. Již předtím byly publikovány četné práce o této problematice [60,61]. U třetiny pacientů s migrénou bývá skutečně přítomno vertigo, na druhou stranu bolesti za krkem až ztuhlost jsou typickými znaky migrény [62]. Předpokládaným mechanizmem vzniku cervikálního vertiga je konektivita mezi vestibulárními jádry a jádrem n. trigeminus. Předpokládá se, že stimulace vestibulárních jader vede k aktivaci nucleus spinalis n. trigemini, která sekundárně spouští ataku migrény s bolestí krční páteře a vertigem [59]. Dominují pocity rotační závrati, jejichž intenzita se však dá modifikovat změnou polohy hlavy, mohou být přítomny i jiné neurologické příznaky, i když ty jsou méně časté (dysartrie, diplopie, brnění či hypestézie rukou a obličeje). Co se týče léčby vestibulární migrény, data jsou relativně chudá [63]. Celá tato teorie však také potřebuje ještě daleko širší a podrobnější výzkum.
Diagnostika
Pokud jde o cervikální vertigo, tak se v podstatě vždy jedná jen o diagnostiku per exclusionem, kdy vylučujeme všechny možné (zejména vestibulární, oční či periferně neurogenní) příčiny závrativých stavů. Neexistuje žádný specifický test pro diagnostiku cervikálního vertiga. Pokud pacient nemá bolesti krční páteře, ale pouze vertigo, tak je tato diagnóza již od počátku vyloučena [7]. Samozřejmostí je podrobné základní neurologické vyšetření, při kterém musíme provést i Dix-Hallpikův test k vyloučení BPPV, které se často mylně považuje za cervikální vertigo [7]. RTG vyšetření krční páteře je bez významu. Zobrazovací vyšetření jako je CT či MR slouží k zobrazení anatomických poměrů (např. malformace), expanzivních lézí (např. tumory mostomozečkového koutu), traumatických změn (kontuzní ložiska mozku a míchy, diskopatie), degenerativní změny (spinální cervikální stenóza) [59]. K diferenciaci od rotačního vertebrálního arteriálního syndromu (Bow Hunterův syndrom) je vhodná MRA nebo CTA, v nejasných případech i DSA s rotací hlavy k postižené straně [59].
Někteří autoři se snažili monitorovat vliv cervikálního podílu na okohybných funkcích pomocí elektrookulografie. Jak však bylo uvedeno výše, vybavení COR je ve specifických podmínkách možné i u zcela zdravých jedinců, nemůžeme jej pokládat za průkaz cervikálního vertiga. Navíc se tento test jeví málo senzitivní i málo specifický [59].
Při vyšetření plynulých sledovacích očních pohybů (smooth pursuit eye movement test) zůstává hlava pacienta ve stejné poloze, pouze sleduje očima pohyby ruky vyšetřujícího. Test je však komplexem mnoha vjemů, závislý i na kognici, věku, sedaci pacienta a slouží především jako jedno ze zásadních vyšetření k posouzení funkce cerebela [59].
Existuje dále celá baterie různých testů k vyšetření vestibulárního aparátu (elektronystagmografie, testy na rotačním křesle, posturografie atd.), jejichž popis však přesahuje rozsah tohoto textu, jsou však detailně popsány v jiných monografiích [4].
Diferenciální diagnostika je uvedena v tab. 1.
1. Diferenciální diagnostika cervikálního vertiga. 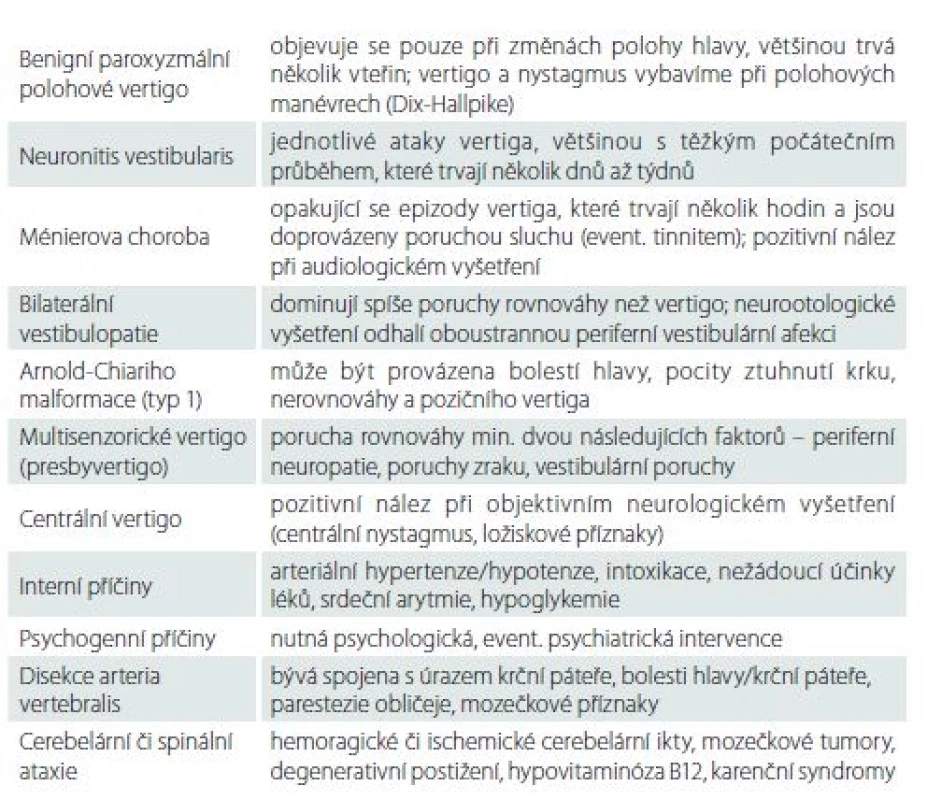
Léčba
Terapie cervikálního vertiga je samozřejmě komplikovaná, protože zdroj obtíží v drtivé většině případů nelze identifikovat.
Někteří autoři navrhují manuální léčbu jako metodu volby [64]. Pokud však byly provedeny systematické analýzy literatury zabývající se manuální terapií pacientů s cervikálním vertigem, tak se zjistilo, že naprostá většina provedených prací byla metodologicky velmi nedokonalá (např. chyběly kontrolní skupiny zdravých jedinců, nekvalitní randomizace, chybně provedené statistické zpracování, chybělo zaslepení atd.) [65]. Na základě výše uvedených poznatků dospěli Reid et al k závěru, že existují jen omezené důkazy (úroveň průkazu 3) pro efekt manipulační léčby v terapii cervikálního vertiga [66]. Neexistují též žádná spolehlivá data o intenzitě, četnosti či jiné specifikace manuální léčby v této indikaci [65].
Další možností je užití „vestibulární rehabilitace”, která zahrnuje mentální cvičení, fyzická cvičení s cílem obnovení správného vnímání pozice kloubů, zlepšení koordinace pohybů, oční trénink – vše s cílem posílení VOR [67]. Stejně jako u manuální léčby však v této indikaci spolehlivý důkaz efektu chybí, vestibulární rehabilitace je prokazatelně účinná jen u periferních vestibulárních lézí [68].
Co se týče léčby poranění typu whiplash injury, tak nejsilnější důkazy jsou v případě léčby akutního postižení. Možná poněkud překvapivě se častěji doporučují fyzioterapie a lehká mobilizační cvičení než úplná imobilizace krční páteře a absolutní klidový režim [68]. Trakce není účinná [69]. Neexistuje žádná studie, která by prokázala efekt klidového režimu a imobilizace měkkým krčním límcem oproti jiné léčbě [69]. Dokonce jsou i důkazy, že pokud pacientovi řekneme, aby se „choval jako normálně”, může být výsledný stav stejně efektivní jako při aktivní léčbě [70]. U pacientů s chronickými potížemi je léčba většinou multioborová a velmi komplikovaná. Může být ovlivněna (a často prodloužena) mnoha sociálními, ekonomickými i psychologickými faktory. Současná literatura předpokládá, že časná mobilizace a brzký návrat k běžné aktivitě mají nejlepší šanci na úspěch. Avšak absence jasných diagnostických a léčebných možností svědčí pro to, že další široký výzkum na tomto poli je nadále potřebný [71].
Závěr
Cervikální vertigo zůstává i nadále kontroverzní klinickou jednotkou, jejíž existence není jednoznačně prokázána. Neexistuje žádná přesná ani jednotná definice cervikálního vertiga.
Nejsou k dispozici žádná relevantní epidemiologická data o této jednotce (či data z populačních registrů). Neexistuje žádný test specifický pro cervikální vertigo. Není jasný patofyziologický podklad vzniku cervikálního vertiga. Cervikální vertigo je silně přediagnostikované (při správné diagnostice se odhalí jiná příčina až u 90 % případů). Léčba je komplikovaná, často víceoborová a empirická, nemáme k dispozici kvalitní randomizované studie, které by prokázaly efekt nejčastěji poskytované terapie. Při absenci bolestí krční páteře je tato diagnóza vyloučena.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
MUDr. Zdeněk Kadaňka Jr.
Neurologická klinika LF MU a FN Brno
Jihlavská 20
625 00 Brno
e-mail: kadanka.zdenek2@fnbrno.cz
Přijato k recenzi: 20. 3. 2018
Přijato do tisku: 18. 7. 2018
Sources
1. Schappert SM. National Ambulatory Medical Care Survey: 1989 summary. Vital Health Stat 1992; 13(110): 1 – 80.
2. Kerber KA, Meurer WJ, West BT et al. Dizziness presentations in U.S. emergency departments, 1995-2004. Acad Emerg Med 2008; 15(8): 744 – 750. doi: 10.1111/ j.1553-2712.2008.00189.x.
3. Brandt T. Cervical vertigo – reality or fiction? Audiol Neurootol 1996; 1(4): 187 – 196.
4. Jeřábek J. Diagnostika pacienta s akutní závratí. Cesk Slov Neurol N 2015; 78/ 111(5): 503 – 509. doi: 10.14735/ amcsnn2015503.
5. Ryan GM, Cope S. Cervical vertigo. Lancet 1955; 31; 269(6905): 1355 – 1358.
6. Hain TC. Cervicogenic causes of vertigo. Curr OpinNeurol 2015; 28(1): 69 – 73. doi: 10.1097/ WCO.000000000 0000161.
7. Brandt T, Bronstein AM. Cervical vertigo. J Neurol Neurosurg Psychiatry 2001; 71(1): 8 – 12.
8. Cullen KE, Roy JE. Signal processing in the vestibular system during active versus passive head movements. J Neurophysiol 2004; 91(5): 1919 – 1933. doi: 10.1152/ jn.00988.2003.
9. Yahia A, Ghroubi S, Jribi S et al. Chronic neck pain and vertigo: is a true balance disorder present? Ann Phys Rehabil Med 2009 52(7 – 8): 556 – 567. doi: 10.1016/ j.rehab. 2009.07.033.
10. Furman JM, Cass SP. A practical work-up for vertigo. Contemp Intern Med 1995; 7(3): 24 – 27.
11. Wrisley DM, Sparto PJ, Whitney SL et al. Cervicogenic dizziness: a review of diagnosis and treatment. J Orthop Sports Phys Ther 2000; 30(12): 755 – 766. doi: 10.2519/ jospt.2000.30.12.755.
12. Lewit K. Pathomechanism of cervico-cranial headache. Cesk Neurol Neurochir 1978; 41(1): 26 – 34.
13. van Dieën JH, van Drunen P, Happee R. Sensory contributions to stabilization of trunk posture in the sagittal plane. J Biomech 2017; 70 : 219 – 227. doi: 10.1016/ j.jbiomech.2017.07.016.
14. Yang L, Yang C, Pang X et al. Mechanoreceptors in diseased cervical intervertebral disc and vertigo. Spine (Phila Pa 1976) 2017; 42(8): 540 – 546. doi: 10.1097/ BRS.000 0000000001801.
15. Shevell M. The tripartite origins of the tonic neck reflex: Gesell, Gerstmann, and Magnus. Neurology 2009; 72(9): 850 – 853. doi: 10.1212/ 01.wnl.0000343961.35429.09.
16. Mahfuz MM, Schubert MC, Figtree WVC. Optimal human passive vestibulo-ocular reflex adaptation does not rely on passive training. J Assoc Res Otolaryngol 2018; 19(3): 261 – 271. doi: 10.1007/ s10162-018-0657-9.
17. Bárány R. Augenbewgungen durch Thoraxbewegungen ausgelost. Zentralbl Physiol 1906; 20 : 298 – 302.
18. de Jong PT, de Jong JM, Cohen B et al. Ataxia and nystagmus induced by injection of local anesthetics in the neck. Ann Neurol 1977; 1(3): 240 – 246. doi: 10.1002/ ana.410010307.
19. Gesell A. The tonic neck reflex in the human infant: morphogenetic and clinical signifikance. J Pediatr 1938; 13(4): 455 – 464.
20. Sağlam M, Lehnen N. Gaze stabilization in chronic vestibular-loss and in cerebellar ataxia: interactions of feedforward and sensory feedback mechanisms. J Vestib Res 2014; 24(5 – 6): 425 – 431. doi: 10.3233/ VES-140538.
21. Mergner T, Siebold C, Schweigart G et al. Human perception of horizontal trunk and head rotation in space during vestibular and neck stimulation. Exp Brain Res 1991; 85(2): 389 – 404.
22. Huygen PL, Verhagen WI, Nicolasen MG. Cervico-ocular reflex enhancement in labyrinthine-defective and normal subjects. Exp Brain Res 1991; 87(2): 457 – 464.
23. Bronstein AM, Mossman S, Luxon LM. The neck-eye reflex in patients with reduced vestibular and optokinetic function. Brain 1991; 114(1A): 1 – 11.
24. de Vries J, Ischebeck BK, Voogt LP et al. Cervico-ocular reflex is increased in people with nonspecific neck pain. Phys Ther 2016; 96(8): 1190 – 1195. doi: 10.2522/ ptj.20150211.
25. Ischebeck BK, de Vries J, van Wingerden JP et al. The influence of cervical movement on eye stabilization reflexes: a randomized trial. Exp Brain Res 2018; 236(1): 297 – 304. doi: 10.1007/ s00221-017-5127-9.
26. Schweigart G, Chien RD, Mergner T. Neck proprioception compensates for age-related deterioration of vestibular self-motion perception. Exp Brain Res 2002; 147(1): 89 – 97. doi: 10.1007/ s00221-002-1218-2.
27. Kelders WP, Kleinrensink GJ, van der Geest JN et al. Compensatory increase of the cervico-ocular reex with age in healthy humans. J Physiol 2003; 553(1): 311 – 317.
28. Dieterich M, Pöllmann W, Pfaffenrath V. Cervicogenic headache: electronystagmography, perception of verticality and posturography in patients before and after C2-blockade. Cephalalgia 1993; 13(4): 285 – 288. doi: 10.1046/ j.1468-2982.1993.1304285.x.
29. Brandt T, Büchele W, Arnold F. Arthrokinetic nystagmus and ego-motion sensation. Exp Brain Res 1977; 30(2 – 3): 331 – 338.
30. Hinoki M, Ushio N. Lumbomuscular proprioceptive reflexes in body equilibrium. Acta Otolaryngol Suppl 1975; 330 : 197 – 210.
31. Hülse M. Differential diagnosis of vertigo in functional cervical vertebrae joint syndromes and vertebrobasilar insufficiency. HNO 1982; 30(12): 440 – 446.
32. Ament JD, Karnati T, Kulubya E et al. Treatment of cervical radiculopathy: a review of the evolution and economics. Surg Neurol Int 2018; 9 : 35. doi: 10.4103/ sni.sni_441_17.
33. Kolev OI, Sergeeva M. Vestibular disorders following different types of head and neck trauma. Funct Neurol 2016; 31(2): 75 – 80. doi: 10.11138/ FNeur/ 2016.31.2.075.
34. Biendara J, Otte A. Whiplash syndrome – a disorder of the brain? Hell J Nucl Med 2017; 20(2): 110 – 112. doi: 10.1967/ s002449910550.
35. Chetana N, Claussen CF. Vertigo in whiplash injury: a presentation of prevalent butterfly patterns of caloric tests. Indian J Otolaryngol Head Neck Surg 2010; 62(2): 208 – 214. doi: 10.1007/ s12070-010-0026-4.
36. Kasch H, Qerama E, Kongsted A et al. Clinical assessment of prognostic factors for long-term pain and handicap after whiplash injury: a 1-year prospective study. Eur J Neurol 2008; 15(11): 1222 – 1230. doi: 10.1111/ j.1468-1331.2008.02301.x.
37. Campbell L, Smith A, McGregor L et al. Psychological factors and the development of chronic whiplash associated disorder(s): a systematic review. Clin J Pain 2018; 34(8): 755 – 768. doi: 10.1097/ AJP.0000000000000597.
38. Rydman E, Ponzer S, Brisson R. Long-term follow-up of whiplash injuries reported to insurance companies: a cohort study on patient-reported outcomes and impact of financial compensation. Eur Spine J 2018; 27(6): 1255 – 1261. doi: 10.1007/ s00586-018-5507-2.
39. Ellis MJ, Leddy JJ, Willer B. Physiological, vestibulo-ocular and cervicogenic post-concussion disorders: an evidence-based classification system with directions for treatment. Brain Inj 2015; 29(2): 238 – 248. doi: 10.3109/ 02699 052.2014.965207.
40. Cheever K, Kawata K, Tierney R. Cervical injury assessments for concussion evaluation: a review. J Athl Train 2016; 51(12): 1037 – 1044. doi: 10.4085/ 1062-6050-51.12.15.
41. Endo K, Ichimaru K, Komagata M et al. Cervical vertigo and dizziness after whiplash injury. Eur Spine J 2006; 15(6): 886 – 890.
42. Vállez García D, Doorduin J, Willemsen AT et al. Altered regional cerebral blood flow in chronic whiplash associated disorders. EBioMedicine 2016; 10 : 249 – 257. doi: 10.1016/ j.ebiom.2016.07.008.
43. Yokota J, Shimoda S. Neuro-otological studies of patients suffering from dizziness with cerebrospinal fluid hypovolemia after traffic accident-associated whiplash injuries. Brain Nerve 2015; 67(5): 627 – 634. doi: 10.11477/ mf.1416200191.
44. Morganti LO, Salmito MC, Duarte JA et al. Vestibular migraine: clinical and epidemiological aspects. Braz J Otorhinolaryngol 2016; 82(4): 397 – 402. doi: 10.1016/ j.bjorl.2015.06.003.
45. Toole JF, Tucker SH. Influence of head position upon cerebral circulation. Studies on blood flow in cadavers. Arch Neurol 1960; 2 : 616 – 623.
46. Takahashi I, Kaneko S, Asaoka K et al. Angiographic examination of the vertebral artery at the atlantoxial joint during head rotation. No Shinkei Geka 1994; 22(8): 749 – 753.
47. Iida Y, Murata H, Johkura K et al. Bow Hunter‘s syndrome by nondominant vertebral artery compression: a case report, literature review, and significance of downbeat nystagmus as the diagnostic clue. World Neurosurg 2018; 111 : 367 – 372. doi: 10.1016/ j.wneu.2017.12.167.
48. Cai DZ, Roach RP, Weaver JP. Bow Hunter‘s syndrome in a patient with a right hypoplastic vertebral artery and a dynamically compressible left vertebral artery. Asian J Neurosurg 2018; 13(1): 133 – 135. doi: 10.4103/ 1793-5482.181129.
49. Strickland BA, Pham MH, Bakhsheshian J. BowHunter‘s syndrome: surgical management (video) and review of the literature. World Neurosurg 2017; 103 : 953.e7 – 953.e12. doi: 10.1016/ j.wneu.2017.04.101.
50. Choi KD, Shin HY, Kim JS et al. Rotational vertebral artery syndrome: oculographic analysis of nystagmus. Neurology 2005; 65(8): 1287 – 1290. doi: 10.1212/ 01.wnl.0000180405.00560.51.
51. Barré JA. Sur un syndrome sympathique cervical postérieur et sa cause frequente, l’arthrite cervicale. Rev Neurol (Paris); 1926; 1 : 1246 – 1248.
52. Sadoshima S, Heistad DD. Regional cerebral blood flow during hypotension in normotensive and stroke-prone spontaneously hypertensive rats: effect of sympathetic denervation. Stroke 1983; 14(4): 575 – 579.
53. Li Y, Peng B. Pathogenesis, diagnosis, and treatment of cervical vertigo. Pain Physician 2015; 18(4): E583 – E595.
54. Benito-León J, Díaz-Guzmán J, Madero S et al. Vertigo as an atypical symptom of intraspinal cord tumor. Rev Neurol 1996; 24(129): 564 – 566.
55. Yang YG, Ren XS, Yang C et al. Percutaneous laser disc decompression for cervical vertigo. Zhonghua Wai Ke Za Zhi 2007; 45(20): 1408 – 1410.
56. Freppel S, Bisdorff A, Colnat-Coulbois S et al. Visuo--proprioceptive interactions in degenerative cervical spine diseases requiring surgery. Neuroscience 2013; 255(10): 226 – 232. doi: 10.1016/ j.neuroscience.2013.09.060.
57. Jonas WB, Crawford C, Colloca L et al. To what extent are surgery and invasive procedures effective beyond a placebo response? A systematic review with meta-analysis of randomised, sham controlled trials. BMJ Open 2015; 5(12): e009655. doi: 10.1136/ bmjopen-2015-009655.
58. Kallmes DF, Comstock BA, Heagerty PJ et al. A randomized trial of vertebroplasty for osteoporotic spinal fractures. N Engl J Med 2009; 361(16): 569 – 579. doi: 10.1056/ NEJMoa0900563.
59. Yacovino DA, Hain TC. Clinical characteristics of cervicogenic-related dizziness and vertigo. Semin Neurol 2013; 33(3): 244 – 255. doi: 10.1055/ s-0033-1354592.
60. Cha YH. Migraine-associated vertigo: diagnosis and treatment. Semin Neurol 2010; 30(2): 167 – 174. doi: 10.1055/ s-0030-1249225.
61. Reploeg MD, Goebel JA. Migraine-associated dizziness: patient characteristics and management options. Otol Neurotol 2002; 23(3): 364 – 371.
62. Lance JW. Impact commentaries. Observations on 500 cases of migraine and allied vascular headache. J Neurol Neurosurg Psychiatry 2012; 83(7): 673 – 674. doi: 10.1136/ jnnp-2011-301630.
63. Strupp M, Versino M, Brandt T. Vestibular migraine. Handb Clin Neurol 2010; 97 : 755 – 771. doi: 10.1016/ S0072-9752(10)97062-0.
64. Jung FC, Mathew S, Littmann AE el al. Clinical deci-sion making in the management of patients with cervicogenic dizziness: a case series. J Orthop Sports Phys Ther 2017; 47(11): 874 – 884. doi: 10.2519/ jospt.2017.7425.
65. Lystad RP, Bell G, Bonnevie-Svendsen M et al. Manual therapy with and without vestibular rehabilitation for cervicogenic dizziness: a systematic review. Chiropr Man Therap 2011; 19 : 21. doi: 10.1186/ 2045-709X-19-219999999.
66. Reid SA, Rivett DA. Manual therapy treatment of cervicogenic dizziness: a systematic review. Man Ther 2005; 10(1): 4 – 13. doi: 10.1016/ j.math.2004.03.006.
67. Spiegel R, Rust H, Baumann T et al. Treatment of dizziness: an interdisciplinary update. Swiss Med Wkly 2017; 147: w14566. doi: 10.4414/ smw.2017.14566.
68. Kunelskaya NL, Baibakova EV, Guseva AL et al. The compensation of the vestibulo-ocular reflex during rehabilitation of the patients presenting with vestibular neuritis. Vestn Otorinolaringol 2018; 83(1): 27 – 31. doi: 10.17116/ otorino201883127-31.
69. Wong JJ, Shearer HM, Mior S et al. Are manual therapies, passive physical modalities, or acupuncture effective for the management of patients with whiplash-associated disorders or neck pain and associated disorders? An update of the bone and joint decadetask force on neck pain and its associated disorders by the OPTIMa collaboration. Spine J 2016; 16(12): 1598 – 1630. doi: 10.1016/ j.spinee.2015.08.024.
70. Barnsley L. An evidence-based approach to the treatment of acute whiplash injury. Pain Res Manag 2003; 8(1): 33 – 36.
71. Ritchie C, Ehrlich C, Sterling M. Living with ongoing whiplash associated disorders: a qualitative study of individual perceptions and experiences. BMC Musculoskelet Disord 2017; 18(1): 531. doi: 10.1186/ s12891-017-1882-9.
Labels
Paediatric neurology Neurosurgery Neurology
Article was published inCzech and Slovak Neurology and Neurosurgery

2018 Issue 5-
All articles in this issue
- Anaesthesia and neuromuscular disorders
- The best approach in motorized Parkinson‘s disease therapy is INTRADUODENAL LEVODOPA
- The best approach in motorized Parkinson‘s disease therapy is APOMORPHINE INFUSION
- The best approach in motorized Parkinson‘s disease therapy is DEEP BRAIN STIMULATION
- Cervical vertigo – fiction or reality?
- Care for patients with dysphagia after acute stroke in the Czech republic
- Computational fluid dynamics of intracranial aneurysms and its potential contribution in clinical practice from a neurosurgeon’s perspective
- Review of diseases with restricted diffusion on magnetic resonance imaging of the brain
- New insights in the diagnosis and treatment of amyotrophic lateral sclerosis
- Gamma knife stereotactic radiosurgery in recurrent or residual glioblastoma multiforme – our experience in two neurosurgical units
- Validation of questionnaire for patients with myotonia – Czech version of Myotonia Behaviour Scale
- The first documented case of Japanese encephalitis imported to the Czech Republic
- Early complication after treatment of dissecting intracranial aneurysm in vertebrobasilar circulation with a flow-diverter
- Harvey Cushing as Nobel Prize nominee
- Muscular dystopia in the fallopian canal
- Acute and subacute silent cerebral infarction in patients before elective coronary intervention
- Relationship between epidemiology and subjective perception of pain in patients with carpal tunnel syndome
- Speech intelligibility and clinical parameters in patients with Parkinson‘s disease
- The relationship of the basilar artery bifurcation and dorsum sel lae
- Spinální schwannom v oblasti hrudní páteře s masivním intratumorálním krvácením
- Czech and Slovak Neurology and Neurosurgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- New insights in the diagnosis and treatment of amyotrophic lateral sclerosis
- Review of diseases with restricted diffusion on magnetic resonance imaging of the brain
- Cervical vertigo – fiction or reality?
- Anaesthesia and neuromuscular disorders
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

