-
Medical journals
- Career
Kombinovaná chemoradioterapie karcinomu hrdla děložního – retrospektivní hodnocení vlastního souboru
Authors: Z. Pechačová 1; R. Lohynská 1,2; Z. Weitoschová 1; Michal Zikán 3; Olga Dubová 3; V. Tomancová 1,4; E. Kmoníčková 1; M. Pála 1; T. Drbohlavová 1
Authors‘ workplace: Ústav radiační onkologie, 1. LF UK a FN Bulovka, Praha 1; Onkologická klinika 1. LF UK a FTN Praha 2; Gynekologicko-porodnická klinika 1. LF UK a FN Bulovka, Praha 3; Onkologická klinika 1. LF UK a VFN v Praze 4
Published in: Klin Onkol 2022; 35(2): 139-149
Category: Original Articles
doi: https://doi.org/10.48095/ccko2022139Overview
Východiska: Cílem sdělení je retrospektivní analýza výsledků léčby a toxicity v souboru pacientek s karcinomem hrdla děložního, které v Ústavu radiační onkologie FN Bulovka v Praze podstoupily v letech 2014–2017 radikální (chemo) radioterapii. Soubor pacientek a metody: V uvedeném období bylo na pracovišti léčeno 141 pacientek, kombinovanou (chemo) radioterapii s radikálním záměrem podstoupilo 105 (74,5 %) z nich a paliativní radioterapie byla provedena ve 36 (25,5 %) případech. Dle klasifikace Mezinárodní federace gynekologie a porodnictví (International Federation of Gynecology and Obstetrics – FIGO) z roku 2009 byly nejpočetnějšími stadii IIB v 39 (27,7 %) a IIIB v 64 (45,4 %) případech, po překlasifikování dle FIGO 2018 je zřejmé výrazné početní zastoupení nově ustanovených stadií IIIC1 v 55 (39,0 %) případech a IIIC2 ve 22 (15,6 %) případech. Výsledky: Medián přežití bez progrese (progression-free survival – PFS) a celkového přežití (overall survival – OS) dosáhl v celém souboru 31,3, resp. 40,1 měsíce. V podskupině pacientek léčených s radikálním záměrem bylo dosaženo mediánu PFS 44,0 měsíce, OS 48,8 měsíce a v podskupině paliativně léčených činil medián PFS 9,4 měsíce a OS 14,8 měsíce. U radikálně léčené podskupiny byly zjištěny u 7 (6,7 %) pacientek gastrointestinální nebo genitourinární projevy toxicity v intenzitě G3–4 a celková akutní toxicita vč. kožních a hematologických projevů G3–4 se vyskytla u 18 (17,1 %) pacientek. Pozdní toxicita G3–4 byla zaznamenána ve 13 (12,4 %) případech. Pacientky, které podstoupily aplikaci brachyterapie (BRT) v souladu se standardním léčebným plánem (dávka v bodě A min. 24 Gy), vykázaly signifikantně lepší přežití oproti pacientkám s nižší aplikovanou dávkou BRT. Byl potvrzen prognostický potenciál vstupního performance statusu (PS) a stupně anemie – u pacientek v celkově dobrém stavu nebo bez anemie bylo zaznamenáno signifikantně delší přežití. Závěr: Výsledná data potvrdila v našem souboru pacientek klíčovou roli BRT pro doručení kurativní dávky do cílového objemu, je také zřejmý prognostický potenciál vstupního PS a hladiny hemoglobinu. Zastoupení nežádoucích účinků je akceptovatelné, ale do budoucna očekáváme zlepšení díky využití moderních technologií radioterapie.
Klíčová slova:
radioterapie – karcinom děložního hrdla – chemoradioterapie – brachyterapie
Úvod
Karcinom hrdla děložního tvoří v ČR necelá 3 % všech malignit [1] a patří mezi častá nádorová onemocnění u žen. V rámci gynekologických novotvarů se řadí na 2. místo v incidenci (1. místo zaujímají novotvary děložního těla) a na 2. místo v mortalitě (na 1. místě jsou nádory ovarií) [1]. V pokročilém stadiu bývá toto onemocnění diagnostikováno ve 20–30 % případů [1] i přes dostupné možnosti screeningových vyšetření [2].
Kombinovaná radioterapie představuje základní léčebnou metodu lokálně pokročilého karcinomu hrdla děložního po více desetiletí. Využívání zdrojů ionizujícího záření v léčbě tohoto onemocnění bylo předmětem výzkumu již v první polovině 20. století, kdy byly vypracovány ozařovací techniky, jež jsou ve svých základních principech užívány dosud. S rozvojem technologií v radioterapii a výpočetní technice došlo k četným inovacím technik zevní radioterapie (external beam radiotherapy – EBRT) i brachyterapie (BRT), které umožňují větší přesnost plánování ozařování i následného provedení léčby [2]. Přínos konkomitantní chemoterapie (CHT) byl opakovaně prokázán [3,4] a kombinovaná chemoradioterapie (CHRT) je v současnosti standardem léčby lokálně pokročilého karcinomu hrdla děložního [2,5–7]. Z důvodu četných relapsů onemocnění i přes provedenou kompletní radikální léčbu se jeví jako potenciálně přínosné přidání další systémové léčby ke kombinované CHRT [8–9] a předmětem výzkumu jsou různé strategie se záměrem dosažení lepších léčebných výsledků. Jedná se zejména o neoadjuvantní CHT následovanou chirurgickým výkonem [10] nebo CHRT [9,11], dále je zkoumán přínos adjuvantní CHT po ukončení CHRT [9], možnosti uplatnění imunoterapie check - point inhibitory [12] a cílených preparátů [11]. Probíhá také výzkum nových prognostických a prediktivních faktorů, které by umožnily přesnější odhad rizika šíření mimo primární lokalizaci a mohly by přispět k individualizaci multimodální léčby [13]. Dosud publikovaná data stran nových léčebných postupů nejsou jednoznačná a závěry velkých multicentrických studií jsou očekávány [9]. Přidání adjuvantní systémové léčby po primární CHRT je v současné době dle European Society of Gynaecological Oncology (ESGO) guidelines doporučeno pouze v případě metastatického postižení limitovaného na oblast levostranných nadklíčkových lymfatických uzlin [5]. Pro lokálně pokročilý karcinom hrdla děložního zůstává standardem kombinovaná CHRT ve složení: EBRT, intrakavitární BRT uterovaginálním aplikátorem a konkomitantní CHT [2,5–7,14]. Pro doručení dostatečně účinné dávky na oblast primárního tumoru hrdla děložního zůstává nezbytná BRT, která zaručuje největší přínos – boost pomocí různých technik zevní radioterapie vykázal výrazně horší výsledky [15].
Pro diagnostiku i rozvahu o léčebném postupu je přínosem technologický rozvoj zobrazovacích metod: expertního onkogynekologického ultrazvuku (UZ) [16], magnetické rezonance (MR) [17] i funkčního zobrazování v nukleární medicíně – zejména vyšetření CT kombinované s pozitronovou emisní tomografií (PET/CT) [18]. Významnou roli v rámci stagingových vyšetření si získala laparoskopická lymfadenektomie [5]. Tyto metody dnes umožňují přesnější diagnostiku i individualizaci léčebných postupů. Vzhledem k vysokým nárokům na správnost diagnostických a léčebných postupů mají být pacientky léčeny ve specializovaných centrech se širokým zázemím radiodiagnostiky, onkogynekologické chirurgie, klinické onkologie a radioterapeutických metod.
Cílem předkládaného sdělení je retrospektivní analýza výsledků léčby a toxicity v souboru pacientek Ústavu radiační onkologie Fakultní nemocnice Bulovka v Praze (ÚRO FNB) léčených primární kombinovanou CHRT.
Soubor pacientek a metody
V letech 2014–2017 bylo v ÚRO FNB léčeno 141 pacientek s lokálně pokročilým karcinomem hrdla děložního. Kombinovanou (CH) RT s radikálním záměrem podstoupilo 105 (74,5 %) pacientek, paliativní radioterapie byla provedena u 36 (25,5 %) pacientek. Základní charakteristiky souboru shrnuje tab. 1. Medián věku pacientek v době diagnózy činil 61,0 roku, v rozmezí 27–87 let. Většina žen byla vstupně ve velmi dobrém klinickém stavu – performance status (PS) dle Eastern Cooperative Oncology Group (ECOG) byl stanoven na stupni 0–1 ve > 80 % případů a je zřejmé větší zastoupení PS 0–1 v podskupině radikálně léčených pacientek (graf 1). Histologicky se v 90 % jednalo o spinocelulární karcinom, stupeň diferenciace většinou G2–3. Vstupní hodnota nádorového markeru antigen skvamózních nádorových buněk (squamous cell carcinoma antigen – SCCA) byla k dispozici u 90 (63,8 %) pacientek a zvýšená hladina byla zaznamenána v 69 (76,7 %) případech. Vstupní hodnota hemoglobinu byla rozdělena dle Radiation Therapy Oncology Group (RTOG) kritérií (nejednalo se sice o toxicitu léčby, pro jejíž hodnocení jsou tato kritéria určena, nicméně tato kritéria jsou obecně známá a jiný způsob odstupňování anemií není v onkologii běžně užívaný) a je zřejmé vyšší zastoupení anemie v podskupině paliativně léčených pacientek (graf 2).
Table 1. Charakteristika souboru pacientek (n = 141). 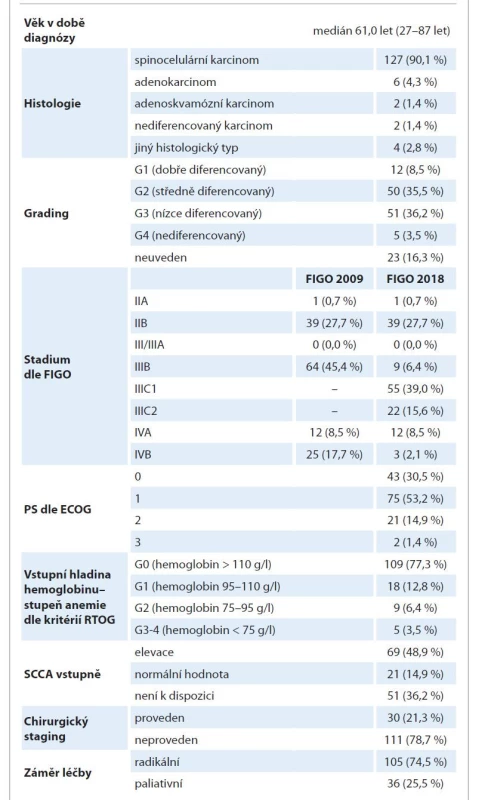
ECOG – Eastern Cooperative Oncology Group, FIGO – International Federation of Gynecology and Obstetrics, G – stupeň závažnosti anémie dle kritérií Radiation Therapy Oncology Group (RTOG), Grading – histopatologický stupeň diferenciace nádorových buněk, PS – performance status, SCCA – nádorový marker spinocelulárních karcinomů Graph 1. Vstupní performance status (PS) dle Eastern Cooperative Oncology Group (ECOG) v podskupinách dle záměru léčby. PS 0 – pacient plně aktivní, bez omezení, PS 1 – pacient soběstačný, mírné příznaky choroby, PS 2 – soběstačný, neschopen práce, mimo lůžko více než 50 % dne, PS 3 – soběstačnost omezena, upoután na lůžko více než 50 % dne, PS 4 – pacient ležící, odkázán na péči. 
Graph 2. Vstupní anemie: stupeň podle kritérií Radiation Therapy Oncology Group (RTOG) v podskupinách dle záměru léčby. G0 – hemoglobin >110 g/l, G1 – hemoglobin 95–110 g/l, G2 – hemoglobin 75–95 g/l, G3 – hemoglobin 50–75 g/l, G4 – hemoglobin < 50 g/l. 
V uvedeném období byla užívána klasifikace FIGO 2009, podle níž byly nejpočetnějšími stadii IIB v 39 (27,7 %) a IIIB v 64 (45,4 %) případech. Za účelem porovnání léčebných výsledků dle klinických stadií bylo provedeno překlasifikování dle FIGO 2018 [14], které ukázalo výrazné početní zastoupení nově ustanovených stadií – IIIC1 v 55 (39,0 %) a IIIC2 v 22 (15,6 %) případech (tab. 1).
Pacientky léčené s kurativním záměrem podstoupily kombinovanou terapii dle standardů ÚRO FNB: EBRT, BRT a CHT. EBRT byla aplikována na oblast pánve, v indikovaných případech vč. oblasti paraaortálních uzlin (PALU) nebo tříselných uzlin v dávce 44–46 Gy ve 22–23 frakcích po 2 Gy, poté radioterapie pokračovala zmenšeným objemem na oblast pánevních uzlin a parametrií do celkové dávky 54–60 Gy normofrakcionovaně po 2 Gy na frakci. Ve sledovaném období byla používána převážně technika 3D konformní radioterapie (3D-CRT). BRT byla prováděna typem HDR (high dose rate) BRT ve fyzikální dávce 24 Gy (ekvivalent low dose rate /LDR/ dávky 36 Gy) v bodě A ve 4 frakcích po 6 Gy. Plánování BRT probíhalo ve 2D na podkladě rentgenových snímků ve dvou kolmých projekcích. Konkomitantně byla podávána CHT cisplatinou (cDDP) v dávce 40 mg/m2 1× týdně ve 4–5 cyklech u pacientek v dobrém celkovém stavu s nepřítomností kontraindikací podání CHT. Celkové trvání léčby se u radikální kombinované léčby pohybovalo mezi 35 a 58 dny, medián 50,0 dne.
Pacientky léčené s paliativním záměrem podstoupily zevní radioterapii – rozvaha o rozsahu cílového objemu a frakcionačním schématu probíhala individuálně dle rozsahu onemocnění, léčebného záměru, stavu pacientky a její motivace k léčbě – ozařovací schéma bylo voleno tak, aby přineslo rychlý efekt při nízké akutní toxicitě a akceptovatelném riziku pozdních nežádoucích účinků s přihlédnutím k očekávané délce života pacientky. U pacientek únosných k intenzivnější léčbě byla aplikována zevní radioterapie na oblast pánve (popř. vč. paraaortálních uzlin) v dávce 44–46 Gy normofrakcionovaně s pokračováním na oblast tumoru, pánevních lymfatických uzlin a parametrií až do celkové dávky 50–60 Gy. U pacientek v celkově horším stavu byla aplikována paliativní dávka na oblast pánve, popř. pouze na oblast tumoru a lymfatických uzlin s užitím různých frakcionačních schémat (25× 2 Gy, 10× 3 Gy, 1× 8 Gy) za účelem paliativního efektu a zmírnění symptomů, zejména krvácení nebo bolesti.
Akutní a pozdní toxicita byla v souboru vyhodnocována dle kritérií RTOG [19]. Pro statistické zpracování dat byla užita Kaplan-Meierova metoda a log rank test.
Výsledky
Z celkového počtu 141 pacientek podstoupilo léčbu s radikálním záměrem 105 (74,5 %) pacientek, paliativní léčba byla aplikována ve 36 (25,5 %) případech. V podskupině radikálně léčených pacientek byla podána kompletní kombinovaná (CH) RT ve > 80 % případů, u ostatních musela být léčba redukována z důvodu horší tolerance léčby nebo překážek k provedení BRT – rozpis zastoupení léčebných modalit je popsán v tab 2.
Table 2. Radikální a paliativní léčba– kombinace léčebných modalit, akutní a pozdní toxicita, relapsy a úmrtí. 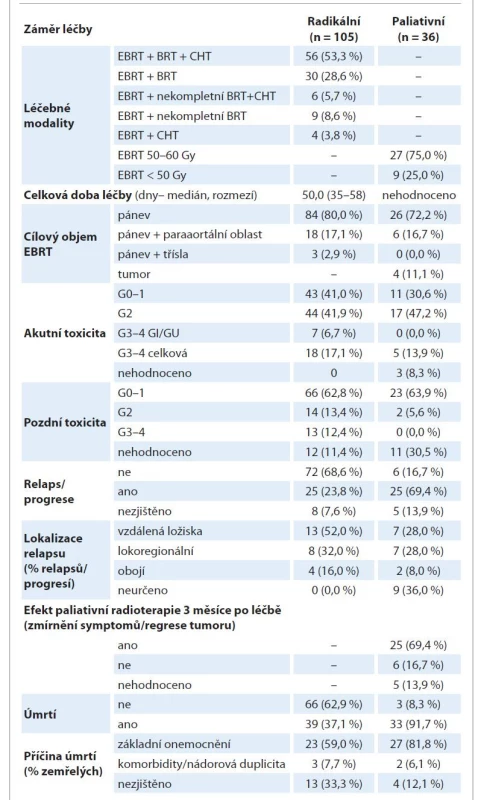
BRT – brachyterapie (za nekompletní BRT byla stanovena aplikace 1–2 frakcí BRT z plánovaných 4 aplikací), CHT – konkomitantní chemoterapie cDDP 1x týdně, EBRT – zevní radioterapie, G – stupeň toxicity léčby dle kritérií Radiation Therapy Oncology Group (RTOG), GI – gastrointestinální trakt, GU – genitourinární trakt, Gy – gray Léčebné výsledky v našem souboru pacientek potvrdily prognostický potenciál vstupního PS (graf 3) a vstupní hodnoty hemoglobinu (graf 4): pacientky vstupně v dobrém stavu nebo bez anemie vykazovaly signifikantně delší přežití ve srovnání s pacientkami ve zhoršeném stavu nebo s anemií.
Graph 3. Celkové přežití dle vstupního performance statusu (PS) dle Eastern Cooperative Oncology Group (ECOG). PS 0 – plně aktivní, bez omezení, PS 1 – soběstačný, mírné příznaky choroby, PS 2 – soběstačný, neschopen práce, upoután na lůžko méně než 50 % dne, PS 3 – soběstačnost omezena, upoután na lůžko více než 50 % dne, PS 4 – ležící, odkázán na péči. 
Graph 4. Celkové přežití dle vstupního stupně anémie podle kritérií Radiation Therapy Oncology Group (RTOG). G0 – hemoglobin >110 g/l, G1 – hemoglobin 95–110 g/l, G2 – hemoglobin 75–95 g/l, G3 – hemoglobin 50–75 g/l, G4 – hemoglobin < 50 g/l. 
Akutní toxicita byla zaznamenávána v průběhu léčby a do 3 měsíců po ukončení léčby. Projevy byly dobře zvládnutelné – většinou se jednalo o stupeň G0–2 dle kritérií RTOG. V podskupině radikálně léčených pacientek byly zjištěny u 7 (6,7 %) pacientek nežádoucí účinky v intenzitě G3–4 v oblasti pánve, tedy gastrointestinální (GI) nebo genitourinární (GU) manifestace, celková akutní toxicita G3–4 (vč. hematologických a kožních nežádoucích účinků) se v této podskupině vyskytla u 18 (17,1 %) pacientek. Akutní toxicita stupně G3–4 se nevyskytla u paliativně léčené podskupiny. Pacientky s významnější akutní toxicitou byly během léčby hospitalizovány k podpůrné léčbě, aby bylo možné dokončit léčbu dle plánu.
EBRT byla kompletně dokončena u všech radikálně léčených pacientek, kompletní BRT (3–4 aplikace) bylo dosaženo u 86 (81,9 %) pacientek, za nekompletní BRT jsme pro účely vyhodnocení považovali 1–2 aplikace BRT, které obdrželo 15 (14,3 %) pacientek.
Konkomitantní CHT byla podána 66 (62,9 %) radikálně léčeným pacientkám. Počet cyklů konkomitantní CHT byl v některých případech limitován z důvodu komorbidit nebo horší tolerance léčby – 4 nebo více cyklů CHT bylo podáno 50 (47,6 %) pacientkám, pro účely hodnocení byly do podskupin s podanou konkomitantní CHT zahrnuty pacientky, které obdržely alespoň 2 cykly CHT (tab. 2).
Jednoznačně byla v našem souboru potvrzena stěžejní role BRT v léčbě karcinomu hrdla děložního – při srovnání kompletnosti léčebného schématu s důrazem na BRT vykazují pacientky s kompletní BRT (3–4 frakce) signifikantně lepší přežití oproti pacientkám s nižším počtem frakcí BRT (1–2 aplikace) nebo při chybějící BRT (tab. 3, graf 5). Signifikantní rozdíl délky přežití byl zaznamenán také při srovnání dávky doručené při BRT do bodu A v podskupině radikálně léčených pacientek (graf 6).
Table 3. Parametry přežití dle provedené léčby. 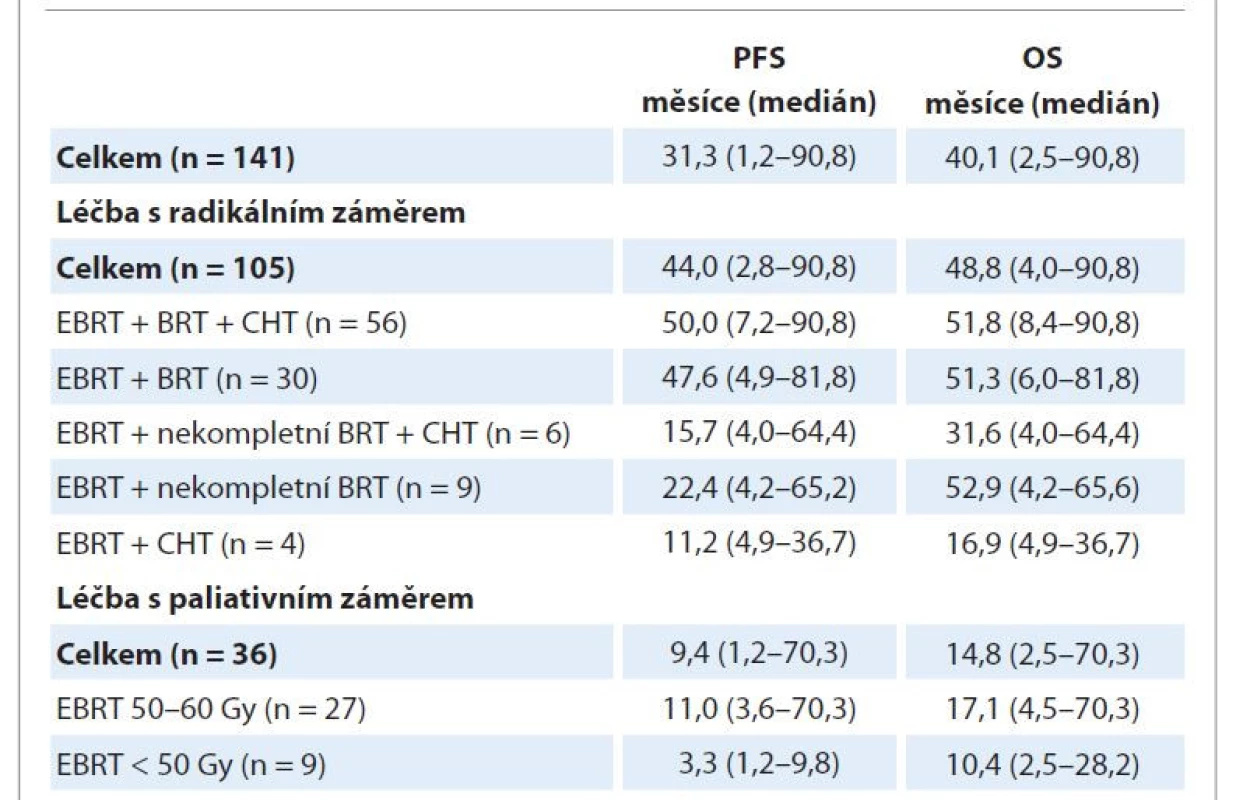
BRT – brachyterapie, CHT– konkomitantní chemoterapie cDDP weekly, EBRT – zevní RT na oblast pánve +/− paraortálních uzlin nebo třísel, Gy – gray, OS – celkové přežití, PFS – doba do progrese Graph 5. Celkové přežití dle kompletnosti léčby v podskupině radikálně léčených pacientek. EBRT – zevní radioterapie, BRT – 3–4 aplikace brachyterapie, nekompletní BRT – 1–2 aplikace brachyterapie, CHT – konkomitantní chemoterapie cDDP 1x týdně. 
Graph 6. Celkové přežití v radikální léčbě dle dávky z brachyterapie (BRT). Dávka v bodě A 24 Gy odpovídá ekvivalentu LDR (low dose rate) BRT 36 Gy, dávka v bodě A 12 Gy odpovídá ekvivalentu LDR 18 Gy. Při jedné aplikaci BRT je doručena dávka 6 Gy do bodu A, ekvivalent LDR 9 Gy. 
Pozdní toxicita byla vyhodnocována při pravidelných kontrolách pacientek po ukončení léčby. Většina pacientek měla dobře zvládnutelné projevy G0–2 dle kritérií RTOG. Pozdní toxicita G3–4 byla zaznamenána u 13 pacientek (9,2 % z celého souboru) – jednalo se o pacientky po radikální léčbě a v této podskupině činí zastoupení pozdní toxicity vážnějšího stupně 12,4 %. V 11 (10,5 %) případech došlo k rozvoji GI toxicity G3–4 (ulcerace, píštěl, ileózní stav), v 1 případě došlo k rozvoji GU toxicity G4 (vezikovaginální píštěl) a u 1 pacientky byla zjištěna fraktura stydké kosti (G4).
Medián doby sledování v celém souboru pacientek je 40 měsíců, v podskupině radikálně léčených pacientek 49 měsíců. Po radikální léčbě byl během sledování zjištěn relaps onemocnění u 25 (23,8 %) pacientek, přičemž ve 13 (52,0 %) případech se jednalo o vzdálená metastatická ložiska. Izolovaná lokoregionální recidiva byla zjištěna u 8 (32,0 %) pacientek a u dalších 4 (16,0 %) pacientek došlo k rozvoji relapsu současně jak lokoregionálně, tak i ve vzdálených lokalizacích. Po paliativní léčbě byla pozorována progrese onemocnění u 25 (69,4 %) pacientek: vzdálená meta ložiska v 7 (28,0 %) případech, lokoregionální progrese u 7 (28,0 %) pacientek, k současné lokoregionální progresi i vzdálené generalizaci došlo ve 2 případech, blíže neurčená nebo nedovyšetřená progrese byla popsána u 9 (36,0 %) pacientek. Bez průkazu relapsu onemocnění tedy ve sledovaném období zůstalo 66 (62,9 %) pacientek po radikální léčbě a 6 (16,7 %) pacientek po paliativní léčbě (tab. 2). Medián PFS dosáhl v celém souboru hodnoty 31,3 měsíce, přičemž v podskupině pacientek léčených s radikálním záměrem byl medián PFS 44,0 měsíce a v podskupině paliativně léčených 9,4 měsíce.
Ve sledovaném období zemřelo 39 (37,1 %) radikálně léčených a 33 (91,7 %) paliativně léčených pacientek, příčinou úmrtí byla většinou progrese základního onemocnění (tab. 2). Medián OS činil v celém souboru 40,1 měsíce, v podskupině radikálně léčených 48,8 měsíce, v paliativně léčené podskupině 14,8 měsíce. Podrobnější shrnutí parametrů přežití v jednotlivých podskupinách pacientek dle rozsahu provedené léčby shrnuje tab. 3.
Paliativní radioterapie potvrdila v našem souboru dobrý efekt – ústup symptomů (většinou se jednalo o krvácení) a klinická regrese tumoru byly zaznamenány u 25 (69,4 %) pacientek, u ostatních 11 (30,6 %) pacientek nebylo efektu dosaženo, nebo nebyl hodnocen (tab. 2). Je zřejmý přínos pro přežití při aplikaci vyšší dávky záření v této podskupině (tab. 3).
Diskuze
Nádory hrdla děložního patří k častým nádorovým onemocněním a většinou jsou díky pravidelnému screeningu zachyceny v neinvazivním in situ stadiu [1], zhruba polovina z invazivních karcinomů však bývá diagnostikována v pokročilém stadiu i přes širokou dostupnost screeningových vyšetření. Již po mnoho desetiletí je základní léčebnou metodou lokálně pokročilého onemocnění kombinovaná radioterapie (EBRT + BRT), v současné době vč. konkomitantní CHT, jejíž přínos byl jednoznačně prokázán. ÚRO FNB se ve spolupráci s Gynekologicko-porodnickou klinikou FNB a dalšími onkogynekologickými pracovišti dlouhodobě věnuje multimodální kombinované léčbě a sledování pacientek s karcinomem hrdla děložního. Statistické zpracování výsledků léčby a toxicity ve vlastních souborech pacientů považujeme obecně za důležité k vyhodnocení efektu i kvality terapie prováděné na pracovišti [20–22] a produktem této činnosti je i prezentovaný soubor pacientek léčených v ÚRO FNB v období 4 let, v rozmezí 2014–2017.
Pacientky v našem souboru podstoupily vstupní stagingová vyšetření v různých kombinacích dle aktuálně platných doporučení, dle indikace lékaře i dle dostupnosti – expertní onkogynekologický UZ, PET/CT trupu, CT hrudníku, břicha a malé pánve, MR pánve. Lapararoskopickou lymfadenektomii pánevních a paraaortálních uzlin podstoupila v našem souboru menšina pacientek a je zřejmý trend delšího přežití v této podskupině, který zřejmě souvisí s dalšími faktory a nebyl podrobněji analyzován.
Ve sledovaném období byla v ÚRO FNB užívána pro léčbu gynekologických tumorů technika 3D konformní radioterapie (3D-CRT). V současné době je již užívána technika radioterapie s modulovanou intenzitou záření (intensity modulated radiation therapy – IMRT) / radioterapie s objemově modulovanou intenzitou (volumetric modulated arc therapy – VMAT) s využitím radioterapie naváděné obrazem (image guided radiation therapy – IGRT) za účelem zpřesnění léčby a snížení toxicity léčby díky lepšímu šetření rizikových orgánů (organ at risk – OaR). Dávkové limity (dose constraints) na oblast OaR jsou definovány vč. šetření kostní dřeně – přínos těchto metod při radioterapii na oblast pánve byl opakovaně prokázán [23].
FIGO provádí pravidelné aktualizace stagingových systémů gynekologických nádorů tak, aby jednotlivá stadia odrážela přesněji prognózu onemocnění a indikaci k léčebným modalitám. Po intenzivních diskuzích v rámci mezinárodních onkogynekologických odborných společností byla v roce 2018 schválena nová klasifikace FIGO [14]. V této klasifikaci byla podskupina pacientek s metastatickým postižením limitovaným na oblast PALU zařazena jako samostatné stadium IIIC2, u nějž je indikována radikální kombinovaná (CH) RT. Postižení PALU je obecně spojeno s horší prognózou ve skupině radikálně léčených pacientek, nicméně díky možnosti kurativní léčby lze v této podskupině dosáhnout lepších výsledků než u dalších pacientek ve stadiu IVB. S těmito změnami FIGO klasifikace korespondují naše léčebné výsledky, které jsme analyzovali pro FIGO 2009 i po překlasifikování dle FIGO 2018. Jsou zde zřejmé výrazně lepší výsledky u stadia IIIC1, resp. IIIC2 ve srovnání se stadiem IIIB, resp. IVB (graf 7). Důvody horšího přežití pacientek ve stadiu IIB v našem souboru nejsou jasné a nebyly podrobněji analyzovány.
Graph 7. Celkové přežití podle stadia onemocnění. Klasifikace International Federation of Gynecology and Obstetrics (FIGO). A) FIGO 2009; B) FIGO 2018. 
V našem dříve publikovaném souboru pacientek léčených pro karcinom hrdla děložního s metastatickým postižením limitovaným na oblast PALU [20] byl potvrzen významný benefit kombinované (CH) RT: v podskupině léčené kombinací EBRT + BRT + CHT bylo dosaženo mediánu PFS 37,3 měsíce, mediánu OS 39,2 měsíce a v podskupině léčené EBRT + BRT činil medián PFS 22,7 měsíce a medián OS 30,3 měsíce [20]. Jedná se tedy o dosažení kratších intervalů než u nemetastatických stadií, ale díky možnosti radikální léčby vč. BRT je zde možnost dosáhnout dlouhodobé kompletní remise u podstatného podílu pacientek.
Kombinovaná (CH) RT karcinomu hrdla děložního přináší pacientkám řadu nežádoucích účinků daných principem prováděné terapie a vlivem jednotlivých léčebných modalit na orgánové systémy. Podpůrná léčba je obecně nedílnou součástí onkologické léčby [24,25] a je nezbytná pro dosažení maximálního léčebného přínosu, k minimalizaci diskomfortu způsobeného léčbou a k zajištění dobré kvality života pacientů v průběhu léčby i během dalšího sledování, což platí obecně pro kurativní i paliativní onkologickou léčbu. Rovnováha protinádorové, podpůrné a paliativní léčby se v průběhu onemocnění mění podle odpovědi na onkologickou léčbu a klinického stavu pacienta [25–27]. Pro dosažení optimálního managementu symptomů je vhodné rozhodování v rámci mezioborového týmu se zapojením odborníků různých specializací dle rizika rozvoje nežádoucích efektů léčby [24–26]; v případě kombinované léčby karcinomu hrdla děložního musí být zapojen klinický a radiační onkolog, onkogynekolog, radiodiagnostik, urolog, gastroenterolog, proktolog, nutriční specialista, klinický farmaceut, klinický psycholog, paliatr a další specializace. Na našem pracovišti je s komplexní podpůrnou léčbou dlouhodobě dobrá zkušenost – akutní nebo pozdní toxicita léčby se v našich souborech [20–22] vyskytuje v míře srovnatelné s literárními údaji a s využitím intenzivní multidisciplinární podpůrné terapie je negativní dopad na kvalitu života pacientek relativně malý a dobře akceptovatelný.
RT s paliativním záměrem přináší obecně benefit pacientům s pokročilým nebo metastatickým nádorovým onemocněním – jedná se o účinnou, efektivní a relativně snadno proveditelnou metodu, která má své pevné místo v rámci komplexní paliativní péče v onkologii [25], a je vhodné ji využívat i v případě pokročilého karcinomu hrdla děložního a dalších gynekologických tumorů [28]. Léčebné výsledky u našeho podsouboru pacientek léčených s paliativním záměrem potvrzují v souladu s literárními údaji významnou roli paliativní radioterapie u této gynekologické malignity.
Závěr
Léčebné výsledky v našem souboru pacientek s lokálně pokročilým karcinomem hrdla děložního léčených kombinovanou (CH) RT potvrdily klíčovou roli BRT pro doručení kurativní dávky do cílového objemu. Pacientky, které podstoupily BRT ve 4 frakcích dle léčebných standardů, vykázaly signifikantně lepší přežití oproti pacientkám s nižším počtem frakcí BRT nebo bez aplikace BRT. Byl potvrzen prognostický potenciál vstupního PS a stupně anemie; u pacientek v celkově dobrém stavu nebo bez anemie v době diagnózy bylo zaznamenáno signifikantně delší přežití. Medián PFS a OS dosáhl v celém souboru hodnoty 31,3, resp. 40,1 měsíce. V podskupině pacientek léčených s radikálním záměrem bylo dosaženo mediánu PFS 44,0 měsíce a OS 48,8 měsíce a v podskupině paliativně léčených činil medián PFS 9,4 měsíce a OS 14,8 měsíce. V podskupině radikálně léčených pacientek byly zjištěny u 7 (6,7 %) pacientek GI nebo GU projevy toxicity v intenzitě G3–4, celková akutní toxicita vč. kožních a hematologických projevů G3–4 se vyskytla u 18 (17,1 %) pacientek. Pozdní toxicita G3–4 byla zaznamenána ve 13 (12,4 %) případech v podskupině pacientek po radikální léčbě. Zastoupení akutních i pozdních nežádoucích účinků je akceptovatelné, ale nyní i do budoucna očekáváme další snížení toxicity léčby díky využití moderních možností EBRT i zavedení 3D BRT s plánováním na podkladě MR snímků. Vzhledem k náročnosti kombinované radikální léčby je pro dosažení maximálního léčebného přínosu nezbytná intenzivní multidisciplinární podpůrná léčba.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
The Editorial Board declares that the manuscript met the ICMJE recommendation for biomedical papers.MUDr. Zdeňka Pechačová
Ústav radiační onkologie
1. LF UK a FN Bulovka
Budínova 67/2
180 81 Praha 8
e-mail: zdenka.pechacova@bulovka.cz
Obdrženo/Submitted: 5. 10. 2021
Přijato/Accepted: 24. 10. 2021
Sources
1. Dušek L, Mužík J, Kubásek M et al. Epidemiologie zhoubných nádorů v České republice. [online]. Dostupné z: http: //www.svod.cz.
2. Stankušová H. Současná radioterapie a chemoterapie ca hrdla děložního. XVI. Jihočeské onkologické dny, abstrakt 009. [online]. Dostupné z: https: //www.linkos.cz/lekar-a-multidisciplinarni-tym/celozivotni-vzdelavani/kongresy/kongresovy-kalendar/xxvi-jihoceske-onkologicke-dny/.
3. Green JA, Kirwan JM, Tierney JF et al. Survival and recurrence after concomitant chemotherapy and radiotherapy for cancer of the uterine cervix: a systematic review and meta-analysis. Lancet 2001; 358 (9284): 781–786. doi: 10.1016/S0140-6736 (01) 05965-7.
4. Chemoradiotherapy for Cervical Cancer Meta-Analysis Collaboration. Reducing uncertainties about the effects of chemoradiotherapy for cervical cancer: a systematic review and meta-analysis of individual patient data from 18 randomized trials. J Clin Oncol 2008; 26 (35): 5802–5812. doi: 10.1200/JCO.2008.16.4368.
5. Cibula D, Pötter R, Planchamp F et al. The European Society of Gynaecological Oncology/European Society for Radiotherapy and Oncology/European Society of Pathology guidelines for the management of patients with cervical cancer. Int J Gynecol Cancer 2018; 28 (4): 641–655. doi: 10.1016/j.radonc.2018.03.003.
6. Modrá kniha České onkologické společnosti, 27. aktualizace. [online]. Dostupné z: https: //www.linkos.cz/lekar-a-multidisciplinarni-tym/personalizovana-onkologie/modra-kniha-cos/aktualni-vydani-modre-knihy/.
7. Národní radiologické standardy – radiační onkologie. Věstník Ministerstva zdravotnictví České republiky 2/2016. Praha 2016.
8. Naga Ch P, Gurram L, Chopra S et al. The management of locally advanced cervical cancer. Curr Opin Oncol 2018; 30 (5): 323–329. doi: 10.1097/CCO.0000000000000471.
9. Gupta S. Adjuvant chemotherapy in locally advanced cervical cancer: the ceiling remains unbroken. J Gynecol Oncol 2019; 30 (4): e97. doi: 10.3802/jgo.2019.30.e97.
10. Gupta S, Maheshwari A, Parab P et al. Neoadjuvant chemotherapy followed by radical surgery versus concomitant chemotherapy and radiotherapy in patients with stage IB2, IIA, or IIB squamous cervical cancer: a randomized controlled trial. J Clin Oncol 2018; 36 (16): 1548–1555. doi: 10.1200/JCO.2017.75.9985.
11. Benson R, Pathy S, Kumar L et al. Locally advanced cervical cancer – neoadjuvant chemotherapy followed by concurrent chemoradiation and targeted therapy as maintenance: a phase II study. J Cancer Res Ther 2019; 15 (6): 1359–1364. doi: 10.4103/jcrt.JCRT_39_18.
12. Kagabu M, Nagasawa T, Sato C et al. Immunotherapy for uterine cervical cancer using checkpoint inhibitors: future directions. Int J Mol Sci 2020; 21 (7): 2335. doi: 10.3390/ijms21072335.
13. Mouková L, Nenutil R, Fabian P et al. Prognostické faktory karcinomu děložního hrdla. Klin Onkol 2013; 26 (2): 83–90. doi: 10.14735/amko201383.
14. Sehnal B, Kmoníčková E, Sláma J et al. Současný FIGO staging karcinomu děložního hrdla a léčba jednotlivých stadií. Klin Onkol 2019; 32 (3): 224–231. doi: 10.14735/amko2019224.
15. Gill BS, Lin JF, Krivak TC et al. National Cancer Data Base analysis of radiation therapy consolidation modality for cervical cancer: the impact of new technological advancements. Int J Radiat Oncol Biol Phys 2014; 90 (5): 1083–1090. doi: 10.1016/j.ijrobp.2014.07. 017.
16. Fischerova D, Cibula D, Stenhova H et al. Transrectal ultrasound and magnetic resonance imaging in staging of early cervical cancer. Int J Gynecol Cancer 2008; 18 (4): 766–772. doi: 10.1111/j.1525-1438.2007.01072.x.
17. Haldorsen IS, Lura N, Blaakær J et al. What is the role of imaging at primary diagnostic work-up in uterine cervical cancer? Curr Oncol Rep 2019; 21 (9): 77. doi: 10.1007/s11912-019-0824-0.
18. Viswanathan C, Faria S, Devine C et al. [18F]-2-fluoro-2-deoxy-D-glucose-PET assessment of cervical cancer. PET Clin 2018; 13 (2): 165–177. doi: 10.1016/j.cpet.2017.11. 004.
19. Cox JD, Stetz J, Pajak TF. Toxicity criteria of the Radiation Therapy Oncology Group (RTOG) and the European Organization for Research and Treatment of Cancer (EORTC). Int J Radiat Oncol Biol Phys 1995; 31 (5): 1341–1346. doi: 10.1016/0360-3016 (95) 00060-C.
20. Pála M, Holečková P, Veselý J et al. Konkomitantní chemoradioterapie v léčbě nádorů ORL oblasti. Výsledky ÚRO 2002-2005. Klin Onkol 2007; 20 (3): 248–252.
21. Holečková P, Pála M, Mašek M et al. Retrospektivní hodnocení léčebných výsledků u pacientů s nasofaryngeálním karcinomem léčených v ÚRO FNB Praha od roku 1990 do roku 2005. Klin Onkol 2007; 20 (1): 35–37.
22. Pechačová Z, Kmoníčková E, Zikán M et al. Léčba karcinomu hrdla děložního s postižením paraaortálních uzlin – retrospektivní hodnocení vlastního souboru. Klin Onkol 2020; 33 (2): 123–131. doi: 10.14735/amko2020123.
23. Lohynská R, Nýdlová A, Drbohlavová T et al. Hematologická toxicita u IMRT/VMAT v kurativní léčbě análního karcinomu. Klin Onkol 2020; 33 (4): 288–294. doi: 10.14735/amko2020288.
24. Sochor M, Sláma O, Loučka M. Časná integrace paliativní péče do standardní onkologické péče – benefit, limitace, bariéry a druhy paliativní péče. Klin Onkol 2015; 28 (3): 171–176. doi: 10.14735/amko2015171.
25. Pechačová Z, Končeková J, Lohynská R et al. Paliativní radioterapie v managementu symptomů pokročilého onkologického onemocnění. Onkologie 2020; 14 (6): 271–277.
26. Vorlíček J, Skřičková J. Paliativní léčba u onkologických nemocných. Klin Onkol 1993; 6 (4): 119–122.
27. Klastersky J. Podpůrná léčba onkologicky nemocných. Klin Onkol 1994; 7 (1): 9–13.
28. Skliarenko J, Barnes EA. Palliative pelvic radiotherapy for gynaecologic cancer. [online]. Available from: https: //link.springer.com/article/10.1007/s13566-012-0050-y.
Labels
Paediatric clinical oncology Surgery Clinical oncology
Article was published inClinical Oncology

2022 Issue 2-
All articles in this issue
- Předsednictví Francie a České republiky v Radě Evropské unie – informace k významným akcím v oblasti onkologie
- Akupunktura z pohledu medicíny založené na důkazech – možnosti klinického využití na podkladě doporučení National Comprehensive Cancer Network (NCCN)
- Hepatocelulární karcinom – prognostická kritéria individualizované léčby
- Rehabilitácia a pohybová aktivita pri gynekologických onkologických ochoreniach
- Radioterapie a radiosenzitivní syndromy u mutací genů reparace DNA
- Koherencí řízená holografická mikroskopie – nástroj pro hledání nových biomarkerů dlaždicobuněčného karcinomu hlavy a krku
- Metabolický syndróm u pacientov po alogénnej transplantácii kmeňových krvotvorných buniek
- Kombinovaná chemoradioterapie karcinomu hrdla děložního – retrospektivní hodnocení vlastního souboru
- Aktuality z odborného tisku
- Informace z České onkologické společnosti
- Pozdní nástup plicní a srdeční toxicity u pacienta léčeného checkpoint inhibitorem v monoterapii
- Ruptura podklíčkové tepny hrozící po chemoradioterapii
- Clinical Oncology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Akupunktura z pohledu medicíny založené na důkazech – možnosti klinického využití na podkladě doporučení National Comprehensive Cancer Network (NCCN)
- Radioterapie a radiosenzitivní syndromy u mutací genů reparace DNA
- Hepatocelulární karcinom – prognostická kritéria individualizované léčby
- Rehabilitácia a pohybová aktivita pri gynekologických onkologických ochoreniach
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

