-
Medical journals
- Career
Integrovaná diagnostika difúzních gliomů
Authors: M. Hendrych 1; H. Valeková 2; T. Kazda 3; R. Lakomý 4; J. Šána 5; R. Jančálek 2; O. Slabý 5; M. Hermanová 1
Authors‘ workplace: I. ústav patologie, LF MU a FN u sv. Anny v Brně 1; Neurochirurgická klinika LF MU a FN U sv. Anny v Brně 2; Klinika radiační onkologie LF MU a MOÚ Brno 3; Klinika komplexní onkologické péče LF MU a MOÚ Brno 4; CEITEC – Středoevropský technologický institut, MU Brno 5
Published in: Klin Onkol 2020; 33(4): 248-259
Category: Review
doi: https://doi.org/10.14735/amko2020248Overview
Klasifikace nádorů centrálního nervového systému (CNS) Světové zdravotnické organizace (World Health Organization – WHO) zaznamenala v posledních letech zásadní změny. V současnosti platná revidovaná WHO klasifikace nádorů CNS z roku 2016 zavádí koncept tzv. integrované diagnostiky, inkorporující kromě histopatologického morfologického nálezu a imunofenotypu i molekulárně-genetické charakteristiky nádoru. Výsledná integrovaná diagnóza tedy zahrnuje jak tradiční morfologické a růstové charakteristiky nádoru vč. jeho histopatologického gradu, tak konkrétní molekulární biomarkery. Klasifikace nádorů založená na kombinaci fenotypu a genotypu nádorů umožňuje přesnější prognostickou stratifikaci, zvyšuje objektivitu diagnostiky a umožňuje lépe predikovat odpověď na protinádorovou léčbu. V roce 2017 bylo současně ustanoveno mezinárodní konsorcium (The Consortium to Inform Molecular and Practical Approaches to CNS Tumor Taxonomy – not official WHO (cIMPACT-NOW)), které v obdobích mezi vydáním jednotlivých WHO klasifikací nádorů CNS tvoří a formuluje praktická doporučení pro integrovanou diagnostiku nádorů CNS a budoucí WHO klasifikaci. Začlenění molekulárních biomarkerů do integrované diagnostiky zásadním způsobem změnilo zejména klasifikaci difúzních gliomů, které v sobě zahrnují jednotky s odlišnými morfologickými charakteristikami, genetickými alteracemi a biologickým chováním. Přehledová práce shrnuje základní morfologické, imunofenotypické a molekulárně genetické charakteristiky difúzních gliomů v rámci integrované diagnostiky dle platné WHO klasifikace nádorů CNS 2016 a následných doporučení diagnostických postupů.
Klíčová slova:
difúzní gliomy – integrovaná diagnóza – WHO 2016
Úvod
Gliomy přestavují nejčastější primární nádory mozku, reprezentující až 75 % primárních malignit mozku, s nejvyšším zastoupením glioblastomu. Definujícím znakem difúzních astrocytárních a oligodendroliálních nádorů je difúzní infiltrativní charakter růstu v mozku či míše bez zřetelného ohraničení nádorového infiltrátu.
V rámci integrované diagnostiky dle revidované WHO klasifikace nádorů centrálního nervového systému (CNS) 2016 [1] jsou difúzní astrocytární a oligodendrogliální nádory klasifikovány na základě mutačního statu IDH (izocitrátdehydrogenázy) jako IDH-mutované nebo IDH-wildtype difúzní gliomy (tab. 1). IDH-mutované nádory jsou dále členěny na IDH-mutované astrocytární nádory a oligodendrogliomy, IDH-mutované, s kodelecí 1p/19q. IDH-mutované low grade difúzní gliomy (WHO grade (G) II) se vyznačují potenciálem progrese v high grade anaplastické gliomy (WHO G III). resp. u astrocytárně diferencovaných nádorů až v glioblastom (WHO G IV). Glioblastomy vznikající progresí z IDH-mutovaných astrocytomů nižšího gradu jsou označovány jako sekundární glioblastomy, na rozdíl od primárních de novo vznikajících, téměř výhradně IDH-wildtype glioblastomů. Samostatně definovanou jednotku představuje v rámci nové integrované diagnostiky difúzní středočarový gliom, s mutací K27M v genech pro histon 3 (H3) [2].
Integrovaná diagnostika gliomů samostatně vyčleňuje skupinu gliomů, pro které je typický ohraničený typ růstu, postrádají mutace IDH genů a jsou často nositeli alterací genu BRAF. Jde o pilocytární astrocytom WHO G I, pleomorfní xantoastrocytom WHO G II nebo III a subependymální obrovskobuněčný astrocytom WHO G I [2].
Integrovaná diagnostika vyžaduje aplikaci rozsáhlého spektra molekulárně-patologických a genetických vyšetření do rutinní diagnostické praxe. V současnosti jsou široce využívány zejména metodiky detekující alterace jednotlivých genů a jejich genových produktů (imunohistochemie, cytogenetické přístupy (např. fluorescenční in situ hybridizace (FISH), techniky polymerázové řetězové reakce (polymerase chain reaction – PCR) a Sangerova metoda či pyrosekvenování). Metody sekvenování nové generace (next generation sequencing, NGS) umožňují současné analýzy více genů, jak na přítomnost mutací a fúzí, tak na detekci změn počtu kopií příslušných genů. V současnosti jsou komerčně dostupné genové panely pro identifikaci genetických alterací v mozkových nádorech vč. gliomů, umožňující v rutinní diagnostické praxi vyšetření biomarkerů s významem nejen diagnostickým, ale i prognostickým a prediktivním.
Doporučené diagnostické postupy difúzních gliomů respektují platnou revidovanou WHO klasifikaci nádorů CNS 2016 a inkorporují recentní doporučení mezinárodního konsorcia neuropatologů a klinických neuroonkologů (The Consortium to Inform Molecular and Practical Approaches to CNS Tumor Taxonomy – not official WHO (cIMPACT-NOW)), které prezentuje praktická doporučení pro tkáňovou diagnostiku mozkových nádorů na základě nových informací a recentních
zjištění [3].Histologická klasifikace a grading difúzních gliomů
Diagnostickou kaskádu zahajuje standardní histopatologické vyšetření a posouzení růstových charakteristik nádoru, jeho diferenciace a stanovení histopatologického gradu. Difúzní gliomy jsou charakterizovány infiltrativním typem růstu v mozkové tkáni, neostrým ohraničením nádorového infiltrátu, průkaznou přítomností reziduální tkáně CNS mezi buňkami nádorového infiltrátu, klesající denzitou nádorových buněk směrem od centra nádoru do periferie a přítomností vysoce specifických tzv. sekundárních struktur difúzně rostoucího gliomu v okraji invazivní fronty gliomu. Zde identifikujeme infiltraci nádorovými buňkami perineuronálně (obraz tzv. perineuronální satelitózy), perivaskulárně a subpiálně. Imunohistochemický průkaz exprese neurofilament v reziduálních axonech mezi nádorovými buňkami podporuje průkaz infiltrativního charakteru růstu difúzních gliomů a jejich diferenciální diagnostiku vzhledem ke gliomům s ohraničeným typem růstu. Tato diferenciální diagnostika je komplikovaná zejména v případech, kdy je pro diagnostické účely k dispozici pouze centrum tumoru a posouzení okraje invazivní fronty difúzně rostoucího gliomu není možné [1].
Difúzní gliomy morfologicky vykazují známky astrocytární (fibrilární či méně často gemistocytární) nebo oligodendrogliální diferenciace. Konvenční známky fibrilární astrocytární diferenciace nádorových buněk zahrnují přítomnost buněk s nenápadnou cytoplazmou, s protáhlými hyperchromními jádry, s jadernými atypiemi a nepravidelnostmi jaderných kontur. Gemistocytárně diferencované buňky se vyznačují objemnou eosinofilní cytoplazmou a krátkými větvícími se výběžky. Oligodendrogliálně diferencované buňky jsou charakterizovány přítomností uniformních kulatých či oválných jader, ostrými jadernými hranicemi, jemně zrnitým chromatinem a perinukleárním projasněním cytoplazmy, s charakteristickou sítí jemných větvících se kapilár na pozadí (obr. 1) [4,5]. U části difúzních gliomů lze morfologicky prokázat přítomnost směsné populace nádorových buněk, oligo - a astrocytárně diferencovaných, či přechodných buněčných typů. Současná klasifikace nádorů CNS WHO 2016 jednotku oligoastrocytomu prakticky eliminovala, difúzní a anaplastický oligoastrocytom přestavují pouze provizorní jednotky, které jsou ve většině případů po provedení molekulárních testů a integrované diagnostiky re-klasifikovány jako astrocytomy (IDH-mutované nebo IDH-wildtype) či oligodendrogliomy (IDH-mutované, s kodelecí 1p/19q) příslušných gradů. Pouze v případě, že molekulární testy nemohou být provedeny či jejich výsledky jsou nekonkluzivní, je oprávněná diagnóza oligoastrocytomu resp. anaplastického oligoastrocytomu, NOS (Not Otherwise Specified) resp. NEC (Not Elsewhere Specified). Zcela raritně byly popsány případy difúzních gliomů s distinktními komponentami astrocytární a oligodendrogliální, morfologicky i molekulárně geneticky, které však v současném klasifikačním schématu nepředstavují samostatné definované jednotky [6].
Image 1. Typická morfologie infiltrujících gliomů.
A) Difúzní astrocytom, středně celulární nádorová proliferace tvořena atypickými fibrilárními astrocyty.
B) Glioblastom, hypercelulární tumor s palisádující nekrózou.
C) Oligodendrogliom, středně celulární proliferace oválných buněk s perinukleárním projasněním v síti bohatě větvených kapilár.
D) Anaplastický oligodendrogliom, hypercelulární proliferace s briskní mitotickou aktivitou.
A–D) Hematoxylin-eozin, původní zvětšení 200×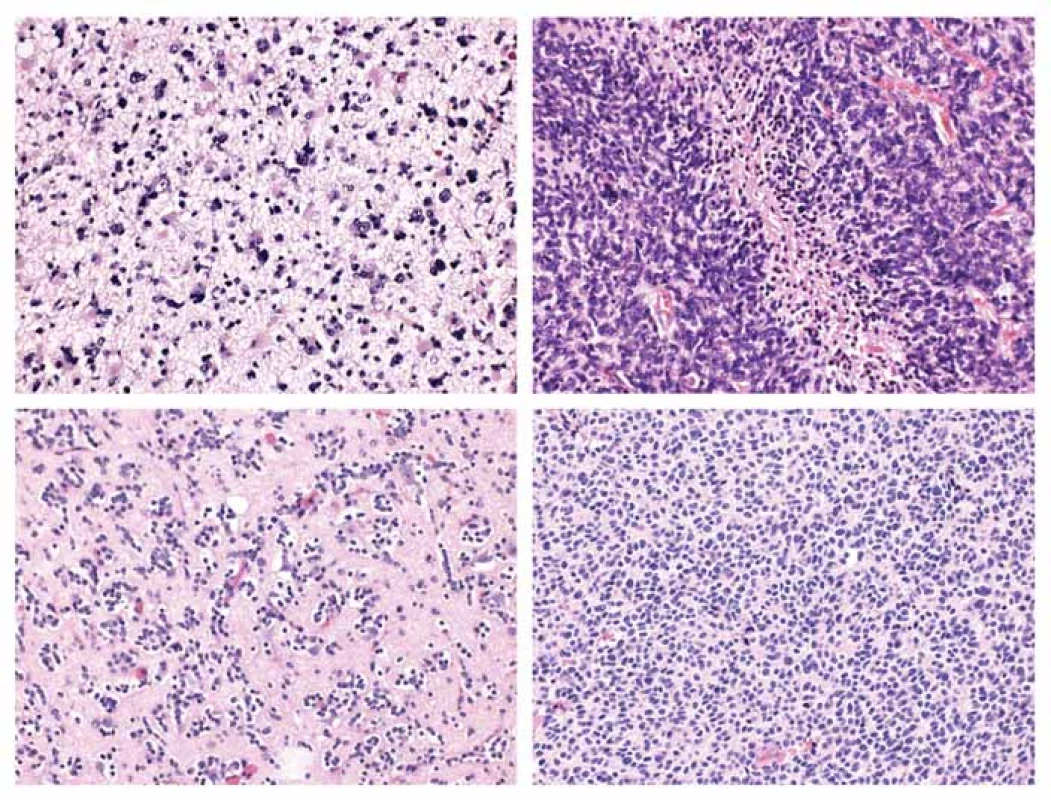
Glioblastomy mohou vykazovat i morfologii sarkomatoidní, epiteloidní či obrovskobuněčnou, reflektovanou v platné WHO klasifikaci přítomností variantních jednotek této jednotky (tab. 1). Gliomatosis cerebri nepředstavuje v klasifikaci WHO 2016 distinktní jednotku, reprezentuje infiltrativní charakter růstu difúzních astrocytárních a oligondrogliálních tumorů. Zrušení této jednotky je však kontroverzní [1].
Table 1. WHO 2016 klasifi kace difúzních gliomů vč. recentních doporučení cIMPACT-NOW. 
*provizorní jednotka ve WHO 2016 klasifi kaci nádorů CNS **dle doporučení cIMPACT-NOW difúzní a anaplastické astrocytomy, IDHwt, ve kterých byly identifi kována amplifi kace EGFR a/nebo kompletní ztráta chromozomu 10 v kombinaci se ziskem chromozomu 7 (-10/+7) a/nebo mutace v promotorové oblasti genu TERT, klasifi kovat jako difúzní astrocytární gliomy, IDHwt, s molekulárními znaky glioblastomu, WHO grade IV cIMPACT-NOW – mezinárodní konsorcium neuropatologů a neuroonkologů The Consortium to Inform Molecular and Practical Approaches to CNS Tumor Taxonomy – not offi cial WHO, ICD-O – mezinárodní klasifi kace onemocnění pro onkologii, NOS – Not Otherwise Specifi ed Grading difúzních gliomů je v rámci WHO 2016 klasifikace nádorů CNS stále založen na histopatologickém morfologickém vyšetření, vychází z hodnocení celularity, přítomnost cytonukleárních atypií (jaderné i buněčné variability, tvarové i velikostní, hyperchromazie jader), známek anaplazie (ztráty diferenciace), signifikantní mitotické aktivity a přítomnosti mikrovaskulárních proliferátů a nekróz. WHO G II difúzních astrocytomů je definován přítomností jaderných atypií, WHO G III anaplastické astrocytomy jsou charakterizovány zvýšenou mitotickou aktivitou, obvykle provázenou i výraznějšími cytonukleárními atypiemi a hypercelularitou, definujícím znakem WHO G IV glioblastomů je pak přítomnost mikrovaskulárních proliferátů a/nebo nekróz, geografických či často palisádujících. Konvenční oligodendrogliomy představují WHO G II difúzní gliomy, přičemž hypercelularita, přítomnost jaderných atypií, nekrotizace, mikrovaskulárních proliferátů a briskní mitotické aktivity podmiňuje diagnózu WHO G III anaplastického oligodendrogliomu (obr. 2) [1].
Image 2. Grading.
A) Cytonukleární atypie a briskní mitotická aktivita u anaplastického astrocytomu.
B) Palisádující nekróza zachycena v glioblastomu.
C+D) Glomeruloidní vaskulární proliferát zastižen u glioblastomu.
D) Imunohistochemické vyšetření exprese CD31.
A–C) Hematoxylin-eozin, původní zvětšení 200×, D) Původní zvětšení 100×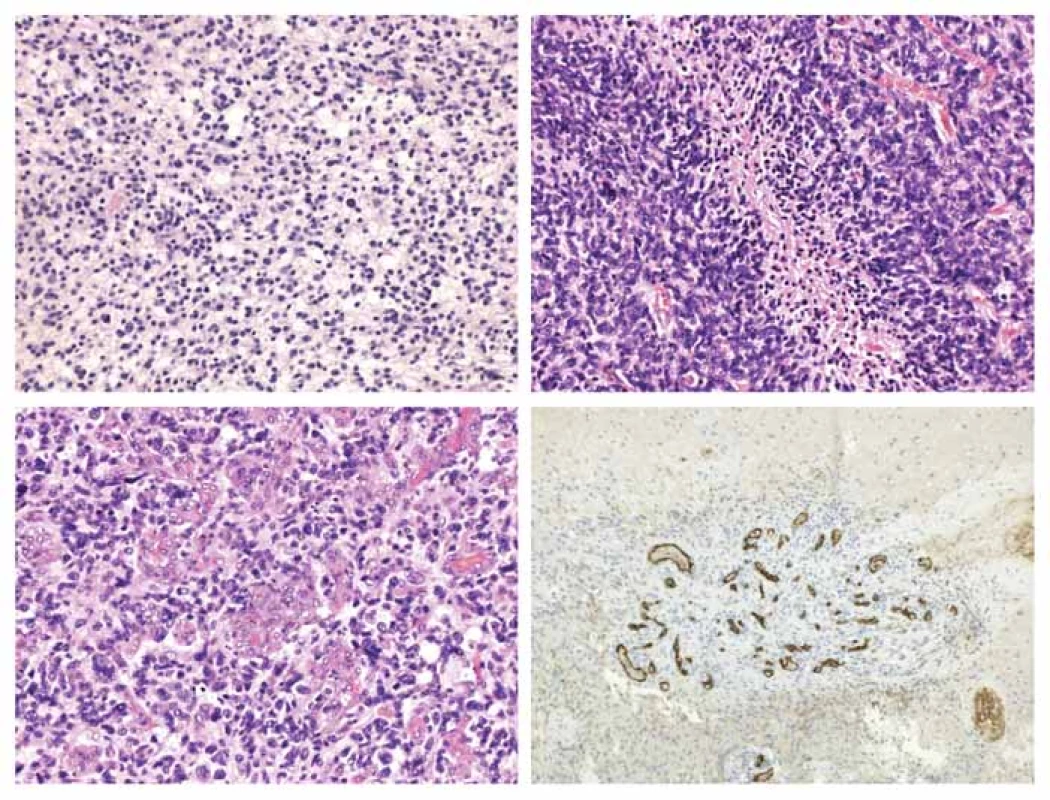
Výjimku z tohoto schématu představuje difúzní středočarový gliom, H3-K27-mutovaný, který je vzhledem ke své nepříznivé prognóze vždy klasifikován jako WHO G IV, bez ohledu na morfologicky stanovený grade. Obdobně by dle recentních doporučení mezinárodního konsorcia cIMPACT-NOW měly být klasifikovány gradem IV také difúzní astrocytární gliomy, IDH-wildtype, s molekulárními znaky glioblastomu [7].
IDH mutační analýza a diferenciální diagnostika IDH-mutovaných difúzních gliomů
Součástí standardního diagnostického postupu je v rámci integrované diagnostiky stanovení mutačního statu IDH (schéma 1). Mutace R132 genu IDH1 nebo R172 genu IDH2 byly prokázány v 80–90 % adultních WHO G II a GIII difúzních astrocytomů, oligodendrogliomů a sekundárních glioblastomů. Izocitrátdehydrogenáza představuje enzym, který je zodpovědný za konverzi izocitrátu na -ketoglutarát v citrátovém cyklu. Mutovaná forma IDH navíc získává schopnost katalyzovat redukci -ketoglutarátu na D-2-hydroxyglutarát, onkometabolit, který interferuje s celou řadou buněčných procesů a nepřímo inhibuje transkripci důležitých tumor supresorových genů a přispívá ke vzniku IDH-mutovaného difúzního gliomu [8]. Mutace R132H genu IDH1 vznikající substitucí
c.395G>A a vedoucí k záměně argininu za histidin v polypeptidovém řetězci (mutace měnící smysl; missense mutation) představuje nejčastější mutaci a je detekovatelná imunohistochemicky vysoce senzitivní a specifickou protilátkou proti takto mutovanému proteinu. Imunohistochemicky prokázaná pozitivita IDH1–R132H (obr. 3A) potvrzuje diagnózu IDH-mutovaného difúzního gliomu. U imunohistochemicky IDH1-R132H negativních nádorů (obr. 3B) je za účelem identifikace vzácnějších mutací IDH genů indikována sekvenace kodonu 132 genu IDH1 a kodonu 172 genu IDH2 [9]. Sekvenace genů IDH není v případě negativity imunohistochemického vyšetření indikována u pacientů starších 54 let, s histologicky klasickým glioblastomem v nestředočarové lokalizaci, bez gliomu nižšího gradu či gliomu ve středočarové lokalizaci v anamnéze. V těchto případech je pravděpodobnost výskytu mutace IDH zanedbatelná a pro průkaz statu IDH-wildtype je dostačující negativní imunohistochemické vyšetření exprese IDH1-R132H [10].Image 3. Imunohistochemické vyšetření exprese IDH1-R132H, ATRX a p53.
A) Pozitivní reakce prokazující mutaci R132H genu IDH1.
B) Negativní reakce vylučující mutaci R132H genu IDH1.
C) Wildtype nukleární exprese ATRX.
D) Ztráta nukleární exprese ATRX v jádrech nádorových buněk při zachované nukleární expresi v nenádorových buňkách – průkaz mutace genu ATRX.
E) Wildtype nukleární exprese p53.
F) Akumulace mutovaného proteinu p53 intranukleárně.
A–F) Původní zvětšení 200×
Schéma 1. Algoritmus pro vyšetření genů IDH. IDH – izocitrátdehydrogenáza 
Integrovaná diagnostika difúzních gliomů definuje oligodendrogliomy jako nádory IDH mutované, s kodelecí 1p/19q. Vyšetření kodelecí 1p/19q tedy stratifikuje IDH-mutované astrocytomy a IDH-mutované oligodendrogliomy s kodelecí 1p/19q. Genotyp je v rámci integrované diagnostiky nadřazen fenotypu difúzního gliomu. IDH-mutovaný difúzně rostoucí gliom je klasifikován jako oligodendrogliom i v případě astrocytární morfologie, pokud je prokázána kodelece 1p/19q. Pro diagnózu oligodendrogliomu je rozhodující pouze kompletní ztráta obou chromozomálních ramének asociována se signifikantně delším přežíváním pacientů. Inkompletní chromozomální ztráty v předmětných lokalizacích nejsou pro diagnózou oligodendrogliomu určující, a naopak jsou často identifikovány v astrocytárních tumorech [11]. Pro detekci delecí 1p/19q je v praxi nejčastěji využívána fluorescenční in situ hybridizace (FISH), která se však vyznačuje rizikem falešně pozitivního výsledku průkazu kodelecí 1p/19q vzhledem k tomu, že nejčastěji využívané a komerčně dostupné proby se váží na distální konce ramének chromozomů 1 a 19, s čímž je spojeno riziko průkazu pouze fokální delece. Doporučené postupy molekulárního testování kodelecí 1p/19q tedy zahrnují metodiky umožňující identifikaci kompletních ztrát chromozomálních ramének (např. MLPA (Multiplex Ligation-dependent Probe Amplification), array CGH (comparative genomic hybridization) nebo analýza variability počtu kopií vybraných sekvencí (copy number variation; CNV) pomocí NGS). Možné a v budoucnu žádoucí je využití FISH s komerčně dostupnými probami detekujícími proximálnější úseky sledovaných chromozomálních ramének.
V IDH-mutovaných astrocytomech je častá alterace genu ATRX (a-thalassemia mental retardation syndrom X-linked), obvykle provázená i mutacemi v tumor supresorového genu TP53. ATRX představuje protein hrající roli v zachování chromatinové struktury telomer. Inaktivační mutace ATRX je asociovaná s procesem alternativního prodlužování telomer, esenciálního procesu poskytující nádorové buňce schopnost se nekonečně množit [12]. Jaderná exprese ATRX je rutinně vyšetřována imunohistochemicky, mutace ATRX jsou obvykle asociovány se ztrátou jaderné exprese ATRX (obr. 3C, D). Hodnocení imunohistochemických vyšetření exprese ATRX vyžaduje velkou pozornost, je citlivé na postupy v preanalytické fázi (např. fixaci) a pro průkaz ztráty jaderné exprese ATRX v nádorových buňkách indikující přítomnost mutovaného ATRX je nutná přítomnost interní pozitivní kontroly – průkazná exprese ATRX v buňkách nenádorového pozadí, endoteliálních, zánětlivých, atd. v hodnoceném
úseku.Interpretace výsledků imunohistochemického vyšetření exprese p53 vyžaduje rovněž velkou pozornost. Většina mutací TP53 jsou tzv. „missense“ mutace, v důsledku kterých dochází k jaderné akumulaci proteinu. Imunohistochemické vyšetření není senzitivní ani specifické pro průkaz mutací TP53 a musí být interpretováno v kontextu s morfologií a dalšími imunohistochemickými a molekulárně genetickými nálezy. Pouze případy vykazující extenzivní a silnou jadernou pozitivitu p53 ve více než 10 % gliálních buněk mohou být s velkou pravděpodobností interpretovány jako p53 pozitivní/TP53 mutované a současně absence jaderné pozitivity p53 nevylučuje mutovaný TP53 (např. v důsledku delece TP53) (obr. 3E, F) [13].
Doporučení cIMPACT-NOW konsorcia umožňuje integrovanou diagnózou IDH-mutovaného astrocytomu pro případ difúzních gliomů histologicky s astrocytární morfologií, s imunohistochemicky prokázanou ztrátou jaderné exprese ATRX a/nebo silnou difúzní imunopozitivitou p53 bez nutnosti dalšího testování na přítomnost kodelecí 1p/19q. Genotyp difúzního gliomu IDH/ATRX a/nebo TP53 mutovaný je tedy konzistentní s diagnózou astrocytomu [7].
V diagnostickém algoritmu je nutné vzít v úvahu i skutečnost, že ne všechny mutace ATRX jsou asociovány se ztrátou jaderné exprese ATRX a přítomnost jaderné exprese ATRX v IDH-mutovaném nádoru nevylučuje diagnózu astrocytomu. U IDH-mutovaných difúzních gliomů se zachovalou jadernou expresí ATRX a bez signifikantní imunopozitivity p53 je tedy indikováno vyšetření kodelecí 1p/19q pro vyloučení diagnózy oligodendrogliomu i v případech, kdy morfologický histopatologický nález není pro oligodendrogliom typický (schéma 2).
Schéma 2. Diagnostický algoritmus IDH-mutovaných difúzních gliomů. IDH – izocitrátdehydrogenáza 
Telomerázová reverzní transkriptáza (TERT) představuje funkční jednotku enzymu telomerázy, která se uplatňuje v procesu zachování délky telomer při buněčném dělení, zamezující jejich zkracování. Mutace v promotorové oblasti genu TERT byly prokázány i v difúzních gliomech, v oligodendrogliomech a primárních glioblastomech. Mutace promotoru TERT se téměř nevyskytují v IDH-mutovaných astrocytomech, kde se preferenčně uplatňuje v procesu zachování délky telomer mutovaný ATRX, obvykle provázený i mutacemi TP53. Sekvenace promotorové oblasti genu TERT představuje účinný nástroj pro detekci této alterace, imunohistochemický průkaz TERT nekoreluje s mutačním statem TERT. Amplifikace TERT či rearanže promotoru TERT představují alternativní mechanismy zachování délky
telomer [12].IDH-wildtype difúzní gliomy
Většina difúzně/infiltrativně rostoucích gliomů bez mutace v genech IDH1/2 vykazuje morfologické charakteristiky glioblastomu a je takto klasifikována (glioblastom, IDH-wildtype, WHO G IV). Ztráta jaderné exprese ATRX v IDH-wildtype difúzních gliomech obvykle není vyjádřena.
IDH-wildtype difúzní astrocytomy (WHO G II) a anaplastické astrocytomy (WHO G III) představují v platné WHO 2016 klasifikaci nádorů CNS provizorní jednotky a zahrnují v sobě nádory s rozdílným biologickým chování a prognózou [1].
U dospělých se IDH-wildtype difúzní a anaplastické astrocytomy vyskytují poměrně často, zejména ve vyšších věkových skupinách. Ve srovnání s hlavními onkologickými diagnózami jako jsou nádory prsu, plic nebo prostaty se však jedná o onemocnění vzácná. Přes absenci morfologických znaků WHO grade IV glioblastomu často vykazují molekulárně-patologické alterace typické pro IDH-wildtype glioblastomy, vyznačují se nepříznivou prognózou a predisponují k obdobnému biologickému chování jako primární glioblastom, přestože morfologicky nesplňují kritéria pro zařazení do WHO grade IV kategorie. cIMPACT-NOW konsorcium tedy doporučuje u wildtype difúzních a anaplastických astrocytomů vyšetření genetických alterací typických pro glioblastom a v případě prokázané amplifikace genu pro receptor epidermálního růstového faktoru (EGFR) na 7. chromozomu a/nebo mutace v promotoru TERT a/nebo kompletní ztráty chromozomu 10 v kombinaci se ziskem chromozomu 7 (–10/+7), klasifikovat tyto nádory jako difúzní astrocytární gliomy, IDH-wildtype, s molekulárními znaky glioblastomu, WHO grade IV (schéma 3). Amplifikaci genu EGFR s následnou overexpresí EGFR receptorů vykazuje 40–50 % IDH-wildtype glioblastomů. U asi poloviny EGFR amplifikovaných primárních glioblastomů lze prokázat přítomnost intragenové delece exonů 2–7 produkující trvale aktivní variantu EGFR, tzv. EGFRvIII. Přítomnost této deleční varianty EGFR lze prokázat imunohistochemicky, standardní průkaz amplifikace EGFR je metodou FISH [14].
Schéma 3. Diagnostický algoritmus IDH-wildtype difúzních gliomů. Tmavě modře podbarvené jednotky jsou součástí doporučení cIMPACT-NOW a nejsou specifikovány v platné WHO klasifikaci nádorů centrálního nervového systému 2016. cIMPACT-NOW – mezinárodní konsorcium neuropatologů a klinických neuroonkologů, IDH – izocitrátdehydrogenáza 
Až 40 % IDH-wildtype glioblastomů vykazuje hypermetylaci promotoru genu MGMT (O-6-metylguanin-DNA metyltrasferáza), což je asociováno s lepší odpovědí na terapii alkylačními agens vč. temozolomidu, nejčastěji používaného cytostatika v neuroonkologii. Vyšetření metylace promotoru MGMT u IDH-wildtype high grade gliomů tedy přináší důležité informace prediktivního charakteru, průkaz hypermetylace promotoru MGMT může identifikovat pacienty profitující z terapie alkylačními agens a ovlivnit klinický a terapeutický management pacienta [15]. Příkladem je léčba pacientů s glioblastomem, kteří jsou starší 70 let. Na základě výsledků německé studie NOA-08 a skandinávské studie Nordic trial byl stanoven nový léčebný postup, založený na testování metylace MGMT promotoru [16,17]. Obě dvě studie prospektivně srovnávaly samotnou pooperační radioterapii se samotnou pooperační chemoterapií temozolomidem. Na základě jejich výsledků je možné u této kohorty pacientů v případě prokázané metylace promotoru MGMT indikovat samotnou chemoterapii (podávanou v domácím prostředí, ve formě tablet) a tohoto staršího vulnerabilního pacienta nevystavovat náročnému ozařování, které je pro tyto pacienty často organizačně komplikované (každodenní cestování na pracoviště radiační onkologie). Vyšetření metylačního statu promotoru pro MGMT se provádí nejčastěji metylačně specifickou PCR, MS-MLPA (methylation-specific multiplex ligation probe amplification) nebo analýzou teplot tání s vysokým rozlišením (high resolution melting analysis – HRM) po bisulfitové konverzi nemetylovaných cytosinů na uracil. Posledně zmiňovaná metoda je sice na zpracování více náročná, avšak oproti dvěma předchozím snižuje riziko falešně pozitivních výsledků [18].
Další terapeutické konsekvence výše diskutovaných biomarkerů přesahují rámec textu, proto odkazujeme čtenáře na práce zabývající se touto topikou [19–23].
Difúzní astrocytomy pediatrického typu
Přestože jsou pediatrické difúzní astrocytomy od svých adultních protějšků morfologicky nerozlišitelné, liší se jak geneticky, tak prognosticky. Na rozdíl od adultních jsou pediatrické difúzní astrocytomy pouze vzácně nositeli mutace genů IDH, ATRX, TP53 a zároveň se vyznačují výrazně nižším rizikem progrese do high grade gliomů, což je spojené s lepší prognózu. V pediatrických difúzních gliomech (IDH-wildtype a H3-wildtype) jsou časté alterace v genech BRAF, FGFR1, MYB či MYBL1, resp. jiné alterace MAPK signální dráhy.
Dle doporučení cIMPACT konsorcia [24] byla navržena klasifikace pediatrických difúzních astrocytomů, IDH-wildtype/H3-wildtype, WHO G II histologického gradu následovně:
- Difúzní gliom, MYB-alterovaný
- Difúzní gliom, MYBL-alterovaný
- Difúzní gliom, FGFR1 TKD duplikovaný
- Difúzní gliom, FGFR1-mutovaný
- Difúzní gliom, BRAF-mutovaný (bez delece CDKN2A/B)
- Difúzní gliom, s jinými alteracemi MAPK signální dráhy
Pediatrické difúzní astrocytomy s IDH mutací se chovají obdobně jako adultní a vyskytují se výhradně u dětí starších 14 let [25].
Samostatnou, v rámci integrované diagnostiky definovanou, jednotku představuje dále blíže specifikovaný prognosticky nepříznivý difúzní středočarový gliom, H3-K27-mutovaný.
U adolescentů a mladých dospělých byly rovněž popsány difúzní gliomy postihující mozkové hemisféry, IDH-wildtype, s mutacemi v genu H3F3A v pozici G34 (H3 G34 mutované) a ve většině případů s prokázanou ztrátou jaderné exprese ATRX a/nebo signifikantní imunopozitivitou p53. Vyznačují se high grade biologickým chováním, s pouze mírně příznivější prognózou ve srovnání s ostatními subtypy IDH-wildtype glioblastomů [25]. Hypermetylace promotoru MGMT byla popsána u většiny H3 G34-mutovaných nádorů, což pravděpodobně přispívá k lepší prognóze těchto nádorů. H3 G34-mutované nádory v současné integrované diagnostice nepředstavují definovanou jednotku, je doporučováno zařazení do kategorie „NEC“ (Not Elsewhere Classified) a popisná diagnóza zahrnující morfologii, grading a molekulární profil nádoru [26].
Difúzní středočarový gliom, H3-K27-mutovaný
Je definován jako infiltrující středočarový high grade gliom s dominující astrocytární diferenciací a mutací K27M v genech pro histon 3 (H3F3A nebo HIST1H3B/C). Vyskytuje se častěji v dětském věku, může však postihovat i dospělé. Typicky postihuje středočarové struktury, tj. mozkový kmen, thalamus nebo míchu, postižení mozečku je vzácné. Difúzní středočarové gliomy, H3 K27M-mutované se vyznačují nepříznivou prognózou a jsou klasifikovány jako WHO G IV gliomy bez ohledu na morfologicky stanovený histopatologický grade (obr. 4) [7,26].
V diagnostice je využíván imunohistochemický průkaz mutace při použití mutačně-specifické a vysoce senzitivní protilátky proti K27M-mutovanému histonu 3 s průkaznou jadernou pozitivitou v K27M-mutovaných nádorech. V případě nejednoznačného výsledku imunohistochemického vyšetření předmětné mutace je pro průkaz mutace H3 K27M indikována sekvenace genu H3F3A, případně genů HIST1H3B nebo HIST1H3C, které jsou mutovány méně často [28].
Klasifikace nádorů CNS WHO 2016 nesprávně uvádí, že mutace H3 K27M se vyskytují výhradně v difúzních středočarových gliomech, recentně však byly tyto mutace prokázány i v jiných typech mozkových nádorů, např. v ependymomu, gangliogliomu, pilocytárním astrocytomu či pediatrických difúzních astrocytomech. Klinický prognostický význam mutací v genech pro histon 3 není v těchto typech nádorů na rozdíl od difúzního středočarového gliomu H3 K27-mutovaného znám [7,29,30].
Vzhledem k výše uvedeným recentním zjištěním je v souladu s doporučením cIMPACT-NOW diagnóza difúzního středočarového gliomu H3K27M-mutovaného vyhrazena pouze pro nádory ve středočarové lokalizaci, s difúzním infiltrativním typem růstu a mutacemi H3K27M a nelze ji aplikovat na jiné nádory, u nichž tato mutace byla rovněž identifikována [7].
Aplikace termínů „NOS“ a „NEC“ v integrované diagnostice difúzních gliomů
Klasifikace nádorů CNS WHO 2016 aplikuje diagnostické označení nádorové jednotky jako „NOS (Not Otherwise Specified) “ pro případy, kdy nebylo provedeno příslušné molekulárně genetické vyšetření umožňující zařazení jednotky do příslušné kategorie integrované diagnózy, i pro případy, kdy toto vyšetření provedeno bylo, získané výsledky však nebyly konkluzivní, diagnostické genetické alterace nebyly prokázány a neumožnily zařazení do definované kategorie integrované diagnostiky [1].
Dle doporučení cIMPACT-NOW by označení „NOS“ mělo být vyhrazeno pouze pro případy, kdy diagnostické informace (morfologické či molekulární) nutné pro zařazení do příslušené definované kategorie integrované diagnostiky nejsou dostupné, a nově představuje kategorii „NEC (Not Elsewhere Classified) “ vyhrazenou pro nádory, u nichž komplexní histologické, imunohistochemické i genetické vyšetření bylo v souladu s guidelines provedeno, ale získané výsledky neumožňují přesné zařazení do akceptované a definované jednotky dle platné klasifikace nádorů CNS WHO 2016. V těchto případech je nutné využití popisné diagnózy, specifikující morfologii, histopatologický grade a prokázaný molekulární profil nádoru [27].
Závěr
Revidovaná WHO klasifikace nádorů CNS 2016 zásadním způsobem restrukturalizuje klasifikaci gliomů a jako první integruje molekulární znaky do diagnostiky difúzních gliomů definovaných nejen na základě konvenčních histopatologických nálezů a imunofenotypu, ale i příslušných molekulárních biomarkerů. Nutnost podrobnější klasifikace difúzních gliomů vychází zejména ze skutečnosti, že nádory obdobné morfologie v sobě zahrnují heterogenní jednotky, které se významně liší svojí molekulární patogenezou, biologickým chováním, prognózou i odpovědí na terapii. Integrovaná diagnostika tedy nejen zpřesňuje diagnostiku, ale přináší i významné informace prognostického a prediktivního charakteru s využitím v klinickém managementu neuroonkologických pacientů a individualizované léčbě nádorů CNS.
Tato práce byla podpořena Ministerstvem zdravotnictví České republiky – Koncepční rozvoj výzkumné organizace (MMCI 00209805) a Grantovou agenturou Masarykovy univerzity (MUNI/A/1562/2018).
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
MUDr. Michal Hendrych
I. ústav patologie
FN u sv. Anny v Brně
Pekařská 53
656 91 Brno
e-mail: michal.hendrych@fnusa.cz
Obdrženo/Submitted: 3. 1. 2020
Přijato/Accepted: 2. 2. 2020
Sources
1. Louis DN, Ohgaki H, Wiestler OD et al. WHO Classification of Tumours of the Central Nervous System. World Health Organization classification of tumours. Revised 4th edition. Lyon: International Agency for Research on Cancer 2016.
2. Louis DN, von Deimling A, Cavenee WK. Diffuse astrocytic and oligodendroglia tumours – introduction. In: Louis DN, Ohgaki H, Wiestler OD et al. WHO Classification of Tumours of the Central Nervous System. World Health Organization classification of tumours. Revised 4th edition. Lyon: International Agency for Research on Cancer 2016 : 16–17.
3. Louis DN, Ellison DW, Brat DJ et al. cIMPACT-NOW: a practical summary of diagnostic points from Round 1 updates. Brain Pathol 2019; 29 (4): 469–472. doi: 10.1111/bpa.12732.
4. Perry A, Wesseling P. Histologic classification of gliomas. In: Berger MS, Weller M. Handbook of clinical neurology. Vol 134: Gliomas. Cambridge: Elsevier 2016 : 71–95. doi: 10.1016/B978-0-12-802997-8.00005-0.
5. Wesseling P, Capper D. WHO 2016 Classification of gliomas. Neuropathol Appl Neurobiol 2018; 44 (2): 139–150. doi: 10.1111/nan.12432.
6. Barresi V, Lionti S, Valori L et al. Dual-genotype diffuse low-grade glioma: is it really time to abandon oligoastrocytoma as a distinct entity? J Neuropathol Exp Neurol2017; 76 (5): 342–346. doi: 10.1093/jnen/nlx024.
7. Louis DN, Giannini C, Capper D et al. cIMPACT-NOW update 2: diagnostic clarifications for diffuse midline glioma, H3 K27M-mutant and diffuse astrocytoma/anaplastic astrocytoma, IDH-mutant. Acta Neuropathol 2018; 135 (3): 481–484. doi: 10.1007/s00401-018-1826-y.
8. Dang L, White DW, Gross S et al. Cancer-associated IDH1 mutations produce 2-hydroxyglutarate. Nature 2009; 462 (7274): 739–744. doi: 10.1038/nature08
617.9. Gondim DD, Curless KL, Cheng L et al. Determining IDH-mutational status in gliomas using IDH1-R132H antibody and polymerase chain reaction. Appl Immunohistochem Mol Morphol 2019; 27 (10): 722–725. doi: 10.1097/PAI.0000000000000702.
10. Dewitt JC, Frosch MP, Samore WR et al. Cost-effectiveness of IDH testing in diffuse gliomas according to the 2016 WHO classification of tumors of the central
nervous system recommendations. Neuro Oncol 2017; 19 (12): 1640–1650. doi: 10.1093/neuonc/nox120.11. Vogazianou AP, Chan R, Pearson DM et al. Distinct patterns of 1p and 19q alterations identify subtypes of human gliomas that have different prognoses. Neuro Oncol 2010; 12 (7): 664–678. doi: 10.1093/neuonc/nop075.
12. Lee J, Solomon DA, Tihan T. The role of histone modifications and telomere alterations in the pathogenesis of diffuse gliomas in adults and children. J Neurooncol 2017; 132 (1): 1–11. doi: 10.1007/s11060-016-2349-9.
13. Takami H, Yoshida A, Fukushima S et al. Revisiting TP53 mutations and immunohistochemistry-a comparative study in 157 diffuse gliomas. Brain Pathol 2015; 25 (3): 256–265. doi: 10.1111/bpa.12173.
14. Brat DJ, Aldape K, Colman H et al. cIMPACT-NOW update 3: recommended diagnostic criteria for “Diffuse astrocytic glioma, IDH-wildtype, with molecular features of glioblastoma, WHO grade IV”. Acta Neuropathol 2018; 136 (5): 805–810. doi: 10.1007/s00401-018-1913-0.
15. Hegi ME, Diserens AC, Hamou MF etal. MGMT gene silencing and benefit from temozolomide in glioblastoma. N Engl J M 2005; 352 (10): 997–1003. doi: 10.1056/NEJMoa043331.
16. Wick W, Platten M, Meisner C et al. Temozolomide chemotherapy alone versus radiotherapy alone for malignant astrocytoma in the elderly: the NOA-08 randomised, phase 3 trial. Lancet Oncol 2012; 13 (7): 707–715. doi: 10.1016/S1470-2045 (12) 70164-X.
17. Malmström A, Grønberg BH, Marosi C et al. Temozolomide versus standard 6-week radiotherapy versus hypofractionated radiotherapy in patients older than 60 years with glioblastoma: the Nordic randomised, phase 3 trial. Lancet Oncol 2012; 13 (9): 916-926. doi: 10.1016/S1470-2045 (12) 70265-6.
18. Mansouri A, Hachem LD, Nassiri F et al. MGMT promoter methylation status testing to guide therapy for glioblastoma: Refining the approach based on emerging evidence and current challenges. Neuro Oncol 2019; 21 (2): 167–178. doi: 10.1093/neuonc/noy132.
19. Lakomý R, Kazda T, Poprach A et al. The role of chemotherapy in the treatment of low-grade gliomas. Klin Onkol 2017; 30 (5): 343–348. doi: 10.14735/amko2017343.
20. Kazda T, Lakomý R, Poprach A et al. Controversy in the postoperative treatment of low-grade gliomas. Klin Onkol 2017; 30 (5): 337–342. doi: 10.14735/amko2017337.
21. Kazda T, Dziacky A, Burkon P et al. Radiotherapy of glioblastoma 15 years after the landmark Stupp’s trial: More controversies than standards? Radiol Oncol 2018; 52 (2): 121–128. doi: 10.2478/raon-2018-0023.
22. Weller M, van den Bent M, Tonn JC et al. European Association for Neuro-Oncology (EANO) guideline on the diagnosis and treatment of adult astrocytic and oligodendroglial gliomas. Lancet Oncol 2017; 18 (6): e315–e329. doi: 10.1016/S1470-2045 (17) 30194-8.
23. Berghoff A, van den Bent M. How I treat anaplastic glioma without 1p/19q codeletion. ESMO Open 2019; 4 (Suppl 2): e000534. doi: 10.1136/esmoopen-2019-000534.
24. Ellison DW, Hawkins C, Jones DTW et al. cIMPACT-NOW update 4: diffuse gliomas characterized by MYB, MYBL1, or FGFR1 alterations or BRAF (V600E) mutation. Acta Neuropathol 2019; 18 (6): 683–687. doi: 10.1007/s00401-019-01987-0.
25. Ryall S, Tabori U, Hawkins C. A comprehensive review of paediatric low-grade diffuse glioma: pathology, molecular genetics and treatment. Brain Tumor Pathol 2017; 34 (2): 51–61. doi: 10.1007/s10014-017-0282-z.
26. Sturm D, Witt H, Hovestadt V et al. Hotspot mutations in H3F3A and IDH1 define distinct epigenetic and biological subgroups of glioblastoma. Cancer Cell 2012; 22 (4): 425–437. doi: 10.1016/j.ccr.2012.08.024.
27. Louis DN, Wesseling P, Paulus W et al. cIMPACT-NOW update 1: Not otherwise specified (NOS) and not elsewhere classified (NEC). Acta Neuropathol 2018; 135 (3): 481–484. doi: 10.1007/s00401-018-1808-0.
28. Huang T, Garcia R, Qi J et al. Detection of histone H3 K27M mutation and post-translational modifications in pediatric diffuse midline glioma via tissue immunohistochemistry informs diagnosis and clinical outcomes. Oncotarget 2018; 9 (98): 37112–37124. doi: 10.18632/oncotarget.26430.
29. Kleinschmidt-DeMasters BK, Donson A, Foreman NK et al. H3 K27M mutation in gangliogliomas can be associated with poor prognosis. Brain Pathol 2017; 27 (6): 846–850. doi: 10.1111/bpa.12455.
30. Orillac C, Thomas C, Dastagirzada Y et al. Pilocytic astrocytoma and glioneuronal tumor with histone H3 K27M mutation. Acta Neuropathol Commun 2016; 4 (1): 84. doi: 10.1186/s40478-016-0361-0.
Labels
Paediatric clinical oncology Surgery Clinical oncology
Article was published inClinical Oncology

2020 Issue 4-
All articles in this issue
- Integrovaná diagnostika difúzních gliomů
- Úloha CDK12 v rozvoji nádorů
- Zhubné nádory krčka maternice v gravidite
- Role exozomů u nádorových onemocnění
- Nemoc těžkých řetězců imunoglobulinu gama
- Hematologická toxicita u IMRT/VMAT v kurativní léčbě análního karcinomu
- Atypický průběh typického karcinoidu plic
- Karcinom děložního hrdla v graviditě
- Akademická studie XR-TEMinDREC – kombinace konkomitantní neoadjuvantní chemoradioterapie následované lokální excizí operačním rektoskopem a akcelerovanou dispenzarizací u pacientů s mírně pokročilými stadii nízce sedícího adenokarcinomu konečníku a její průběh v MOÚ
- Efektivita blokády pektorálneho nervu typu II oproti torakálnej paravertebrálnej blokáde v analgézii po operácii tumoru prsníka
- Clinical Oncology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Zhubné nádory krčka maternice v gravidite
- Integrovaná diagnostika difúzních gliomů
- Atypický průběh typického karcinoidu plic
- Nemoc těžkých řetězců imunoglobulinu gama
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

