-
Medical journals
- Career
Katetrizační ablace fibrilace síní a přímá antikoagulancia
Authors: J. Špinar; R. Lábrová
Authors‘ workplace: Interní kardiologická klinika LF MU a FN Brno
Published in: Kardiol Rev Int Med 2017, 19(3): 183-186
Overview
Přímá antikoagulancia (blokátory faktoru II nebo faktoru Xa) se v posledních letech dostaly do základní klinické praxe a v mnoha indikacích nahrazují blokátory kumarinu (warfarin) s větší bezpečností a účinností. Je to především nevalvulární fibrilace síní, hluboká žilní trombóza a plicní embolie. Nově se objevují informace o jejich nepřerušovaném použití při katetrizační ablaci fibrilace síní. Studie VENTURE AF prokázala noninferioritu nepřerušovaného podání rivaroxabanu oproti nepřerušovanému podání warfarinu u 248 nemocných podstupujících ablaci fibrilace síní. Studie RE-CIRCUIT srovnávala nemocné (n = 704) s nepřetržitou léčbou dabigatranem vs. warfarinem a podstupující ablaci fibrilace síní a prokázala superioritu dabigatranu, především v oblasti bezpečnosti, protože u nemocných léčených dabigatranem bylo méně krvácení.
Klíčová slova:
antikoagulace – fibrilace síní – ablace – bezpečnost
Tromboembolická onemocnění jsou jednou z hlavních příčin nemocnosti a úmrtnosti ve světě. Postihují ročně asi 6,5 milionu lidí. Terapeutické možnosti byly po celá desetiletí omezeny na nefrakcionovaný heparin a antagonisty vitaminu K (VKA). Teprve zavedení nízkomolekulárních heparinů koncem 80. let 20. století přineslo možnost zlepšit antikoagulační léčbu. Vývoj nových léků v posledním desetiletí zavedl do praxe nová antitrombotika (NOAC) – apixaban, dabigatran, edoxaban a rivaroxaban, působící na různé fáze koagulační kaskády. Přímá antikoagulancia mají několik zásadních výhod oproti warfarinu a o výsledcích s již v ČR registrovanými preparáty, jako je dabigatran, apixaban, rivaroxaban či edoxaban, jsme referovali již opakovaně [1 – 5]. V tomto článku se zaměříme na přímá antikoagulancia u ablace fibrilace síní.
Obecně platí, že katetrizační ablace představuje 2. linii léčby po selhání terapie antiarytmiky nebo při jejich intoleranci. Jako primární léčba jsou ablace indikovány u vybraných symptomatických pacientů, kteří dávají přednost léčbě invazivní.
Katetrizační ablace se během posledních let stala metodou volby pro pacienty s paroxysmální či perzistující fibrilací síní (FS), která vede k výrazným obtížím a je rezistentní na farmakologickou léčbu. Základním cílem výkonu je úplná elektrická izolace plicních žil od svaloviny levé síně, které je dosaženo vytvořením série lézí v proximálním segmentu plicních žil. U pacientů s perzistující či dlouhodobě perzistující formou arytmie bývá izolace doplněna o další linie s cílem větší modifikace arytmogenního substrátu. Účinnost výkonu v odstranění FS se pohybuje okolo 70 – 90 % v závislosti na studované populaci, použité technice a metodě sledování po zákroku.
Kdo je tedy vhodný ke katetrizační léčbě FS? Většina studií prozatím dokumentovala především zlepšení kvality života a odstranění symptomů vyplývajících z atak arytmie. Z tohoto důvodu by primárně měli být k ablaci indikováni pacienti se symptomy, u kterých antiarytmická léčba není účinná či žádoucí. Jednoznačně není zatím zodpovězena otázka, zda má být katetrizační ablace prováděna jako metoda první volby bez předchozí antiarytmické léčby. V tomto smyslu byla doposud publikována randomizovaná studie, jejíž výsledky vyzněly pro ablaci příznivě [6]. Dále prozatím neexistují důkazy o účinnosti katetrizační ablace u asymptomatických pacientů. Provedení ablace lze zvážit v případě, kdy se jedná o mladého pacienta a je podezření na tachykardickou kardiomyopatii. V případě srdečního selhání, dysfunkce levé komory srdeční a nekontrolovatelné odpovědi komor totiž dochází po katetrizační ablaci a úpravě srdečního rytmu ke zlepšení až normalizaci ejekční frakce levé komory [7].
V klinické praxi je katetrizační ablace někdy vyhledávána pacienty, kteří jsou asymptomatičtí a nechtějí dlouhodobě užívat antikoagulační léčbu. Dosud však chybí data o účinnosti katetrizační ablace v prevenci tromboembolických příhod. Proto by pacientovo přání vysadit antikoagulační léčbu nemělo být bráno v potaz jako indikační kritérium. Ale některé observační studie naznačují, že úspěšná katetrizační ablace příznivě ovlivňuje přežití nemocných na úroveň očekávanou u jedinců stejného věku bez FS, co se týká rizika tromboembolických komplikací. Užívání warfarinu je jednoznačně indikováno minimálně 2 – 3 měsíce po výkonu. Rozhodnutí, zda lze antikoagulační léčbu po tomto období nahradit antiagregací, by mělo být založeno na míře rizika tromboembolie (např. CHADS2 skóre), nikoli na přítomnosti/ absenci epizod FS po výkonu. Mezi parametry, které významně ovlivňují úspěšnost výkonu, patří především rozměr levé síně. Výrazná dilatace levé síně (obvykle nad 50 – 55 mm) je obvykle spojena s elektrickou a mechanickou remodelací, která snižuje šanci na dlouhodobé udržení sinusového rytmu [8]. Také anamnéza dlouhodobě se udržující perzistující FS zvyšuje riziko neúspěchu ablace (obvykle při trvání FS déle než 2 roky) [9,10].
V roce 2015 vyšla inovovaná Evropská doporučení pro používání antikoagulancií – non-vitamin K antagonistů – u pacientů s nonvalvulární FS, která přinášejí především jasné pokyny jak podávat tuto léčbu u pacientů s ischemickou chorobou srdeční a především jak doporučit či nedoporučit současné podávání antikoagulační a antiagregační léčby u pacientů s FS a ischemickou chorobou srdeční [11]. Tato doporučení byla ještě upravena v roce 2016 [12].
Guidelines uvádějí, že pacienti užívající VKA by měli v léčbě pokračovat i během ablace (s INR 2 – 3). Nepřerušené podávaní NOAC se podle observačních dat jeví jako podobně bezpečné. Během ablace je namístě podáváni heparinu. Studie uvádějí poměrně nízkou četnost cévní mozkové příhody v prvních letech po ablaci, nicméně indikace OAC by se měla odvíjet od tromboembolického rizika (obr. 1) [11 – 13].
Image 1. Antikoagulace u pacientů s plánovanou katetrovou ablací. 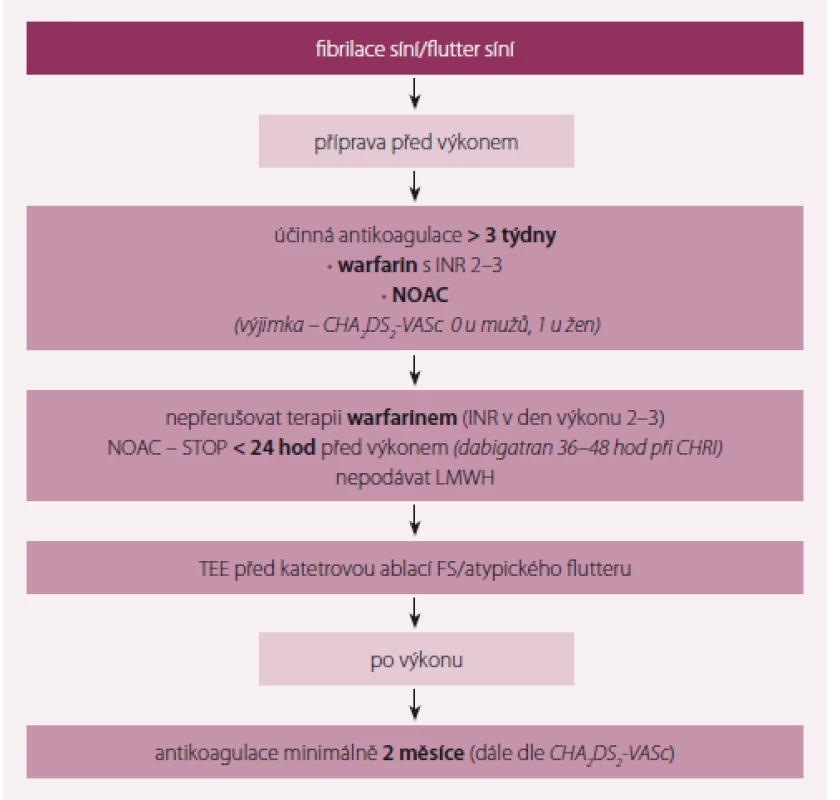
NOAC – nová antikoagulancia, LMWH – nízkomolekulární heparin, TEE – vrcholová hodnota při FS , FS – fibrilace síní Již v roce 2015 byla v European Heart Journal publikována první randomizovaná studie srovnávající nepřerušované podání nového antikoagulancia rivaroxabanu s nepřetržitým podánín warfarinu u nemocných podstupujících ablaci nevalvulární FS. Studie je známa pod akronymem VENTURE AF [14]. Studie randomizovala 248 nemocných s nevalvulární FS na léčbu rivaroxabanem nebo warfarinem po dobu minimálně 4 týdnů před katetrovou ablací. Primárním cílem bylo krvácení po katetrové ablaci, sekundární cíl byl složen z cévní mozkové příhody, infarktu myokardu či vaskulární smrti a jakéhokoli krvácení. Průměrný věk nemocných byl 59,5 ± 10 let, 71 % byli muži, 74 % mělo paroxysmální FS a CHA2DS2-VASC skóre bylo 1,6. Výskyt velkého krvácení byl velmi nízký (0,4 %) stejně jako výskyt trombembolické příhody (0,8 %). Celkový počet příhod byl stejný v obou skupinách (tab. 1).
Table 1. Hlavní výsledky studie VENTURE-AF. 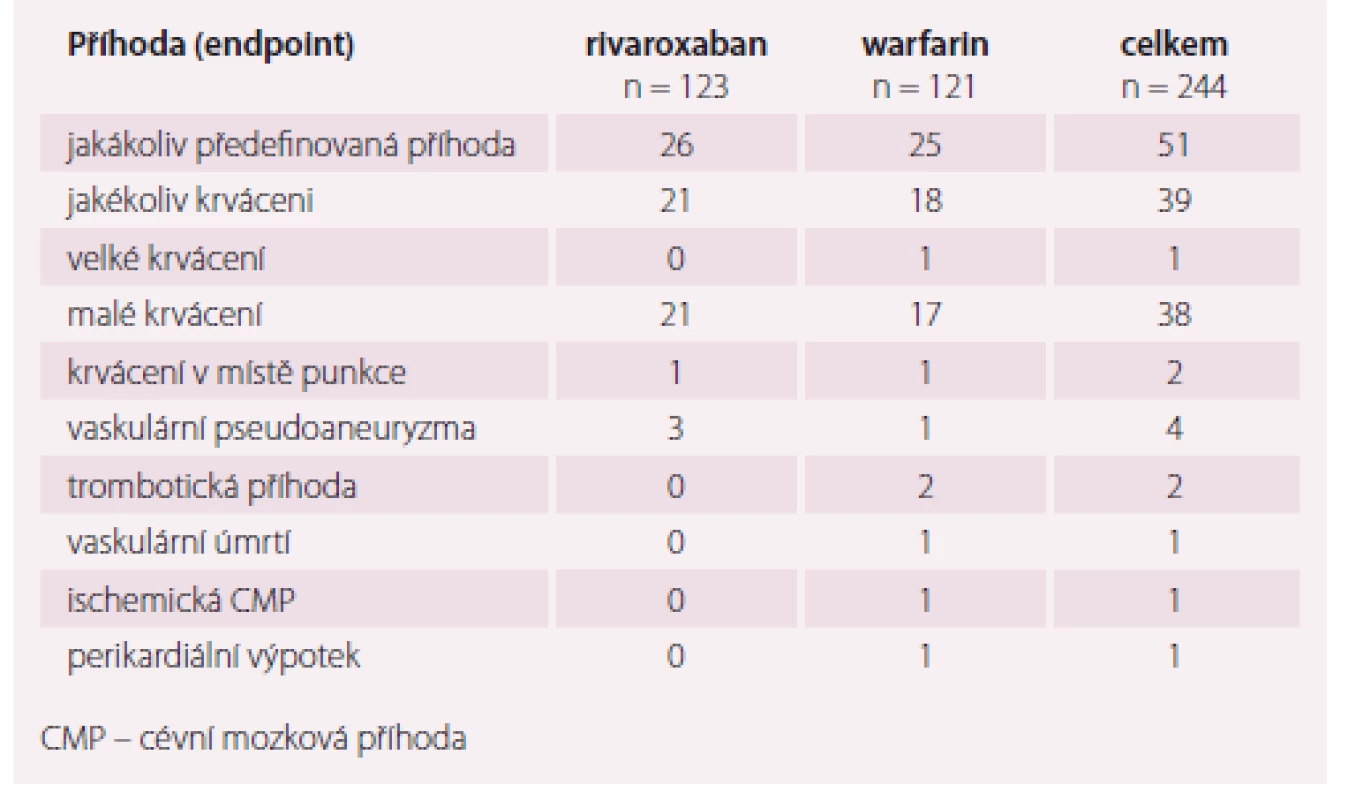
V roce 2017 na Americkém kardiologickém kongresu (ACC) ve Washingtonu byly prezentovány výsledky studie RE-CIRCUIT a simultánně publikovány v časopise New England Journal of Medicine [15]. Tato studie hodnotila nepřerušované podání warfarinu vs. nepřerušované podávání dabigatranu během ablace u nemocných s paroxysmální nebo perzistující nevalvulární FS. Na tomto klinickém hodnocení spolupracovalo 104 pracovišť z 11 zemí. Polovina nemocných při něm dostávala dabigatran etexilát v dávce 150 mg 2× denně, druhá polovina užívala warfarin v dávce cílené na INR v rozmezí 2,0 – 3,0. Zařazeni mohli být nemocní nad 18 let s paroxysmální nebo perzistentní nevalvulární FS s plánovanou katetrovou ablací. Fibrilace síní musela být dokumentována během 24 měsíců před screeningem a nemocní museli být vhodní na léčbu dabigatranem 2 × 150 mg. Hlavním vylučovacím kritériem byla permanentní FS anebo valvulární typ FS. Nemocní byli randomizováni na 1 : 1 na 2 × 150 mg dabigatranu nebo na léčbu warfarinem (1, 3 nebo 5 mg, případně kombinace) s cílovým INR 2,0 – 3,0. Studie měla nejprve 0 – 2 týdny screeningové a 4 – 8 týdnů léčby k dosažení cílového INR. Všichni pacienti měli před ablací provedeno transezofageální echo. Po ablaci byli antikoagulováni a sledováni dalších 8 týdnů. Dabigatran byl podán ráno i v den ablace a následně večer v plánovanou hodinu, maximálně s 3hodinovým odložením. Nefrakcionovaný heparin byl podán těsně před transseptální punkcí nebo těsně po punkci. Dále se nefrakcionovaný heparin podává kontinuálně během výkonu s udržením aktivovaného koagulačního testu (ACT) 300 – 350 s.
Ablace byla provedena ve 4. až 8. týdnu nepřerušené antikoagulace a pokračovala minimálně 8 týdnů po zákroku. Ablaci za těchto podmínek podstoupilo celkem 635 pacientů (317 na dabigatranu a 318 na warfarinu).
Primárním cílovým ukazatelem byla incidence závažného krvácení během výkonu a 8 týdnů po něm. Mezi sekundární cíle patřily další krvácivé komplikace a tromboembolické příhody. Do studie bylo zařazeno 704 nemocných, z nichž 678 bylo randomizováno a 635 podstoupilo ablaci. Adherence k dabigatranu byla kalkulována podle vybraných tabletek. Jako dobrá byla ohodnocena, pokud byla 80 – 120% adherence k warfarinu podle hodnot INR. V 66% byla kalkulovaná adherence k dabigatranu 97,6% a INR v rozmezí 2 – 3 (tab. 2).
Table 2. Hlavní výsledky studie RE-CIRCUIT. 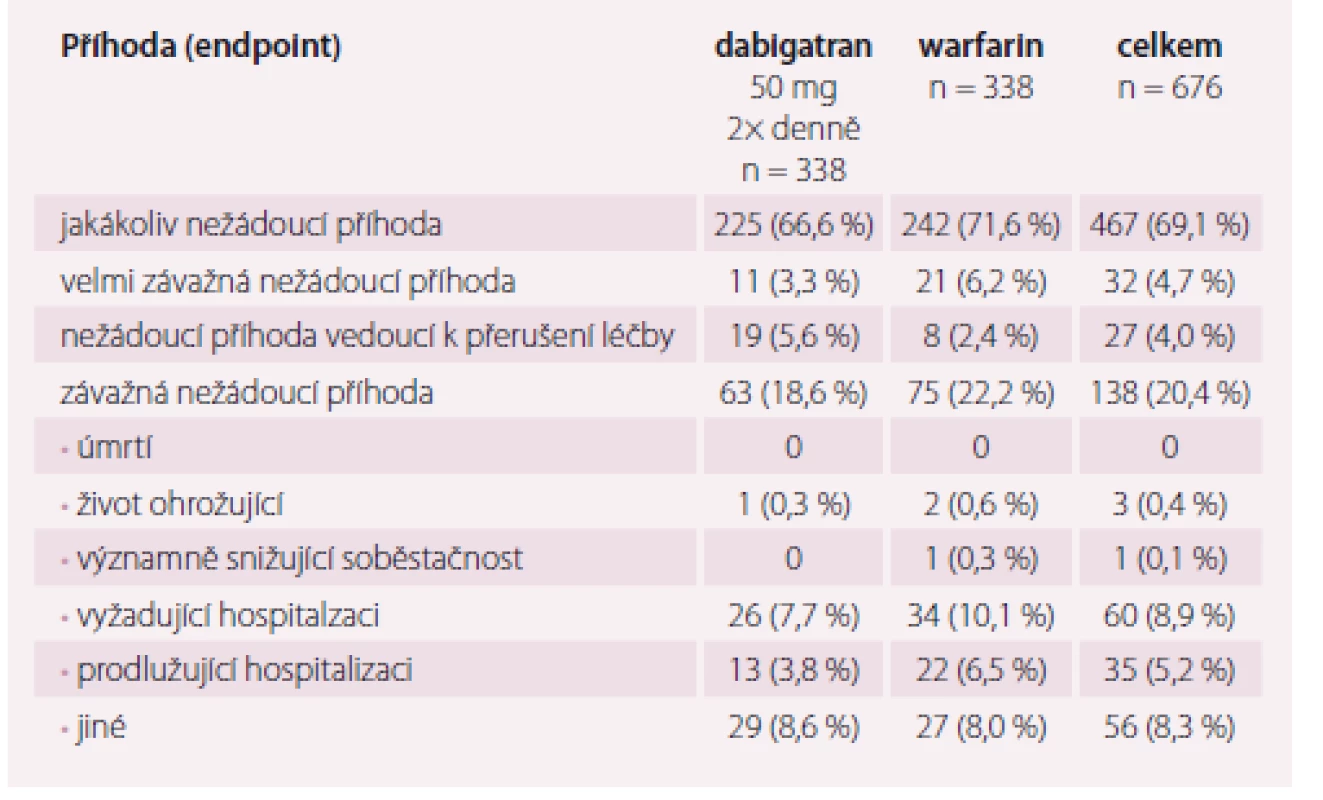
Výsledky jednoznačně favorizují NOAC, resp. dabigatran. Celkem bylo zaznamenáno velké krvácení u 27 nemocných. Incidence závažného krvácení byla u dabigatranu statisticky významně nižší než u warfarinu (p < 0,001) (graf 1) [15]. Ve skupině s dabigatranem k němu došlo u pěti pacientů (5/ 317; 1,6 %), u warfarinu u 22 nemocných, tedy u 6,9 % (22/ 318) (p < 0,001). To znamená snížení relativního rizika o 77,2 %. U dabigatranu byl nižší především výskyt srdeční tamponády a také hematomů v oblasti třísla. Obě skupiny byly srovnatelné v incidenci menšího krvácení. Tromboembolická příhoda byla zaznamenána pouze jedna, a to u warfarinu – šlo o tranzientní ischemickou ataku.
Graph 1. Krvácení ve studii RE-CIRCUIT. 
Žádná nežádoucí krvácivá příhoda u nemocných léčených dabigatranem nevyžadovala trvalé přerušení léčby, což je plně v souladu s výsledky studie Randomised Evaluation of Long-Term Anticoagulation Therapy (RE-LY) trial u 18 113 nemocných s FS [16], ale také s výsledky velkých celosvětových registrů s dabigatranem či jinými přímými antikoagulancii [17].
Výsledky studie RE-CIRCUIT jasně ukázaly, že ablační léčba fibrilace síní prováděná za nepřerušeného podávání dabigatranu je superiorní v porovnání s nepřerušeným podáváním warfarinu.
Práce byla podpořena projektem (Ministerstva zdravotnictví ČR) koncepčního rozvoje výzkumné organizace 65269705 (FN Brno).
Doručeno do redakce: 22. 6. 2017
Přijato po recenzi: 3. 7. 2017
prof. MU Dr. Jindřich Špinar, CSc., FESC
www.fnbrno.cz
spinar.jindrich@fnbrno.cz
Sources
1. Špinar J. Dabigatran v klinických studiích a reálném životě. Cor Vasa 2013; 55(5): 202 – 206. doi: 10.1016/ j.crvasa.2013.04.006.
2. Špinar J, Vítovec J. Antikoagulační léčba fibrilace síní. Acta medicinae 2014; 9 : 18 – 23.
3. Špinar J, Vítovec J, Špinarová L et al. Rivaroxaban v léčbě fibrilace síní. Farmakoterapie 2013; 1 : 6 – 12.
4. Vítovec J, Špinar J. Antikoagulační léčba u srdečního selhání a hypertenze. In: Widimský J jr. Arteriální hypertenze – současné klinické trendy XIII. Praha: Triton 2016 : 157 – 162.
5. Špinar J, Vítovec J. Edoxaban v klinických studiích a v klinické praxi. Remedia 2016; 26(4): 348 – 353.
6. Wazni OM, Marrouche NF, Martin DO et al. Radiofrequency ablation vs antiarrhythmic drugs as first-line treatment of symptomatic atrial fibrillation: a randomized trial. JAMA 2005; 293(21): 2634 – 2640.
7. Hsu LF, Jais P, Sanders P et al. Catheter ablation for atrial fibrillation in congestive heart failure. N Engl J Med 2004; 351(23): 2373 – 2383.
8. Arya A, Piorkowski C, Sommer P et al. Ablation of atrial fibrillation: patient selection, techniques, and the results. Herzschrittmacherther Elektrophysiol 2008; 19(2): 68 – 72. doi: 10.1007/ s00399-008-0003-8.
9. Lábrová R, Špinar J. Katetrizační ablace fibrilace síní. Kardiologická revue 2008; 10(3): 103 – 110.
10. Špinar J, Vítovec J, Špinarová L. Edoxaban v klinických studiích. Cor Vasa 2016; 58(6): 788 – 496.
11. Heidbuchel H, Verhamme P, Alings M et al. Updated European Heart Rhythm Association Practical Guide on the use of non-vitamin K antagonist anticoagulants in patients with non-valvular atrial fibrillation. Europace 2015; 17(10): 1467 – 1507. doi: 10.1093/ europace/ euv309.
12. Kirchov P, Benussi S, Dipak Kotecha D et al. 2016 ESC Guidelines for the management of atrial fibrillation developed in collaboration with EACTS. Eur Heart J 2016; 37(38): 2893 – 2962. doi: 10.1093/ eurheartj/ ehw210.
13. Čihák R, Haman L, Táborský M. Doporučené postupy ESC 2016 pro léčbu fibrilace síní formulované ve spolupráci s EACTS. Cor Vasa 2016; 58: e636 – e683. doi: 10.1016/ j.crvasa.2016.11.005
14. Cappato R, Marchlinski FE, Hohnloser SH et al. Uniterrupted rivaroxaban vs. uninterrupted vitamin K antagonist for catheter ablation in non-valvular atrial fibrillation. Eur Heart J 2015; 36(28): 1805 – 1811. doi: 10.1093/ eurheartj/ ehv177.
15. Calkins H, Willems S, Gerstenfeld EP et al. Uninterrupted dabigatran versus warfarin for ablation in atrial fibrillation. NEJM 2017; 376(17): 1627 – 1636. doi: 10.1056/ NEJMoa1701005.
16. Eikelboom JW, Walentin L, Conolly SJ et al. Risk of bleeding with 2 dosesof dabigatran compared with warfarin in older and younger patients with atrial fibrillation: an analysis of the randomised evaluation of long-term anticoagulation therapy (RE-LY) trial. Circulation 2011; 123(21): 2363 – 2372. doi: 10.1161/ CIRCULATIONAHA.110.004747.
17. Larsen TB, Skjoth F, Nielsen PB et al. Comparative effectiveness and safety of non-vitamin K antagonist oral anticoagulans and warfarin in patients with atrial fibrillation: propensity weighted nationwide cohort study. BMJ 2016; 353: i3189. doi: 10.1136/ bmj.i3189.
Labels
Paediatric cardiology Internal medicine Cardiac surgery Cardiology
Article was published inCardiology Review

2017 Issue 3-
All articles in this issue
- Stratifikace kardiovaskulárního rizika a nové cílové hodnoty sérových lipidů
- Management dyslipidemií v definovaných skupinách pacientů
- Statinová intolerance a její praktická řešení
- Co nedělat a proč aneb kardiovaskulární prevence ve světle posledních doporučení
- Je srdcové zlyhávanie so zachovalou ejekčnou frakciou vážne ochorenie?
- Ularitid v léčbě akutně dekompenzovaného srdečního selhání – výsledky studie TRUE-AHF
- Infekční endokarditida
- Katetrizační ablace fibrilace síní a přímá antikoagulancia
- 30 let inhibice systému renin-angiotensin-aldosteron u srdečního selhání
- SGLT2 (glifloziny) antidiabetika, antihypertenziva nebo léky na srdeční selhání?
- Zoletorv – farmakologický profil
- Edukační činnost sester u pacientů po infarktu myokardu – přehledová studie
- Cardiology Review
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- SGLT2 (glifloziny) antidiabetika, antihypertenziva nebo léky na srdeční selhání?
- Stratifikace kardiovaskulárního rizika a nové cílové hodnoty sérových lipidů
- Statinová intolerance a její praktická řešení
- Infekční endokarditida
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career
