-
Medical journals
- Career
Význam zobrazovacích metod v prevenci kardiovaskulárních onemocnění
: MUDr. Jan Baxa, Ph.D.
: FN Plzeň a LF UK v Plzni ; Klinika zobrazovacích metod
: Kardiol Rev Int Med 2013, 15(4): 224-229
:
Zobrazovací metody byly v minulosti využívány zejména v sekundární prevenci kardiovaskulárních onemocnění, v posledních letech však výrazně stoupá jejich uplatnění i v prevenci primární. Detekce a kvantifikace kalcifikací koronárního řečiště pomocí výpočetní tomografie patří mezi nejjednodušší a zároveň nejrozšířenější vyšetření v rámci prevence, praktický význam tohoto vyšetření je však stále diskutabilní. CT angiografie představuje jedinou neinvazivní metodu s možností nejen kvantifikace stenózy koronárních tepen, ale také hodnocení charakteru aterosklerotického plátu. Využití tohoto faktu v rutinní praxi je v současnosti velmi diskutovaným tématem. Nejnověji je možné hodnotit pomocí CT také perfuzní parametry myokardu, což z výpočetní tomografie dělá nejkomplexnější zobrazovací metodu, která má díky technickému pokroku stále menší radiační zátěž. Hlavní předností magnetické rezonance v primární prevenci je možnost detekce tzv. „němé ischemie”. Scintigrafické metody jsou výrazně limitovány vysokou radiační zátěží.
Klíčová slova:
zobrazovací metody – kalciové skóre – výpočetní tomografie – magnetická rezonance – prevence kardiovaskulárních onemocněníÚvod
Zobrazovací metody patří obecně mezi velmi dynamicky se rozvíjející medicínské obory. V minulosti, před rozšířením metod jako ultrazvuk, výpočetní tomografie a magnetická rezonance, byly možnosti uplatnění zobrazovacích metod, tzn. zejména konvenční skiagrafie, velmi omezené. Pomocí této metody bylo možné zachytit až pokročilé projevy kardiovaskulárních nemocí (KVN), např. pokročilé kalcifikace tepen nebo dilataci srdečního stínu. V současnosti jsou pro prevenci KVN používány výhradně moderní zobrazovací metody. Obecně lze konstatovat, že nejvíce uznávaným přínosem zobrazovacích metod v prevenci KVN je jejich vysoká negativní prediktivní hodnota. Tedy v případě negativního nálezu je velmi nízká pravděpodobnost výskytu kardiovaskulární příhody [1]. Stále se zvyšující kvalita zobrazovacích metod však umožňuje lepší detekci aterosklerotického postižení. Zobrazovací metody tak mohou hrát důležitou roli nejen v identifikaci aterosklerotických lézí, ale i v posouzení jejich progrese nebo regrese a dokonce i jejich vulnerability (tendence ke vzniku akutních komplikací).
Kalciové skóre
Z patofyziologie aterosklerózy je známo, že množství vápníku usazeného ve stěnách koronárních tepen odpovídá úrovni aterosklerotického postižení [2]. Metody využívající RTG paprsky jsou obecně vhodné k zobrazení kalcifikovaných struktur vzhledem k vysoké atenuaci paprsků X ve sloučeninách obsahujících atomy vápníku. Výrazně kalcifikované pláty v koronárním stromu jsou patrné i na prostých rentgenových vyšetřeních plic. Přesněji lze kalcifikace v koronárním řečišti zobrazit a zároveň kvantifikovat neinvazivními metodami pomocí EBCT (electron-beam computed tomography) nebo spirálního CT, které je v současnosti jednoznačně nejrozšířenější, technicky zcela nenáročné a lze ho provádět i na starších typech CT přístrojů. Podmínkou je pouze možnost synchronizace skenování s EKG křivkou [3,4].
Před vyšetřením ani během něho se nepodává kontrastní látka, samotné skenování probíhá v nádechu a trvá několik vteřin. Riziko radiační zátěže u tohoto typu vyšetření je velmi nízké. Pro samotné vyhledání a hodnocení kalcifikací existují speciální softwarové aplikace, které kalcifikace definují jako léze o určité hutnosti, tzv. denzitním rozhraní (od 130 Hounsfieldových jednotek výše). Kalcifikace jsou zobrazeny v celém vyšetřeném rozsahu, tedy nejen v koronárním řečišti, ale i na srdečních chlopních nebo ve stěně aorty. Je tedy nutné manuálně označit ty kalcifikace, které jsou přítomny v koronárních tepnách [5]. Pro následnou kvantifikaci kalcifikací koronárního řečiště bylo stanoveno tzv. Agatstonovo kalciové skóre založené na objemu a denzitě jednotlivých kalcifikací (obr. 1). Jeho hodnota je výsledkem součtu plochy kalcifikací na získaných CT obrazech vynásobeného kofaktorem, jehož hodnota vychází z denzity kalcifikace. Toto číslo je bezrozměrné a byla prokázána jeho dobrá korelace se stupněm koronární aterosklerózy [6]. Kromě Agatstonova skóre existují ještě další způsoby hodnocení založené např. na objemu kalcifikací, ale jejich využití se zatím výrazně nerozšířilo. Kromě hodnot kalciového skóre lze tedy pomocí hodnoticích programů získat i objem kalcifikací a také množství hydroxyapatitu (hydrogenfosforečnanu vápenatého) v miligramech.
1. Stanovení kalciového skóre: zobrazení četných kalcifikací koronárních tepen. Označení kalcifikací v jednotlivých větvích koronárního stromu (A). Protokol s kvantifikací a stanovením Agatstonova čísla (B). 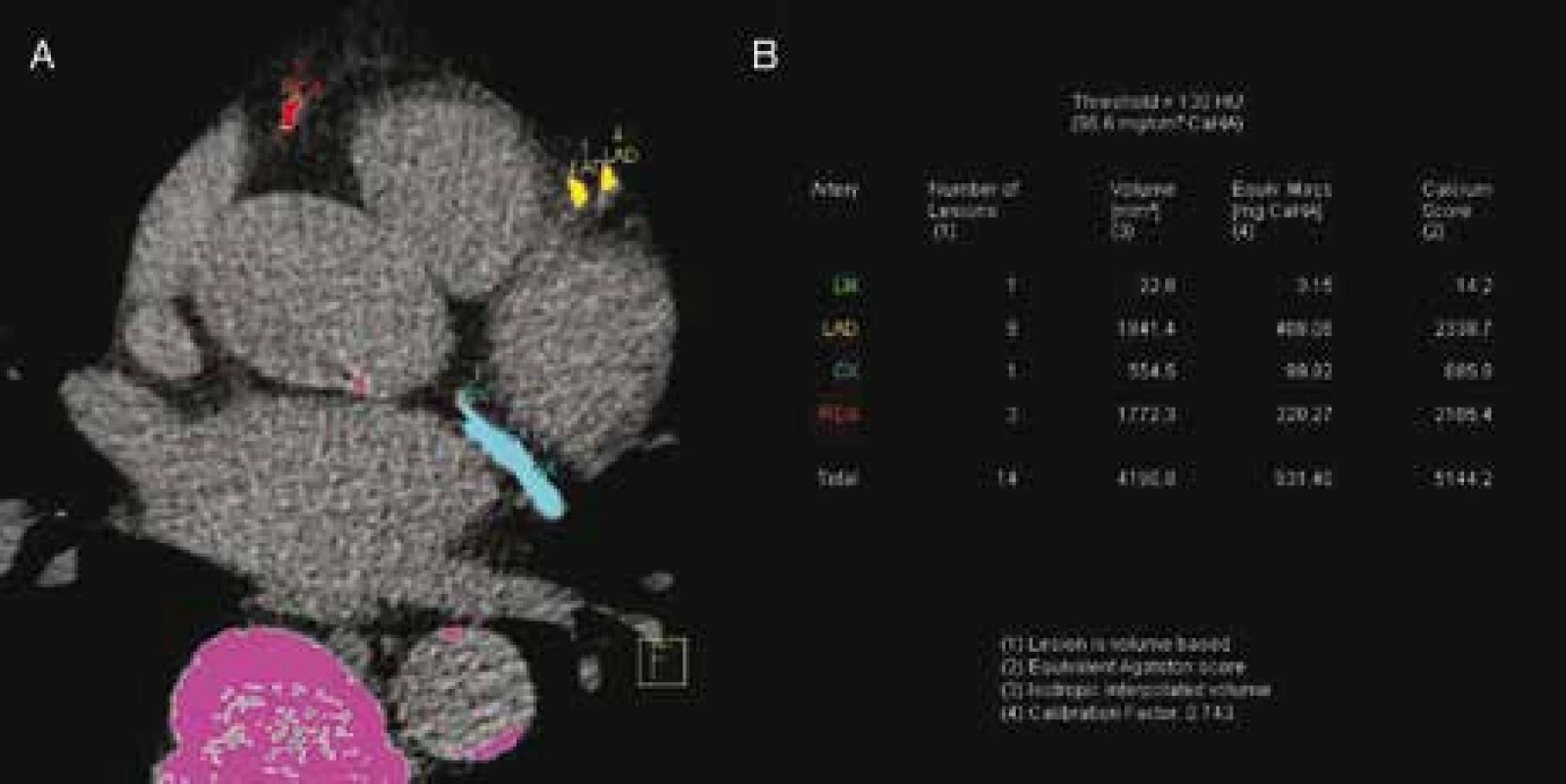
Na základě histopatologických studií byla prokázána úzká souvislost mezi množstvím kalcifikací a celkovým zatížením aterosklerotickými změnami. Stanovení této hodnoty je dnes nejběžněji užívaným způsobem stanovení rizika vzniku kardiovaskulární příhody, zejména u vysoce rizikových osob [7]. Největší dosavadní studie zabývající se prognostickou hodnotou rizikových faktorů a kalciového skóre ve vztahu k mortalitě prokázala několik důležitých faktů ohledně vztahu množství kalcia ve stěně koronárních tepen a průběhu ICHS. Zejména byla prokázána stoupající mortalita v závislosti na hodnotách kalciového skóre (tab. 1). Z této studie vyplývá, že u osob s kalciovým skóre 11–100 bylo relativní riziko kardiovaskulárního úmrtí 2,6krát vyšší, u osob s kalciovým skóre 101–400 3,8krát vyšší, u osob s hodnotou 401–1 000 6,3krát vyšší a u osob s hodnotou 1 001 a více pak 12,3krát vyšší než u osob s hodnotou kalciového skóre 0–10. Z výsledků této práce dále vyplývá, že stanovení kalciového skóre má vysokou prediktivní hodnotu ve stanovení mortality a kombinace kalciového skóre a rizikových faktorů významně zvyšuje prediktivní hodnotu obou metod [8].
1. Závislost mortality na hodnotě kalciového skóre [8]. ![Závislost mortality na hodnotě kalciového skóre [8].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/94fea277bb30ebb7ccbcf989758f3b2e.png)
Význam a kvalita hodnoty kalciového skóre v predikci rizika kardiovaskulárních onemocnění byla potvrzena v řadě dalších multicentrických studií (nejnověji MESA – multiethnic study of atherosclerosis) a v současnosti je považována za velmi vhodnou metodu pro osoby s nízkým až středním rizikem. Tato studie potvrdila, že použití kalciového skóre společně se standardními rizikovými faktory způsobilo zařazení více osob do kategorie s vysokým rizikem a zároveň zlepšilo celkové stanovení rizika u sledovaných osob [9]. Na druhou stranu je nutné tyto hodnoty správně interpretovat, protože přestože byla prokázána jejich souvislost s celkovým aterosklerotickým postižením, jedná se pouze o jednu materiálovou entitu případného aterosklerotického plátu. Nejčastější příčinou akutního koronárního syndromu je přitom ruptura plátu, který kalcifikace často neobsahuje. Zároveň není jednoznačně stanoven algoritmus dalšího postupu u osob po zjištění vyšších hodnot kalciového skóre. Většina dosud provedených studií potvrzuje, že u osob s nízkým až středním rizikem znamená malá hodnota Agatstonova skóre (do 10) velmi nízké riziko vzniku kardiovaskulární příhody v následujících pěti letech [7].
Velmi často je v různých studiích posuzován přínos stanovení hodnoty kalciového skóre u diabetiků vzhledem k jejich vysokému riziku. Diabetici 2. typu bez anamnézy ICHS mají přibližně stejné riziko vzniku akutního infarktu myokardu jako osoby bez diabetu s anamnézou infarktu myokardu [10]. Studie PREDICT (patients with renal impairment and diabetes undergoing computed tomography) prokázala, že hodnota kalciového skóre je velmi silným nezávislým prediktorem vzniku kardiovaskulární příhody u asymptomatický osob s diabetem 2. typu [11].
CT angiografie
Metodika vyšetření koronárního řečiště pomocí výpočetní tomografie se provádí již více než 10 let a v současnosti se jedná o rutinně využívanou a zároveň jedinou neinvazivní metodu (obr. 2–4). Dostupnost a kvalita se postupně vyvíjela spolu s technickým vývojem multidetektorových CT přístrojů. Oproti vyšetření ostatních oblastí lidského těla je nutností synchronizace akvizice dat s EKG křivkou a hlavním cílem technického vývoje bylo, co nejvýraznější zkrácení časového intervalu nutného k vyšetření celého objemu srdce (tzv. časové rozlišení – temporal resolution). Zkrácením tohoto časového intervalu došlo postupně k významné redukci pohybových artefaktů, a tím ke zlepšení kvality hodnocení. Současný vývoj dospěl do stadia, kdy na vyšetření celého objemu srdce za určitých podmínek postačí jeden R-R interval EKG křivky [3,4].
2. CT angiografie: „měkký“ plát způsobující hemodynamicky nevýznamnou stenózu ACD (A), který obsahuje poměrně významné lipoidní jádro (B). Jedná se tedy o vysoce rizikový cholesterolový plát. Charakter plátu je patrný při cílené analýze i (C, D – lipoidní jádro tmavě zelené). 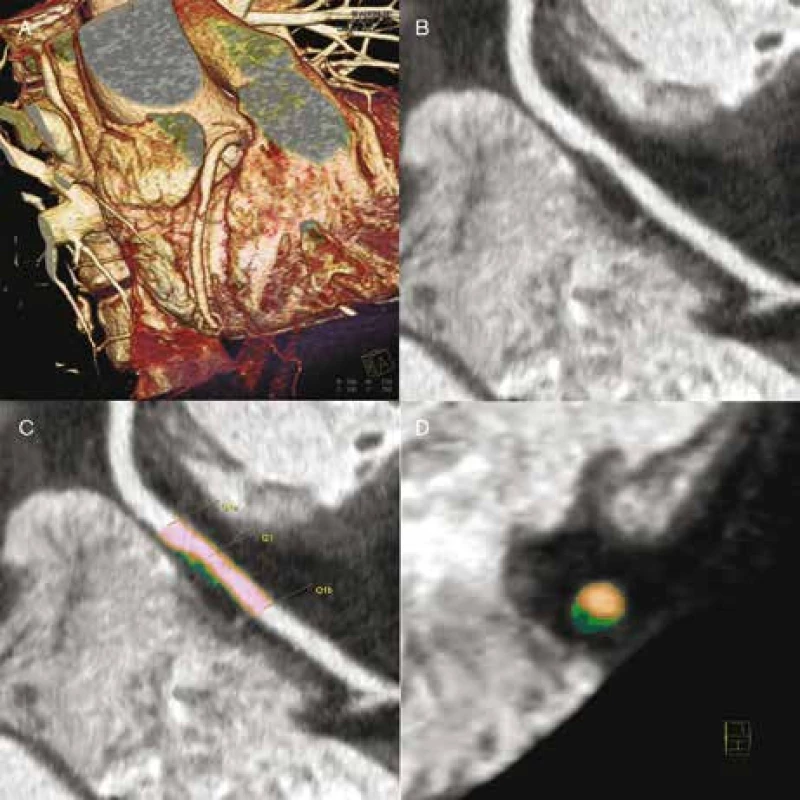
3. CT angiografie: rozsáhlé postižení proximální a střední třetiny RIA fibrózními pláty (A–B) s několika kalcifikacemi, které způsobují až hemodynamicky významnou stenózu (C) u osoby s vysokým kardiovaskulárním rizikem bez anamnézy klinických potíží. 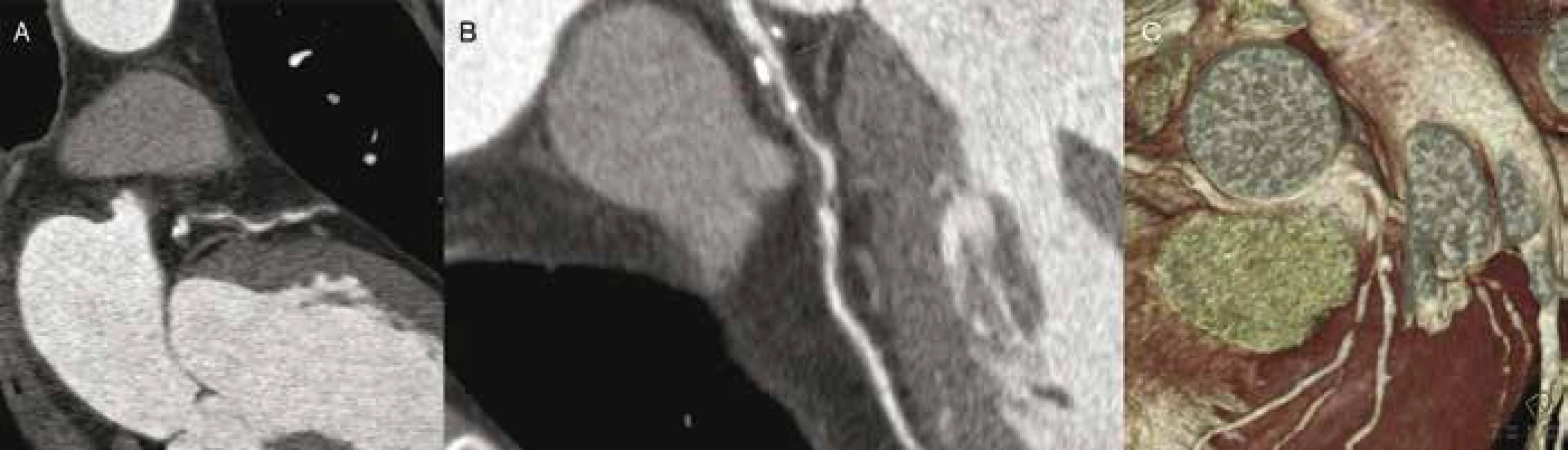
4. CT angiografie: typický zcela kalcifikovaný aterosklerotický plát proximální třetiny RIA, který nezpůsobuje hemodynamicky významnou stenózu (A–B). Cílená rekonstrukce na kalcifikace (C). 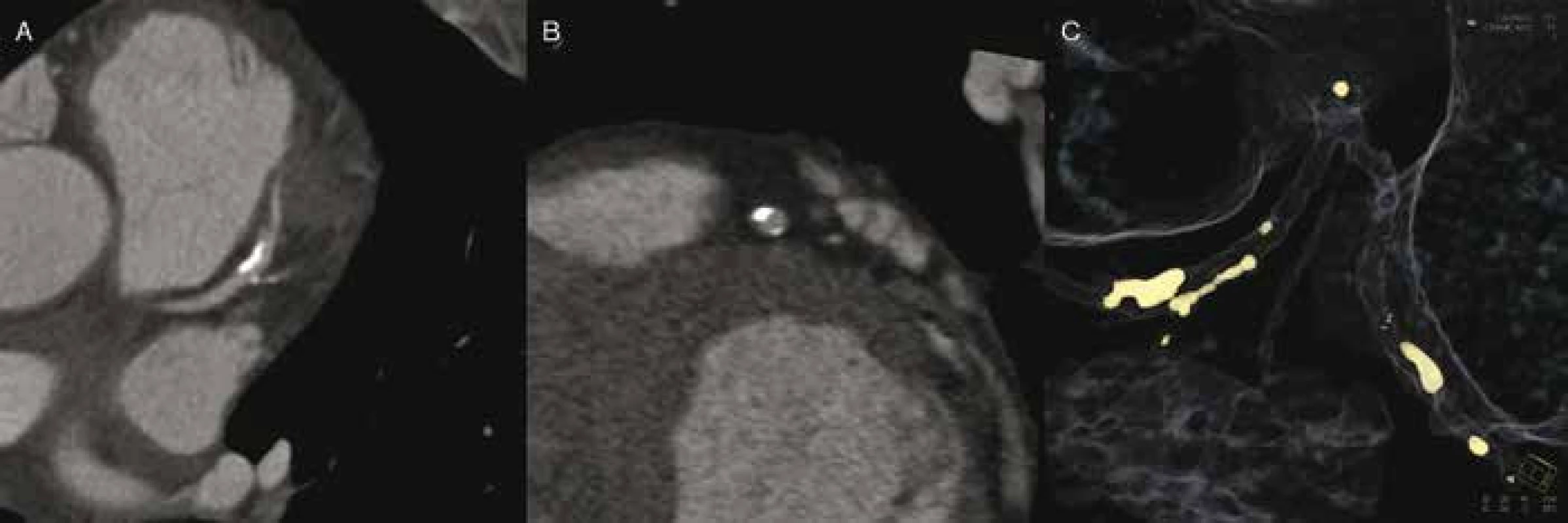
Průběh CT vyšetření srdce je velmi jednoduchý, nutností je však podání jodové kontrastní látky, a tedy zajištění periferního žilního přístupu. Radiační zátěž, která je často označována za hlavní limitaci metody, se díky technickému vývoji podařilo redukovat až na úroveň diagnostické invazivní koronarografie. Také kontrastní látka představuje určité riziko přechodného zhoršení funkce ledvin, u osob s normálními renálními funkcemi je však toto riziko velmi malé. V současnosti se množství jodové kontrastní látky používané pro CT angiografii běžně pohybuje od 60 do 80 ml.
Kvalita metody byla již mnohokrát ověřena srovnáním přesnosti detekce stenotického postižení oproti selektivní koronarogafii jako referenční metodě [12]. Nejen vzhledem k vysoké kvalitě, ale také díky jednoduchosti a bezpečnosti provedení je v současnosti CT angiografie často využívána v sekundární prevenci ICHS. Zejména se jedná o osoby po chirurgické revaskularizaci k ověření průchodnosti koronárních bypassů nebo postižení vlastního řečiště mimo bypassy. Také u osob po endovaskulární léčbě je v případě rozvoje netypických potíží vhodné provést CT angiografii [13].
Zejména s ohledem na primární prevenci ICHS je přínos CT nejen v hodnocení zúžení koronárních větví, ale také v možnosti detailního posouzení charakteru případných aterosklerotických změn, tedy zejména složení aterosklerotických plátů. Nejvyšší riziko akutního koronárního syndromu představují pláty s přítomným lipidovým (cholesterolovým) jádrem, více stabilní jsou pak fibrózní pláty bez cholesterolového jádra. Ukládání vápníku do plátu je obecně považováno za významnou známku „stability“ plátu a ty jsou častěji odpovědné za chronický průběh ICHS. Možnosti a kvalita CT jsou v této problematice srovnatelné s intravaskulárním ultrazvukovým vyšetřením (IVUS) [14–16].
Otázka využití CT angiografie u asymptomatických rizikových osob je samozřejmě velmi diskutovaným tématem, kdy zásadní nevýhodou je výše zmíněná radiační zátěž a kontrastní látka. Na druhou stranu hlavní předností metody je její komplexnost a jednoduchost. Na základě již provedených velkých studií lze konstatovat velmi vysokou negativní prediktivní hodnotu CT angiografie, kdy v případě zcela negativního nálezu z hlediska přítomnosti aterosklerózy je riziko kardiální příhody v následujícím sledovaném období (většinou 5–10 let) velmi nízké. Zároveň bylo také prokázáno zvyšující se riziko v závislosti na významnosti a charakteru postižení při CT angiografii u osob s dosud nediagnostikovanou ICHS [17,18] Současná doporučení mezinárodních organizací (např. American College of Cardiology/American Heart Association) ještě neobsahují jasná pravidla pro indikaci CT angiografie u zcela asymptomatických rizikových osob, nicméně díky postupnému zvyšování kvality zobrazení a redukci radiační zátěže lze předpokládat postupné výraznější využití této metody v oblasti primární prevence [19].
Jako vhodná skupina pro využití CT angiografie v prevenci se ukazují diabetici, i s ohledem na to, že byl u nich prokázán častější výskyt tzv. měkkých aterosklerotických plátů, které nejsou zachytitelné pomocí kalciového skóre. V dosud provedených vyšetřeních je patrný relativně vysoký výskyt významných aterosklerotických změn u dosud asymptomatických osob (25–50 %) a vždy s vyšší četností u diabetiků. A zároveň byla prokázána i prognostická schopnost zvýšeného rizika vzniku kardiovaskulární příhody u takto postižených osob [20,21].
V posledním období došlo k poměrně výraznému rozvoji metodiky objemového perfuzního vyšetření myokardu na výpočetní tomografii. Pomocí farmakologicky navozeného zvýšeného průtoku krve koronárním řečištěm a případným porovnáním s vyšetřením v klidu lze detekovat oblasti myokardu se zátěží podmíněnou nebo fixní hypoperfuzí. Na rozdíl od scintigrafie či magnetické rezonance je velkým přínosem možnost porovnání perfuzních změn s aktuálním stavem koronárního řečiště [22]. Metodika samotná a zejména její využití v praxi se stále vyvíjí, na několika menších studiích již však byla prokázána vysoká kvalita ve srovnání s již zavedenými metodami (scintigrafie, MR). Z hlediska prevence se nabízí možnost vyšetřování vysoce rizikových osob – např. osoby s pokročilou ischemickou chorobou dolních končetin před chirurgickým řešením.
Magnetická rezonance
Magnetická rezonance (MR) zaznamenala za posledních 20 let významný technický vývoj vedoucí k dnes běžnému využití v zobrazení srdce. Tato metoda je vhodná k vyšetření kinetiky myokardu, srdečních chlopní či zkratových vad včetně velmi kvalitního morfologicko-patologického hodnocení srdečních oddílů (obr. 5). Z hlediska možností hodnocení ICHS je možné pomocí MR hodnotit perfuzi myokardu při prvním průchodu podané kontrastní látky (first-pass perfusion). Redistribuce této látky v myokardu dovoluje provedení pozdních vyšetření (8–20 min od podání kontrastní látky) s možností hodnocení tzv. pozdního sycení myokardu (delayed enhancement) v oblasti s většího extracelulátního//extravaskulárního prostoru (akutní destrukce myocytů či fibrózní tkáň) [23]. Okrsky myokardu s perzistujícím nasycením kontrastní látkou jsou tedy přímou známkou poškození svalové tkáně. Hodnocením charakteru a lokalizace těchto změn lze s poměrně vysokou senzitivitou i specificitou rozlišit etiologii tohoto postižení mezi ischemickou (fibrózní jizva či akutní ischemie) a neischemickou (zánětlivé postižení, sarkoidóza, amyloidóza a další vzácné choroby). Při porovnání s perfuzní scintigrafií je výhoda MR ve větším prostorovém rozlišení, které umožňuje zobrazení i drobných jizev. To platí i při porovnání s echokardiografií, kdy drobné změny v subendokardiálních vrstvách po minimálních infarktech často nemusí negativně ovlivnit kinetiku.
5. Magnetická rezonance: okrsky pozdního sycení v subendokardiální lokalizaci (šipky) v rozsahu apikální a střední třetiny svědčící pro proběhlou ischemii (nonQ AIM). 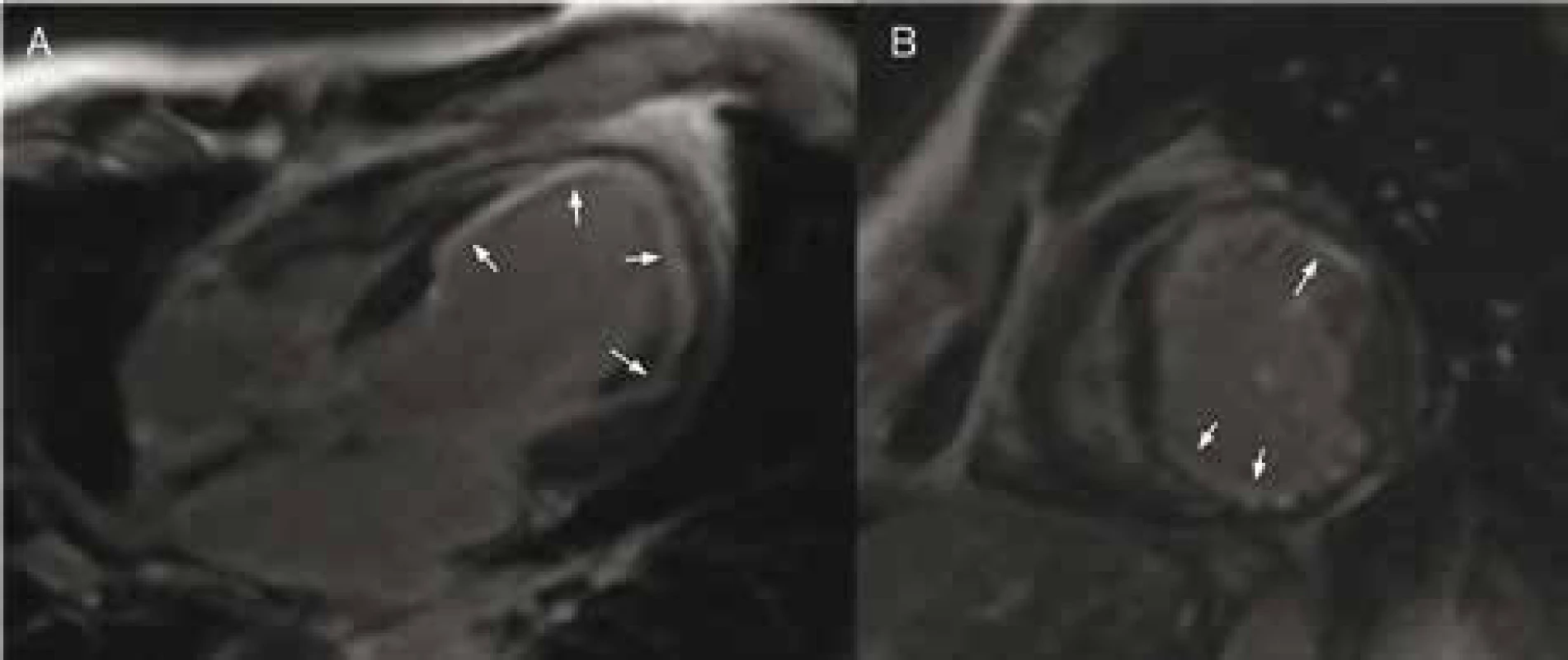
Magnetická rezonance má však potenciál ve stanovení kardiovaskulárního rizika, a to zejména v oblasti diagnostiky tzv. němé ischemie (silent ischaemia), kdy dojde k průkazu většinou drobných fibrózních jizev u osob doposud bez anamnézy klinicky proběhlého akutního infarktu myokardu. Nález proběhlé ischemie u jinak asymptomatické osoby výrazně zvyšuje riziko budoucích závažných projevů ICHS. V několika studiích byla zaznamenána přítomnost těchto změn u vysokého procenta, a to zejména u diabetiků (až 40 %), u kterých je pravděpodobnost vyšší vzhledem k vyvíjející se neuropatii [24]. Možnosti využití této neinvazivní metody se mohou výrazně zvýšit při provedení kombinovaného vyšetření v klidu a při farmakologické zátěži. Při provedení vyšetření tímto způsobem lze dosáhnout výsledků odpovídajících zátěžovému echokardiografickému vyšetření a perfuzní scintigrafii myokardu. V porovnání se zátěžovou echokardiografií představuje MR více komplexní metodu, která je za pomocí paramagnetické kontrastní látky schopna kromě hodnocení změn kinetiky myokardu posoudit i změny perfuze, stupeň poškození myokardu a částečně i viabilitu [25].
Přes svou nespornou kvalitu a komplexnost není MR k primární prevenci ICHS využívána. Jedním z důvodů je relativní technická a také ekonomická náročnost vyšetření v porovnání s echokardiografií. Některé další nedostatky vyplývají z různých technických možností samotných přístrojů.
Perfuzní scintigrafie
Perfuzní scintigrafie myokardu patří mezi metody nukleární medicíny, podává se tedy nitrožilně radiofarmakum, které má afinitu k myocytům a jeho přítomnost v srdečním svalu zjištěná následnou detekcí odpovídá jeho prokrvení (obr. 6). V dnešní době se nejčastěji využívá preparátu značeného metastabilním izotopem 99Tc (např. MIBI – metylizobutylizonitrát). Dříve často používaný 201Tl chlorid se vzhledem k vysoké radiační zátěži dnes využívá minimálně. Detekce aktivity se dnes nejčastěji provádí metodou SPECT (single-photon emission computed tomography) a tato metoda se může provádět v klidu i po předchozí fyzické či farmakologicky navozené zátěži. V případě postižení koronární tepny může dojít k deficitu přísunu kyslíku vzhledem k potřebám myokardu a následnému rozvoji ischemie, která se projeví nižší aktivitou radiofarmaka v postižené oblasti [26,27].
6. Perfuzní CT + CTA + SKG: asymptomatický pacient bez anamnézy ICHS před pánevní cévní rekonstrukcí. Perfuzní deficit inferoseptální oblasti při zátěžovém perfuzním CT vyšetření (A) a normální perfuze při klidovém vyšetření (B). Příčinou zátěží podmíněné hypoperfuze byla stenóza proximální ACD (CT angiografie – C, koronarografie – D). 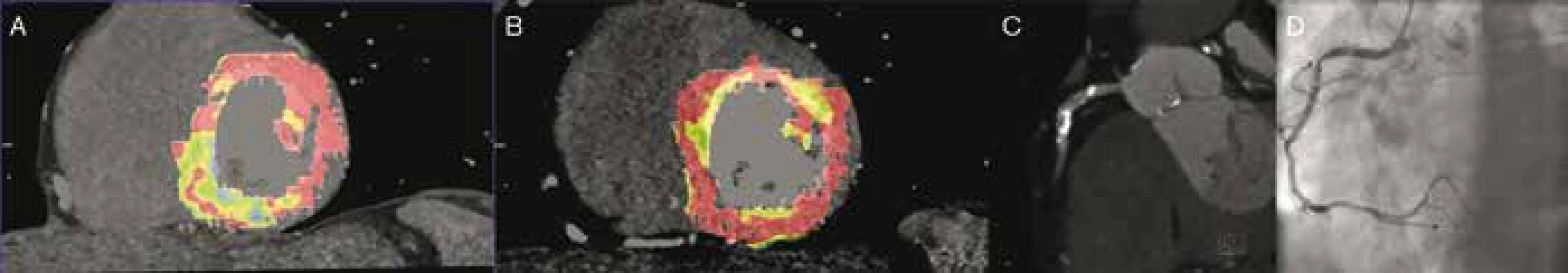
Perfuzní scintigrafie je spolehlivě nejčastěji používanou metodou ve studiích zabývajících se hodnocením rizika, přestože doposud nebyla prokázána přímá souvislost mezi přítomností zátěží vyvolaných perfuzních defektů a budoucí akutní manifestací ICHS u asymptomatických dobrovolníků. Na druhou stranu normální nález při kombinovaném scintigrafickém vyšetření myokardu znamená velmi nízkou pravděpodobnost vzniku kardiovaskulární příhody v pětiletém sledování [28].
Perfuzní scintigrafie je dnes rutinně využívána v klinické praxi u pacientů s chronickou formou ICHS k identifikaci a rozlišení zátěžových a fixních poruch perfuze myokardu v návaznosti na revaskularizační intervenční či chirurgické výkony. Jejich využití v hodnocení rizika u asymptomatických osob je velmi problematické. Bylo publikováno několik studií, ve kterých byli vyšetřováni např. asymptomatičtí diabetici pomocí perfuzního vyšetření myokardu. Výsledky těchto studií potvrdily přínos metody v záchytu klinicky němé ischemie s prognostickou schopností vyšší mortality u osob s patologickým nálezem. V jedné studii byl identifikován velmi rizikový nález při SPECT myokardu u 18 % asymptomatických diabetiků se zvýšenou mortalitou [29,30]. V současnosti se však perfuzní scintigrafie i vzhledem k technické náročnosti a zátěži v primární prevenci ICHS rutinně nepoužívá.
Závěr
Moderní zobrazovací metody mají jistě potenciál i v oblasti prevence kardiovaskulárních chorob a jejich praktické uplatnění se výrazně zvyšuje díky zvyšující se kvalitě a klesající zátěži pro vyšetřované osoby v případě výpočetní tomografie.
Doručeno do redakce: 16. 10. 2013
Přijato po recenzi: 25. 11. 2013
MUDr. Jan Baxa, Ph.D.
Klinika zobrazovacích metod,
FN Plzeň a LF UK v Plzni
baxaj@fnplzen.cz
Sources
1. van Werkhoven JM, Schuijf JD, Gaemperli O et al. Prognostic value of multislice computed tomography and gated single-photon emission computed tomography in patients with suspected coronary artery disease. J Am Coll Cardiol 2009; 53 : 623–632.
2. Budoff MJ. Prevalence of soft plaque detection with computed tomography. J Am Coll Cardiol 2006; 48 : 319–321.
3. Ohnesorge B et al. Multi-slice and dual-source CT in cardiac imaging. Berlin Heidelberg: Verlag-Springer 2007.
4. Baxa J, Ferda J. Multidetektorová výpočetní tomografie srdce. Praha: Galén 2012.
5. Budoff MJ, Gul K. Computed tomographic cardiovascular imaging. Semin Ultrasound CT MR 2006; 27 : 32–41.
6. Agatston AS, Janowitz WR, Hildner FJ et al. Quantification of coronary artery calcium using ultrafast computed tomography. J Am Coll Cardiol 1990; 15 : 827–832.
7. Hadamitzky M, Distler R, Meyer T et al. Prognostic value of coronary computed tomographic angiography in comparison with calcium scoring and clinical risk scores. Circ Cardiovasc Imaging 2011; 4 : 16–23.
8. Shaw LJ, Raggi P, Schisterman E et al. Prognostic value of cardiac risk factors and coronary artery calcium screening for all-cause mortality. Radiology 2003; 228 : 826–833.
9. Polonsky TS, McClelland RL, Jorgensen NW et al. Coronary artery calcium score and risk classification for coronary heart disease prediction. JAMA 2010; 303 : 1610–1616.
10. Haffner SM, Lehto S, Rönnemaa T et al. Mortality from coronary heart disease in subjects with type 2 diabetes and in nondiabetic subjects with and without prior myocardial infarction. N Engl J Med 1998; 339 : 229–234.
11. Elkeles RS, Godsland IF, Feher MD et al. Coronary calcium measurement improves prediction of cardiovascular events in asymptomatic patients with type 2 diabetes: the PREDICT study. Eur Heart J 2008; 29 : 2244–2251.
12. Johnson TR, Nikolaou K, Busch S et al. Diagnostic accuracy of dual-source computed tomography in the diagnosis of coronary artery disease. Invest Radiol 2007; 42 : 684–691.
13. Williams MC, Reid JH, McKillop G et al. Cardiac and coronary CT comprehensive imaging approach in the assessment of coronary heart disease. Heart 2011; 97 : 1198–1205.
14. Ferda J, Baxa J. Hodnocení aterosklerotických plátů koronárních tepen při CT-angiografii. Ces Radiol 2009; 63 : 281–289.
15. Achenbach S, Moselewski F, Ropers D et al. Detection of calcified and noncalcified coronary atherosclerotic plaque by contrast-enhanced, submillimeter multidetector spiral computed tomography: a segment-based comparison with intravascular ultrasound. Circulation 2004; 109 : 14–17.
16. Fischer C, Hulten E, Belur P et al. Coronary CT angiography versus intravascular ultrasound for estimation of coronary stenosis and atherosclerotic plaque burden: a meta-analysis. J Cardiovasc Comput Tomogr 2013; 7 : 256–266.
17. Ostrom MP, Gopal A, Ahmadi N et al. Mortality incidence and the severity of coronary atherosclerosis assessed by computed tomography angiography. J Am Coll Cardiol 2008; 52 : 1335–1343.
18. Chow BJ, Wells GA, Chen L et al. Prognostic value of 64-slice cardiac computed tomography severity of coronary artery disease, coronary atherosclerosis, and left ventricular ejection fraction. J Am Coll Cardiol 2010; 55 : 1017–1028.
19. Taylor AJ, Cerqueira M, Hodgson JM et al. ACCF/SCCT/ACR/AHA/ASE/ASNC/NASCI/SCAI/SCMR 2010 Appropriate use criteria for cardiac computed tomography. Circulation 2010; 122: e525–e555.
20. Hadamitzky M, Meyer T, Hein F et al. Prognostic value of coronary computed tomographic angiography in asymptomatic patients. Am J Cardiol 2010; 105 : 1746–1751.
21. Baxa J, Ferda J, Zikmund M et al. CT angiografie koronárních tepen u pacientů se zvýšeným rizikem vzniku ischemické choroby srdeční – prospektivní studie s dvouletým sledováním. Ces Radiol 2010; 64 : 301–306.
22. Greif M, von Ziegler F, Bamberg F et al. CT stress perfusion imaging for detection of haemodynamically relevant coronary stenosis as defined by FFR. Heart 2013; 99 : 1004–1011.
23. Burke AP, Kolodgie FD, Zieske A et al. Morphologic findings of coronary atherosclerotic plaques in diabetics: a postmortem study. Arterioscler Thromb Vasc Biol 2004; 24 : 1266–1271.
24. Bogaert J et al. Clinical cardiac MRI. Berlin Heidelberg: Springer-Verlag 2005.
25. Kitagawa K, Sakuma H, Nagata M et al. Diagnostic accuracy of stress myocardial perfusion MRI and late gadolinium-enhanced MRI for detecting flow-limiting coronary artery disease: a multicenter study. Eur Radiol 2008; 18 : 2808–2816.
26. Burgess DC, Hunt D, Li L et al. Incidence and predictors of silent myocardial infarction in type 2 diabetes and the effect of fenofibrate: an analysis from the Fenofibrate Intervention and Event Lowering in Diabetes (FIELD) study. Eur Heart J 2010; 31 : 92–99.
27. Di Carli MF, Hachamovitch R. New technology for noninvasive evaluation of coronary artery disease. Circulation 2007; 115 : 1464–1480.
28. Fleischmann KE, Hunink MG, Kuntz KM et al. Exercise echocardiography or exercise SPECT imaging? A meta-analysis of diagnostic test performance. JAMA 1998; 280 : 913–920.
29. Elhendy A, Schinkel A, Bax JJ et al. Long-term prognosis after a normal exercise stress Tc-99m sestamibi SPECT study. J Nucl Cardiol 2003; 10 : 261–266.
30. Rajagopalan N, Miller TD, Hodge DO et al. Identifying high-risk asymptomatic diabetic patients who are candidates for screening stress single-photon emission computed tomography imaging. J Am Coll Cardiol 2005; 45 : 43–49.
Labels
Paediatric cardiology Internal medicine Cardiac surgery Cardiology
Article was published inCardiology Review

2013 Issue 4-
All articles in this issue
- End organ damage in arterial hypertension and cardiovascular risk
- Current approach to the options of primary and secondary prevention of ischemic cerebrovascular accident
- The importance of imaging methods in the cardiovascular disease prevention
- Psychosocial risk factors of cardiovascular diseases and possibilities of their intervention
- Acute cardiac liver injury and levosimendan
- Levosimendan treatment as a „bridge therapy“ in a patient with metastatic testicular cancer and severe systolic heart failure - competition case report
- Syncope of multifactorial etiology or several symptoms of the same disease? - competition case report
- Cardiology Review
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- End organ damage in arterial hypertension and cardiovascular risk
- Syncope of multifactorial etiology or several symptoms of the same disease? - competition case report
- The importance of imaging methods in the cardiovascular disease prevention
- Psychosocial risk factors of cardiovascular diseases and possibilities of their intervention
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

