-
Medical journals
- Career
Je prognóza nemocných s chronickým srdečním selháním stále tak špatná?
Authors: O. Ludka; L. Galková; M. Šablaturová; Jiří Jarkovský; L. Dušek; J. Špinar
Published in: Kardiol Rev Int Med 2011, 13(1): 30-36
Category: From Hypertension to Heart Failure
Overview
Úvod:
Podle Framinghamské studie umírá do pěti let po vzniku klinických příznaků srdeční nedostatečnosti více než 60 % nemocných a do jednoho roku přibližně 17 % nemocných.Cíl:
Zjistit mortalitu nemocných s chronickým srdečním selháním sledovaných v ambulanci srdečního selhání ve FN Brno.Metodika:
Retrospektivní sběr dat z ambulantních záznamů konsekutivních pacientů se srdečním selháním.Soubor:
159 pacientů, 70,4 % mužů, 29,6 % žen, věk 66 (40; 84) let, délka sledování 32,5 (11,1; 61,9) měsíce (8 až 66 měsíců), NYHA I–II/II/III 26,4/61,6/12 %, EF LK 30 (15; 45) %, diastolická dysfunkce 94,3 %, etiologie CHSS – 68,6 % ICHS, 22,6 % DKMP, ostatní 8,8 %, komorbidity – hypertenze 67,9 %, infarkt myokardu 49,1 %, dyslipoproteinemie 56,6 %, diabetes mellitus 34 %, CMP + TIA 11,3 %, CHOPN 8,8 %, anémie 16,4 %, fibrilace síní 15,1 %, GF dle Cockrofta 66,8 (27,2; 125,2) ml/s, GF < 60 ml/s 44,7 %, farmakologická léčba: ACE-I 84,3 %, ARB 13,2 %, BB 95,6 %, kličková diuretika 60,4 %, hydrochlorothiazid 21,7 %, spironolacton 52,8 %, digitalis 22,6 %, statiny 61,6 %, nefarmakologická léčba: PM 18,9 %, CRT-D 5 %, CRT-P 7,5 %, PCI 30,2 %, CABG 10,1 %.Výsledky:
Za dobu sledování zemřelo 24 pacientů (15,1 %), z toho na kardiovaskulární komplikace 18 pacientů (11,3 %). Kumulativní přežití bylo v 1. roce 96,2 %, ve 2. roce 90,8 %, ve 3. roce 87,6 % a ve 4. roce 82,7 %.Závěr:
Mortalita udávaná ve Framinghamské studii vysoce převyšuje mortalitu našeho souboru, což je pravděpodobně dáno jednak zlepšením farmakologické i nefarmakologické terapie pacientů se srdečním selháním, jednak také mírně odlišným spektrem pacientů.Klíčová slova:
chronické srdeční selhání – prognóza – farmakologická léčba – nefarmakologická léčbaÚvod
Stárnutí populace a výrazné zlepšení péče o akutní koronární syndromy vedou k neustálému nárůstu incidence i prevalence srdečního selhání [1]. Prevalence srdečního selhání se v evropských zemích pohybuje mezi 1 a 2 % a výrazně stoupá s věkem [2]. Počet hospitalizací pro srdeční selhání se za posledních 20 let zvýšil v rozvinutých zemích takřka čtyřnásobně. Akutní srdeční selhání patří mezi nejčastější příčiny hospitalizací pacientů starších 65 let [3,4] a je spojeno s velmi špatnou prognózou. Asi 45 % nemocných s akutním srdečním selháním je rehospitalizováno do jednoho roku [5]. Hospitalizační mortalita se pohybuje od 4 % [6] do 29 % [7], roční od 17 % (Framingham) do 47 % [7]. Dle Framinghamské studie umírá do pěti let po vzniku klinických příznaků srdeční nedostatečnosti více než 60 % nemocných a do osmi let dle Sosina kolem 90 % nemocných hospitalizovaných pro akutní srdeční selhání [8]. Tato prognóza se v průběhu druhé poloviny minulého století výrazněji neměnila. Stárnutí populace, nárůst incidence, prevalence a počtu rehospitalizací zvyšuje i ekonomickou náročnost léčby srdečního selhání, která dnes ve vyspělých evropských zemích představuje 1–2 % celkových nákladů na zdravotnictví [9]. Pro pacienty se srdečním selháním je kromě kvality života důležité stanovení prognózy.
Cíl
Cílem naší práce bylo zjistit, zda může mít zlepšení terapie nemocných s chronickým srdečním selháním na přelomu století vliv na mortalitu těchto nemocných.
Metodika
Do studie byli zařazeni všichni pacienti s diagnózou chronického srdečního selhání, splňující diagnostická kritéria České a Evropské kardiologické společnosti, sledovaní u prvního autora ve specializované ambulanci srdečního selhání Interní kardiologické kliniky Fakultní nemocnice Brno. Jedná se o retrospektivní sběr dat z ambulantních záznamů konsekutivních pacientů. Základní popis získaných dat je prováděn s použitím standardních statistických metod. Pro kontinuální proměnné bylo použito průměru a směrodatné odchylky, popřípadě mediánu a percentilů v případě nedodržení předpokladů o normalitě rozložení, pro kategoriální proměnné byl popis proveden pomocí procentuálního zastoupení kategorií. Pro stanovení rozdílů v kontinuálních proměnných mezi dvěma skupinami nemocných je použit dle normality t-test nebo Mann-Whitney U test. Vztah mezi dvěma kategoriálními proměnnými je stanoven pomocí Fisherova přesného testu v případě 2 × 2 tabulek nebo pomocí ML Chi-square testu. Hodnoty p < 0,05 jsou brány jako standardní hranice pro statistickou významnost, případně jsou korigovány na mnohonásobné testování. Pro vizualizaci přežívání pacientů byly použity Kaplan-Meierovy křivky přežití. Statistická významnost rozdílu v přežívání mezi skupinami pacientů je hodnocena pomocí Log-rank testu, ke stanovení relativního rizika byl použit jednorozměrný a vícerozměrný Coxův model proporcionálních rizik. Statistická analýza byla provedena v SPSS 18.0.2 and Statistica 9.1.
Charakteristika souboru
Do studie bylo zařazeno 159 pacientů (70,4 % mužů, 29,6 % žen), základní charakteristika souboru včetně rozdílů mezi muži a ženami je uvedena v tab. 1.
Table 1. Základní charakteristika pacientů. 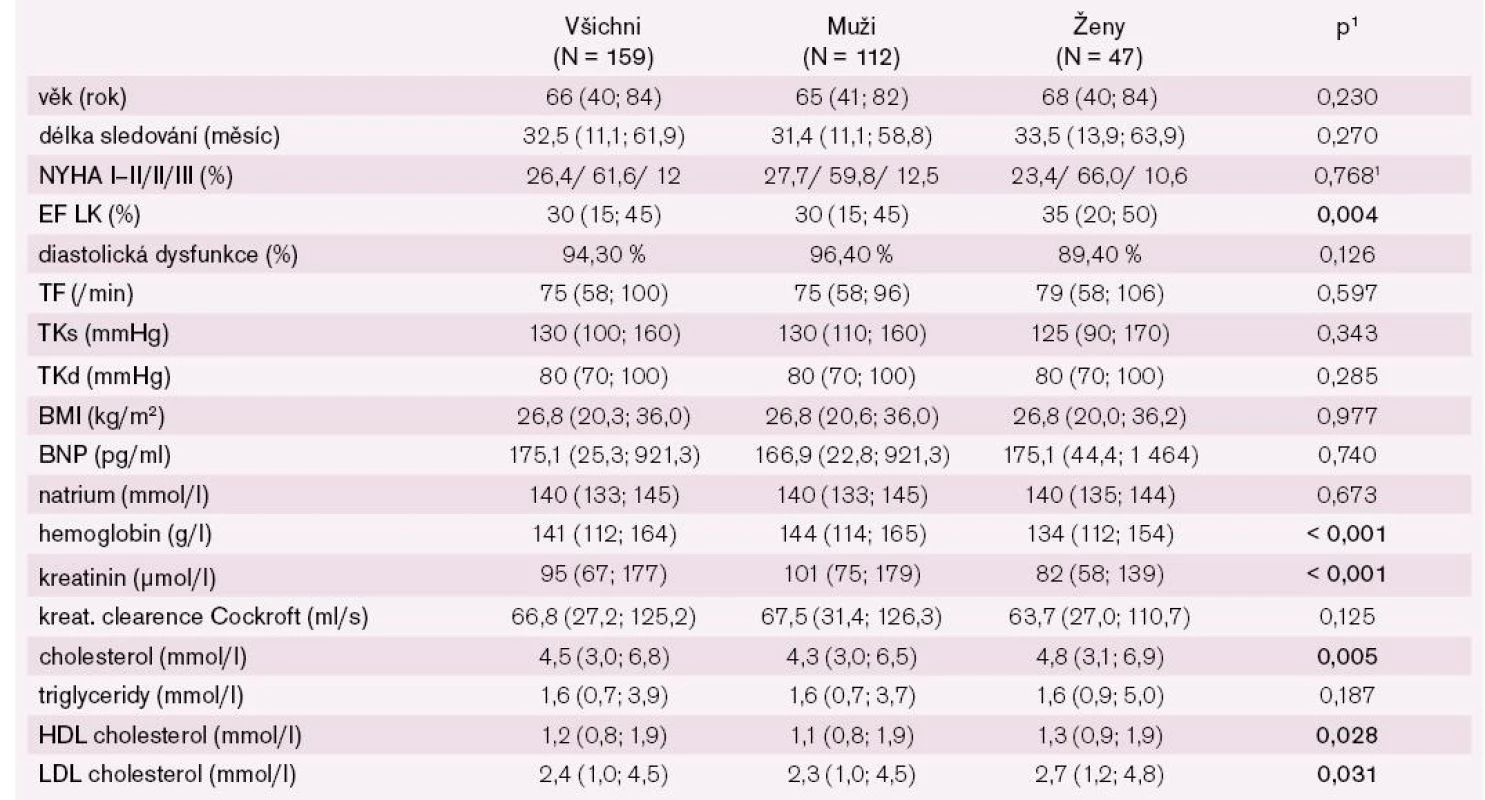
kontinuální proměnné – medián (percentily 5; 95), kategoriální proměnné – četnost 1statistická významnost hodnocena Fisherovým přesným testem Muži měli statisticky významně nižší ejekční frakci levé komory srdeční, celkový, HDL a LDL cholesterol, naopak vyšší hodnotu hemoglobinu a kreatininu. Kreatininová clearence kalkulovaná dle Cockroft-Gaulta již nevykazovala statisticky významný rozdíl mezi muži a ženami. Věkové rozložení pacientů v našem souboru ukazuje graf 1.
Graph 1. Věkové rozložení pacientů. 
Více než 2/3 jedinců byly starší 61 let a nejvíce nemocných bylo ve věkové kategorii 71–80 let. V grafu 2 je znázorněno rozložení pacientů podle ejekční frakce levé komory srdeční. Naprostá většina nemocných sledovaných ve specializované ambulanci srdečního selhání měla systolickou dysfunkci levé komory srdeční.
Graph 2. Rozložení ejekční frakce levé komory srdeční. 
V etiologii srdečního selhání převažuje ischemická choroba srdeční nad dilatační kardiomyopatií a ostatními příčinami (graf 3).
Graph 3. Etiologie srdečního selhání. 
Mezi ostatní příčiny patří hypertenze, chlopenní vady, kardiomyopatie po chemoterapii, posttachykardická kardiomyopatie či kardiomyopatie po prodělané myokarditis. Mezi nejčastější komorbidity patřila hypertenze a dyslipoproteinemie, nezanedbatelný je ale samozřejmě i poměrně vysoký výskyt fibrilace síní (tab. 2).
Table 2. Komorbidity. 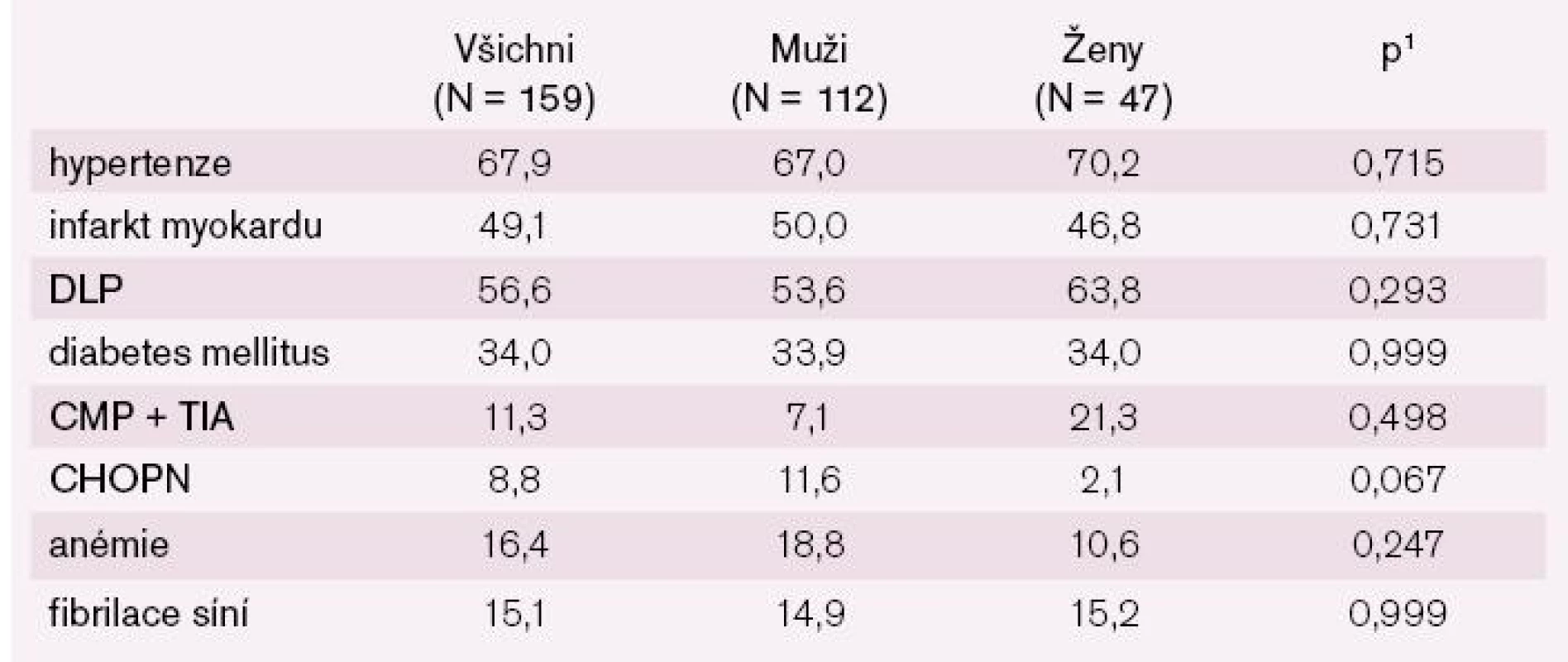
kategoriální proměnné – relativní četnost (%) 1statisticka významnost hodnocena Fisherovým přesným testem Téměř všichni nemocní měli zavedenou léčbu blokátory RAAS a betablokátory (graf 4). Resynchronizační léčbu mělo více než 12 % nemocných a revaskularizaci myokardu více než 40 % nemocných (graf 5). Délku sledování pacientů ukazuje graf 6.
Graph 5. Nefarmakologická léčba. 
Graph 6. Délka sledování pacientů. 
Výsledky
Za dobu sledování zemřelo 24 pacientů (15,1 %), z toho na kardiovaskulární komplikace 18 pacientů (11,3 %). Mortalita, zejména však kardiovaskulární, narůstala s věkem, což je v souladu s literárními údaji (graf 7). Přežívání nemocných v různých věkových kategoriích ukazuje graf 8. Mezi jednotlivými věkovými kategoriemi jsme nenalezli statisticky významné rozdíly v mortalitě. Celková ani kardiovaskulární mortalita mužů a žen se v našem souboru nelišila, což ukazuje graf 9 a 10. Kumulativní přežití bylo v 1. roce 96,2 %, ve 2. roce 90,8 %, ve 3. roce 87,6 % a ve 4. roce 82,7 %.
Graph 7. Mortalita dle věkových kategorií. 
Graph 8. Přežívání nemocných podle věkových kategorií. 
Graph 10. Kardiovaskulární mortalita. 
Diskuze
Úmrtnost nemocných se srdečním selháním se po několik desetiletí neměnila, od konce 80. let 20. století lze však pozorovat trend k poklesu mortality [10–12]. Tento pokles je však mnohem menší než pokles v našem souboru. Vývoj mortality mezi nehospitalizovanými pacienty s chronickým srdečním selháním navíc není přesně znám.
Příčiny chronického srdečního selhání jsou na začátku 21. století zcela odlišné, než byly před 50 lety. Dříve byla hlavní příčinou hypertenze a porevmatické srdeční vady, především mitrální stenóza. V současné době při správné kontrole hypertenze a včasné indikaci zákroku na chlopních je nejčastější příčinou chronického srdečního selhání, stejně jako v našem souboru, ischemická choroba srdeční a dilatační kardiomyopatie. Pacienti se srdečním selháním způsobeným chlopenní vadou měli ve Framinghamské studii horší prognózu než ti, u kterých bylo způsobeno ischemickou chorobou srdeční [13]. Zlepšení léčby ischemické choroby srdeční a hypertenze, hlavních příčin chronického srdečního selhání, může tedy kromě snížení incidence srdečního selhání vést i ke zlepšení prognózy nemocných.
Zavedení nových léčebných modalit v posledních 20 letech vedlo nejen ke zlepšení symptomů pacienta, redukci rehospitalizací, ale i k poklesu mortality v selektovaných skupinách nemocných zařazených ve farmakologických studiích [14,15]. Data z velkých randomizovaných studií zaměřených na hodnocení farmakologické i nefarmakologické léčby srdečního selhání jsou významným zdrojem poznatků o rizikové stratifikaci těchto pacientů. Nezpochybnitelnou výhodou těchto souborů je jejich rozsah, na druhou stranu jsou podrobeny významné selekci vedoucí k nižšímu zastoupení starších nemocných a polymorbidních jedinců, navíc se ve svém multicentrickém uspořádání potýkají s možnými metodickými či technickými odlišnostmi mezi centry. Ve farmakologické léčbě posledních 15 let se jasně ukázalo, že základním lékem volby, který prodlužuje život, je inhibitor angiotenzin konvertujícího enzymu. První studie ukazující pozitivní prognostický efekt ACE-I byla publikována v roce 1987 [16]. ACE-I se však začaly v léčbě srdečního selhání široce používat až po zveřejnění výsledků studie SOLVD v roce 1991 [17]. Jestliže extrapolujeme 12leté zkušenosti ze studie SOLVD, tak ACE-I mohou prodloužit život o 3–4 roky [18]. Národní průzkumy však bohužel ukazují, že ACE-I jsou, i přes data z velkých klinických studií, stále nedostatečně předepisovány nemocným s chronickým srdečním selháním. Podle studie IMPROVEMENT, do které bylo v letech 1999–2000 zařazeno více než 11 000 nemocných, bylo ACE-I léčeno pouze 60 % nemocných se srdečním selháním [19], což je výrazně méně než v našem souboru. Blokátory beta adrenergních receptorů, častěji zvané betablokátory, patří k nejrozšířenějším preparátům v léčbě hypertenze, ischemické choroby srdeční a v poslední době i chronického srdečního selhání. Benefit z podávání betablokátorů u nemocných s chronickým srdečním selháním byl plně prokázán až v roce 1999 [15]. Dle studie IMPROVEMENT je těmito léky léčeno ale jen 34 % nemocných s chronickým srdečním selháním, opět výrazně méně než v našem souboru. Léčba je tedy dalším zkreslujícím faktorem, který vrhá stín na data získaná v době, kdy drtivá většina pacientů zcela jistě nedostávala kombinovanou léčbu ACE inhibitory či sartany a betablokátory.
Kromě farmakologické léčby došlo koncem minulého století také k významnému rozmachu nefarmakologické terapie nemocných se srdečním selháním. Individualizace rizika náhlé srdeční smrti přináší od roku 1980 do klinické praxe novou nefarmakologickou metodu – implantaci kardioverter-defibrilátoru. Efektivita kardioverter-defibrilátorů v redukci mortality byla prokázána v 80. a 90. letech minulého století nejdříve v rámci sekundární prevence (studie AVID, CASH) a posléze i v rámci primární prevence (studie MUSTT, CIDS, MADIT I) [20–24]. Další multicentrické studie MADIT II a SCD HeFT doplnily další indikaci pro primárně preventivní implantace kardioverter-defibrilátorů [25,26]. První zkušenosti s biventrikulární stimulací u nemocných s chronickým srdečním selháním byly popsány v roce 1994 [27]. Od té doby bylo provedeno mnoho rozsáhlých studií potvrzujících přínos biventrikulární stimulace u nemocných s chronickým srdečním selháním. Všechny randomizované studie potvrdily signifikantní zlepšení klinických symptomů a taktéž zlepšení kvality života. K rozšíření srdeční resynchronizační terapie přispěly především výsledky dvou recentních mortalitních studií. Ve studii COMPANION byla redukována mortalita při použití samotné biventrikulární stimulace oproti konzervativně léčené skupině o 24 %, v případě kombinace s implantabilním kardioverter-defibrilátorem (ICD) to bylo dokonce o 36 % [28]. Efekt biventrikulární stimulace na kombinovaný cíl (mortalita, hospitalizace pro významnou kardiovaskulární morbiditu) byl prokázán také ve studii CARE-HF [29]. Zatím poslední studií poukazující na efekt kombinované nefarmakologické léčby (srdeční resynchronizační terapie + implantabilní kardioverter-defibrilátor – CRT-D) u pacientů s chronickým srdečním selháním je studie MADIT-CRT, která byla poprvé prezentována v roce 2009 [30]. Na základě těchto studií je srdeční resynchronizační terapie indikována především ve spojení s ICD. V našem souboru bylo léčeno ať už samotnou resynchronizační léčbou, nebo její kombinací s kardioverter-defibrilátorem téměř 13 % nemocných, což při posuzování mortality jistě není zanedbatelné množství.
Vedle vývoje farmakologické a nefarmakologické léčby je důležité také zlepšení diagnostiky, především rutinní zavedení echokardiografie, které může vést ke zlepšení mortality díky včasné diagnostice.
V posledních 20 letech došlo k významnému rozvoji diagnostiky a léčby srdečního selhání. Existuje celá řada faktorů, které mohou ovlivňovat vývoj mortality nemocných s chronickým srdečním selháním, a je velmi těžké určit, které mají v současné době hlavní vliv.
Závěr
Mortalita udávaná ve starších studiích vysoce převyšuje mortalitu našeho souboru, což je pravděpodobně dáno zlepšením diagnostiky, farmakologické i nefarmakologické léčby pacientů se srdečním selháním, ale také mírně odlišným spektrem pacientů.
Limitace
Do naší studie byli zařazeni všichni nemocní s chronickým srdečním selháním sledovaní ve specializované ambulanci, čímž jsme se snažili omezit selekci pacientů. K určité selekci však došlo ještě předtím, než bylo zahájeno sledování těchto pacientů v naší ambulanci. Pacienti, kteří z jakéhokoli důvodu nebyli schopni dojíždět na pravidelné kontroly, nebyli do ambulance objednáni a tím ani sledováni. Další limitací souboru je jeho velikost.
Podpořeno grantem IGA MZ 10422-3/2009.
Supported by grant Ministry of Health Czech Republic NS10422-3/2009.Seznam zkratek
ACE-I – inhibitory angiotenzin konvertujícího enzymu, ARB – blokátory receptoru 1 pro angiotenzin II, BB – betablokátory, BMI – body mass index, BNP – B-typ natriuretickeho peptidu, CABG – aortokoronární bypass, CMP – cévní mozková příhoda, CRT-D – srdeční resynchronizační terapie + implantabilní kardioverter-defibrilátor, CRT-D – implantabilni kardioverter defibrilator + resynchronizacni terapie, CRT-P – srdeční resynchronizační terapie (biventrikulární stimulace), DKMP – dilatační kardiomyopatie, DLP – dyslipoproteinemie, EF LK – ejekční frakce levé komory srdeční, GF – glomerulární filtrace, HCTH – hydrochlorothiazid, CHOPN – chronická obstrukční plicní nemoc, CHSS – chronické srdeční selhání, ICD – implantabilní kardioverter-defibrilátor, ICHS – ischemická choroba srdeční, NYHA – New York Heart Association – klasifikace, PCI – perkutánní koronární intervence, PM – pacemaker, TIA – tranzitorní ischemická ataka, TKd – diastolický krevní tlak, TKs – systolický krevní tlak.
Doručeno do redakce 25. 10. 2010
Přijato po recenzi 1. 12. 2010MUDr. Ondřej Ludka, Ph.D.1
Lujza Galková1
Martina Šablaturová1
RNDr. Jiří Jarkovský, Ph.D.2
doc. RNDr. Ladislav Dušek, Ph.D.2
prof. MUDr. Jindřich Špinar, CSc.1
1Interní kardiologická klinika FN Brno a LF MU, Brno
2Institut biostatistiky a analýz MU, Brno
oludka@yahoo.com
Sources
1. McCullough PA, Philbin EF, Spertus JA et al. Resource Utilization Among Congestive Heart Failure (REACH) Study. Confirmation of a heart failure epidemic: findings from the Resource Utilization Among Congestive Heart Failure (REACH) study. J Am Coll Cardiol 2002; 39 : 60–69.
2. Remme WJ, Swedberg K. The task force for the diagnosis and treatment of chronic heart failure. European Society of Cardiology. Guidelines for the diagnosis and treatment of chronic heart failure. Eur Heart J 2001; 22 : 1527–1560.
3. Rich MW. Epidemiology, pathophysiology, and etiology of congestive heart failure in older adults. J Am Geriatr Soc 1997; 45 : 968–974.
4. McMurray J, McDonagh T, Morrison CE et al. Trends in hospitalization for heart failure in Scotland 1980–1990. Eur Heart J 1993; 14 : 1158–1162.
5. Cowie MR, Mosterd A, Wood DA et al. The epidemiology of heart failure. Eur Heart J 1997; 18 : 208–225.
6. Fonarow GC, Adams KF Jr, Abraham WT et al. ADHERE Scientific Advisory Committee, Study Group, and Investigators. Risk stratification for in-hospital mortality in acutely decompensated heart failure: classification and regression tree analysis. JAMA 2005; 293 : 572–580.
7. Zannad F, Mebazaa A, Juillière Y et al. EFICA Investigators. Clinical profile, contemporary management and one-year mortality in patients with severe acute heart failure syndromes: The EFICA study. Eur J Heart Fail 2006; 8 : 697–705.
8. Ho KK, Pinsky JL, Kannel WB et al. The epidemiology of heart failure: the Framingham study. J Am Coll Cardiol 1993; 22A: 6A–13A.
9. Berry C, Murdoch DR, McMurray JJ. Economics of chronic heart failure. Eur J Heart Fail 2001; 3 : 283–291.
10. MacIntyre K, Capewell S, Stewart S et al. Evidence of improving prognosis in heart failure: trends in case fatality in 66,547 patients hospitalized between 1986 and 1995. Circulation 2000; 102: 1126–1131.
11. Murdoch DR, Love MP, Robb SD et al. Importance of heart failure as a cause of death. Changing contribution to overall mortality and coronary heart disease mortality in Scotland 1979–1992. Eur Heart J 1998; 19: 1829–1835.
12. Levy D, Kenchaiah S, Larson MG et al. Long-term trends in the incidence of and survival with heart failure. N Engl J Med 2002; 347 : 1397–1402.
13. Ho KK, Pinsky JL, Kannel WB et al. The epidemiology of heart failure: the Framingham study. J Am Coll Cardiol 1993; 22A: 6A–13A.
14. Garg R, Yusuf S. Overview of randomized trials of angiotensin-converting enzyme inhibitors on mortality and morbidity in patients with heart failure. Collaborative Group on ACE Inhibitor Trials. JAMA 1995; 273 : 1450–1456.
15. McMurray JJ. Major beta blocker mortality trials in chronic heart failure: a critical review. Heart 1999; 82: IV14–IV22.
16. The CONSENSUS Trial Study Group. Effects of enalapril on mortality in severe congestive heart failure. Results of the cooperative North Scandinavian Enalapril Survival Study (CONSENSUS). N Engl J Med 1987; 316 : 1429–1435.
17. The SOLVD Investigators. Effects of enalapril on survival in patients with reduced left ventricular ejection fractions and congestive heart failure. N Engl J Med 1991; 325 : 293–302.
18. Yusuf S, Pitt B. A lifetime of prevention: the case of heart failure. Circulation 2002; 106 : 2997–2998.
19. Cleland JG, Cohen-Solal A, Aguilar JC et al. IMPROVEMENT of Heart Failure Programme Committees and Investigators. Improvement programme in evaluation and management; Study Group on Diagnosis of the Working Group on Heart Failure of The European Society of Cardiology. Management of heart failure in primary care (the IMPROVEMENT of Heart Failure Programme): an international survey. Lancet 2002; 360 : 1631–1639.
20. A comparison of antiarrhythmic-drug therapy with implantable defibrillators in patients resuscitated from near-fatal ventricular arrhytmias. The Antiarrhythmics versus Implantable Defibrillators (AVID) Invesigators. N Engl J Med 1997; 337 : 1576–1583.
21. CASH Investigators. Siebels J, Cappato R, Rüppel R et al. Preliminary results of the Cardiac Arrest Study Hamburg (CASH). Am J Cardiol 1993; 72: 109F–113F.
22. Buxton AE, Lee KL, Fisher JD et al. A randomized study of prevention of sudden death in patients with coronary artery disease: Multicenter Unsustained Tachycardia Trial Investigators. N Engl J Med 1999; 341 : 1882–1890.
23. Connolly SJ, Gent M, Roberts RS et al. Canadian implantable defibrillator study (CIDS): a randomized trial of the implantable cardioverter defibrillator against amiodarone. Circulation 2000; 101 : 1297–1302.
24. Moss AJ, Hall WJ, Cannom DS et al. Improved survival with an implanted defibrillator in patients with coronary disease at high risk for ventricular arrhytmia. Multicenter Automatic Defibrillator Implantation Trial Investigators. N Engl J Med 1996; 335 : 1933–1940.
25. Moss AJ, Zareba W, Hall WJ et al. Multicenter Automatic Defibrillator Implantation Trial II. Prophylactic implantation of a defibrillator in patients with myocardial infarction and reduced ejection fraction. N Engl J Med 2002; 346 : 877–883.
26. Bardy GH, Lee KL, Mark DB et al. Sudden Cardiac Death in Heart Failure Trial (SCD-HeFT) Investigators. Amiodarone or an implantable cardioverter-defibrilator for congestive heart failure. N Engl J Med 2005; 352 : 225–237.
27. Cazeau S, Ritter P, Bakdach S. Four chamber pacing in dilated cardiomyopathy. Pacing Clin Electrophysiol 1994; 17 : 1974–1979.
28. Bristow MR, Saxon LA, Boehmer J et al. Comparison of Medical Therapy, Pacing, and Defibrillation in Heart Failure (COMPANION) Investigators. Cardiac--resynchronization therapy with or without an implantable defibrillator in advanced chronic heart failure. N Engl J Med 2004; 350 : 2140–2150.
29. Cleland JGF, Daubert JC, Erdmann E et al. Cardiac Resynchronization-Heart Failure (CARE-HF) Study Investigators. The effect of cardiac resynchronization on morbidity and mortality in heart failure. N Engl J Med 2005; 352 : 1539–1549.
30. Moss AJ, Hall WJ, Cannom DS et al. MADIT-CRT Trial Investigators. Cardiac-resynchronization therapy for the prevention of heart-failure events. N Engl J Med 2009; 361 : 1329–1338.
Labels
Paediatric cardiology Internal medicine Cardiac surgery Cardiology
Article was published inCardiology Review

2011 Issue 1-
All articles in this issue
- Medikamentózní léčba plicní arteriální hypertenze v roce 2011
- Osud nemocných na čekací listině transplantace srdce
- Postavení TOR inhibitorů po transplantaci srdce
- Index kompatibility: Má své místo u pacientů po transplantaci srdce?
- Mechanické podporné systémy v liečbe srdcového zlyhávania
- Nové poznatky v antiagregační léčbě na ESC 2010
- Latentní obstrukce ve výtokovém traktu levé komory srdeční u pacienta s hypertrofickou kardiomyopatií
- Léčba hypertenze u obezity
- Fixní kombinace u arteriální hypertenze
- Ledviny a akutní koronární syndrom
- Kardiogenní šok
- Jaký význam má modulace srdeční frekvence u nemocných se srdečním selháním
- Je prognóza nemocných s chronickým srdečním selháním stále tak špatná?
- Cardiology Review
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Kardiogenní šok
- Je prognóza nemocných s chronickým srdečním selháním stále tak špatná?
- Mechanické podporné systémy v liečbe srdcového zlyhávania
- Latentní obstrukce ve výtokovém traktu levé komory srdeční u pacienta s hypertrofickou kardiomyopatií
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career



