-
Medical journals
- Career
Rehabilitace po infarktu myokardu
: V. Chaloupka; L. Elbl
: Kardiol Rev Int Med 2005, 7(1): 5-9
Rehabilitace představuje nedílnou součást komplexní léčby nemocných po infarktu myokardu. Pracoviště autorů se touto problematikou cíleně zabývá již více než 10 let. V práci se zaměřují na některé důležité aspekty rehabilitace nemocných po infarktu myokardu a revaskularizačních operacích, především na prognostický význam tolerance zátěže, na efekt rehabilitace u starších nemocných, na problematiku stanovení adekvátní zátěže u nemocných, kteří jsou léčeni betablokátory, a na vliv kombinovaného tréninku na remodelaci levé komory srdeční.
Klíčová slova:
infarkt myokardu – rehabilitace – tepová frekvence – tolerance zátěže – vliv betablokátorů – remodelace levé komoryÚvod
V poslední době se věnuje kardiovaskulární rehabilitaci zvýšená pozornost. Evropská kardiologická společnost vyvíjí řadu aktivit proto, aby se význam rehabilitace u nemocných s kardiovaskulárními onemocněními dostal do povědomí široké kardiologické veřejnosti a aby byla odborně řízená rehabilitace v praxi realizována jako nezbytná součást léčby našich nemocných. Naše pracoviště se problematice kardiovaskulární rehabilitace cíleně věnuje již řadu let. V poslední době jsme publikovali několik prací jak obecného charakteru, tak původní sdělení, která vznikla na podkladě více než 10leté zkušenosti [1,2,3,4]. Na stránkách Kardiologické revue vyšla nedávno práce týkající se pohybové aktivity u nemocných s kardiovaskulárním onemocněním [5]. Proto bychom v tomto sdělení rádi upozornili pouze na některé zajímavé a důležité skutečnosti týkající se rehabilitace nemocných po infarktu myokardu (IM).
Prognostický význam tolerance zátěže
Tělesná inaktivita představuje závažný rizikový faktor ischemické choroby srdeční (ICHS). Zvyšující se úroveň fyzické aktivity je v nepřímém vztahu s dlouhodobou kardiovaskulární mortalitou [6,7]. Metaanalýza 10 randomizovaných studií zjišťující efekt rehabilitace u nemocných po infarktu myokardu uvádí 24% snížení celkové mortality a 25% snížení kardiovaskulární mortality u rehabilitovaných nemocných ve srovnání s kontrolní skupinou [8].
V literatuře jsou dostupné 2 metaanalýzy, které se zabývaly prognostickými informacemi zátěžových testů jak v pretrombolytickém, tak potrombolytickém období.
Jedinými významnými předpovědními ukazateli mortality byly abnormální reakce systolického krevního tlaku a nízká tolerance zátěže. Prognostická hodnota depresí ST segmentu se ukázala pouze u nemocných s dolním a zadním infarktem myokardu [9].
Druhá studie zahrnuje 15 613 nemocných, z nichž 65 % mělo trombolytickou léčbu. Všechny testy byly provedeny do 6 týdnů od infarktu myokardu (IM), v průměru 2. týden. Předpovědní hodnotu pro výskyt smrti nebo reinfarktu měly deprese ST, stenokardie, abnormní odpověď systolického krevního tlaku a omezené trvání zátěže. Opět hlavně abnormní reakce krevního tlaku a nízká tolerance zátěže měly předpovědní hodnotu srdeční smrti [10].
19leté přežití nemocných po IM sledovali Dominguez et al a analyzovali prognostické ukazatele [11]. Jednalo se o nemocné, kteří byli vyšetřeni v období let 1979–1983, kdy nebyla trombolytická léčba, ani se nepoužívala léčba kyselinou acetylsalicylovou nebo betablokátory. Žádný z těchto nemocných nebyl indikován ke koronarografii během hospitalizace a pouze 54 nemocných z celkového počtu 1 773 nemocných mělo ve sledovaném období provedenou chirurgickou revaskularizaci. Autoři prováděli 2.–4. týden hospitalizace symptomy limitovaný zátěžový test. Když srovnali skupinu nemocných, u které byl proveden zátěžový test se skupinou, u které proveden nebyl, žilo po 10 letech v testované skupině 71 % nemocných, zatímco v netestované pouze 31 % nemocných. Po 18 letech byl rozdíl 15,1 % ku 4,6 %. Mortalita v testované skupině byla tedy podstatně nižší než ve skupině nemocných, u kterých z různých důvodů nebyl test proveden (klinický stav, ischemická choroba DK, artritida, plicní onemocnění, atd). Samozřejmě se nabízí otázka, proč jsou tito nemocní tak rizikoví. Jistě jsou mezi nimi nemocní s těžkou dysfunkcí levé komory srdeční. Víme však také, že inaktivita patří mezi hlavní rizikové faktory ICHS. Dá se předpokládat, že různá omezení (artritida, plicní onemocnění, atd) předurčují nemocného k inaktivnímu způsobu života.
Je zajímavé, že ukazatele ischemie myokardu opět neměly větší předpovědní hodnotu. Přítomnost deprese ST > 1 mm nebyla v této studii spojena s vyšší mortalitou. Při další analýze deprese > 2 mm lehce zhoršovaly prognózu. Jako nejlepší prognostický ukazatel se opět projevila zátěžová tolerance v průběhu testu. Každé zvýšení zátěžové tolerance o 1 MET představovalo snížení rizika smrti o 15 %. Tolerance zátěže je v poslední době stále častěji zdůrazňovaná jako velmi důležitý prognostický ukazatel [12,13].
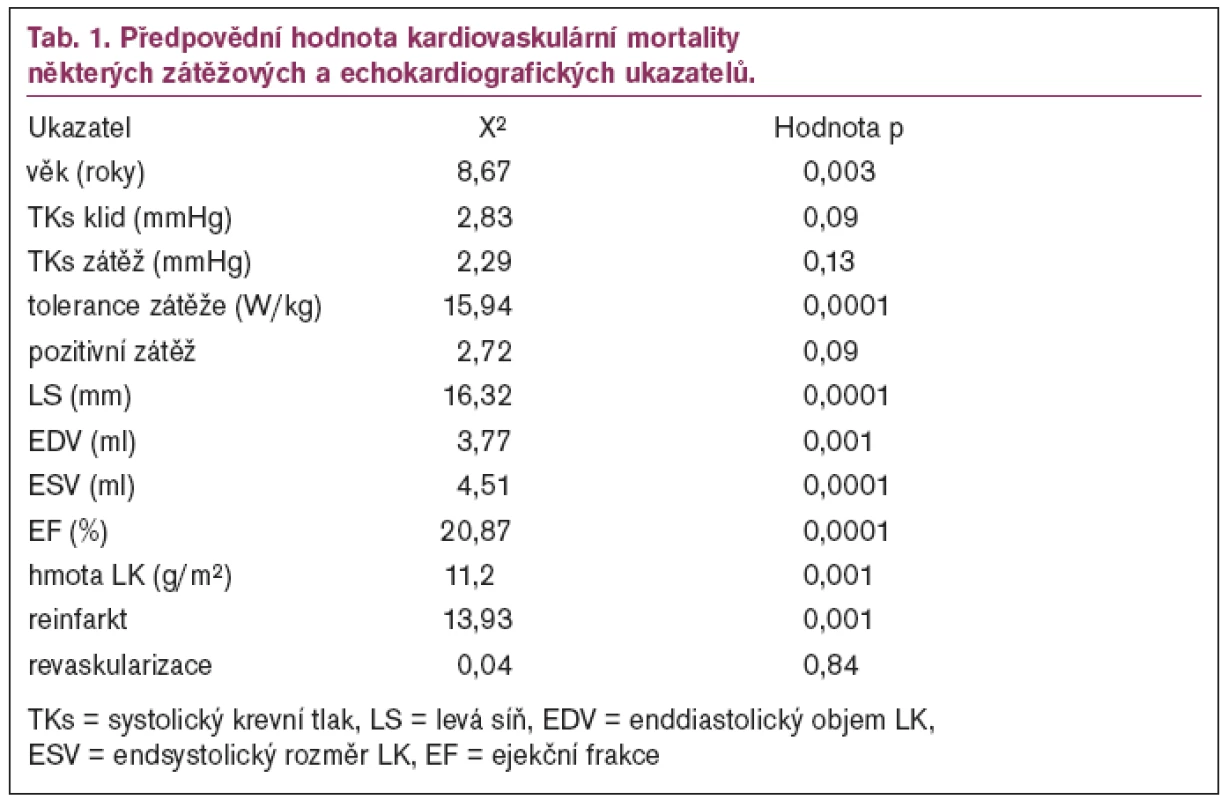
Na našem pracovišti zařazujeme do 2měsíčního rehabilitačního programu nemocné po IM a revaskularizaci. Nedávno jsme publikovali retrospektivní studii na souboru 582 nemocných, kteří absolvovali tento program v letech 1993–2002 [3]. U nemocných jsme před zařazením do rehabilitace a na závěr prováděli zátěžovou echokardiografii. V našem souboru došlo k významnému zlepšení tolerance zátěže během rehabilitace. Průměrné hodnoty celého souboru byly 1,5 ± 0,3 W/kg před rehabilitací a 1,7 ± 0,4 W/kg po rehabilitaci. Tolerance zátěže měla podobnějako v jiných pracích velmi dobroupředpovědní hodnotu kardiovaskulární mortality. V našem souboru měly silnou předpovědní hodnotu kardiovaskulární mortality také některé funkční a morfologické ukazatele levé komory srdeční, především ejekční frakce (tab. 1). Je zajímavé, že stejně jako v řadě jiných prací neměly ukazatele ischemie předpovědní hodnotu kardiovaskulárního úmrtí , v našem případě pozitivita zátěžového testu a stenokardie na konci rehabilitace.
Rehabilitace po IM u starších nemocných
Populace v naší zemi, podobně jako v ostatních zemích západní Evropy, progresivně stárne. Odhaduje se, že podíl osob starších 65 let se v roce 2030 oproti roku 2000 zdvojnásobí [14]. U starších osob je prevalence ICHS vysoká a je hlavní příčinou kardiovaskulární úmrtnosti. U starších osob, které mají často různá omezení fyzického zatěžování, jsou k dispozici pouze omezené údaje o prognostické hodnotě zátěžových ukazatelů [15]. Na druhé straně však některé práce ukázaly, že starší nemocní s ICHS mají schopnost zlepšit svoji trénovanost podobně jako mladší nemocní. Otázka, zda rehabilitace vede u starších nemocných ke zlepšení tolerance zátěže stejně jako u mladších nemocných a zda zlepší jejich prognózu, je samozřejmě velmi aktuální.
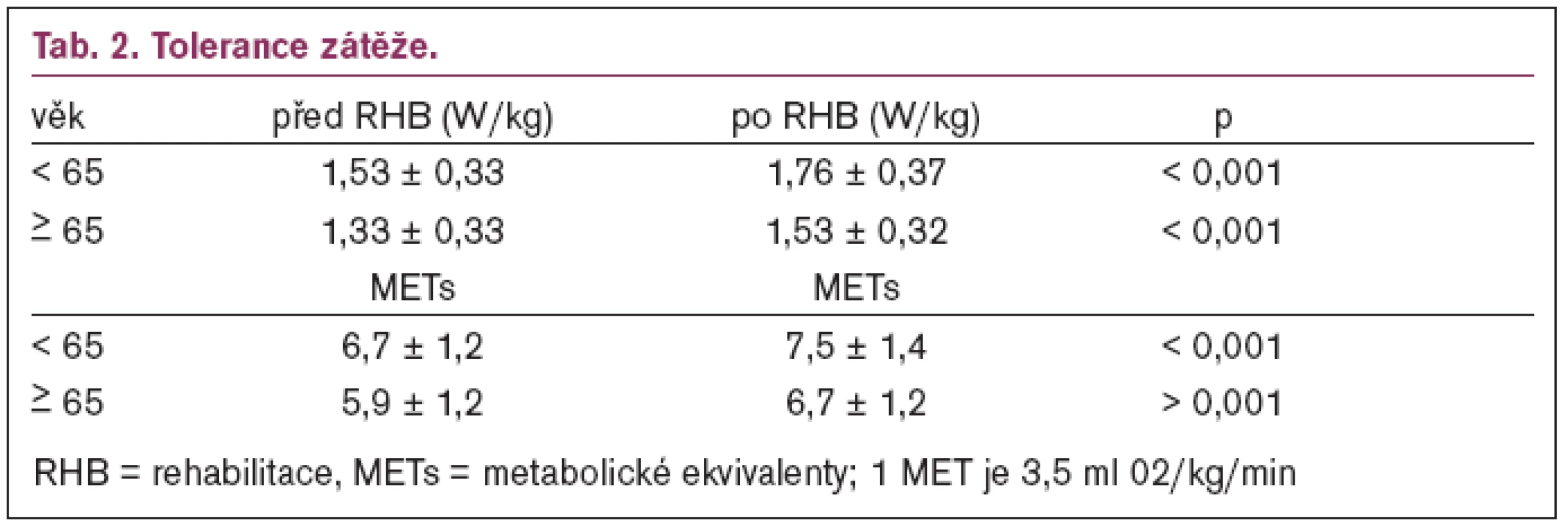
Tab. 2 ukazuje rozdíly v toleranci zátěže u mladších a starších nemocných. V našem souboru tvoří nemocní starší 65 let 25 %. Logicky se toto procento bude progresivně zvyšovat stejně jako v jiných vyspělých zemích západní Evropy a ve Spojených státech [15]. Vidíme, že hodnoty tolerance zátěže před i po rehabilitaci jsou u starších nemocných nižší, ale v obou skupinách představuje zlepšení tolerance zátěže 15 %.
V čem se lišila naše skupina starších nemocných od skupiny mladších? Věkový rozdíl byl v průměru 17 let. Starší nemocní měli vyšší klidovou hodnotu systolického krevního tlaku, vyšší hmotu LK a velikost levé síně, což je v souhlase se známými změnami kardiovaskulárního aparátu. Překvapivá není ani nižší tolerance zátěže. Za důležité pokládáme zjištění, žetolerance zátěže se zlepšuje i u starších nemocných.
Vliv betablokátorů na rehabilitaci nemocných po infarktu myokardu
Léčba nemocných s infarktem myokardu se v posledních letech výrazně změnila. Týká se to jak invazivního přístupu, tak racionální farmakoterapie. Součástí racionální farmakoterapie nemocných po IM je léčba betablokátory, kterými jsou léčeni až na výjimky všichni nemocní v rámci sekundární prevence [16,17].
Betablokátory mají známý hemodynamický účinek, který se projevuje především snížením krevního tlaku a nižší tepovou frekvencí v klidu i při zátěži. U nemocných s anginou pectoris nebo zátěží provokovanou ischemií toleranci zátěže zlepšují, u zdravých a nemocných bez ischemie toleranci zátěže snižují [18].
Při zařazení nemocného do rehabilitačního programu je vedle způsobu, frekvence a trvání cvičení nutné stanovit i vhodnou intenzitu zátěže. Nejsou jednotné názory na to, zda déletrvající zátěž nižší intenzity je srovnatelná s cvičením intenzivnějším. Je pravděpodobné, že zátěž vyšší intenzity přináší nemocným větší prognostický efekt [19,20]. Intenzita zátěže se má blížit anaerobnímu prahu (AP), ale neměla by ho překračovat [21]. Stanovení vhodné tréninkové intenzity má zásadní význam pro úspěšné zvládnutí jak řízených rehabilitačních programů, tak individuální pohybové aktivity. Na jedné straně se snažíme dosáhnout optimálního tréninkového efektu, tj. zlepšení tolerance zátěže, a na druhé straně musíme mít na mysli bezpečnost nemocného a také jeho pozitivní motivaci pro individuální cvičení. Ne každý nemocný je schopen akceptovat intenzivní fyzický trénink.
Tradičně se vychází z relativně lineárního vztahu mezi spotřebou kyslíku a tepovou frekvencí a stanovuje se tréninková tepová frekvence (TTF). Intenzita tréninku se nejčastěji určuje jako procento maximální dosažené frekvence (např. 70 %TF max), nebo jako procento tepové rezervy: TTF = (TF max – TF klid) x (0,6–0,8) ± TF klid.
Zajímalo nás, zda je možné u nemocných po IM léčených betablokátory stanovit tréninkovou intenzitu podle tepové frekvence a jaké jsou vhodné alternativní možnosti stanovení tréninkové intenzity. Na souboru 112 mužů jsme spiroergometricky hodnotili toleranci zátěže ve watech na kg, maximální tepovou frekvenci, tepovou frekvenci na úrovni AP, vrcholovou spotřebu kyslíku, spotřebu kyslíku na úrovni AP, toleranci zátěže na úrovni AP, procenta vrcholové spotřeby kyslíku při AP a procenta maximální tepové frekvence při AP [22].
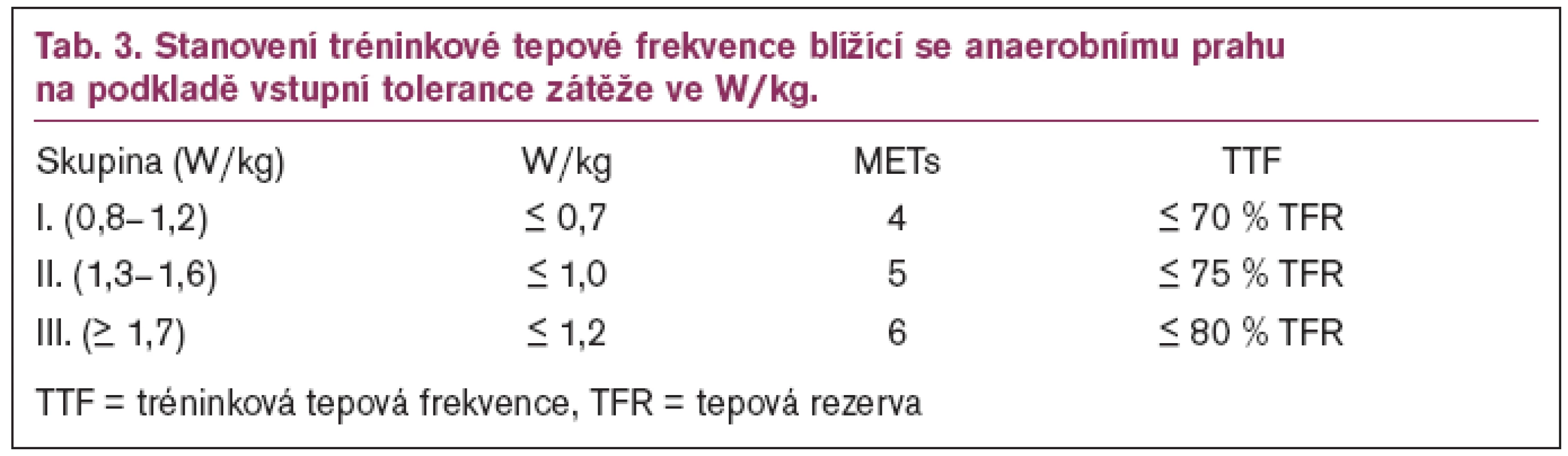
Maximální tepová frekvence při zátěži byla 120 ± 17 tepů/min. Průměrná tepová frekvence při AP byla 104,7 ± 13,3 tepů/min a odpovídala 81,0 ± 8 % vrcholové spotřeby kyslíku a 87,9 ± 5,6 % vrcholové TF. Zjistili jsme těsnou korelaci mezi tepovou frekvencí při AP a hodnotami výpočtů podle tepové rezervy. Zjistili jsme, že intenzita zátěže při AP se poměrně úzce pohybuje kolem hodnoty 1 W/kg. Navrhli jsme výpočet tréninkové intenzity na úrovni AP s přihlédnutím k toleranci zátěže. Uvádíme jak hodnoty pro výpočet TTF podle tepové rezervy, tak i zátěže ve watech/kg a spotřeby kyslíku přepočtené na metabolické ekvivalenty (tab. 3).
Domníváme se, že pro výpočet tréninkové tepové frekvence lze i u nemocných po IM léčených betablokátory použít vzorce odvozené od maximální tepové frekvence nebo tepové rezervy. Jako pomocný ukazatel je použitelná i intenzita zátěže vyjádřená ve W/kg.
Vliv rehabilitace na remodelacilevé komory
Remodelace LK je proces, který odráží řadu patofyziologických mechanizmů. Jednou z nejčastějších příčin je ztráta viabilního myokardu na podkladě srdečního infarktu. Ztráta kontrakční schopnosti určité části myokardu vede ke změně velikosti a tvaru LK za účelem udržení dostatečného tepového objemu komory.
Jedním z faktorů určujících prognózu nemocných po akutním srdečním infarktu je právě funkce LK. Strukturální a funkční změny vedoucí k dilataci komory mají úzký vztah k morbiditě a mortalitě pacientů po srdečním infarktu [23]. Objemy LK jsou významným prediktorem přežívání nemocných po akutním srdečním infarktu. Konečně systolický a diastolický objem je v nepřímém vztahu k přežívání pacientů [24]. Remodelace LK po infarktu je lepším prediktorem pozdní mortality než např. snížená EF, Killipova klasifikace, diabetes, přítomná angina pectoris a dřívější srdeční infarkt v anamnéze [23].
Některé experimentální a klinické práce poukázaly na možnost negativního vlivu aerobní zátěže na zhoršení remodelace LK [25,26]. Nejčastěji citovanou prací zabývající se tímto problémem je práce autorů Jugdutta et al, kteří prokázali u nemocných po předním Q–infarktu negativní vliv tréninku na remodelaci LK [27]. Další práce neprokázaly negativní vliv cvičení na proces remodelace LK. Antiremodelační efekt dlouhodobého aerobního cvičení byl popsán ve studii ELVD–CHF u nemocných s chronickým srdečním selháním po srdečním infarktu [28]. Další studie, které se soustředily na nemocné po IM se sníženou EF, neprokázaly antiremodelační vliv aerobního tréninku na LK [29,30].
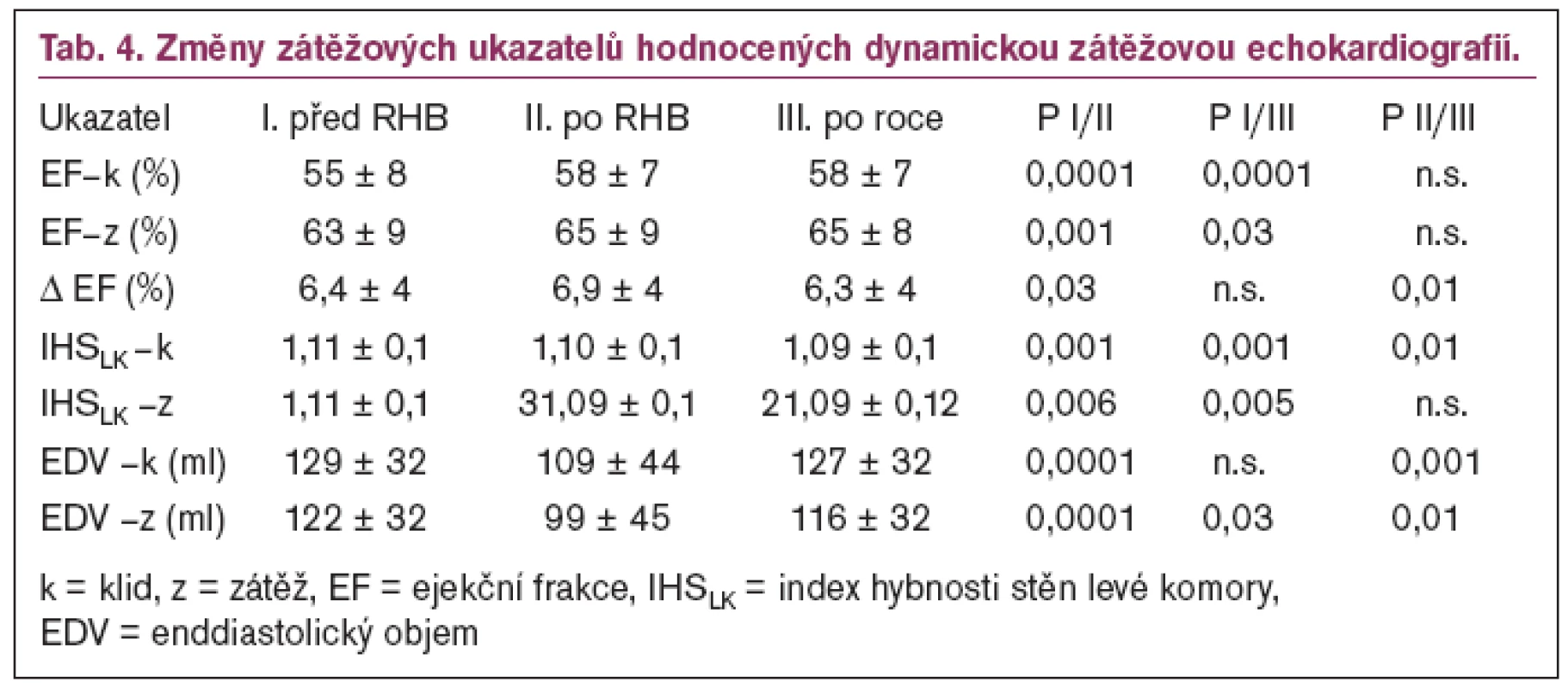
Zaměřili jsme se na prospektivní jednoroční sledování a vyhodnocení procesu remodelace levé komory srdeční u 184 nemocných (21 žen, 163 mužů) s prvním akutním IM, kteří absolvovali časný ambulantní 8týdenní rehabilitační program. Změny zátěžových ukazatelů hodnocených dynamickou zátěžovou echokardiografií po rehabilitaci a po roce ukazuje tab. 4.
Výsledky naší práce ukazují, že kombinace aerobního tréninku na úrovni 60–80 % vrcholového příjmu kyslíku se silovým cvičením na úrovni 50 % 1–RM u nemocných po akutním srdečním infarktu nevede ke zhoršení procesu remodelace LK. Došlo k příznivému ovlivnění ejekční frakce, snížení hodnot ukazatele segmentární poruchy kinetiky IHSLK a k poklesu konečně diastolického objemu LK v tomto období [31].
doc. MUDr. Václav Chaloupka, CSc.
MUDr. Lubomír Elbl, CSc.
Oddělení funkčního vyšetřování
FN Brno Bohunice
doc. MUDr. Václav Chaloupka, CSc.
Po promoci na LF UJEP (nyní MU) v Brně v roce 1971 nastoupil na interní oddělení nemocnice v Jihlavě. Po 2 letech se vrátil do Brna, na I. interní kliniku FNsP U sv. Anny, kde se začal věnovat kardiologii. Po ročním pobytu v zahraničí přechází v roce 1981 do bohunické nemocnice na oddělení funkčního vyšetřování, kde se intenzivně věnuje echokardiografii. Od roku 1993 je přednostou oddělení. Tématem jeho kandidátské disertační práce byla diagnostika ICHS (Isometrická zátěž v diagnostice ICHS), stejně jako později habilitační práce (Zátěžová echokardiografie u nemocných po infarktu myokardu). Hlavním odborným zájmem je vedle echokardiografie také sekundární prevence a rehabilitace nemocných po infarktu myokardu. Je autorem či spoluautorem několika desítek knižních publikací, např. Základy funkčního vyšetřování srdce a krevního oběhu, Klinická echokardiografie, Zátěžová echokardiografie, Zátěžové metody v kardiologii, Epidemiologie ischemické choroby srdeční. Je členem pracovní skupiny pro echokardiografii a pracovní skupiny pro kardiovaskulární rehabilitaci, pracovní skupiny pro echokardiografii Evropské kardiologické společnosti. Je zástupcem ČKS v U.E.M.S.
Sources
1. Nehyba S, Chaloupka V, Elbl L. Rehabilitační péče o nemocné po prodělaném srdečním infarktu. Prakt Lék 1995; 75 : 272–273.
2. Chaloupka V, Elbl L, Nehyba S. Silový trénink u nemocných po infarktu myokardu. Vnitř Lék 2000; 46 : 829–834.
3. Chaloupka V, Elbl L, Nehyba S, Tomášková I. Vliv rehabilitačního programu na prognózu nemocných po infarktu myokardu. Cor Vasa 2004; 46 : 29–35.
4. Chaloupka V. Rehabilitace nemocných po infarktu myokardu. Inter Med Prax 2004; 2 : 74–78.
5. Chaloupka V, Elbl L, Nehyba S, Tomášková I. Pohybová aktivita u nemocných s kardiovaskulárním onemocněním. Kardiol Rev 2003; 1 : 16–20.
6. Paffenberger RS, Hyde RT, Wing A, Hsieh C. Physical activity, all–cause mortality, and longevity of college alumni. N Engl J Med 1986; 314 : 605–613.
7. Manson JE, Stampfer MJ, Wilett WC et al. Physical activity and incidence of coronary heart disease and stroke in women. Circulation 1995; 9 : 927–932.
8. Oldridge NB, Guyatt GH, Fischer ME, Rimm AA. Cardiac rehabilitation after myocardial infarction. Combined experience of randomized clinical trials. JAMA 1988; 260 : 945–950.
9. Froelicher VF, Perdue S, Pewen W et al. Application of meta–analysis using an electronic spread sheet to exercise testing in patients after myocardial infarction. Am J Med 1987; 83 : 1045–1053.
10. Show LJ, Peterson ED, Kesler K et al. A metaanalysis of predischarge risk stratification after acute myocardial infarction with stress electrocardiographic, myocardial perfusion, and ventricular function imaging. Am J Cardiol 1996; 78 : 1327–1333.
11. Domíngues H, Torp–Pedersen C, Koeber L, Ras–Madsen C. Prognostic value of exercise testing in cohort of patients followed for 15 years after acute myocardial infarction. Eur Hear J 2001; 22 : 300–306.
12. Lee CW, Wu YT, Lai CP et al. Factors influencing the long–term effects of supervised cardiac rehabilitation on the exercise capacity of patients with acute myocardial infarction. J Formos Med Assoc 2002; 101 : 60–67.
13. Ghayoumi A, Raxwal V, Cho S et al. Prognostic Value of Exercise Tests in Male Veterans With Chronic Coronary Artery Disease. J Cardiopulm Rehab 2002; 22 : 399–407.
14. Ambler Z. Neurologické i obecně medicínské poruchy ve stáří. PM 2003; 4 : 367–373.
15. Arruda AM, Das MK, Roger VL et al. Prognostic Value of Exercise Echocardiography in 2 632 Patients > 65 Years of Age. J Am Coll Cardiol 2002; 37 : 1036–1041.
16. Van de Werf F, Ardissino D, Betriu A et al. Management of acute myocardial infarction in patients presenting with ST–segment elevation. The Task Force on the Management of Acute Myocardial Infarction of the European Society of Cardiology. Eur Heart J 2003; 24 : 28–66.
17. Niederle P, Staněk V. Zásady péče o nemocné s chronickými formami ischemické choroba srdeční. Cor Vasa 1998; 15 : 1300–1331.
18. Gordon NF, Duncan JJ. Effect of beta–blockers on exercise physiology: implications for exercise training. Med Sci Sports Exerc 1991; 23 : 668–676.
19. Fleg JL, Pina IL, Balady GJ et al. Assessment of Functional Capacity in Clinical and Research Applications. Circulation 2000; 102 : 1591–1607.
20. Jensen BE, Fletcher BJ, Rupp JE et al. Effect of high and low intensity exercise on ventilatory threshold in men with coronary artery disease. J Cardiopulmonary Rehabil 1996; 16 : 227–232.
21. Mahler DA, Franco MJ. Clinical Applications of Cardiopulmonary Exercise Testing. J Cardiopulmonary Rehabil 1996; 16 : 357–365.
22. Chaloupka V, Elbl L, Nehyba S et al. Stanovení intenzity tréninku u nemocných po infarktu myokardu léčených betablokátory. Cor Vasa 2005; 47 (v tisku).
23. de Kam PJ, Nicolosi GL, Voors AA et al. Prediction of 6 months left ventricular dilatation after myocardial infarction in relation to cardiac morbidity and mortality. Eur Heart J 2002; 23 : 536–542.
24. White HD, Norris RM, Brown MA et al. Left ventricular end–systolic volume as the major determinant of survival after recovery from myocardial infarction. Circulation 1987; 76 : 44–51.
25. Gaudron P, Hu K, Schamberger R et al. Effect of endurance training early or late after coronary artery occlusion on left ventricular remodeling, hemodynamics, and survival in rats with chronic transmural myocardial infarction. Circulation 1994; 89 : 402–412.
26. Oh BH, Ono S, Gilpin E et al. Altered left ventricular remodeling with beta–adrenergic blockade and exercise after coronary reperfusion in rats. Circulation 1993; 87 : 608–616.
27. Jugdutt BI, Michorowski BL, Kappagoda CT et al. Exercise training after Q wave myocardial infarction: Importance of regional ventricular function and topography. J Am Coll Cardiol 1988; 12 : 362–372.
28. Giannuzi P, Temporelli PL, Corra U et al. Antiremodeling effect of long–term exercise training in patients with stable chronic heart failure. Results of the Exercise in Left Ventricular Dysfunction and Chronic Heart Failure (ELVD–CHF) Trial. Circulation 2003; 108 : 554–559.
29. Otsuka Y, Takaki H, Okano Y et al. Exercise training without ventricular remodeling in patients with moderate to severe left ventricular dysfunction early after acute myocardial infarction. Int J Cardiol 2003; 87 : 237–244.
30. Karlsdottir AE, Foster C, Porcari JP et al. Hemodynamic Responses During Aerobic and Resistance Exercise. J Cardiopulmonary Rehab 2002; 22 : 170–177.
31. Elbl L, Chaloupka V, Tomášková I et al. Vliv kombinovaného aerobního a silového tréninku na funkci levé komory srdeční u nemocných po akutním infarktu myokardu. Vnitř Lék 2005; 51(2): 190–197.
Labels
Paediatric cardiology Internal medicine Cardiac surgery Cardiology
Article was published inCardiology Review

2005 Issue 1-
All articles in this issue
- Antialdosteronics renaissance in the contemporary cardiology
- Practical aspects and news in pharmacological treatment of arrhythmias
- Trimetazidine in the treatment of angina pectoris and other forms of IHD
- Rehabilitation after myocardial infarction
- Heart infarction and weather changes – further possible correlations
- Cardiology Review
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Trimetazidine in the treatment of angina pectoris and other forms of IHD
- Practical aspects and news in pharmacological treatment of arrhythmias
- Rehabilitation after myocardial infarction
- Antialdosteronics renaissance in the contemporary cardiology
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career