-
Medical journals
- Career
Vliv alirokumabu na kardiovaskulární příhody: Co ukázala studie ODYSSEY OUTCOMES?
Authors: Petr Ošťádal
Authors‘ workplace: Komplexní kardiovaskulární centrum, Nemocnice Na Homolce, Praha
Published in: AtheroRev 2019; 4(1): 53-60
Category: clinical studies
Overview
U nemocných, kteří prodělali akutní koronární syndrom (AKS), zůstává vysoké riziko další kardiovaskulární (KV) příhody i při využití všech opatření v rámci sekundární prevence. Studie ODYSSEY OUTCOMES testovala účinky inhibitoru proprotein konvertázy subtilizin kexin 9 (PCSK9) u pacientů po AKS, u nichž zůstávaly vyšší hodnoty cholesterolu i přes intenzivní statinovou léčbu (LDL-cholesterol/LDL-C > 1,8 mmol/l). Do studie bylo zařazeno 18 924 jedinců, kteří byli randomizováni k léčbě alirokumabem nebo dostávali placebo. Dávka alirokumabu byla zaslepeně upravována s cílem dosáhnout hodnoty LDL-C 0,6–1,3 mmol/l. Střední doba sledování byla 2,8 roku. Alirokumab významně snížil riziko další KV-příhody (primární složený cílový ukazatel: úmrtí pro ICHS, nefatální infarkt myokardu, ischemická cévní mozková příhoda, nestabilní angina pectoris) relativně o 15 %. Léčba alirokumabem byla spojena i s nižší celkovou mortalitou. Alirokumab snižoval nejen riziko první KV-příhody, ale i příhod následných. Účinky alirokumabu byly nejvýraznější v podskupinách s vyšší vstupní hodnotou LDL-C (> 2,6 mmol/l) a u nemocných, léčených alirokumabem déle než 3 roky. Léčba alirokumabem byla bezpečná, pouze ve srovnání s placebem byla lokální reakce v místě vpichu častějším nežádoucím účinkem po alirokumabu. Alirokumab po přidání k intenzivní statinové léčbě u nemocných s AKS významně snižoval riziko další KV-příhody a léčba alirokumabem byla spojena i s nižší celkovou mortalitou.
Klíčová slova:
akutní infarkt myokardu – alirokumab – mortalita – nestabilní angina pectoris
Úvod
Přes všechny pokroky současné medicíny, nemocní, kteří prodělali akutní koronární syndrom (AKS), zůstávají ve vysokém riziku další ischemické kardiovaskulární (KV) příhody. Toto reziduální riziko závisí mimo jiné na hodnotách LDL-cholesterolu (LDL-C) a dalších lipidových parametrů. Dřívější klinické studie ukázaly, že riziko se sníží přidáním intenzivní statinové léčby, a to jak ve srovnání s placebem, tak ve srovnání s nižší dávkou statinu. Navíc současná evidence naznačuje, že čím nižší hladiny LDL-C s pomocí statinu dosáhneme, tím lepší bude prognóza. K dispozici jsou i údaje pro ezetimib, který dále o trochu snižuje riziko kardiovaskulární příhody po přidání ke statinu; účinky ezetimibu však nebyly nikdy ve velké studii testovány po přidání k intenzivní statinové léčbě.
Proprotein konvertáza subtilizin kexin typ 9 (PCSK9) je molekula, která se významně podílí na degradaci LDL-receptorů. Studie ukázaly, že mutace, které vedou ke ztrátě funkce PCSK9, způsobují výrazný pokles hodnot LDL-C a mohou snižovat riziko ischemické choroby srdeční (ICHS). Tato pozorování vedla k vývoji klinicky použitelných monoklonálních protilátek proti PCSK9, jejichž podání je spojeno s výrazným snížením LDL-C; jedním z těchto nově vyvinutých PCSK9 inhibitorů je také alirokumab.
Studie ODYSSEY OUTCOMES testovala hypotézu, že léčba inhibitorem PCSK9 alirokumabem povede ke snížení rizika další ischemické KV-příhody u nemocných po AKS, jejichž hladina aterogenních lipoproteinů zůstává zvýšená i přes intenzivní nebo maximální tolerovanou dávku statinu [1,2].
Design studie ODYSSEY OUTCOMES
Jednalo se o multicentrickou, randomizovanou, dvojitě zaslepenou, placebem kontrolovanou studii sponzorovanou společnostmi Sanofi a Regeneron Pharmaceuticals.
Do studie mohli být zařazeni nemocní starší 40 let, kteří byli hospitalizováni pro akutní koronární syndrom (AKS) 1–12 měsíců před randomizací a měli hodnotu LDL-C alespoň 70 mg/dl (1,8 mmol/l), non-HDL-C alespoň 100 mg/dl nebo apolipoprotein B alespoň 80 mg/dl navzdory nejméně 2týdenní intenzivní nebo maximální tolerované léčbě statinem. Intenzivní statinová léčba byla definována jako atorvastatin 40–80 mg nebo rosuvastatin 20–40 mg denně.
Nemocní byli randomizováni 1 : 1 k léčbě alirokumabem nebo dostávali placebo. Alirokumab byl iniciálně podáván v dávce 75 mg s. c. každé 2 týdny. V rámci studie byl vytvořen speciální protokol úpravy léčby s cílem dosáhnout ve skupině s alirokumabem hladiny LDL-C 25–50 mg/dl (0,6–1,3 mmol/l) a současně zabránit trvalému snížení hladiny LDL-C < 15 mg/dl. U jedinců, u nichž nebylo dosaženo cílového rozmezí a hladina LDL-C zůstávala vyšší, byla proto dávka alirokumabu zaslepeně zvýšena na 150 mg jednou za 2 týdny. Naproti tomu u nemocných, u nichž hladina LDL-C zůstávala < 15 mg/dl, byla dávka alirokumabu buď zaslepeně snížena (ze 150 na 75 mg s. c. každé 2 týdny) nebo bylo podávání alirokumabu zaslepeně nahrazeno placebem. Hodnota LDL-C 15 mg/dl byla nastavena jako bezpečnostní hranice, protože v době plánování ODYSSEY OUTCOMES nebyly k dispozici téměř žádné údaje o snižování LDL-C k těmto extrémně nízkým hodnotám [1,2].
Charakteristika souboru
Do studie bylo mezi listopadem 2012 a listopadem 2015 zařazeno celkem 18 924 jedinců v 1 315 centrech v 57 zemích (včetně České republiky a Slovenské republiky), 9 462 bylo randomizováno k léčbě alirokumabem, 9 462 tvořilo placebovou skupinu. V 83 % případů byl kvalifikujícím AKS akutní infarkt myokardu (IM), u 16,8 % jedinců se jednalo o nestabilní anginu pectoris (NAP). Základní charakteristika souboru je uvedena v tab. 1. V době randomizace byla 88,8 % pacientům podávána intenzivní statinová léčba; po roce sledování bylo vysokou dávkou statinu léčeno 84,7 % skupiny s alirokumabem a 86,2 % placebové skupiny. Střední doba sledování ve studii byla 2,8 roku. K ukončení podávání studijní medikace z důvodů jiných než úmrtí došlo u 14,2 % v alirokumabové skupině a v 15,8 % ve skupině s placebem [2].
Table 1. Demografické a základní charakteristiky pacientů1 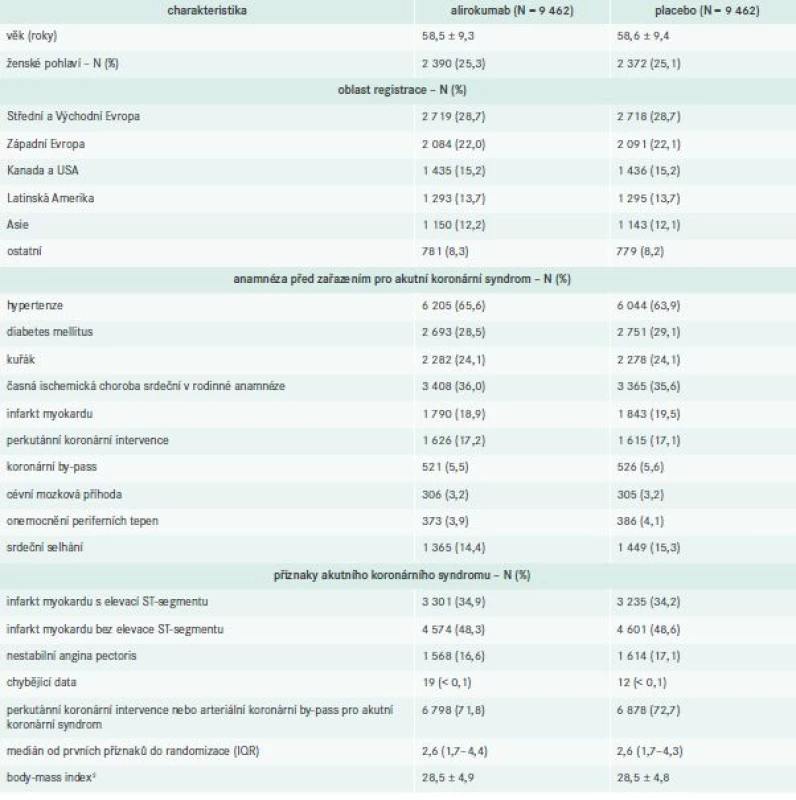
1 Hodnoty plus nebo minus jsou střední hodnoty ± SD. Mezi demografickými ani výchozími charakteristikami obou skupin nebyly žádné významné rozdíly. Další základní charakteristiky jsou uvedeny v tab. 2. Součet procentních podílů se nemusí rovnat hodnotě 100 z důvodu zaokrouhlování. IQR označuje mezikvartilní rozsah.
2 Index tělesné hmotnosti (BMI) je hmotnost v kilogramech dělená druhou mocninou výšky v metrech.Ovlivnění LDL-C
Vstupní hladina LDL-C byla 92 ± 31 mg/dl (2,38 ± 0,80 mmol/l). Ve skupině s alirokumabem dosáhla hodnota LDL-C za 4, 12 a 48 měsíců 40 mg/dl (1,0 mmol/l), 48 mg/dl (1,2 mmol/l) a 66 mg/dl (1,7 mmol/l). Odpovídající hodnoty LDL-C v placebové skupině byly 93 mg/dl (2,4 mmol/l), 96 mg/dl (2,5 mmol/l) a 103 mg/dl (2,7 mmol/l). Při analýze lipidových parametrů u nemocných skutečně léčených alirokumabem (on-treatment analýza) byly hodnoty LDL-C 38 mg/dl (0,98 mmol/l), 42 mg/dl (1,1 mmol/l) a 53 mg/dl (1,4 mmol/l), graf 1 [2]. Nižší hodnoty LDL-C v alirokumabové skupině při „on-treatment“ analýze lze alespoň částečně vysvětlit snižováním dávky nebo ukončením podávání alirokumabu při dosažení výše zmíněné dolní bezpečnostní hranice 15 mg/dl.
Graph 1. Hladiny LDL-cholesterolu v průběhu studie ODYSSEY-OUTCOMES. Upraveno podle [2] ![Hladiny LDL-cholesterolu v průběhu studie ODYSSEY-OUTCOMES. Upraveno podle [2]](https://pl-master.mdcdn.cz/media/image_pdf/ead32d3f60a7709909e4dd0df6d60ea0.jpeg?version=1552334686)
Analýza záměru léčit/Intention-to Treat Population (výsledky označeny plnými čarami) obsahovala všechny hodnoty LDL-C včetně hladin měřených po předčasném přerušení zkušebního režimu, hladin měřených po úpravě dávky za zaslepených podmínek a hladin naměřených po zaslepené substituci alirokumabu za placebo. Analýza během léčby (výsledky označeny přerušovanými čarami) vyloučila hladiny LDL-C naměřené po zaslepené substituci alirokumabu za placebo (ale obsahovala hladiny LDL-C měřené po úpravě dávek alirokumabu za zaslepených podmínek, konkrétně v rozsahu dávky 75–150 mg). Pro převedení hodnot LDL-C na jednotky mmol/l, násobte číslem 0,02586. Ovlivnění rizika KV-příhod
Primární kompozitní cílový ukazatel ve studii ODYSSEY OUTCOMES zahrnoval úmrtí z koronárních příčin, nefatální IM, ischemickou cévní mozkovou příhodu a NAP vyžadující hospitalizaci. K vývoji primárního cílového ukazatele došlo u 903 pacientů (9,5 %) ve skupině s alirokumabem a u 1 052 nemocných (11,1 %) v placebové skupině (tab. 2). Kaplanova-Meierova analýza ukazuje, že pravděpodobnost výskytu primárního ukazatele po 4 letech sledování je 12,5 % ve skupině s alirokumabem a 14,5 % v placebové skupině (hazard ratio/HR 0,85, 95% interval spolehlivosti/CI 0,78–0,93; P < 0,001), graf 2. Z analýzy vyplývá, že k zabránění jedné KV-příhodě primárního cílového ukazatele je třeba léčit 49 nemocných po dobu 4 let [2].
Table 2. Kompozitní primární a sekundární cíle 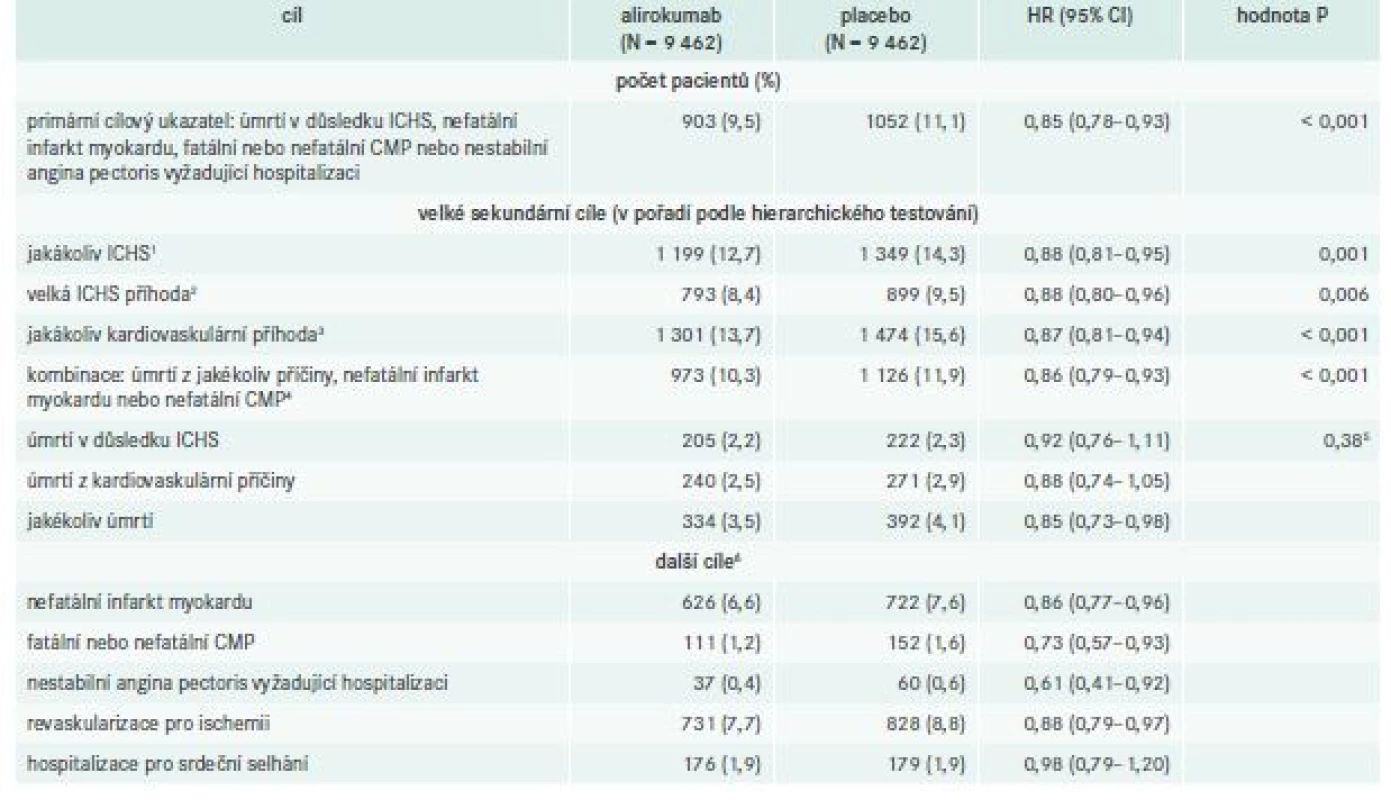
1Tento ukazatel zahrnuje úmrtí na ischemickou chorobu srdeční, nefatální infarkt myokardu, nestabilní anginu pectoris vyžadující hospitalizaci a koronární revaskularizaci pro ischemii.
2 Tento ukazatel zahrnuje úmrtí na ischemickou chorobu srdeční a nefatální infarkt myokardu.
3 Tento ukazatel zahrnuje jakékoli úmrtí z kardiovaskulárních příčin, nefatální infarkt myokardu, nestabilní anginu pectoris vyžadující hospitalizaci, koronární revaskularizaci pro ischemii nebo nefatální ischemickou cévní mozkovou příhodu.
4 Šířky intervalů spolehlivosti pro sekundární cíle nebyly upraveny pro multiplicitu, a tedy intervaly pro dále uvedené výsledky pod tímto výstupem by neměly být použity k vyvození závěrů o konečných účincích léčby.
5 Hierarchická analýza byla zastavena poté, co byla zjištěna první nevýznamná hodnota P, v souladu s plánem hierarchického testování.
6 Analýza ostatních cílů nebyla upravena pro multiplicitu; proto nejsou uvedeny žádné hodnoty P.Graph 2. Kumulativní incidence kompozitního primárního cílového ukazatele. Upraveno podle [2] ![Kumulativní incidence kompozitního primárního cílového ukazatele. Upraveno podle [2]](https://pl-master.mdcdn.cz/media/image_pdf/d9d310e26a92e29e4a01020eb9520be5.jpeg?version=1552334725)
Je zobrazena kumulativní incidence primárního cíle (kompozit úmrtí na koronární onemocnění srdce, nefatální infarkt myokardu, fatální ischemická mozková příhoda nebo nestabilní angina pectoris vyžadující hospitalizaci). Kaplanovy-Meierovy křivky pro primární cíl po 4 letech představují 12,5 % (95% Cl 11,5–13,5) ve skupině s alirokumabem a 14,5 % (95% Cl 13,5–15,6) ve skupině s placebem. Vložený graf zobrazuje stejné údaje na zvětšené ose y. Hodnota P byla vypočtena pomocí log-rank testů rozložených podle geografické oblasti. Ovlivnění hlavních sekundárních cílových ukazatelů je zřejmé z tab. 2, která zobrazuje jednotlivé cílové ukazatele v hierarchickém uspořádání, které bylo stanoveno při přípravě studie (viz níže). Alirokumab významně snížil riziko koronárních a KV-příhod, ale neovlivnil mortalitu z koronárních příčin a KV-mortalitu; Celková mortalita byla nižší ve skupině s alirokumabem (viz níže). Z jednotlivých KV-příhod alirokumab významně snížil riziko nefatálního IM, ischemické cévní mozkové příhody, NAP a koronárních revaskularizací z důvodu ischemie, naproti tomu (ne příliš překvapivě) alirokumab neovlivnil hospitalizace pro srdeční selhání [2].
Hlavním výsledkem studie ODYSSEY OUTCOMES bylo ovlivnění výskytu primárního kompozitního cílového ukazatele hodnocením nezohledňujícím další příhody u jedince, který již prodělal KV-příhodu zahrnutou v primárním ukazateli. Bylo tedy použito hodnocení, které je dnes zlatým standardem pro primární cílový ukazatel ve velkých studiích. Nedávno však byla publikovaná další analýza této studie, která se zaměřila na ovlivnění všech KV-příhod, tedy i druhých, třetích a dalších následných [3]. Do hodnocení byly zahrnuty IM, cévní mozková příhoda, NAP, koronární revaskularizace z důvodu ischemie a hospitalizace pro srdeční selhání; zatímco prvních příhod bylo zaznamenáno 3 064, všech příhod bylo celkem 5 425, tedy o 77 % více. Jestliže alirokumab zabránil 190 prvním příhodám, tak v případě hodnocení všech příhod jich bylo méně dokonce o 385 (graf 3). Pozitivní účinek alirokumabu na výskyt KV-příhod se tedy při hodnocení všech příhod ještě zvýrazní. Z analýzy všech příhod také vyplývá, že stačí léčit 18 pacientů po dobu 4 let, abychom zabránili jedné příhodě [3].
Graph 3. Kumulativní incidence nefatálních kardiovaskulárních příhod. Upraveno podle [3] ![Kumulativní incidence nefatálních kardiovaskulárních příhod. Upraveno podle [3]](https://pl-master.mdcdn.cz/media/image_pdf/3513e259f95a5767754ec01fa483086e.jpeg?version=1552334748)
Křivky průměrných kumulativních funkcí zobrazují očekávaný celkový počet nefatálních KV-příhod pro daného pacienta ve skupinách užívajících placebo a alirokumab v daném čase po randomizaci. Po 4 letech jsou odhady pro skupiny v uvedeném pořadí 0,357 a 0,301. Naopak očekávané podíly pacientů s první nefatální KV-příhodou ve skupinách s placebem a alirokumabem dosáhly 0,183 a 0,160. Ovlivnění mortality
Jak bylo zmíněno výše, léčba alirokumabem byla spojena s nižší celkovou mortalitou (3,5 % vs 4,1 %; HR 0,85; 95% CI 0,93–0,98; P = 0,03). Nicméně vzhledem k předem stanovenému hierarchickému hodnocení cílových ukazatelů je třeba P pro mortalitu považovat za „nominální“, protože nebyly významně ovlivněny ukazatele, které jsou v hierarchii hodnocení nad celkovou mortalitou, tedy KV-mortalita (P = 0,15) a mortalita z koronární příčiny (P = 0,38). Nicméně pokud se podíváme i na další složku celkové mortality, a to mortalitu z jiných než KV-příčin (non-KV), zjistíme, že byl zaznamenán trend k nižšímu riziku úmrtí ve skupině s alirokumabem (P = 0,06), graf 4. Autoři další analýzy studie ODYSSEY OUTCOMES [4] si proto dali za cíl podívat se na otázky ovlivnění mortality blíže. Především se zabývali otázkou, zda může být vztah mezi nefatálními KV-příhodami, jejichž výskyt byl prokazatelně snížen alirokumabem, a non-KV-mortalitou. Hypoteticky, například nemocný s těžkou nefatální cévní mozkovou příhodou by mohl být ve vyšším riziku non-KV-úmrtí (např. na pneumonii). V této práci byl nalezen významný vztah mezi rizikem nefatální KV-příhody a úmrtím z non-KV-příčiny (P < 0,0001) [4]. Je tedy možné, že alirokumab mohl příznivě ovlivnit celkovou mortalitu i tím, že měl vliv na non-KV-mortalitu, což ovšem nebylo zohledněno v předem stanovené hierarchické posloupnosti hodnocení výsledků. Tato analýza tedy nadále posiluje pravděpodobnost, že léčba alirokumabem po AKS může snížit i celkovou mortalitu.
Graph 4. Vliv alirokumabu na celkovou mortalitu, kardiovaskulární mortalitu a mortalitu z nekardiovaskulárních příčin ve studii ODYSSEY OUTCOMES. Upraveno podle [4] ![Vliv alirokumabu na celkovou mortalitu, kardiovaskulární mortalitu a mortalitu z nekardiovaskulárních
příčin ve studii ODYSSEY OUTCOMES. Upraveno podle [4]](https://pl-master.mdcdn.cz/media/image_pdf/837dd9e5e8185fb3a6ac837b9a1020e3.jpeg?version=1552334779)
Ovlivnění kardiovaskulárních příhod u specifických subpopulací
V rámci studie ODYSSEY OUTCOMES bylo předem specifikováno několik subpopulací pacientů, kterým se věnují další analýzy.
Subpopulace podle vstupní hladiny LDL-C. Analýzy ukázaly, že vstupní hladina LDL-C měla vliv na výsledky. Nejvýraznější pozitivní účinek měl alirokumab v podskupině s nejvyšší vstupní hladinou cholesterolu, tedy > 100 mg/dl (> 2,6 mmol/l) V této podskupině bylo podání alirokumabu spojeno jak s výraznějším snížením primárního cílového ukazatele (HR 0,76; 95% CI 0,65–0,87) a snížením výskytu všech KV-příhod (HR 0,79; 95% CI 0,70–0,88), tak s větší redukcí celkové mortality (HR 0,71; 95% CI 0,56–0,90) [2–4]. V podskupině s LDL-C > 2,6 mmol/l je třeba léčit pouhých 16 nemocných po dobu 4 let, aby se zabránilo jedné příhodě z primárního cílového ukazatele [2].
Subpopulace podle doby sledování ve studii. Výraznější účinek alirokumabu byl nalezen také v podskupině nemocných, kteří byli léčeni déle než 3 roky. V této podskupině byla výrazněji nižší celková mortalita (HR 0,78; 95% CI 0,65–0,94), graf 5 [4].
Graph 5. Kumulativní incidence kompozitního primárního cílového ukazatele v podskupinách podle iniciální hladiny LDL- cholesterolu. Upraveno podle [2] ![Kumulativní incidence kompozitního primárního cílového ukazatele v podskupinách podle iniciální
hladiny LDL- cholesterolu. Upraveno podle [2]](https://pl-master.mdcdn.cz/media/image_pdf/ecb9f71b94ccbe9f8cf5364bd5d14f78.jpeg?version=1552334803)
Bezpečnost léčby alirokumabem
Jedna z nejzásadnějších informací, které studie ODYSSEY OUTCOMES přinesla, je, že se léčba alirokumabem ukázala jako bezpečná. Mezi skupinami s alirokumabem a placebem nebyl rozdíl v celkovém výskytu nežádoucích příhod a laboratorních abnormalit (tab. 3). Jedinou nežádoucí příhodou, která byla častěji pozorována po alirokumabu, byla lokální reakce v místě vpichu (3,8 % vs 2,1 %; P < 0,001); skupiny se však nelišily ani ve výskytu závažných nežádoucích příhod, ani ve vzniku či zhoršení diabetu, srovnatelný byl i výskyt alergických reakcí, neurokognitivních poruch či hemoragických cévních mozkových příhod [2].
Table 3. Nežádoucí účinky a laboratorní abnormality 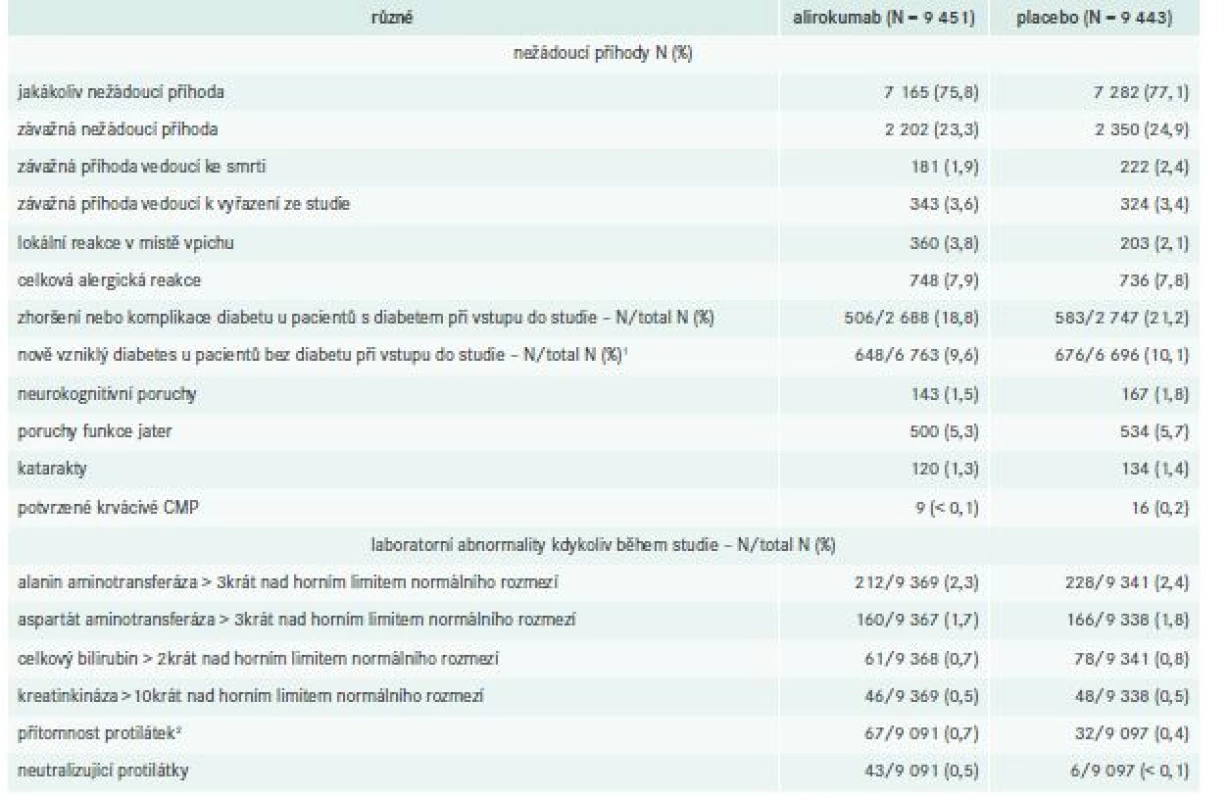
1 Nově diagnostikovaný diabetes byl definován podle přítomnosti jednoho nebo více z následujících faktorů, s potvrzením diagnózy zaslepeným externím posouzením odborníků v oblasti diabetu: hlášení o nežádoucích účincích, nový předpis na léčbu diabetu, hladina glykovaného hemoglobinu nejméně 6,5 % (a výchozí hladina < 6,5 %) při dvou měřeních, nebo hladina glykemie nalačno nejméně 126 mg/dl (7,0 mmol/l) při dvou měřeních (a výchozí hladina < 126 mg/dl).
2 Protilékové protilátky byly definovány podle přítomnosti pozitivních reakcí, které byly zjištěny po zahájení zkoušeného léčebného režimu v nejméně dvou po sobě odebraných vzorcích séra po stanovení základních hodnot, kdy mezi odebráním vzorků uplynula doba nejméně 16 týdnů.Závěr
Studie ODYSSEY Outcomes přinesla zcela zásadní informace, které se již nyní odrazily i ve změně postupů léčby nemocných s AKS. Alirokumab po přidání k intenzivní statinové léčbě u těchto nemocných významně snižoval výskyt KV-příhod a lze předpokládat, že může snížit i celkovou mortalitu. Nejvýrazněji byl pozitivní účinek alirokumabu vyjádřen ve skupině s vyšším vstupním LDL-C. Léčba alirokumabem se navíc ukázala jako bezpečná, s minimem nežádoucích příhod.
doc. MUDr. Petr Ošťádal, Ph.D.
Doručeno do redakce/Doručené do redakcie/Received 1. 2. 2019
Přijato po recenzi/Prijaté po recenzii/Accepted 8. 2. 2019
Sources
- Schwartz GG, Bessac L, Berdan LG et al. Effect of alirocumab, a monoclonal antibody to PCSK9, on long-term cardiovascular outcomes following acute coronary syndromes: rationale and design of the ODYSSEY outcomes trial. Am Heart J 2014; 168(5): 682–689. Dostupné z DOI: <http://dx.doi.org/10.1016/j.ahj.2014.07.028>.
- Schwartz GG, Steg PG, Szarek M et al. Alirocumab and Cardiovascular Outcomes after Acute Coronary Syndrome. N Engl J Med 2018; 379(22): 2097–2107. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1801174>.
- Szarek M, White HD, Schwartz GG et al. Alirocumab Reduces Total Nonfatal Cardiovascular and Fatal Events: The ODYSSEY OUTCOMES Trial. J Am Coll Cardiol 2019; 73(4): 387–396. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jacc.2018.10.039>.
- Schwartz GG, Szarek MM, Bhatt DL et al. Alirocumab Reduces Risk of Death after Acute Coronary Syndrome in Patients with Persistently Elevated Atherogenic Lipoproteins on Intensive Statin Treatment. Circulation 2018; 138(25): E772–E773 (Abstr. 20008). In: Late-Breaking Science Abstracts From the American Heart Association’s Scientific Sessions 2018 and Late-Breaking Abstracts in Resuscitation Science From the Resuscitation Science Symposium 2018. Circulation 2018; 138(25): E751–E782. Dostupné z DOI: <http://doi 10.1161/CIR.0000000000000636>.
Labels
Angiology Diabetology Internal medicine Cardiology General practitioner for adults
Article was published inAthero Review

2019 Issue 1-
All articles in this issue
- Těžká smíšená dyslipidemie jako projev hematologického onemocnění: kazuistika
- Vliv alirokumabu na kardiovaskulární příhody: Co ukázala studie ODYSSEY OUTCOMES?
- Nutraceutika s hypolipidemickým účinkem v klinické praxi: shrnutí stanoviska Mezinárodního expertního panelu lipidologů vypracované výborem České společnosti pro aterosklerózu
- Iniciativa k ustavení aferetických center: indikace a provádění lipoproteinové aferézy v České republice
- Deficit lyzosomální kyselé lipázy v diferenciální diagnostice familiární hypercholesterolemie
- Terapie dyslipidemie u pacienta se svalovou dystrofií: kazuistika
- Psoriáza ako rizikový faktor kardiovaskulárnych príhod: kazuistika
- Intenzívny manažment dyslipidémie u veľmi vysokorizikových pacientov pomocou PCSK9-inhibítorov
- Athero Review
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Nutraceutika s hypolipidemickým účinkem v klinické praxi: shrnutí stanoviska Mezinárodního expertního panelu lipidologů vypracované výborem České společnosti pro aterosklerózu
- Deficit lyzosomální kyselé lipázy v diferenciální diagnostice familiární hypercholesterolemie
- Terapie dyslipidemie u pacienta se svalovou dystrofií: kazuistika
- Psoriáza ako rizikový faktor kardiovaskulárnych príhod: kazuistika
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

