-
Medical journals
- Career
Srovnání opioidní a neopioidní analgezie po císařském řezu v celkové anestezii – prospektivní observační studie
Authors: Štourač Petr 1,3,6,8; Seidlová Dagmar 1,5,8; Bártíková Ivana 1; Kuchařová Eliška 4; Janků Petr 2; Křikava Ivo 1,3; Huser Martin 2; Wágnerová Kristýna 2; Haklová Olga 3; Hakl Lubomír 3; Štoudek Roman 1; Kosinová Martina 1,3; Schwarz Daniel 6; Zelinková Hana 6; Ševčík Pavel 3,7; Gál Roman 1
Authors‘ workplace: Klinika anesteziologie, resuscitace a intenzivní medicíny, FN Brno a LF MU, Brno 1; Gynekologicko-porodnická klinika, FN Brno a LF MU, Brno 2; Oddělení léčby bolesti, FN Brno, Brno 3; Lékařská fakulta, Masarykova univerzita, Brno 4; II. Anesteziologicko-resuscitační oddělení, FN Brno, Brno 5; Institut biostatistiky a analýz, Masarykova univerzita, Brno 6; Anesteziologicko-resuscitační klinika, FN Ostrava a LF OU, Ostrava 7; Expertní skupina pro porodnickou anestezii a analgezii při ČSARIM 8
Published in: Anest. intenziv. Med., 25, 2014, č. 1, s. 8-16
Category: Anaesthesiology - Original Paper
Overview
Cíl studie:
Cílem této prospektivní observační studie bylo srovnání účinnosti opioidních a neopioidních analgetikpři léčbě akutní pooperační bolesti po císařském řezu.Typ studie:
Prospektivní observační studie.Typ pracoviště:
Fakultní nemocnice.Materiál a metoda:
V neopioidní skupině (NO) byla podávána kombinace paracetamol 1000 mg i. v. nebo p. o. s diklofenakem 100 mg rektálně nebo i. m. v předem určených časových intervalech. Opioidní skupině (OP) byl podáván kontinuálně piritramid 3 mg/hod. i. v. V případě nedostatečné analgetické účinnosti byl podán metamizol 2,5 g i. v. V pooperačním období jsme sledovali intenzitu bolesti podle vizuální analogové škály (VAS), počet přídavných analgetických požadavků (AAR) a komplikace. Srovnali jsme hodnoty VAS a počet AAR v obou skupinách v prvních 24 hodinách po císařském řezu.Výsledky:
Se souhlasem Etické komise pro multicentrické studie FN Brno jsme zařadili 160 pacientek(NO, n = 120; OP, n = 40), které podstoupily ukončení těhotenství císařským řezem (SC) v celkové anestezii v období květen 2009 až duben 2010. Medián VAS v první hodině po SC byl v obou sledovaných skupinách 3,5 (p = 0,553). Statisticky významný rozdíl byl nalezen v hodnotách VAS i počtu AAR mezi 1. a 24. hodinou po SC (p < 0,001). V průběhu studie nebyly zaznamenány žádné závažné komplikace.Závěr:
V obou studijních skupinách jsme dosáhli dostatečného analgetického efektu (VAS pod 4), přičemž větší účinnost v prvním pooperačním dni měla opioidní analgezie.Klíčová slova:
léčba akutní pooperační bolesti – císařský řez – opioidy – neopioidní analgetika – porodnictví – celková anestezieÚVOD
V České republice i globálně jsme v posledních letech pozorovali nárůst ukončení těhotenství císařským řezem (SC) [1]. Přes nesporný přínos neuraxiální anestezie u císařského řezu je stále nemalá část prováděna v celkové anestezii [2]. V České republice je to stále takřka 50 % případů [3]. V některých zemích je naproti tomu celková anestezie u SC zastoupena minimálně [4, 5]. Nejčastějšími důvody anesteziologa pro volbu celkové anestezie (CA) pro SC jsou urgentnost výkonu, odmítnutí neuraxiální blokády pacientkou a neurologické komorbidity (Sclerosis Multiplex aj.) [3, 6].
Vzhledem k charakteru výkonu, míře předpokládané střední pooperační bolesti [7] a možnými komplikacemi spojenými s aplikací neuraxiální blokády není zavedení epidurální analgezie pouze z důvodu tlumení pooperační bolesti po císařském řezu indikováno [8].
Pro analgezii po císařském řezu jsou používány i systémově aplikované silné opioidy. Nejrozšířenější je podávání morfinu. Mezi obecné nevýhody opioidů v léčbě pooperační bolesti je udávána nutnost zvýšeného sledování vitálních funkcí pro riziko vzniku útlumu dechového centra a riziko vzniku dalších nežádoucích účinků opioidů (sedace, nauzea, zvracení, svědění, retence moči, paralytický ileus, vertigo). Přestup opioidu do mateřského mléka může dále oddálit kojení i přes malé expoziční dávky novorozenci [9]. S cílem snížení aplikovaných dávek opioidu a tím zmírnění nežádoucích účinků je často opioid podáván v kombinaci s neopioidními analgetiky. Monoterapií neopioidním analgetikem nelze dobré kontroly pooperační bolesti po SC dosáhnout [7]. Při použití kombinace několika neopioidních analgetik s odlišným mechanismem účinku však lze očekávat aditivní účinek [9, 10]. V případě podání neopioidních analgetik již v průběhu celkové anestezie je popisován zvýšený účinek současně podávaných opioidů [11].
Aktuálně nejsou známy studie popisující analgetický účinek kombinace neopioidních analgetik v pooperační péči po císařském řezu vedeném v celkové anestezii. Nejsou známy ani práce přímo srovnávající čistě neopioidní analgezii s analgezií opioidní v této indikaci.
Cílem předkládané studie bylo srovnat analgetickou účinnost opioidního a neopioidního tlumení pooperační bolesti po císařském řezu provedeném v celkové anestezii v prvním pooperačním dni (24 hodin pooperačně). Dalšími cíli bylo zjistit adekvátnost analgezie a míru komplikací spojených s léčbou pooperační bolesti.
MATERIÁL A METODY
Etická komise pro multicentrické studie FN Brno schválila prospektivní observační studii „Hodnocení pooperační analgezie po císařském řezu“. Vzhledem k charakteru studie nebyl od pacientek vyžadován informovaný souhlas se zařazením do studie, pouze souhlas s anonymním zpracováním získaných dat.
Studie probíhala na dvou anesteziologicko-resuscitačních odděleních Fakultní nemocnice Brno. Pacientky byly pooperačně přijaty na oddělení intermediární péče (neopioidní skupina) nebo jednotku intenzivní péče (opioidní skupina) Gynekologicko-porodnické kliniky.
Primární cíl
Srovnání intenzity pooperační bolesti ve skupinách OP a NO 24 hodin po SC v intervalech 0–1 hod., 1–12 hod. a 12–24 hod. pooperačně a v celém sledovaném období (0–24 hod.).
Sekundární cíle
Srovnání počtu výskytů hodnot VAS (Visual Analogue Scale) nad 4 ve skupinách OP a NO 24 hodin po SC.
Srovnání počtu přídavných analgetických požadavků (AAR) ve skupinách OP a NO 24 hodin po SC v intervalech 1–12 hod. a 12–24 hod. pooperačně a v celém sledovaném období (1–24 hod.).
Výskyt komplikací spojených s léčbou bolesti v obou skupinách: hypotenze (systolický tlak krve pod 100 mm Hg), hypertenze (systolický tlak krve nad 160 mm Hg), tachykardie (> 100 pulzů za minutu), bradykardie (< 50 pulzů za minutu), hypoventilace (méně než 10 dechů za minutu).
Kritéria pro zařazení pacientky do studie
Ukončení těhotenství císařským řezem v celkové anestezii v období květen 2009 až duben 2010 (studijní období); vyplněn standardní formulář „Hodnocení pooperační analgezie po císařském řezu“ (obr. 1).
Image 1. Hodnocení pooperační analgezie po císařském řezu 
Kritéria pro vyřazení pacientky ze studie
Císařský řez v jiné formě anestezie než celkové; neuraxiální forma analgezie po císařském řezu; nezaložený, eventuálně nevyplněný formulář „Hodnocení pooperační analgezie po císařském řezu“ (viz obr. 1).
Zaznamenávané parametry
Rodička: věk (roky), hmotnost před těhotenstvím (kg), hmotnost před porodem (kg), výška (cm), parita, gravidita, četnost těhotenství.
Intenzita bolesti podle VAS v časech: 0, 1, 3, 6, 9, 12, 18, 24 hodin po SC.
Novorozenec: pohlaví, Apgar skóre (1. min., 5. min., 10. min.), pH pupečníkové krve.
Císařský řez: indikace k SC (akutní – časný, akutní, neodkladný; plánovaný), indikace k SC v CA.
Strukturovaný formulář „Hodnocení pooperační analgezie po císařském řezu“
Všechna data byla zaznamenána ošetřujícím personálem do strukturovaného formuláře „Hodnocení pooperační analgezie po císařském řezu“ (viz obr. 1) nebo do zdravotnické dokumentace rodičky.
Protokol léčby akutní bolesti po císařském řezu v celkové anestezii
Neopioidní skupina (NO): kombinace paracetamolu 1 000 mg (i. v. či p. o.) každých 8 hodin s diklofenakem 100 mg supp. či i. m. každých 12 hodin. První dávka podána před koncem císařského řezu.
Opioidní skupina (OP): piritramid 3 mg/hod. i. v. kontinuálně. Zahájení aplikace bezprostředně po přijetí na jednotku intenzivní péče.
Záchranná analgetická léčba pro obě skupiny (počet přídavných analgetických požadavků, AAR): metamizol 2,5 g i. v. v případě intenzity bolesti podle VAS > 4.
Monitorování intenzity pooperační bolesti
K monitorování intenzity pooperační bolesti byla použita vizuální analogová škála (VAS), která byla součástí standardizovaného formuláře (viz obr. 1). Po poučení pacientka označila na výseči místo odpovídající intenzitě aktuálně vnímané pooperační bolesti a ošetřujícím personálem byla zaznamenána hodnota v rozsahu 0 (žádná bolest) až 10 (agonizující bolest). Cílem léčby bolesti bylo dosáhnout snesitelné intenzity bolesti VAS < 4.
Protokol celkové anestezie pro císařský řez
Po preoxygenaci rodičky v poloze na levém poloboku 15˚ byla podána indukční dávka thiopentalu 5 mg/kg i. v. a sukcinylcholinu 1 mg/kg i. v. Za aplikace Sellickova hmatu byly po nástupu nervosvalové blokády zajištěny dýchací cesty orotracheální intubací. Anestezie byla udržována sevofluranem (do 1 MAC) a oxidem dusným (do 50 %). Po přestřižení pupečníku byl podán sufentanil 15–25 µg i. v. a podáno cis-atrakurium 0,08 mg/kg nebo vekuronium 0,05 mg/kg i. v. V případě známek reziduální kurarizace byl na konci anestezie proveden zvrat nervosvalové blokády neostigminem 0,03 mg/kg i. v. a atropinem 0,01 mg/kg i. v.
Statistická analýza
Popisná statistika kvantitativních proměnných byla provedena pomocí aritmetického průměru, směrodatné odchylky, mediánu a mezikvartilového rozpětí (MS Excel 2010, Microsoft, USA). Pro jednorozměrné komparativní analýzy kvantitativních proměnných byly použity dvouvýběrové t-testy, a to při normálním rozdělení hodnot, shodnosti rozptylů a množství odlehlých hodnot (věk, hmotnost, hmotnost před SC, BMI, pH pupečníkové krve). U ostatních hodnocených parametrů byl použit neparametrický dvouvýběrový Wilcoxonův test (výška, parita, gravidita, četnost těhotenství). U kategoriálních proměnných (elektivní/akutní SC, indikace CA, pohlaví novorozence) byla hodnocena homogenita obou výběrů pomocí Pearsonova chí-kvadrát testu. Míra bolesti hodnocená na škále VAS nevykazuje ve všech časových intervalech normální rozdělení, a proto byl pro jednorozměrná srovnávání použit neparametrický dvouvýběrový Wilcoxonův test. Pro analýzu počtu AAR byla sestavena kontingenční tabulka ukazující absolutní a relativní četnosti výskytu jednotlivých a vícečetných požadavků. Testování shodnosti mediánů počtů AAR bylo prováděno pomocí neparametrického dvouvýběrového Wilcoxonova testu. Statistické výpočty a testování byly provedeny v prostředí software MATLAB (Mathworks Inc., USA).
VÝSLEDKY
Studie proběhla v období květen 2009 až duben 2010. Do neopioidní skupiny bylo zařazeno 120 pacientek (NO, n = 120), do opioidní skupiny bylo zařazeno 40 pacientek (OP, n = 40).
Demografické parametry souborů
Vyhodnocení demografických parametrů opioidní (OP) i neopioidní (NO) skupiny (rodička, novorozenec, poporodní adaptace novorozence) včetně jejich srovnání je uvedeno v tabulkách 1 a 2. Srovnání indikací k císařskému řezu (akutní, elektivní) v obou skupinách je uvedeno v tabulce 3. Indikace k celkové anestezii u císařského řezu jsou včetně srovnání mezi oběma skupinami uvedeny v tabulce 4.
Table 1. Charakteristika obou souborů rodiček s neopioidní analgezií (NO, n = 120) a opioidní analgezií (OP, n = 40) po císařském řezu 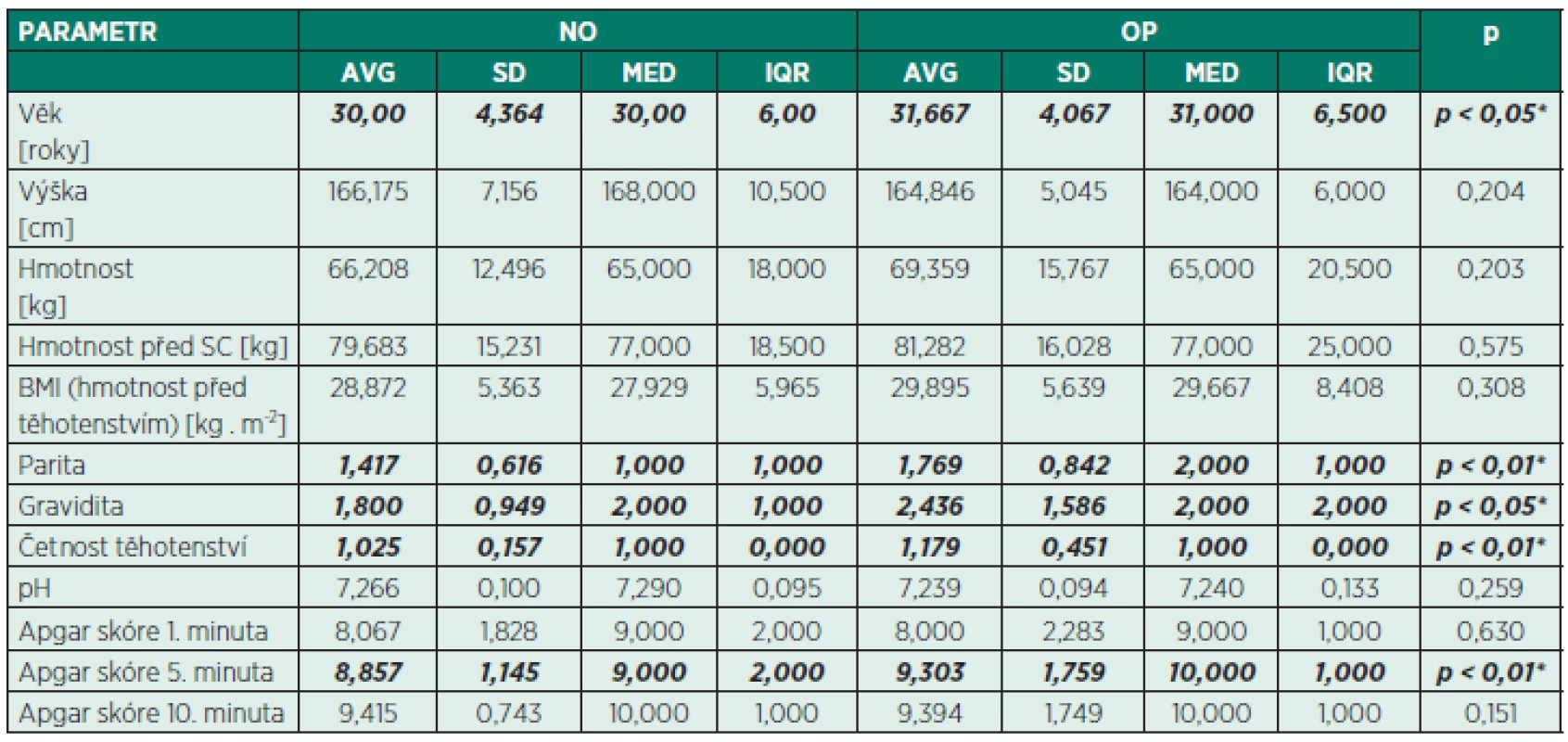
AVG – průměr, SD – směrodatná odchylka, MED – medián, IQR – mezikvartilové rozpětí, p – hladina významnosti, statisticky významné rozdíly mezi soubory jsou označeny tučnou kurzivou a hvězdičkou Table 2. Zastoupení pohlaví novorozence v opioidní (OP) a neopioidní (NO) skupině 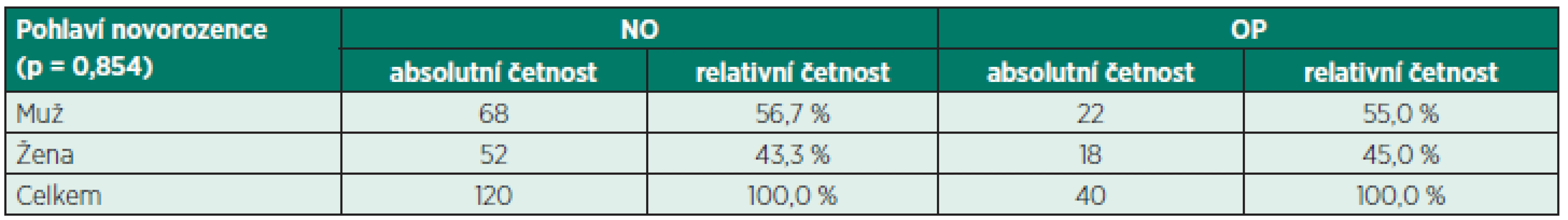
p – hladina významnosti Table 3. Indikace k císařskému řezu v neopioidní skupině (NO) a opioidní skupině (OP) 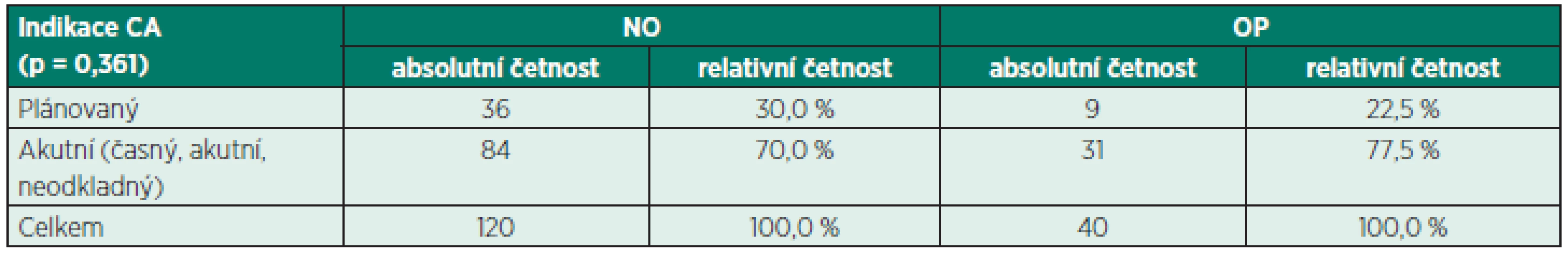
p – hladina významnosti Table 4. Indikace k celkové anestezii u císařskému řezu v opioidní (OP) a neopioidní (NO) skupině 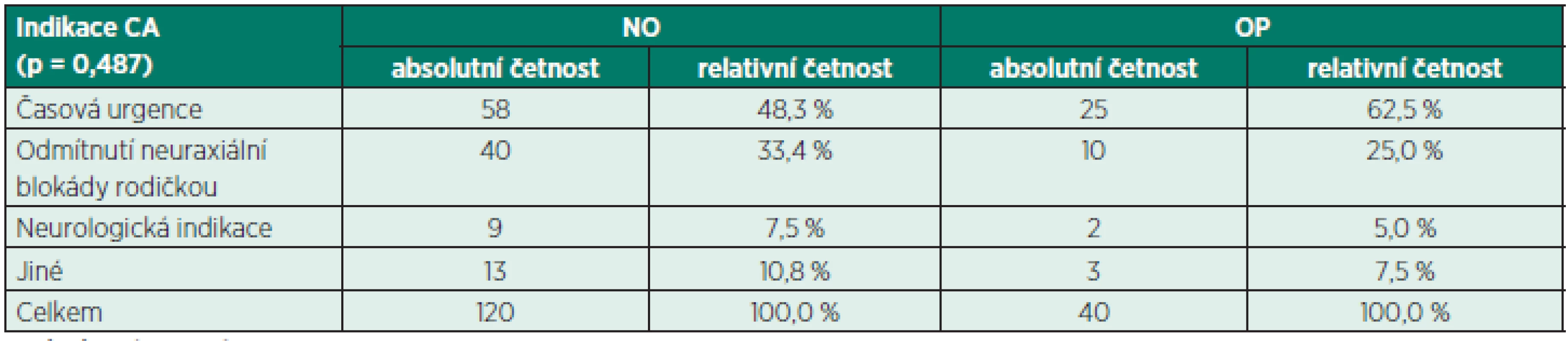
p – hladina významnosti Vyhodnocení primárních cílů
Medián VAS skóre v první hodině po císařském řezu v OP skupině byl 3,5, v NO skupině 3,5. Rozdíl nebyl statisticky významný (p = 0,553). V období 1–12 hodin po císařském řezu byl medián VAS v OP skupině 2,0 a v NO skupině 3,5 (p < 0,001) a mezi 12. a 24. hodinou v OP skupině 1,5 a v NO skupině 3,0 (p < 0,001). V období 0–24 hod. pooperačně byl medián VAS v OP skupině 2,0 a v NO skupině 3,0 (p < 0,001). Výsledky statistické analýzy jsou uvedeny v tabulce 5. Průběh intenzity pooperační bolesti podle VAS v jednotlivých hodnocených časových intervalech a skupinách je znázorněn na obrázku 2.
Table 5. Srovnání intenzity bolesti ve sledovaných intervalech po císařském řezu v opioidní (OP) a neopioidní (NO) skupině 
MED – medián, IQR – mezikvartilové rozpětí, VAS – Visual Analogue Scale, p – hladina významnosti, statisticky významné rozdíly mezi soubory jsou označeny tučnou kurzivou a hvězdičkou Image 2. Průběh VAS v prvních 24 hodinách pooperačně Krabicový graf označuje medián, 1. a 3. kvartil. Mimo hranice krabicového grafu jsou čerchovanou čárou ohraničeny neodlehlé hodnoty. Odlehlé hodnoty jsou označeny křížky. 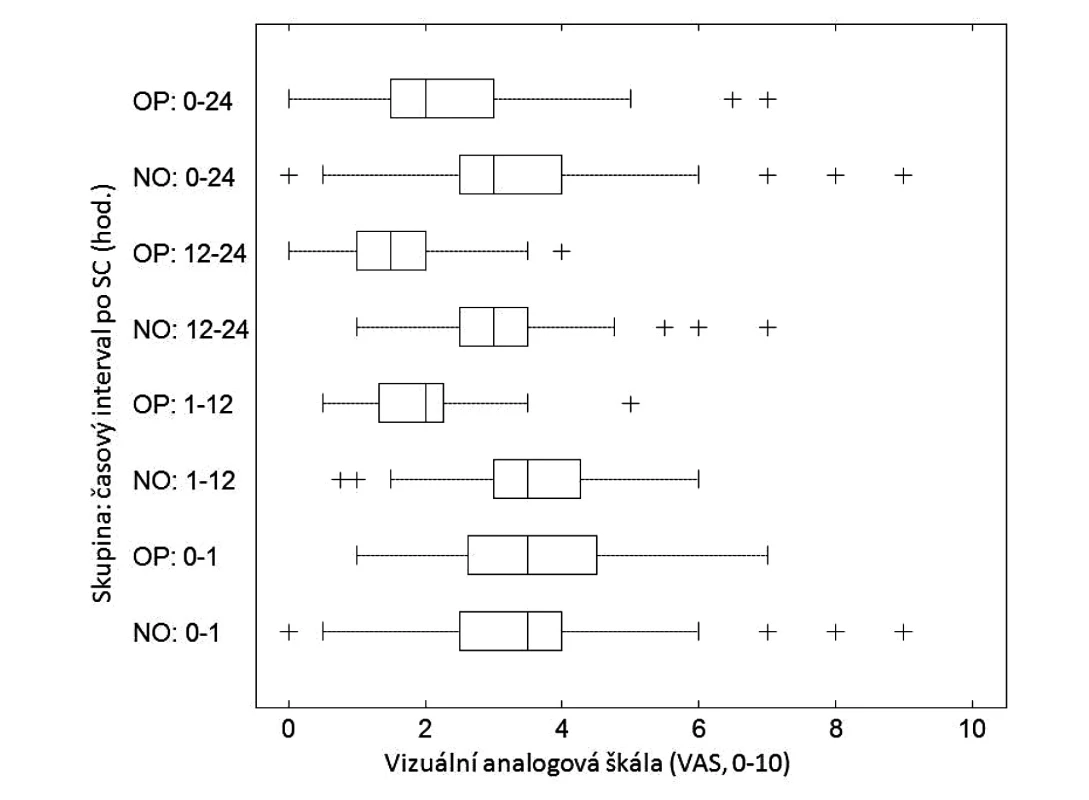
Vyhodnocení sekundárních cílů
Výskyt hodnot Visual Analogue Scale nad 4
V období 1–12 hodin po císařském řezu bylo v NO skupině zaznamenáno 27,5% hodnot VAS > 4, v OP skupině to bylo 2,5 % hodnot (p < 0,001). V dalších dvanácti hodinách byla hodnota VAS > 4 v NO skupině zaznamenána v 10 % případů, v OP skupině nebyla zaznamenána žádná (p < 0,001).
Přídavné analgetické požadavky
Absolutní a relativní četnost přídavných analgetických požadavků v jednotlivých skupinách (OP, NO) včetně jejich srovnání je uvedena v tabulce 6. Sumarizace počtu požadavků a jejich vztažení k jedné rodičce a sledovaným pooperačním intervalům (1–12 hod., 12–24 hod.) je prezentována v tabulce 7.
Komplikace spojené s léčbou bolesti
V průběhu studie nebyly zaznamenány komplikace spojené s podáním opioidní či neopioidní analgezie.
DISKUSE
V době vzniku této studie nám nebyla známa práce přímo srovnávající kombinaci neopioidní a opioidní analgezie po císařském řezu v celkové anestezii. Na výhodnost kombinace tramadolu nebo paracetamolu s diklofenakem v léčbě pooperační bolesti po císařském řezu v subarachnoidální anestezii upozornila studie Mitry et al. [10]. Vysvětlení účinnosti kombinace neopioidních analgetik lze hledat ve studii Mirandy a spolupracovníků, která prokázala supraaditivní účinek při kombinaci více neopioidních analgetik s odlišným mechanismem účinku [11].
Výhodou prezentované studie je homogenita sledovaných skupin rodiček. Rozdíly mezi oběma skupinami nebyly zjištěny ve výšce, hmotnosti a BMI (viz tab. 1). Rozdíl také nebyl nalezen v indikačních kritériích císařského řezu, kdy se potvrdilo, že celková anestezie byla preferenčně používána pro akutní indikace císařského řezu. Anesteziolog se pro ni rozhodl většinou z důvodu časové urgence či při odmítnutí neuraxiální blokády rodičkou, což je v souladu s dříve publikovanými daty [3, 6]. Rozdíl nebyl nalezen ani v míře poporodní adaptace novorozence, a to i přes statisticky významnou rozdílnost mediánů Apgar skóre v 5. minutě, která však byla klinicky nevýznamná. Parametry, ve kterých byly nalezeny statisticky významné rozdíly (věk rodičky, parita, gravidita, četnost těhotenství), jsme nevyhodnotili jako klinicky významné (viz tab. 1).
Naproti tomu limitací studie by mohla být různá velikost obou studijních skupin, která byla způsobena omezenou kapacitou jednotky intenzivní péče gynekologicko-porodnické kliniky, na které bylo možno podávat opioidní analgezii konti-nuálně a která nebyla preferenčně vyhrazena jen pro pacientky po císařském řezu.
Za další omezení studie by mohlo být považováno měření intenzity bolesti pouze v klidu, zatímco některé jiné studie udávají i bolest při chůzi [12]. Je tu nicméně oprávněný předpoklad, že má-li pacientka pooperační bolest v klidu, nebude chůze úlevou [10]. Na našem pracovišti je dodržován prvních 12 hodin po císařském řezu klid na lůžku, proto nucená vertikalizace pacientky jen z důvodu měření intenzity bolesti nebyla považována z etického pohledu za přijatelnou.
Podle některých studií je výskyt střední bolesti po SC (VAS 4–6) odhadován na 50–70 % [13]. Výskyt v naší studii byl mnohem nižší (0–2,5 % v OP skupině, 10–27,5 % v NO skupině). Tuto skutečnost lze vysvětlit kontinuálním (OP skupina) či časovaným (NO skupina) podáváním analgetik v pooperačním období, které je oproti podání na vyžádání při již pociťované bolesti doporučováno pro vyšší účinnost [14].
Z předložených výsledků vyplývá, že pooperační analgezie v první hodině bylo dosaženo spíše přesahem účinku léků podaných při celkové ane-stezii, protože v první hodině nebyl zjištěn rozdíl v intenzitě bolesti mezi skupinami ve srovnání s dalším průběhem pooperačního období. Nejvyšší intenzita bolesti byla u rodiček v obou skupinách zjištěna v 1.–12. hodině po operačním výkonu, kdy byl zároveň nejvyšší počet požadavků na přídavnou analgezii a nejvyšší výskyt měření VAS > 4. V dalších 12 hodinách se intenzita bolesti snížila a s ní klesl i počet výskytu měření s VAS > 4 v obou skupinách, v OP skupině dokonce nebyl zaznamenán žádný. Stejně tak klesl počet přídavných analgetických požadavků. Pokud byla v některém sledovaném parametru jasně patrná vyšší analgetická účinnost opioidní analgezie, bylo to právě v počtu přídavných analgetických požadavků (viz tab. 6). Po korekci (na jednu rodičku a sledovaný časový interval) byl rozdíl mezi skupinami více než desetinásobný a dokladuje skutečnost, že ani dvojkombinace neopioidních analgetik nemusí poskytovat dostatečnou úlevu od bolesti po císařském řezu v celkové anestezii (viz tab. 7). Dále je patrné, že v prvních 24 hodinách pooperačně tlumil piritramid významně lépe pooperační bolesti ve srovnání s čistě neopioidní analgezií.
Table 6. Srovnání četnosti přídavných analgetických požadavků (AAR) v opioidní (OP) a neopioidní (NO) skupině 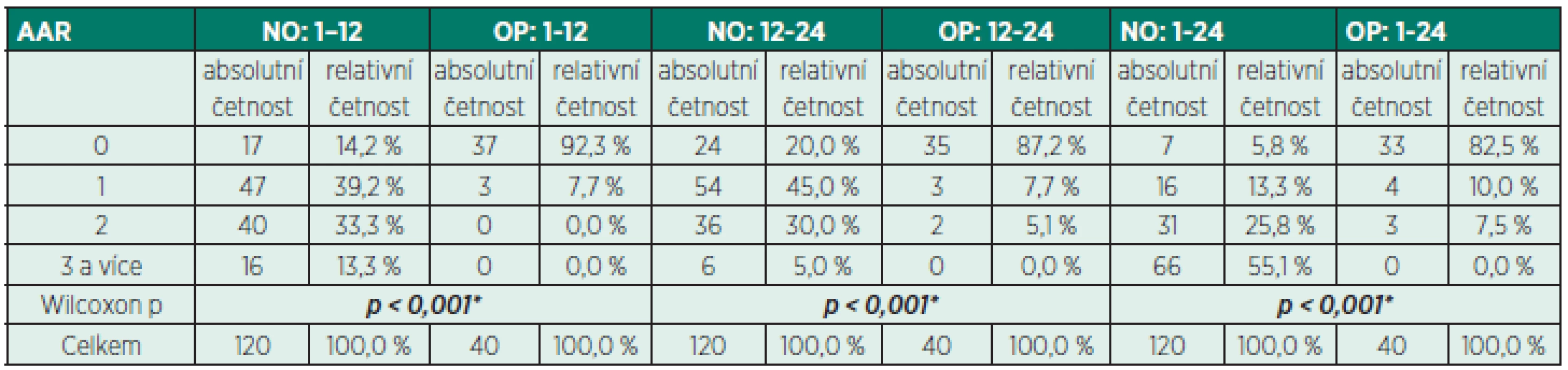
p – hladina významnosti, statisticky významné rozdíly mezi soubory jsou označeny tučnou kurzivou a hvězdičkou Table 7. Sumarizace počtu AAR v neopioidní (NO) a opioidní (OP) skupině 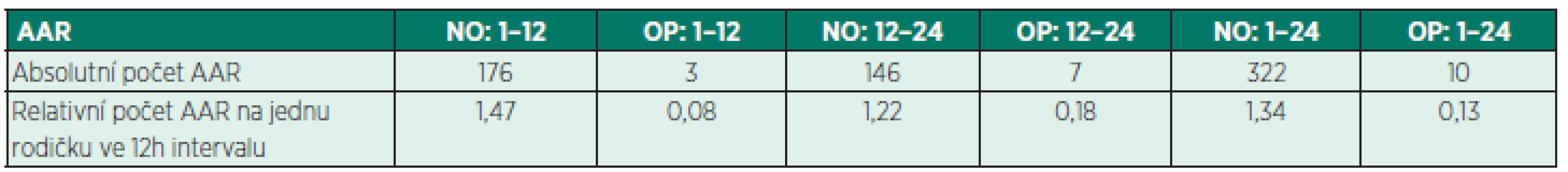
AAR – přídavný analgetický požadavek Piritramid je běžně užíván k tlumení střední až silné pooperační bolesti. Nežádoucí účinky při vyšších dávkách jsou podobné jako u ostatních opioidů. Zvolené dávkování (3 mg/ hod. i. v.) nevedlo u pacientek k výskytu dechového útlumu ani k dalším opioidním nežádoucím účinkům. Rigidní dávka byla zvolena pro jednoduchou přípravu k podání. Z důvodu minimalizace výskytu nežádoucích účinků opioidů a vyšší bezpečnosti nebylo v metodice možné navýšení dávky opioidu a vyšší bolestivost byla řešena i v opioidní skupině podáním neopioidní analgezie (metamizol) s předpokladem opioidšetřícího efektu a snížení intenzity bolesti [15]. Přepočet dávky piritramidu na aktuální či ideální predikovanou hmotnost by mohl vést k větší individualizaci léčby bolesti, v současné době však není tento způsob dávkování podpořen dostupnými studiemi ani klinickou praxí. I výsledky naší studie spíše podporují fixní způsob dávkování vzhledem k minimálnímu počtu přídavných analgetických požadavků rodiček v průběhu prvních 24 hodin pooperačně (viz tab. 7), dobré kontrole bolesti (viz obr. 2) a absenci nežádoucích účinků spojených s podáním opioidu. Kontinuální aplikace navíc nevyžaduje nákup PCA (Patient Controlled Analgesia) pump, jichž je na českých pracovištích nedostatek a bývají vyhrazeny k léčbě pooperační bolesti u výkonů s předpokládanou vysokou pooperační bolestí [3, 12, 14]. PCA režim podání opioidu na druhou stranu vede k vysoké účinnosti a spokojenosti u pacientek [16].
Obava z přestupu analgetik do mateřského mléka je jistě na místě, avšak v bezprostředním pooperačním období, kdy se teprve kojení rozbíhá, jsou expoziční dávky malé [17]. Většina doporučení o vyvarování se neopioidním analgetikům, zejména ze skupiny nesteroidních antiflogistik (NSAID), v peripartálním období je v souvislosti s předčasným uzávěrem ductus arteriosus a vznikem plicní hypertenze plodu, eventuálně z vyvolání tokolýzy inhibicí cyklooxygenázy a je tedy zaměřena na předporodní období [18].
Někteří autoři se dále u neopioidních analgetik obávají nežádoucích gastrointestinálních a krvácivých účinků, avšak jejich výskyt při krátkodobém užívání není podpořen jasnými důkazy. Absence krvácivých a gastrointestinálních nežádoucích účinků v této studii může být způsobena jejich krátkodobým podáváním jen v pooperačním období, což je podpořeno i výsledky jiných studií [10, 13].
Cílem této studie bylo především prospektivní srovnání dvou pooperačních analgetických režimů založených na časovaném či kontinuálním podání analgetik s možnou reakcí na bolest vyšší intenzity. V České republice je četnost podání celkové anestezie u císařského řezu (i plánovaného) oproti jiným zemím stále velmi významná [3], proto mohou být výsledky studie přínosem pro klinickou praxi tam, kde není možné pooperačně použít techniky regionální analgezie.
ZÁVĚR
V obou studijních skupinách jsme dosáhli v prvních 24 hodinách po císařském řezu dostatečného analgetického efektu s vyšší účinností kontinuální opioidní analgezie piritramidem.
Do redakce došlo dne 5. 5. 2013.
Přijato do tisku dne 5. 8. 2013.
Autoři nedeklarují konflikt zájmů.
Část výsledků této práce byla prezentována jako konferenční abstrakt a poster na kongresu European Society of Anaesthesiology, Euroanaesthesia 2012, Paříž, Francie.
Studie byla podpořena Interní grantovou agenturou Ministerstva zdravotnictví České republiky – projekt NT 13906-4/2012.
Adresa pro korespondenci:
MUDr. Petr Štourač, Ph.D.
Klinika anesteziologie, resuscitacea intenzivní medicíny LF MU a FN Brno
Jihlavská 20
625 00 Brno
e-mail: petr.stourac@gmail.com
Sources
1. Mardešićová, N., Velebil, P. Epidemiologie císařských řezů. Postgraduální medicína, 2010, 2, p. 171–174.
2. Pan, P. H. Post cesarean delivery pain management: Multimodal approach. Int. J. Obstet. Anesth., 2006, 15, p. 185–188.
3. Štourač, P. Obstetric Anaesthesia and Analgesia Month Attributes – reálná zpráva o anesteziologické praxi na českých porodních odděleních. Anest. Intenziv. Med., 2013, 24, 2, s. 81–82.
4. Betran, A. P., Merialdi, M., Lauer, J. A. et al. Rates of caesarean section: Analysis of global, regional and national estimates. Paediatr. Perinat. Epidemiol., 2007, 21, p. 98–113.
5. Villar, J., Valladares, E., Wojdyla, D., Zavaleta, N., Carroli, G., Velazco, A. et al. Caesarean delivery rates and pregnancy outcomes: The 2005 WHO global survey on maternal and perinatal health in Latin America. Lancet, 2006, 367, p. 1819–1829.
6. McGlennan, A., Mustafa, A. General anaesthesia for Caesarean section. Contin. Educ. Anaesth. Crit. Care Pain, 2009, 9, 5, p. 148–151.
7. Dolin, S. J., Cashman, J. N., Bland, J. M. Effectiveness of acute postoperative pain management. I. Evidence from published data. Br. J. Anaesth., 2002, 89, p. 409–423.
8. Royakers, A. A. N. M., Willigers, H., van der Ven, A. J. et al. Catheter-related epidural abscesses—don’t wait for neurological deficits. Acta Anaesthesiol. Scand., 2002, 46, p. 611–615.
9. Gadsden, J., Hart, S., Santos, A. C. Post-cesarean delivery analgesia. Anesth. Analg., 2005, 101, p. 62–69.
10. Mitra, S., Khandelwal, P., Sehgal, A. Diclofenac-tramadol vs. diclofenac-acetaminophen combinations for pain relief after caesarean section. Acta Anaesthesiol. Scand., 2012, 56, 6, p. 706–711.
11. Miranda, H. F., Puig, M. M., Prieto, J. C., Pinardi, G. Synergism between paracetamol and nonsteroidal anti-inflammatory drugs in experimental acute pain. Pain, 2006, 121, 1–2, p. 22–28.
12. Samina, I., Khurram, S., Faraz, S. Observational study to assess the effectiveness of postoperative pain management of patients undergoing elective cesarean section. J. Anaesthesiol. Clin. Pharmacol., 2012, 28, 1, p. 36–40.
13. Bush, D., Lyons, G., Macdonald, R. Diclofenac for analgesic after caesarean section. Anaesthesia, 1992, 47, p. 1075–1077.
14. Ševčík, P., Málek, J., Bejšovec, D., Gabrhelík, T., Křikava, I., Lejčko, J., Mach, D., Mixa, V., Vojtíšková, M., Fricová, J. Léčba akutní pooperační bolesti. Anest. Intenziv. Med., 2008, 19, 3, s. 162–169.
15. Steffen, P., Krinn, E., Möller, A., Seeling, W., Rockemann, M. G.Metamizol and diclofenac profoundly reduce opioid consumption after minor trauma surgery. Acute Pain, 2002, 4, 2, p. 71–75.
16. McDonnell, N. J., Keating, M. L., Muchatuta, N. A., Pavy, T. J., Paech, M. J. Analgesia after caesarean delivery. Anaesth. Intensive Care, 2009, 37, p. 539–551.
17. The American Academy of Pediatrics Committee on Drugs The transfer of drugs and other chemicals into human milk. Pediatrics, 2001, 108, p. 776–785.
18. McWhorter, J., Carlan, S. J., O‘Leary, J. D. et al. Rofecoxib versus magnesium sulfate to arrest preterm labor: randomized trial. Obstet. Gynecol., 2004, 103, p. 923–930.
Labels
Anaesthesiology, Resuscitation and Inten Intensive Care Medicine
Article was published inAnaesthesiology and Intensive Care Medicine

2014 Issue 1-
All articles in this issue
- Srovnání opioidní a neopioidní analgezie po císařském řezu v celkové anestezii – prospektivní observační studie
- Souběžně probíhající neodkladný a akutní císařský řez – kazuistika*
- Myasthenia gravis a anestezie – nový bezpečnější postup
- Zaměřeno na prerenální akutní poškození ledvin – nastal čas přepsat učebnice?
-
Current Practice in Obstetric Anaesthesia.
Part III. Regional anaesthesia for caesarean section -
Karl Koller, objevitel lokálně anestetického účinku kokainu,se narodil v Sušici!
Krátká historie lokálních anestetik
- Anaesthesiology and Intensive Care Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Myasthenia gravis a anestezie – nový bezpečnější postup
-
Current Practice in Obstetric Anaesthesia.
Part III. Regional anaesthesia for caesarean section -
Karl Koller, objevitel lokálně anestetického účinku kokainu,se narodil v Sušici!
Krátká historie lokálních anestetik - Zaměřeno na prerenální akutní poškození ledvin – nastal čas přepsat učebnice?
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career


