-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Blokáda receptoru pro interleukin-1 preparátem anakinra vedla u pacienta s Erdheimovou-Chesterovou nemocí k vymizení patologické únavy, k poklesu markerů zánětu a ústupu fibrózy v retroperitoneu – popis případu a přehled literárních údajů
Interleukin-1 receptor blockade with anakinra provided cessation of fatigue, reduction in inflammation markers and regression of retroperitoneal fibrosis in a patient with Erdheim-Chester disease – case study and a review of literature
We describe a case of an Erdheim-Chester disease patient. First line chemotherapy treatment with 2-chlorodeoxyadenosine did not reduce fluorodeoxyglucose accumulation in pathological lesions. The patient had continuously increased CRP values of 17–20 mg/l. The disease continued to cause subfebrile temperatures and significant fatigue that made the patient to spend most of the daytime in bed. To manage the permanently increased inflammation markers, we decided to start treatment with anakinra, successfully used in some other autoinflammatory diseases (e.g. Schnitzler syndrome). We have now been able to evaluate the first 6 months of treatment. Daily subcutaneous administration of anakinra (KineretTM 100 mg daily) led to normalization of CRP values, cessation of subfebrile temperatures and, importantly, significant reduction of fatigue. Time periods the patient was able to spend out of the bed increased significantly. Consequent to the reduced fatigue, the patient was able to perform basic household tasks he was unable to undertake without treatment. After 3 months of treatment, fatigue of the same intensity returned following a short interruption of therapy. The CRP values went up again to 12 mg/l. CRP value returned back to norm and fatigue ceased after re-initiation of daily Kineret injections. Objective treatment response was assessed by measuring the degree of fluorodeoxyglucose accumulation in pathological bone lesions. PET-CT was performed before and 3 and 6 months after anakinra initiation. Intensity of accumulation did not change significantly after the first 3 months of therapy but decreased after 6 month therapy. Follow up CT of abdominal cavity was performed at the end of the 6th month of treatment. Presented CT images from before and 6 months after the treatment evidence an obvious reduction in fibroid changes in the retroperitoneum. Daily administration of anakinra to a patient with active Erdheim-Chester disease significantly reduced intensity of fatigue and improved quality of life, led to a reduction in inflammatory markers and regression in retroperitoneal fibrotization.
Key words:
anakinra – interleukin-1 receptor blocker – Erdheim-Chester disease – juvenile xantogranuloma – fatigue – autoinflammatory diseases
Autoři: Z. Adam 1; P. Szturz 1; P. Bučková 1; I. Červinková 2; R. Koukalová 3; Z. Řehák 3; M. Krejčí 1; L. Pour 1; L. Zahradová 1; R. Hájek 1; Z. Král 1; J. Mayer 1
Působiště autorů: Interní hematoonkologická klinika Lékařské fakulty MU a FN Brno, pracoviště Bohunice, přednosta prof. MUDr. Jiří Mayer, CSc. 1; Radiodiagnostická klinika LF MU a FN Brno, přednosta doc. MUDr. Jarmila Skotáková, Ph. D. 2; Oddělení nukleární medicíny, centrum PET, Masarykův onkologický ústav, prim. MUDr. Karol Bolčák 3
Vyšlo v časopise: Vnitř Lék 2012; 58(4): 313-318
Kategorie: Kazuistiky
Souhrn
Popisujeme pacienta s Erdheimovou-Chesterovou nemocí. V rámci iniciální léčby byla použita chemoterapie obsahující 2-chlorodeoxyadenosin. Tato léčba však u popisovaného pacienta nevedla k poklesu akumulace fluorodeoxyglukózy v patologických ložiscích. Pacient měl trvale zvýšené hodnoty CRP 17–20 mg/l. Nemoc dále způsobovala subfebrilie a výraznou patologickou únavu, která nutila nemocného trávit většinu dne na lůžku. Pro trvale zvýšené markery zánětu jsme se rozhodli zahájit léčbu preparátem anakinra, který se s úspěchem podává u některých chorob ze skupiny autoinflamatorních nemocí (např. Schnitzlerův syndrom). Nyní hodnotíme prvních 6 měsíců této léčby. Ihned po zahájení denní aplikace preparátu anakinra (KineretTM 100 mg denně) ve formě podkožních injekcí poklesly hodnoty CRP na normální úroveň, vymizely subfebrilie, a hlavně signifikantně poklesla intenzita patologické únavy. Signifikantně se prodloužil interval, který byl pacient schopen trávit mimo lůžko. Díky poklesu intenzity patologické únavy byl pacient schopen zastat běžné domácí práce, což bez této léčby nebylo možné. Po krátkém přerušení léčby po 3. měsíci se opět navrátila patologická únava ve stejné intenzitě jako dříve. Opět došlo k vzestupu hodnoty CRP na 12 mg/l. Po obnovení denních injekcí KineretuTM se opět hodnota CRP vrátila do normy a vymizela patologická únava. Objektivní léčebnou odpověď jsme hodnotili měřením míry akumulace fluorodeoxyglukózy v patologických kostních ložiscích. PET-CT vyšetření bylo provedeno před zahájením aplikace anakinry a po 3 měsících léčby. Intenzita akumulace fluorodeoxyglukózy se zatím po prvních 3 měsících léčby signifikantně nezměnila, při kontrole po 6. měsíci mírně poklesla. Kontrolní CT břišní dutiny bylo provedeno ke konci 6. měsíce léčby. Při srovnání CT obrazu před aplikací KineretuTM a po 6 měsících léčby byl zřetelný ústup fibrotických změn v retroperitoneu, jak dokládají publikované obrázky. Denní aplikace anakinry pacientovi s aktivní Erdheimovou-Chesterovou nemocí signifikantně snížila intenzitu patologické únavy, a zlepšila tak kvalitu života, vedla k poklesu markerů zánětu a vedla k ústupu fibrotizace retroperitonea.
Klíčová slova:
anakinra – blokátor receptoru interleukinu-1 – Erdheimova-Chesterova nemoc – juvenilní xantogranulom – patologická únava (fatigue) – autoinflamatorní chorobyÚvod
Erdheimova-Chesterova nemoc je velmi vzácná choroba dospělých. Typicky způsobuje hyperostózu dlouhých končetin, fibrózu retroperitonea, zesílení stěny aorty a může tvořit i infiltráty ve stopce hypofýzy a v dalších částech mozku. Patologické fagocytující histiocyty, které jsou původci Erdheimovy-Chesterovy nemoci, produkují hodně prozánětlivých cytokinů, které způsobují subfebrilie až febrilie. Důsledkem zvýšených koncentrací prozánětlivých cytokinů je zvýšená hodnota C-reaktivního proteinu (CRP) a zvýšená hodnota sedimentace erytrocytů. Zvýšená tvorba prozánětlivých cytokinů je zodpovědná za patologickou únavu.
Patologická únava (fatigue dle anglosaské literatury) je termín pro subjektivní pocit únavy, nedostatku energie, vyčerpanosti, který nemocní pociťují bez jakékoli předchozí příčiny. Za fyziologickou únavu (tiredness) se označuje pocit únavy, vyčerpání či nedostatku energie po předchozí vyvolávající zátěži.
Erdheimova-Chesterova nemoc probíhá pozvolna a je obtížně léčitelná. U některých pacientů se podaří docílit zlepšení po aplikaci 2-chlorodeoxyadenosinu, výjimečně jiných cytostatik. Jsou zprávy i o účinné léčbě interferonem α. Nicméně u některých nemocných je choroba na tyto léky rezistentní.
Ale i pro tyto pacienty, u nichž selhala léčba cytostatiky či interferonem α a kteří trpí patologickou únavou (patologickým nedostatkem energie) nedovolující jim opustit lůžko, je zde lék, který jim výrazně zlepší kvalitu života. Tím lékem je preparát anakinra, firemním názvem KineretTM. Je to rekombinantní antagonista lidského receptoru pro interleukin-1. Interleukin-1 je spouštěcím mechanizmem kaskády prozánětlivých cytokinů. Rodina interleukinu-1 sestává ze 2 agonistických proteinů, interleukinu-1α (převáženě v membránové formě) a interleukinu-1β (pouze v solubilní formě), a dále pak z inhibitoru receptoru pro interleukin-1, který se váže na receptor pro interleukin-1 a inaktivuje jej. Po zablokování receptoru pro interleukin-1 nemůže interleukin-1, tvořený histiocytárními buňkami, iniciovat zvýšenou tvorbu dalších prozánětlivých cytokinů. Preparát anakinra tak zmírní až zastaví systémovou zánětlivou reakci, což se u pacientů s Erdheimovou-Chesterovou nemocí projeví vymizením subfebrilií či febrilií a vymizením patologické únavy.
První zprávu o úspěšné léčbě pacientů tímto lékem publikovali francouzští autoři [1]. V následujících odstavcích hodnotíme šestiměsíční aplikaci anakinry pacientovi s Erdheimovou-Chesterovou nemocí.
Popis případu
Muž, narozený roku 1965, byl až do roku 2004 (do svých 39 let) zcela zdráv. Prvním příznakem nemoci byla polydipsie a polyurie. Diagnóza centrálního diabetes insipidus byla potvrzena koncentračním testem v září roku 2004. Správná diagnóza nemoci byla však stanovena až koncem roku 2008. Popis nemoci byl v české odborné literatuře opakovaně zveřejněn [2–5] a texty jsou dostupné na adrese www.vnitrnilekarstvi.cz, a proto jej zde neopakujeme. Po prostudování publikovaných informací o terapii této nemoci jsme v rámci léčby první linie podali 2-chlorodeoxyadenosin. Hodnocení této léčby bylo již zveřejněno [6]. Efektem léčby bylo výrazné zmenšení infiltrátů v CNS. Dle PET-CT zobrazení však zůstávala akumulace fluorodeoxyglukózy v dlouhých kostech a v dalších patologických ložiscích stejná. V rámci 2. linie léčby jsme v rámci programu CUP (Compassionate Use Program určený pro pacienty se vzácnými hematoonkologickými onemocněními) použili léčbu lenalidomidem. V průběhu léčby lenalidomidem došlo k dalšímu zmenšení infiltrátů v CNS. Zásadní je však pro hodnocení aktivity nemoci celotělové PET-CT zobrazení. Dle PET-CT zobrazení nevedla u tohoto pacienta léčba 2-chlorodeoxyadenosinem ani lenalidomidem ke snížení akumulace fluorodeoxyglukózy v extrakraniálních patologických ložiscích, zatímco v druhém případě jsme pomocí 2-chlorodeoxyadenosinu dosáhli velmi výrazného snížení akumulace fluorodeoxyglukózy ve všech ložiscích nemoci, a tak i velmi dobré léčebné odpovědi.
Jak léčbu 2-chlorodeoxyadenosinem, tak později lenalidomidem snášel pacient bez vedlejších nežádoucích účinků. Po celou dobu však trpěl závažnou patologickou únavou [7].
Léčba anakinrou
Dne 21. 3. 2011 jsme u pacienta po podepsání informovaného souhlasu s touto léčbou zahájili denní podávání podkožních injekcí anakinry (preparátu KineretTM, 100 mg denně). Tato léčba probíhala po dobu 3 měsíců. Již 2. den po zahájení léčby anakinrou udával pacient výrazně zlepšení celkového stavu a zmenšení patologické únavy. Výrazně se prodloužil čas, který pacient trávil mimo lůžko, a zkrátil se čas, který pacient trávil na lůžku. Toto zlepšení trvalo po celé 3 měsíce aplikace injekcí anakinry. Po přerušení aplikace anakinry se navrátila velká patologická únava. Pacient byl po celou dobu sledován klinickým psychologem a zde shrneme jeho vyšetření, provedené 3 týdny po prvním přerušení aplikace anakinry.
Hodnocení psychologem
Kognitivní funkce pacienta (pozornost, paměť, exekutivní funkce, inteligence, zrakově-prostorové dovednosti) byly v době vyšetření (3 týdny po ukončení aplikace KineretuTM) zcela v normě. Exekutivní funkce inteligence byla v horní části průměru. Práceschopnost však byla narušena zvýšenou unavitelností a pomalým pracovním tempem. Osobnostní charakteristicky pacienta jako vnitřní stabilita, sebejistota, klidný až flegmatický temperament a střízlivá věcnost mu pomáhají snášet tuto nemoc. Nejvýraznější potíž pacienta, točení hlavy, trvá stále, stejně jako dysartrie a únava. Projevy se zhoršují a zmírňují v 5–7denních cyklech.
V době, když užíval KineretTM, patologická únava výrazně ustoupila, pacient se cítil výrazně lépe. Točení hlavy přetrvávalo v mírné podobě, byla zlepšená dysartrie. Vařil jídlo, chodil na procházky, zvládal péči o domácnost. Vzhledem k točení hlavy se musel výrazně soustředit, což jej unavovalo, a tak odpočíval asi 5krát denně.
Nyní po vysazení KineretuTM cítí výrazné zhoršení stavu. Hlava se mu točí i vsedě, vleže ne. Cítí nevolnost jako při mořské nemoci, související s neustálými závratěmi (pacient používá termín „točení hlavy“). Pacient nemá pocit stability, může chodit pouze s oporou. Vycházky nyní po ukončení léčby KineretemTM vynechává, protože jsou pro něj moc únavné. Pacient říká, že leží téměř celý den na svém lůžku. Odpočinek na lůžku přerušuje jen drobnými domácími pracemi, jako je např. zašroubování šroubku. K této aktivitě se ale již musí nutit. Dále si např. poté, co si nachystá snídani, musí lehnout a odpočinout, než začne jíst. Všechny tyto činnosti zvládal při léčbě preparátem anakinra bez potíží. Nyní po ukončení léčby má pocit zhoršení řečových schopností. Dokonce hůře vidí, obraz není ostrý, pokud se soustředí, obraz přečte.
Vše odpovídá výraznému ústupu patologické únavy po dobu aplikace preparátu anakinra a opětovnému návratu závažné patologické únavy po přerušení podávání preparátu anakinra.
Laboratorní hodnocení
Prozánětlivá aktivita cytokinů produkovaných patologickými fagocytujícími histiocyty Erdheimovy-Chesterovy nemoci se odráží v hodnotě C-reaktivního proteinu (CRP), sedimentace erytrocytů a dalších markerů zánětlivé odpovědi organizmu (tab. 1). Před zahájením léčby preparátem anakinra se hodnoty CRP pohybovaly v rozmezí 17–25 mg/l. V období, kdy probíhala léčba, se hodnoty pohybovaly mezi 0,0–3,0 mg/l. Po dočasném přerušení podávání anakinry se hodnoty CRP opět zvýšily, takže 3 týdny po přerušení léčby byla hodnota CRP 12 mg/l (graf 1). Stejně tak sedimentace byla zvýšená před podáváním KineretuTM, normalizovala se v době jeho podávání a opět stoupla po přerušení pravidelné aplikace KineretuTM (graf 2). Při léčbě došlo rovněž k částečnému poklesu zvýšených sérových hladin triacylglycerolů a vzestupu hodnot HDL-cholesterolu do fyziologického rozmezí. Po přerušení léčby je však patrný návrat do původního patologického pásma. Nízké hodnoty ferritinu odpovídají současně přítomné sideropenii (sérové železo 6,5 µmol/l v červnu roku 2011). I přesto lze pozorovat dynamiku koncentrace ferritinu v závislosti na aktivitě onemocnění.
Tab. 1. Vybrané laboratorní hodnoty pacienta s Erdheimovou-Chesterovou chorobou před zahájením léčby Kineretem, v průběhu léčby a po ukončení léčby. 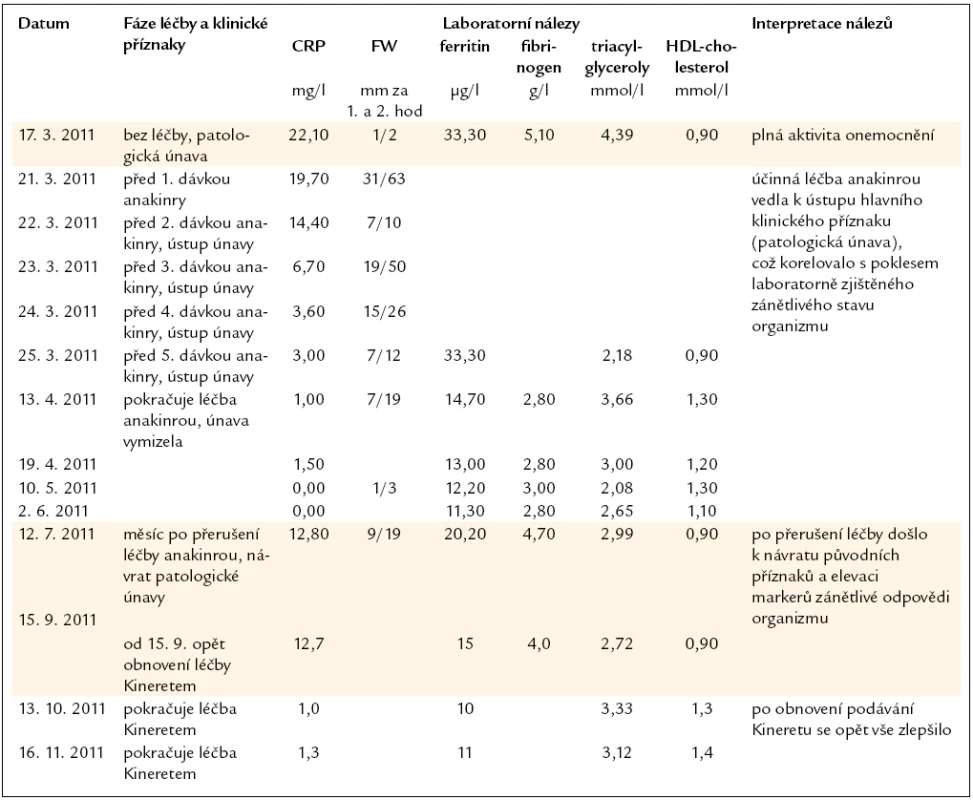
Graf 1. Postupná normalizace hodnot CRP jako markeru prozánětlivého stavu organizmu u pacienta s Erdheimovou-Chesterovou nemocí po zahájení léčby anakinrou. Po přerušení terapie došlo k opětovnému nárůstu. 
Graf 2. Postupná normalizace hodnot sedimentace erytrocytů jako markeru prozánětlivého stavu organizmu u pacienta s Erdheimovou-Chesterovu chorobou po zahájení léčby anakinrou. Po přerušení terapie došlo k opětovnému nárůstu. 
Po obnovení léčby v září roku 2011 se opět všechny markery zánětu vrátily do fyziologického rozmezí.
V ostatních standardně vyšetřovaných laboratorních parametrech nedošlo v průběhu léčby k žádnému pohybu.
Hodnocení aktivity xantogranulomových ložisek metodou PET-CT zobrazení
PET-CT vyšetření bylo provedeno před zahájením aplikace preparátu anakinra po 3 měsících léčby a po 6 měsích léčby. Hodnocena byla metabolická aktivita v 15 měřených místech skeletu a v játrech (jako referenční oblasti) pomocí SUVmax, tedy maximálních hodnot „standardized uptake value“. Číselně byla akumulace fluorodeoxyglukózy vyjádřena jako index SUVmax kostní oblast/SUVmax jater. Zatímco po 3 měsících léčby jen v jednom z 15 měřených míst došlo ke zvýšení indexu o 20 % a v dalších 14 měřených místech skeletu nedošlo ke změnám indexu přesahujícím 20 %, tak po 6 měsících léčby naopak došlo k více než 20% poklesu míry akumulace radiofarmaka (vyjádřené indexem SUVmax kostní oblast/SUVmax jater) v 8 z 15 sledovaných kostních oblastí, tento nález bylo možné interpretovat jako pokles metabolické aktivity kostních ložisek.
Hodnocení vlivu léčby na fibrotizaci v oblasti retroperitonea
Po 6 měsících léčby bylo provedeno CT vyšetření dutiny břišní. Pozitivním zjištěním bylo, že došlo k ústupu míry fibrotizace v oblasti retroperitonea.
V CT obraze trvalo zesílení stěny aorty na 6 mm, stejně jako na předchozím vyšetření. V okolí ledvin, perirenálně, byla zvýšená denzita tuku. Fibrózní změny byly ve srovnání s předchozím vyšetřením méně výrazné. Na obr. 1 je CT zobrazení dutiny břišní před léčbou, na obr. 2 je tentýž obraz po 6 měsících léčby. Na snímku je zřetelný ústup fibrotických změn.
Obr. 1. CT zobrazení dutiny břišní před léčbou Kineretem. Písmenkem F jsou označena místa s nejvýraznějšími fibrotickými změnami. Tyto fibrotické změny mohou komprimovat ureter a způsobit hydronefrózu. 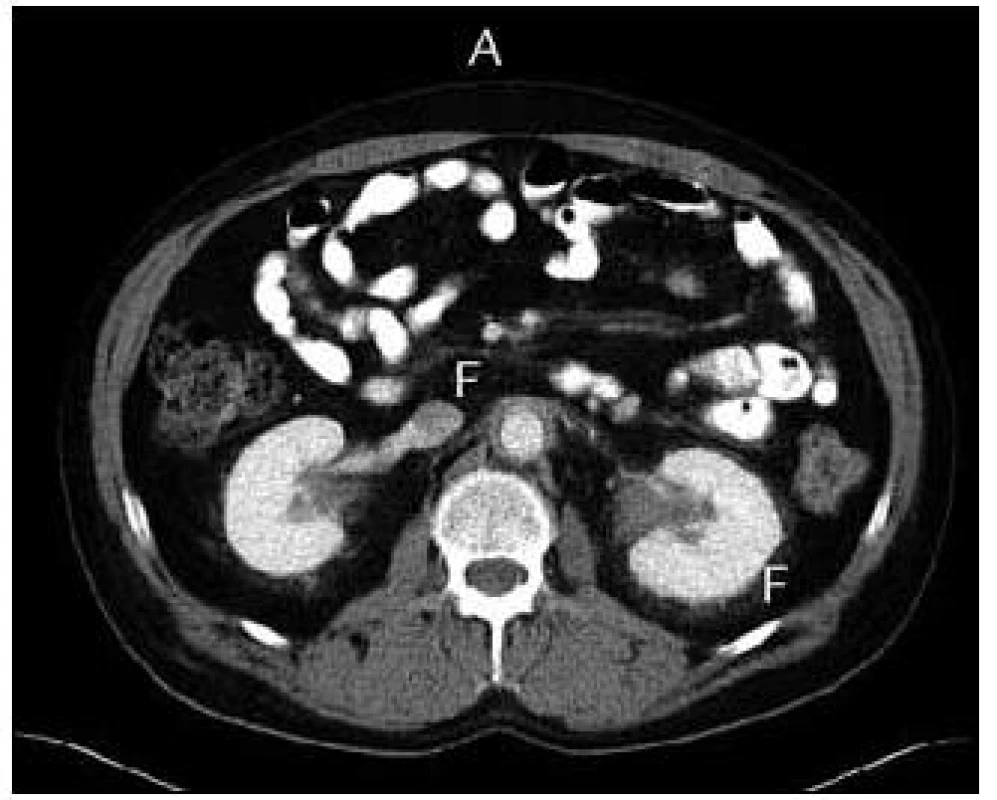
Obr. 2. CT zobrazení břišní dutiny v průběhu 6. měsíce léčby. Stále sice trvá retroperitoneální fibróza perirenálně oboustranně a fibróza okolí nadledvin a aorty. Je rozšířená stěna aorty. Fibrózní změny perirenálně však již při tomto vyšetření jsou méně výrazné než při předchozím vyšetření. 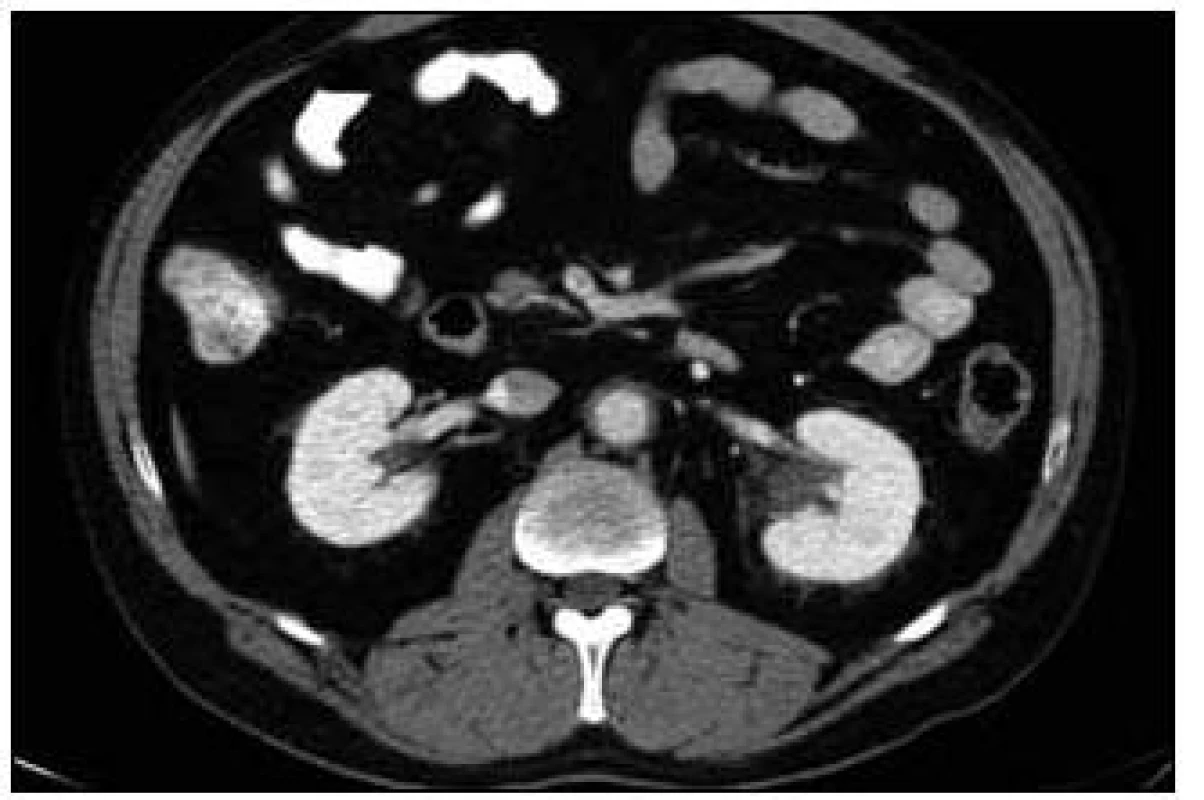
Diskuze
Erdheimova-Chesterova nemoc je řazena dle poslední WHO klasifikace krevních chorob do velké skupiny nazývané juvenilní xantogranulom. Přehled klasifikace histiocytárních chorob a přehled chorob řazených do skupiny juvenilní xantogranulom shrnuje tab. 2.
Tab. 2. Přehled všech histiocytárních forem a dále přehled forem onemocnění, které mohou způsobovat pěnité histiocyty, jejichž ložiska histologickým popisem odpovídají juvenilnímu xantogranulomu. 
Nemoci ze skupiny juvenilního xantogranulomu nelze odlišit pouze na základě histologického vyšetření, pro zařazení do jednotlivých kategorií je nutné přihlédnout ke klinickému obrazu [6].
Tento fakt dává tušit, že patofyziologie všech nemocí ze skupiny juvenilního xantogranulomu, včetně Erdheimovy-Chesterovy nemoci, zůstává zatím neobjasněná.
Pro raritnost těchto případů neexistují žádná oficiální léčebná doporučení založená na klinických studiích, takže poučení pro léčbu konkrétního pacienta je třeba hledat v popsaných případech a snažit se pak domluvit s revizními lékaři zdravotních pojišťoven na úhradě této léčby. Nové léky jsou registrované pro často se vyskytující nemoci, a nikoli pro vzácně se vyskytující nemoci, protože investice do registračního řízení léku pro vzácně se vyskytující diagnózy by byla pro farmaceutickou firmu prodělečná. Pacienti s raritními nemocemi jsou diskriminováni, protože nové léky pro ně obvykle nejsou registrovány, a důsledku toho jsou i problémy s úhradou.
V případě Erdheimovy-Chesterovy nemoci lze v literatuře nalézt případy, kdy pomohla léčba 2-chlorodeoxadenosinem. Tento lék pomohl velmi dobře u jednoho z našich pacientů s touto chorobou, u něhož po léčbě došlo dle PET-CT zobrazení k výrazné redukci akumulace fluorodeoxyglukózy v patologických ložiscích, ale i k vymizení všech příznaků nemoci. V literatuře jsou dále popsány případy léčené alkylačními cytostatiky či cytostatiky ze skupiny vinka-alkaloidů, ale bez dlouhodobého efektu. Odborná literatura popisuje léčebný efekt interferonu α, ale autoři popisů případů s pozitivním hodnocením interferonu α obvykle připouštějí, že jeho efekt byl jenom dočasný [7–12].
V jednotlivých publikacích se liší i forma hodnocení účinku léčby. Nejlepší metodou pro vyhodnocování efektivity léčby této nemoci je opakované PET-CT hodnocení [13,14]. V popisech případů s pozitivním hodnocením interferonu α nebylo použito pro hodnocení léčebné odpovědi PET-CT zobrazení.
Další z možností léčebného ovlivnění je dle některých zpráv glivec, lék standardně používaný u chronické myeloidní leukemie [15,16], ale léčba glivecem je podstatně dražší než léčba KineretemTM.
Patologické pěnité fagocytující histiocyty Erdheimovy-Chesterovy choroby produkují prozánětlivé cytokiny. Výsledkem jejich působení jsou subfebrilie až febrilie a patologická únava. Laboratorně tomu odpovídá zvýšená hodnota CRP i sedimentace erytrocytů. Tato systémová zánětlivá reakce obvykle neprovází jiné formy histiocytárních chorob, ale je typická pro Erdheimovu-Chesterovu nemoc [17].
Zvýšená hodnota prozánětlivých cytokinů, zvláště interleukinu-1, zvýšená hodnota CRP a špatná tolerance interferonu α (který jak známo má ve spektru nežádoucích účinků patologickou únavu a indukci deprese) byla důvodem, proč francouzští lékaři použili blokátor receptoru pro interleukin-1, preparát anakinra. Francouzští autoři zjistili, že při léčbě preparátem anakinra vymizely bolesti dlouhých kostí a zmenšily se patologické infiltráty na víčkách. Dále zjistili, že téměř kompletně regredovala retroperitoneální fibróza. Francouzští autoři popisují normalizaci CRP a interleukinu-6 a dále snížení exprese interleukinu-1α na monocytech (hladiny interleukinu-1β se pohybovaly mezi normálními a zvýšenými hodnotami) [1].
Naše pozorování zcela koreluje s výše uvedeným. U popsaného pacienta došlo po aplikaci KineretuTM k bleskovému ústupu patologické únavy, ale také k okamžitému poklesu všech zánětlivých markerů. Při přerušení léčby z administrativních důvodů vždy došlo okamžitě ke vzplanutí patologické únavy a ke vzestupu markerů zánětu. Po obnovení léčby KineretemTM však patologická únava opět rychle ustoupila a markery zánětu se opět navrátily na normální hodnoty, jak ilustruje tab. 1. Podstatné je, že v průběhu léčby došlo k regresi fibrotických změn v retroperitoneu, v okolí ledvin a aorty (obr. 1 a 2).
Anakinra neutralizuje biologickou aktivitu interleukinu-1α (Il-1α) a interleukinu-1β (Il-1β) kompeticí s jejich vazbou na receptory pro interleukin-1. Interleukin-1 je přitom klíčovým prozánětlivým cytokinem, který zprostředkovává řadu buněčných odpovědí. Anakinru používají revmatologové pro revmatoidní artritidu, a hlavně pro autoinflamatorní choroby. Na našem pracovišti dlouhodobě používáme tento lék u 2 pacientů se Schnitzlerovým syndromem, což je nosologická jednotka ze skupiny autoinflamatorních chorob [18–20], kterou s krevními chorobami pojí obligátní přítomnost monoklonální gamapatie, obvykle typu IgM. Můžeme říci, že roky trvající léčba 2 pacientů se Schnitzlerovým syndromem tímto lékem je zatím prosta nežádoucích účinků. Terapie cytokiny zasahuje do důležitých interakcí organizmu a má samozřejmě také svá rizika, proto je u každého pacienta nutné zvážit potenciální přínos a rizika léčby anakinrou [19].
Erdheimova-Chesterova nemoc je další chorobou, u níž může pravidelná aplikace preparátu anakinra výražně zlepšit kvalitu života nemocných, zastavit progresi fibrotických změn, a v oblasti retroperitonea dokonce navodit regresi fibrotických změn.
Závěr pro praxi
Preparát anakinra (KineretTM) představuje dle zkušeností francouzských lékařů a nyní i dle naší zkušenosti lék, který výrazně tlumí symptomy provázející Erdheimovu-Chesterovu nemoc. Dle našich, ale i francouzských zkušeností vede tato léčba k ústupu vazivových (fibrotických) změn v retroperitoneu. Fibrotizace je pro pacienta nebezpečný proces, který může vyústit v oboustrannou hydronefrózu. Nalezení léčby, která tyto procesy zastavuje, je zásadním přínosem pro pacienty s diagnózou Erdheimovy-Chesterovy nemoci.
Poděkování
Děkujeme Zdravotní pojišťovně Ministerstva vnitra ČR za hrazení léčby této vzácné nemoci. Děkujeme firmě SOBI (Swedish Orphan Biovitrum) za poskytnutí léku pro zahájení terapie.
Práce byla vypracována v rámci aktivity následujících grantů: výzkumného záměru MZ ČR: FUNDIN MZ0MOU2005, výzkumného záměru MŠMT MSM0021622434, specifického výzkumu MUNI/A/0784/2011 a grantů IGA MZd NT11154, NT12130 a NT12215.
prof. MUDr. Zdeněk Adam, CSc.
www.fnbrno.cz
e-mail: z.adam@fnbrno.cz
Doručeno do redakce: 27. 7. 2011
Přijato po recenzi: 12. 9. 2011, aktualizace 16. 12. 2011
Zdroje
1. Aouba A, Georgin-Lavialle S, Pagnoux C et al. Rationale and efficacy of interleukin-1 targeting in Erdheim-Chester disease. Blood 2010; 116 : 4070–4076.
2. Adam Z, Balšíková K, Pour L at al. Diabetes insipidus, následovaný po 4 letech dysartrií a lehkou pravostrannou hemiparézou – první klinické příznaky Erdheimovy-Chesterovy nemoci. Popis a zobrazení případu s přehledem informací o této nemoci. Vnitř Lék 2009; 55 : 1173–1188.
3. Adam Z, Balšíková K, Krejčí M et al. Centrální diabetes insipidus u dospělých osob – první příznak histiocytózy z Langerhansových buněk a Erdheimovy-Chesterovy choroby. Popis tří případů a přehled literatury. Vnitř Lék 2010; 56 : 138–148.
4. Szturz P, Adam Z, Koukalová R et al. Erdheimova-Chesterova nemoc v obrazech. Vnitř Lék 2010; 56 (Suppl 2): 2S170–2S178.
5. Adam Z, Koukalová R, Šprláková A et al. Úspěšná léčba Erdheimovy-Chesterovy nemoci chemoterapií obsahující 2-chlorodeoxyadenosin. Popis dvou případů a přehled literatury. Vnitř Lék 2011; 57 : 576–589.
6. Guo J, Wang J. Adult orbital xanthogranulomatous disease: review of the literature. Arch Pathol Lab Med 2009; 133 : 1994–1997.
7. Adam Z, Šprláková A, Řehák Z et al. Parciální regrese ložisek Erdheimovy-Chesterovy nemoci v CNS po léčbě 2-chlorodeoxadenosinem a jejich kompletní vymizení při léčbě lenalidomidem. Popis případu a přehled literárních údajů. Klinická Onkologie 2011; v tisku.
8. Arnaud L, Hervier B, Néel A et al. J. CNS involvement and treatment with interferon-α are independent prognostic factors in Erdheim-Chester disease: a multicenter survival analysis of 53 patients. Blood 2011; 117 : 2778–27782.
9. Jeon IS, Lee SS, Lee MK. Chemotherapy and interferon-alpha treatment of Erdheim-Chester disease. Pediatr Blood Cancer 2010; 55 : 745–757.
10. Suzuki HI, Hosoya N, Miyagawa K et al. Erdheim-Chester disease: multisystem involvement and management with interferon-alpha. Leuk Res 2010; 34: e21–e24.
11. Haroche J, Amoura Z, Trad SG et al. Variability in the efficacy of interferon-alpha in Erdheim-Chester disease by patient and site of involvement: results in eight patients. Arthritis Rheum 2006; 54 : 3330–3336.
12. Braiteh F, Boxrud C, Esmaeli B et al. Successful treatment of Erdheim-Chester disease, a non-Langerhans-cell histiocytosis, with interferon-alpha. Blood 2005; 106 : 2992–2994.
13. Arnaud L, Malek Z, Archambaud F et al. 18F-fluorodeoxyglucose-positron emission tomography scanning is more useful in followup than in the initial assessment of patients with Erdheim-Chester disease. Arthritis Rheum 2009; 60 : 3128–3138.
14. Steňová E, Steňo B, Povinec P et al. FDG-PET in the Erdheim-Chester disease: its diagnostic and follow-up role. Rheumatol Int 2010 Dec 7. [Epub ahead of print].
15. Janku F, Amin HM, Yang D et al. Response of histiocytoses to imatinib mesylate: fire to ashes. J Clin Oncol 2010; 28: e633–e636.
16. Haroche J, Amoura Z, Charlotte F et al. Imatinib mesylate for platelet-derived growth factor receptor-beta-positive Erdheim-Chester histiocytosis. Blood 2008; 111 : 5413–5415.
17. Arnaud L, Gorochov G, Charlotte F et al. Systemic perturbation of cytokine and chemokine networks in Erdheim-Chester disease: a single-center series of 37 patients. Blood 2011; 117 : 2783–2790.
18. Toplak N, Dolezalová P, Constantin T. Eastern/Central European autoinflammatory collaborating group for the Paediatric Rheumatology International Trials Organization (PRINTO) and Eurofever Project. Periodic fever syndromes in Eastern and Central European countries: results of a pediatric multinational survey. Pediatr Rheumatol Online J 2010; 8 : 29–30.
19. Šedivá A. Poruchy regulace zánětu a periodické horečky. Alergie 2006; 1 : 36–41.
20. Schedel J, Bach B, Kümmer-Deschner JB et al. Autoinflamatorische Syndrome/Fiebersyndrome. Hautarzt 2011; 62 : 389–402.
Štítky
Diabetologie Endokrinologie Interní lékařství
Článek Diabetes mellitus a demence
Článek vyšel v časopiseVnitřní lékařství
Nejčtenější tento týden
2012 Číslo 4- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Magnosolv a jeho využití v neurologii
- Moje zkušenosti s Magnosolvem podávaným pacientům jako profylaxe migrény a u pacientů s diagnostikovanou spazmofilní tetanií i při normomagnezémii - MUDr. Dana Pecharová, neurolog
- Biomarker NT-proBNP má v praxi široké využití. Usnadněte si jeho vyšetření POCT analyzátorem Afias 1
-
Všechny články tohoto čísla
- Predikce neurologické prognózy po srdeční zástavě – editorial
- Význam biomarkerů NGAL a cystatin C u kardiovaskulárních onemocnění – editorial
- Gastrin bez gastrinomu – editorial
- Elevace proteinu S-100B u pacientů s akutním koronárním syndromem po resuscitaci je prediktorem nepříznivé neurologické prognózy
- Krátkodobá prognóza a léčba pacientů hospitalizovaných pro akutní srdeční selhání v regionální nemocnici bez kardiocentra
- Stratifikace rizika u pacientů s Brugada syndromem
- Význam biomarkerů NGAL a cystatinu C u kardiovaskulárních onemocnění
- Nové poznatky v patogenezi Crohnovy choroby
- Lékové interakce u starších diabetiků
- Diabetes mellitus a demence
- Specifika diabetické edukace u dětí
- Blokáda receptoru pro interleukin-1 preparátem anakinra vedla u pacienta s Erdheimovou-Chesterovou nemocí k vymizení patologické únavy, k poklesu markerů zánětu a ústupu fibrózy v retroperitoneu – popis případu a přehled literárních údajů
- Akutní infarkt myokardu navozený požitím drogy pervitin
- Hypergastrinemie bez detekce gastrinomu
- Akutní intoxikace mědí při suicidiálním pokusu
- Skrytá cystická fibróza u nemocného se sarkoidózou
- Vnitřní lékařství
- Archiv čísel
- Aktuální číslo
- Pouze online
- Informace o časopisu
Nejčtenější v tomto čísle- Akutní infarkt myokardu navozený požitím drogy pervitin
- Význam biomarkerů NGAL a cystatinu C u kardiovaskulárních onemocnění
- Akutní intoxikace mědí při suicidiálním pokusu
- Nové poznatky v patogenezi Crohnovy choroby
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



